IKATAN ION BAHAN AJAR IKATAN KIMIA STANDAR KOMPETENSI
IKATAN ION
BAHAN AJAR IKATAN KIMIA STANDAR KOMPETENSI DASAR INDIKATOR TUJUAN PEMBELAJARAN MATERI PEMBELAJARAN

BAHAN AJAR IKATAN KIMIA STANDAR KOMPETENSI DASAR INDIKATOR TUJUAN PEMBELAJARAN MATERI PEMBELAJARAN § Memahami struktur atom, sifat-sifat periodik unsur, dan ikatan kimia

BAHAN AJAR IKATAN KIMIA STANDAR KOMPETENSI DASAR INDIKATOR TUJUAN PEMBELAJARAN MATERI PEMBELAJARAN § Membandingkan proses pembentukan ikatan ion, ikatan kovalen, ikatan koordinasi, dan ikatan logam serta hubungannya dengan sifat fisika senyawa yang terbentuk.

BAHAN AJAR IKATAN KIMIA STANDAR KOMPETENSI DASAR INDIKATOR TUJUAN PEMBELAJARAN MATERI PEMBELAJARAN § Menjelaskan kecenderungan suatu unsur untuk mencapai kestabilannya dengan cara melepaskan atau menerima elektron valensi. § Membandingkan susunan elektron valensi (struktur Lewis) atom gas mulia (duplet dan oktet) dan susunan elektron valensi atom bukan gas mulia. § Menjelaskan proses terbentuknya ikatan ion dan contoh senyawanya.

BAHAN AJAR IKATAN KIMIA § Menggambarkan struktur Lewis atom unsur gas mulia dan atom unsur bukan STANDAR KOMPETENSI gas mulia. § Menjelaskan unsur-unsur yang mudah melepaskan elektron valensinya membentuk ion positif dan unsur-unsur KOMPETENSI DASAR yang mudah menerima elektron valensi dari unsur lain membentuk ion negatif untuk mencapai kestabilan. INDIKATOR § Menjelaskan penyebab kestabilan atom unsur gas mulia. § Menjelaskan proses terjadinya ikatan ion dari unsur yang elektro positif TUJUAN PEMBELAJARAN (unsur logam) dengan unsur yang elektronegatif (unsur nonlogam). § Memberi contoh senyawa ion sederhana dan kegunaannya dalam MATERI PEMBELAJARAN kehidupan sehari-hari

Kestabilan unsur gas mulia TERJADINYA IKATAN ION KESIMPULAN SOAL LATIHAN

KESTABILAN UNSUR GOL VIII A § Apa yang anda ketahui tentang unsur gas mulia ?

Perhatikan beberapa konfigurasi elektron unsur – unsur gas mulia berikut! § 2 He: 2 10 Ne: 2 18 Ar: 2 8 8 36 Kr: 2 8 18 8 54 Xe: § 8 2 8 18 18 8 86 Rn: 2 8 18 32 18 8 NEXT
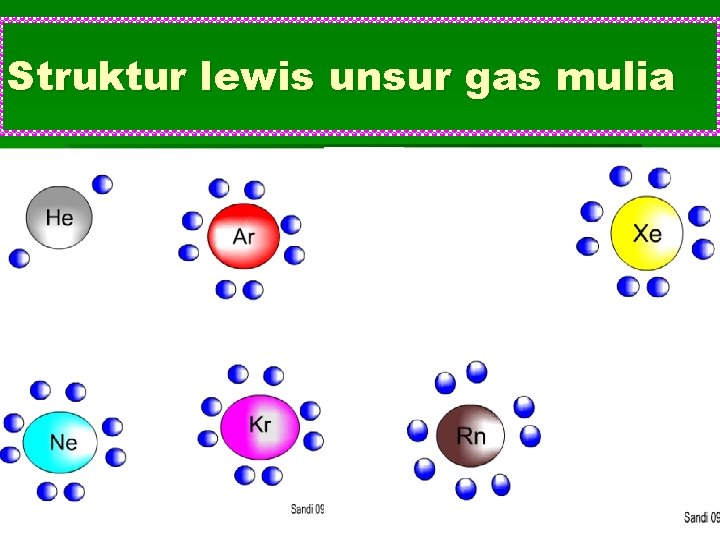
Struktur lewis unsur gas mulia

§ Dari konfigurasi elektron gas mulia diatas dapat dilihat bahwa keistimewaan unsur gas mulia adalah mempunyai 8 elektron valensi (octet) kecuali He yang mempunyai 2 elektron valensi (duplet). Hal itu telah diteliti pada tahun 1916 oleh Gilbert Newton Lewis (1875 -1946) seorang kimiawan Amerika dan Albrecht Kossel (1853 -1927) seorang kimiawan Jerman yang menghasilkan konsep ikatan kimia. NEXT

§ Menurut Lewis dan Kossel, unsur-unsur gas mulia sangat sulit membentuk senyawa kimia karena komfigurasi elektronnya merupakan konfigurasi elektron yang stabil. § Bagaimana dengan unsur lainnya ? BACK TO MENU

Kecenderungan Atom untuk Stabil § Sebelum mempelajari ikatan kimia lebih jauh, kamu harus memehami lebih dulu mengapa ikatan kimia terbentuk. Perlu kamu ketahui bahwa setiap unsur memiliki kecenderungan untuk mencapai konfigurasi electron yang stabil (sama dengan konfigurasi gas mulia). § Bagaimana caranya untuk mencapai kestabilan ? NEXT

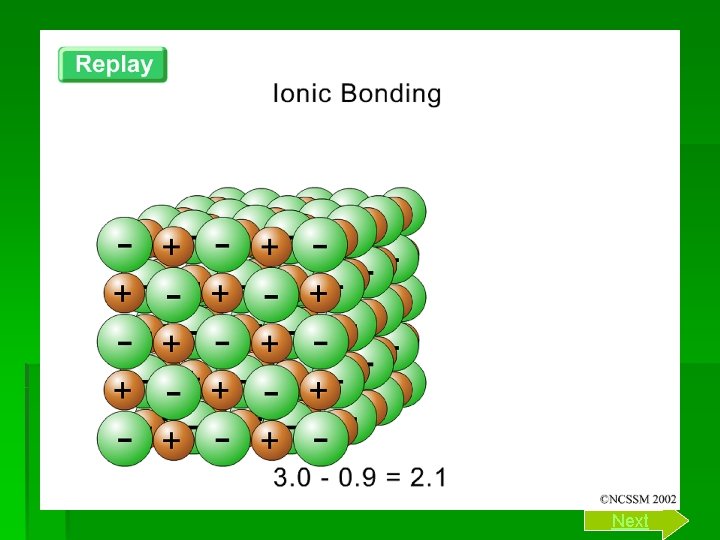
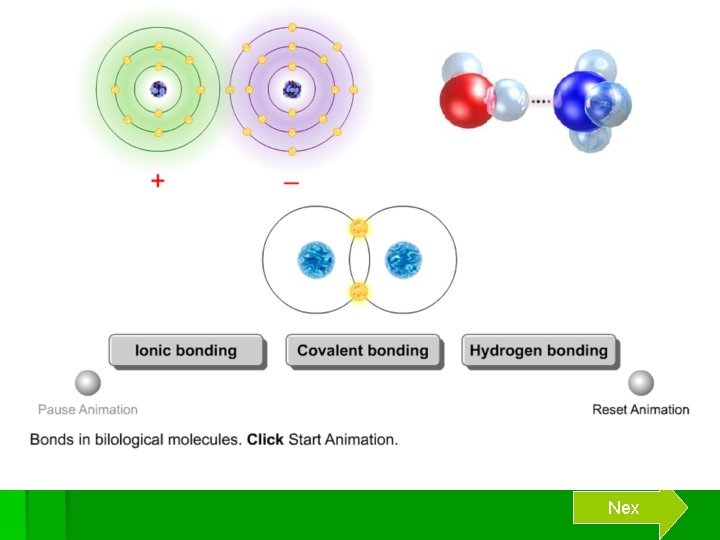
§ Hal itu dapat dilakukan dengan berikatan dengan unsur lain. Pada saat berikatan, suatu unsur dapat melepas atau menerima electron sehingga mencapai konfigurasi yang sama dengan gas mulia. Unsur – unsur yang terdapat dalam suatu golongan yang memiliki electron valensi yang sama, sehingga unsur – unsur tersebut memiliki cara yang sama untuk mencapai kestabilan § Coba perhatikan gambar berikut !
Next
Nex
Next Reaksi atom Ca dengan Cl

Setelah memperhatikan tampilan berikut Back apa yang dapat anda simpulkan ?

§ Ikatan kimia adalah ikatan yang terjadi karena adanya gaya tarik antara partikel yang berikatan. jika unsur membentuk senyawa (membentuk ikatan kimia), unsur itu mengalami perubahan konfigurasi elektron gas mulia yang stabil. Next

§ Elektron terluar (elektron valensi) mempunyai peranan penting dalam pembentukan ikatan kimia. § Pembentukan ikatan kimia terjadi karena perpindahan elektron dari satu atom ke atom lain. Atom yang melepas elektron membentuk ion positif, sedangkan atom yang menerima electron membentuk ion negative. Ikatan antara ion positif dan ion negative disebut ikatan ion. back

Latihan soal Uraian I. Tentukan jumlah elektron yang dapat dilepaskan atau diterima unsur-unsur berikut ini untuk mencapai kestabilannya? (Perhatikan tabel periodik) 1. Oksigen 4. kalium 2. Natrium 5. kalsium 3. Klor Next

II. Gambarkan susunan elektron valensi (struktur Lewis) dari unsur berikut. 1. Nitrogen 4. Belerang 2. Flour 5. Klor 3. Posfor Next

III. Dengan menggambarkan konfigurasi elektron, ilustrasikan ikatan ion yang terbentuk dari : 11 Na dengan 8 O 1. 12 Mg dengan 17 Cl 2. 20 Ca dengan 8 O 3. 19 K dengan 17 Cl 4. 5. 12 Mg dengan 8 O Next

Soal Objektif 1. Konfigurasi elektron yang manakah di bawah ini yang menunjukkan konfigurasi elektron gas mulia ? A. 3 X : 2 1 B. 12 W: 2 8 2 C. 18 Y : 2 8 8 D. 35 Z : 2 8 18 7 E. 46 R : 2 8 18 18 Back



§ Kasihan deh lu …… salah menjawab Coba lagi ………. dong ……. !
Cui………iiiiiii benar …. . Anda pintar



- Slides: 31