PEMBENTUKAN IKATAN MENURUT TEORI ORBITAL PEMBENTUKAN IKATAN MENURUT

PEMBENTUKAN IKATAN MENURUT TEORI ORBITAL
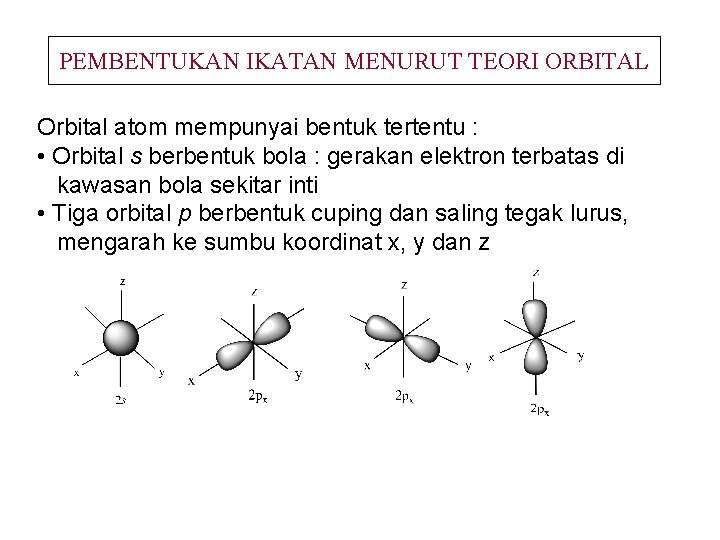
PEMBENTUKAN IKATAN MENURUT TEORI ORBITAL Orbital atom mempunyai bentuk tertentu : • Orbital s berbentuk bola : gerakan elektron terbatas di kawasan bola sekitar inti • Tiga orbital p berbentuk cuping dan saling tegak lurus, mengarah ke sumbu koordinat x, y dan z
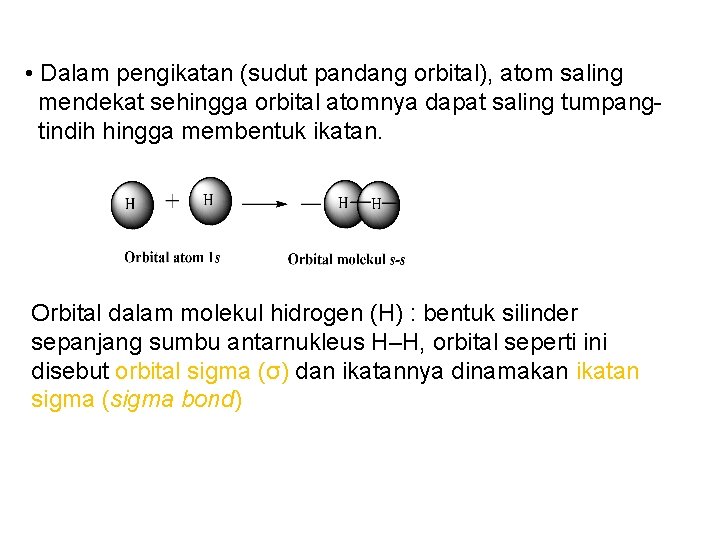
• Dalam pengikatan (sudut pandang orbital), atom saling mendekat sehingga orbital atomnya dapat saling tumpangtindih hingga membentuk ikatan. Orbital dalam molekul hidrogen (H) : bentuk silinder sepanjang sumbu antarnukleus H–H, orbital seperti ini disebut orbital sigma (σ) dan ikatannya dinamakan ikatan sigma (sigma bond)
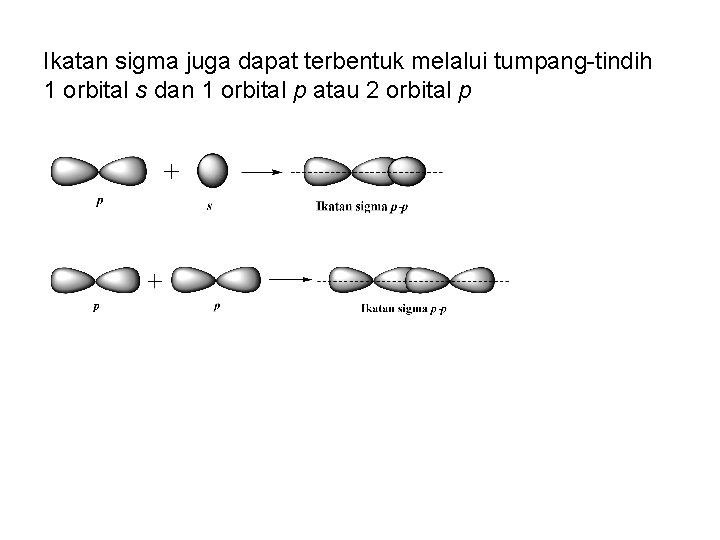
Ikatan sigma juga dapat terbentuk melalui tumpang-tindih 1 orbital s dan 1 orbital p atau 2 orbital p

PEMBENTUKAN IKATAN MENURUT ORBITAL HIBRIDISASI Hibridisasi– istilah yang digunakan untuk pencampuran orbital 2 atom dalam satu atom. 1. Merupakan pencampuran dari sedikitnya dua orbital atom yang tidak setara. 2. Jumlah orbital hibrida yg dihasilkan sama dengan jumlah orbital atom asli yang terlibat dalam proses hibridisasi 3. Hibridisasi membutuhkan energi; tetapi sistem memperoleh kembali energi ini, bahkan lebih selama pembentukan ikatan. 4. Ikatan kovalen terbentuk akibat tumpang-tindihnya orbital hibrida dengan orbital yang tidak terhibridisasi.

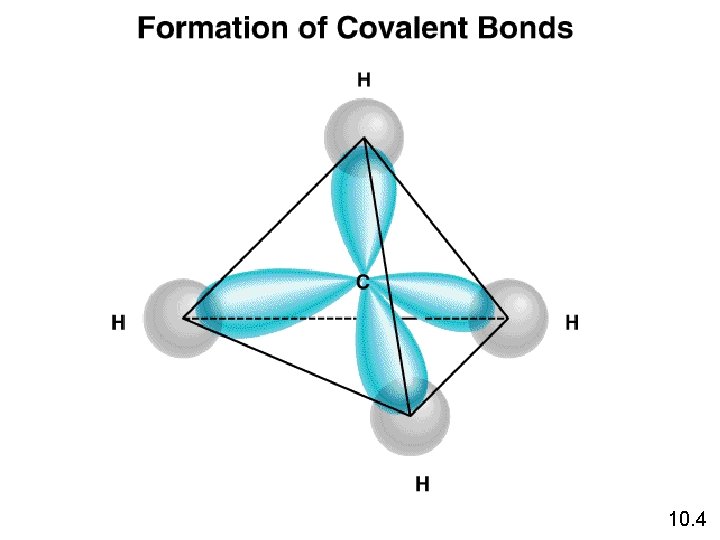
Orbital Hibrida Sp 3 karbon Berdasar konfigurasi di atas, salah tafsir bahwa karbon : hanya membentuk 2 ikatan (orbital 2 p yang ½ terisi atau 3 ikatan jika ada beberapa atom yang menyumbangkan 2 elektron pada orbital 2 p yang kosong
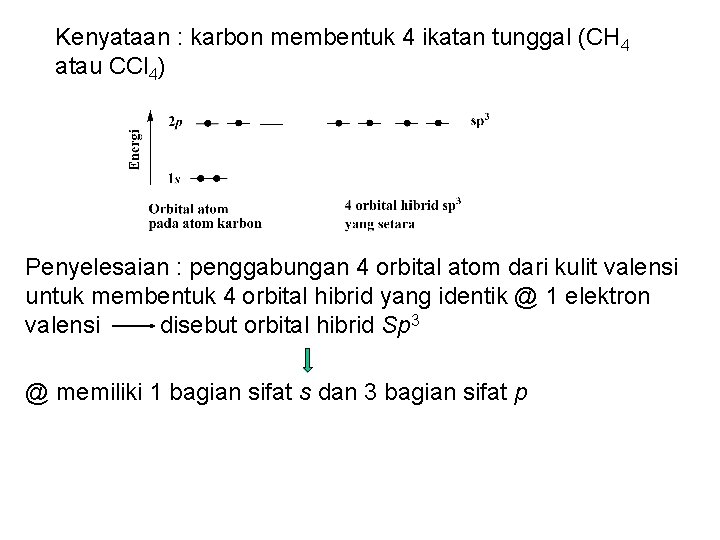
Kenyataan : karbon membentuk 4 ikatan tunggal (CH 4 atau CCl 4) Penyelesaian : penggabungan 4 orbital atom dari kulit valensi untuk membentuk 4 orbital hibrid yang identik @ 1 elektron valensi disebut orbital hibrid Sp 3 @ memiliki 1 bagian sifat s dan 3 bagian sifat p
10. 4
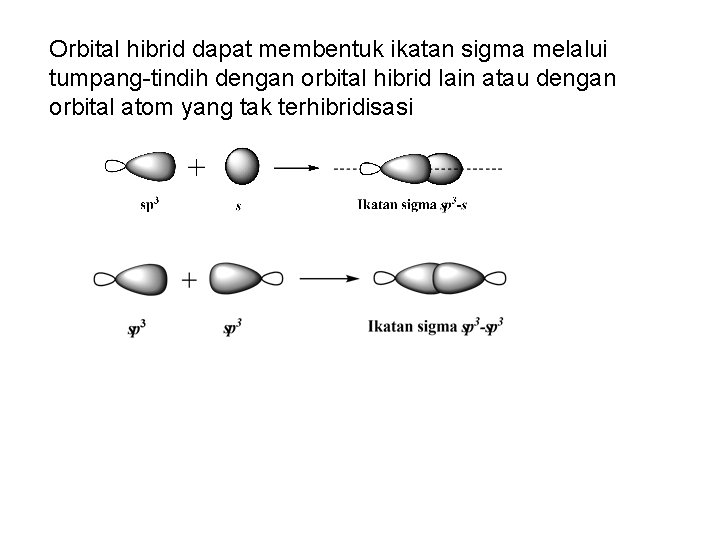
Orbital hibrid dapat membentuk ikatan sigma melalui tumpang-tindih dengan orbital hibrid lain atau dengan orbital atom yang tak terhibridisasi
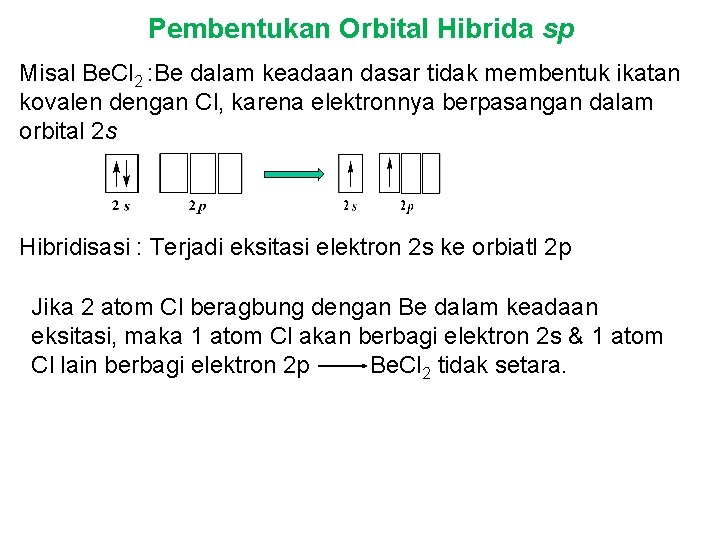
Pembentukan Orbital Hibrida sp Misal Be. Cl 2 : Be dalam keadaan dasar tidak membentuk ikatan kovalen dengan Cl, karena elektronnya berpasangan dalam orbital 2 s Hibridisasi : Terjadi eksitasi elektron 2 s ke orbiatl 2 p Jika 2 atom Cl beragbung dengan Be dalam keadaan eksitasi, maka 1 atom Cl akan berbagi elektron 2 s & 1 atom Cl lain berbagi elektron 2 p Be. Cl 2 tidak setara.
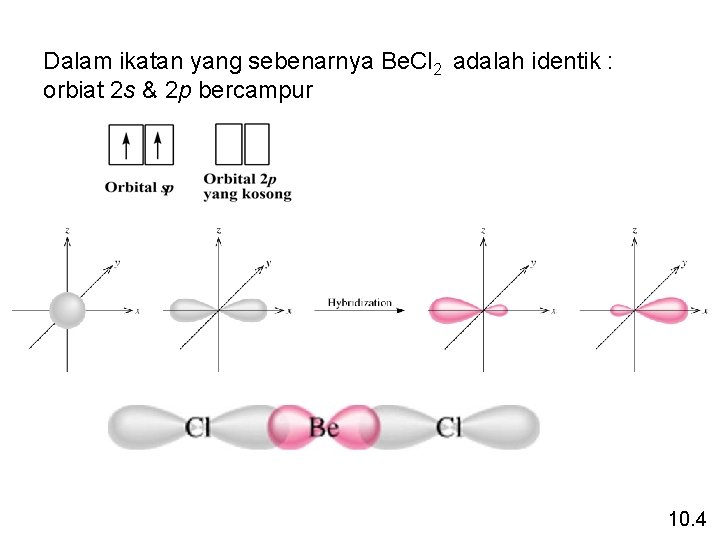
Dalam ikatan yang sebenarnya Be. Cl 2 adalah identik : orbiat 2 s & 2 p bercampur 10. 4
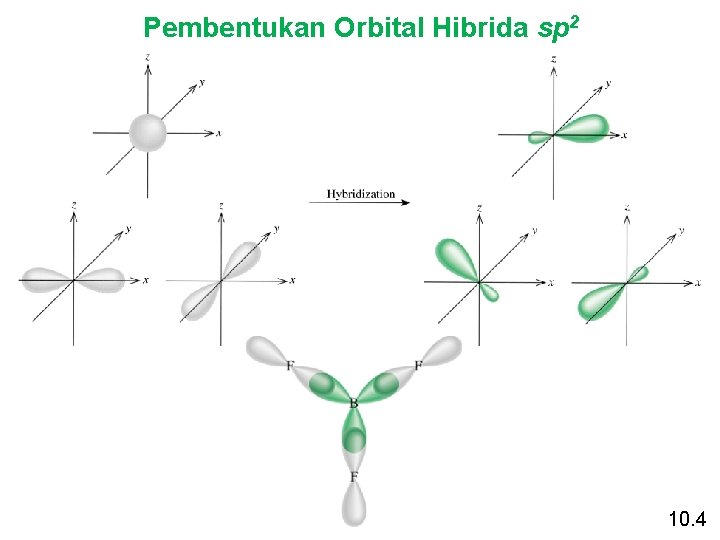
Pembentukan Orbital Hibrida sp 2 10. 4
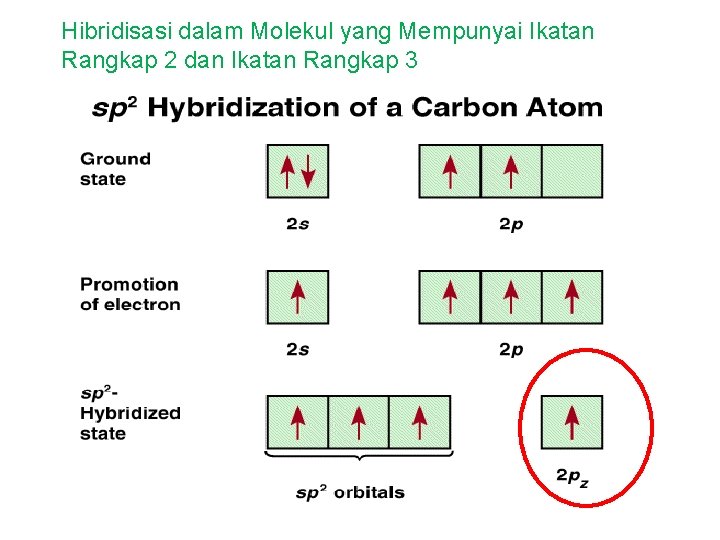
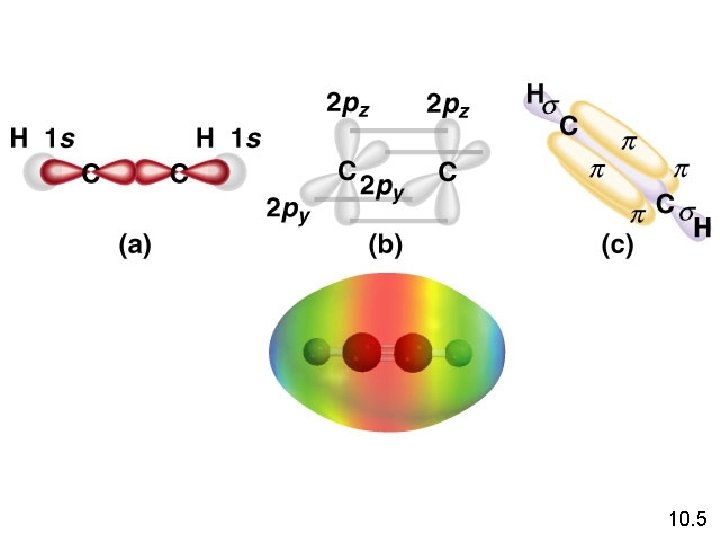
Hibridisasi dalam Molekul yang Mempunyai Ikatan Rangkap 2 dan Ikatan Rangkap 3
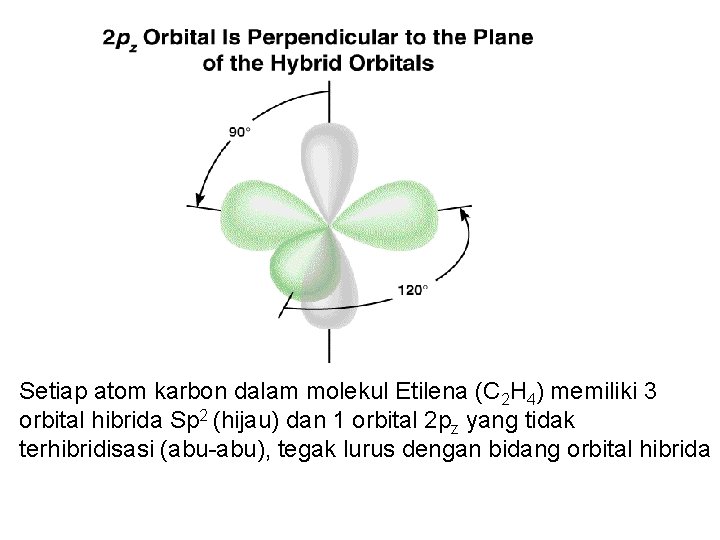
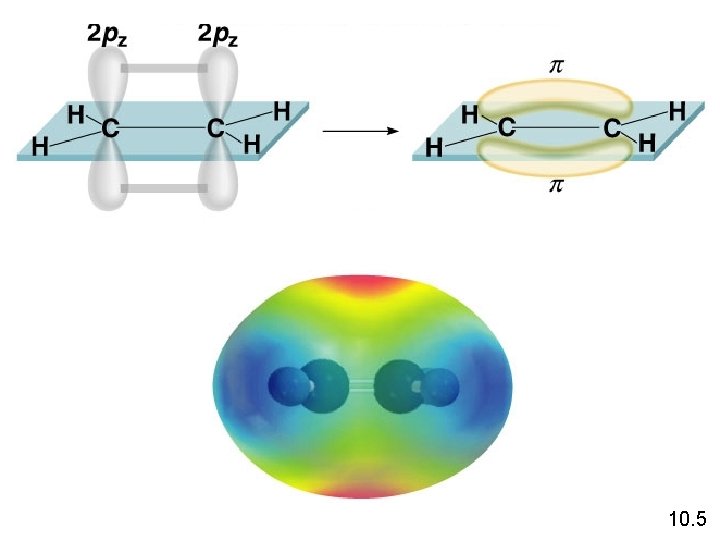
Setiap atom karbon dalam molekul Etilena (C 2 H 4) memiliki 3 orbital hibrida Sp 2 (hijau) dan 1 orbital 2 pz yang tidak terhibridisasi (abu-abu), tegak lurus dengan bidang orbital hibrida
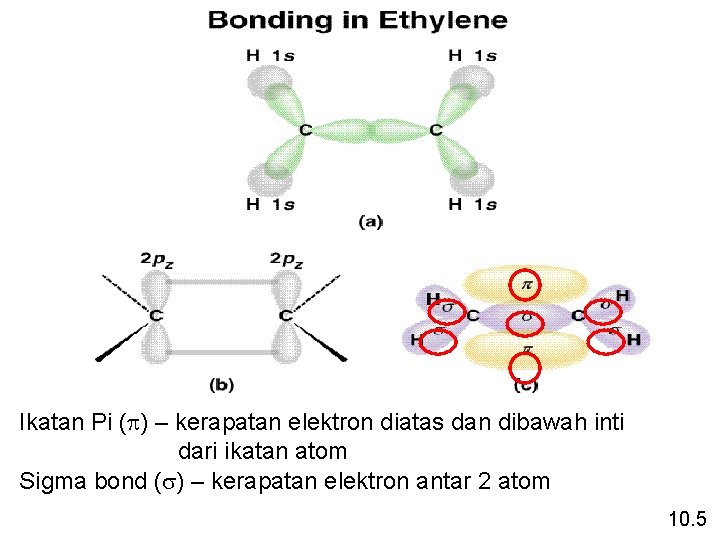
Ikatan Pi (p) – kerapatan elektron diatas dan dibawah inti dari ikatan atom Sigma bond (s) – kerapatan elektron antar 2 atom 10. 5
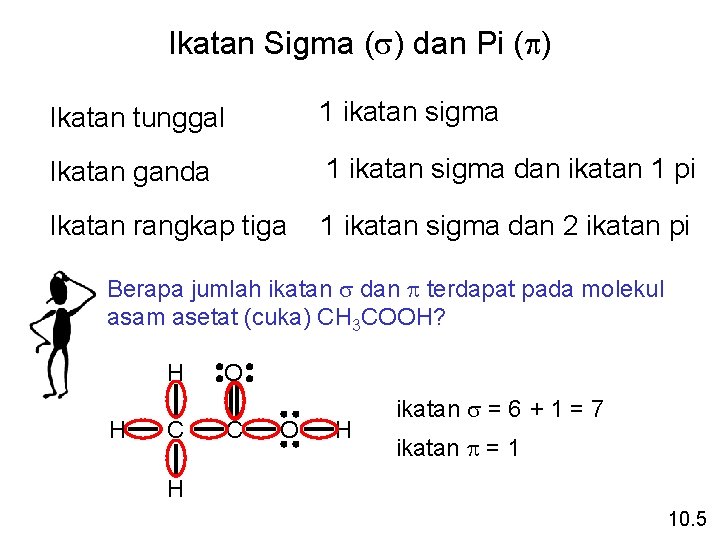
Ikatan Sigma (s) dan Pi (p) Ikatan tunggal 1 ikatan sigma Ikatan ganda 1 ikatan sigma dan ikatan 1 pi Ikatan rangkap tiga 1 ikatan sigma dan 2 ikatan pi Berapa jumlah ikatan s dan p terdapat pada molekul asam asetat (cuka) CH 3 COOH? H C O H ikatan s = 6 + 1 = 7 ikatan p = 1 H 10. 5
10. 5
10. 5

Daftar Pustaka 1. Hart, H. , Craine, L. E. , Hart, D. J. , 2003, Kimia Organik, Suatu Kuliah Singkat, Alih Bahasa : Achmadi, S. S. , Edisi ke-11, Penerbit Erlangga, Jakarta. 2. Chang, Raymond, 2003, Kimia Dasar : Konsep-Konsep Inti, Alih Bahasa : Martoprawiro, M. A. , Jilid 1/Edisi ke-3. , Penerbit Erlangga, Jakarta.
- Slides: 19