ASSALAMMUALAIKUM WR WB IKATAN KIMIA Ikatan Kimia Standar

ASSALAMMUALAIKUM WR. WB

IKATAN KIMIA
Ikatan Kimia Standar Kompetensi Indikator Kompetensi Dasar Materi

Memahami struktur atom, sifat-sifat periodik unsur

Membandingkan proses pembentukan ikatan ion, ikatan kovalen koordinasi, dan ikatan logam serta hubungannya dengan sifat fisik senyawa yang terbentuk.

Menjelaskan kecendrungan suatu unsur untuk mencapai kestabilannya. q Menjelaskan proses terbentuknya ikatan ion q Menjelaskan beda ikatan ion dan ikatan kovalen q Menjelaskan beda ikatan kovalen polar dan non polar q Menjelaskan contoh ikatan kovalen tunggal, rangkap dua, rangkap tiga dan koordinasi q
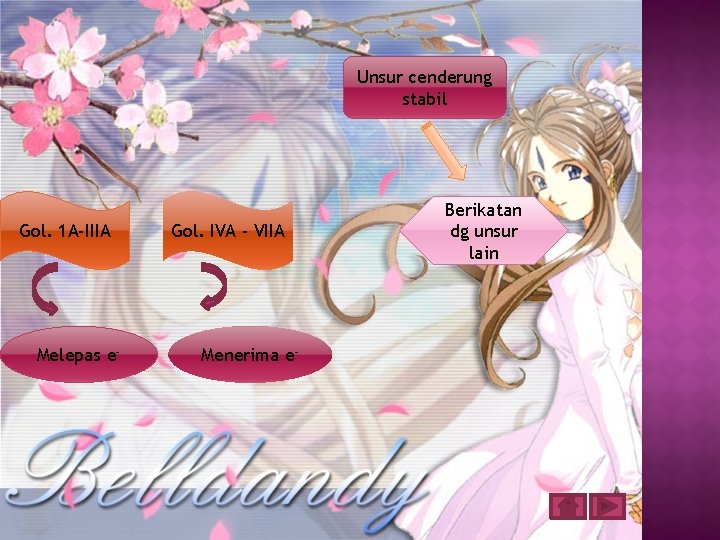
Unsur cenderung stabil Gol. 1 A-IIIA Melepas e- Gol. IVA - VIIA Menerima e- Berikatan dg unsur lain
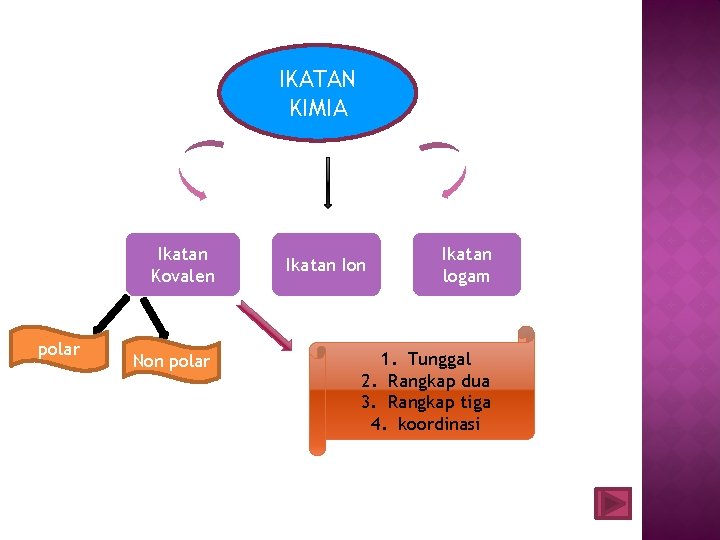
IKATAN KIMIA Ikatan Kovalen polar Non polar Ikatan Ion Ikatan logam 1. Tunggal 2. Rangkap dua 3. Rangkap tiga 4. koordinasi

BEDA IKATAN ION & KOVALEN Ø Ø IKATAN ION Memberi dan menerima elektron Tdd unsur logam (ion positif), unsur non logam (ion negatif) TD dan TL tinggi Wujud padat (pd T kamar) Ø Ø IKATAN KOVALEN Atom membentuk molekul dg memakai elektron bersamaan Tdd unsur non logam Dlm keadaan murni bersifat isolator Wujud padat, cair, atau gas (pd T kamar)
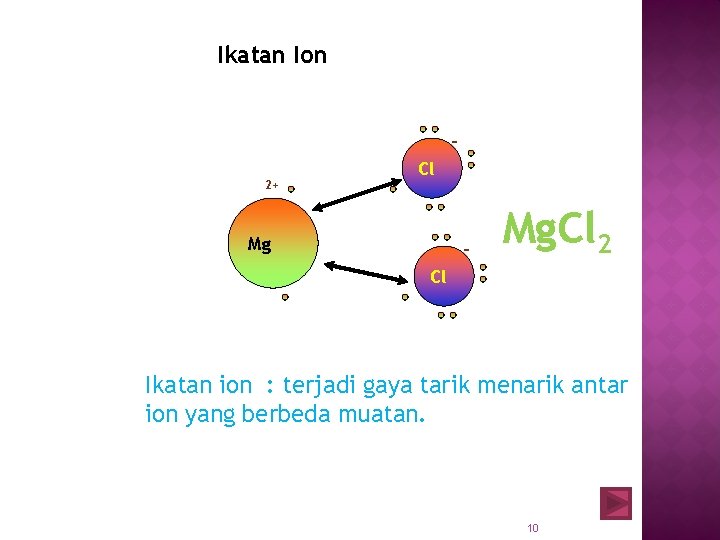
Ikatan Ion 2+ Cl Mg - Mg. Cl 2 Cl Ikatan ion : terjadi gaya tarik menarik antar ion yang berbeda muatan. 10

v Kovalen tunggal : kedua atom yg berikatan menyumbangkan 1 ev Kovalen rangkap 2 : kedua atom yg berikatan menyumbangkan 2 ev Kovalen rangkap 3 : kedua atom yg berikatan menyumbangkan 3 ev Kovalen koordinasi : elektron yg digunakan berikatan berasal dr 1 atom.
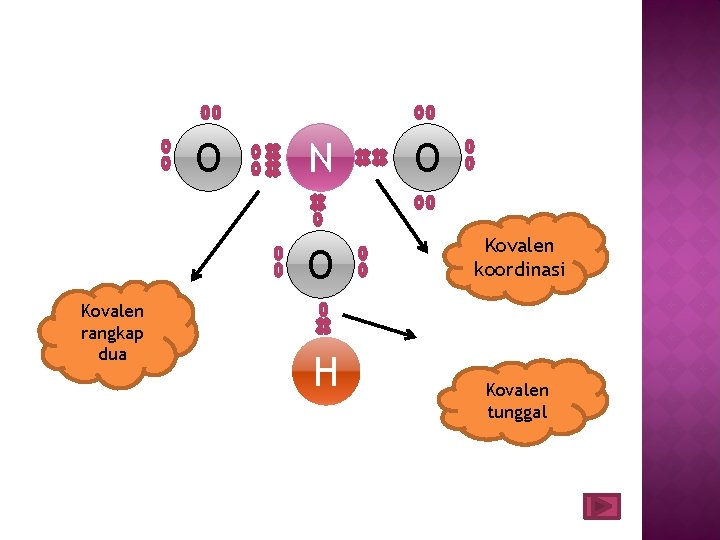
O N O Kovalen rangkap dua H O Kovalen koordinasi Kovalen tunggal
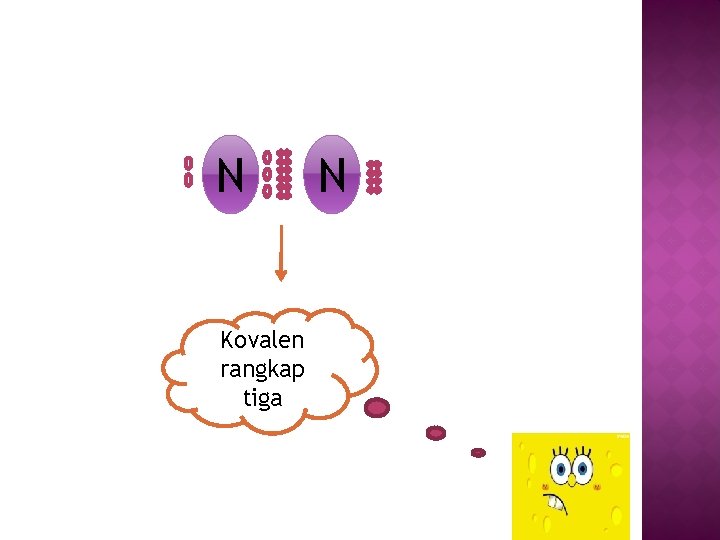
N Kovalen rangkap tiga N
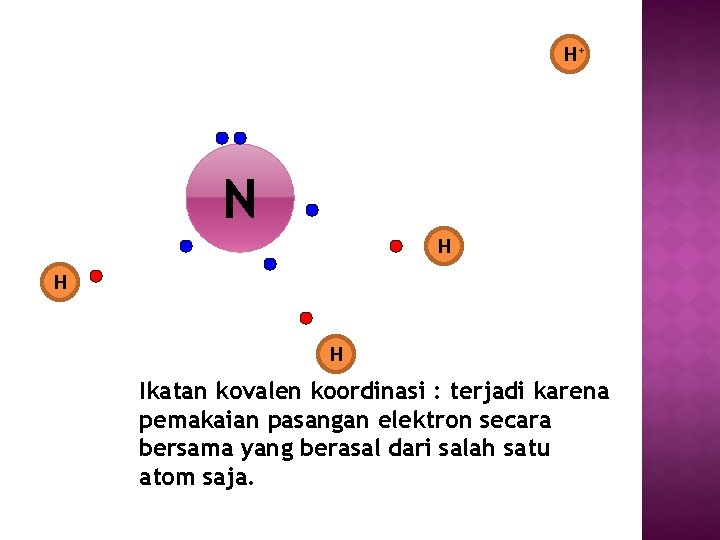
H+ N H H H Ikatan kovalen koordinasi : terjadi karena pemakaian pasangan elektron secara bersama yang berasal dari salah satu atom saja.

BEDA KOVALEN POLAR & NON POLAR ü ü ü Kovalen polar PEI tertarik lebih kuat ke salah satu atom Tdd 2 unsur berbeda Memiliki perbedaan keelektronegatifan Bentuk molekul tidak simetris Ada PEB di atom pusat ü ü ü Kovalen non polar PEI tertarik sama kuat ke seluruh atom Tdd dua unsur sama/beda Tidak memiliki perbedaan keelektronegatifan Bentuk molekul simetris Tidak ada PEB di atom pusat
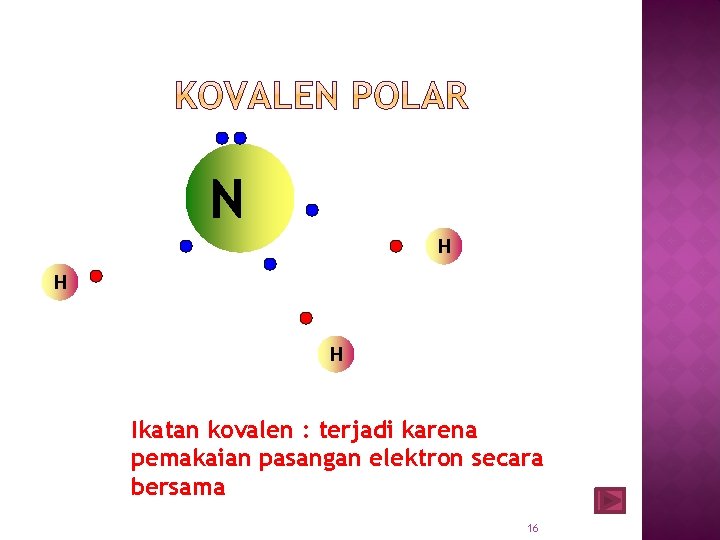
N H H H Ikatan kovalen : terjadi karena pemakaian pasangan elektron secara bersama 16
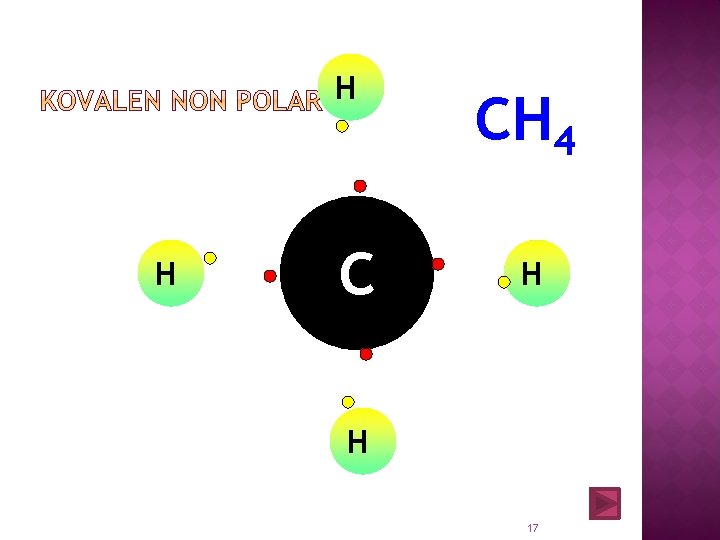
H H C CH 4 H H 17
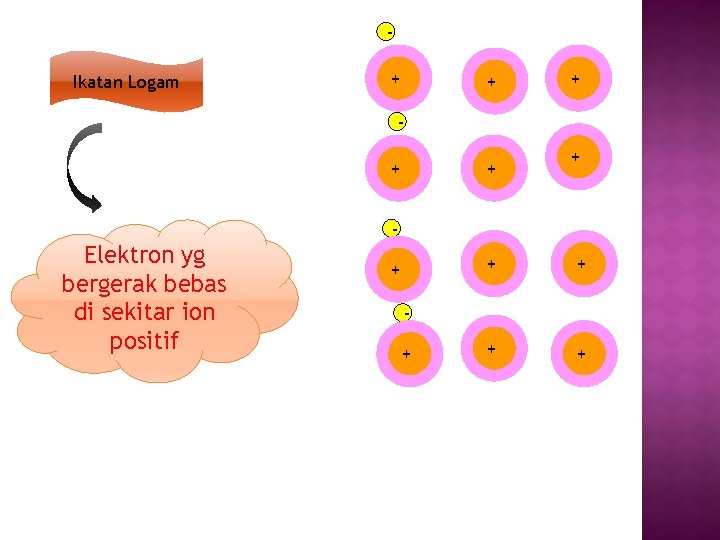
Ikatan Logam ++ ++ ++ - Elektron yg bergerak bebas di sekitar ion positif ++ ++ ++

THANK YOU
- Slides: 19