Pojem prvku alchymie Paracelsus 16 st alchymie teorie















- Slides: 46


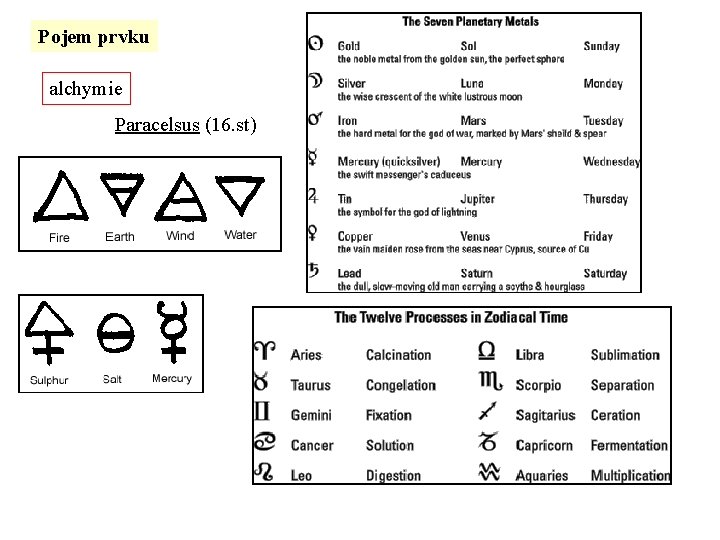
Pojem prvku alchymie Paracelsus (16. st)

alchymie …. teorie flogistonu 17. -18. st při hoření látky ztrácí těkavou součást - flogiston. látky = flogiston + popel (. . . nesouhlasila hmotnost) chemie kvantitativní záznamy postupů pojem čistá látka ‘přesné’ vážení Lavoisier: (1743– 1794) … zdokonalení střelného prachu … hmota (určená hmotností) zůstává zachována v průběhu reakcí. proces hoření, dýchání … 33 ‘prvků’, mj. caloric (teplo) voda = HO

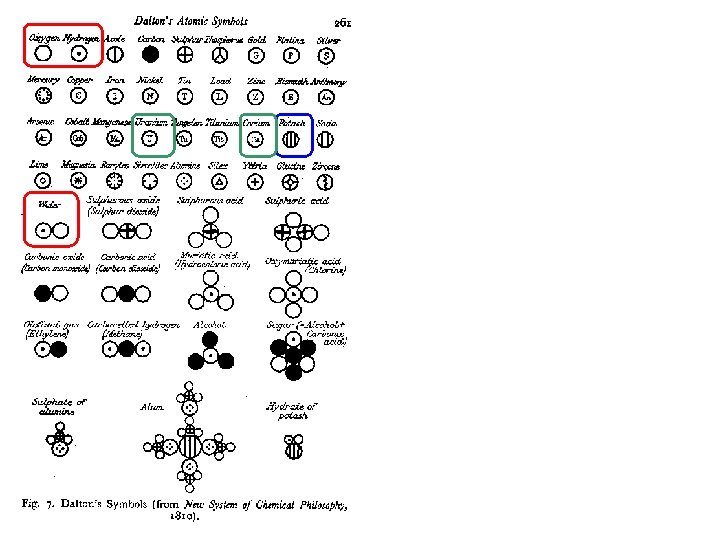
John Dalton (1766 -1844) … meteorologie … chemie: pojem prvku a sloučeniny: prvek - nedá se již rozložit na jiné prvky, sloučenina - rozložitelné C a O 2 sloučeniny, MO : MC = (1. 33: 1 nebo 2. 66: 1) CO, CO 2 zákony o stálých a množných poměrech slučovacích Atomová teorie: všechny prvky sestávají z malých částeček - atomů, ty jsou nedělitelné a neměnné všechny atomy daného prvku jsou stejné (stejná hmotnost) různé atomy různé hmotnosti (atomová váha) konečnýsoubor prvků (char. hmotnost) sloučenina = kombinace atomů více prvků (pevné poměry, případně násobné) chem. reakce = přeskupení kombinací atomů


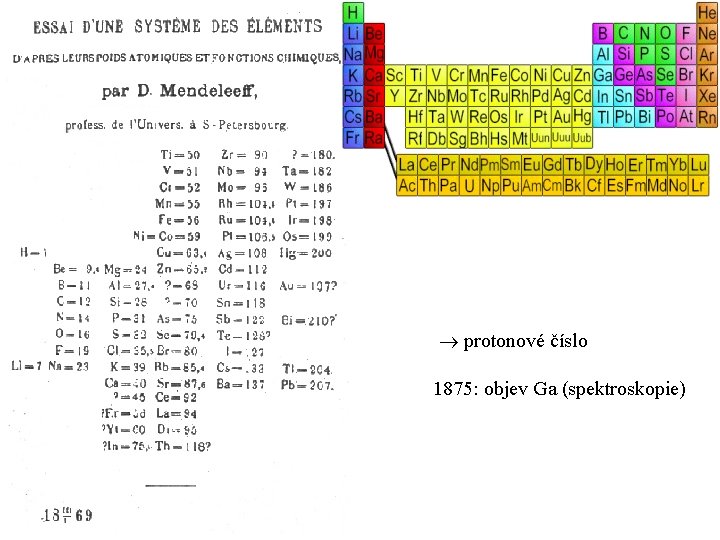
pojem prvku a optická spektroskopie vlastnosti prvků: - vážení (. . . Lavoisier, Dalton, . . . ) atomová váha (rel. at. hmotnost) - chemické chování tvorba sloučenin, oxidů, hydridů ~ 1860. . . molekula vs prvek, kvantitativní popis 1869: Mendeleev - periodická tabulka

protonové číslo 1875: objev Ga (spektroskopie)

kahan. . zbarvení plynu. . . atomová spektroskopie 1852 - Heidelberg objev Cs, Rb (1860)


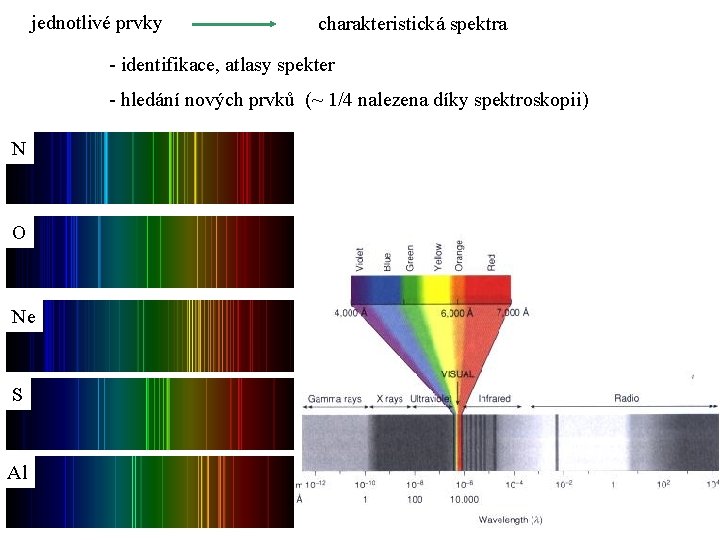
jednotlivé prvky charakteristická spektra - identifikace, atlasy spekter - hledání nových prvků (~ 1/4 nalezena díky spektroskopii) N O Ne S Al

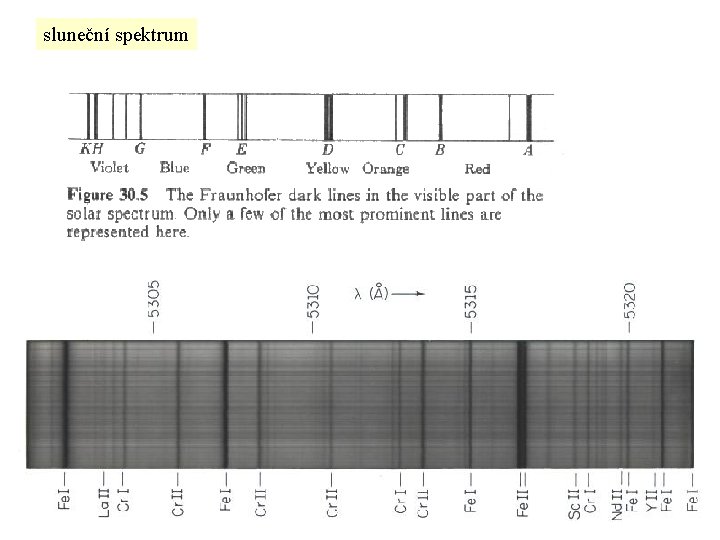
sluneční spektrum

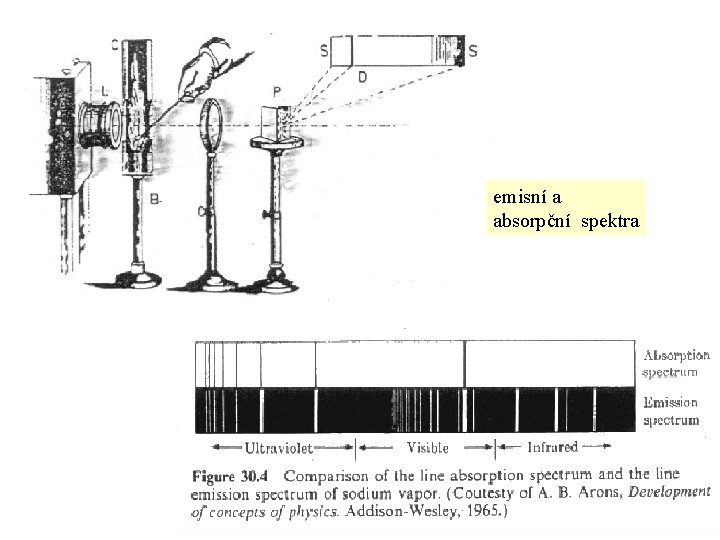
emisní a absorpční spektra

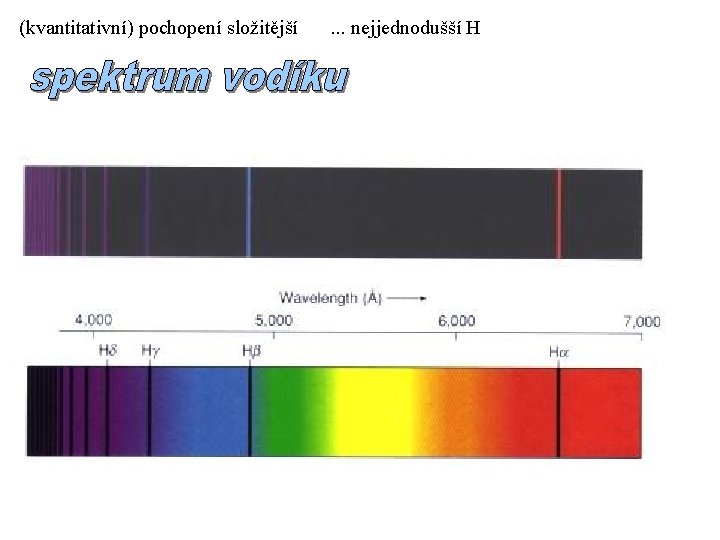
(kvantitativní) pochopení složitější . . . nejjednodušší H

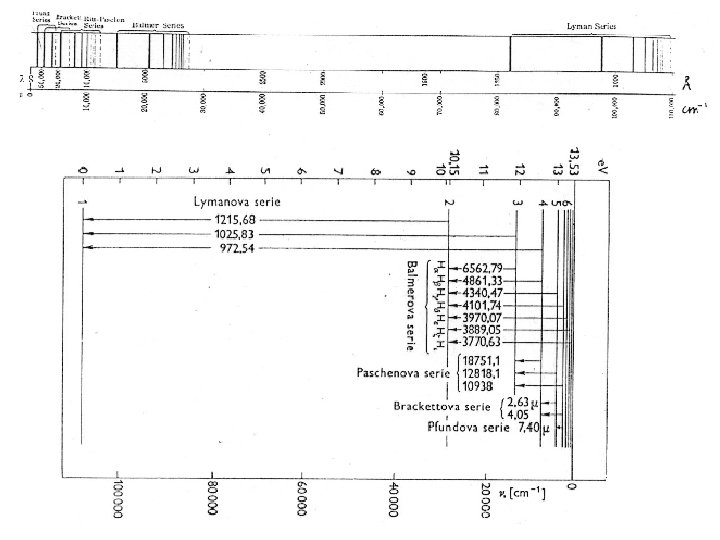
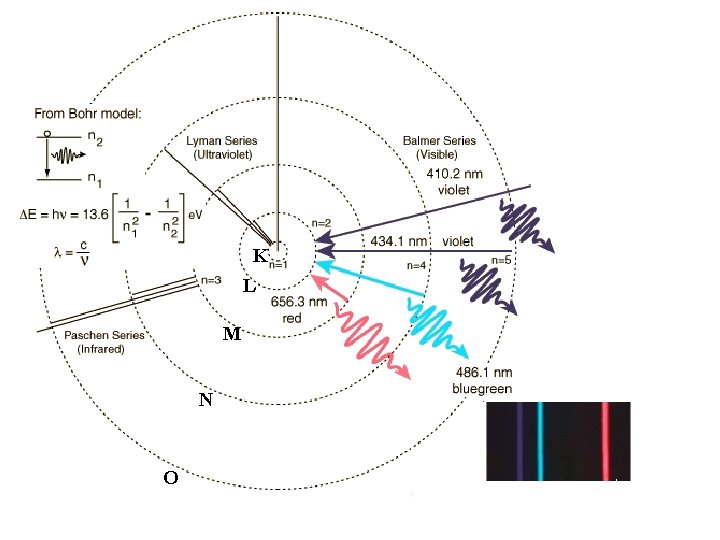
empirický popis vodíkového spektra: viditelný obor: 4 čáry H H H H n = 3, 4, 5, 6, . . . 1885: Balmerova série: objeveny další série 1906: Lymanova série: n = 2, 3, 4, . . . Ritz-Rydberg kombinačí princip: (1878 -1909) term: 1908: Paschenova série: . . . a další m = 4, 5, 6, . . . (IČ oblast)


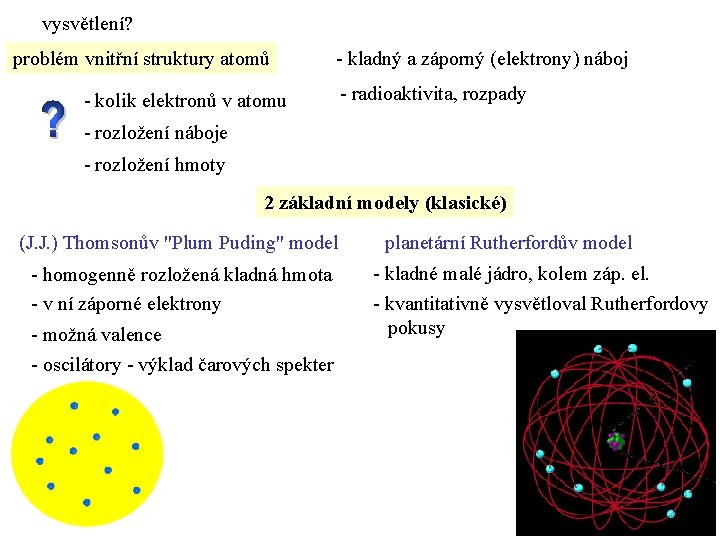
vysvětlení? problém vnitřní struktury atomů - kladný a záporný (elektrony) náboj - kolik elektronů v atomu - radioaktivita, rozpady - rozložení náboje - rozložení hmoty 2 základní modely (klasické) (J. J. ) Thomsonův "Plum Puding" model - homogenně rozložená kladná hmota - v ní záporné elektrony - možná valence - oscilátory - výklad čarových spekter planetární Rutherfordův model - kladné malé jádro, kolem záp. el. - kvantitativně vysvětloval Rutherfordovy pokusy

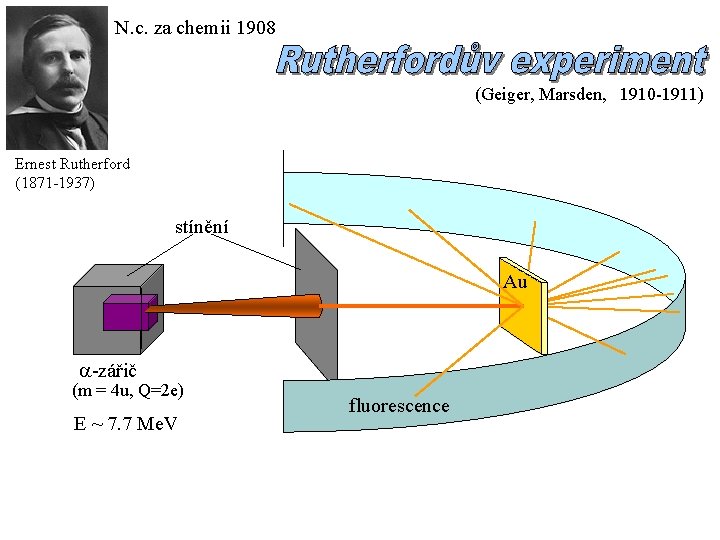
N. c. za chemii 1908 (Geiger, Marsden, 1910 -1911) Ernest Rutherford (1871 -1937) stínění Au -zářič (m = 4 u, Q=2 e) E ~ 7. 7 Me. V fluorescence

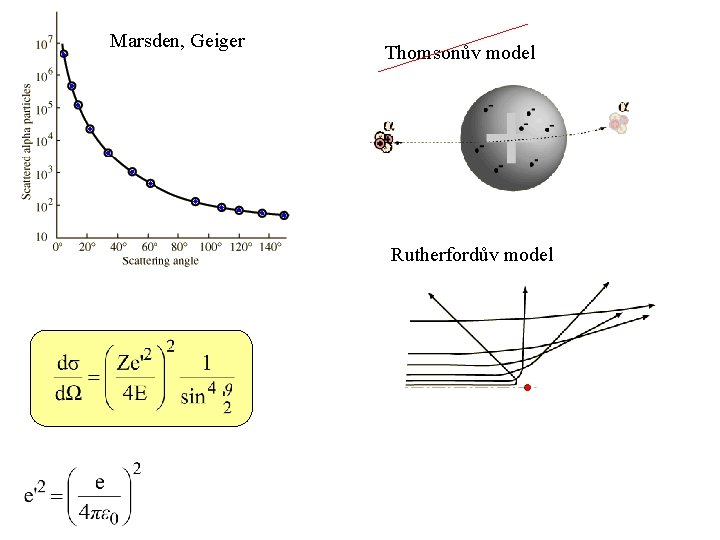
Marsden, Geiger Thomsonův model Rutherfordův model

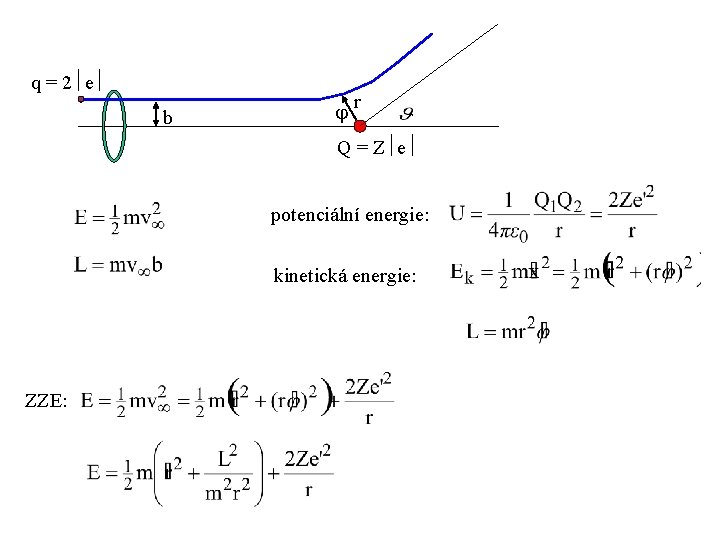
q = 2 e b r Q = Z e potenciální energie: kinetická energie: ZZE:

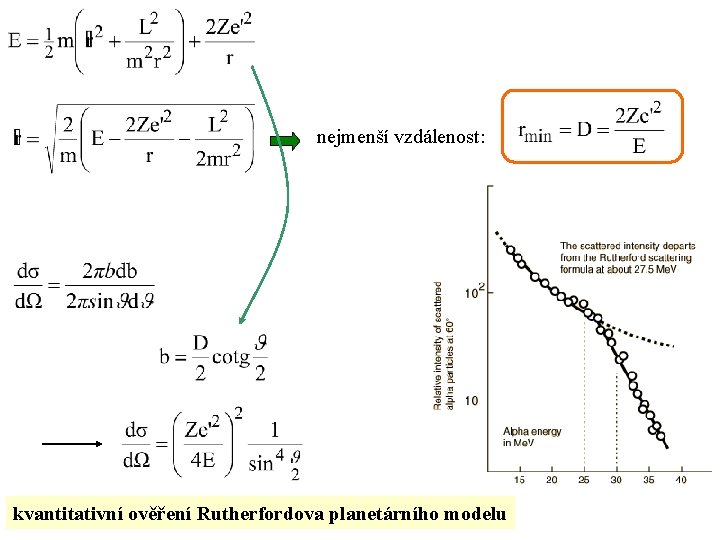
nejmenší vzdálenost: kvantitativní ověření Rutherfordova planetárního modelu

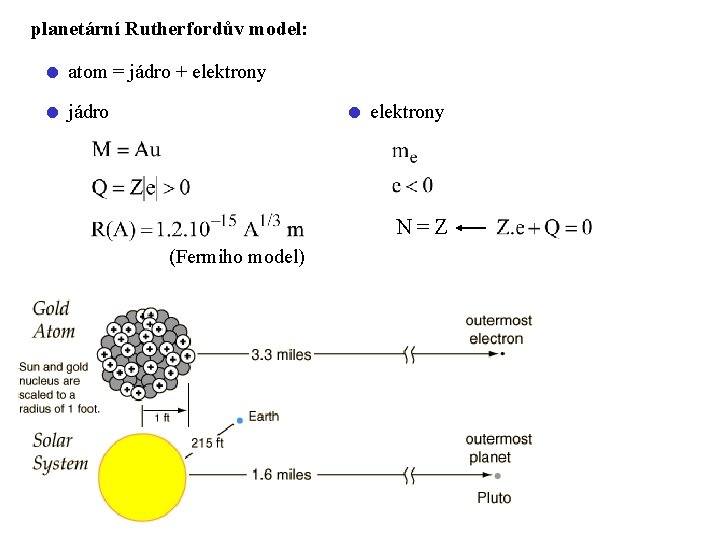
planetární Rutherfordův model: atom = jádro + elektrony jádro elektrony N=Z (Fermiho model)

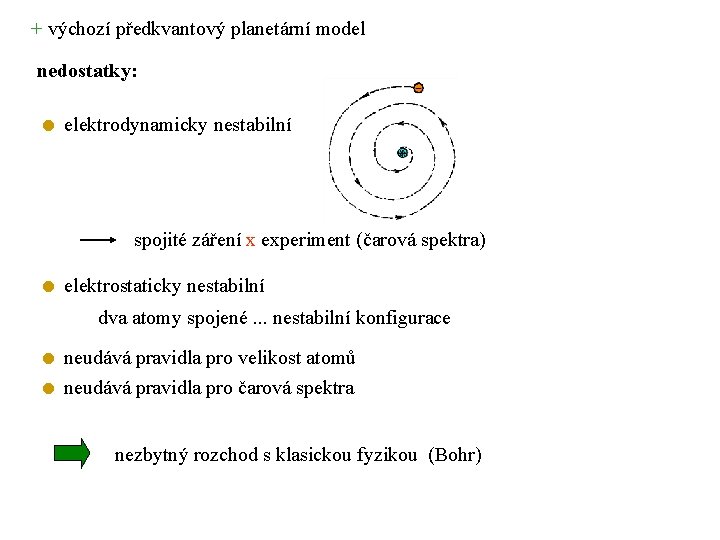
+ výchozí předkvantový planetární model nedostatky: elektrodynamicky nestabilní spojité záření x experiment (čarová spektra) elektrostaticky nestabilní dva atomy spojené. . . nestabilní konfigurace neudává pravidla pro velikost atomů neudává pravidla pro čarová spektra nezbytný rozchod s klasickou fyzikou (Bohr)

1) Elektrony krouží kolem jader po kruhových drahách. 2) Přípustné jsou jen vybrané stacionární orbity - na nich elektron obíhá a nezáří. 3) Stacionární orbity vybereme kvantováním momentu hybnosti: 4) Elektrony mohou přeskakovat mezi jednotlivými orbity; přeskoky jsou spojeny s vyzářením nebo pohlcením fotonu. Niels Bohr (1885 -1962) Aage Niels Bohr (*1922)

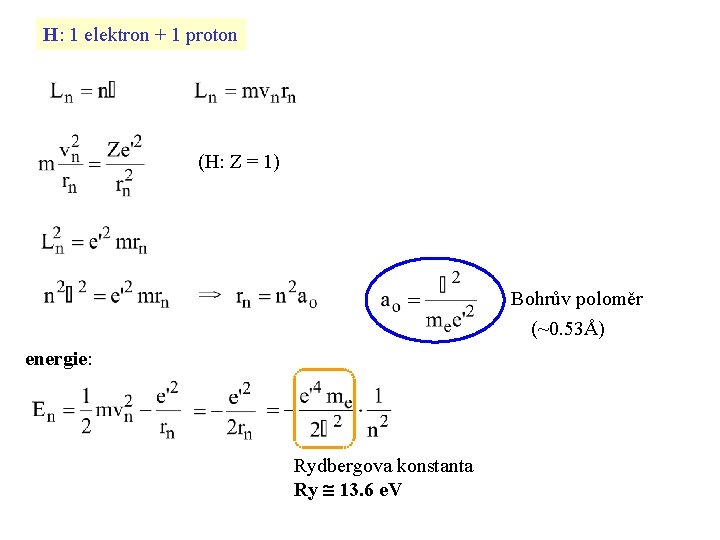
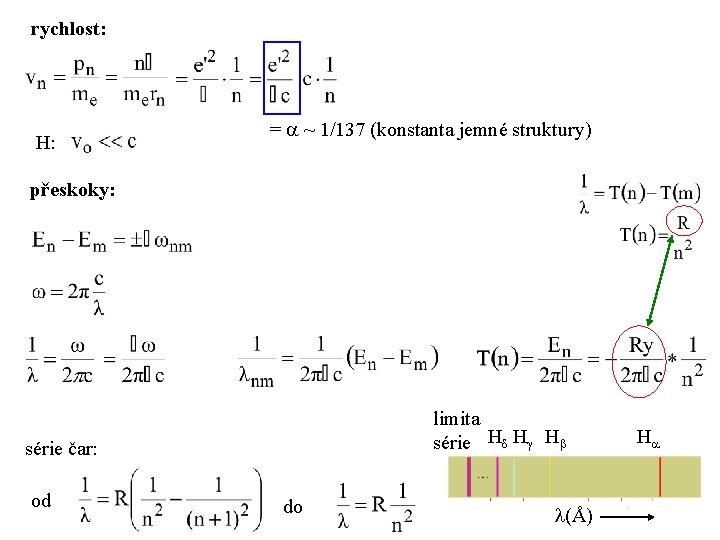
H: 1 elektron + 1 proton (H: Z = 1) Bohrův poloměr (~0. 53Å) energie: Rydbergova konstanta Ry 13. 6 e. V

rychlost: H: = ~ 1/137 (konstanta jemné struktury) přeskoky: limita série H H H série čar: od do (Å) H

K L M N O

(H: ~ Ry/1. 0005) Harold Clayton Urey (1893 - 1981) 1934: N. c. za chemii

komentář k Bohrovu modelu: - kvaziklasické přiblížení - přenesl ħ na hmotné soustavy (předtím pro popis fotonů) - inspirace pro Heisenberga a kvantový popis atomů (kvantový popis H: stejný výsledek jako Bohr) - neudává pravděpodobnosti přechodů – proč nějaká spektrální čára silnější než jiná? - elektron jako malá planeta s danou polohou a hybností x relace neurčitosti - nepodařilo se zobecnění na víceelektronové atomy (problém e-e interakce) nutný úplný kvantový popis

Bohr Schrödinger klasické orbity stacionární orbity kvantování L přeskoky centrálně sym. problém mohu separovat proměnné Zlaté pravidlo poruchového počtu

kvantové řešení úlohy vodíku (shrnutí):

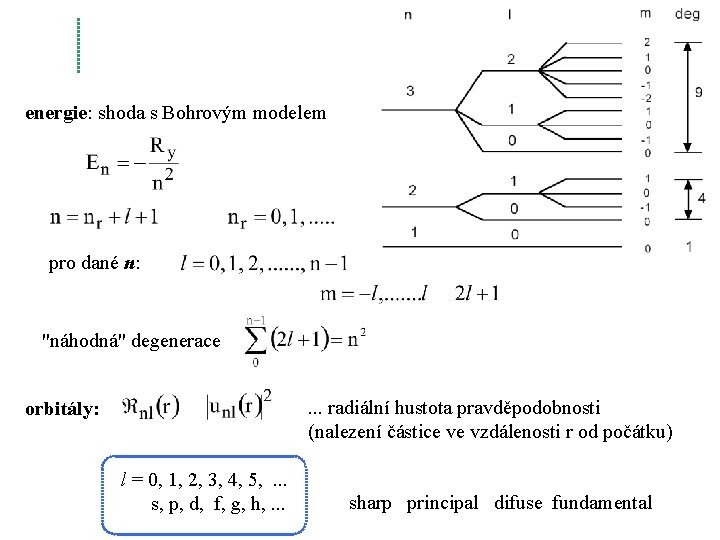
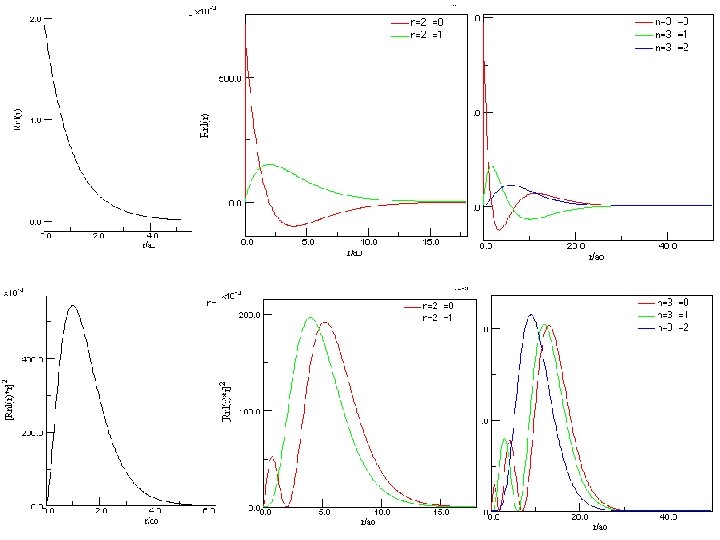
energie: shoda s Bohrovým modelem pro dané n: "náhodná" degenerace. . . radiální hustota pravděpodobnosti (nalezení částice ve vzdálenosti r od počátku) orbitály: l = 0, 1, 2, 3, 4, 5, . . . s, p, d, f, g, h, . . . sharp principal difuse fundamental


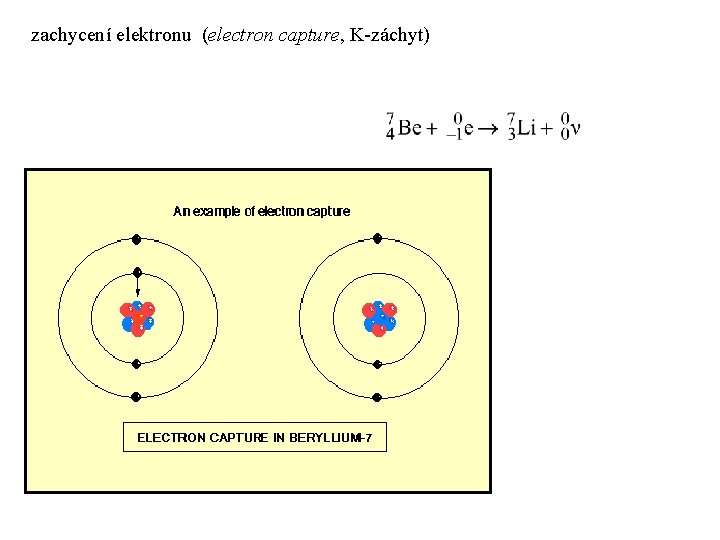
zachycení elektronu (electron capture, K-záchyt)

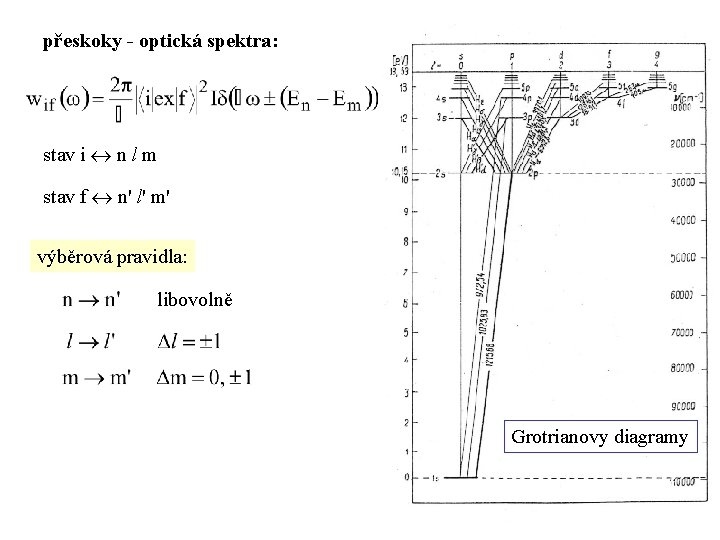
přeskoky - optická spektra: stav i n l m stav f n' l' m' výběrová pravidla: libovolně Grotrianovy diagramy

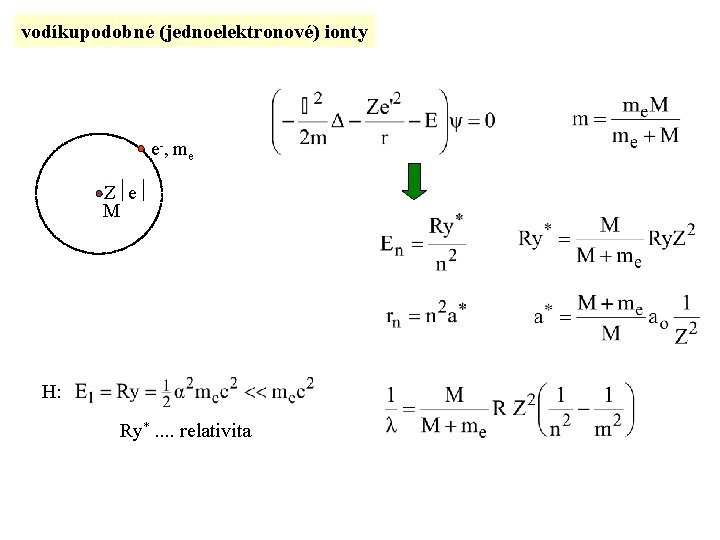
vodíkupodobné (jednoelektronové) ionty e-, me Z e M H: Ry*. . relativita

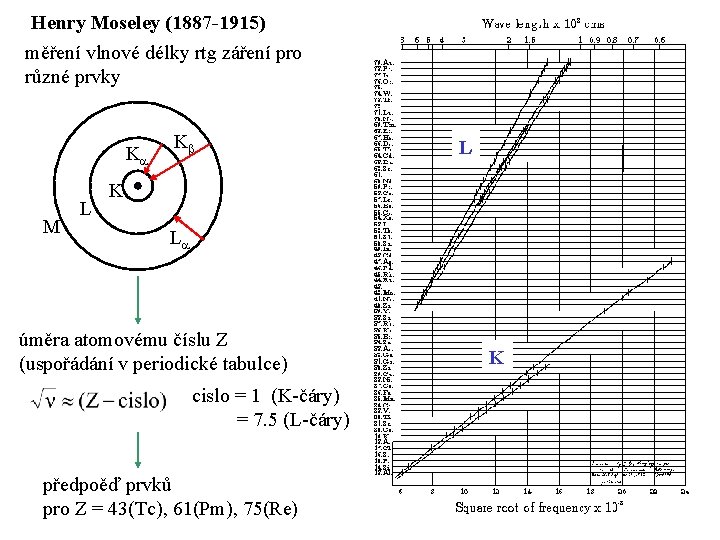
Henry Moseley (1887 -1915) měření vlnové délky rtg záření pro různé prvky K M L K L úměra atomovému číslu Z (uspořádání v periodické tabulce) cislo = 1 (K-čáry) = 7. 5 (L-čáry) předpoěď prvků pro Z = 43(Tc), 61(Pm), 75(Re) K

1 elektron. . . možné hladiny energie i. . . n, l, m více elektronů. . . obsazení jednotlivých hladin elektron má spin n, l, m, = 1 degenerace: n 2 2 n 2 Pauliho princip: žádný jednočásticový stav nemůže být obsazen více než 1 elektronem. v jednom atomu nemohou mít dva elektrony všechna 4 kv. č. stejná.

obecněji. . . N elektronů zjednodušení: 1 -elektronová aproximace elektron se pohybuje pod vlivem ostatních elektronů, ve středním poli které je v důsledku působení ostatních elektronů ("mean field") nábojová hustota Hartreeho rovnice hustota elektronů jako částic v r

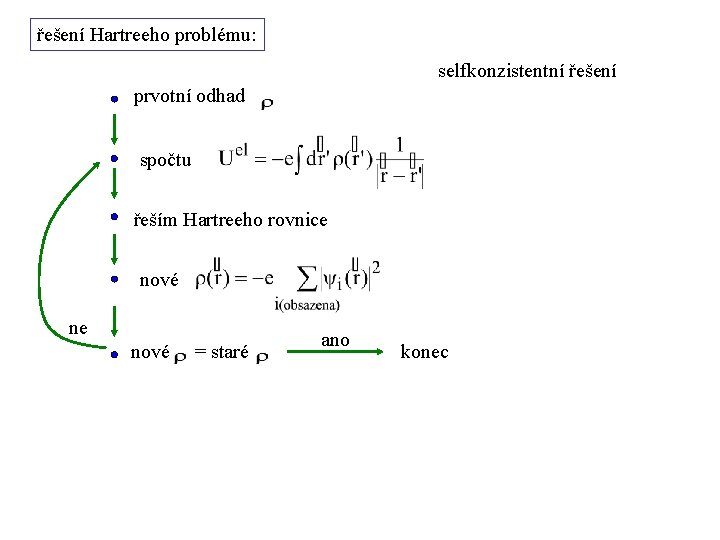
řešení Hartreeho problému: selfkonzistentní řešení prvotní odhad spočtu řeším Hartreeho rovnice nové ne nové = staré ano konec

Hartreeho přiblížení - nesplňuje podmínku antisymetrie zobecnění (splňuje AS) - Hartree-Fockova aproximace: H-F rovnice: Hartree + výměnný člen

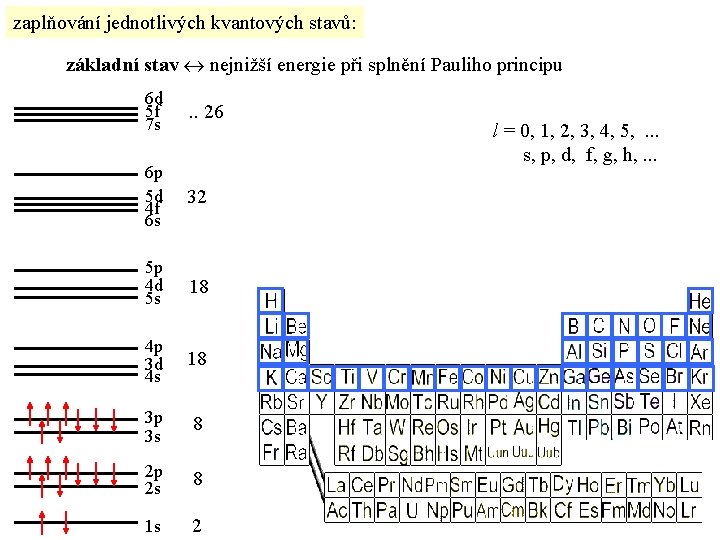
zaplňování jednotlivých kvantových stavů: základní stav nejnižší energie při splnění Pauliho principu 6 d 5 f 7 s . . 26 6 p 5 d 4 f 6 s 32 5 p 4 d 5 s 18 4 p 3 d 4 s 18 3 p 3 s 8 2 p 2 s 8 1 s 2 l = 0, 1, 2, 3, 4, 5, . . . s, p, d, f, g, h, . . .

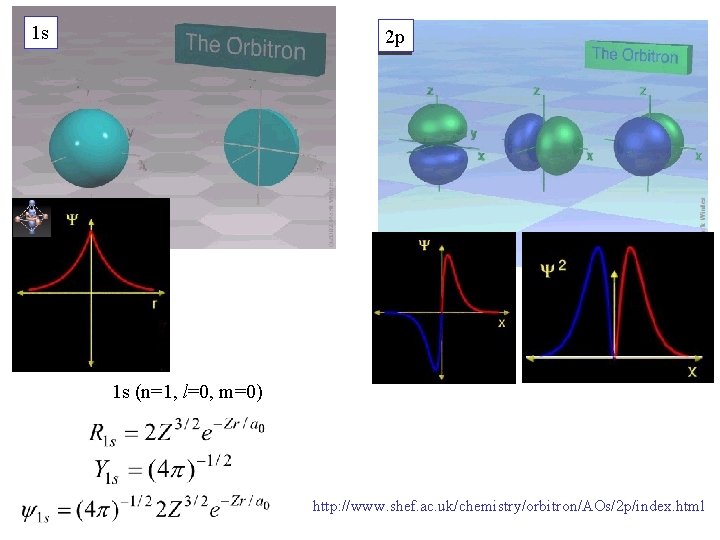
1 s 2 p 1 s (n=1, l=0, m=0) http: //www. shef. ac. uk/chemistry/orbitron/AOs/2 p/index. html

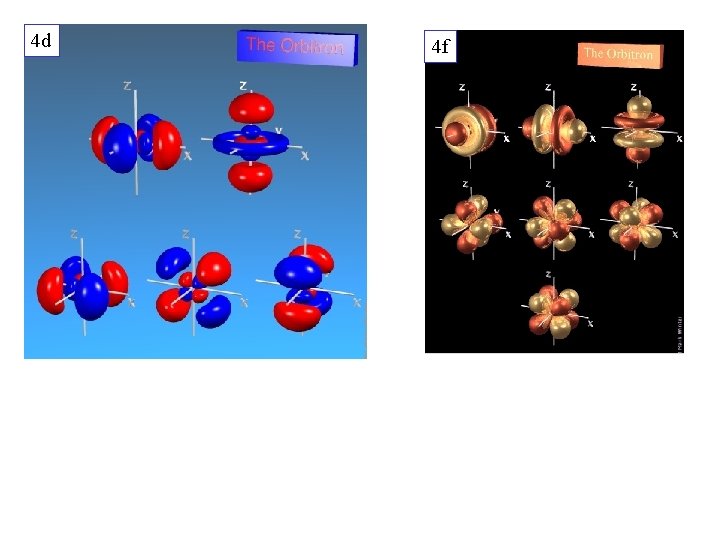
4 d 4 f

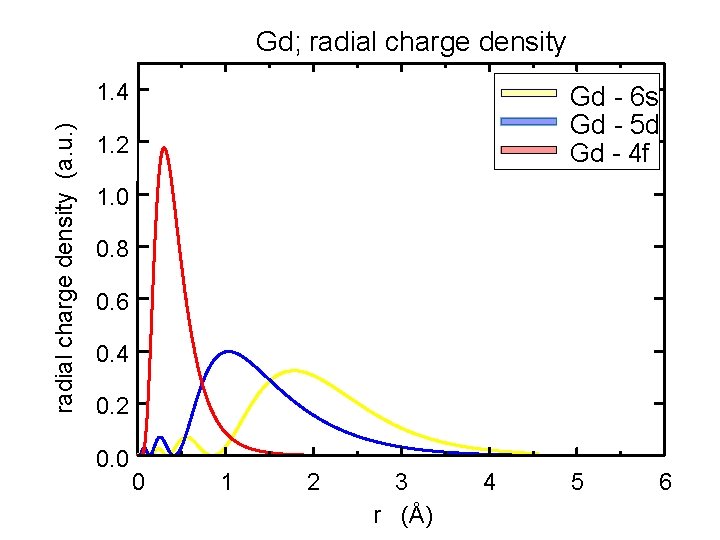
Gd; radial charge density (a. u. ) 1. 4 Gd - 6 s Gd - 5 d Gd - 4 f 1. 2 1. 0 0. 8 0. 6 0. 4 0. 2 0. 0 0 1 2 3 r (Å) 4 5 6

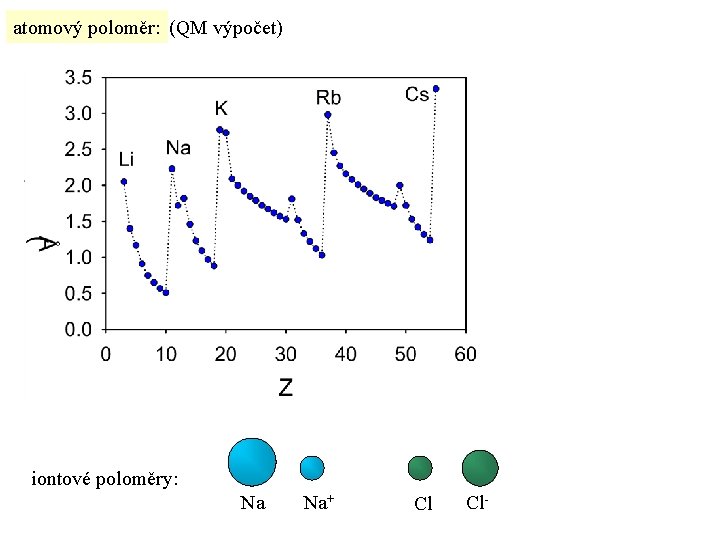
atomový poloměr: (QM výpočet) iontové poloměry: Na Na+ Cl Cl-

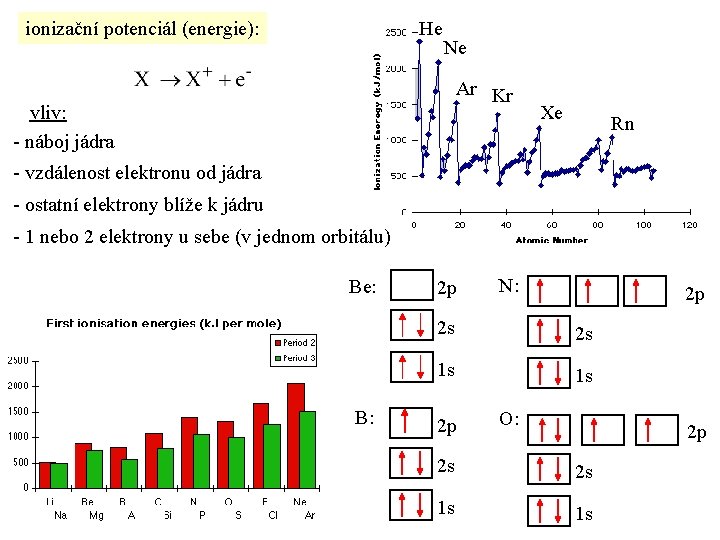
ionizační potenciál (energie): He Ne Ar Kr vliv: - náboj jádra Xe Rn - vzdálenost elektronu od jádra - ostatní elektrony blíže k jádru - 1 nebo 2 elektrony u sebe (v jednom orbitálu) Be: B: 2 p N: 2 p 2 s 2 s 1 s 1 s 2 p O: 2 p 2 s 2 s 1 s 1 s