nergie ractifs Cours de Cintique chimique produits temps
























- Slides: 31

énergie réactifs Cours de Cinétique chimique produits temps Guy COLLIN, 2014 -12 -29

Cinétique chimique énergie Chapitre 1 réactifs Caractères généraux de la cinétique des réactions homogènes produits temps 2014 -12 -29

CARACTÈRES GÉNÉRAUX DE LA CINÉTIQUE DES RÉACTIONS HOMOGÈNES énergie • Quel est le lien, quels sont les liens qui existent entre le déroulement réactifs d’une réaction chimique et le temps ? produits temps 2014 -12 -29

Objectifs spécifiques • Assimiler le vocabulaire utilisé. • Comprendre les différentes définitions de vitesse énergie de réaction. • Aborder les relations qui existent entre : – la vitesse d’une réaction et le mécanisme réactionnel ; – la vitesse de réaction et la température de réaction ; réactifs – la thermochimie et la cinétique chimique ; produits – … temps 2014 -12 -29

Notions de mécanismes élémentaires • Réaction élémentaire : A+B M+N énergie C’est une réaction qui a lieu en une étape, par exemple, au moment de la collision des deux réactifs Autre exemple : cyclo-C 4 H 8 2 C 2 H 4 produits temps • Molécularité : H 2 + I 2 2 HI, molécularité : 2 2014 -12 -29

Notions de mécanismes élémentaires • La succession d’étapes élémentaires énergie forme un mécanisme global : • réactifs Autre exemple : produits temps Réaction globale : 2 NO· + 2 H 2 O + N 2 2014 -12 -29

Vitesses de réaction : définitions • Soit la réaction a A + b B m M + n N énergie • Par rapport à un réactif, la vitesse totale est : v. A = - d. NA/dt ; v. M = + d. NM/dt • Par unité de volume V, la vitesse spécifique est : réactifs VA = v. A /V ; VM = v. M /V • À volume constant : produits Ø -1/V d. NA/dt = - 1/dt d(d. NA/V) = - d[A]/dt temps • À pression constante (le volume V varie). 2014 -12 -29

L’ordre d’une réaction • Soit la réaction a A + b B m M + n N énergie • Si VA = k [A]a [B] b • L’ordre partiel de la réaction est : a est l’ordre partiel par rapport à A, . . . • L’ordre global de la réaction est : réactifs a + b = s, s est l’ordre global. produits temps L’ordre est une notion expérimentale ! 2014 -12 -29

Réaction globale = réaction élémentaire : La règle de Van’t Hoff • Condition nécessaire : – ordres partiels coefficients stœchiométriques; – ordre global molécularité de la réaction. énergie réactifs • L’ordre global est égal à la molécularité. produits temps • En fait, est-on bien sûr du mécanisme ? 2014 -12 -29

La règle de Van’t Hoff • C’est une condition insuffisante. Exemple : énergie réactifs KT = [C]/([A] [B]) ou encore [C] = KT [A] [B] produits temps v = k [C] [D] = k KT [A] [B] [D] 2014 -12 -29

La règle de Van’t Hoff (suite) • Ordre simple mais différent de la énergie stœchiométrie : – la réaction n’est pas élémentaire, mais une suite de réactions élémentaires ; – ordre peu ou pas simple : la réaction est globale et peut-être même complexe. réactifs produits H 2 + Br 2 2 HBr temps k [H 2] [Br 2]1/2 où v = [HBr] 1 + k' [Br ] 2 2014 -12 -29

Principes guidant le choix d’un mécanisme réactionnel énergie • Grande simplicité. • Respect de la thermodynamique. • Changement très simple dans les structures. • En résumé, exercer son sens critique de réactifs chimiste. produits temps 2014 -12 -29

Nature de l’activation des processus de réaction énergie • L’activation peut être de nature : – thermique (pyrolyse) • CH 3 -N=N-CH 3 C 2 H 6 + N 2 ( 400 ˚C) – photochimique (photolyse, radiolyse) • iso-C 4 H 8 + hn H + CH 3 + C 3 H 4 réactifs – électrochimique (l’électrolyse) • électrolyse de l’alumine –. . . produits temps 2014 -12 -29

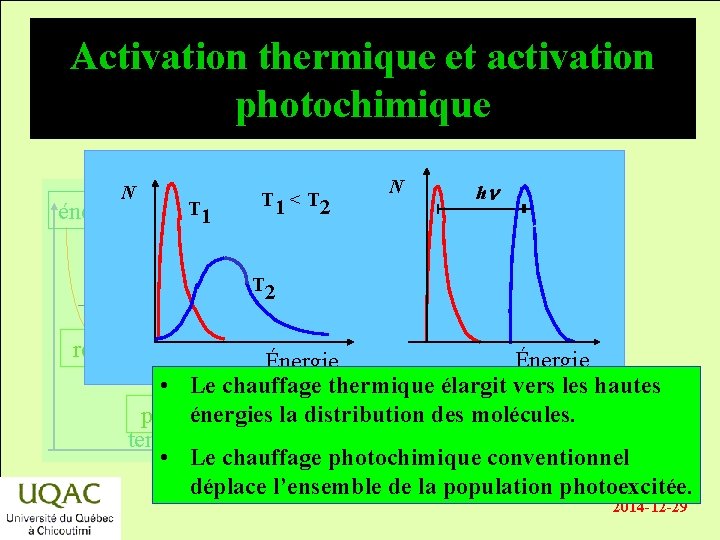
Activation thermique et activation photochimique N énergie T 1 < T 2 N hn T 2 réactifs Énergie • Le chauffage thermique élargit vers les hautes énergies la distribution des molécules. produits temps • Le chauffage photochimique conventionnel déplace l’ensemble de la population photoexcitée. 2014 -12 -29

Nature des entités participant aux actes élémentaires • Les formes réactives (en plus des espèces elles-mêmes). énergie • Les formes intermédiaires. – Exemple : forme énolisée des cétones. • Les atomes : réactifs produits temps – • H, • Cl, • Br, He, . . . • Les radicaux libres : – • CH 3, • C 2 H 5, . . . • Les ions positifs et négatifs : – NH 4+, Cl -, OH -, . . . 2014 -12 -29

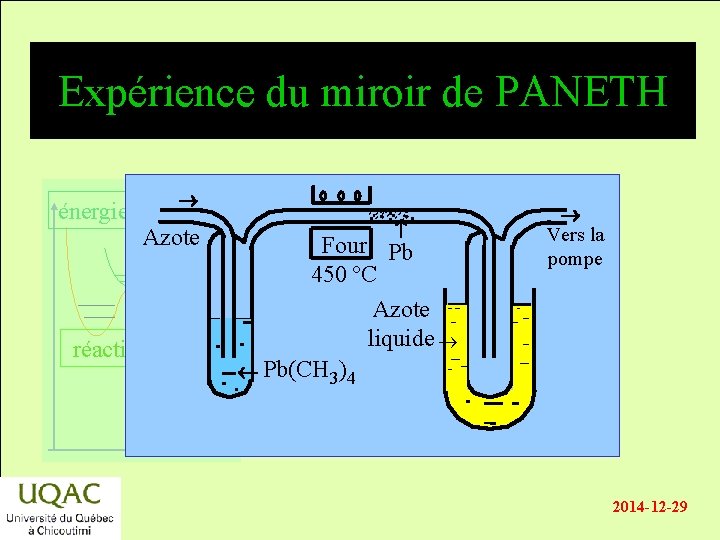
Expérience du miroir de PANETH énergie Azote réactifs Four Pb 450 ºC Azote liquide Pb(CH 3)4 Vers la pompe produits temps 2014 -12 -29

Dispositif de POLANYI énergie CH Cl 3 réactifs Na CH 3 Cl + Na CH 3 + I 2 CH 3 I Na. Cl I 2 produits temps La décomposition du CH 3 Cl libère des radicaux méthyles qui réagissent avec l’iode. 2014 -12 -29

Influence de la température sur la vitesse de réaction • La constante de vitesse (coefficient de vitesse) : – V = k. T ƒ([A], [B], …); énergie – k. T ne dépend que de T. • L’équation d’ARRHÉNIUS : réactifs – Ln k. T = B - C/T • L’énergie d’activation : – k. T = A e-Ea/RT produits temps • L’influence de la température : – Si T croît, k. T croît. 2014 -12 -29

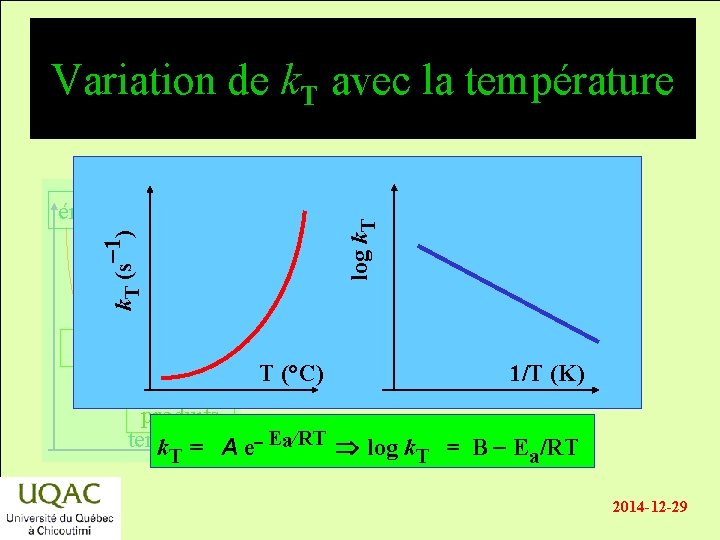
Variation de k. T avec la température k. T (s-1) log k. T énergie réactifs T (°C) 1/T (K) produits temps k. T = A e- Ea/RT log k. T = B - Ea/RT 2014 -12 -29

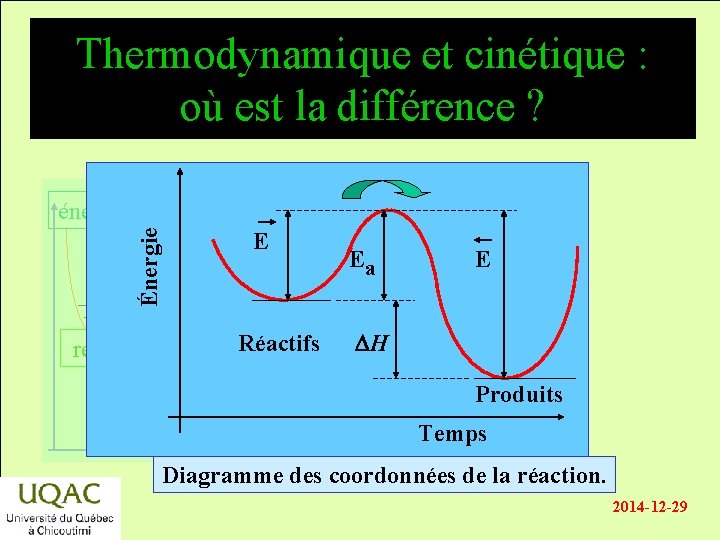
Thermodynamique et cinétique : où est la différence ? Énergie énergie E Réactifs réactifs produits temps Ea E DH Produits Temps Diagramme des coordonnées de la réaction. 2014 -12 -29

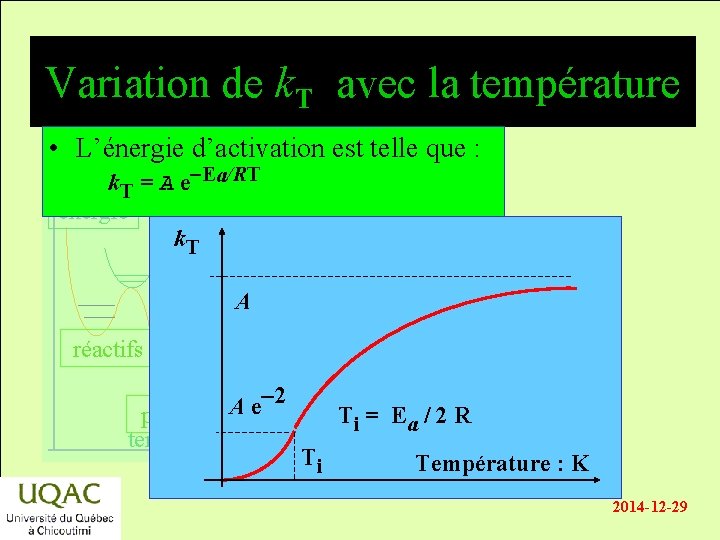
Variation de k. T avec la température • L’énergie d’activation est telle que : k. T = A e-Ea/RT énergie k. T A réactifs -2 A e produits temps Ti = E a / 2 R Ti Température : K 2014 -12 -29

Établissement d’un mécanisme réactionnel énergie • Méthodes expérimentales : – physiques : mesures électriques; – chimiques : titrages chimiques; – continues : spectroscopies; – discontinues : chromatographies; réactifs – destructives : titrages chimiques; produits – non destructives : mesures physiques. temps • Obligation du contrôle fin de T. 2014 -12 -29

Exemple de méthode expérimentale • Titrage acide – base : énergie – Exemple : hydrolyse en milieu acide, H+ ester + eau acide + alcool • Titrages chimiques : – Dosage de l’iode par le thiosulfate ; réactifs – Dosage des ions halogénures par Ag. NO 3 ; –. . . produits temps 2014 -12 -29

Exemple de méthode expérimentale • Variation de propriété physique : énergie – densité ; – Volume : • Acétal + eau aldéhyde + 2 alcools • Polymérisation en phase liquide, . . . réactifs – Masse : • Thermobalance : décomposition des carbonates Masse produits temps Température 2014 -12 -29

Exemple de méthode expérimentale Conductivité énergie Temps • Variation des propriétés électriques. • Par exemple, la conductivité électrique : Hydrolyse d’un ester par les ions OH - réactifs CH 3 COOC 2 H 5 + OH- CH 3 COO- + C 2 H 5 OH Les ions CH 3 COO- sont moins bons conducteurs que produits les ions OH -. temps 2014 -12 -29

Exemple de méthode expérimentale énergie • Variation dans le spectre d’absorption (infrarouge, visible, UV, Raman, RMN, …). Exemples : – CH 3 COCH 3 + Br 2 - + H+ CH COCH Br + Br réactifs 3 2 – On suit la disparition du brome par spectroscopie dans le visible. . . produits temps 2014 -12 -29

Exemple de méthode expérimentale énergie réactifs • Variations de l’indice de réfraction, du pouvoir rotatoire. • Exemple : inversion du sucrose C 12 H 22 O 11 + H 2 O + H+ C 6 H 12 O 6 + H + produits temps Le pouvoir rotatoire du sucrose est différent de la somme de ceux des deux sucres formés. 2014 -12 -29

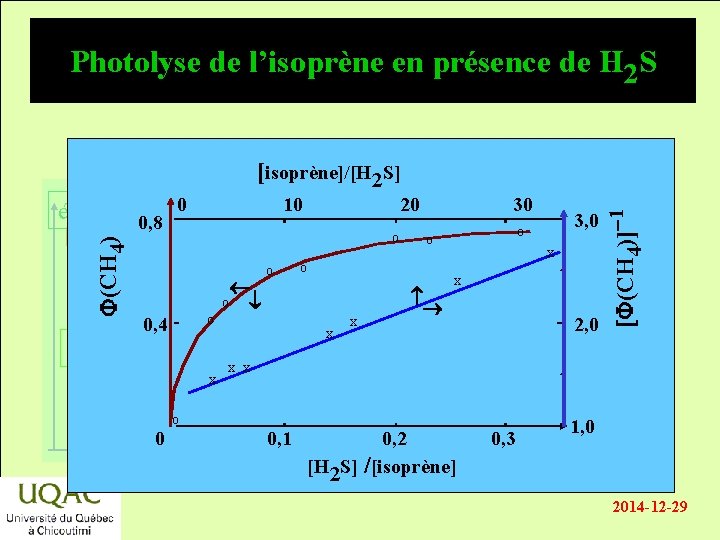
Exemple de méthode expérimentale • Chromatographie, spectrométrie de masse, . . . énergie – Exemple : photolyse de l’isoprène, cinétique de réaction des radicaux méthyles : [1] • CH 3 + H 2 S CH 4 + HS • [2] • CH 3 + C 5 H 8 • C 6 H 11 réactifs [F(CH 4)]-1 = a + a (k 2/k 1) [C 5 H 8]/[H 2 S] produits La figure ci-jointe donne k 2/k 1 temps 2014 -12 -29

Photolyse de l’isoprène en présence de H 2 S F(CH 4) énergie 0, 8 0 0, 4 10 20 o o réactifs x produits o 0 temps o ¯ o 30 o o x x 3, 0 o x x 2, 0 [F(CH 4)]-1 [isoprène]/[H 2 S] x x 0, 1 0, 2 [H 2 S] /[isoprène] 0, 3 1, 0 2014 -12 -29

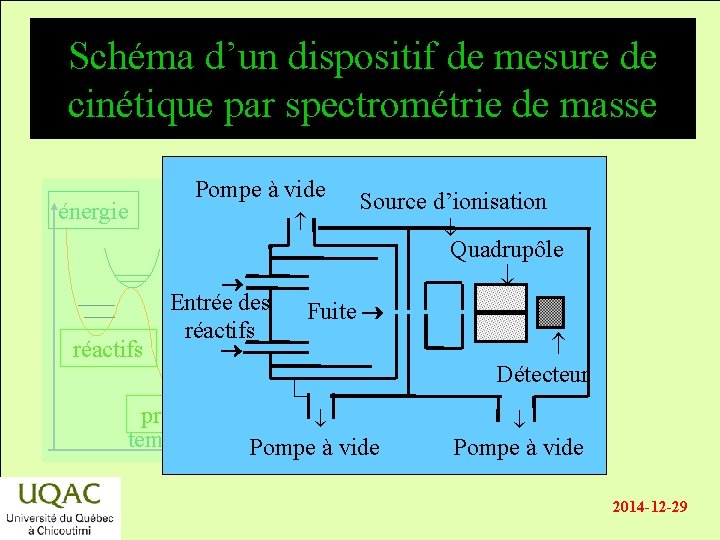
Schéma d’un dispositif de mesure de cinétique par spectrométrie de masse énergie Pompe à vide Source d’ionisation Quadrupôle réactifs Entrée des réactifs produits temps Fuite Détecteur Pompe à vide 2014 -12 -29

Conclusion • L’ordre : une notion fondamentale. • La température intervient à travers énergie l’énergie d’activation. • En cinétique, l’énergie d’activation est le paramètre important. réactifs k T = A e-Ea/RT • Rappel : en thermodynamique, produits temps l’enthalpie est le paramètre important. 2014 -12 -29