KIMIA ORGANIK SENYAWA KARBON Apa Senyawasenyawa yang ditemukan

KIMIA ORGANIK: SENYAWA KARBON


Apa • Senyawa-senyawa yang ditemukan pada organisme sebagian besar disusun oleh unsur karbon • Senyawa yang berasal dari organisme hidup (senyawa organik) ada unsur selain karbon

• kurang tepat karena senyawa organik dapat juga disintesis dari senyawa anorganik • sebutan senyawa organik untuk senyawa yang berhubungan dengan sistem kehidupan mahluk hidup
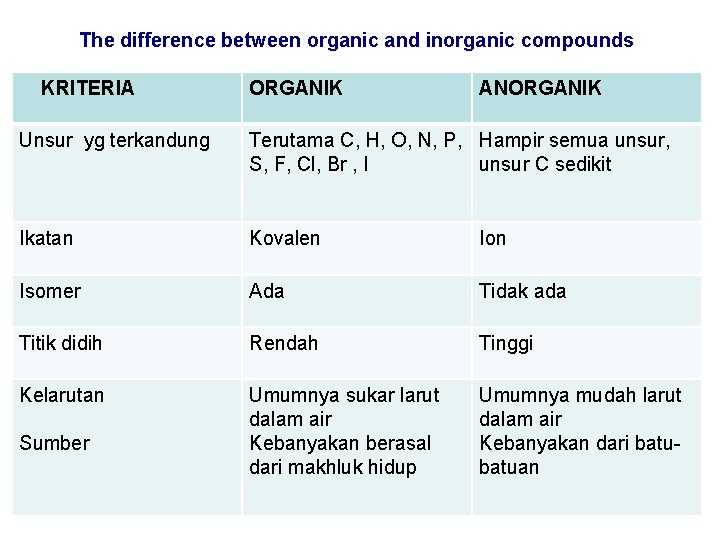
The difference between organic and inorganic compounds KRITERIA ORGANIK ANORGANIK Unsur yg terkandung Terutama C, H, O, N, P, Hampir semua unsur, S, F, Cl, Br , I unsur C sedikit Ikatan Kovalen Ion Isomer Ada Tidak ada Titik didih Rendah Tinggi Kelarutan Umumnya sukar larut dalam air Kebanyakan berasal dari makhluk hidup Umumnya mudah larut dalam air Kebanyakan dari batuan Sumber

Contoh senyawa karbon organik - karbohidrat, mengandung C, H, dan O - Protein, mengandung C, H, O, N, dan ada juga yang mengandung unsur S - Lemak, mengandung C, H, dan O - Minyak bumi, mengandung C dan H - Urea, mengandung C, H, O, dan N - Plastik, umumnya mengandung C dan H

Contoh senyawa karbon anorganik - Oksida karbon (CO dan CO 2) - Batu kapur (Ca. CO 3) - Batu karbid (Ca. C 2) - Soda kue (Na. HCO 3)

Perbedaan senyawa karbon organik dan anorganik No Senyawa karbon organik Senyawa karbon anorganik 1 Jika dibakar menghasilkan arang dan gas CO 2 Jika dibakar _ _ d _ _ menghasilkan a_ _ dan gas ___ 2 Hampir semua memiliki ikatan kovalen 3 Tidak stabil terhadap pemanasan Ada yang memiliki ikatan k_ _ _ ada yang i_ _ T_ _ terhadap pemanasan 4 Umumnya memiliki Mr yang cukup besar antara puluhan lebih _ _ l sampai ratusan ribu Jenis senyawanya sangat Jenis senyawa hanya sedikit banyak 5
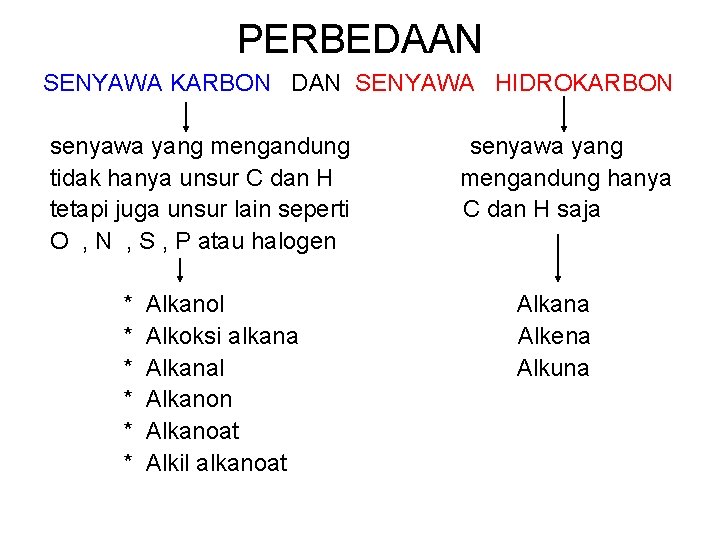
PERBEDAAN SENYAWA KARBON DAN SENYAWA HIDROKARBON senyawa yang mengandung tidak hanya unsur C dan H tetapi juga unsur lain seperti O , N , S , P atau halogen * * * Alkanol Alkoksi alkana Alkanal Alkanon Alkanoat Alkil alkanoat senyawa yang mengandung hanya C dan H saja Alkana Alkena Alkuna
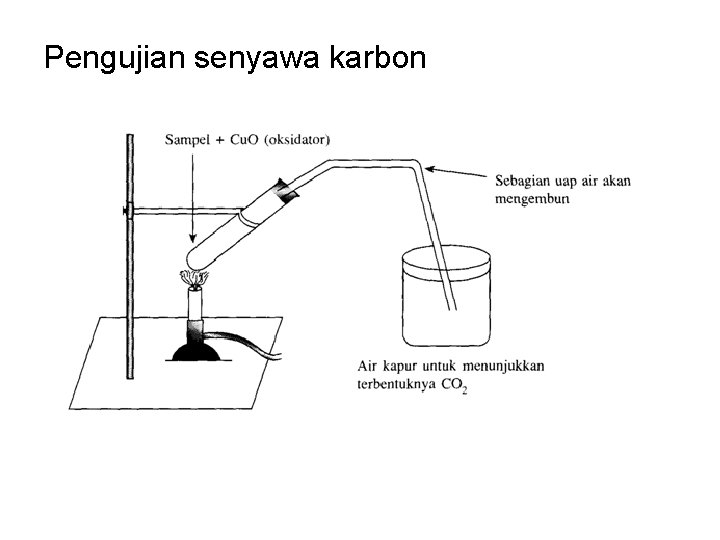
Pengujian senyawa karbon

Karbon sebagai unsur pokok memiliki keistimewaan sbb : ELEKTRON VALENSI Dengan ev = 4 membentuk 4 ikatan kovalen sbb : | ― C― | Dapat membentuk rantai karbon , yaitu ikatan antara atom karbon yang satu dengan atom karbon yang lain.
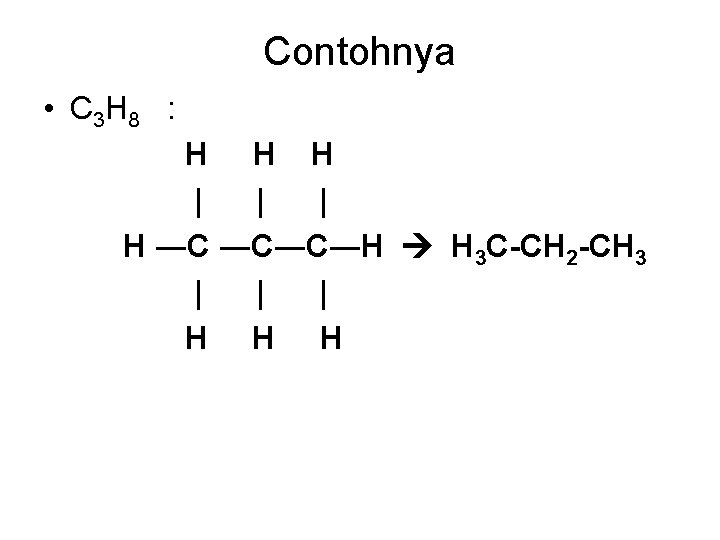
Contohnya • C 3 H 8 : H H H | | | H ―C ―C―C―H H 3 C-CH 2 -CH 3 | | | H H H
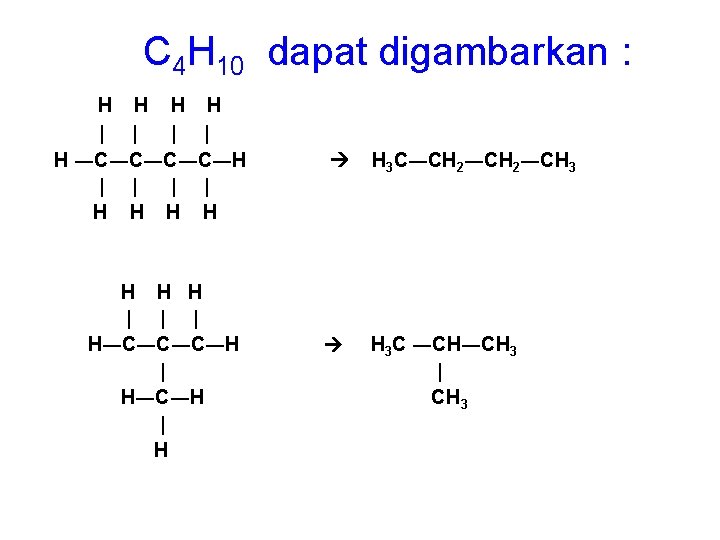
C 4 H 10 dapat digambarkan : H H | | H ―C―C―H | | H H H H | | | H―C―C―C―H | H H 3 C―CH 2―CH 3 H 3 C ―CH―CH 3 | CH 3

Bandingkan dengan unsur se-periode : 5 B 7 N Bandingkan dengan unsur se-golongan : 14 Si

JARI-JARI ATOM HARGA KEELEKTRONEGATIFAN

Bilangan oksidasi atom C dalam beberapa senyawa karbon 1. Metana, CH 4 2. Metanol, CH 3 OH 3. Formalin, HCOH 4. Asam metanoat/asam formiat, HCOOH 5. Karbonmonoksida 6. Karbondioksida
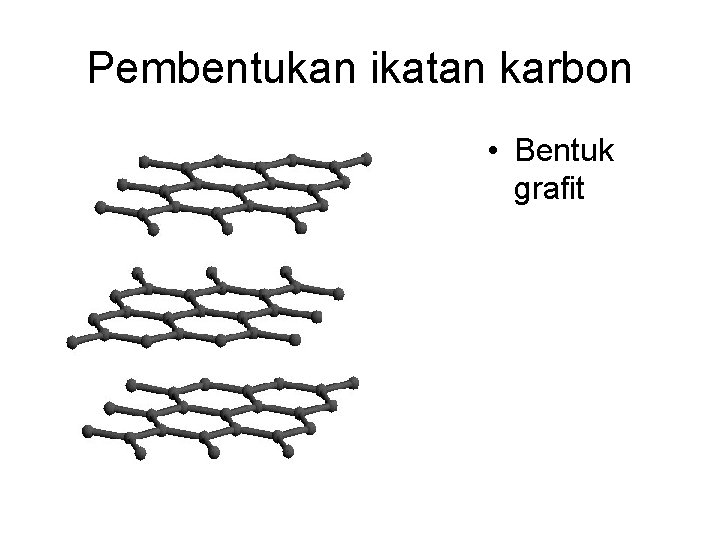
Pembentukan ikatan karbon • Bentuk grafit
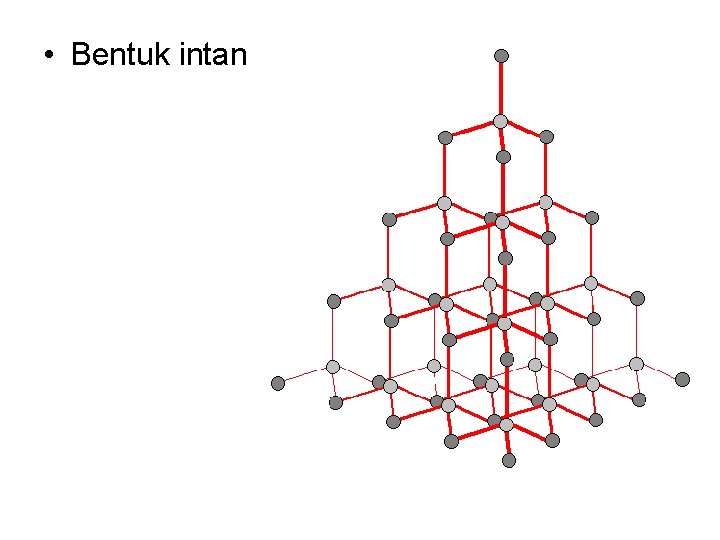
• Bentuk intan
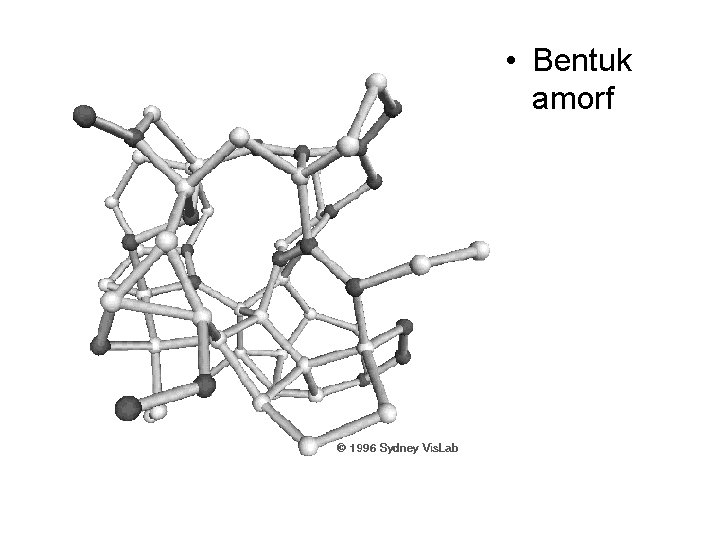
• Bentuk amorf
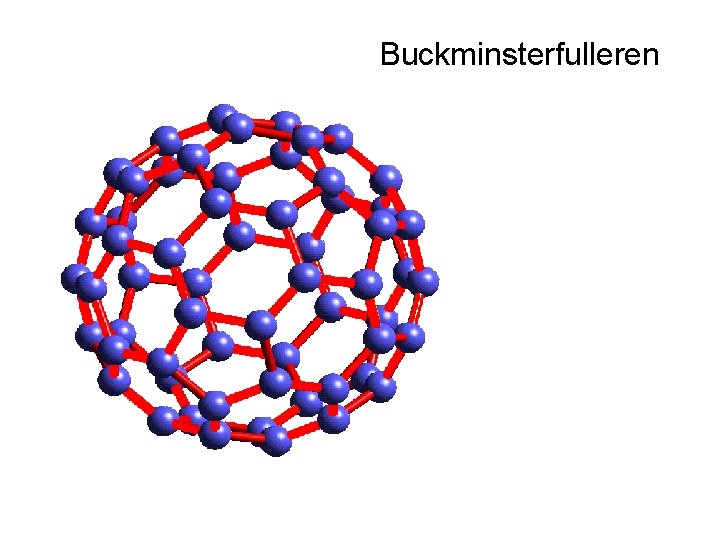
Buckminsterfulleren

Perhatikan istilah ini • Rantai karbon yang terbuka disebut : Rantai alifatik • Rantai karbon yang tertutup disebut : Rantai alisiklik • Rantai karbon yang hanya dihubungkan oleh ikatan tunggal disebut rantai jenuh • Rantai karbon yang hanya dihubungkan oleh ikatan rangkap baik rangkap 2 atau rangkap 3 disebut rantai tak jenuh • Rantai karbon alisiklik yang memiliki ikatan konjugasi yaitu ikatan tunggal dan rangkap selang seling disebut Rantai karbon aromatik.

CONTOH SOAL • H 3 C―CH 2―CH 3 • H 3 C ―CH―CH- OH | CH 3 • H 3 C―CH = CH―CH 3 • 0 ║ H 3 C ―CH―CH 2 - C | H CH 3 Senyawa hidrokarbon alifatik jenuh Senyawa karbon alifatik jenuh bercabang Senyawa hidrokarbon alifatik tak jenuh Senyawa karbon alifatik bercabang
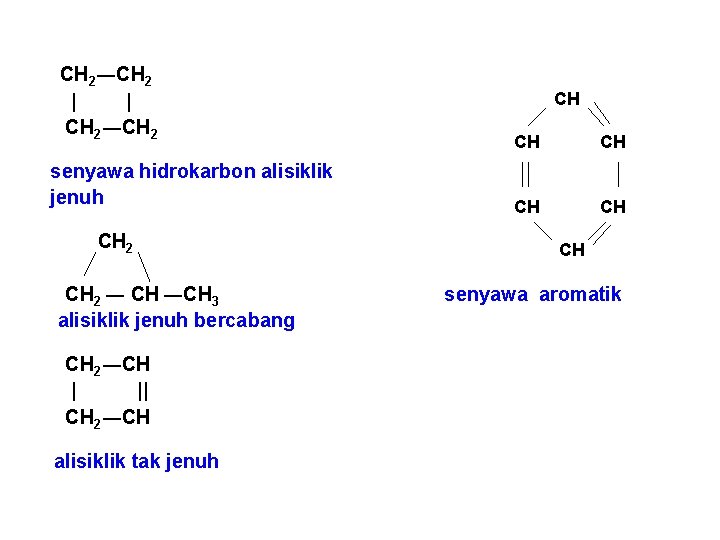
CH 2―CH 2 | | CH 2―CH 2 senyawa hidrokarbon alisiklik jenuh CH 2 ― CH ―CH 3 alisiklik jenuh bercabang CH 2―CH | || CH 2―CH alisiklik tak jenuh CH CH CH senyawa aromatik

ADA 4 JENIS ATOM C • Atom C primer : bila menggunakan 1 valensi untuk mengikat atom C yang Lain. • Atom C sekunder : menggunakan 2 valensi • Atom C tersier : menggunakan 3 valensi • Atom C kwarterner : menggunakan seluruh valensi untuk mengikat atom C yang lain.
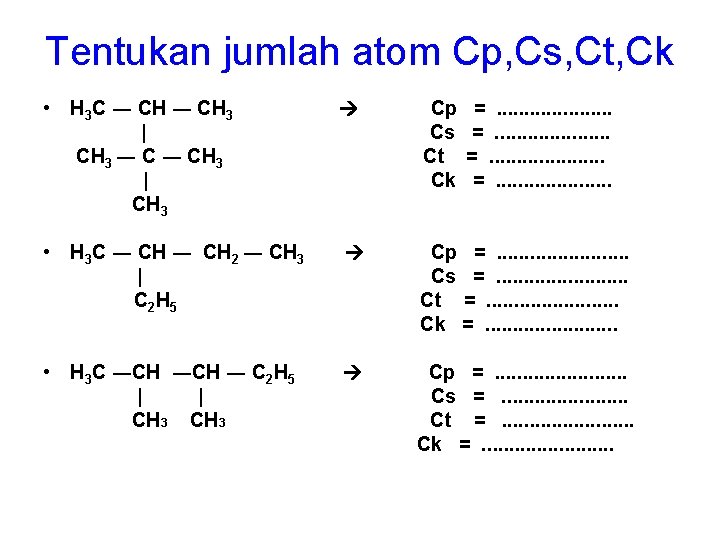
Tentukan jumlah atom Cp, Cs, Ct, Ck • H 3 C ― CH 3 | CH 3 Cp Cs Ct Ck • H 3 C ― CH 2 ― CH 3 | C 2 H 5 Cp =. . . Cs =. . . Ct =. . . Ck =. . . • H 3 C ―CH ― C 2 H 5 | | CH 3 Cp =. . . Cs =. . . Ct =. . . Ck =. . . . =. . . . .
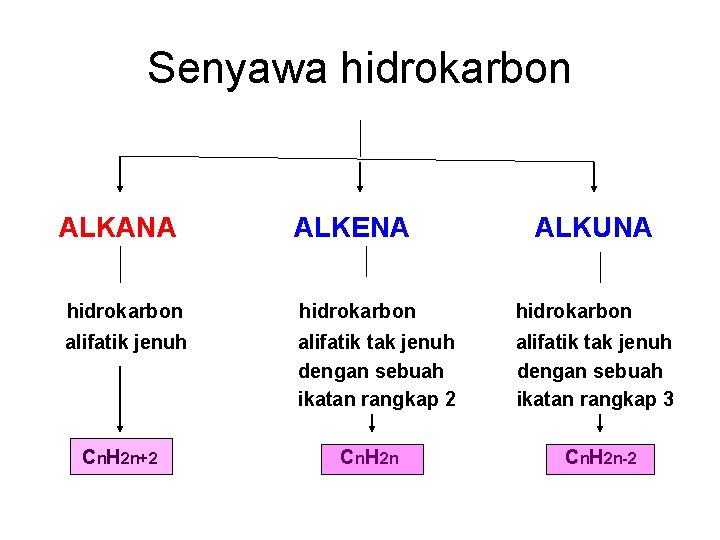
Senyawa hidrokarbon ALKANA ALKENA ALKUNA hidrokarbon alifatik jenuh alifatik tak jenuh dengan sebuah ikatan rangkap 2 alifatik tak jenuh dengan sebuah ikatan rangkap 3 Cn. H 2 n+2 Cn. H 2 n-2

ALKANA

Deret Homolog Deretan rumus molekul alkana menunjukkan bahwa setiap anggota yang satu ke anggota berikutnya bertambah sebanyak CH 2. Deret senyawa karbon demikian disebut dengan deret homolog.

Sifat-sifat deret homolog: 1. Mempunyai rumus umum Cn. H 2 n+2 2. Antara satu anggota ke anggota berikutnya mempunyai pembeda CH 2 3. Selisih massa rumus antara satu anggota ke anggota berikutnya adalah 14 4. Semakin panjang rantai atom karbonnya, semakin tinggi titik didihnya


Tata nama alkana Pemberian nama senyawa karbon didasarkan pada aturan IUPAC (International Union and Pure Applied Chemistry) sebagai berikut: 1. Nama alkana diambil berdasarkan jumlah atom karbon yang menyusunnya dan diakhiri dengan akhiran “ana”
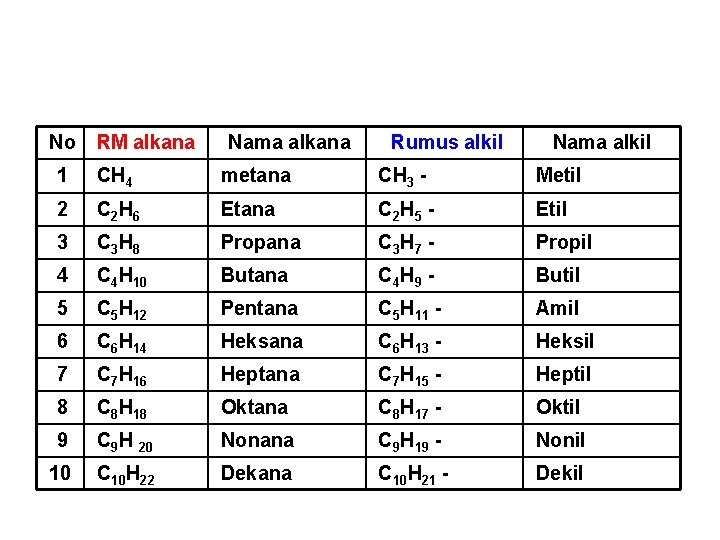
No RM alkana Nama alkana Rumus alkil Nama alkil 1 CH 4 metana CH 3 - Metil 2 C 2 H 6 Etana C 2 H 5 - Etil 3 C 3 H 8 Propana C 3 H 7 - Propil 4 C 4 H 10 Butana C 4 H 9 - Butil 5 C 5 H 12 Pentana C 5 H 11 - Amil 6 C 6 H 14 Heksana C 6 H 13 - Heksil 7 C 7 H 16 Heptana C 7 H 15 - Heptil 8 C 8 H 18 Oktana C 8 H 17 - Oktil 9 C 9 H 20 Nonana C 9 H 19 - Nonil 10 C 10 H 22 Dekana C 10 H 21 - Dekil

2. Jika strukturnya telah diketahui dan merupakan rantai karbon tak bercabang, di depan nama tersebut diberi huruf n (dari kata normal) Contoh: CH 3 CH 2 CH 3 n-butana

3. Jika rantai karbonnya bercabang, ditentukan dahulu rantai utama (rantai induk), yaitu rantai atom karbon terpanjang, dan diberi nomor urut dari ujung yang paling dekat dengan letak cabang

4. Menetapkan gugus cabang yang terikat pada rantai utama. Gugus cabang pada alkana umumnya merupakan alkil. Gugus alkil merupakan gugus hidrokarbon (alkana) yang kehilangan sebuah atom hidrogen. Rumus umum alkil adalah Cn. H 2 n+1 Nama gugus alkil disesuaikan dengan nama alkananya dengan mengganti akhiran –ana dengan akhiran -il

5. Gugus alkil yang mempunyai rantai bercabang atau tidak terikat pada atom karbon primer diberi nama tertentu
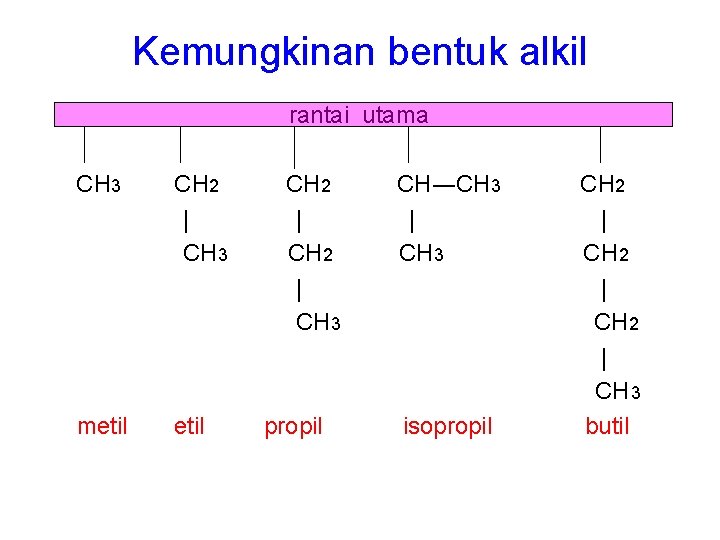
Kemungkinan bentuk alkil rantai utama CH 3 CH 2 | CH 3 metil CH 2 | CH 3 propil CH―CH 3 | CH 3 isopropil CH 2 | CH 3 butil
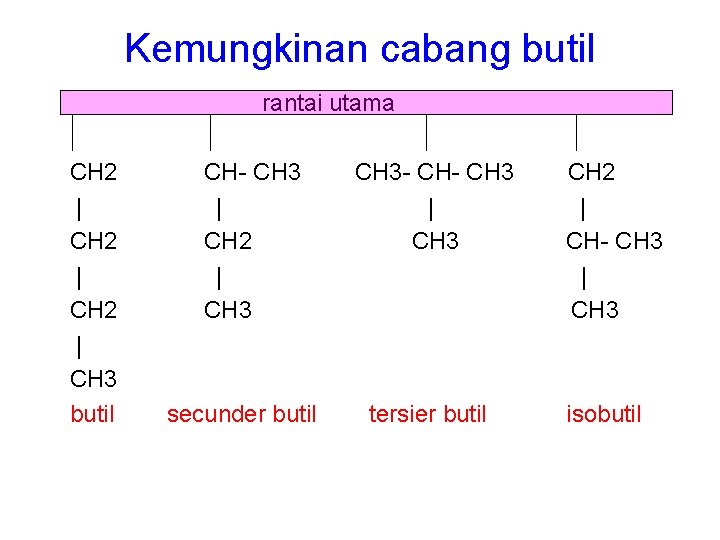
Kemungkinan cabang butil rantai utama CH 2 | CH 3 butil CH- CH 3 | CH 2 | CH 3 secunder butil CH 3 - CH 3 | CH 3 tersier butil CH 2 | CH- CH 3 | CH 3 isobutil
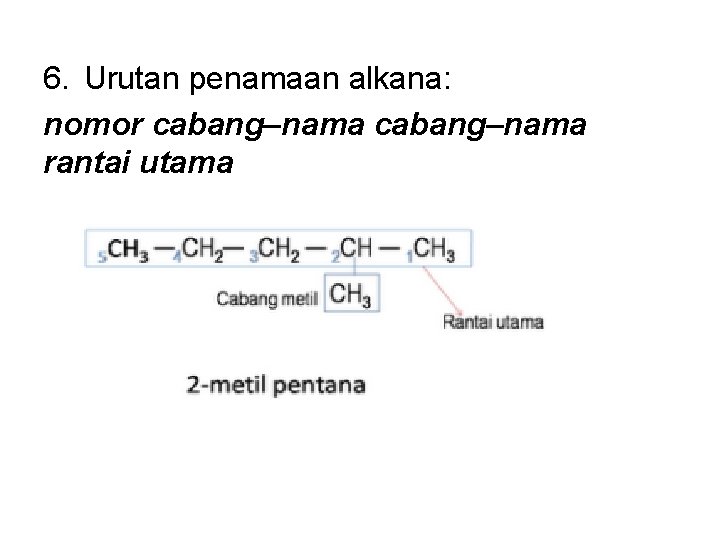
6. Urutan penamaan alkana: nomor cabang–nama rantai utama
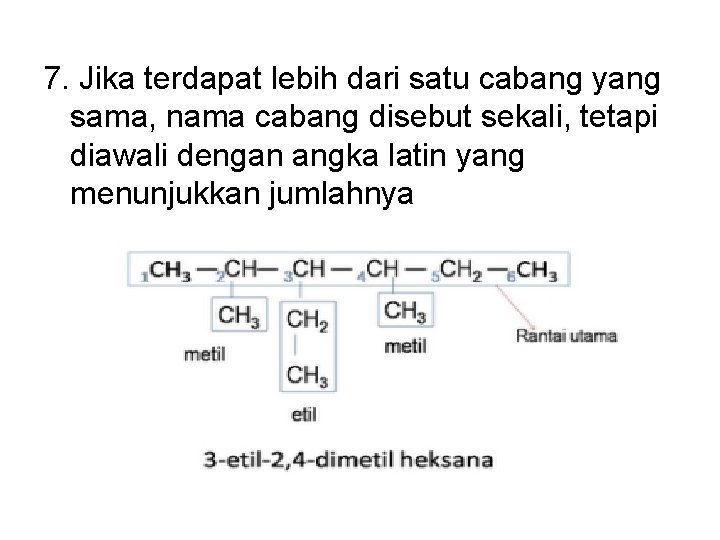
7. Jika terdapat lebih dari satu cabang yang sama, nama cabang disebut sekali, tetapi diawali dengan angka latin yang menunjukkan jumlahnya

ALKENA

Alkena merupakan hidrokarbon yang mempunyai ikatan rangkap dua antar atom karbonnya. Anggota alkena paling sederhana adalah etena (etilena)

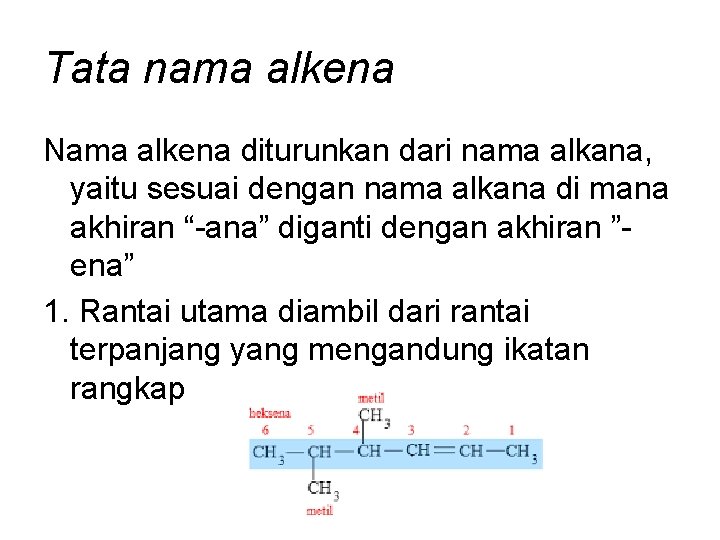
Tata nama alkena Nama alkena diturunkan dari nama alkana, yaitu sesuai dengan nama alkana di mana akhiran “-ana” diganti dengan akhiran ”ena” 1. Rantai utama diambil dari rantai terpanjang yang mengandung ikatan rangkap

2. Penomoran atom karbon dimulai dari ujung yang paling dekat dengan ikatan rangkap 3. Ikatan rangkap diberi nomor untuk menunjukkan letaknya 4. Cara penulisan dan penamaan cabang sama dengan pada alkana 5. Urutan penamaan alkena: nomor cabang – nama cabang – nomor ikatan rangkap – nama rantai utama
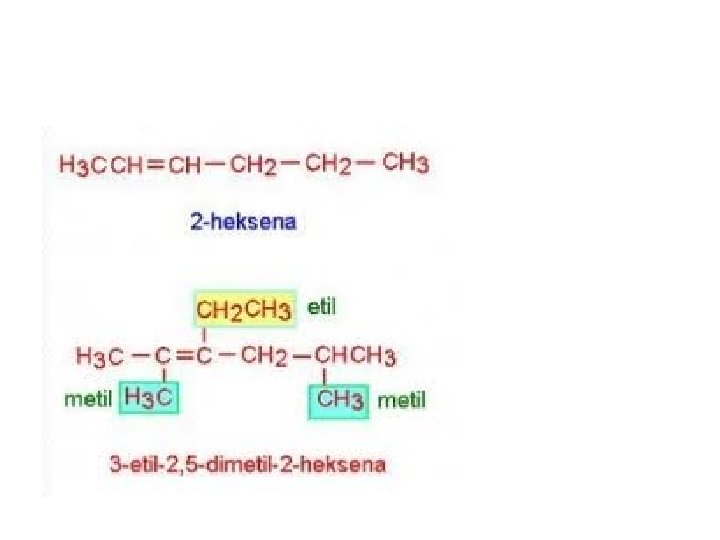

ALKUNA

Alkuna merupakan hidrokarbon yang mempunyai ikatan rangkap tiga antar atom karbonnya

Tata nama alkuna Alkuna diberi nama seperti pada alkena, dengan akhiran “-ena” diganti dengan “una” Tata cara pemberian nomor ikatan dan cabang sama dengan alkena
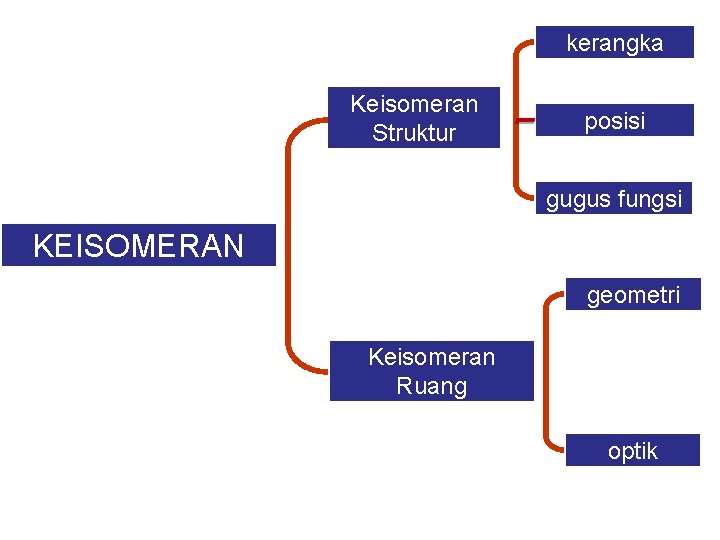
kerangka Keisomeran Struktur posisi gugus fungsi KEISOMERAN geometri Keisomeran Ruang optik

Isomeri alkana, alkena, dan alkuna Isomeri adalah peristiwa di mana suatu senyawa karbon mempunyai rumus molekul sama tetapi mempunyai struktur berbeda.

Isomer Rangka Butana, C 4 H 10 mempunyai CH 3 CH 2 CH 3 bentuk rangka C lurus : n-butana CH 3 CH CH 3 2 -metil propana CH 3 bentuk rangka C bercabang :

Isomer Posisi Isomeri posisi terjadi karena adanya perbedaan posisi letak cabang atau posisi letak ikatan rangkapnya Contoh: 1 -butena dan 2 -butena

Isomer Geometri Isomer geometri merupakan isomer yang terjadi karena perbedaan letak suatu gugus di dalam ruangan. Isomeri geometri dapat terjadi bila di dalam senyawa karbon tersebut terdapat rantai karbon yang membentuk bidang dan terdapat gugus yang sama pada dua tom karbon yang berbeda.
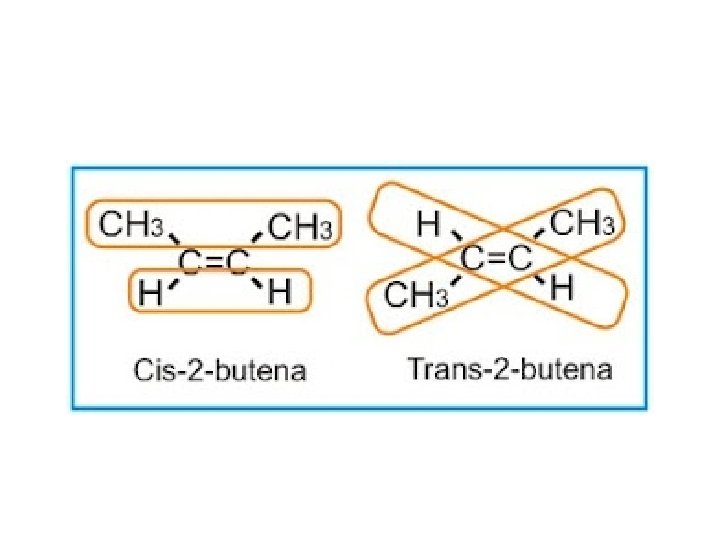

SIFAT FISIS ALKANA 1. Semakin banyak atom karbon atau semakin panjang rantai karbon suatu alkana, semakin tinggi titik didih dan titik leburnya 2. Untuk jumlah atom karbon yang sama, isomer dengan rantai karbon tidak bercabang mempunyai titik didih dan titik lebur yang lebih tinggi daripada isomer dengan rantai karbon bercabang 3. Semakin banyak cabang pada rantai karbonnya, semakin rendah titik didih dan tiitk leburnya

SIFAT KIMIA ALKANA Alkana merupakan hidrokarbon jenuh dan semua ikatan yang ada merupakan ikatan kovalen sempurna. Akibatnya hidrokarbon merupakan senyawa yang kurang reaktif sehingga disebut “parafin” yang berarti daya gabung atau daya reaksinya rendah. Semakin panjang rantai karbon, semakin berkurang kereaktiannya. Reaksi pada alkena umumnya merupakan eaksi substitusi yaitu reaksi penggantian gugus atom hidrogen pada suatu alkana.

Reaksi Substitusi : Penggantian gugus atau atom yang terikat pada atom karbon. Contoh : • R – H + Cl 2 → R – Cl + HCl

SIFAT ALKENA DAN ALKUNA Semakin panjang rantai atom karbonnya, semakin tinggi titik didih dan titik leburnya Alkena dan alkuna merupakan hidrokarbon yang lebih reaktif dari alkana. Reaksi penghilangan ikatan rangkap karena penambahan zat lain pada senyawa karbon disebut dengan reaksi adisi

Reaksi Adisi : Reaksi pemutusan ikatan rangkap Contoh : • CH 3 – CH = CH + H 2 → CH 3 – CH 2 – CH 3 • adisi markovnikov prinsip “yang kaya makin kaya dengan H”
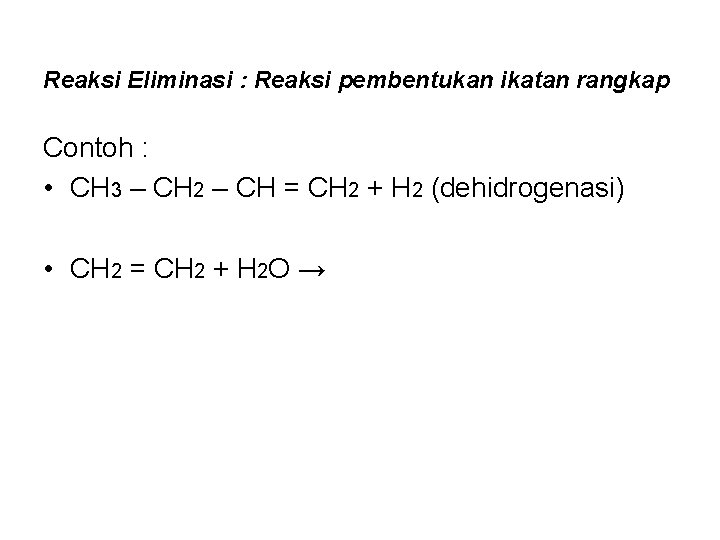
Reaksi Eliminasi : Reaksi pembentukan ikatan rangkap Contoh : • CH 3 – CH 2 – CH = CH 2 + H 2 (dehidrogenasi) • CH 2 = CH 2 + H 2 O →

KEGUNAAN • Alkana digunakan sebagai bahan bakar, di antaranya: 1. metana merupakan senyawa utama yang terkandung dalam gas alam cair atau LNG. 2. Alkana dengan jumlah atom C 2 sampai 5 terkandung dalam LPG 3. Butana digunakan sebagai pengisi korek api Oktana merupakan senyawa utama dalam bensin Lilin dan aspal merupakan senyawa alkana

• Plastik Molekul-molekul etena dapat bergabung membentuk polietena, yaitu suatu polimer yang digunakan untuk membuat peralatan dari plastik. Molekul propena dapat bergabung membentuk polipropena yang digunakan untuk membuat peralatan masak dan serat sintetis.

• Karet alam dan getah perca Alkena alami yang banyak dimanfaatkan yaitu karet dan getah perca. Karet (dicampur dengan belerang) digunakan untuk membuat ban kendaraaan, sedangkan getah perca untuk bahan insulasi • Las karbit etuna atau asetilena merupakan gas yang dihasilkan jika gas karbid direaksikan dengan air. Gas ini sering digunakan sebagai bahan bakar untuk proses pengelasan.
- Slides: 64