GAYA YANG MENGUKUHKAN ATOM DALAM MOLEKUL ATAU IONION














- Slides: 53

GAYA YANG MENGUKUHKAN ATOM DALAM MOLEKUL ATAU ION-ION

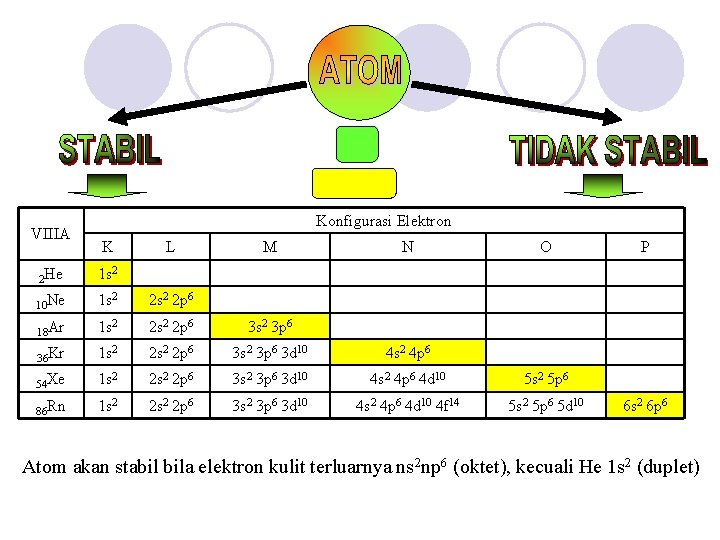
VIIIA Konfigurasi Elektron K L M N O 2 He 1 s 2 10 Ne 1 s 2 2 p 6 18 Ar 1 s 2 2 p 6 3 s 2 3 p 6 36 Kr 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 54 Xe 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 5 s 2 5 p 6 86 Rn 1 s 2 2 p 6 3 s 2 3 p 6 3 d 10 4 s 2 4 p 6 4 d 10 4 f 14 5 s 2 5 p 6 5 d 10 P 6 s 2 6 p 6 Atom akan stabil bila elektron kulit terluarnya ns 2 np 6 (oktet), kecuali He 1 s 2 (duplet)

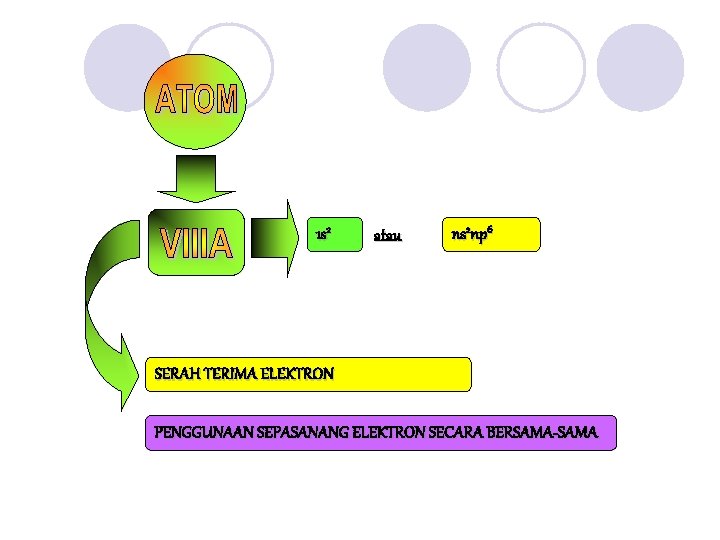
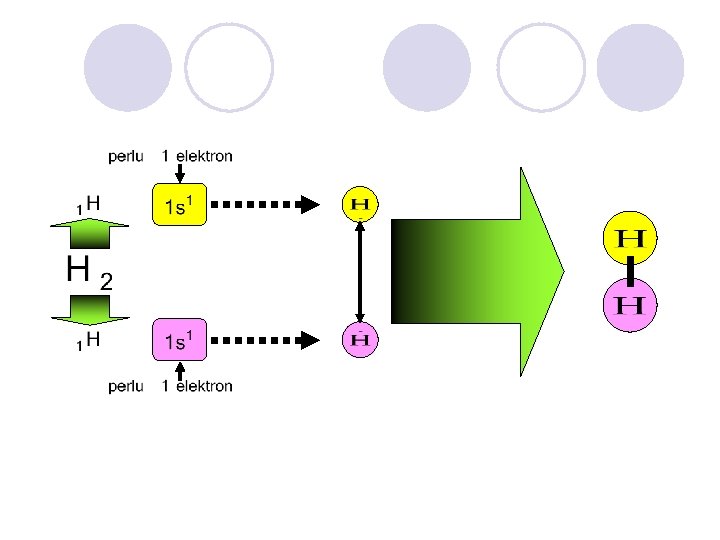
1 s 2 atau ns 2 np 6 SERAH TERIMA ELEKTRON PENGGUNAAN SEPASANANG ELEKTRON SECARA BERSAMA-SAMA

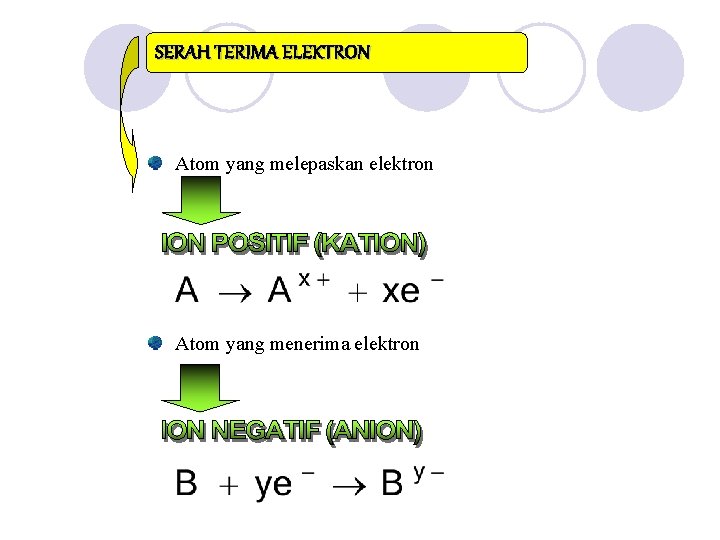
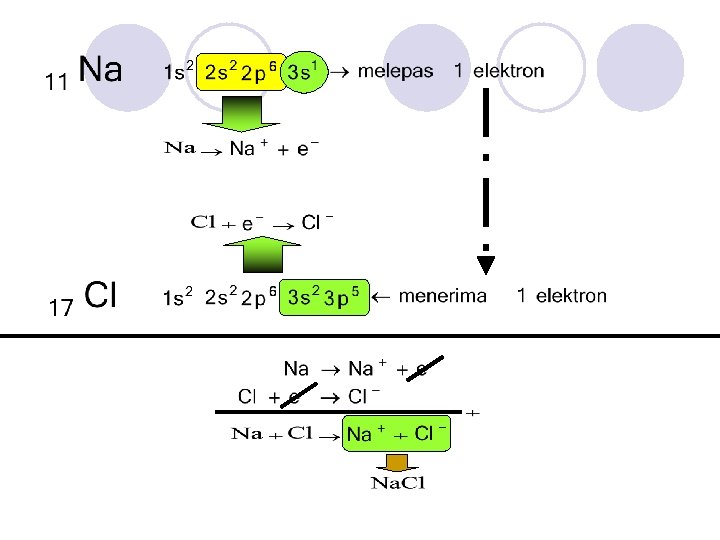
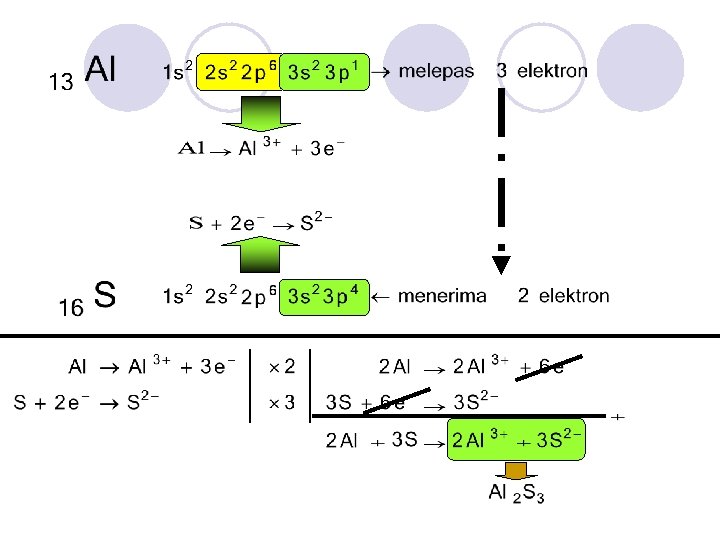
SERAH TERIMA ELEKTRON Atom yang melepaskan elektron Atom yang menerima elektron

GAYA TARIK MENARIK ANTARA ION POSITIF (KATION) DAN ION NEGATIF (ANION)



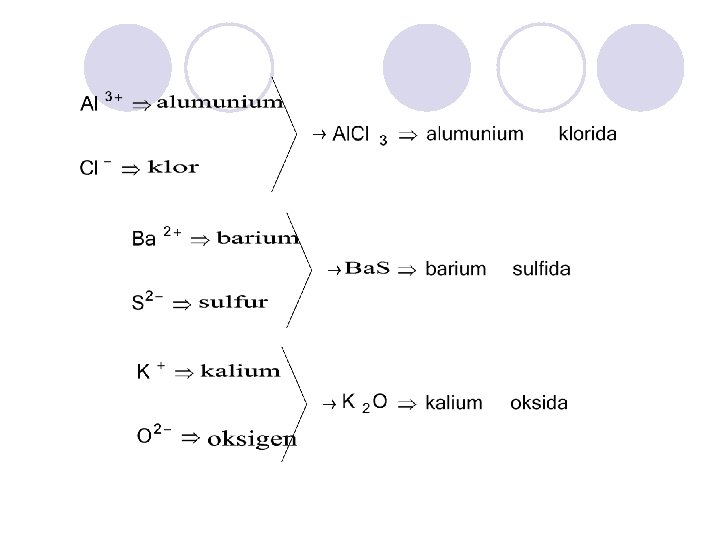
DIDASARKAN PADA NAMA ION LOGAM YANG BERMUATAN POSITIF DAN ION NEGATIF DITAMBAH AKHIRAN IDA

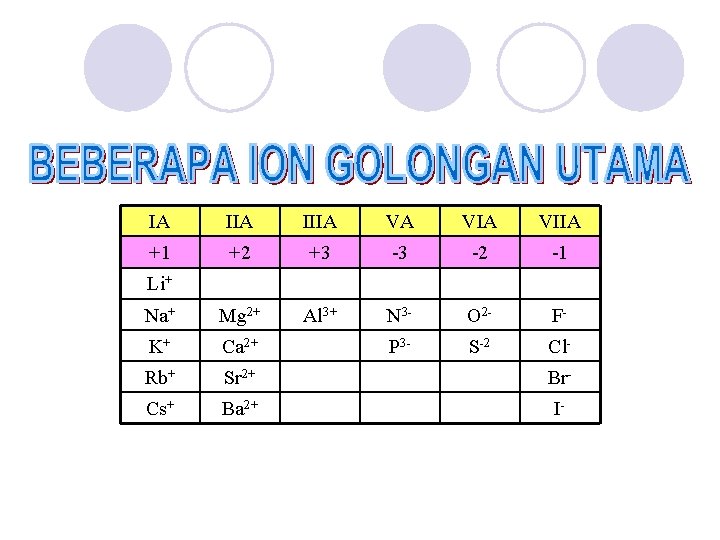
IA IIIA VA VIIA +1 +2 +3 -3 -2 -1 Na+ Mg 2+ Al 3+ N 3 - O 2 - F- K+ Ca 2+ P 3 - S-2 Cl- Rb+ Sr 2+ Br- Cs+ Ba 2+ I- Li+


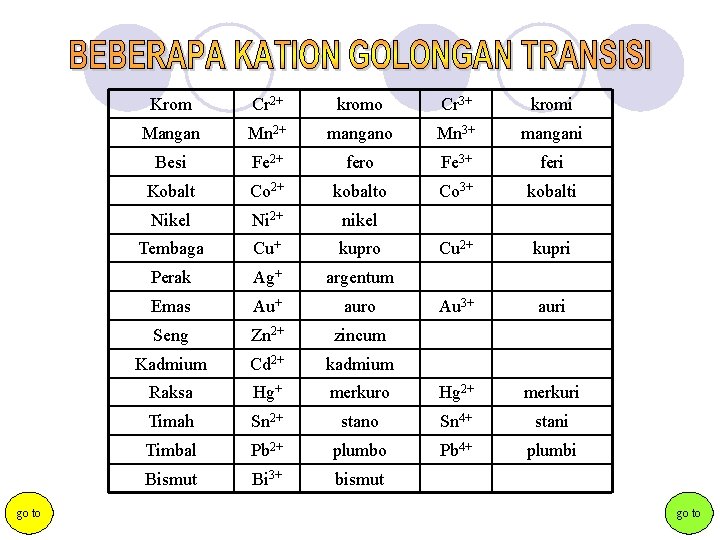
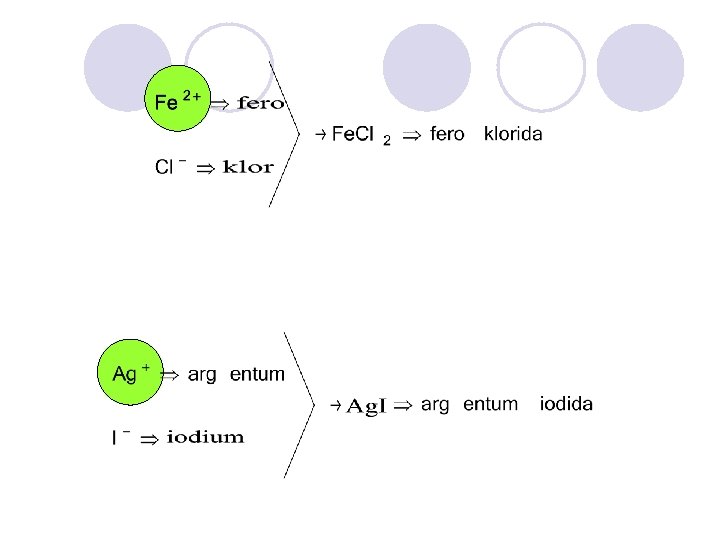
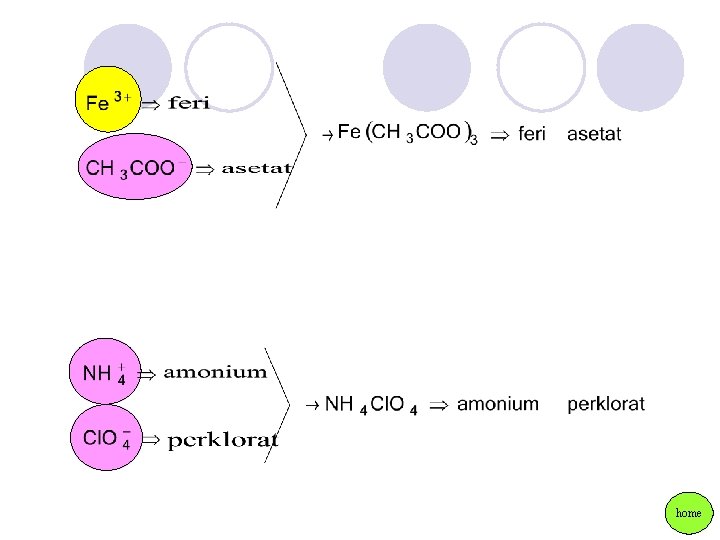
go to Krom Cr 2+ kromo Cr 3+ kromi Mangan Mn 2+ mangano Mn 3+ mangani Besi Fe 2+ fero Fe 3+ feri Kobalt Co 2+ kobalto Co 3+ kobalti Nikel Ni 2+ nikel Tembaga Cu+ kupro Cu 2+ kupri Perak Ag+ argentum Emas Au+ auro Au 3+ auri Seng Zn 2+ zincum Kadmium Cd 2+ kadmium Raksa Hg+ merkuro Hg 2+ merkuri Timah Sn 2+ stano Sn 4+ stani Timbal Pb 2+ plumbo Pb 4+ plumbi Bismut Bi 3+ bismut go to


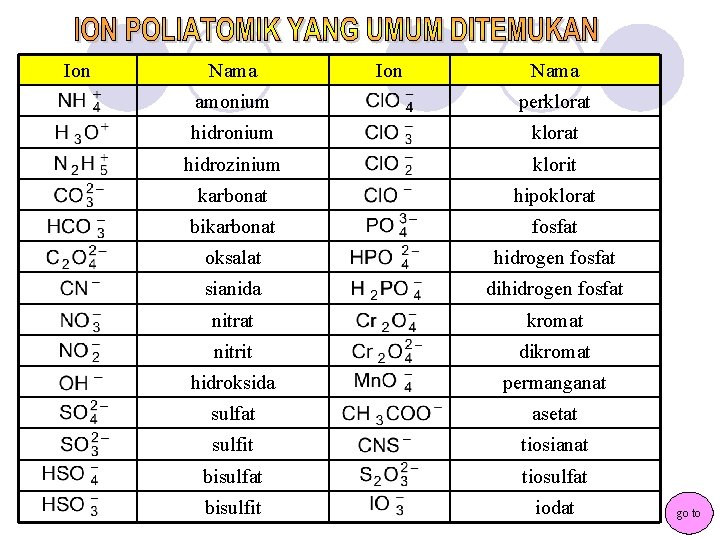
Ion Nama amonium perklorat hidronium klorat hidrozinium klorit karbonat hipoklorat bikarbonat fosfat oksalat hidrogen fosfat sianida dihidrogen fosfat nitrat kromat nitrit dikromat hidroksida permanganat sulfat asetat sulfit tiosianat bisulfat tiosulfat bisulfit iodat go to

home

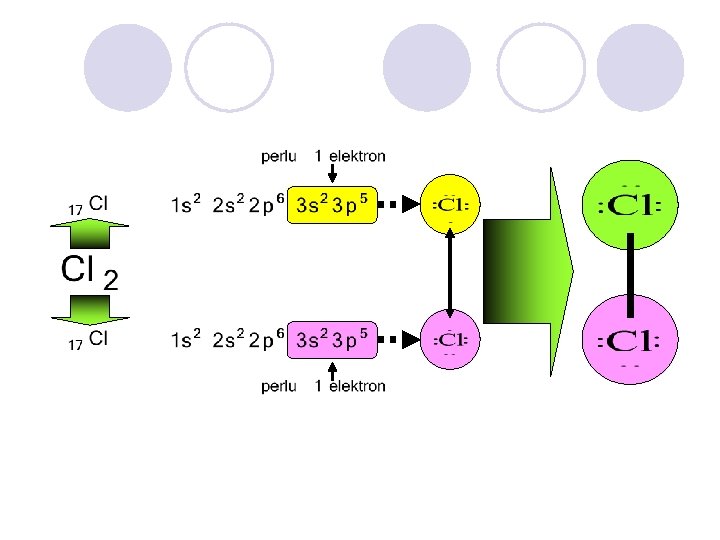
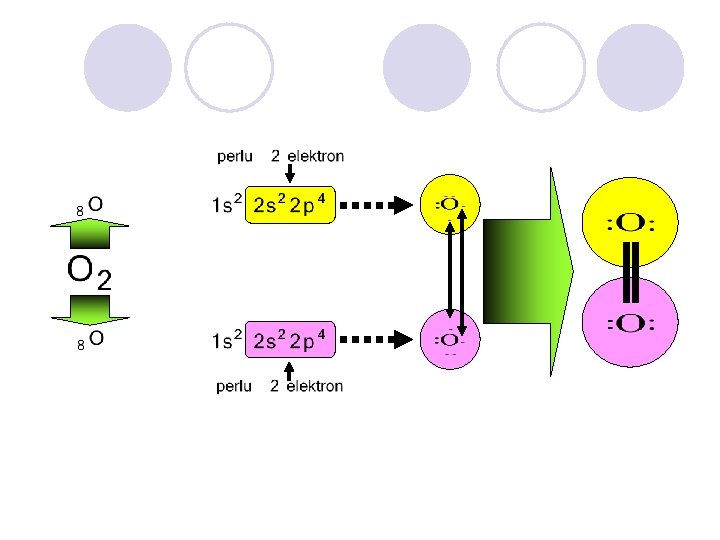
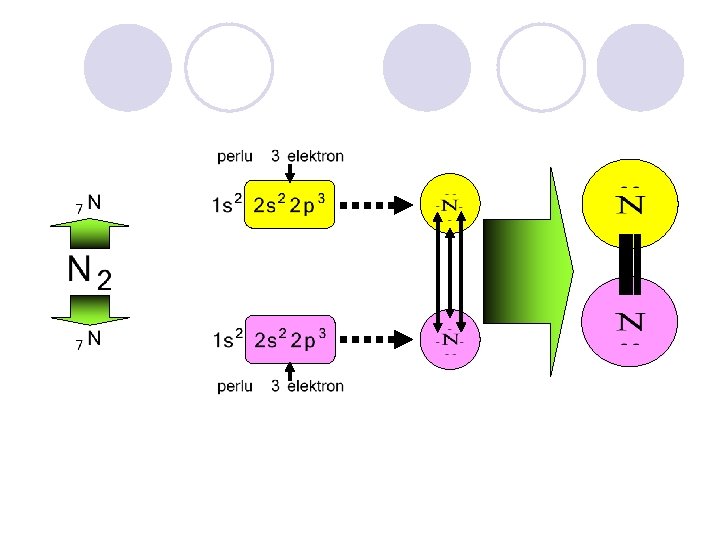
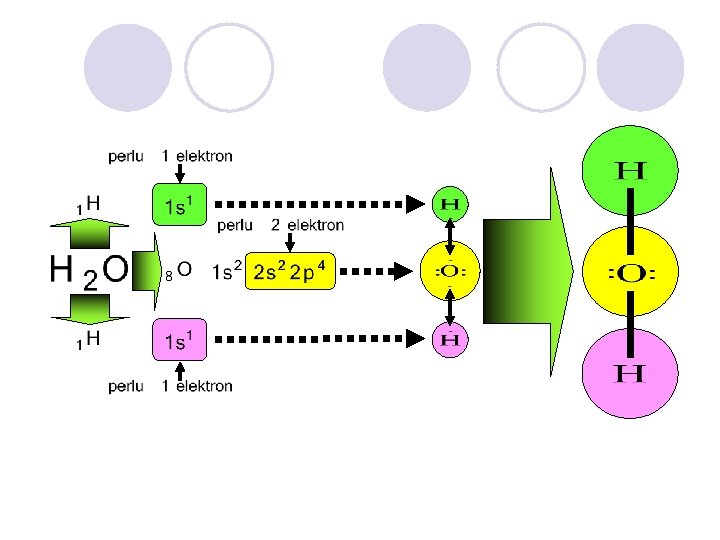
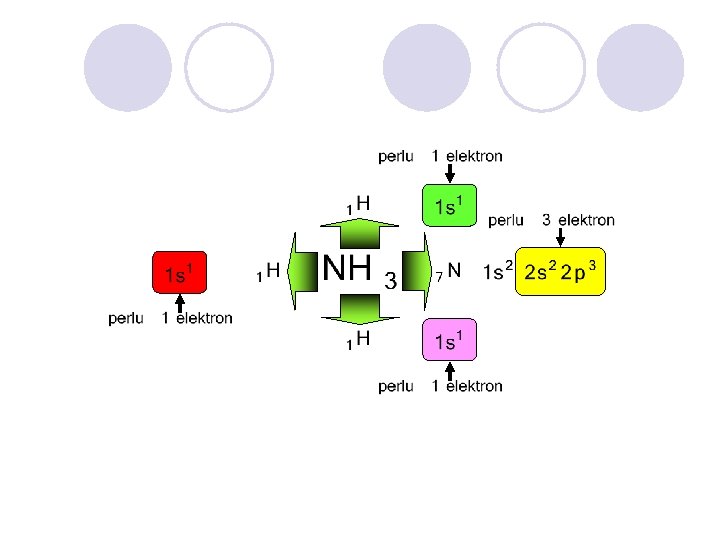
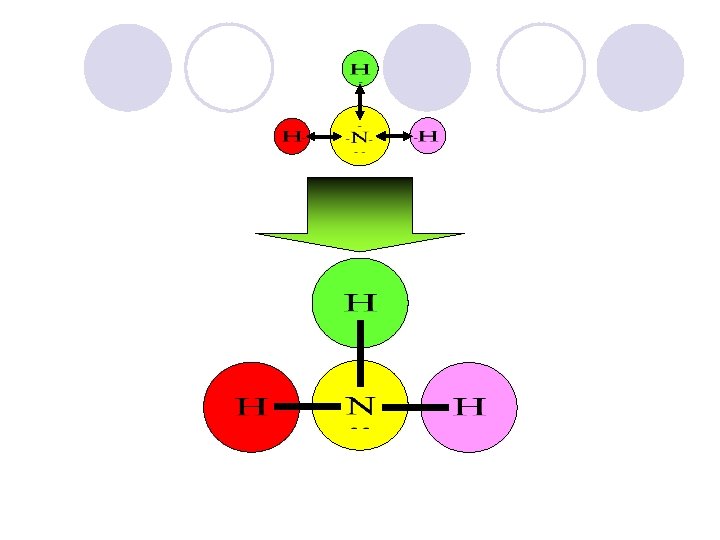
PENGGUNAAN SEPASANANG ELEKTRON SECARA BERSAMA G. N. LEWIS (1916) IRVING LANGMUIR









DIDASARKAN PADA NAMA KEDUA UNSUR PEMBENTUKNYA SECARA BERURUTAN DITAMBAH AKHIRAN IDA

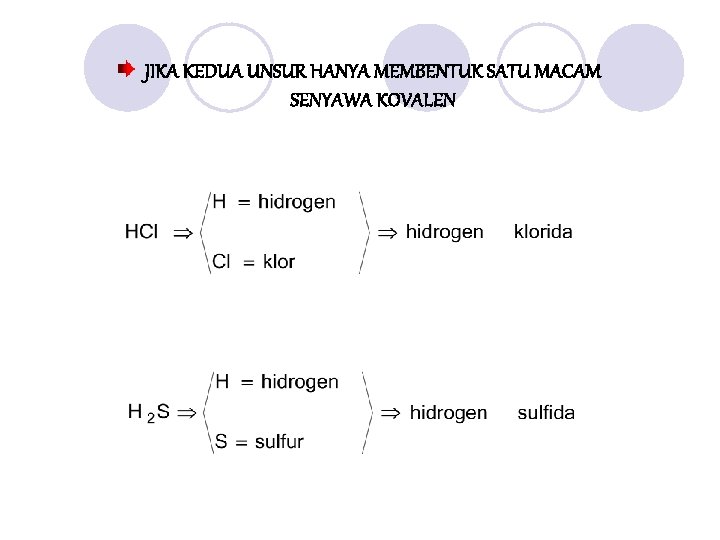
JIKA KEDUA UNSUR HANYA MEMBENTUK SATU MACAM SENYAWA KOVALEN

JIKA KEDUA UNSUR MEMBENTUK DUA MACAM SENYAWA KOVALEN ATAU LEBIH, PEMBERIAN NAMA HARUS MENGGUNAKAN AWALAN 1 mono 6 heksa 2 di 7 hepta 3 tri 8 okta 4 tetra 9 nona 5 penta 10 deka

JIKA UNSUR PERTAMA INDEKSNYA HANYA SATU, MAKA UNSUR PERTAMA TIDAK DIBERI AWALAN DAN UNSUR KEDUA DIBERI AWALAN DAN AKHIRAN IDA

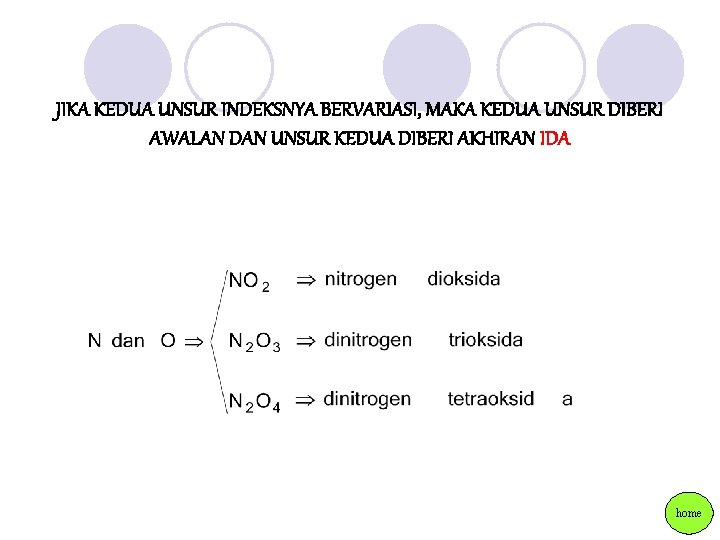
JIKA KEDUA UNSUR INDEKSNYA BERVARIASI, MAKA KEDUA UNSUR DIBERI AWALAN DAN UNSUR KEDUA DIBERI AKHIRAN IDA home

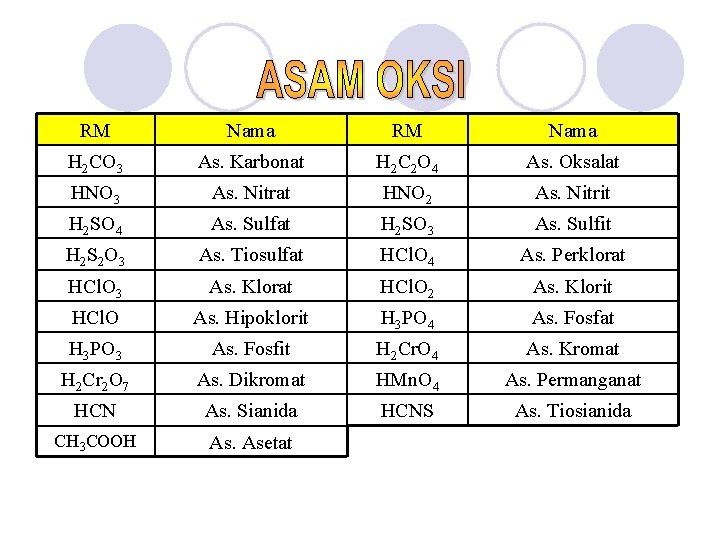
ASAM OKSI SENYAWA ORGANIK

RM Nama H 2 CO 3 As. Karbonat H 2 C 2 O 4 As. Oksalat HNO 3 As. Nitrat HNO 2 As. Nitrit H 2 SO 4 As. Sulfat H 2 SO 3 As. Sulfit H 2 S 2 O 3 As. Tiosulfat HCl. O 4 As. Perklorat HCl. O 3 As. Klorat HCl. O 2 As. Klorit HCl. O As. Hipoklorit H 3 PO 4 As. Fosfat H 3 PO 3 As. Fosfit H 2 Cr. O 4 As. Kromat H 2 Cr 2 O 7 As. Dikromat HMn. O 4 As. Permanganat HCN As. Sianida HCNS As. Tiosianida CH 3 COOH As. Asetat

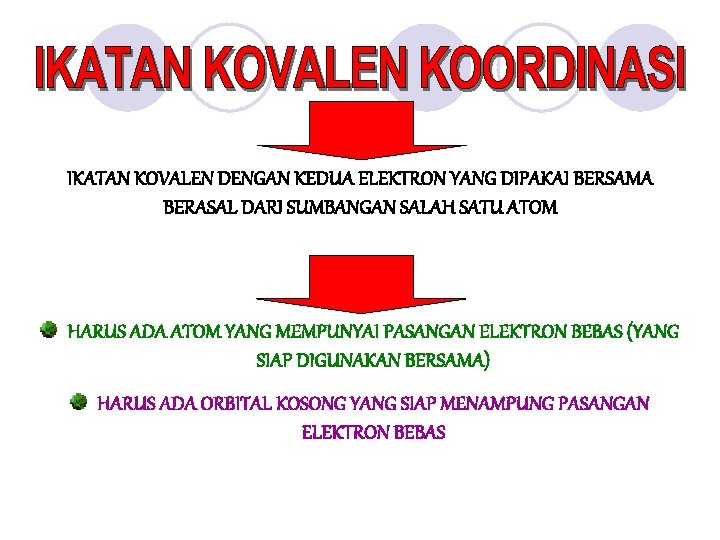
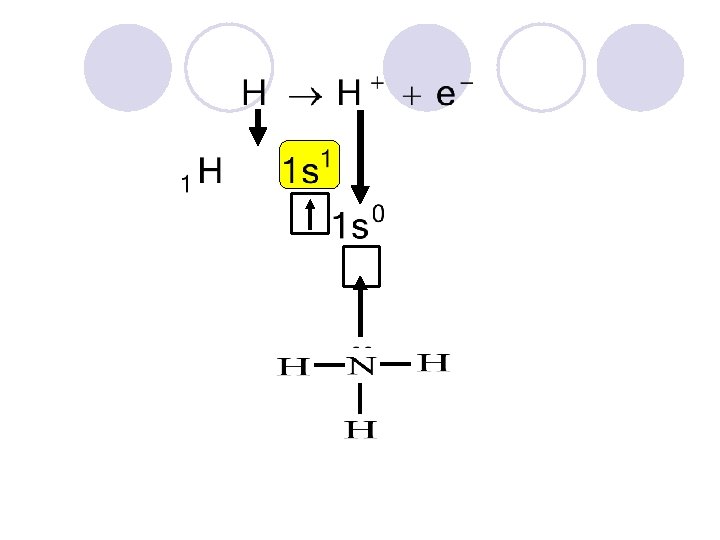
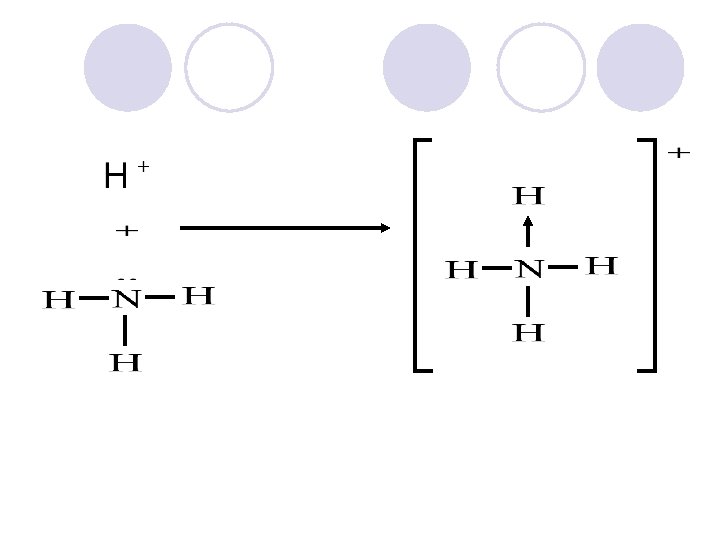
IKATAN KOVALEN DENGAN KEDUA ELEKTRON YANG DIPAKAI BERSAMA BERASAL DARI SUMBANGAN SALAH SATU ATOM HARUS ADA ATOM YANG MEMPUNYAI PASANGAN ELEKTRON BEBAS (YANG SIAP DIGUNAKAN BERSAMA) HARUS ADA ORBITAL KOSONG YANG SIAP MENAMPUNG PASANGAN ELEKTRON BEBAS



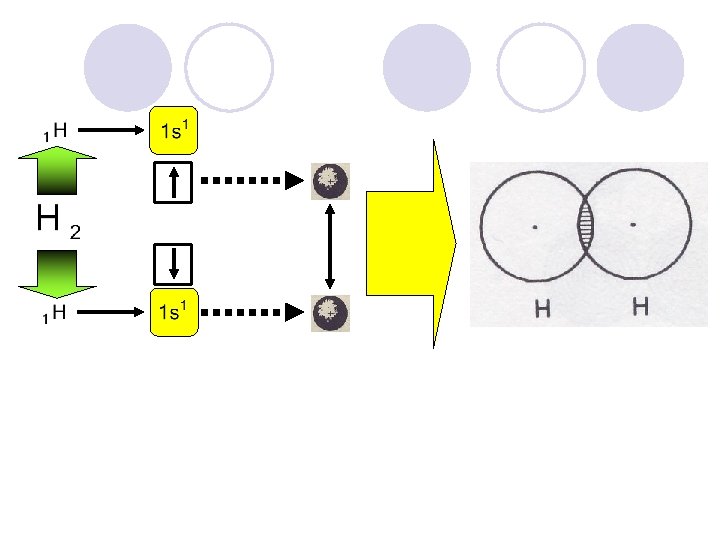
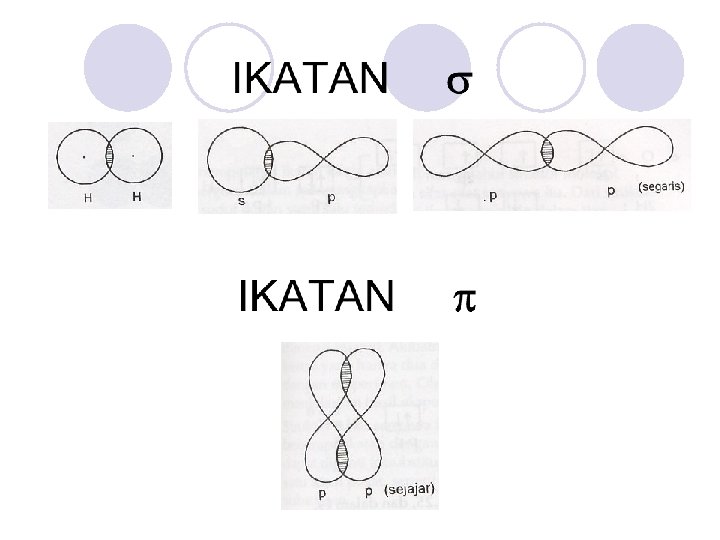
IKATAN ANTARA DUA BUAH ATOM TERBENTUK MELALUI SALING TINDIH DUA ORBITAL ATOM (SATU ORBITAL BERASAL DARI TIAP ATOM)


Pertindihannya lebih besar, sehingga ikatannya lebih kuat Pertindihannya lebih kecil, sehingga ikatannya lebih lemah


PROSES PENGGABUNGAN (PERKAWINAN) BEBERAPA ORBITAL SUATU ATOM DAN KEMUDIAN DITATA ULANG SEHINGGA MELAHIRKAN ORBITAL BARU YANG EKIVALEN DALAM MOLEKUL

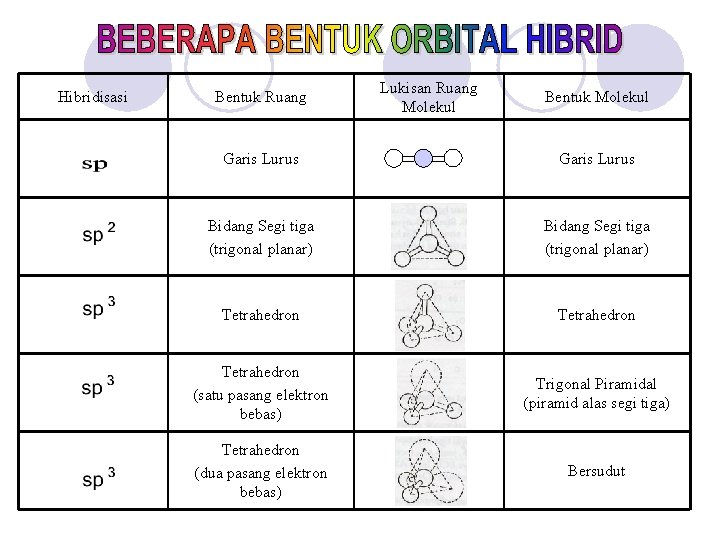
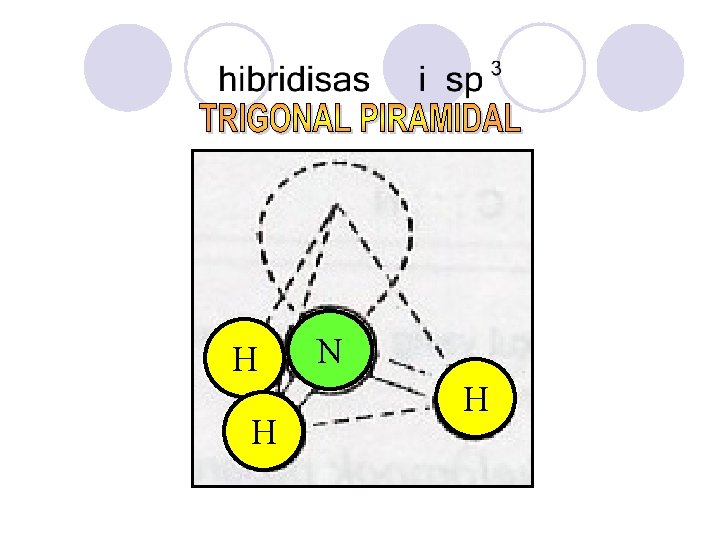
Hibridisasi Bentuk Ruang Lukisan Ruang Molekul Bentuk Molekul Garis Lurus Bidang Segi tiga (trigonal planar) Tetrahedron (satu pasang elektron bebas) Trigonal Piramidal (piramid alas segi tiga) Tetrahedron (dua pasang elektron bebas) Bersudut

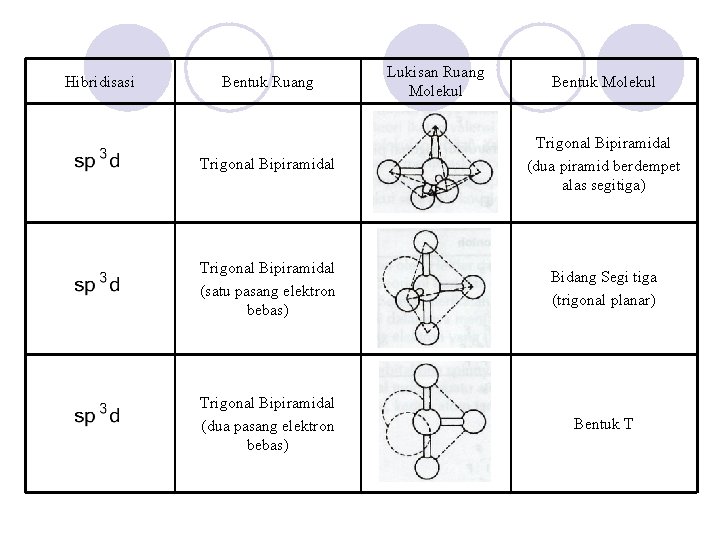
Hibridisasi Bentuk Ruang Lukisan Ruang Molekul Bentuk Molekul Trigonal Bipiramidal (dua piramid berdempet alas segitiga) Trigonal Bipiramidal (satu pasang elektron bebas) Bidang Segi tiga (trigonal planar) Trigonal Bipiramidal (dua pasang elektron bebas) Bentuk T

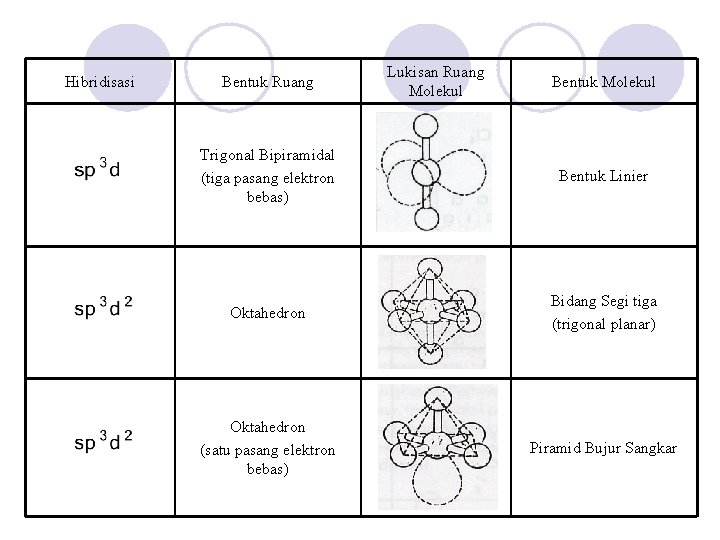
Hibridisasi Bentuk Ruang Lukisan Ruang Molekul Bentuk Molekul Trigonal Bipiramidal (tiga pasang elektron bebas) Bentuk Linier Oktahedron Bidang Segi tiga (trigonal planar) Oktahedron (satu pasang elektron bebas) Piramid Bujur Sangkar

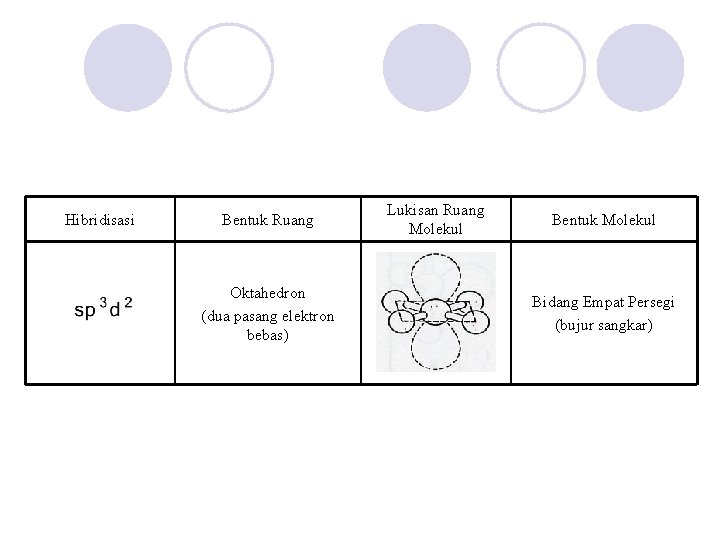
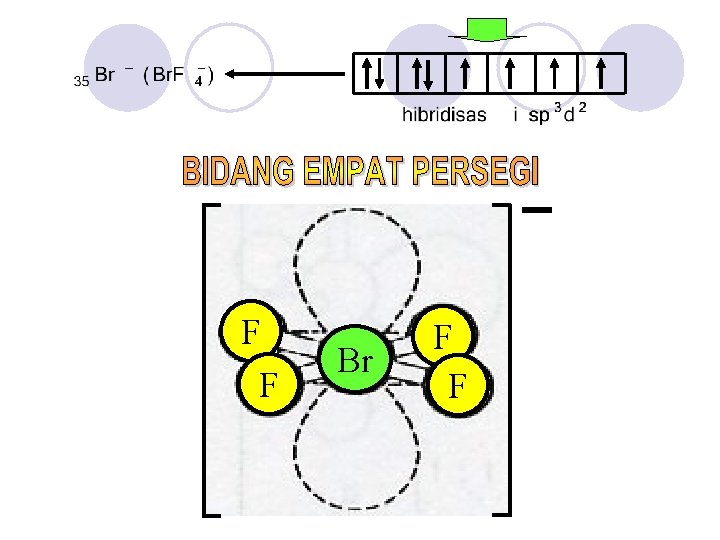
Hibridisasi Bentuk Ruang Oktahedron (dua pasang elektron bebas) Lukisan Ruang Molekul Bentuk Molekul Bidang Empat Persegi (bujur sangkar)


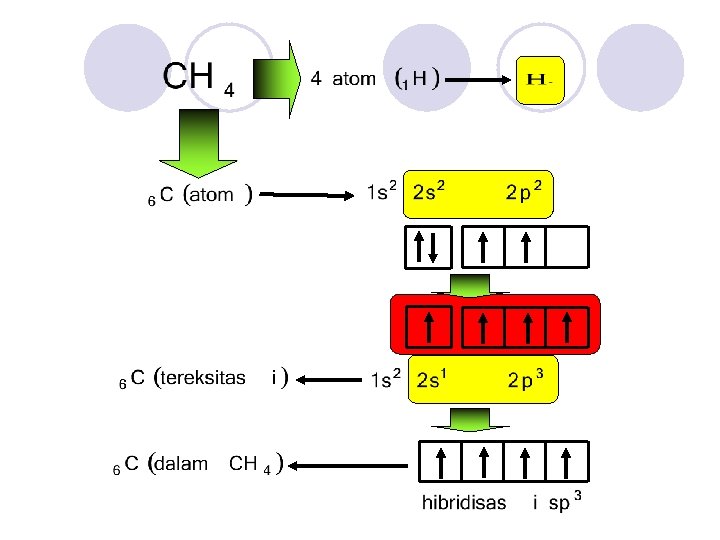
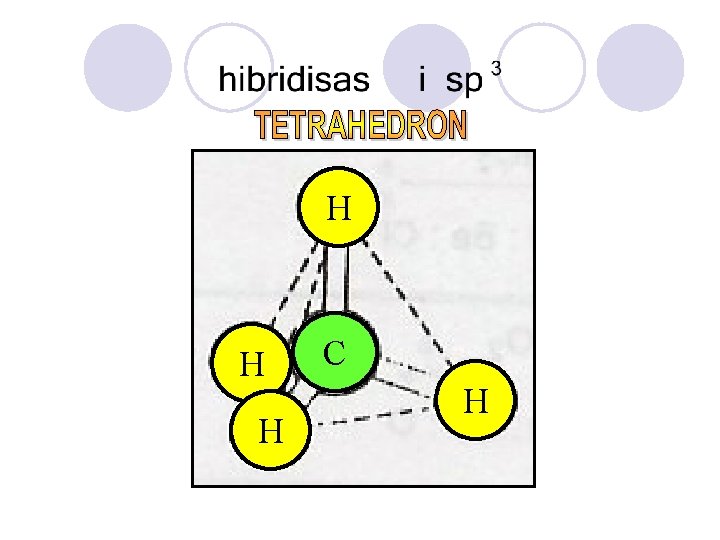
H H H C H


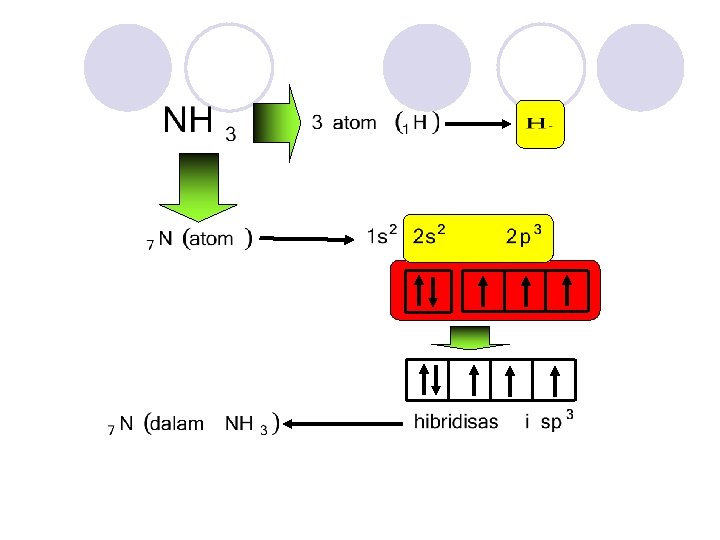
H H N H


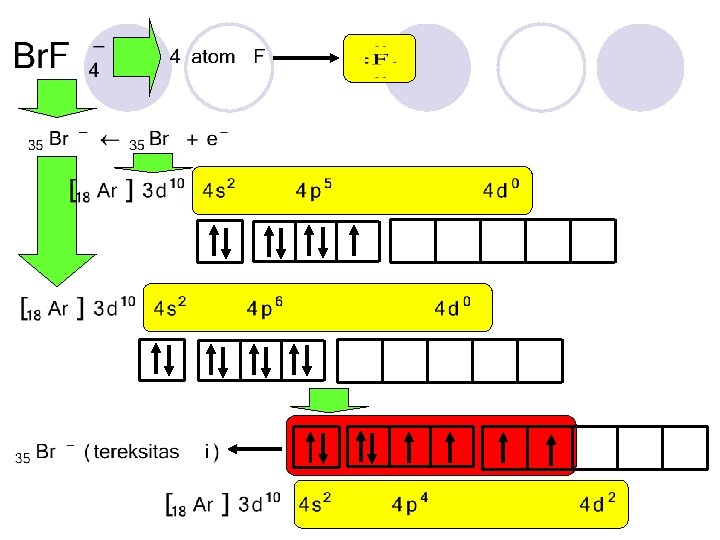
F F Br F F


YANG MENGALAMI HIBRIDISASI HANYA ORBITAL YANG MEMBENTUK IKATAN SIGMA, SEDANGKAN IKATAN PI DALAM IKATAN RANGKAP TIDAK DIHITUNG


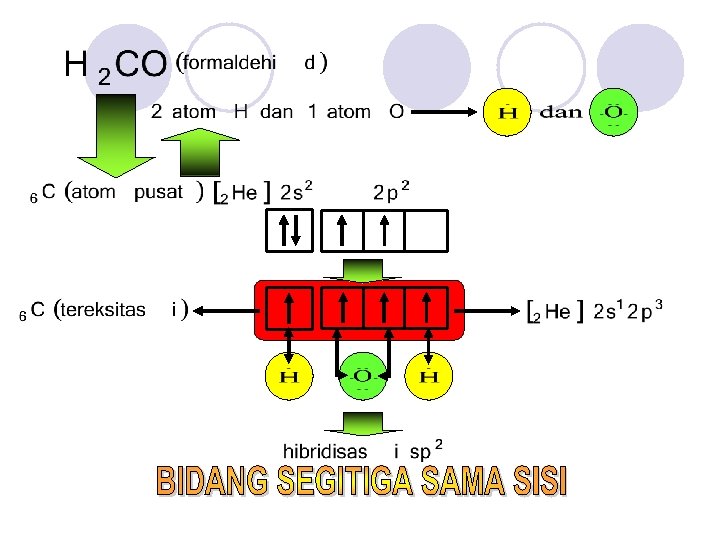
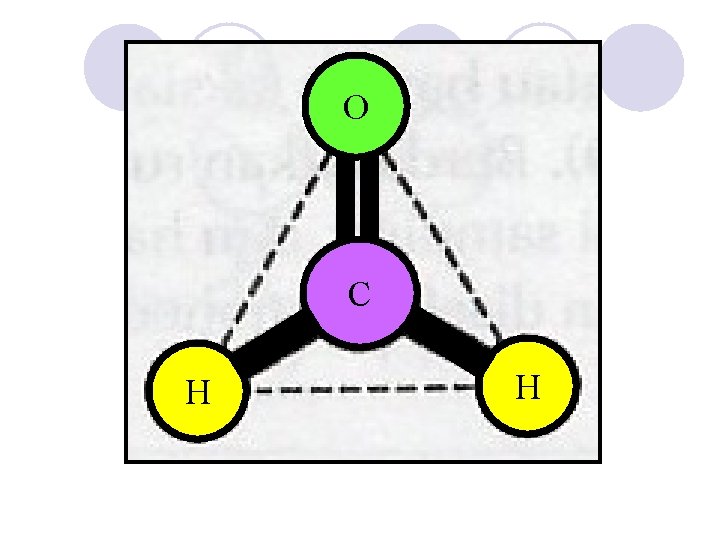
O C H H
