KIMIA ATOM ION MOLEKUL Atom bgn terkecil dari

KIMIA

ATOM, ION & MOLEKUL • Atom : bgn terkecil dari suatu unsur yang sifatnya identik dgn unsur tsb. • Partikel dasar atom : Elektron Proton Netron Massa 1/1837 1 sma Muatan 1 +1 0 Massa elektron kecil skl diabaikan

ATOM • Atom tdd : inti : berisi proton & netron kulit : mrpk lintasan dr elektron Elektron elektron bergerak mengelilingi inti ( ada “orbit”nya ) • Pd 1 atom : jml elektron = jml proton ≠ jml netron • Tiap unsur punya jml proton, netron & elektron yang berlainan

ION & MOLEKUL • Ion adl atom / gugusan atom yang bermuatan listrik sebanyak valensinya Kation : ion bermuatan positif mis : H+, Na+, K+, NH 4+, Ca 2+ Anion : ion bermuatan negatif mis : OH−, Cl−, PO 43−, SO 42− • Molekul : bgn terkecil senyawa, dimana sifat molekul tsb identik dgn sifat seny ybs

UNSUR & SENYAWA • Unsur : zat tunggal yg tak dapat diuraikan menjadi zat lain yg lebih sederhana secara kimia 3 macam unsur : logam non logam semi logam • Senyawa : gabungan 2 atau lebih unsur secara kimia

Struktur elektron dari atom • Elektron beredar mengelilingi inti pada tingkat orbit ( = kulit ) yg berbeda. • Kulit elektron ada : K, L, M, N, O, P, Q Kulit K adl orbit yg paling dekat dgn inti • Elektron pd masing kulit berada pd tingkat energi yg berbeda Elektron pd kulit K ( paling dekat dgn inti ) punya energi paling rendah

BILANGAN QUANTUM Tk. Energi Ke 1 Ke 2 Ke 3 Ke 4 Ke 5 Ke 6 Ke 7 Bil. Quantum n=1 n=2 n=3 n=4 n=5 n=6 n=7 Kulit K L M N O P Q Ada 7 kemungkinan tk. Energi untuk n = 1, 2, 3, 4, 5, 6 dan 7

Jumlah elektron pada kulit • Banyaknya elektron maximum pada tiap kulit adl : 2 n 2 Bil. Quantum Kulit Jml max elektron 1 K 2 x 12 = 2 2 L 2 x 22 = 8 3 M 2 x 32 = 18 4 N 2 x 42 = 32 5 O 2 x 52 = 50

Ketentuan jml max elektron • Kulit paling luar jml max elektron adl 8 • 1 kulit sebelah dalamnya dari kulit terluar, maximum 18 elektron • Pengisian elektron pd 1 kulit harus sampai maximum, baru kemudian menempati kulit berikutnya • Tetapi : ada beberapa pengecualian dlm hal pengisian elektron

Susunan elektron ( contoh ) Unsur H O Na Ca Xe N. A. 1 8 11 20 54 K 1 2 2 L M N O P 6 8 8 8 18 2 18 8 2

Elektron Valensi • Elektron valensi adl banyaknya elektron yg terdapat pd kulit paling luar suatu atom • Valensi adl bilangan yg menunjukkan jml atom H (atau yg ekuivalen dgn H) yg dpt bergabung dgn sebuah atom unsur tsb. • Elektron valensi menentukan sifat kimia suatu atom ( Atom atom dgn jml elektron valensi yg sama, punya sifat kimia sama )

Variable valence Unsur Hidrogen Chlorida Oksigen Sulfida Natrium Na. H Na. Cl Na 2 O Na 2 S Kalium Ca. H 2 Ca. Cl 2 Ca. O Ca. S Aluminium Al. H 3 Al. Cl 3 Al 2 O 3 Al 2 S 3 • Valensi berubah / Variable valence : unsur yg punya >1 valensi Contoh : Cu. O & Cu 2 O; Fe. Cl 2 & Fe 2 Cl 3

NOMOR ATOM • Menyatakan jumlah proton dalam inti ( jumlah proton = jumlah elektron ) MASSA ATOM • = Bilangan massa bobot atom ( B. A. ) • Massa atom = massa Inti atom ( massa elektron diabaikan ) Massa inti tdd massa proton + netron

Contoh Nomor atom & Berat atom Atom Jumlah Berat proton netron elektron atom Hidrogen 1 0 1 1 Cesium 55 78 55 133

ISOTOP • Atom dari unsur yang sama, tetapi punya massa yang berbeda, krn jumlah netron dalam inti berbeda. • Bobot atom beda tetapi nomor atom sama • Jumlah proton dalam inti sama, jumlah elektron juga sama.

BERAT EKUIVALEN • Berat dari unsur tsb yg dapat mengikat atau menggantikan 8 gram Oksigen atau 1, 008 gram Hidrogen • Hub. Berat ekuivalen dgn Berat Atom : B. A. = B. E. X Valensi

Susunan Berkala Unsur • Unsur unsur dikelompokkan atas persamaan sifatnya, & disusun dalam tabel menurut kenaikan nomor atomnya. • Hukum Oktaf : sifat unsur ditemukan lagi secara periodik / berkala pada unsur ke 8. ( tidak termasuk gas inert ) Unsur ke 1 sangat mirip dgn unsur ke 8, unsur ke 2 mirip unsur ke 9 dst.

IKATAN KIMIA 1. Ikatan ion ( ikatan elektrovalen ) Terbentuk oleh pemindahan elektron dari 1 atom ke atom yang lain. Kation : atom yg kehilangan elektron Anion : atom yg mendapatkan elektron Energi ionisasi : energi unt mengeluarkan sebuah elektron dari suatu atom Afinitas elektron : energi unt penambahan 1 atau lebih elektron

IKATAN KIMIA 2. Ikatan kovalen : Penggunaan bersama sepasang elektron oleh 2 atom. Penggunaan bersama 2 atau 3 pasang elektron oleh 2 atom Ikatan rangkap Penggunaan bersama 3 pasang elektron Ikatan ganda 3

IKATAN KIMIA 3. Ikatan Hidrogen : Ikatan antara 1 atom H dengan 2 atom lain dgn selisih elektronegativitas yg besar. 4. Ikatan van der Waals : Gaya tarik menarik antara molekul yang berdekatan

RADIKAL BEBAS • Atom atau molekul yg sangat reaktif krn memiliki 1 atau lebih elektron yg tidak mempunyai pasangan. • Reaksi tsb : reaksi oksidasi • Untuk menangkal bahaya radikal bebas yg berlebihan dlm tubuh : Sistem Anti oksidan • Contoh anti oksidan : vit C, vit E, β karoten Glutation peroksidase, Superoksida dismutase dll
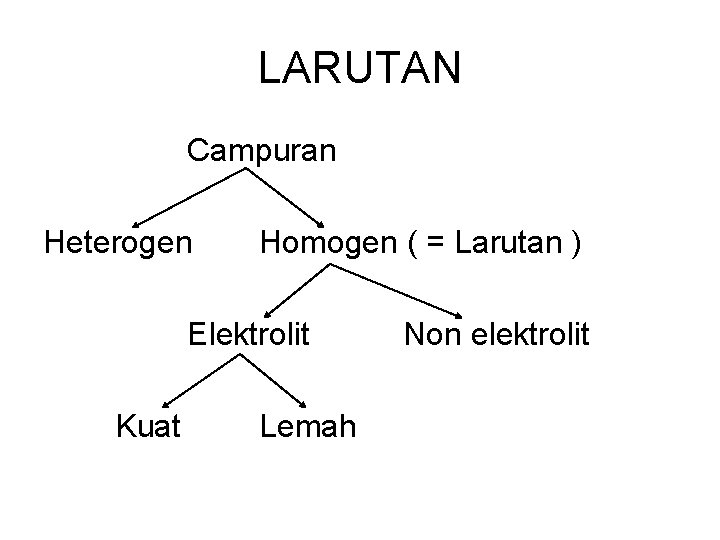
LARUTAN Campuran Heterogen Homogen ( = Larutan ) Elektrolit Kuat Lemah Non elektrolit

LARUTAN • Larutan tdd : zat terlarut ( = solute ) zat pelarut ( = solvent ) • Ada 9 kemungkinan larutan : Zat pelarut Zat terlarut Contoh Cair : air Cair : alkohol 70% Cair : aseton Gas : asetilen zat unt ngelas Cair : air Padat : garam lar. garam

LARUTAN Zat pelarut Zat terlarut Padat : Cadmium Cair : Hg Padat : Paladium Gas : H 2 Padat : Emas Padat : Ag Gas : Udara Cair : minyak wangi Gas : O 2 Gas : He Gas : O 2 Pdt : naftalen Contoh Amalgam gigi Gas oven Sinsin Spray Gas untuk menyelam Kamfer

ELEKTROLIT • Larutan non elektrolit : tidak menghantar arus listrik Contoh : senyawa organik : alkohol, urea, gula • Larutan elektrolit : dapat menghantarkan arus listrik Elektrolit kuat : molekul lar. terionisasi sempurna Elektrolit lemah : molekul lar. tidak seluruhnya terionisasi jadi ion
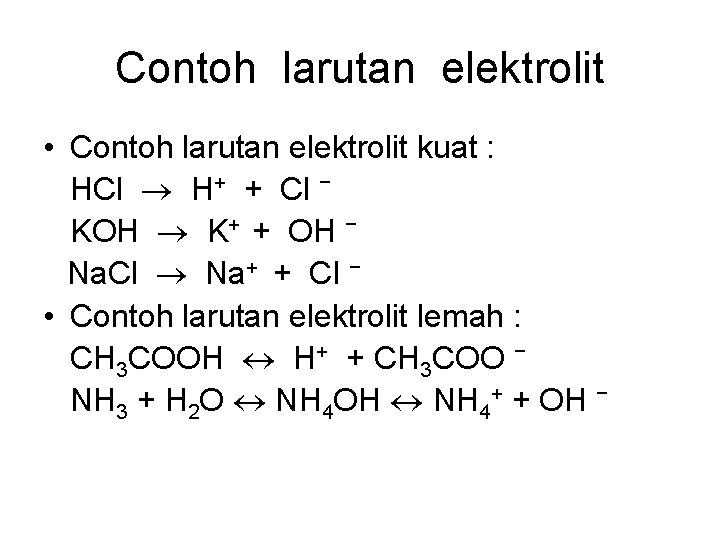
Contoh larutan elektrolit • Contoh larutan elektrolit kuat : HCl H+ + Cl − KOH K+ + OH − Na. Cl Na+ + Cl − • Contoh larutan elektrolit lemah : CH 3 COOH H+ + CH 3 COO − NH 3 + H 2 O NH 4 OH NH 4+ + OH −

Konsentrasi larutan • % berat : jml gram zat terlarut dlm 100 gram larutan lar. Na. OH 10% : 10 gram Na. OH dlm 90 gram air ( 100 gram lar. Na. OH ) • Molalitas : jml mole zat terlarut dlm 1000 gram zat pelarut 1 mole zat mengandung jml partikel yg sama : 6, 02 X 10 23

Konsentrasi larutan • Fraksi mole: jml mole zat dibanding dgn mole zat yg ada dlm larutan mole zat pelarut = n 1 mole zat terlarut = n 2 Fraksi mole zat pelarut = n 1 + n 2 Fraksi mole zat terlarut = n 2 n 1 + n 2

KONSENTRASI LARUTAN • % Mole : adalah fraksi mole x 100 • Molaritas ( M ) = mole / liter jumlah mole zat terlarut dlm 1 liter larutan Osmol : banyaknya partikel per liter Contoh : H 2 SO 4 2 H+ + SO 42− 1 M H 2 SO 4 = 3 osmol 1 m. Mol ( milimol ) = 10 − 3 M 1 μMol ( mikromol ) = 10 − 6 M 1 n. Mol ( nanomol ) = 10 − 9 M

Konsentrasi larutan • Normalitas ( N ) : jml gram ekuivalen zat terlarut dlm 1 liter larutan. N = M x Valensi ( grek = mol x valensi ) Contoh : 0, 2 M H 2 SO 4 = 0, 4 N • mg% : banyaknya mg zat terlarut dalam 100 ml. larutan Contoh : kadar gula darah 150 mg % berarti tiap 100 ml darah mengandung 150 gram glukosa

PENGENCERAN • Massa zat terlarut adalah tetap walaupun volumenya berubah, yg berubah adalah konsentrasinya. • Rumus pengenceran : M 1 x V 1 = M 2 x V 2 M 1 = konsentrasi sebelum pengenceran V 1 = volume sebelum pengenceran M 2 = konsentrasi sesudah pengenceran V 2 = volume sesudah pengenceran
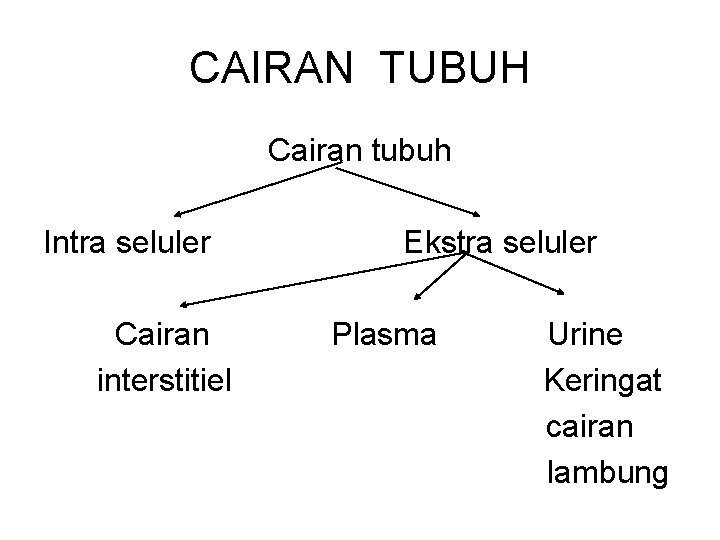
CAIRAN TUBUH Cairan tubuh Intra seluler Cairan interstitiel Ekstra seluler Plasma Urine Keringat cairan lambung

MEMBRAN SEMI PERMEABEL • Contoh : membran sel & dinding kapiler • Membran sel : memisahkan cairan intra seluler dgn cairan interstitiel • Dinding kapiler memisahkan plasma darah dgn cairan interstitiel • Air dpt melintasi membran sel dgn bebas tetapi transpor elektrolit & zat lain terbatas. • Air dpt melintasi dinding kapiler, protein tidak dapat

KOMPOSISI CAIRAN TUBUH Kation m. Eq/liter Anion m. Eq/iiter Na+ K+ Ca 2+ Mg 2+ HCO 3− Cl − Prot Fosfat lain Intra sel 15 160 30 10 40 150 Ekstra sel 142 5 5 3 27 103 16 2 7

PROTEIN PLASMA • Jml m. Eq / liter cairan intrasel > ekstrasel, tetapi osmolaritasnya sama ( N = M x valensi ) Osmolaritas ditentukan oleh [ ] molar, tidak oleh m. Eq / l • [ ] Protein plasma > Protein ekstra seluler • Normal : Protein plasma tak dpt melintasi dinding kapiler ( semi permeable ) • Protein plasma juga “ memegang “ air dlm pembuluh darah

HIDRODINAMIKA 1. 2. 3. 4. PENYERAPAN AIR DLM USUS → PEMB. DARAH → SELURUH TUBUH → FILTRASI KE RUANG ANTAR SEL → DIFUSI MASUK SEL → KELUAR LAGI KE RUANG ANTAR SEL → PEMBULUH DARAH. FILTRASI DI GINJAL → URINE EKSKRESI KE SAL. CERNA ( LIUR PENCERNAAN ) → DISERAP KEMBALI KE KULIT & SAL NAFAS → KERINGAT & UAP AIR (PERSPIRASI INSENSIBILIS )
![Mekanisme keseimbangan cairan dan elektrolit 1. Osmolaritas [ ] zat intrasel & ekstrasel ≠ Mekanisme keseimbangan cairan dan elektrolit 1. Osmolaritas [ ] zat intrasel & ekstrasel ≠](http://slidetodoc.com/presentation_image_h2/733382fde3a0c48e8cbae72425c462d9/image-37.jpg)
Mekanisme keseimbangan cairan dan elektrolit 1. Osmolaritas [ ] zat intrasel & ekstrasel ≠ , tetapi osmolaritas sama. Osmolaritas ditentukan oleh jml partikel dalam larutan. Tekanan osmotik cairan tubuh : 285 5 m. Osm / liter

Mekanisme keseimbangan cairan dan elektrolit • Cairan isotonik : osmolaritas = cairan tbh Cairan hipertonik : , , > cairan tbh Cairan hipotonik : , , < cairan tbh • Osmolaritas berubah air akan bergerak dari 1 ruang ke ruang lain sampai terjadi keseimbangan baru. • Osmo reseptor di otak mengatur osmolaritas cairan tbh dgn hormon ADH

Mekanisme keseimbangan cairan dan elektrolit 2. Tekanan koloid osmotik Koloid pada plasma t. u. tdd : protein dgn berat molekul tinggi tek. koloid osmotik sbgn besar dipengaruhi protein plasma. Permeabilitas kapiler thd koloid : kecil. Efek koloid : menahan air dlm plasma. Tekanan koloid osmotik plasma : 20 – 25 mm. Hg.

Mekanisme keseimbangan cairan dan elektrolit 3. Starling‘s forces Tek. Koloid osmotik plasma 25 mm Hg Tek. darah ujung arteri kapiler 36 mm. Hg Tek. darah ujung vena kapiler 15 mm. Hg Keadaan ini menyebabkan difusi air & ion keluar kapiler msk cairan interstitiel pd ujung arteri reabsorbsi 95% cairan ini pd ujung vena kapiler.

Mekanisme keseimbangan cairan dan elektrolit 4. Sodium pump Protein intra sel : menarik air ke dalam sel Na+ ikut masuk sel mekanisme Sodium pump pd dinding sel segera memompa Na+ keluar ke cairan interstitiel. ( [Na+] ekstra sel > intra sel )

Mekanisme keseimbangan cairan dan elektrolit 5. Keseimbangan Donnan Teori keseimbangan antara elektrolit renik dgn elektrolit koloid yg dibatasi membran shg terjadi beda potensial. Ion koloid tak dpt berdifusi melalui membran, ion lain dpt berdifusi pd kead. seimbang : pembagian ion & tek. osmotiknya tidak akan sama.

Mekanisme keseimbangan cairan dan elektrolit Contoh keseimbangan Donnan: Eritrosit mengandung Hb, protein, K+, Na+, Cl−, HCO 3−. Plasma jugamengandung protein, K+, Na+, Cl−, HCO 3−. Membran sel eritrosit impermeabel thd prot, Hb, K+, Na+, tetapi permeabel thd HCO 3−, Cl− Antara eritrosit & plasma terjadi keseimb Donnan

SISTEM KOLOID Pembagian larutan menurut besarnya diameter partikel : Jenis larutan Diameter Lar. sejati ( dispers molekuler ) : < 1 mμ Lar. koloid ( dispers halus ) : 1 – 100 mμ Suspensi ( dispers kasar ) : > 100 mμ Campuran 2 zat dimana zat yg satu terbagi halus dlm zat yg lain disbt : Sistem dispers

SISTEM DISPERS • Sistem dispers tdd 2 fase : Fase terdispersi = fase dalam Medium dispersi = fase luar Fase terdispersi tersebar dlm medium dispersi • Fase terdispersi & medium dispersi dpt tdd dari fase padat, cair & gas. • Kecuali : fase terdispersi & medium dispersi tak dpt sama berupa gas.
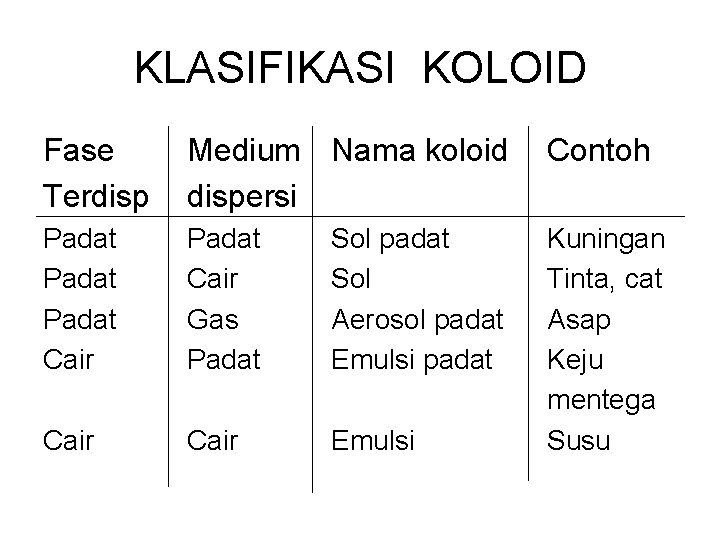
KLASIFIKASI KOLOID Fase Terdisp Medium Nama koloid dispersi Contoh Padat Cair Gas Padat Sol padat Sol Aerosol padat Emulsi padat Cair Emulsi Kuningan Tinta, cat Asap Keju mentega Susu
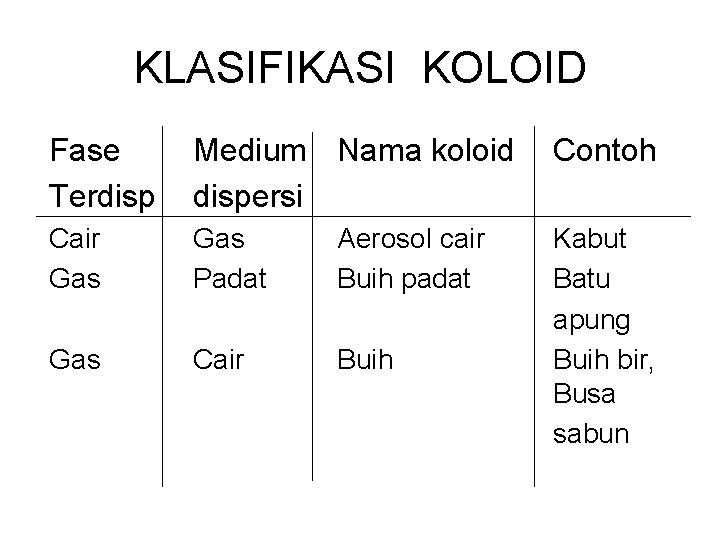
KLASIFIKASI KOLOID Fase Terdisp Medium Nama koloid dispersi Contoh Cair Gas Padat Aerosol cair Buih padat Gas Cair Buih Kabut Batu apung Buih bir, Busa sabun

SOL & GEL • Koloid yg berupa : cairan encer : Sol agak padat : Gel paling encer : jelly paling kaku : tanduk Sol : liofob = suspensoid liofil = emulsoid ( hidrofob = takut air; hidrofil = senang air )

HIDROSOL Kesanggupan bolak balik : • Sol Gel Contoh : Gelatin • Setelah fase terdispersi dipisah dr medium dispersnya ( mis. dikeringkan ) dapat membentuk koloid kembali, bila ditambahkan medium dispersnya lagi. Contoh : mi instant

Sifat sifat umum sistem koloid 1. 2. 3. 4. Besar partikel 1 – 100 mμ Penyaringan : dengan ultra filter Difusi : sukar Efek Tyndall : cahaya yg jatuh pd sistem koloid akan disebar oleh partikel koloid. 5. Luas permukaan besar daya adsorbsi besar 6. Sedimentasi : partikel koloid dapat diendapkan

Sifat sifat umum sistem koloid 7. Muatan listrik partikel koloid : ( + ) atau ( ) Medium pendispersnya memp muatan berlawanan. Elektroforesa : gerakan fase terdispersi melalui medium dispersnya dibawah pengaruh arus listrik. 8. Gerak Brown : gerakan acak partikel koloid dlm medium pendispersnya

IMBIBISI • Gel dikeringkan susut. Bila ditambahkan pelarutnya kembali partikel koloid menyerap pelarut tsb partikel menggelembung Pembersihan lar. koloid : Dialisa Ultra filtrasi

KESEIMBANGAN ASAM BASA • Konsep Arrhenius : Asam : dlm air : H+ dan anion Basa : dlm air : OH− dan kation • Teori proton Bronsted & Lowry : Asam : donor proton Basa : menerima proton Asam kuat : mudah melepas H+ Basa kuat : afinitas thd proton besar

ASAM DAN BASA • Teori pasangan elektron Lewis : asam : penerima elektron basa : donor elektron Teori Lewis berlaku untuk semua pelarut & netralisasi asam – basa walaupun tak ada pelarutnya.

ELEKTROLIT AMFOTIR • Senyawa yg bila dilarutkan dlm air, dapat menghasilkan H 3 O+ atau OH− • Dpt bersifat sbg donor proton dan juga sbg akseptor proton Al 3+ + 3 OH− Al(OH)3 Al. O 2 + H 2 O • Umumnya berupa senyawa organik mis : asam amino & protein

TETAPAN KESEIMBANGAN • Tetapan keseimbangan ( K ) menggambarkan seberapa jauh reaksi berlangsung sampai berkesudahan • Tetapan keasaman = Ka • Tetapan kebasaan = Kb
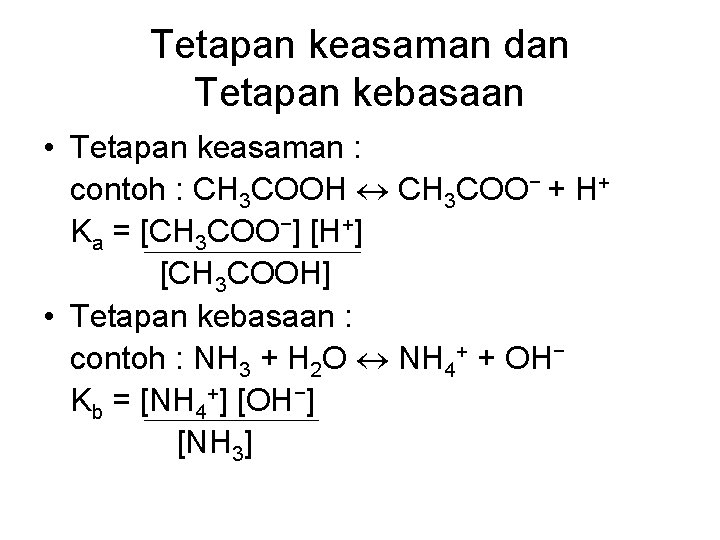
Tetapan keasaman dan Tetapan kebasaan • Tetapan keasaman : contoh : CH 3 COOH CH 3 COO− + H+ Ka = [CH 3 COO−] [H+] [CH 3 COOH] • Tetapan kebasaan : contoh : NH 3 + H 2 O NH 4+ + OH− Kb = [NH 4+] [OH−] [NH 3]
![DERAJAT KEASAMAN • p. H = log [H+] • Rentang p. H untuk larutan DERAJAT KEASAMAN • p. H = log [H+] • Rentang p. H untuk larutan](http://slidetodoc.com/presentation_image_h2/733382fde3a0c48e8cbae72425c462d9/image-58.jpg)
DERAJAT KEASAMAN • p. H = log [H+] • Rentang p. H untuk larutan : asam netral basa ↓ 0 7 makin kuat 14 makin kuat

Keseimbangan asam – basa dalam tubuh • p. H cairan tubuh normal : 7, 35 – 7, 45 p. H cairan tubuh terlalu asam : Asidosis p. H cairan tubuh terlalu basa : Alkalosis • p. H normal harus selalu dipertahankan. • Ada 2 mekanisme unt mempertahankan p. H cairan tubuh : Homeostasis respiratorik & ginjal Sistem buffer tubuh

HOMEOSTASIS RESPIRATORIK DAN GINJAL = Regulasi keseimbangan asam – basa Pengeluaran ion H+ dlm jumlah yg sama dgn yg dibentuk oleh metabolisme sel. 1. Sistem pernafasan : Mengatur pengeluaran CO 2 p. H↓ merangsang pusat pernafasan CO 2 akan dikeluarkan melalui paru.

Regulasi keseimbangan asam basa 2. Ginjal : Mengatur pengeluaran kelebihan asam dan basa melalui ginjal.

Sistem buffer tubuh • Larutan buffer adalah larutan yg dapat mempertahankan p. H nya, bila pada lar. tsb ditambahkan asam atau basa. • Sistem buffer tubuh : Buffer bikarbonat Buffer fosfat Buffer protein Buffer Hb ( dlm eritrosit )

ANALISA KIMIA • Analisa kualitatif : untuk identifikasi zat • Analisa kuantitatif : untuk mengetahui jml / kadar zat Analisa kualitatif : cara fisika : organoleptik tetapan fisika mikroskopis cara kimia : reagens ttt.

Analisa kuantitatif • Gravimetri • Volumetri : Titrasi asam – basa ( penetralan ) Titrasi pengendapan Titrasi pembentukan komplex Titrasi redoks • Instrumental: Polarimetri, Spektrofotometri Kromatografi

Analisis volumetri Zat yg mau ditentukan kadarnya direaksikan dgn zat lain yg tlh diketahui konsentrasinya, ( = larutan standar / larutan baku ) • Cara kerja dlm analisa volimetri : Titrasi berdasarkan reaksi : a. A + t. T produk A = analit T = titran a molekul analit A bereaksi dgn t molekul titran T

Syarat untuk reaksi dlm analisa titrimetrik 1. Reaksi harus berlangsung cepat 2. Harus sesuai persamaan reaksi tertentu, tak boleh ada reaksi samping. 3. Reaksi harus berjalan lengkap pd titik ekuivalensi ( tetapan keseimbangan reaksi harus sangat besar ) 4. Ada indikator untuk menunjukkan kapan titik ekuivalensi tercapai ( kapan penambahan titran dihentikan ).

Reaksi reaksi untuk analisis volumetri / titrasi 1. Reaksi kombinasi ion : a. Reaksi penetralan ( asam – basa ) b. Reaksi pengendapan c. Reaksi pembentukan komplex yg mudah larut 2. Reaksi redoks ( berdsrkan perpindahan elektron ) a. Oksidimetri b. Iodometri

TITIK EKUIVALEN & TITIK AKHIR TITRASI • Titik ekuivalen adl titik dimana banyaknya titran yg ditambahkan, ekuivalen dgn banyaknya zat yg dititrasi. • Titik akhir titrasi adalah saat dimana terjadi perubahan yang terlihat pada titrasi. • Keadaan ideal : Titik akhir titrasi berimpit dgn titik ekuivalen. • Perbedaan antara T. E. dgn titik akhir titrasi disebut : Kesalahan titrasi

Perubahan sifat larutan pada T. E. • • • Perubahan warna larutan / indikator Kekeruhan Perubahan potensial elektroda Perubahan konduktivitas larutan Perubahan arus listrik dlm larutan

INDIKATOR Contoh indikator asam – basa Indikator Perubahan warna Jangka p. H dgn naiknya p. H Biru brom timol Jingga metil Merah metil Lakmus Phenolphthalein kuning ke biru merah ke kuning merah ke biru tak berwarna ke merah 6, 0 – 7, 6 3, 1 – 4, 4 4, 2 – 6, 2 5, 0 – 8, 0 – 9, 6
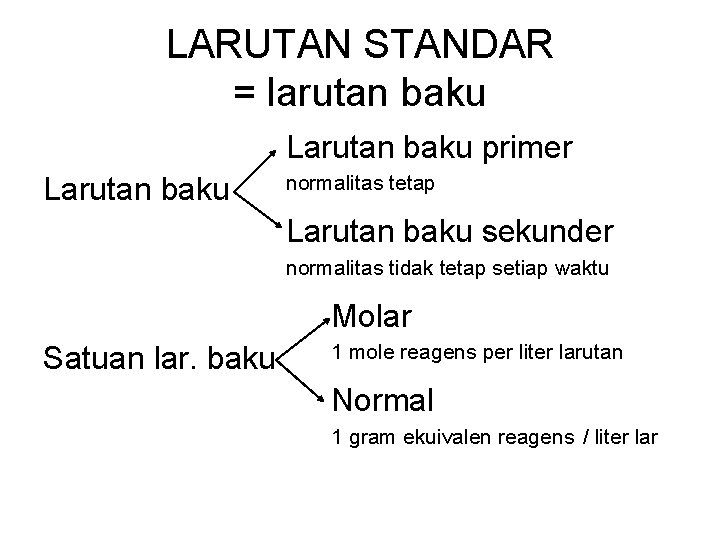
LARUTAN STANDAR = larutan baku Larutan baku primer Larutan baku normalitas tetap Larutan baku sekunder normalitas tidak tetap setiap waktu Molar Satuan lar. baku 1 mole reagens per liter larutan Normal 1 gram ekuivalen reagens / liter lar

Syarat zat untuk larutan baku primer 1. Murni, rumus molekul pasti 2. Stabil 3. Tidak higroskopis, mudah dikeringkan 4. Berat ekuivalen zat harus tinggi Contoh larutan baku primer : Kalium bikromat Natrium oksalat Natrium karbonat Boraks

STOIKIOMETRI 1. Berat atom (B. A. ) & Berat molekul (B. M. ) Bobot dlm gram dari 1 mole zat mgd 6, 023 x 1023 partikel B. M. adl jml berat total dr atomnya 2. Berat ekuivalen ( B. E. ) B. A. = B. E. x Valensi valensi = angka yg menunjukkan berapa banyak atom H / atom lain yg ekuivalen dgn atom H yg dapat bergabung dgn unsur tsb.

BERAT EKUIVALEN • Definisi B. E. suatu zat tgt dari macam reaksinya. Suatu senyawa dpt memp B. E. yg tak sama pd reaksi yg berlainan • Pd titik akhir titrasi jml ekuivalen zat yg dititrasi = jml ekuivalen zat penitrasi (titran)

Perhitungan dlm analisis volumetri V 1 x N 1 = V 2 x N 2 V 1 = Volume titran N 1 = Titer titran ( normalitas ) V 2 = Volume zat yg dititrasi N 2 = Titer zat yg dititrasi ( normalitas )

KARBOHIDRAT • Senyawa mengandung C, H, dan O • Mrpk polihidroksi dari aldehida & keton atau turunan mereka • 3 gol utama K. H. : Monosakarida Oligosakarida Polisakarida

MONOSAKARIDA • Tdd 1 unit polihidroksi aldehid atau keton • Rumus empiris : ( CH 2 O )n n≥ 3 • Kerangka monosakarida : rantai atom C : berikatan tunggal tak bercabang 1 diantara atom C tsb berikatan ganda dgn 1 atom O membtk gugus karbonil

Kerangka Monosakarida Atom atom C lainnya berikatan dengan gugus hidroksil ( OH ) • Aldosa : gugus karbonil pd ujung rantai C • Ketosa : gugus karbonil di tengah rantai C Rangka atom C 3 buah : triosa Rangka atom C 4 buah : tetrosa Rangka atom C 5 buah : pentosa Rangka atom C 6 buah : hexosa
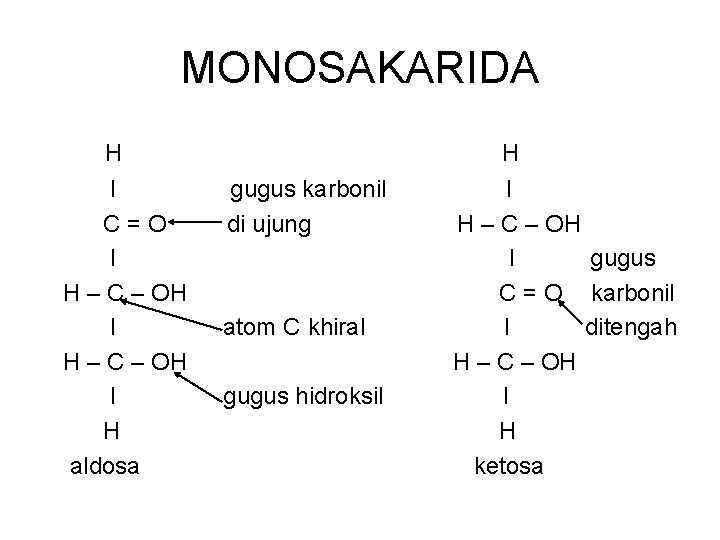
MONOSAKARIDA H I C=O I H – C – OH I H aldosa H gugus karbonil di ujung atom C khiral gugus hidroksil I H – C – OH I gugus C = O karbonil I ditengah H – C – OH I H ketosa

MONOSAKARIDA Punya ≥ 1 atom C khiral ( kecuali dihidroksi aseton ) Bersifat optik aktif : dpt memutar bidang polarisasi dari polarimeter ke satu arah. Dextro – rotary : memutar bid. Polarisasi kekanan : ( d ) Levo – rotary : memutar bid. Polarisasi kekiri : ( l ) Huruf kecil ‘d’ dan ‘l’ tak boleh ditulis dgn huruf besar ‘D’ dan ‘L‘

PROYEKSI FISHER • Struktur aldosa & ketosa ditulis dlm bentuk rantai lurus. • Bentuk ‘D’ : gugus hidroksil pd atom C khiral yg paling jauh dr atom C karbonil mengarah ke kanan • Bentuk ‘L’ : gugus hidroksil pd atom C khiral yg paling jauh dr atom C karbonil mengarah ke kiri Monosakarida di alam umumnya berbentuk ‘D’

RUMUS HAWORTH Monosakarida rantai atom C ≥ 5 di dalam larutan sbgn besar ada dlm bentuk siklik (lingkaran / cincin) Siklisasi monosakarida terjadi akibat reaksi pembentukan hemiasetal • Bentuk cincin 6 anggota : Piranosa • Bentuk cincin 5 anggota : Furanosa

RUMUS KONFORMASI Cincin piranosa monosakarida umumnya bukan bidang datar, tetapi dlm konformasi: ‘ kursi ‘ ‘ kapal ‘

Contoh MONOSAKARIDA • Glukosa : ‘bahan bakar’ utama untuk sumber energi pd manusia. Disimpan sbg Glikogen. • Fruktosa : suatu ketosa, gula yg paling manis • Galaktosa : berikatan dgn glukosa → laktosa • Ribosa : membentuk kerangka polimer dari asam nukleat

GULA PEREDUKSI • Monosakarida yg dpt dioksidasi oleh zat oksidan (senyawa pengoksidasi) lemah Gula dioksidasi pd gugus karbonil Senyawa pengoksidasi jadi ter reduksi • Banyaknya senyawa pengoksidasi yg ter reduksi dpt diukur → [ ] gula dpt dihitung • Untuk analisa kadar gula darah & urine pd penyakit D. M.

DISAKARIDA • K. H. tersusun dari 2 Monosakarida dihubungkan oleh ikatan Glikosida Contoh : Maltosa : glukosa – glukosa Laktosa : glukosa – galaktosa Sukrosa : glukosa fruktosa

GULA INVERSI • Campuran D glukosa dan D fruktosa dlm konsentrasi molar yg sama. • Diperoleh dgn. hidrolisis dr sukrosa Hidrolisis dgn cara : enzim invertase pemanasan sukrosa dlm air • Inversi sukrosa jadi glukosa & sukrosa terjadi dlm suasana asam.

POLISAKARIDA ( = GLIKAN ) • Polisakarida berbeda satu sama lain dlm hal : kandungan unit monosakarida panjang rantai tingkat percabangan • 2 jeis polisakarida : Homopolisakarida Heteropolisakarida Contoh homopolisakarida : pati, glikogen Contoh heteropolisakarida: asam hyaluronat

PATI Berbagai macam pati ≠ sifatnya tergantung: panjang rantai unit monosakaridanya rantai lurus / bercabang Pati tdd 2 fraksi : amilosa : ( ± 20% ), larut dlm air panas amilopektin : (± 80% ), tak larut dlm air panas

AMILOSA • Polimer tak bercabang dari glukosa • Hidrolisis partial → maltosa Hidrolisis lengkap → D glukosa • Molekul amilosa membentuk spiral sekitar molekul Yodium → warna biru Dipakai untuk Uji garam ber Yodium

AMILOPEKTIN • Rantai glukosa yang bercabang • Hidrolisis lengkap → D glukosa Hidrolisis partial → Dekstrin

GLIKOGEN • Struktur mirip amilopektin, tetapi cabangnya lebih banyak • Glukosa disimpan sbg glikogen dalam hati dan otot

PROTEIN • Polimer tak bercabang dari Asam Amino • Saling berhubungan dgn ikatan Peptida • Termasuk suatu Polipeptida ada yg bukan protein, mis : Glutation, Vasopresin, Oksitosin • Ada 20 macam A. A. pada protein tubuh manusia, yg dirangkai oleh sel tubuh dlm berbagai kombinasi → ber macam protein

ASAM AMINO • Asam organik, yg punya ciri khas sbb : • Gugus karboksil ( COOH ) & Gugus amina ( NH 2 ) terikat pada 1 atom C yg sama ( Karbon α)
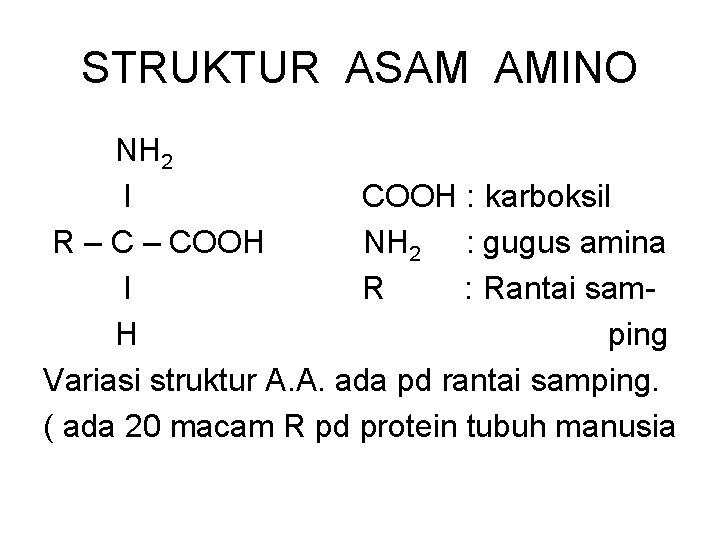
STRUKTUR ASAM AMINO NH 2 l COOH : karboksil R – COOH NH 2 : gugus amina l R : Rantai sam H ping Variasi struktur A. A. ada pd rantai samping. ( ada 20 macam R pd protein tubuh manusia

ASAM AMINO ESENSIEL • Asam amino yg diperlukan untuk sintesis protein tubuh • A. A. tsb tidak disintesis tubuh manusia • A. A. tsb harus terdapat dlm makanan kita • Spy sintesis protein tbh dpt berlangsung : 20 macam A. A. harus lengkap & dalam jumlah yg cukup
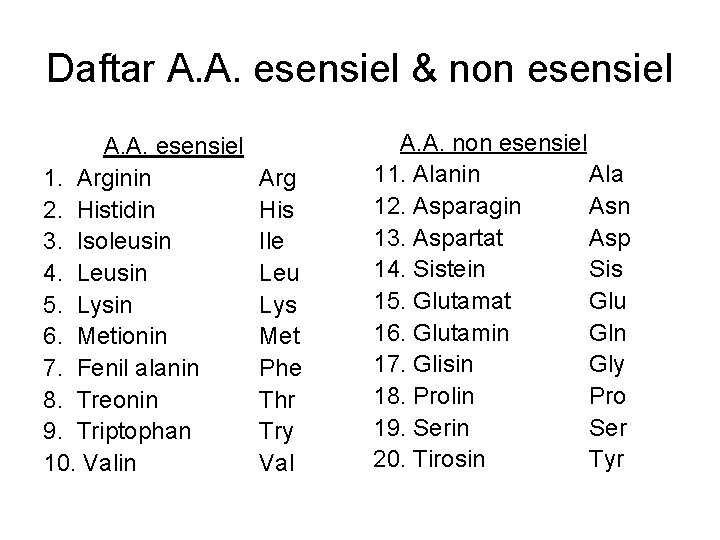
Daftar A. A. esensiel & non esensiel A. A. esensiel 1. Arginin 2. Histidin 3. Isoleusin 4. Leusin 5. Lysin 6. Metionin 7. Fenil alanin 8. Treonin 9. Triptophan 10. Valin Arg His Ile Leu Lys Met Phe Thr Try Val A. A. non esensiel 11. Alanin Ala 12. Asparagin Asn 13. Aspartat Asp 14. Sistein Sis 15. Glutamat Glu 16. Glutamin Gln 17. Glisin Gly 18. Prolin Pro 19. Serin Ser 20. Tirosin Tyr

SINTESIS ASAM AMINO Manusia mensintesis A. A. dgn. 3 jalan : • Transaminasi • Asimilasi dari amonia bebas • Modifikasi rangka atom C dari A. A. yg sudah ada

PEPTIDA • Ikatan peptida adl : ikatan amida antara gugus α amino dari satu A. A. dgn gugus karboksil dari A. A. lain. • Tiap A. A. dari satu molekul protein disebut Satuan, atau Unit, atau Residu.

STRUKTUR PROTEIN Rangkaian A. A. dari protein dpt melipat & ber rotasi ( mluntir ) Tiap prot. punya struktur 3 dimensi yg unik. Ada 4 tingkat struktur dasar protein : • Struktur primer • Struktur sekunder • Struktur tersier • Struktur kuarterner

Struktur protein / lipatan polipeptida • Struktur primer : rentetan A. A. dlm suatu molekul protein Identitas suatu protein ditentukan struktur primernya. • Struktur sekunder : Lipatan lokal dlm suatu bgn polipeptida Yg plg sering adl heliks α, pleated sheet, & reverse turn

Struktur protein / lipatan polipeptida • Struktur tersier : Pelipatan secara keselu ruhan suatu rantai poli – peptida → membentuk bulatan ( 3 dimensi ) • Struktur kuarterner : susunan beberapa polipeptida bersama

DENATURASI PROTEIN • Hilangnya sifat struktur sekunder, tersier & kuarterner krn terkacaunya ikatan yg mengutuhkan molekul tsb. • Struktur primer tetap utuh • Protein dpt berfungsi hanya bila ia melipat pd konformasi aslinya. • Akibat denaturasi : hilangnya banyak sifat biologis protein tsb.

Faktor penyebab denaturasi protein • Suhu tinggi • Perubahan p. H yg ekstrim • Perubahan tipe pelarut ( yg memperlunak ikatan ) • Radiasi • Zat zat tertentu : mis. deterjen

SINTESIS PROTEIN • Tiap sel dpt mensintesis proteinnya sendiri • Jenis protein dlm sel menentukan fungsi sel tsb. • Dlm inti sel tubuh manusia ada 23 pasang kromosom. Tiap kromosom tdd ratusan gen. Gen terbuat dari a. l. D N A ( suatu asam nukleat ). Dlm inti sel ada asam nukleat lain : R N A

SINTESIS PROTEIN • D N A : menentukan susunan A. A. yang membentuk protein ( jumlah, jenis dan urutannya ) • R N A : mengambil A. A. dari sitoplasma dan merangkainya sesuai perintah D N A

TAHAP SINTESIS PROTEIN • • • Aktivasi A. A. Inisiasi rantai polipeptida Pemanjangan rantai polipeptida Terminasi ( penghentian pemanjangan ) Pelipatan & pengolahan polipeptida

KLASIFIKASI PROTEIN Menurut bentuknya : 1. Protein serat ( = protein struktural ) Contoh : kolagen, elastin, keratin 2. Protein globular Albumin, globulin, fibrinogen, hormon 3. Protein konyugasi Glukoprotein, lipoprotein, nukleoprotein

KLASIFIKASI PROTEIN Berdasarkan peran biologis : 1. Enzim 2. Protein transport : Hb, lipoprotein 3. Protein nutrien & penyimpan : Kasein, Feritin 4. Protein kontraktil : aktin, myosin 5. Protein struktural : kolagen, keratin 6. Protein pertahanan : Imunoglobulin, fibrinogen, trombin 7. Protein pengatur : Hormon

LIPIDA Penggolongan berdasarkan struktur kimia : 1. Lipida sederhana : Trigliserida, wax 2. Lipida majemuk : Fosfolipida, spingolipid 3. Lipida turunan : Steroid, karotenoid

TRIGLISERIDA = Tri asil gliserol = lipida =lemak = lemak netral Adl : ester dari gliserol dgn 3 molekul A. L. 3 molekul tsb bisa sama, bisa berbeda Komponen utama dr depot lemak pd tubuh Tidak terdapat pd membran sel

SIFAT TRIGLISERIDA • Tidak larut dalam air • Larut dlm pelarut organik : eter, kloroform, benzena dll. • Terhidrolisi jika : dididihkan dgn asam atau basa diberi enzim lipase
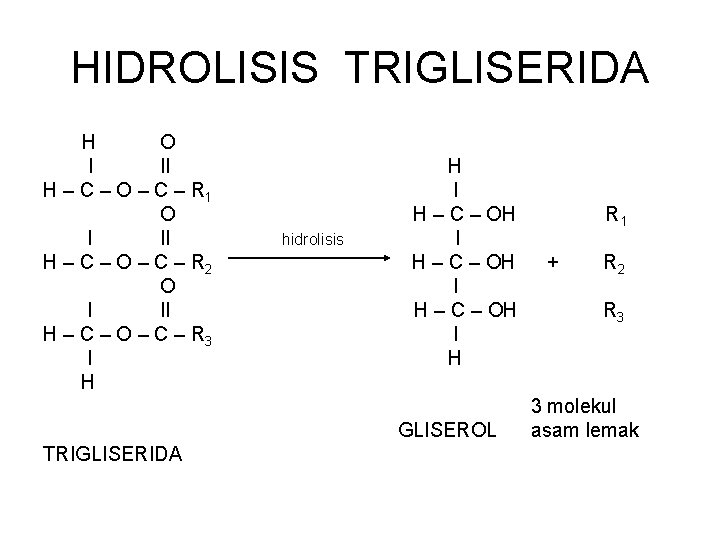
HIDROLISIS TRIGLISERIDA H O I II H – C – O – C – R 1 O I II H – C – O – C – R 2 O I II H – C – O – C – R 3 I H hidrolisis H I H – C – OH I H GLISEROL TRIGLISERIDA R 1 + R 2 R 3 3 molekul asam lemak
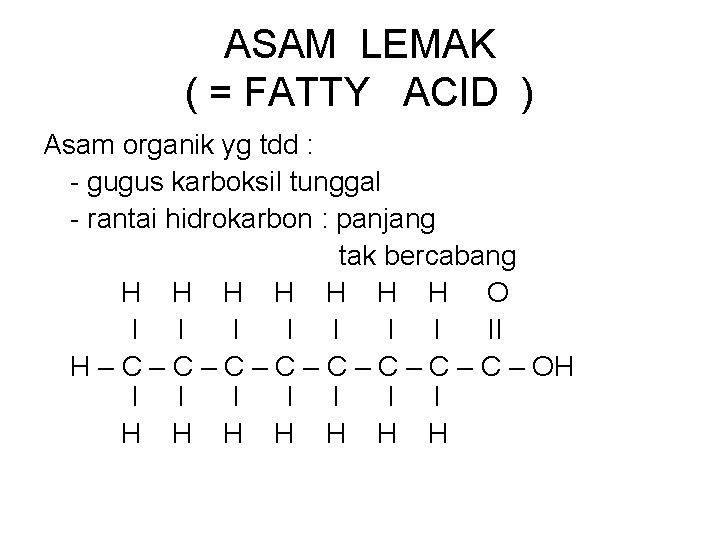
ASAM LEMAK ( = FATTY ACID ) Asam organik yg tdd : gugus karboksil tunggal rantai hidrokarbon : panjang tak bercabang H H H H O I I I II H – C – C – OH I I I I H H H H
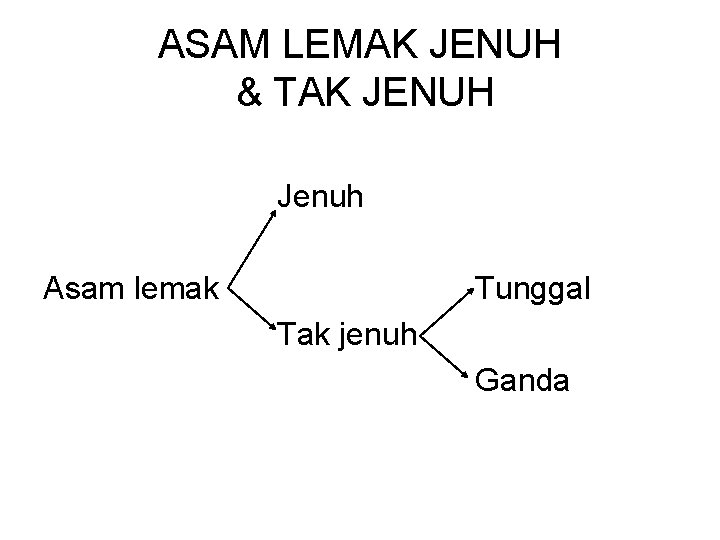
ASAM LEMAK JENUH & TAK JENUH Jenuh Asam lemak Tunggal Tak jenuh Ganda

ASAM LEMAK ESENSIEL Asam lemak yg : Diperlukan untuk metabolisme tubuh Tidak disintesis oleh tubuh manusia Harus terdapat dlm makanan kita Ada 2 : Linoleat Linolenat

SABUN & DETERJEN • Sabun : garam logam alkali ( Na atau K ) dari asam lemak. • Deterjen : garam sulfonat atau sulfat berantai panjang dari Na. • Penyabunan : peristiwa hidrolisa lipida oleh pemanasan dgn alkali menghasilkan sabun dr komponen A. L. nya
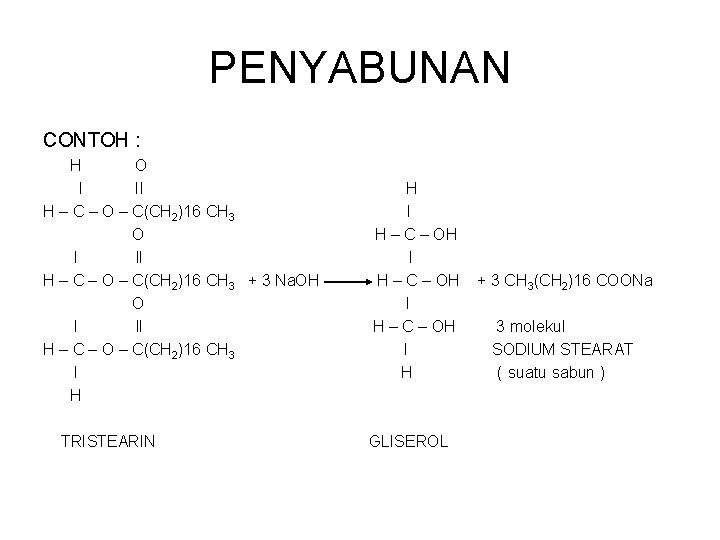
PENYABUNAN CONTOH : H O l II H – C – O – C(CH 2)16 CH 3 O l ll H – C – O – C(CH 2)16 CH 3 + 3 Na. OH O l ll H – C – O – C(CH 2)16 CH 3 l H TRISTEARIN H l H – C – OH l H GLISEROL + 3 CH 3(CH 2)16 COONa 3 molekul SODIUM STEARAT ( suatu sabun )

SABUN Didalam air, molekul sabun terurai sbb : CH 3(CH 2)16 COONa CH 3(CH 2)16 COO + Na+ Tidak semua lipida dapat tersabunkan : Contoh : Steroid, Terpena (minyak atsiri, terpentin) Sabun punya kemampuan mengemulsi kotoran berminyak, sehingga dpt dibuang dgn pembilasan.

MISEL • Asam lemak tidak larut dlm air, tetapi dpt terdispersi menjadi MISEL dlm larutan encer Na. OH atau KOH • Lemak terdispersi menjadi tetesan lemak yg dikelilingi molekul sabun. • Misel adalah butiran lemak dlm medium air, butir lemak tsb dikelilingi oleh segerombol (50 – 150) molekul sabun. Rantai hidrokarbon dari molekul sabun mengarah ke – tengah butiran lemak, & ujung ion nya menghadap ke air.

SURFACE ACTIVE AGENT = SENYAWA SURFAKTAN = SENYAWA YG DAPAT MENURUNKAN TEGANGAN PERMUKAAN AIR. Contoh : Sabun, deterjen • Sabun mengendap dlm air sadah ( air yg banyak mengandung Ca 2+, Fe 3+, Mg 2+ dll. ) • Deterjen tidak mengendap bersama ion logam dari air sadah, tetapi tak dpt diuraikan oleh mikro org. shg menimbulkan limbah yg ber busa

LILIN / WAX LILIN adalah ester asam lemak dgn alkohol berantai panjang. Contoh : sekresi kelenjar kulit sbg pelindung rambut. Lilin juga sbg bahan bakar, misalnya pd : lebah, plankton

FOSFOLIPID • LIPIDA yg mengandung gugus fosfat • Fungsi : t. u. sbg unsur struktural membran sel. • Tak pernah disimpan dlm jumlah banyak. • Lipida membran tdd : Fosfolipid ( plg banyak Spingolipid Kolesterol Jenis fosfolipid utama pe membran sel adl : Fosfogliserid

FOSFOGLISERID • Tdd : Rangka gliserol 2 molekul asam lemak ( berikatan ester dgn gugus hidroksil ke 1 & ke 2 dari gliserol ) Asam Fosfat (berikatan ester dgn gugus hidroksil ke 3 gliserol) “Gugus kepala” (berikatan ester dgn asam fosfat ) Mis : Etanolamin, Kolin, Serin, Inositol )
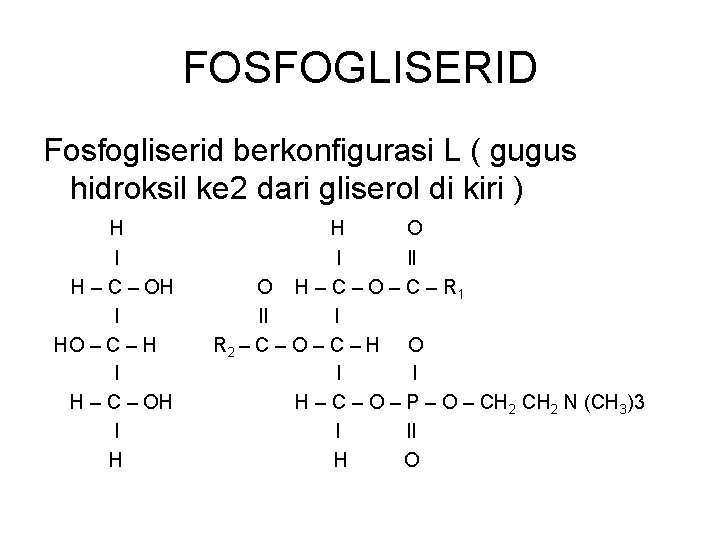
FOSFOGLISERID Fosfogliserid berkonfigurasi L ( gugus hidroksil ke 2 dari gliserol di kiri ) H l H – C – OH l HO – C – H l H – C – OH l H H O l ll O H – C – O – C – R 1 ll l R 2 – C – O – C – H O l l H – C – O – P – O – CH 2 N (CH 3)3 l ll H O

SPINGOLIPID • Lipida membran ke 2 terbanyak setelah fosfolipid • Tidak mengandung gliserol • Tdd : 1 spingosin 1 asam lemak 1 gugus kepala Spingosin adl. Molekul alkohol amino berantai panjang at. Turunannya dibentuk dari Serin dan Palmitat Seramida : Spingosin dgn 1 molekul asam lemak

Serebrosida & Gangliosida • Contoh Spingolipid : Spingomyelin : gugus kepala : Fosfokolin Terdapat pd selubung myelin sel syaraf ttt Serebrosida & Gangliosida : Spingolipid dgn gugus kepala mengand. Unit K. H. Tergolong Glikolipid ( lipid yg mengand. gugus gula )

STEROID • Steroid yg paling banyak : STEROL ( suatu steroid alkohol ) • KOLESTEROL : sterol utama pd jar. hewan mrpk komponen penting dr : lipoprotein membran sel • Guna kolesterol : membentuk berbagai hormon membentuk membran sel membentuk vit. D & garam empedu

LIPOPROTEIN • Lipida yg berikatan dgn protein • Ada 4 jenis lipoprotein dlm plasma darah : Kilomikron LDL VLDL HDL • Trigliserida & kolesterol ditranspor dlm tubuh oleh 4 jenis lipoprotein plasma tsb. • Kilomikron mrpk tetesan lemak T. G. yg hampir murni, dilapisi 1 lapis protein amat tipis
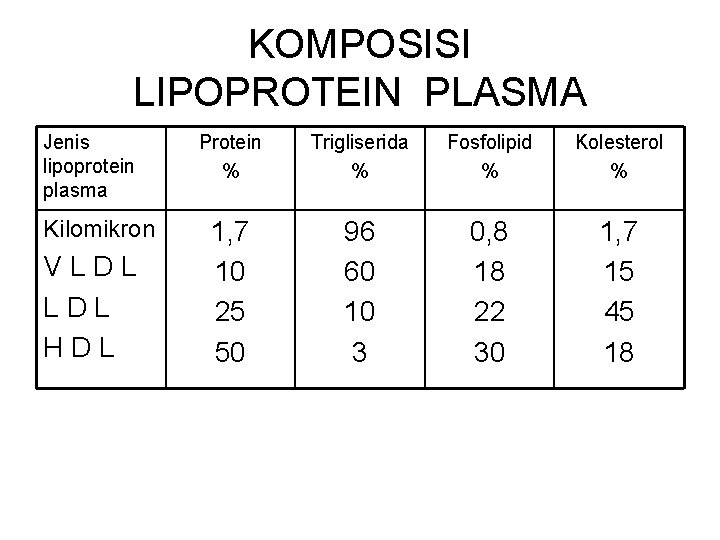
KOMPOSISI LIPOPROTEIN PLASMA Jenis lipoprotein plasma Kilomikron VLDL HDL Protein % Trigliserida % Fosfolipid % Kolesterol % 1, 7 10 25 50 96 60 10 3 0, 8 18 22 30 1, 7 15 45 18
- Slides: 130