IKATAN KIMIA Menentukan geometri bentuk molekul dengan 1

IKATAN KIMIA Menentukan geometri (bentuk) molekul dengan: 1. Teori domain 2. Hibridisasi

1. Teori Domain • Suatu cara meramalkan geometri molekul berdasarkan tolak menolak elektron pada kulit luar atom pusat. • Domain elektron berarti kedudukan elektron atau daerah keberadaan elektron. • Jumlah domain ditentukan sbb: 1. Setiap elektron ikatan merupakan 1 domain. 2. Setiap PEB merupakan 1 domain.

Prinsip Dasar Teori Domain • Antardomain elektron pada kulit luar atom pusat saling tolak-menolak, sehingga domain elektron akan mengatur diri, sehingga tolak-menolak menjadi minimum. • Urutan tolakan domain elektron PEB-PEB > PEB-PEI > PEI-PEI
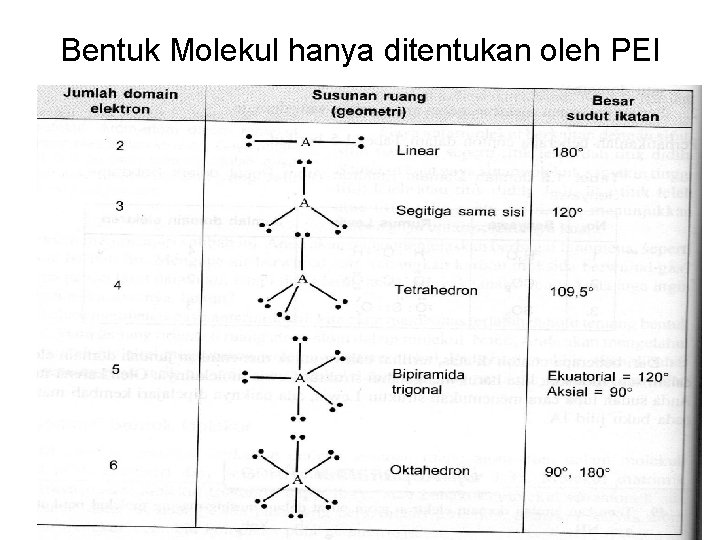
Bentuk Molekul hanya ditentukan oleh PEI

Merumuskan tipe molekul • Atom pusat dinyatakan dengan lambang A • Setiap domain elektron ikatan dinyatakan dengan X • Setiap domain elektron bebas dinyatakan dengan E • Contoh : IF 3 ; IF 5

Tipe molekul • Senyawa biner berikatan tunggal EV = elektron valensi atom pusat • Senyawa biner berikatan rangkap atau ikatan kovalen koordinat X’ = jumlah elektron yang digunakan atom pusat Contoh: SO 2 ; Xe. O 4 ; POCl 3

Menentukan geometri molekul • Menentukan tipe molekul • Menentukan geometri domain-domain elektron sekitar atom pusat • Menetapkan domain elektron terikat • Menentukan geometri molekul (bentuk molekul) • Contoh: H 2 O Tipe molekul : AX 2 E 2 domain elektron : 4 (2 bebas 2 terikat) Bentuk geometri : tetrahedron Bentuk molekul : planar bentuk V

Berbagai Bentuk molekul PEI PEB TIPE Bentuk molekul 2 3 4 3 2 5 4 0 0 0 1 2 0 1 AX 2 AX 3 AX 4 AX 3 E AX 2 E 2 AX 5 AX 4 E 3 2 AX 3 E 2 Linier Segitiga sama sisi Tetrahedron Piramida Trigonal Planar bentuk V Bipiramida trigonal Bidang 4 / seesaw / jungkat-jungkit Planar bentuk T 2 3 AX 2 E 3 Linier
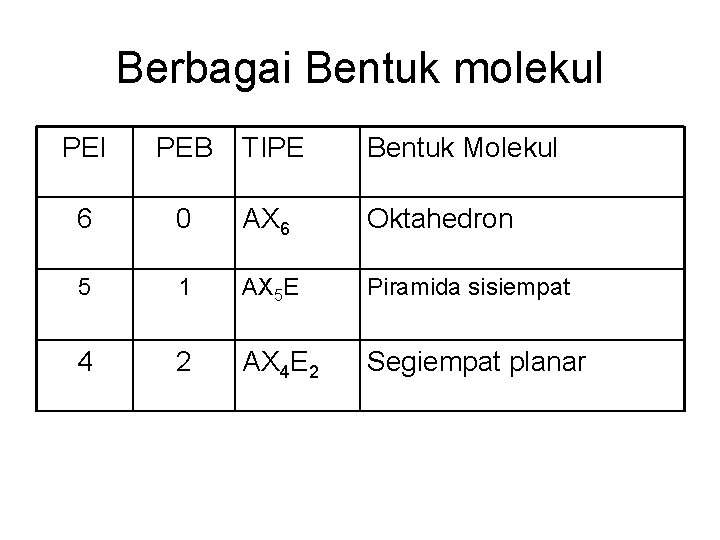
Berbagai Bentuk molekul PEI PEB TIPE Bentuk Molekul 6 0 AX 6 Oktahedron 5 1 AX 5 E Piramida sisiempat 4 2 AX 4 E 2 Segiempat planar
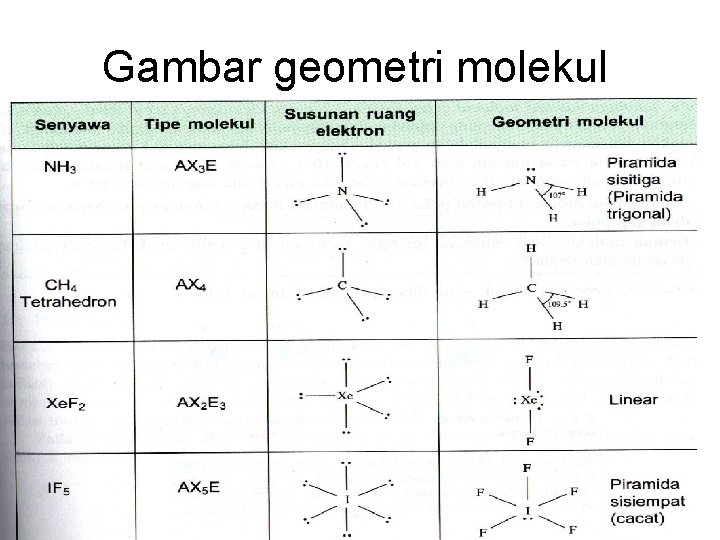
Gambar geometri molekul

Gambar Geometri Molekul
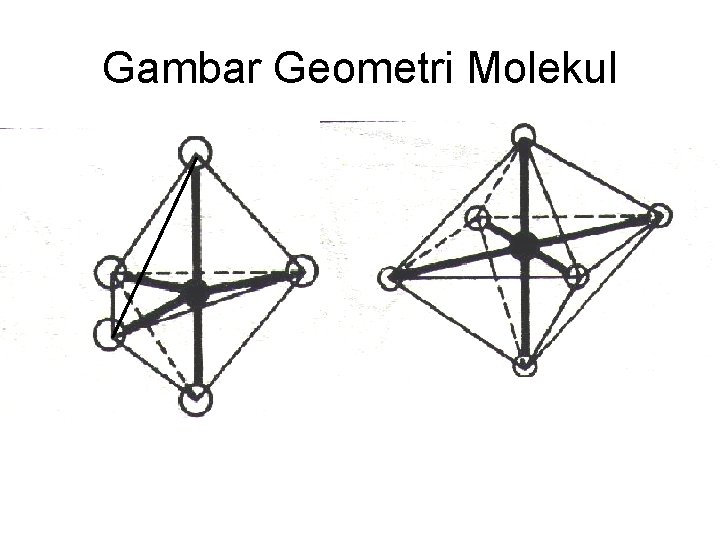
Gambar Geometri Molekul
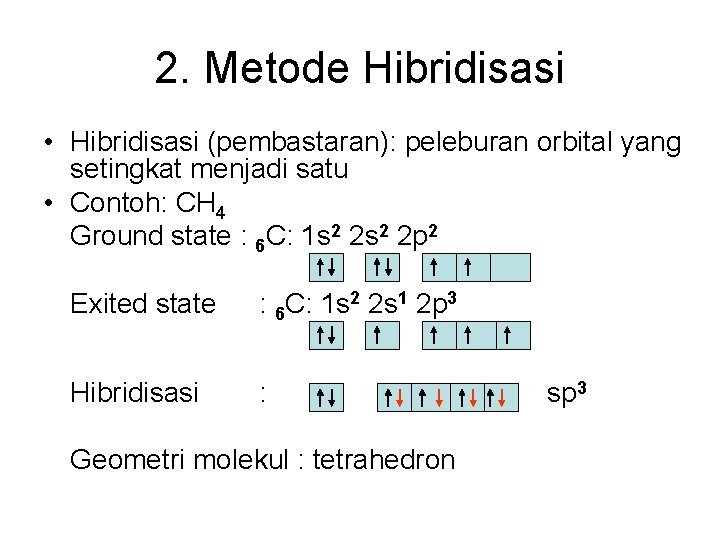
2. Metode Hibridisasi • Hibridisasi (pembastaran): peleburan orbital yang setingkat menjadi satu • Contoh: CH 4 Ground state : 6 C: 1 s 2 2 p 2 Exited state : 6 C: 1 s 2 2 s 1 2 p 3 Hibridisasi : Geometri molekul : tetrahedron sp 3
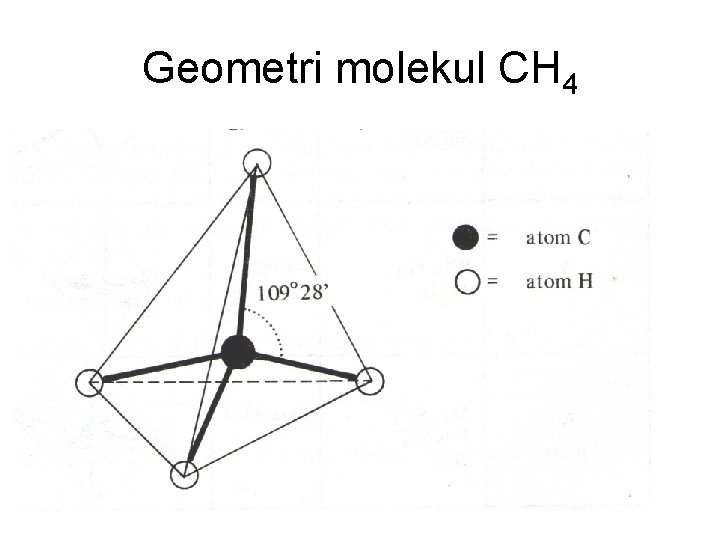
Geometri molekul CH 4
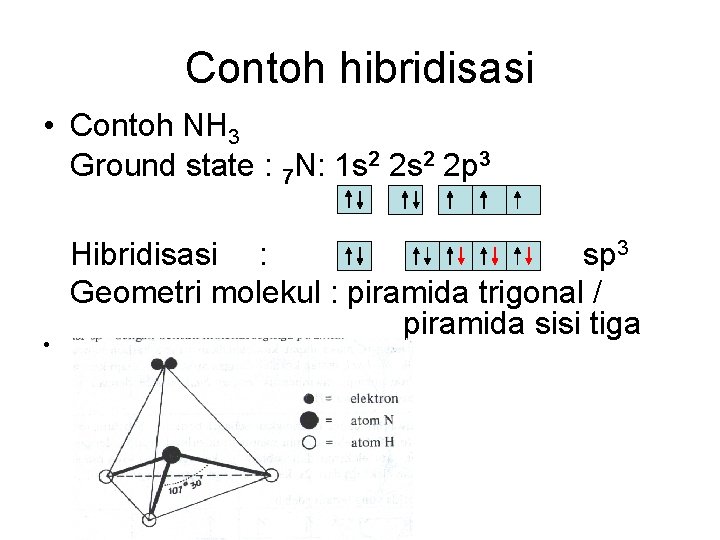
Contoh hibridisasi • Contoh NH 3 Ground state : 7 N: 1 s 2 2 p 3 • Hibridisasi : sp 3 Geometri molekul : piramida trigonal / piramida sisi tiga
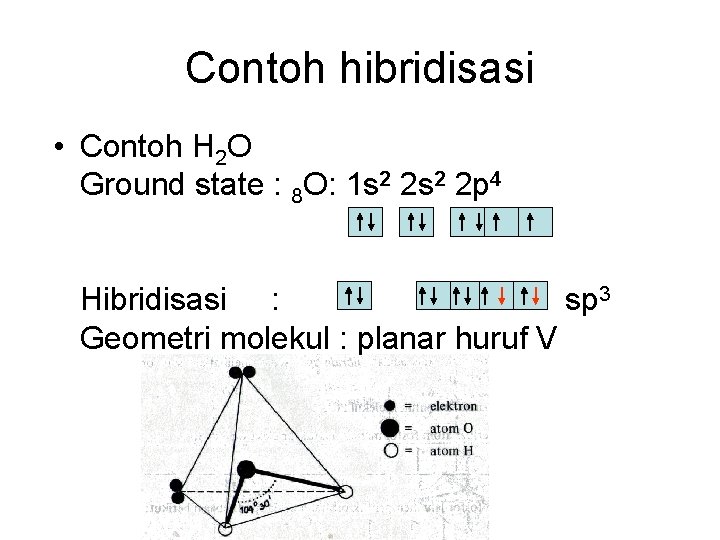
Contoh hibridisasi • Contoh H 2 O Ground state : 8 O: 1 s 2 2 p 4 Hibridisasi : sp 3 Geometri molekul : planar huruf V

Gambar orbital hibrida
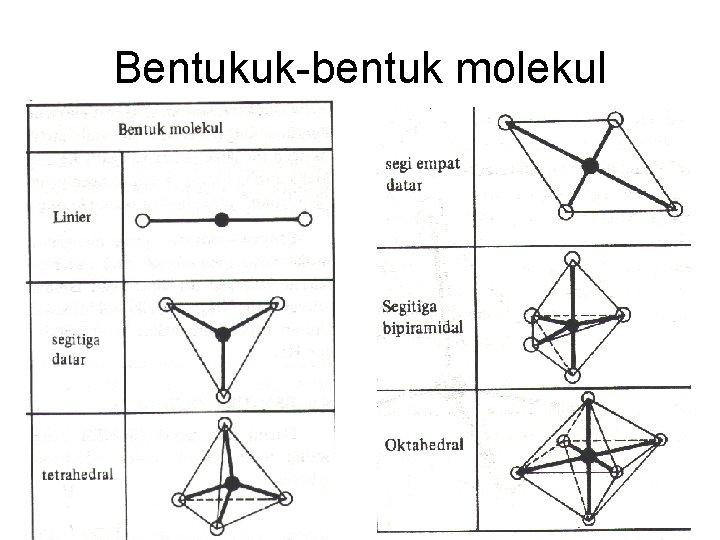
Bentukuk-bentuk molekul

2. Molekul Polar dan Nonpolar • Suatu molekul akan bersifat polar jika memenuhi 2 syarat : 1. Ikatan dalam molekul bersifat polar. 2. Bentuk molekul tidak simetris.

Gaya tarik antar molekul • Berkaitan dengan sifat-sifat fisis (titik leleh, titik didih) • Semakin kuat gaya tarik antar molekul, semakin tinggi titik didih maupun titik lelehnya • Ada 3 : a. gaya London b. gayatarik dipol-dipol c. gaya tarik dipol-dipol terimbas

Gaya London= gaya dispersi (gaya tarik dipol sesaat-dipol terimbas) • Gaya tarik antar molekul dalam zat yang non polar. • Molekul non polar mempunyai sebaran muatan (awan elektron) yang simetris. • Pergerakan elektron menghasilkan dipol sesaat. • Dipol sesaat mampu mengimbas molekul dipol sesaat yang lain sehingga menghasilkan gaya tarik dipol sesaat dipol terimbas.

Gaya London • Polarisabilitas berkaitan dengan Mr dan bentuk molekul • Semakin besar Mr, semakin mudah mengalami polarisasi, semakin kuat gaya London Contoh : He = 4 (4 K) dan Rn = 222 (221 K) • Molekul yang memanjang lebih mudah mengalami polarisasi dibanding molekul yang membulat, kompak dan simetris. Contoh: n-pentana (36, 1 o. C) dan neo pentana (9, 5 o. C) • Zat-zat yang molekulnya bertarikan hanya berdasarkan gaya London, mempunyai titik leleh dan titik didih yang rendah dibandingkan dengan Mr relatif sama

Gaya tarik dipol-dipol • Gaya tarik antar molekul dalam zat yang polar. • Lebih kuat dibanding gaya London • Zat polar cenderung lebih tinggi titik didih dan titik lelehnya dibanding zat non polar yang Mr-nya relatip sama • Contoh: n-butana (tc = -138, 36 o. C ; td = - 0, 5 o. C) aseton (Tc = -94, 8 o. C ; td = 56, 2 o. C)

Gaya tarik dipol-dipol • Membandingkan zat dengan Mr yang berbeda jauh, gaya London menjadi lebih penting • Contoh : HCl (momen dipol = 1, 08) td = 188, 1 K HI (momen dipol = 0, 38) td = 237, 8 K Fakta menunjukkan bahwa gaya London dalam HI mampu mengimbangi kontribusi gaya dipol-dipol dalam HCl

Gaya tarik dipol-dipol terimbas • Terjadi antara molekul polar dengan molekul non polar • Contoh : Gaya tarik antara molekul HCl dan molekul CCl 4 Dipol melekul polar akan mengimbas molekul non polar di sekitarnya, sehingga mengalami dipol sesaat.

Ikatan Hidrogen • Gaya antar molekul yang relatif kuat terdapat dalam senyawa hidrogen dengan unsur-unsur yang mempunyai keelektronegatifan besar (N, F, O) • Contoh: Ikatan hidrogen dalam HF • Ikatan hidrogen jauh lebih kuat daripada gaya-gaya van der waals (gaya-gaya antar molekul secara kolektif)
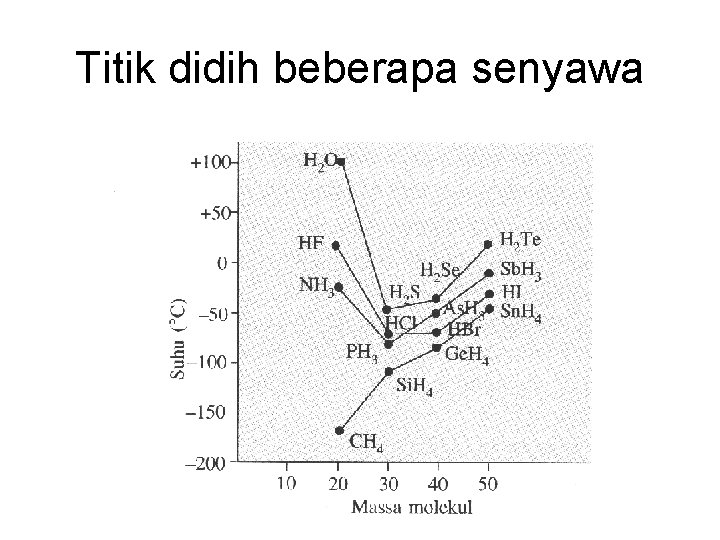
Titik didih beberapa senyawa
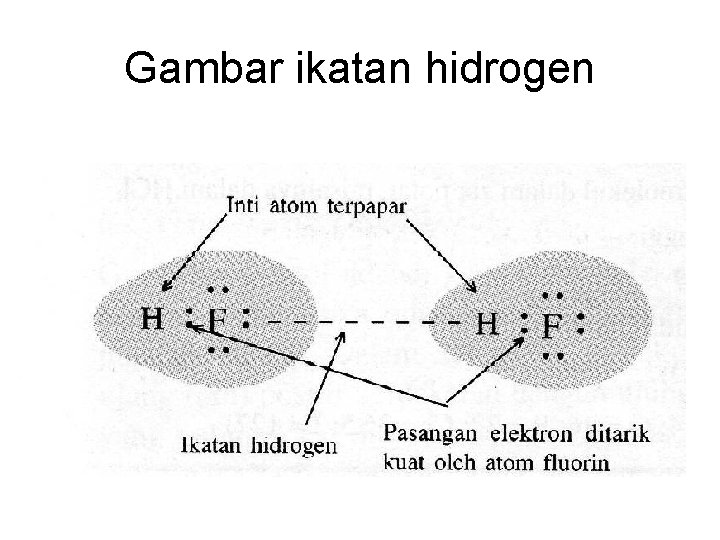
Gambar ikatan hidrogen

Jaringan ikatan Kovalen (covalent network) • Ikatan antar partikel yang sangat kuat • Zat yang memiliki covalent network mempunyai titik didih dan titik leleh yang sangat tinggi • Contoh : Intan t. l. = 3. 550 o. C, t. d. = 4. 827 o. C; Grafit t. l. = 3. 652 - 3. 697 o. C, t. d. = 4. 200 o. C; Silika (Si. O 2) t. l. = 1. 410 o. C; t. d. = 2. 355 o. C
- Slides: 29