Struktur Molekul Bentuk molekul Molekul Linier sudut ikatan
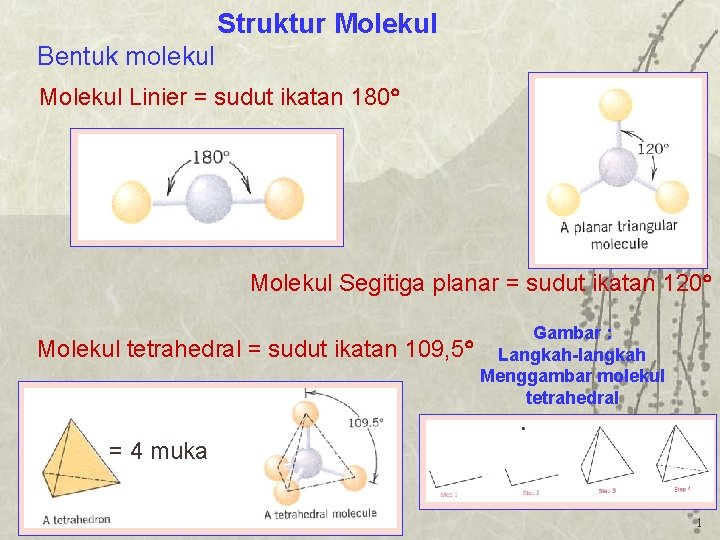
Struktur Molekul Bentuk molekul Molekul Linier = sudut ikatan 180 Molekul Segitiga planar = sudut ikatan 120 Molekul tetrahedral = sudut ikatan Gambar : 109, 5 Langkah-langkah Menggambar molekul tetrahedral = 4 muka 1
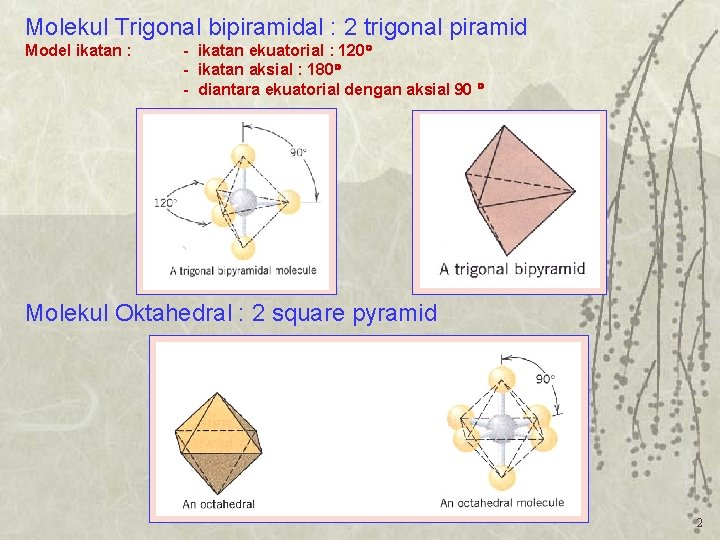
Molekul Trigonal bipiramidal : 2 trigonal piramid Model ikatan : - ikatan ekuatorial : 120 - ikatan aksial : 180 - diantara ekuatorial dengan aksial 90 Molekul Oktahedral : 2 square pyramid 2
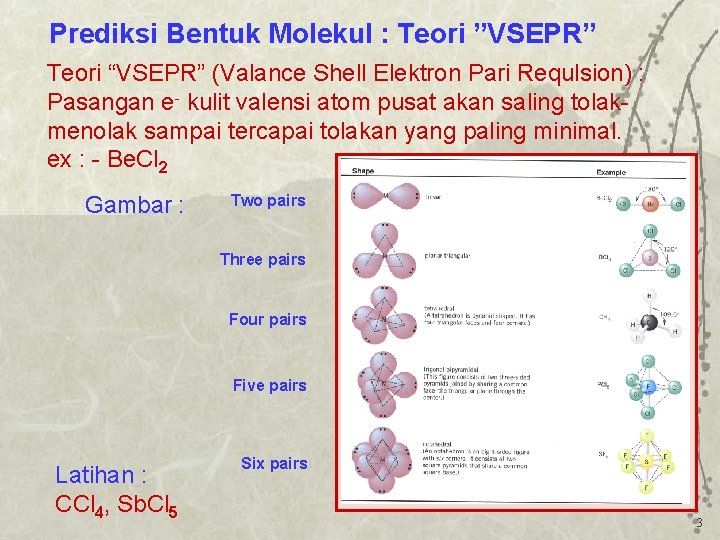
Prediksi Bentuk Molekul : Teori ”VSEPR” Teori “VSEPR” (Valance Shell Elektron Pari Requlsion) : Pasangan e- kulit valensi atom pusat akan saling tolakmenolak sampai tercapai tolakan yang paling minimal. ex : - Be. Cl 2 Gambar : Two pairs Three pairs Four pairs Five pairs Latihan : CCl 4, Sb. Cl 5 Six pairs 3
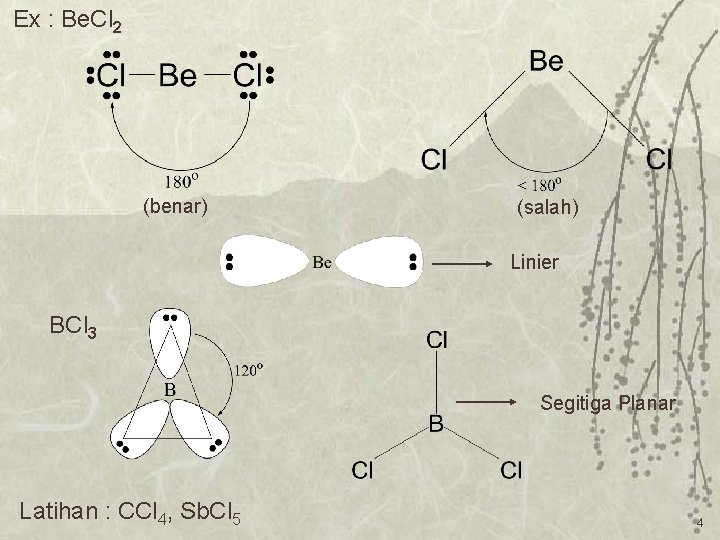
Ex : Be. Cl 2 (benar) (salah) Linier BCl 3 Segitiga Planar Latihan : CCl 4, Sb. Cl 5 4
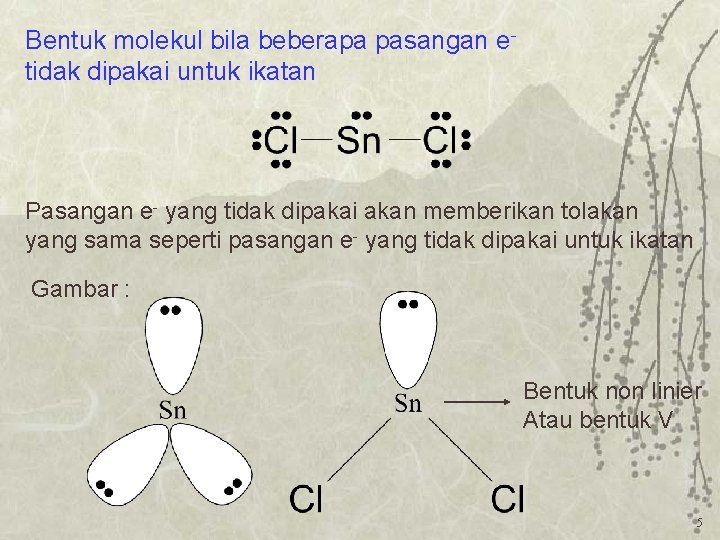
Bentuk molekul bila beberapa pasangan etidak dipakai untuk ikatan Pasangan e- yang tidak dipakai akan memberikan tolakan yang sama seperti pasangan e- yang tidak dipakai untuk ikatan Gambar : Bentuk non linier Atau bentuk V 5
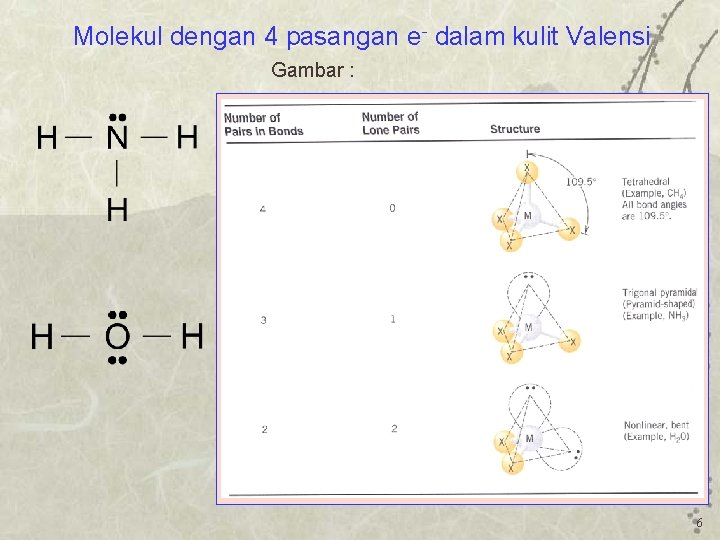
Molekul dengan 4 pasangan e- dalam kulit Valensi Gambar : 6
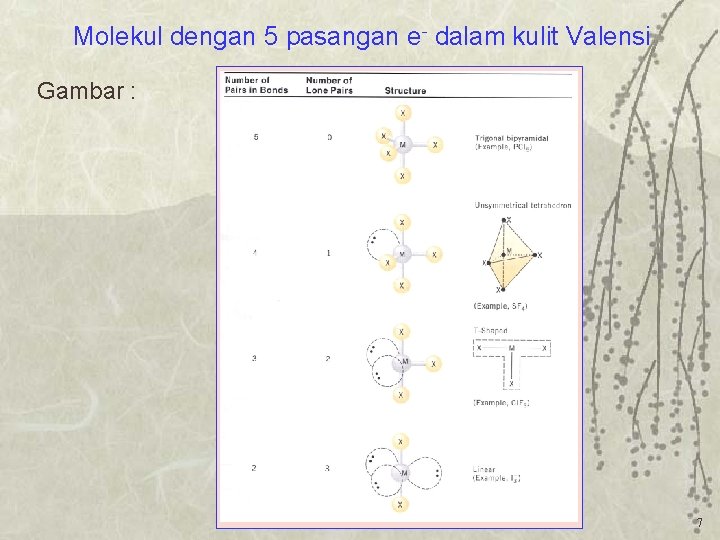
Molekul dengan 5 pasangan e- dalam kulit Valensi Gambar : 7

Molekul dengan 6 pasangan e- dalam kulit Valensi Gambar : Latihan : Cl. O 2 -, Xe. F 2, Xe. OF 4 8
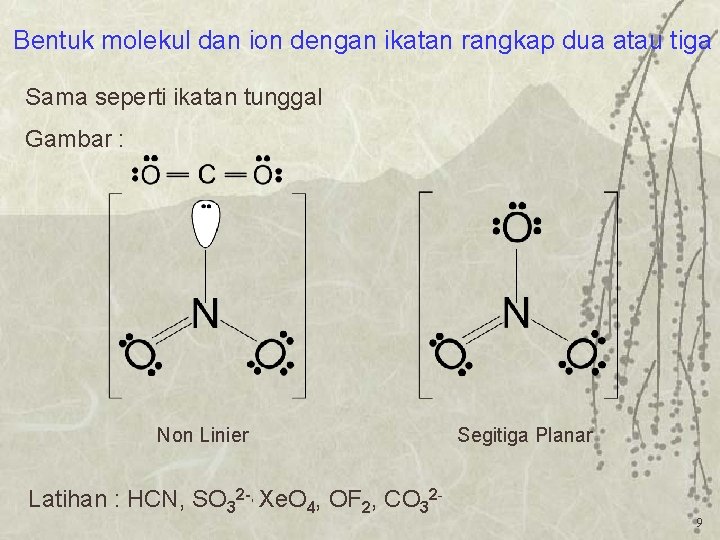
Bentuk molekul dan ion dengan ikatan rangkap dua atau tiga Sama seperti ikatan tunggal Gambar : Non Linier Segitiga Planar Latihan : HCN, SO 32 -, Xe. O 4, OF 2, CO 329
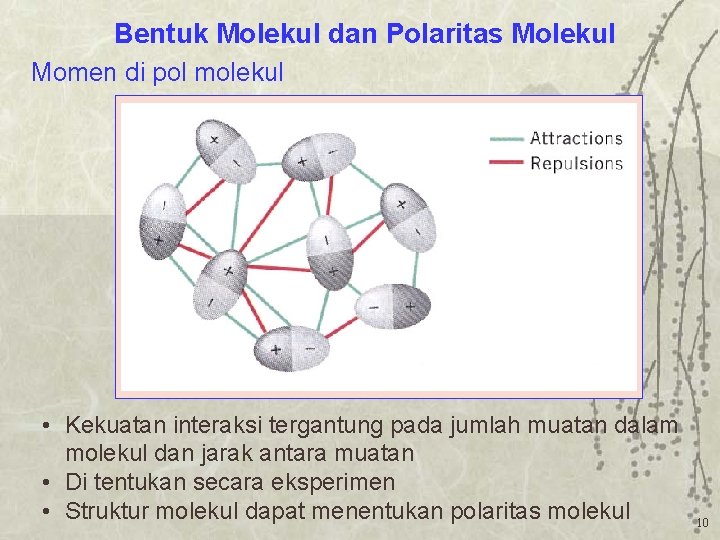
Bentuk Molekul dan Polaritas Molekul Momen di pol molekul • Kekuatan interaksi tergantung pada jumlah muatan dalam molekul dan jarak antara muatan • Di tentukan secara eksperimen • Struktur molekul dapat menentukan polaritas molekul 10
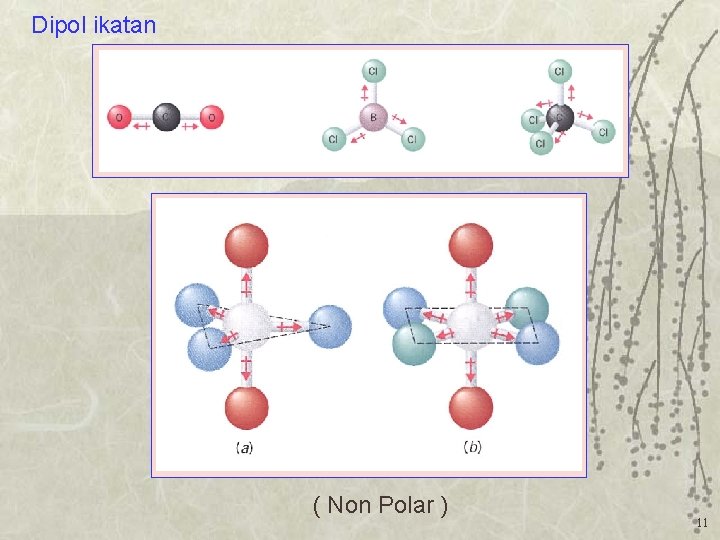
Dipol ikatan ( Non Polar ) 11
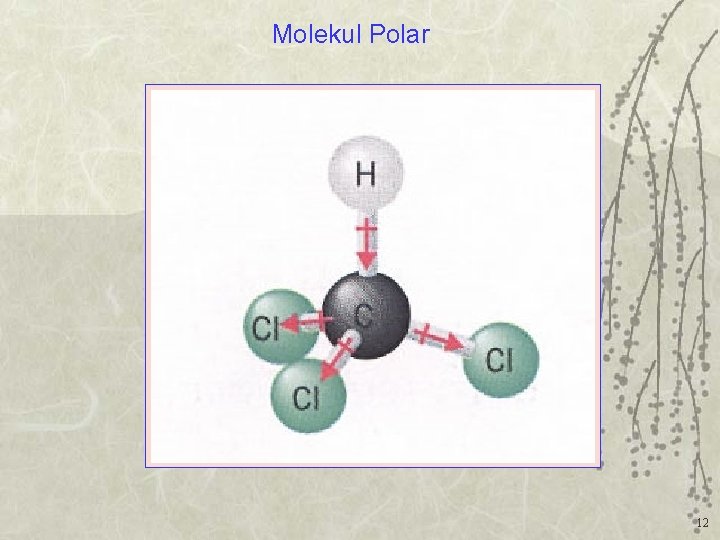
Molekul Polar 12
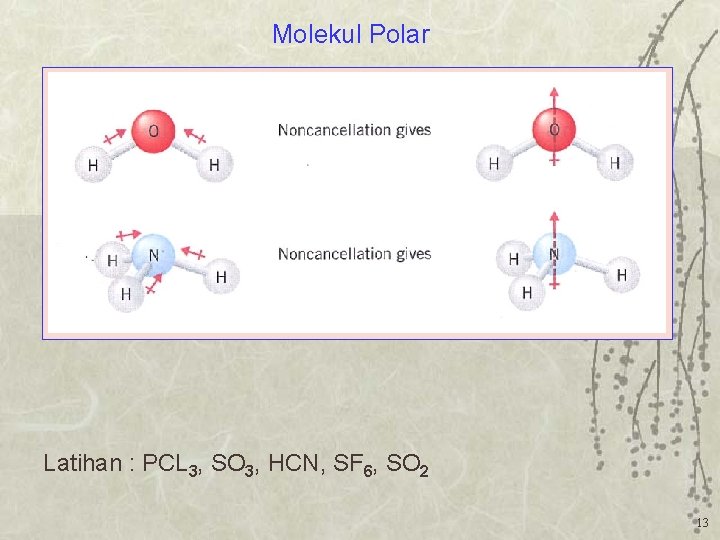
Molekul Polar Latihan : PCL 3, SO 3, HCN, SF 6, SO 2 13

Mekanika Gelombang dan Ikatan Kovalen : Teori Ikatan Valensi • Bagaimana atom-atom berpatungan elektron antara kulit-kulit valensi mekanika kuantum untuk mempelajari bagaimana orbital-orbital atom berinteraksi satu sama lain • Teori modern ikatan berdasarkan fungsi-fungsi mekanika gelombang • Teori ikatan modern : 1. Teori ikatan valensi 2. Teori orbital molekul 14
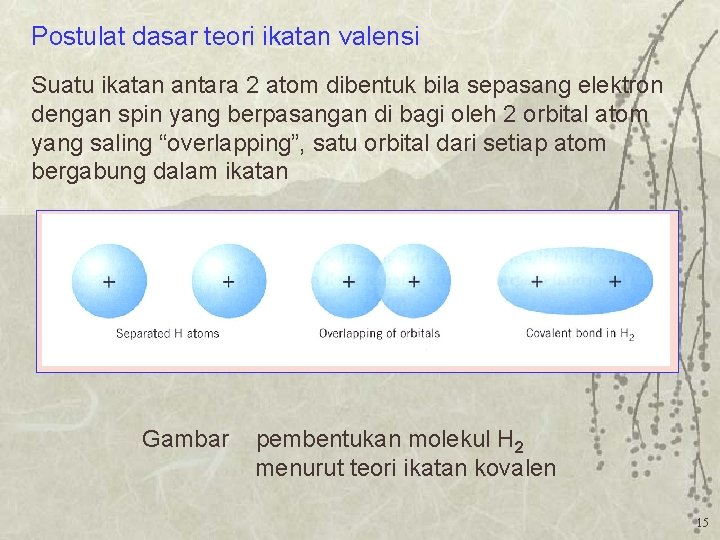
Postulat dasar teori ikatan valensi Suatu ikatan antara 2 atom dibentuk bila sepasang elektron dengan spin yang berpasangan di bagi oleh 2 orbital atom yang saling “overlapping”, satu orbital dari setiap atom bergabung dalam ikatan Gambar pembentukan molekul H 2 menurut teori ikatan kovalen 15
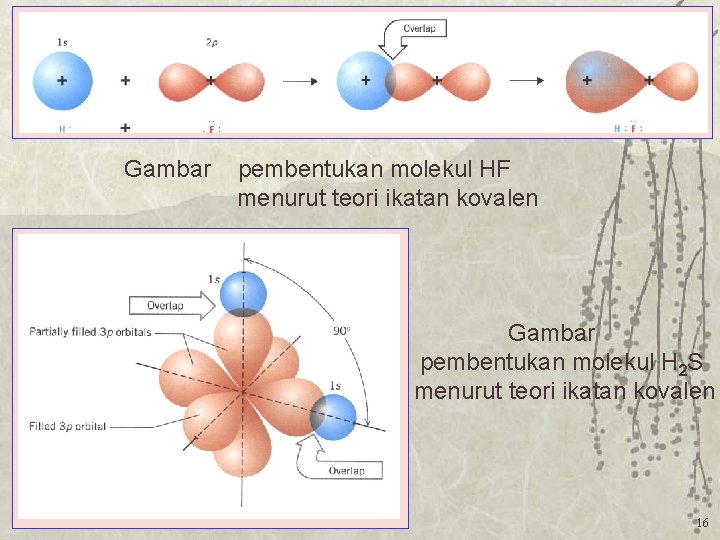
Gambar pembentukan molekul HF menurut teori ikatan kovalen Gambar pembentukan molekul H 2 S menurut teori ikatan kovalen 16
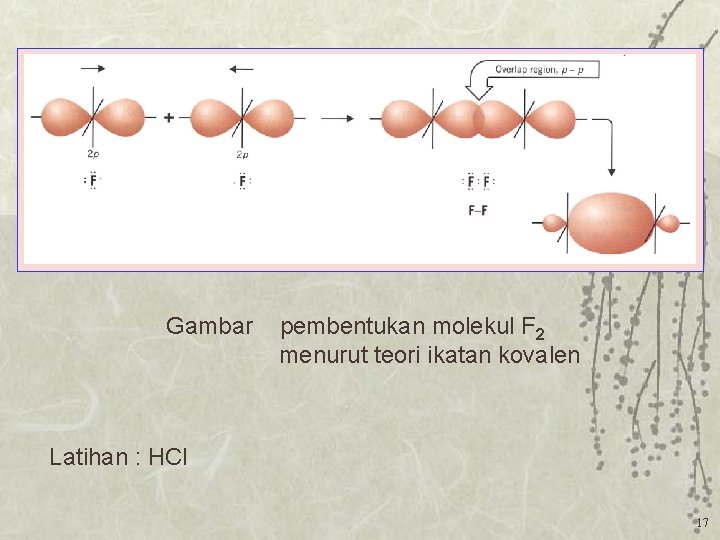
Gambar pembentukan molekul F 2 menurut teori ikatan kovalen Latihan : HCl 17
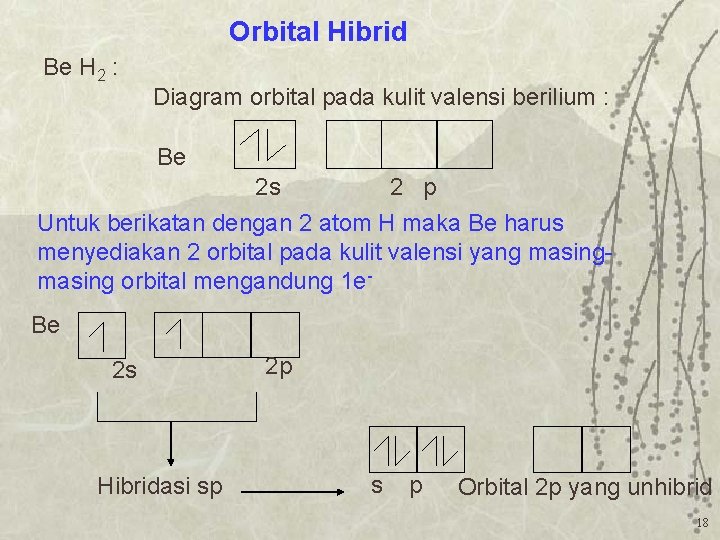
Orbital Hibrid Be H 2 : Diagram orbital pada kulit valensi berilium : Be 2 s 2 p Untuk berikatan dengan 2 atom H maka Be harus menyediakan 2 orbital pada kulit valensi yang masing orbital mengandung 1 e. Be 2 s Hibridasi sp 2 p s p Orbital 2 p yang unhibrid 18
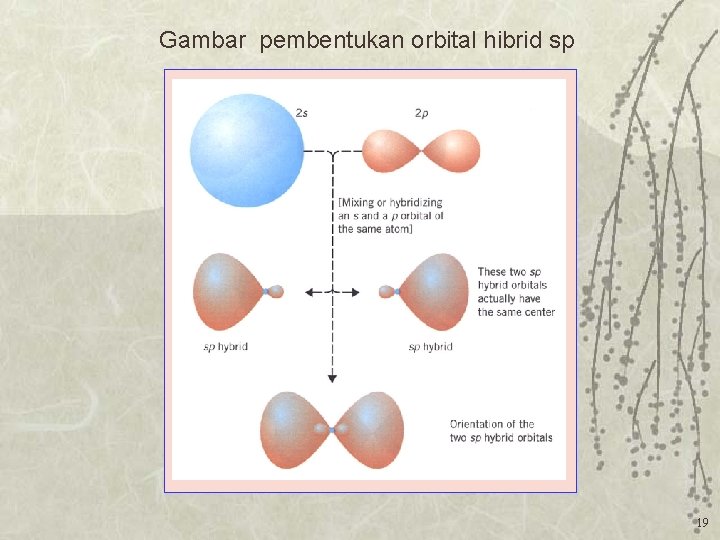
Gambar pembentukan orbital hibrid sp 19
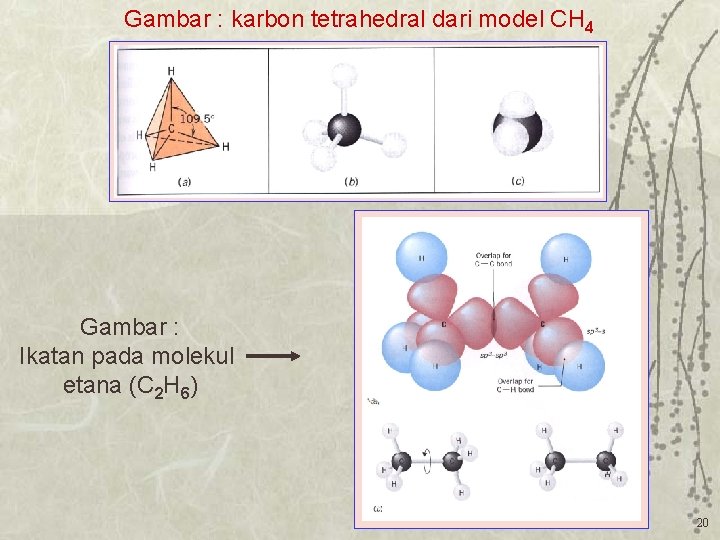
Gambar : karbon tetrahedral dari model CH 4 Gambar : Ikatan pada molekul etana (C 2 H 6) 20
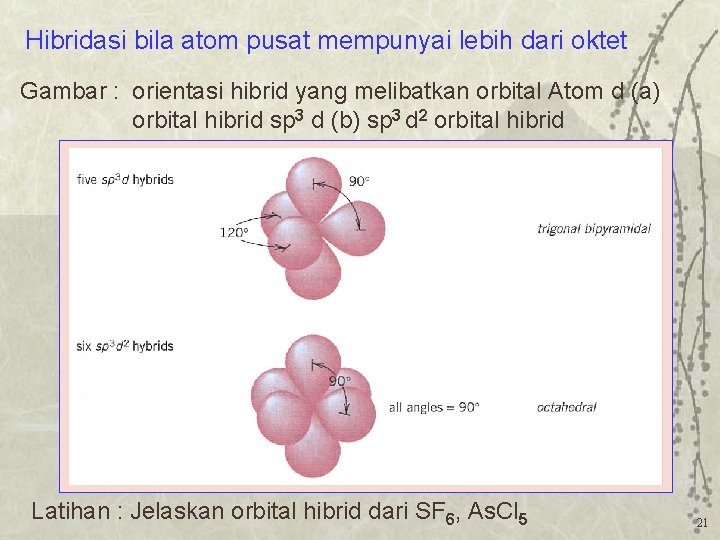
Hibridasi bila atom pusat mempunyai lebih dari oktet Gambar : orientasi hibrid yang melibatkan orbital Atom d (a) orbital hibrid sp 3 d (b) sp 3 d 2 orbital hibrid Latihan : Jelaskan orbital hibrid dari SF 6, As. Cl 5 21

Penggunaan teori VSEPR untuk memprediksi Hibridasi CH 4 tetrahedral hibridasi sp 3 SF 6 oktahedral hibridasi sp 3 d 2 Latihan : Si. H 4, PCl 5 Hibridasi dalam molekul yang mempunyai pasangan elektron bebas CH 4 adalah molekul tetrahedral hibridasi sp 3 orbital karbon Sudut ikatan H - C - H = 109, 5 NH 3, sudut ikatan H - N - H = 107 H 2 O, sudut ikatan H - O - H = 104, 5 Sudut ikatan H – X – H mendekati sudut untuk molekul yang atom pusat mempunyai hibrid sp 3 22
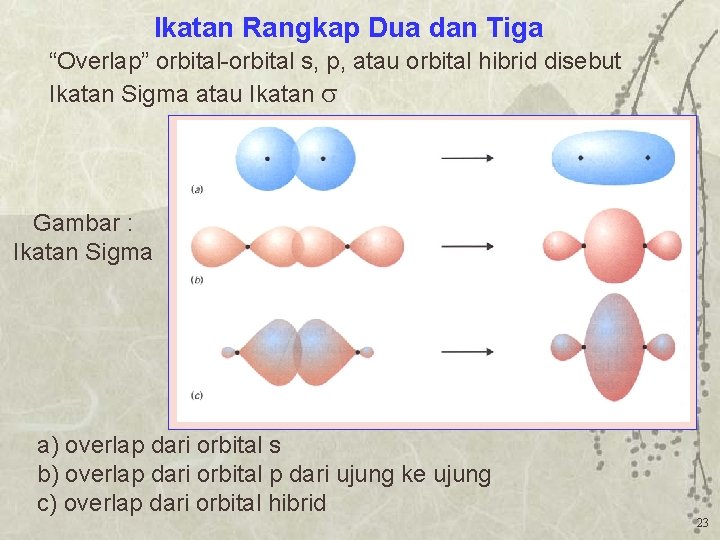
Ikatan Rangkap Dua dan Tiga “Overlap” orbital-orbital s, p, atau orbital hibrid disebut Ikatan Sigma atau Ikatan Gambar : Ikatan Sigma a) overlap dari orbital s b) overlap dari orbital p dari ujung ke ujung c) overlap dari orbital hibrid 23
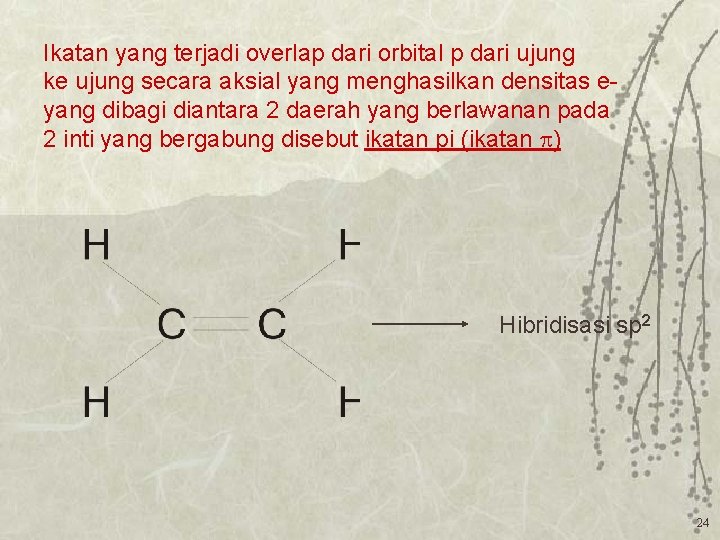
Ikatan yang terjadi overlap dari orbital p dari ujung ke ujung secara aksial yang menghasilkan densitas eyang dibagi diantara 2 daerah yang berlawanan pada 2 inti yang bergabung disebut ikatan pi (ikatan ) Hibridisasi sp 2 24
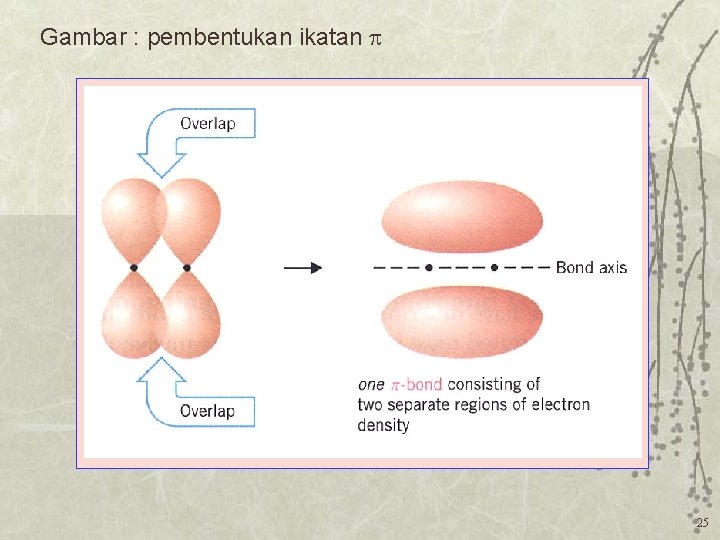
Gambar : pembentukan ikatan 25

Teori Orbital Molekul Memandang bahwa suatu molekul mirip dengan atom dalam Satu respek yang penting level energi tergantung kepada Variasi orbital yang dipopulasikan oleh e-. Atom orbital atom Molekul orbital molekul Orbital molekul yang dibentuk = orbital atom-atom yang Berkombinasi Molekul terdiri dari susunan inti atom tertentu, dan di sekitar Inti tersebut tersebar satu set orbital molekul. 26
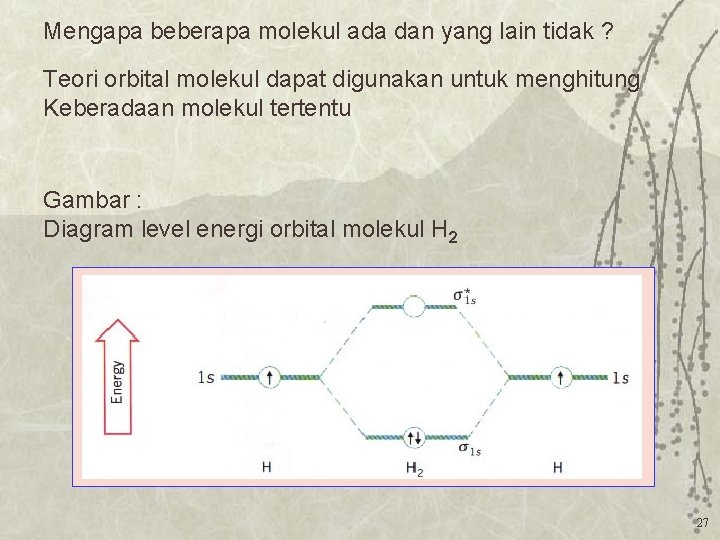
Mengapa beberapa molekul ada dan yang lain tidak ? Teori orbital molekul dapat digunakan untuk menghitung Keberadaan molekul tertentu Gambar : Diagram level energi orbital molekul H 2 27
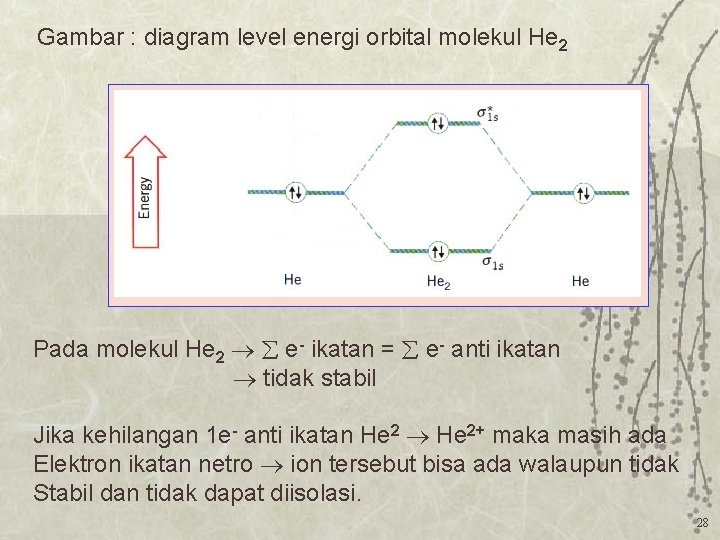
Gambar : diagram level energi orbital molekul He 2 Pada molekul He 2 e- ikatan = e- anti ikatan tidak stabil Jika kehilangan 1 e- anti ikatan He 2+ maka masih ada Elektron ikatan netro ion tersebut bisa ada walaupun tidak Stabil dan tidak dapat diisolasi. 28
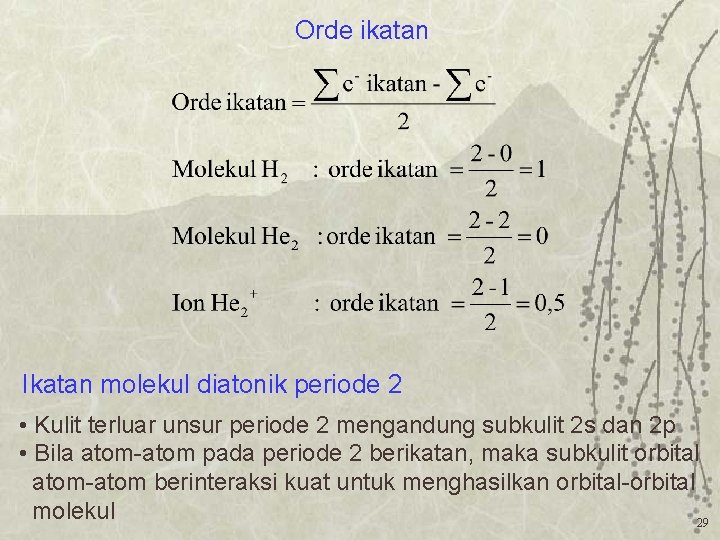
Orde ikatan Ikatan molekul diatonik periode 2 • Kulit terluar unsur periode 2 mengandung subkulit 2 s dan 2 p • Bila atom-atom pada periode 2 berikatan, maka subkulit orbital atom-atom berinteraksi kuat untuk menghasilkan orbital-orbital molekul 29

Konfigurasi e- orbital molekul diperoleh dengan aturan yang sama seperti pengisian orbital atom dalam atom 1. Pengisian e- dimulai dari orbital energi terendah 2. Dalam setiap orbital, diisi maksimal 2 e- dengan spin berlawanan 3. Penyebaran e- dengan spin tidak berpasangan di atas orbital yang mempunyai energi yang sama 30

Teori orbital molekul memprediksikan molekul Be 2 dan Ne 2 tidak ada lain orde ikatan = 0 Orde ikatan meningkat dari B C N dan berkurang dari N O F Teori orbital molekul dapat menjelaskan struktur e- molekul O 2 - Dari eksperimen O 2 : paramagnetik ( terikat lemah dengan magnet ) - Mempunyai 2 e- yang tidak berpasangan - panjang ikatan O 2 ikatan O - O dengan teori e- valensi hal tersebut telah dapat dijelaskan ex : struktur lewis : (tidak diterima berdasarkan eksperimen karena semua elektron berpasangan) (tidak diterima berdasarkan eksperimen karena ikatan tunggal O – O) 31
- Slides: 31