STOIKIOMETRI DISUSUN OLEH NUR DEWI S BASAREWAN 1701031

STOIKIOMETRI DISUSUN OLEH : NUR DEWI S. BASAREWAN (1701031) FITRI ISDRIS (1701096) CINDY Z. M. MAMALA (1701137)

STOIKIOMETRI � Stoikiometri adalah cabang kimia yang berhubungan dengan hubungan kuantitatif yang ada antara reaktan dan produk dalam reaksi kimia. Reaktan adalah zat yang berpartisipasi dalam reaksi kimia, dan produk adalah zat yang diperoleh sebagai hasil dari reaksi kimia. Stoikiometri bergantung pada kenyataan bahwa unsur-unsur berperilaku dengan cara yang dapat diprediksi, dan materi yang tidak dapat diciptakan atau dihancurkan

Karena itu, ketika unsur digabungkan menghasilkan reaksi kimia, sesuatu yang dikenal dan spesifik yang akan terjadi dan hasil reaksi dapat diprediksi berdasarkan unsur-unsur dan jumlah yang terlibat. � Stoikiometri adalah matematika di balik ilmu kimia. Perhitungan stoikiometri dapat menemukan bagaimana unsur-unsur dan komponen yang diencerkan dalam larutan yang konsentrasinya diketahui, bereaksi dalam kondisi eksperimental. Kata “Stoikiometri” berasal dari kata stoicheion Yunani, yang berarti “unsur” dan metron yang berarti “ukuran”. �

MASSA ATOM, JUMLAH PARTIKEL, MOL.

MASSA ATOM RELATIF Massa Atom relatif adalah perbandingan relatif massa atom unsur tertentu terhadap massa atom unsur lainnya. Satuan Massa Atom disingkat sma. 1 sma = x massa atom C-12 � Contoh massa atom relatif: Jika massa atom Karbon (C) adalah 12, 01115 » 12 maka perhitungan massa atom relatif dilakukan dengan cara sebagai berikut : Karena massa atom C 12 sama dengan 1 sma, maka yang berarti : Ar X = massa rata-rata 1 atom unsur X » Ar X = pembulatan massa rata-rata 1 atom unsur X. �

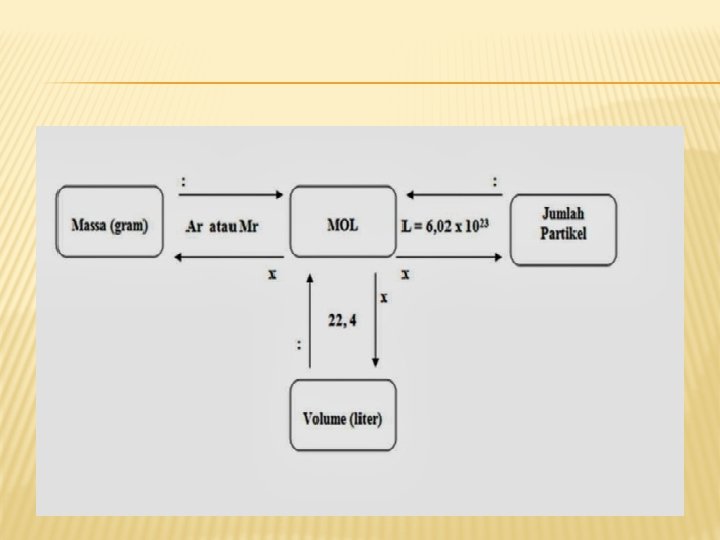
KONSEP MOL � � Mol (1896 - Wilhelm Ostwald) adalah jumlah zat yang mengandung partikel zat itu sebanyak atom/molekul/ion yang terdapat dalam 12 gram C-12 1 mol = 6, 02 x 1023. Bilangan 6, 02 x 1023 ini disebut tetapan avogadro dan dinyatakan dengan lambang L. Mol = g = JP = V(liter) x M Ar atau Mr L = 1 mol Ket : JP = Jumlah Partikel L = Bilangan Avogadro = 6, 02 x 1023 �

Contoh : � Tentukan jumlah mol dari : � 12 gram kalsium (Ar Ca = 40) � 3, 01 x 10²³ atom Cu � 100 m. L H 2 SO 4 0, 1 M Jawab : � Mol Ca = 12/40 = 0, 3 mol � Mol Cu = 3, 01 x 10²³/6, 02 x 10²³ = 0, 5 mol � Mol H 2 SO 4 = 1000/100 x 0, 1 = 1 mo

Hubungan Jumlah Mol dengan Jumlah Partikel JP = n x 6, 02 x 1023 Dimana : JP = jumlah partikel n = jumlah mol Contoh : 1. Tentukan jumlah partikel (ion/ atom/molekul) yang terdapat dalam : a. 1 mol Ca b. 2 mol H 2 Jawab : Gunakan rumus : JP = n x 6, 02 x 1023 a. JP = 1 mol x 6, 02 x 1023 atom/mol = 6, 02 x 1023 atom b. JP = 2 mol x 6, 02 x 1023 molekul/mol = 12, 05 x 1023 molekul

2. Tentukan Jumlah mol dari : a. 3, 01 x 1022 atom besi b. 1, 204 x 1023 molekul air Jawab : Rumus JP = n x 6, 02 x 1023

Hubungan Jumlah Mol dengan Massa Molar ( Ar / Mr ) dan Massa � 1. Massa Atom Relatif (Ar) � Perbandingan massa satu atom dengan massa atom standar disebut massa atom relatif (Ar). Karena atom sangat ringan, maka tidak dapat digunakan satuan g dan kg untuk massa atom, maka digunakan satuan massa atom (s. m. a). 1 s. m. a = 1, 66 x 10 -24 g


Hubungan jumlah mol, massa dan massa molar m = n x mm , dimana : m = massa; n =jumlah mol; dan mm = Ar atau Mr Contoh : 1. Hitunglah massa dari : a. 2 mol atom magnesium b. 2 molekul magnesium hidroksida (Mg(OH)2) (Ar H=1; Ar O=16; Ar Mg =24) Jawab : a. m = n x Ar = 2 x Ar Mg = 2 x 24 = 48 gram b. m = n x Mr = 2 x Mr Mg(OH)2 = 2 x (Ar Mg + 2. Ar H + 2. Ar O) = 2 x (24+2. 16)= 2 x 58 = 116 gram


PERSEN MASSA Persen Massa adalah massa zat terlarut dibagi dengan massa dari larutan (massa zat terlarut ditambah massa pelarut ), dikalikan dengan 100. Contoh : Sebuah bongkah gula berbentuk kubus 4 g (Sukrosa: C 12 H 22 O 11 ) dilarutkan dalam gelas 350 ml air dengan temperatur 80°C. Bagaimana komposisi persen massa dari larutan gula tersebut? Diketahaui: Kepadatan air pada 80°C = 0, 975 g/ml

� Langkah 1 – Tentukan massa zat terlarut, massa zat terlarut adalah 4 g C 12 H 22 O 11 � Langkah 2 – Tentukan massa pelarut density = massa / volume massa = densitas x volume massa = 0, 975 g/ml x 350 ml massa = 341, 25 g

� Langkah 3 – Tentukan massa total solusi m larutan = m zat terlarut + m pelarut m larutan = 4 g + 341, 25 g m larutan = 345, 25 g � Langkah 4 – Tentukan komposisi persen oleh massa larutan gula. persen komposisi = (m terlarut / m larutan ) x 100 persen komposisi = (4 g / 345, 25 g) x 100 persen komposisi = (0. 0116) x 100 Komposisi persen = 1, 16%

RUMUS EMPIRIS DAN RUMUS MOLEKUL � Rumus Empiris Rumus empiris adalah rumus yang menyatakan perbandingan terkecil atom-atom dari unsur yang menyusun suatu senyawa. Rumus kimia senyawa ion merupakan rumus empiris. � Rumus Molekul Rumus molekul adalah rumus yang menyatakan jumlah atom-atom dari unsur-unsur yang menyusun satu molekul senyawa. Jadi rumus molekul menyatakan susunan sebenarnya dari molekul zat.

� Contoh : Suatu senyawa hidrokarbon mengandung 24 gram C dan 8 gram H. Tentukan rumus molekul senyawa tersebut jika diketahui massa molekul relatifnya 32.

Perbandingan massa C : H = 24 : 8 � Perbandingan mol: n. C : n. H = m. C : m. H Ar. C Ar. H = 24 : 8 12 4 = 1 : 4 � Jadi, rumus empiris senyawa tersebut adalah CH 4.

� Rumus molekul dapat ditentukan dengan rumus (RE)n = Mr. (CH 4)n = 32 16 n = 32 n = 2 Jadi rumus molekul senyawa tersebut adalah (CH 4)2 = C 2 H 8.

APLIKASI STOIKIOMETRI

STOIKIOMETRI REAKSI � Stoikiometri Reaksi merupakan bidang kajian ilmu kimia, yang mempelajari hubungan kuantitatif zat-zat kimia yang terlibat dalam reaksi kimia. Contoh : 2 H 2 + O 2 2 H 2 O Persamaan kimia ini mengandung makna : 2 molekul H 2 + 1 molekul O 2 2 molekul H 2 O Atau 2 n molekul H 2 + n molekul O 2 2 n molekul H 2 O Dengan demikian dapat disimpulkan bahwa koefisien reaksi pada pe persamaan kimia menunjukkan Perbandingan jumlah mol zat-zat yang bereaksi dan zat hasil reaksi.

STOIKIOMETRI LARUTAN � Pada stoikiometri larutan diantara zat – zat yang terlibat reaksi sebagian atau seluruhnya berada dalam bentuk larutan. Soal – soal yang menyangkut bagian ini dapat diselesaikan dengan cara hitungan kimia sederhana yang menyangkut kuantitas antara suatu komponen dengan komponen lain dalam suatu reaksi. Jika larutan asam dicampurkan dengan larutan basa akan terjadi reaksi, yaitu : reaksi pengikatan ion H+ dari asam oleh OH- dari basa menghasilkan air (H 2 O), reaksi ini disebut reaksi netralisasi. Contoh : Asam + Basa garam + air HCL + Na. OH Na. Cl + H 2 O 2.

STOIKIOMETRI GAS � Perilaku gas mudah dikarakterisasi karena hampir semua sifat-sifat gas tidak bergantung pada jati diri gas. Terdapat beberapa hukum dasar yang dapat menerapkan perilaku gas berdasarkan eksperimen laboratorium, diantaranya adalah hokum Boyle Hukum Gay Lussac. Hukum Boyle berkenaan dengan hubungan antara volume gas dan tekanan gas pada suhu tetap. Hukum Boyle berbunyi: Tekanan gas berbanding terbalik dengan volumenya asalkan suhunya tetap dalam bentuk persamaan, Hukum Boyle dapat dirumuskan dengan: p. V = konstan, atau p 1 V 1 = p 2 V 2 Dimana, p = tekanan V = volume gas.

DAFTAR PUSTAKA � � � � http: //usaha 321. net/pengertian-stoikiometri-dan-jenis-stoikiometri. html http: //smpsma. com/sebutkan-pengertian-massa-atom-relatif-ar-dancontohnya. html http: //sumbermaterikimia. blogspot. co. id/2014/03/sem-2 -konsepmol_9. html http: //ladinaatqadar. blogspot. co. id/2016/06/mol-pengertian-danperhitungan-konsep. html https: //urip. wordpress. com/2011/05/14/persen-massa-satuankonsentrasi/ http: //www. nafiun. com/2013/03/rumus-kimia-rumus-molekul-dan-empiris -contoh-perbedaan-persamaan. html https: //www. slideshare. net/165264/aplikasi-stoikiometri-54198669 http: //www. kimiamath. com/cara-menentukan-rumus-empiris-dan-rumusmolekul-senyawa/

TERIMA KASIH
- Slides: 28