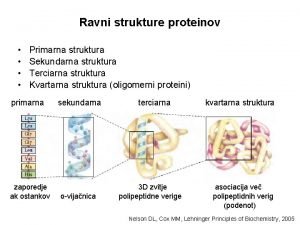
Funkcije proteinov Transportskladienje doloenih molekul ligandov npr Hb

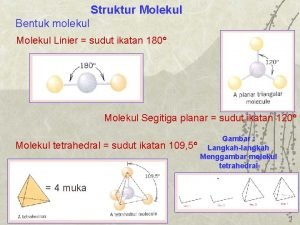
Funkcije proteinov • Transport/skladiščenje določenih molekul (ligandov, npr. Hb, Mb) • Uravnavanje procesov (DNA-vezavni proteini) • Oporna funkcija (strukturni proteini, npr keratini, kolagen. . . ) • Kontraktilni proteini • Membranski proteini, vključeni v transport molekul/ionov preko membrane • Proteini, vključeni v prenos signala (receptorji, G-proteini, kinaze. . . ) • Obramba pred tujki/invazivnimi organizmi (Ig) • Kataliza biokemijskih reakcij (encimi)

Vezava ligandov na protein • Molekula – ligand se reverzibilno veže na protein • Ligand se veže na vezavno mesto proteina, ki je komplementarno glede velikosti in oblike liganda, naboja, hidrofobnih in hidrofilnih interakcij • Vezavno mesto je selektivno, torej specifično za določen ligand • Vezava liganda povzroči konformacijsko spremembo proteina, ki vodi k močnejši vezavi; strukturna adaptacija med proteinom in ligandom – inducirano prilagajanje • Pri multimernih proteinih povzroči vezava liganda na eno podenoto konformacijsko spremembo drugih podenot • Interakcije med proteini in ligandi so uravnavane s specifičnimi interakcijami drugih ligandov. Ti drugi ligandi povzročijo konformacijsko spremembo proteina, ki vpliva na vezavo prvega liganda.

Vezava liganda na protein: proteini, ki vežejo kisik mioglobin (Mb) in hemoglobin (Hb) • • • Prostetična skupina hem Mioglobin – eno vezavno mesto za kisik Kvantitativni opis interakcije protein-ligand Transport kisika s hemoglobinom Struktura Hb Strukturne spremembe Hb po vezavi kisika Kooperativna vezava kisika na Hb Alosterični proteini – kvantitativni opis vezave Hb prenaša tudi H+ in CO 2 Uravnavanje vezave kisika na Hb z 2, 3 -bisfosfogliceratom Anemija srpastih celic

Topnost nekaterih plinov v vodi Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005 • Večje živali – potreba po sistemu, ki prenaša in shranjuje kisik • Za vezavo kisika primerni elementi prehoda – Fe veže kisik in ga s tem naredi manj reaktivnega • Fe – bistven del prostetične skupine (hem) proteinov, ki vežejo kisik (Mb. Hb)
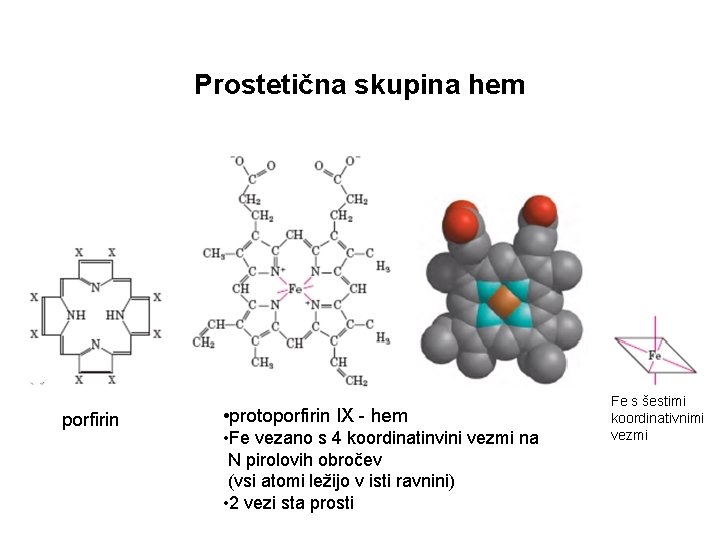
Prostetična skupina hem porfirin • protoporfirin IX - hem • Fe vezano s 4 koordinatinvini vezmi na N pirolovih obročev (vsi atomi ležijo v isti ravnini) • 2 vezi sta prosti Fe s šestimi koordinativnimi vezmi

Struktura mioglobina (Mb) • 3 D struktura – globinsko zvitje (“fold”) • kompaktna molekula, v notranjosti le 4 molekule H 2 O • 8 segmentov (A-H) -vijačnic (7 -23 ak) • 75% strukture: α-vijačnica • hidrofobni –R v notranjosti, hidrofilni –R proti vodnemu okolju • nehelični segmenti označeni AB, CD. . . • Pro na mestih β-zavojev • prostetična skupina hem vezan v žep med E in F vijačnicama • Mb se nahaja v mišičnih celicah, rdeče/rjave barve • Mr = 16 700, 1 polipeptidna veriga, 153 ak • 3 D strukturo ugotovil l. 1950, John Kendrew s sod. z uklonom Rtg. žarkov

Umestitev hema v protein (globin) Pogled s strani Ravnina, v kateri leži porfirin His • Fe vezano s 4 vezmi v hemu, • z eno vezjo na His ostanek proteina, • prostane ena koordinavina vez • za ligande • O 2 • NO • CO
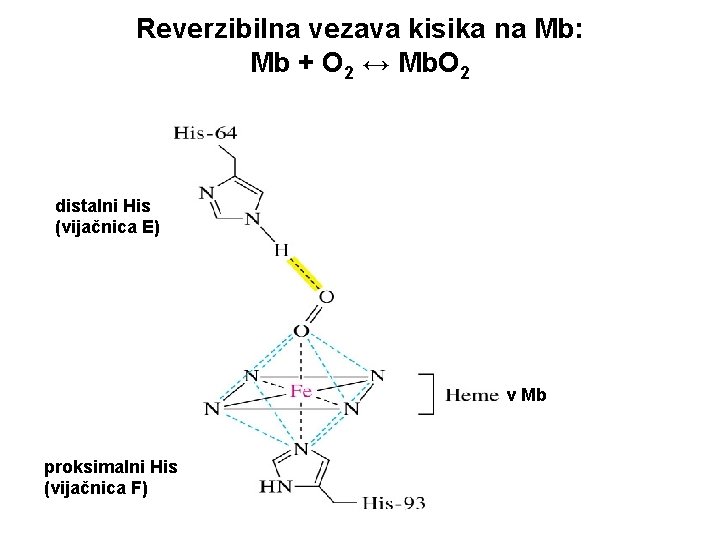
Reverzibilna vezava kisika na Mb: Mb + O 2 ↔ Mb. O 2 distalni His (vijačnica E) v Mb proksimalni His (vijačnica F)

Reverzibilna vezava liganda na protein P + L ↔ PL P – protein L – ligand PL – kompleks protein-ligand Ka – asociacijska konstanta za nastanek kompleksa PL Kd – disociacijska konstanta kompleksa PL
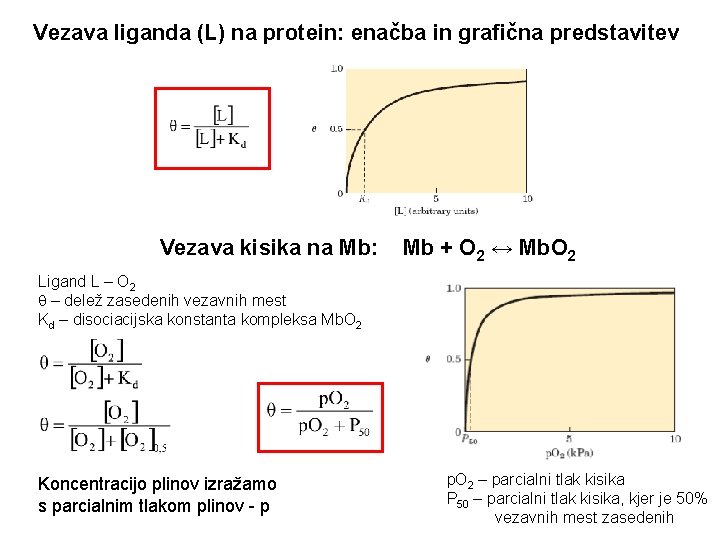
Vezava liganda (L) na protein: enačba in grafična predstavitev Vezava kisika na Mb: Mb + O 2 ↔ Mb. O 2 Ligand L – O 2 – delež zasedenih vezavnih mest Kd – disociacijska konstanta kompleksa Mb. O 2 Koncentracijo plinov izražamo s parcialnim tlakom plinov - p p. O 2 – parcialni tlak kisika P 50 – parcialni tlak kisika, kjer je 50% vezavnih mest zasedenih
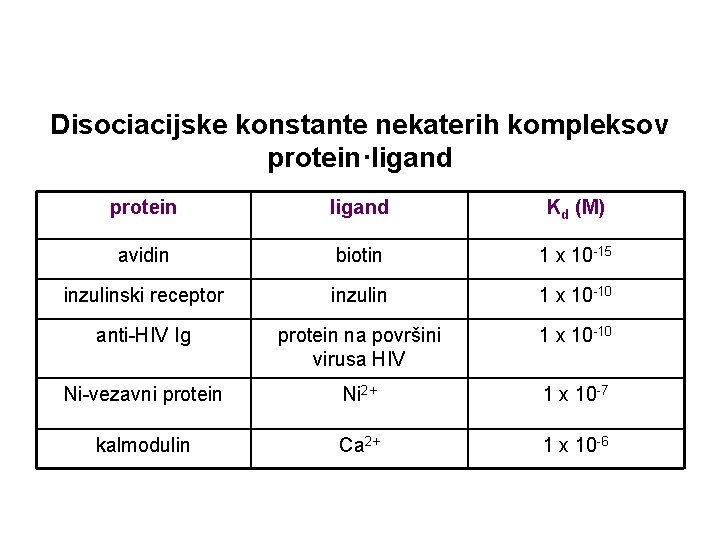
Disociacijske konstante nekaterih kompleksov protein·ligand protein ligand Kd (M) avidin biotin 1 x 10 -15 inzulinski receptor inzulin 1 x 10 -10 anti-HIV Ig protein na površini virusa HIV 1 x 10 -10 Ni-vezavni protein Ni 2+ 1 x 10 -7 kalmodulin Ca 2+ 1 x 10 -6

Sterični vplivi za vezavo liganda (O 2, CO) na hem Mb Vezava CO na hem v raztopini: CO veže z 200 000 x večjo afiniteto kot O 2 (a) Vezava kisika pod določenim kotom (b) Vezava CO pravokotno na ravnino hema Vezava CO in O 2 na hem v Mb: His v E 7 Mb prepreči vezavo CO pod pravim kotom – afiniteta Mb do CO le še 200 x večja kot do O 2 Zaradi prostorskih ovir, ki jih predstavlja His v vijačnici E 7, se O 2 veže pod določenim kotom na Fe v hemu

Mb ni primeren za prenos kisika iz pljuč v tkiva Vezava O 2 na Mb • Razmere v pljučih: PO 2 13, 3 k. Pa oz. 90 mm Hg • Razmere v tkivih: PO 2 4 k. Pa oz. ~30 mm Hg • Glede na vezavno krivuljo bi bil O 2 stalno vezan na Mb • Mb ni primeren prenašalec kisika od pljuč v tkiva • To nalogo opravlja hemoglobin (Hb)

Kisik se prenaša po krvi s hemoglobinom (Hb) • • Hb se nahaja v eritrocitih Eritrociti – nepopolne celice, namenjene prenosu O 2 V citosolu vsebujejo ~34% Hb Arterijska kri ~96% zasičena s kisikom, venska ~64% → O 2 se sprosti v tkivih, kjer se porabja za oksidacijo metaboličnih hranil (glukoza), pri čemer nastajata CO 2 in H+, ki se prenašata iz tkiv v pljuča • Hb prenese v telesu 500 g O 2/dan = 15, 6 molov O 2/dan • Eritrociti – ploščate krvne celice premera 6 -9 m • Rdeča barva izvira is hema

Vloga Hb v prenosu kisika oksigeniran Hb neoksigeniran Hb pljuča srce tkiva O 2 dobimo z dihanjem in se prenaša iz pljuč (PO 2 13, 3 k. Pa oz. 90 mm Hg) v tkiva (PO 2 4 k. Pa oz. ~30 mm Hg)
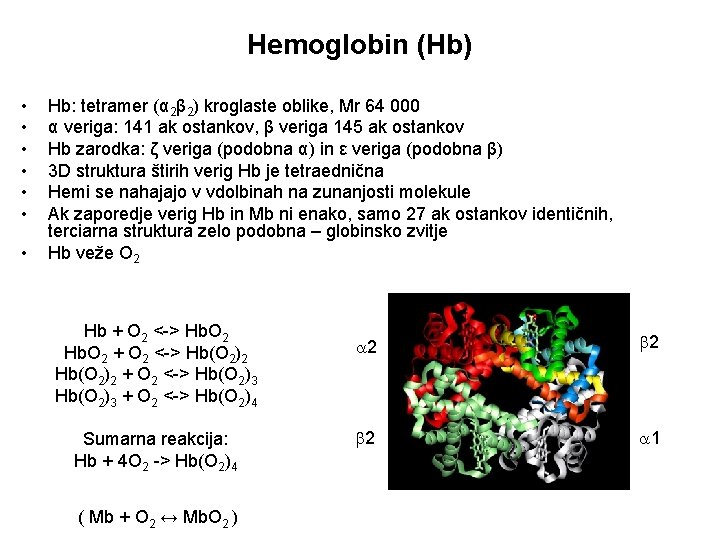
Hemoglobin (Hb) • • Hb: tetramer (α 2β 2) kroglaste oblike, Mr 64 000 α veriga: 141 ak ostankov, β veriga 145 ak ostankov Hb zarodka: ζ veriga (podobna α) in ε veriga (podobna β) 3 D struktura štirih verig Hb je tetraednična Hemi se nahajajo v vdolbinah na zunanjosti molekule Ak zaporedje verig Hb in Mb ni enako, samo 27 ak ostankov identičnih, terciarna struktura zelo podobna – globinsko zvitje Hb veže O 2 Hb + O 2 <-> Hb. O 2 + O 2 <-> Hb(O 2)2 + O 2 <-> Hb(O 2)3 + O 2 <-> Hb(O 2)4 Sumarna reakcija: Hb + 4 O 2 -> Hb(O 2)4 ( Mb + O 2 ↔ Mb. O 2 ) 2 2 2 1
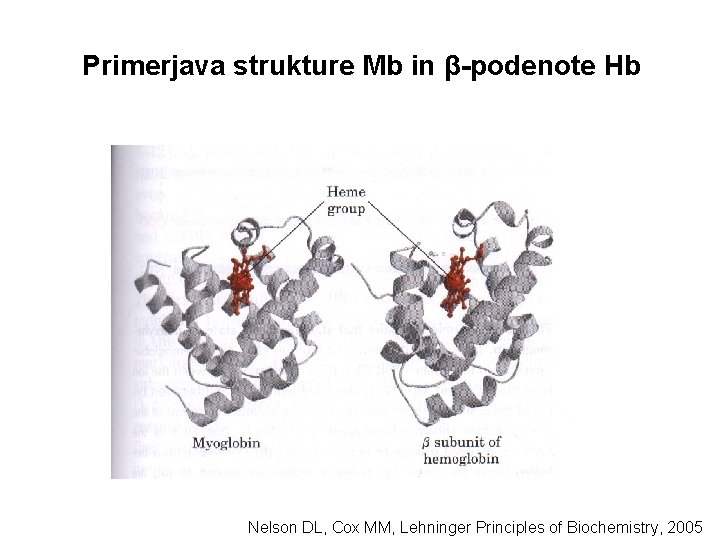
Primerjava strukture Mb in β-podenote Hb Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005
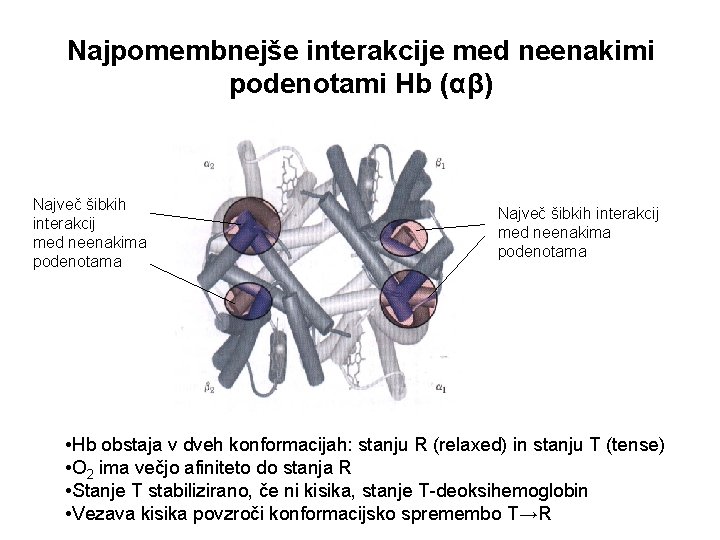
Najpomembnejše interakcije med neenakimi podenotami Hb (αβ) Največ šibkih interakcij med neenakima podenotama • Hb obstaja v dveh konformacijah: stanju R (relaxed) in stanju T (tense) • O 2 ima večjo afiniteto do stanja R • Stanje T stabilizirano, če ni kisika, stanje T-deoksihemoglobin • Vezava kisika povzroči konformacijsko spremembo T→R

Stabilizacija T konformacije Hb z ionskimi interakcijami Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005
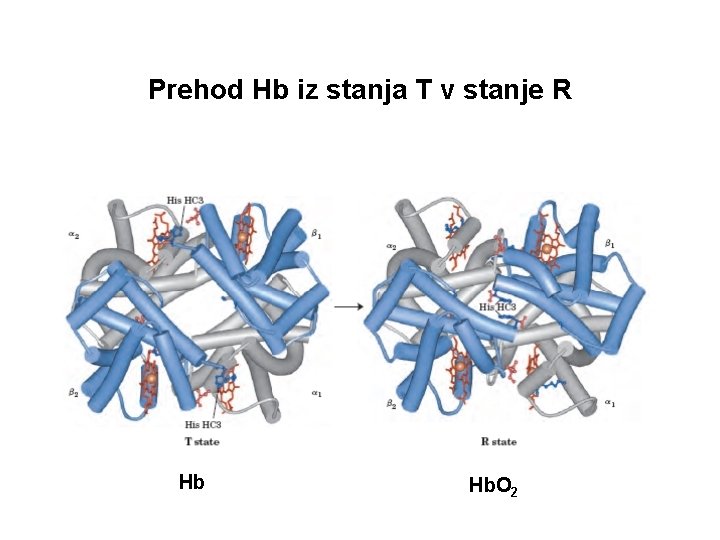
Prehod Hb iz stanja T v stanje R Hb Hb. O 2
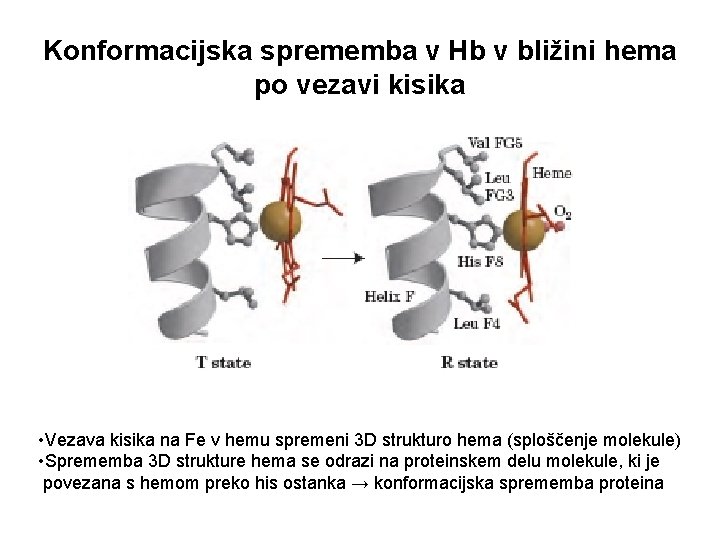
Konformacijska sprememba v Hb v bližini hema po vezavi kisika • Vezava kisika na Fe v hemu spremeni 3 D strukturo hema (sploščenje molekule) • Sprememba 3 D strukture hema se odrazi na proteinskem delu molekule, ki je povezana s hemom preko his ostanka → konformacijska sprememba proteina
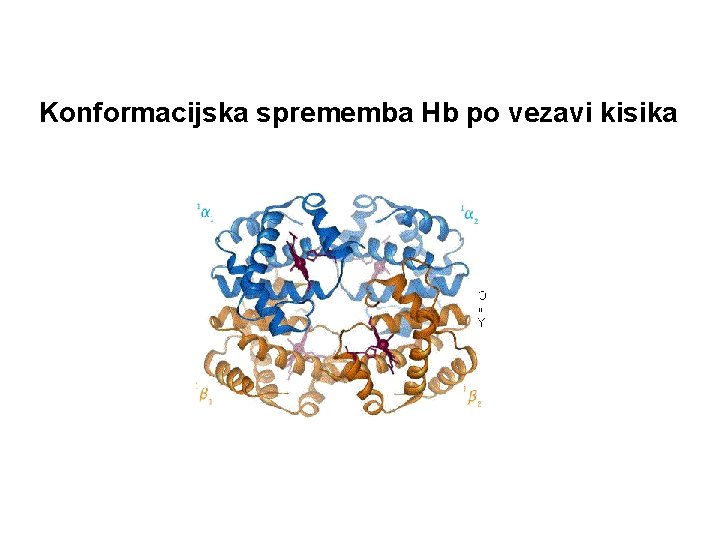
Konformacijska sprememba Hb po vezavi kisika
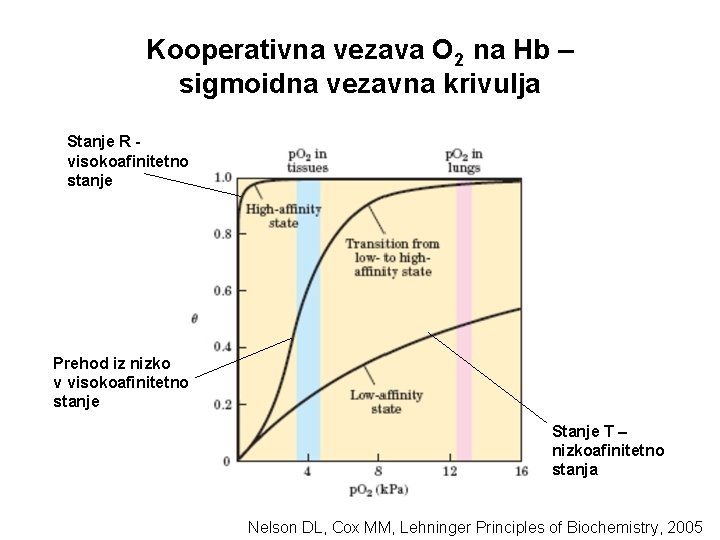
Kooperativna vezava O 2 na Hb – sigmoidna vezavna krivulja Stanje R visokoafinitetno stanje Prehod iz nizko v visokoafinitetno stanje Stanje T – nizkoafinitetno stanja Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005

Alosterični proteini • Vezava liganda (modulatorja) na eno vezavno mesto spremeni vezavne lastnosti drugih vezavnih mest • Konformacijska sprememba, povzročena z vezavo modulatorja: manj aktiven protein v bolj aktiven protein • Modulatorji: inhibitorji ali aktivatorji • Modulator - normalni ligand, homotropična interakcija • Modulator - druga molekula, heterotropična interakcija • Hb in O 2 – pozitivna homotropična interakcija (modulator O 2 je aktivator); kooperativna vezava, značilna sigmoidna krivulja
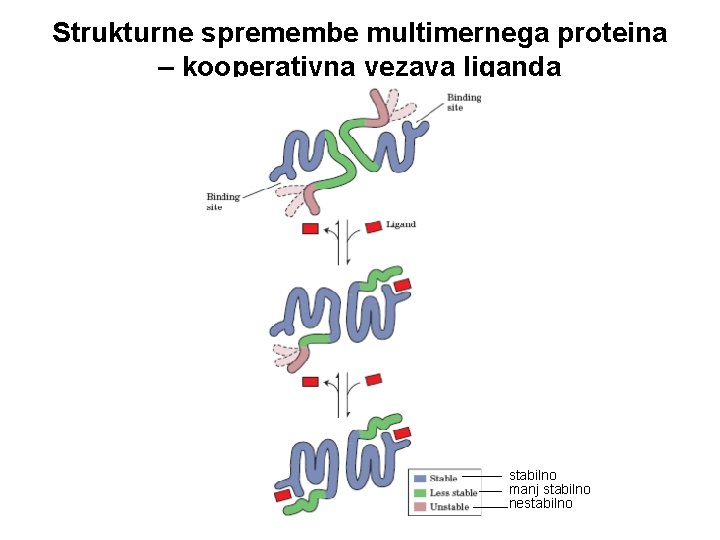
Strukturne spremembe multimernega proteina – kooperativna vezava liganda stabilno manj stabilno nestabilno

Hb prenaša tudi CO 2 in H+ med pljuči in mišicami CO 2, ki nastaja z oksidacijo organskih hranil, reagira z vodo (reakcijo katalizira encim karbonska anhidraza) CO 2 + H 2 O ↔ HCO 3 - + H+ Reverzibilna vezava kisika na Hb: Hb + O 2 ↔ Hb. O 2 Na vezavo kisika na Hb vpliva H+ (Bohrov efekt) Hb. O 2 + H+ ↔ HHb+ + O 2 Posledica: - v pljučih se na Hb veže kisik, sprosti se H+ - v tkivih se s Hb. O 2 sprosti kisik, veže se H+

Vpliv p. H na vezavo kisika na Hb O 2 in H+ se vežeta na Hb z obratno afiniteto
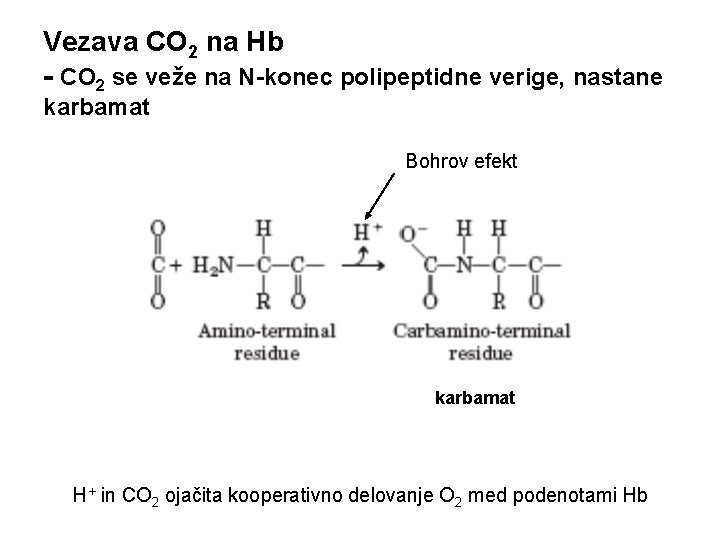
Vezava CO 2 na Hb - CO 2 se veže na N-konec polipeptidne verige, nastane karbamat Bohrov efekt karbamat H+ in CO 2 ojačita kooperativno delovanje O 2 med podenotami Hb

Heterotropični alosterični modulator vezave O 2 na Hb - 2, 3 -bisfosfoglicerat BPG • • Visoka koncentracija BPG v eritrocitih BPG se veže v centralni žep med β podenotami v stanju T – 1 molekula BPG se veže na 1 molekulo Hb Vezavni žep za BPG izgine po prehodu T → R stanje BPG zniža afiniteto do O 2, stabilizira T stanje Hb Hb. BPG + O 2 ↔ Hb. O 2 + BPG T stanje R stanje
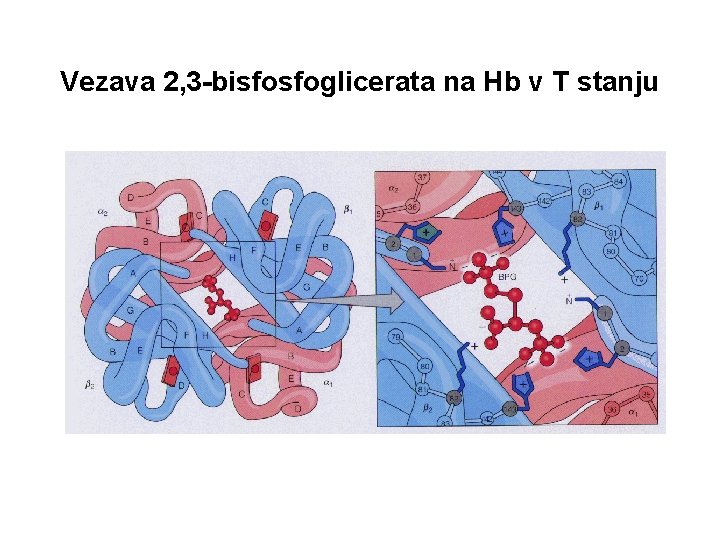
Vezava 2, 3 -bisfosfoglicerata na Hb v T stanju
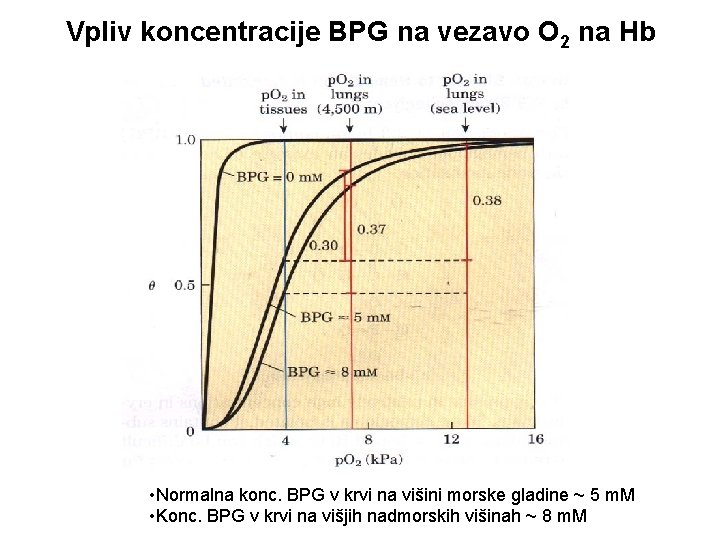
Vpliv koncentracije BPG na vezavo O 2 na Hb • Normalna konc. BPG v krvi na višini morske gladine ~ 5 m. M • Konc. BPG v krvi na višjih nadmorskih višinah ~ 8 m. M

Modulatorji aktivnosti alosteričnega proteina Hb glede vezave O 2 • O 2 - pozitivni homotropični modulator vezave O 2 na Hb • CO 2, H+, BPG negativni heterotropični modulatorji vezave O 2 na Hb – vsi se vežejo na Hb z obratno afiniteto kot O 2

Najpomembnejši človeški Hb Vrsta Struktura podenot Razširjenost Hb. A (odrasli) α 2 β 2 97% Hb odraslih Hb. A 2 (odrasli) α 2 δ 2 2 -3% Hb odraslih Hb. F (fetalni) α 2γ 2 Najpomembnejši Hb v 3. trimestru nosečnosti

Vezavna krivulja Hb matere in zarodka Zaradi večje afinitete zarodkovega Hb do kisika je omogočen prenos kisika iz materine v zarodkovo kri
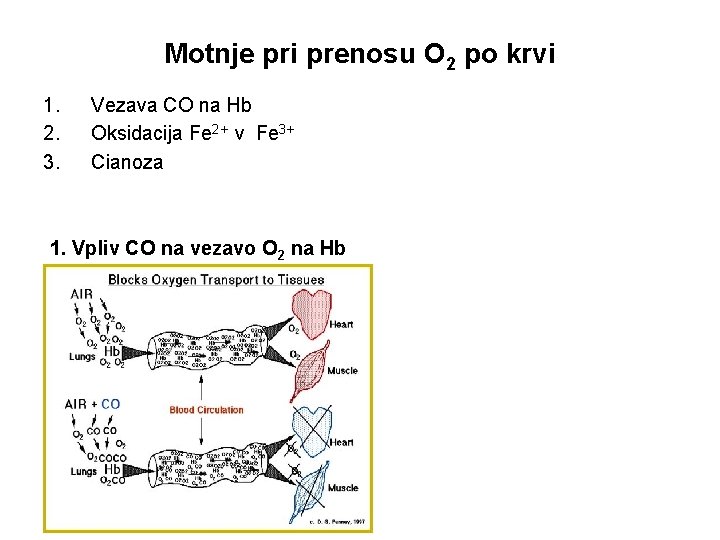
Motnje pri prenosu O 2 po krvi 1. 2. 3. Vezava CO na Hb Oksidacija Fe 2+ v Fe 3+ Cianoza 1. Vpliv CO na vezavo O 2 na Hb

1. Vpliv CO na vezavo O 2 na Hb Koncentracija CO v krvi odvisno od koncentracije CO v okolju Vezavne krivulje O 2 na Hb Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005

2. Oksidacija Fe 2+ v Fe 3+ v hemu: methemoglobim • methemoglobin ne veže O 2 • methemoglobin normalno prisoten do 3% • oksidanti (anilinska barvila, aromatske nitro spojine, nitriti) spremenijo Fe 2+ v Fe 3+ • obramba eritrocitov pred oksidacijo Fe 2+ v Fe 3+ - eritrociti vsebujejo antioksidante (askorbinska kislina, glutation) - encim methemoglobin-reduktaza reducira Fe 3+ v Fe 2+ (redek genski defekt: pomanjkanje reduktaze → kongenitalna methemoglobinemija; zdravljenje z barvilom mtilensko modro)

3. Cianoza • bolnik ima sivo/škrlatno barvo kože • vzrok – visoka koncentracija deoksi-Hb pod površino • zvišana koncentracija deoksi-Hb je posledica bolezni srčnega ali pljučnega sistema → slaba cirkulacija → nezadostna oksigenacija krvi • anemični bolniki niso cianotični – imajo premalo Hb v krvi

Nenormalna tvorba Hb - bolezni • Ak zaporedje globinskih verig je določeno v globinskih genih (kromosoma 11 in 16) • Znanih je ~ 1000 nenormalnih Hb • Hemoglobinopatije – nastanek nenormalnih globinskih verig (primer srpasta anemija - Hb. S) • Talasemije – globinske verige so strukturno normalne, nastajajo pa v manjši količini ali določene verige sploh ni - napaka v regulatornem delu globinskega gena (primer talasemija α, talasemija β)
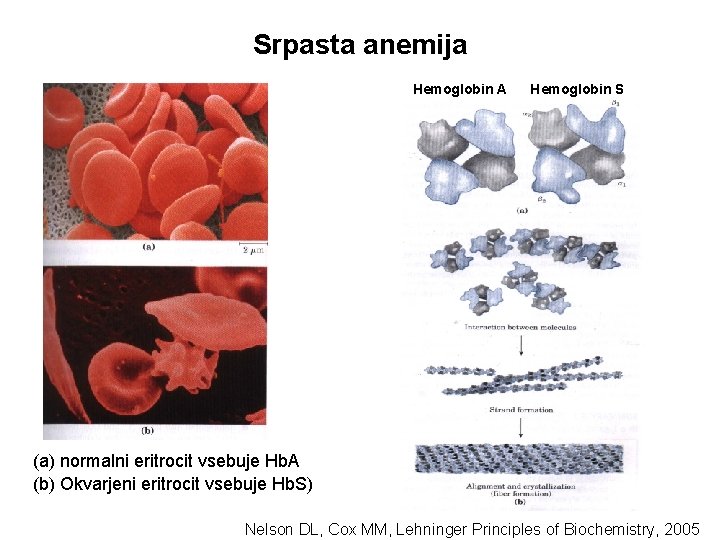
Srpasta anemija Hemoglobin A Hemoglobin S (a) normalni eritrocit vsebuje Hb. A (b) Okvarjeni eritrocit vsebuje Hb. S) ( Nelson DL, Cox MM, Lehninger Principles of Biochemistry, 2005

Vzrok za nastanek Hb. S (α 2βS 2) – mutacija v β verigi Hb: Glu → Val Glu • • • Val Hb. S - nespremenjena hitrost sinteze Hb Hb. S - nespremenjena afiniteta do O 2 Hb. S - hidrofobne interakcije med Val na površini verige Hb → zlepljanje molekul Hb. S zmanjšana topnost Hb. S v deoksigenirani obliki netopni skupki Hb. S preprečujejo normalen pretok krvi v kapilarah
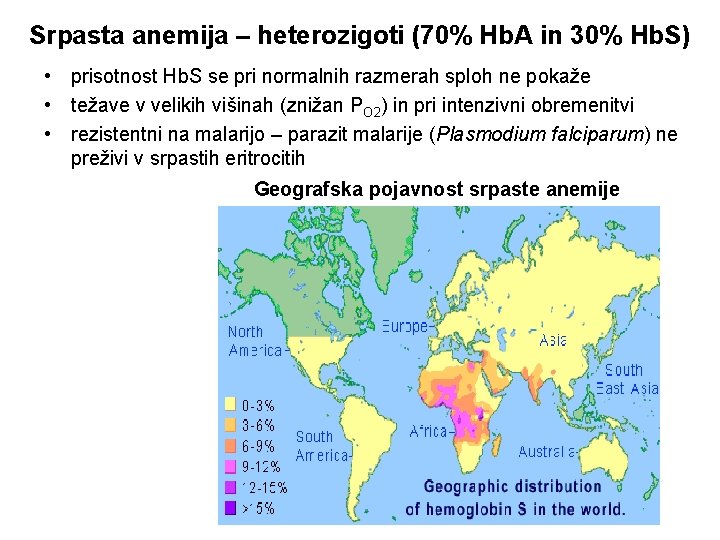
Srpasta anemija – heterozigoti (70% Hb. A in 30% Hb. S) • prisotnost Hb. S se pri normalnih razmerah sploh ne pokaže • težave v velikih višinah (znižan PO 2) in pri intenzivni obremenitvi • rezistentni na malarijo – parazit malarije (Plasmodium falciparum) ne preživi v srpastih eritrocitih Geografska pojavnost srpaste anemije

Talasemije • globinske verige strukturno normalne • globinske verige nastajajo v manjši količini ali določene verige sploh ni • napaka v regulatornem delu globinskega gena talasemija α - napake pri nastajanju α verig talasemija β - napake pri nastajanju β verig
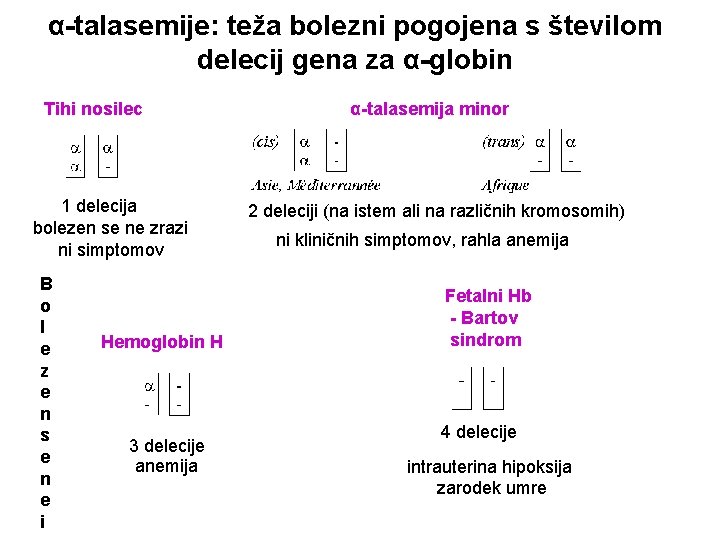
α-talasemije: teža bolezni pogojena s številom delecij gena za α-globin Tihi nosilec 1 delecija bolezen se ne zrazi ni simptomov B o l e z e n s e n e i Hemoglobin H 3 delecije anemija α-talasemija minor 2 deleciji (na istem ali na različnih kromosomih) ni kliničnih simptomov, rahla anemija Fetalni Hb - Bartov sindrom 4 delecije intrauterina hipoksija zarodek umre

β-talasemije: mutacije v β-globinski podenoti • β 0 talasemija – ni β-verige • β+ talasemija – zmanjšana tvorba β-verig
- Slides: 45