Mol Kavram Hafta 10 Ders Ak ElementAtom BileikMolekl

Mol Kavramı Hafta 10

Ders Akışı • Element-Atom, Bileşik-Molekül • Mol ve İlgili Hesaplamalar – Sabit Oranlar-Katılı oranlar 2

Atom-Element • Element, aynı cins atomlardan oluşan ve kimyasal yollarla kendinden daha basit ve farklı maddelere ayrılamayan saf maddelere verilen isimdir. • Kimyasal elementler aynı atom numarasına sahiptirler. Atom numarası atomdaki proton sayısını (çekirdek yükünü) gösteren sayıdır. Bir elementin böylece tüm atomlarında aynı sayıda proton bulunur. • Örnek: – Li, Na, Cl, He, Fe, vb.

Molekül-Bileşik • Bileşik, iki ya da daha fazla cinste atomun bir araya gelerek oluşturduğu saf maddelere denir. Bileşiklerin en küçük yapı taşı moleküllerdir. • Molekül, birbirine bağlı gruplar halindeki atomların oluşturduğu kimyasal bileşiklerin en küçük temel yapısına verilen addır. • Diğer bir ifadeyle bir molekül bir bileşiği oluşturan atomların eşit oranlarda bulunduğu en küçük birimdir. • Moleküller yapılarında birden fazla atom içerirler. Bir molekül aynı iki atomun bağlanması sonucu ya da farkı sayılarda farklı atomların bağlanması sonucu da oluşabilirler. – Bir su molekülü 3 atomdan oluşur; iki hidrojen ve bir oksijen. Bir hidrojen peroksit molekülü iki hidrojen ve iki oksijen atomundan oluşur. Diğer taraftan bir kan proteini olan gamma globulin 1996 sayıda atomdan oluşmakla birlikte sadece 4 çeşit farklı atom içerir; hidrojen, karbon, oksijen ve nitrojen.

Molekül Kütlesi • Bir kimyasal bileşiğin moleküler kütlesi veya moleküler ağırlığı, bu bileşiğin bir molekülünün birleşik atom kütle birimi (bir karbon-12 atomunun 1/12'sine eşit) cinsinden kütlesidir. Bağıl bir değer olduğundan bir maddenin molekül kütlesine yaygın olarak bağıl moleküler kütle denir. • Molekül kütlesi hesaplanırken molekülü oluştururan atomların akb cinsinden miktarları toplanır. • Örnek: Fe. Cl 2: Demir (II) klorür: Fe: 55, 85 g/mol ve Cl: 35, 5 g/mol – Fe akb + 2 x Cl akb = 55, 85 g + 2 x 35, 5 = 126, 85 g/mol • Alıştırma: N 2 O 5: Diazot pentoksit, N 2 O 4: Diazot tetroksit, Hg 2 O: Civa (I) oksit, PCl 3: Fosfor triklorür, PCl 5: Fosfor pentaklorür

Mol Kavramı • Bir düzinenin 12, bir destenin 10 ettiği gibi, herhangi bir parçanın bir molü, o parçanın 6, 023 x 1023’ü kadardır. • Bir düzine yumurtanın ağırlığı, bir düzine portakalın ağırlığı ile aynı değildir. Benzer şekilde, bir elementin bir mol atomunun ağırlığı başka bir elementin bir mol atomunun ağırlığı ile aynı değildir. • Herhangi bir parça veya birimin bir molünün gram olarak ifade edilen ağırlığı, atomik kütle birimi (akb) olarak ifade edilen, bireysel bir parça veya birimin tekinin ağırlığına sayısal olarak eşittir.

Mol Kavramı • Hidrojenin atom ağırlığı 1, 0079 olarak verilmiştir. Bu bir H atomunun kütlesinin 1, 0079 akb’ye eşit olduğu, aynı zamanda 1 mol H atomunun 1, 0079 g olduğu manasına gelmektedir. – Tek bir H atomunun kütlesi 1, 643 x 10 -24 g’dır. Yani, 1, 0079 g 6, 023 x 1023 tane H atomunun toplam kütlesidir; dolayısıyla, bir H atomunun kütlesi 1, 0079 g’ın 6, 023 x 1023’e bölünmesiyle elde edilen 1, 673 x 10 -24 g’a eşittir. • 2. Elementer hidrojen için verilen H 2 formülü, her bir hidrojen molekülünün iki hidrojen atomundan oluştuğu anlamına gelmektedir. İki H atomunun kütlesi 2 x 1, 0079 akb = 2, 0158 akb’dir. – 1 mol H 2 molekülünün kütlesi 2, 0158 g’dır. Tek bir H 2 molekülünün ağırlığı 3, 347 x 10 -24 g’dır. • NO 3 -(nitrat) iyonunun bir azot ve üç oksijen atomundan oluşmaktadır. – Dolayısıyla bir nitrat iyonunun kütlesi, bir azot atomunun ve üç oksijen atomunun kütleleri toplamıdır, ya da (iki yaklaşık sonuca göre) 62, 01 akb’dir. Bundan dolayı, 1 mol nitrat iyonunun kütlesi 62, 01 g ve tek bir nitrat iyonunun kütlesi ise 1, 03 x 10 -22 g’dır.

Mol Kavramı • • • Bir molün; atom, iyon veya molekül gibi taneciklerden 6, 023 x 1023 (Avagadro sayısı) tanedir. Bu kadar sayıdaki taneciğin ağırlığı gram olarak ifade edilir. Bir mol hidrojen iyonu (H+): Kaç tane hidrojen iyonu içerir? Kütlesi ne kadardır? Aksi belirtilmediği müddetçe, mol terimi gram-mol terimi anlamına gelmektedir. Bir grammol 6, 023 x 1023 taneciğin ağırlığının gram olarak ifadesidir. Bir gram-mol atom gram olarak ifade edilen atom ağırlığına denktir. – Bir mol karbon atomu (C) kaç gramdır – Karbon’un atom ağırlığı kaç gramdır? Bir mol kurşun (Pb) elementi. . . tane atom içerir ve. . . . ağırlığındadır. Cevap: 6, 023 x 1023, 207, 2 g Bir molekül karbon disülfür (CS 2) elde etmek için kaç karbon ve kükürt atomu gerekmektedir? Cevap: bir C ve iki S atomu Hesaplamalarda, mol kısaltması mol veya moller anlamına gelmektedir. 1 mol karbon disülfür (CS 2) elde etmek, kaç mol karbon ve kükürt atomlarını gerektirmektedir? Cevap: 1 mol C ve 2 mol S

Mol Kavramı • • • • Bir mol karbon tetraklorür (CCl 4) kaç mol C ve kaç mol Cl atomu içerir? Cevap: 1 mol C ve 4 mol Cl ve 1 mol C atomu 1 mol CCl 4 oluşturabildiğine göre 1 mol CCl 4 molekülünün ağırlığı ne kadardır? Cevap: 153, 81 g Yarım mol H 2 SO 4 kaç gramdır? Cevap: 49, 04 g (Ağırlık H 2 SO 4 = 0, 5 mol H 2 SO 4 x 98, 08 g H 2 SO 4 / 1 mol H 2 SO 4= 49, 04 g H 2 SO 4) Otuz altı gram H 2 O kaç mol eder? Cevap: 2 mol (mol H 2 O=36 g H 2 O x 1 mol H 2 O / 18, 02 g H 2 O = 2, 00 mol H 2 O) Dokuz gram H 2 O kaç mol eder? Cevap: 0, 50 mol ( mol H 2 O= 9 g H 2 O x 1 mol H 2 O / 18, 02 g H 2 O = 0, 50 mol H 2 O) Metil alkolün (CH 3 OH) formül ağırlığı 32, 05 gramdır. Yarım gram CH 3 OH kaç mol eder ? Cevap: 0, 016 mol (0, 50 g CH 3 OH x 1 mol CH 3 OH/32, 05 g CH 3 OH = 0, 016 mol CH 3 OH) Bir mol Cl atomu mu yoksa 1 mol Na atomu mu daha ağırdır? Cevap: Bir mol Cl atomu

Mol Kavramı • Denkleştirilmiş Zn + 2 HCl → H 2 + Zn. Cl 2 reaksiyonunda çinko metali hidroklorik asit ile reaksiyona sokulduğunda hidrojen gazı ve çinko klorür oluşur. 1 mol Zn. Cl 2 elde etmek için kaç mol HCl gerekmektedir? • Cevap: 2 • Bir önceki reaksiyonda yalnızca yarım mol Zn’nin olduğu varsayılmaktadır. Buna göre, kaç mol Zn. Cl 2 oluşabilir? Kaç mol HCl kullanılması gerekmektedir? • Cevap: ½; 1 • 2 KCl. O 3 → 2 KCl + 3 O 2 reaksiyonu laboratuvarda genellikle oksijen gazı elde etmek için kullanılmaktadır. Bu reaksiyonda, 2 mol KCl ve 3 mol O 2 elde etmek için 2 mol KCl. O 3 gerekmektedir. Reaksiyona giren 2 mol KCl. O 3’ün tamamı tükendiğinde ağırlıkça ne kadar oksijen (O 2) elde edilir? (Oksijen gazı iki atomlu bir molekül halinde bulunur ve 3 mol O 2 molekülü ile 6 mol O atomu aynı ağırlıktadır. ) • Cevap: ağırlık O 2 = 3 mol O 2 x 32, 00 g O 2 / 1 mol O 2 = 96, 00 g O 2

Mol Kavramı • Yalnızca 122, 6 gram KCl. O 3 olduğunda, kaçar mol KCl ve O 2 elde edilebilmektedir? (İlk önce verilen KCl. O 3 miktarının kaç mol ettiği hesaplanmalıdır. ) – mol KCl =. . . – mol O 2 =. . . • Cevap: mol KCl. O 3 = 122, 6 g KCl. O 3 x 1 mol KCl. O 3 / 122, 55 g KCl. O 3= 1 mol KCl. O 3 – 2 mol KCl. O 3’den 2 mol KCl ve 3 mol O 2 elde edilmektedir • 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 reaksiyonuna göre; – 32, 44 gram Fe. Cl 3 elde etmek için kaç mol demir (Fe) ve klor gazı (Cl 2) gerekmektedir? (Öncelikle Fe. Cl 3’ün gram miktarı mole dönüştürülmelidir. ) • Cevap: mol Fe. Cl 3 = 32, 44 g Fe. Cl 3 x 1 mol Fe. Cl 3 / 162, 20 g Fe. Cl 3 = 0, 20 mol Fe. Cl 3 – 1 mol Fe and 1, 5 mol Cl 2’den 1 mol Fe. Cl 3 elde edilmektedir

Mol Kavramı: Sınırlayıcı Bileşen • Günlük hayattaki çoğu kimyasal reaksiyonda, girenlerden biri veya daha fazlasının miktarı sınırlıdır. • Örnek olarak, çalışır haldeki bir arabanın motorunda benzin ile havadaki oksijen reaksiyona girerek 1 litre benzin yaktığında, bu kimyasal reaksiyondan başlıca CO (karbon monoksit) ve H 2 O yanında diğer ürünler oluşur. • Bir litre benzinin hepsi tükendiğinde dahi havada hala yeterince oksijen bulunmaktadır. Aslında bir depo benzinin harcanması durumda da havada yeterince oksijen vardır. Bu durumda reaksiyonda tamamen tükenen benzin sınırlayıcı bileşendir.

Mol Kavramı • C + O 2 → CO 2 reaksiyonunda yeterince oksijen bulunmasına rağmen yalnızca 3 gram karbon (C) vardır. – (a) Girenlerden hangisi sınırlayıcı bileşendir, C veya O 2? – (b) Kaç gram CO 2 elde edilebilir? • Cevap: • (a) C • (b) mol C = 3 g C x 1 mol C / 12, 01 g C = 0, 25 mol C – 1 mol C’dan 1 mol CO 2 elde edildiğine göre; – 0, 25 mol C’dan 0, 25 mol CO 2 elde edilir – Kaç g CO 2 = 0, 25 mol CO 2 x 44, 01 g CO 2/ 1 mol CO 2=11, 00 g CO 2

Mol Kavramı • Aşağıdaki reaksiyonda 18, 02 gram su oluştuğunda, yeterince oksijen kalmasına rağmen silanın (Si. H 4) tamamı tükenmektedir: Si. H 4 + 2 O 2 → Si. O 2 + 2 H 2 O. – (a) Kaç mol silan (Si. H 4) kullanılmıştır? – (b) Sınırlayıcı bileşen hangisidir? • Cevap: (a) 0, 50 mol Si. H 4; (b) silan (Si. H 4)

Sabit Oranlar Kanunu Bir bileşiği oluşturan elementlerin, bileşikteki kütleleri arasında sabit (belirli) bir oran vardır. Bu durumu açıklayan kanuna sabit oranlar kanunu denir.

Katlı Oranlar Kanunu İki element kendi aralarında birden fazla bileşik oluşturduklarında, elementlerden birinin sabit kütlesiyle birleşen diğer elementin kütleleri arasında, basit ve tam sayılarla ifade edilen bir oran vardır. ” Bu ifadeye katlı oranlar kanunu denir.
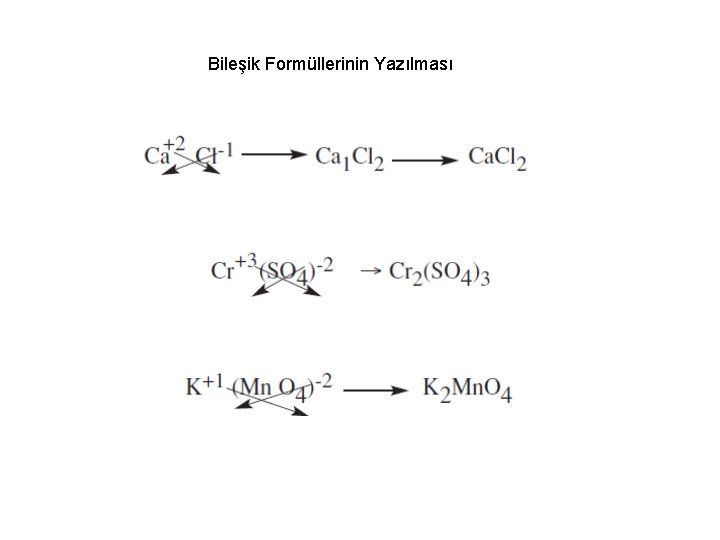
Bileşik Formüllerinin Yazılması
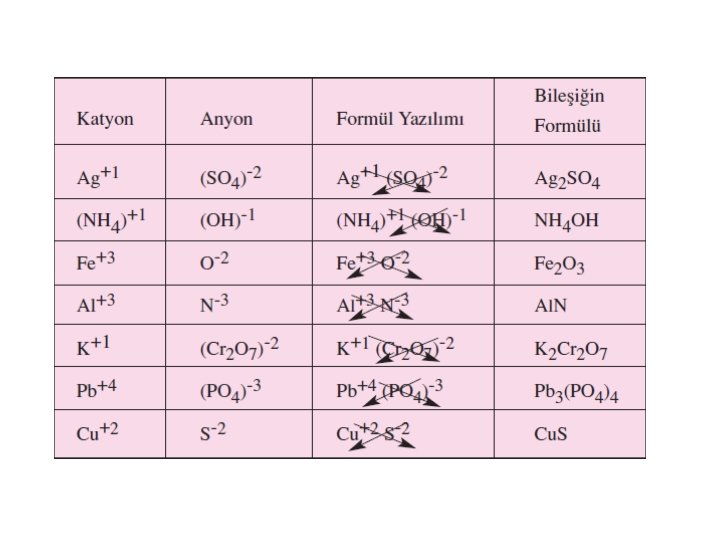

Bir bileşiğin bulunan formülü, o bileşiğin biriminde bulunan atomların sayısını verir. Bir bileşiğin formülünü bulmak için genellikle kütle yüzdesinden faydalanılır ve kütle yüzdeleri deneysel olarak belirlenir.





Kaynaklar • Yurttaş, L. http: //home. anadolu. edu. tr/~lyurttas/Genel%20 Kim ya%20 I%202014/ • https: //tr. wikipedia. org/wiki/Molekül
- Slides: 24