Como podemos maximizar a diferena de velocidade eletrofortica













- Slides: 56

Como podemos maximizar a diferença de velocidade eletroforética (mobilidade) em CE?

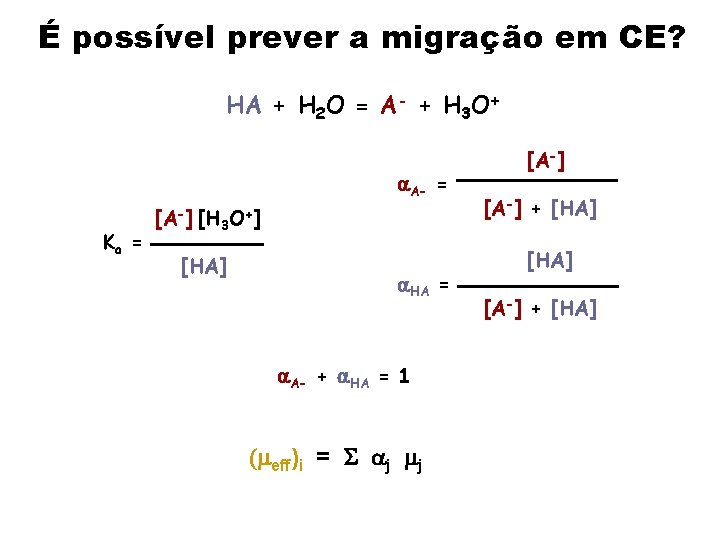
É possível prever a migração em CE? HA + H 2 O = A- + H 3 O+ A- = Ka = [A-] [H + 3 O ] [HA] HA = A- + HA = 1 (meff)i = S j mj [A-] + [HA]

Desde que se conheça os valores de p. Ka e mobilidade iônica (meff)ácido = A- m. A- + HA m. HA = 0, espécie neutra (meff)ácido = A- m. A- = Ka Ka + [H 3 O+] m. A-

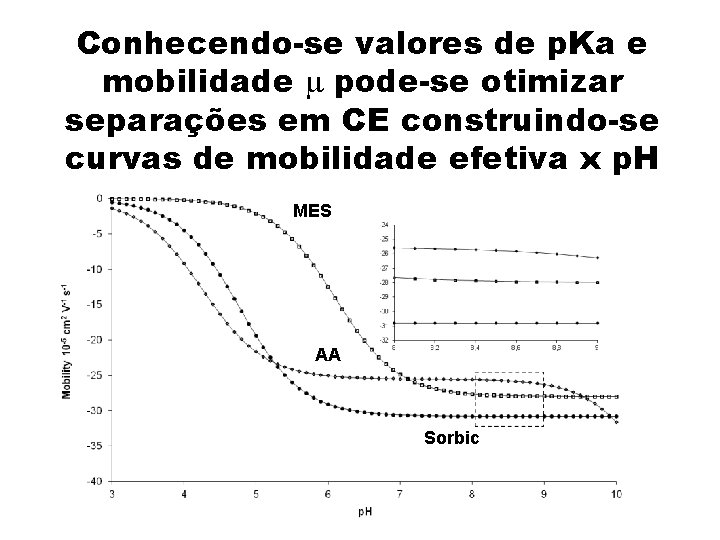
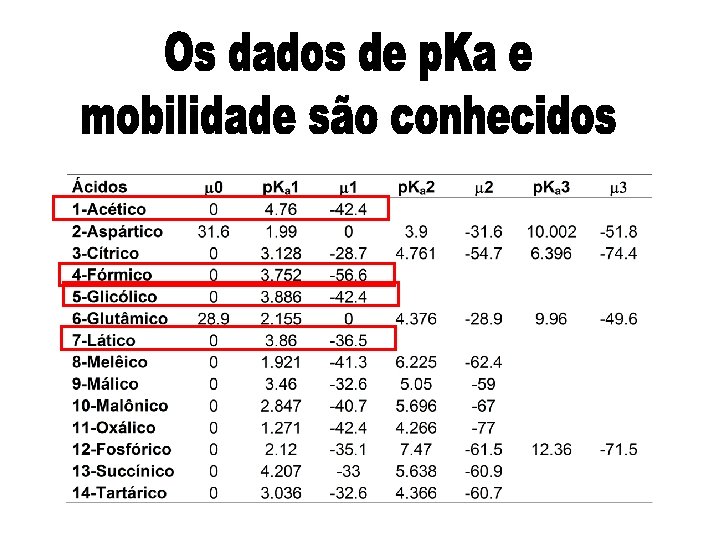
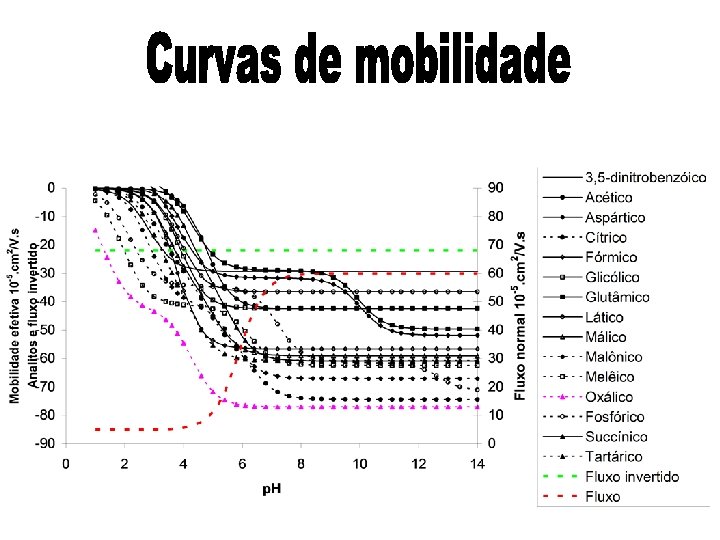
Conhecendo-se valores de p. Ka e mobilidade pode-se otimizar separações em CE construindo-se curvas de mobilidade efetiva x p. H MES AA Sorbic

Pode-se maximizar as diferenças de velocidade eletroforética, porém qual a causa do alargamento dos picos? Lembrando que uma boa análise cromatográfica apresenta uma boa resolução, alta eficiência e um curto tempo de análise.

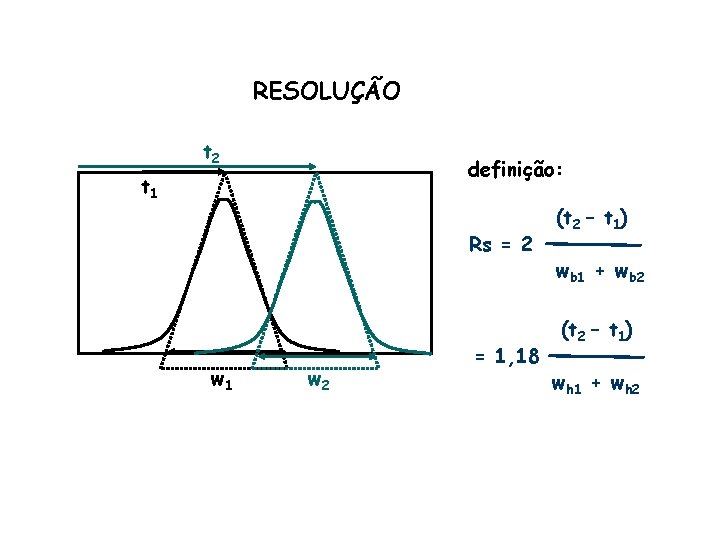
RESOLUÇÃO t 2 definição: t 1 Rs = 2 w 1 w 2 = 1, 18 (t 2 – t 1) wb 1 + wb 2 (t 2 – t 1) wh 1 + wh 2

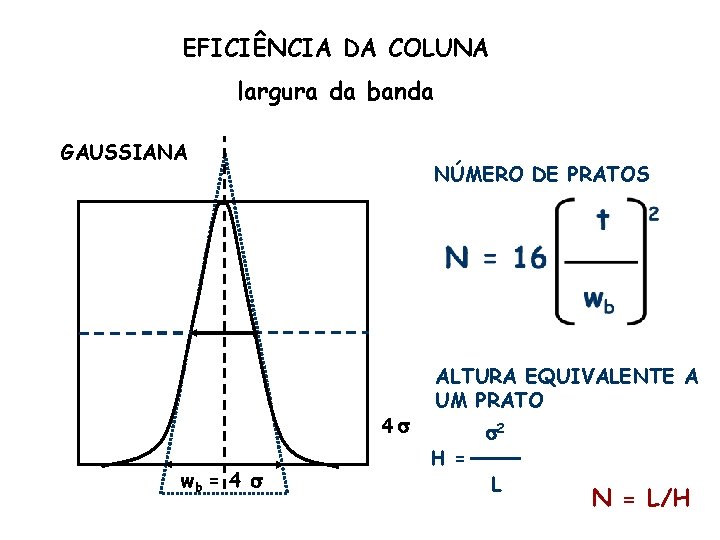
EFICIÊNCIA DA COLUNA largura da banda GAUSSIANA NÚMERO DE PRATOS 4 s wb = 4 s ALTURA EQUIVALENTE A UM PRATO s 2 H = L N = L/H

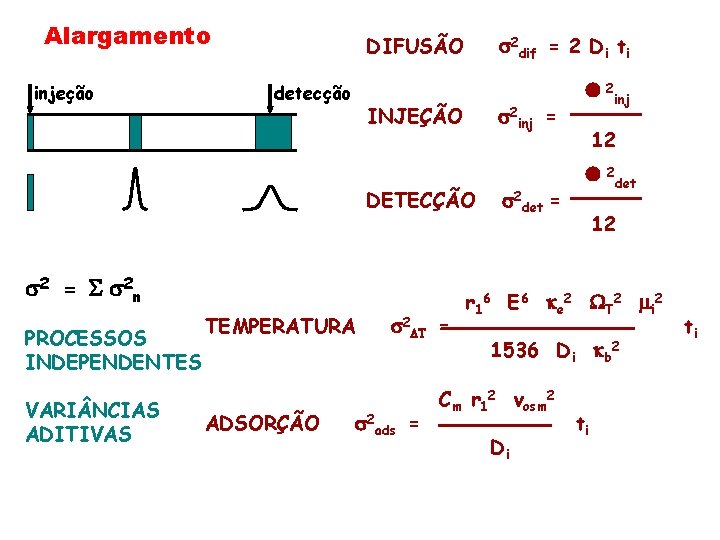
Alargamento injeção DIFUSÃO detecção s 2 dif = 2 Di ti INJEÇÃO s 2 inj = DETECÇÃO s 2 = S s 2 n PROCESSOS INDEPENDENTES VARI NCIAS ADITIVAS TEMPERATURA ADSORÇÃO s 2 DT = s 2 ads = s 2 det = l 2 inj 12 l 2 det 12 r 16 E 6 ke 2 T 2 mi 2 1536 Di kb 2 Cm r 12 vosm 2 Di ti ti

Dispersão por eletromigração Lembrando. . . U = R. i ou E = R. i Numa região onde os componentes têm: a R E = R. i O que significa que se: Como a velocidade = E

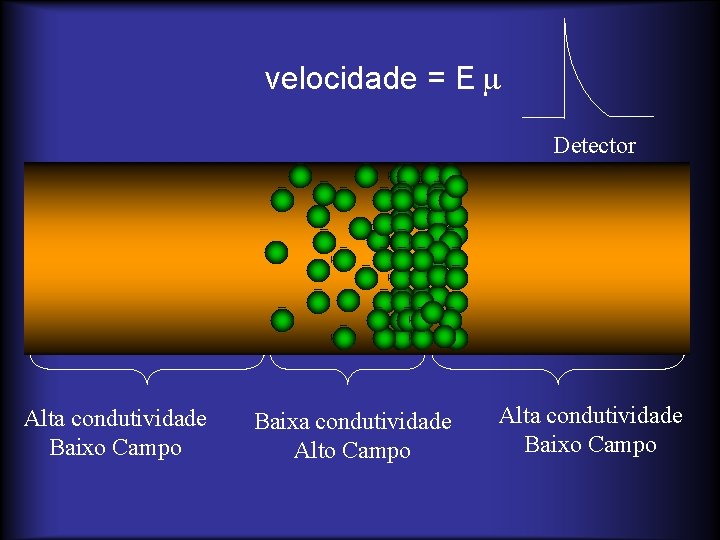
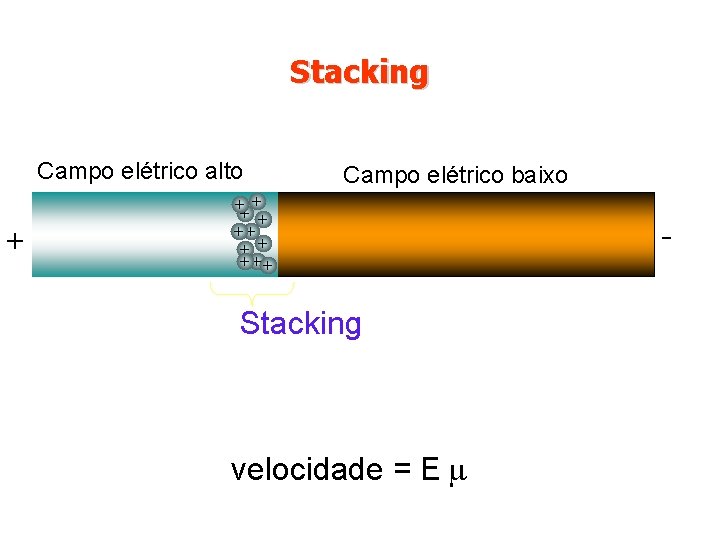
velocidade = E Detector Alta condutividade Baixo Campo Baixa condutividade Alto Campo Alta condutividade Baixo Campo

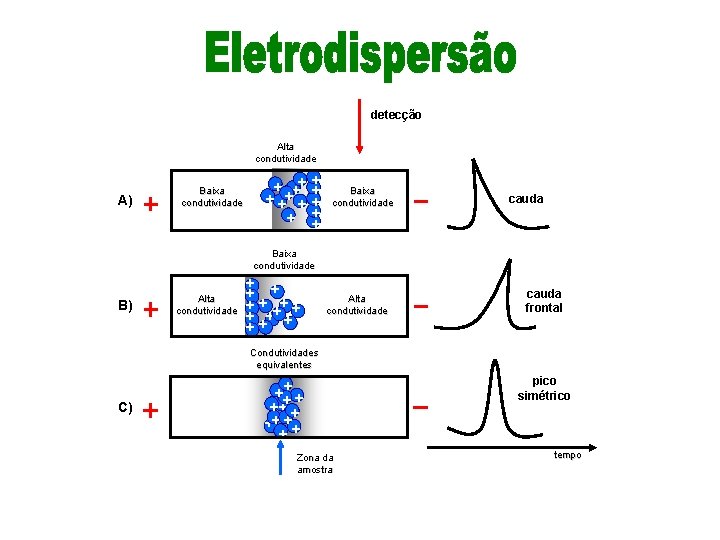
detecção Alta condutividade Baixa condutividade + ++ ++ ++ + A) Baixa condutividade cauda Baixa condutividade B) Alta condutividade + + ++ Alta condutividade cauda frontal Condutividades equivalentes ++ +++++ + C) pico simétrico + Zona da amostra tempo

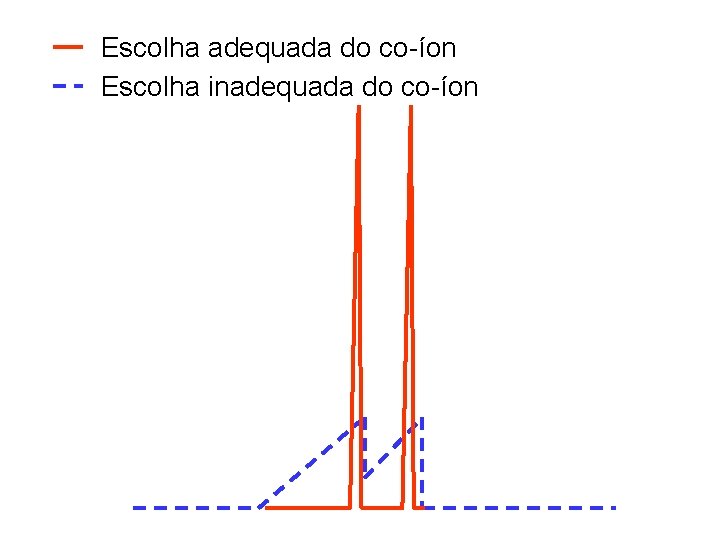
Escolha adequada do co-íon Escolha inadequada do co-íon

Curva de mobilidade versus p. H Escolha um p. H onde os analitos estejam totalmente dissociados e apresentem boa diferença de mobilidade efetiva Escolha do co-íon: totalmente ionizado e eff analito Escolha do contra íon: p. Ka p. H Escolha do padrão interno: totalmente ionizado e ( IS co-ion Analyte ) Porque p. Ka p. H na etapa 3? Para que serve um padrão interno?

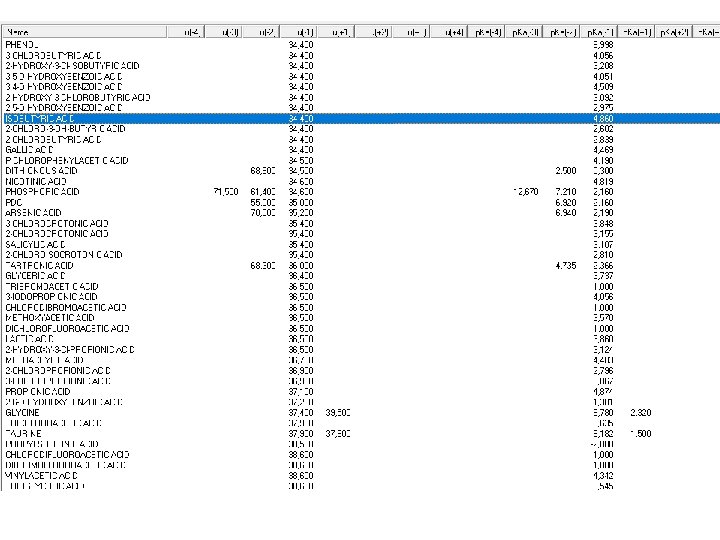
Determinação rápida de AAS em tabletes de aspirina Utilização se softwares de simulação

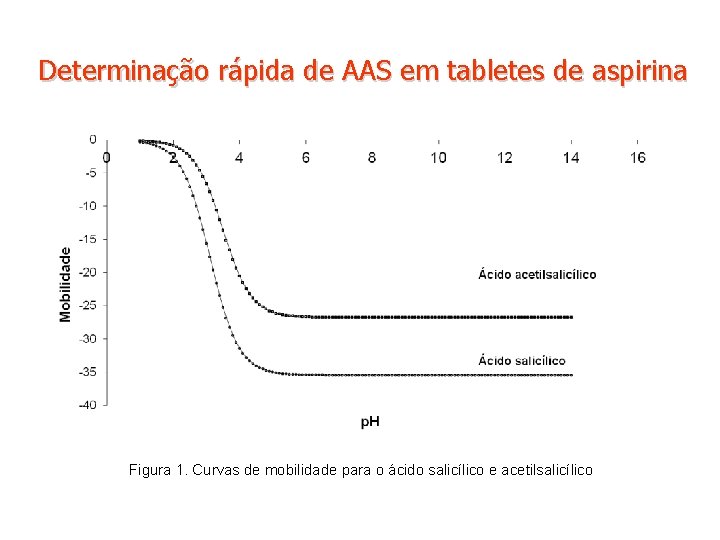
Determinação rápida de AAS em tabletes de aspirina Figura 1. Curvas de mobilidade para o ácido salicílico e acetilsalicílico

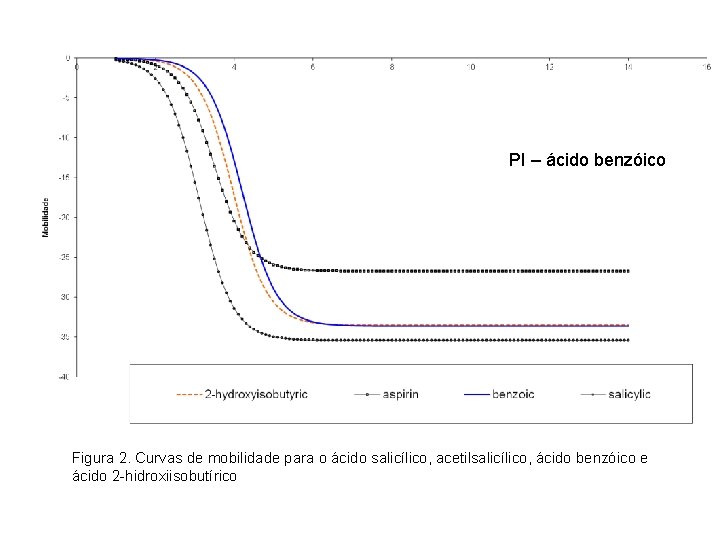
PI – ácido benzóico Figura 2. Curvas de mobilidade para o ácido salicílico, acetilsalicílico, ácido benzóico e ácido 2 -hidroxiisobutírico

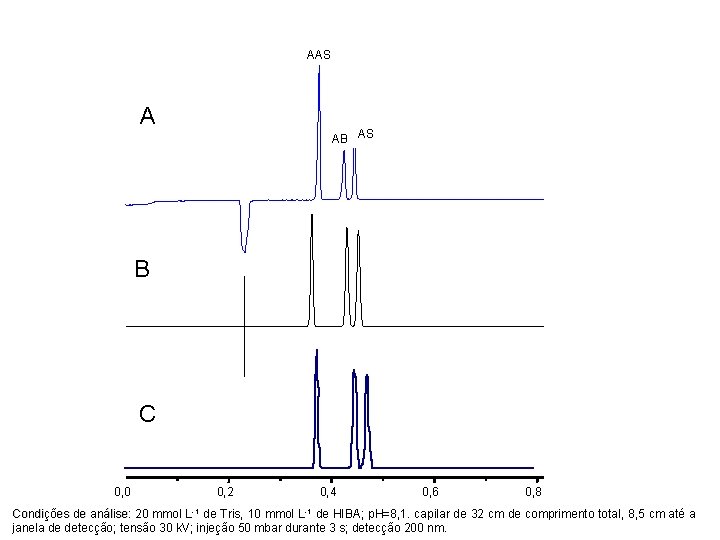
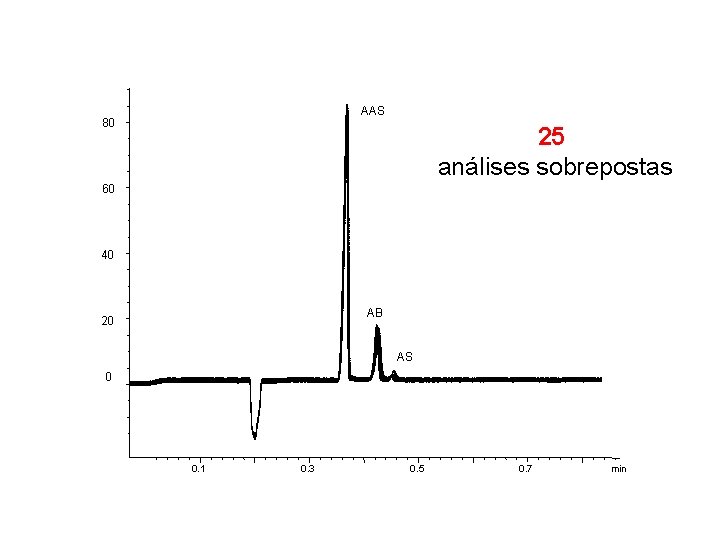
AAS A AB AS B C 0, 0 0, 2 0, 4 0, 6 0, 8 1, 0 . Condições de análise: 20 mmol L-1 de Tris, 10 mmol L-1 de HIBA; p. H=8, 1. capilar de 32 cm de comprimento total, 8, 5 cm até a janela de detecção; tensão 30 k. V; injeção 50 mbar durante 3 s; detecção 200 nm.

AAS 80 25 análises sobrepostas 60 40 AB 20 AS 0 0. 1 0. 3 0. 5 0. 7 min


Determinação simultânea de Cr(III) e Cr(VI) em água O limite para Crtotal em água é de 50 ppb. Como era mesmo a história da diferença de sensibilidade entre CE e HPLC?

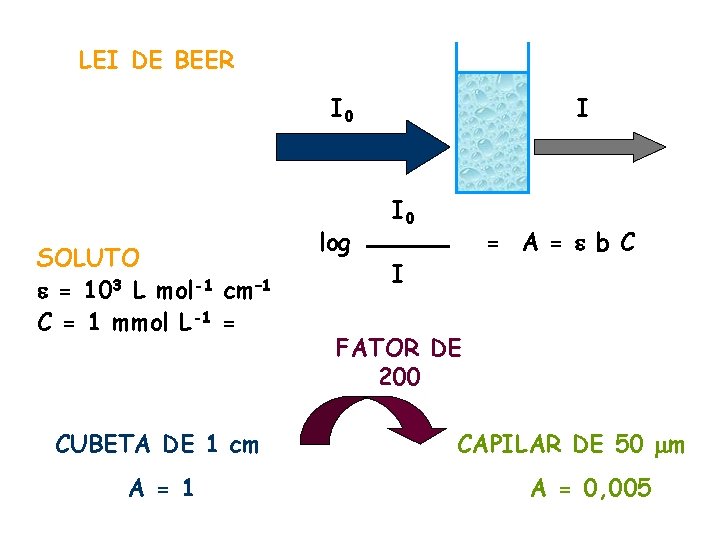
LEI DE BEER I 0 SOLUTO e = 103 L mol-1 cm– 1 C = 1 mmol L-1 = CUBETA DE 1 cm A = 1 log I I 0 = A = e b C I FATOR DE 200 CAPILAR DE 50 mm A = 0, 005

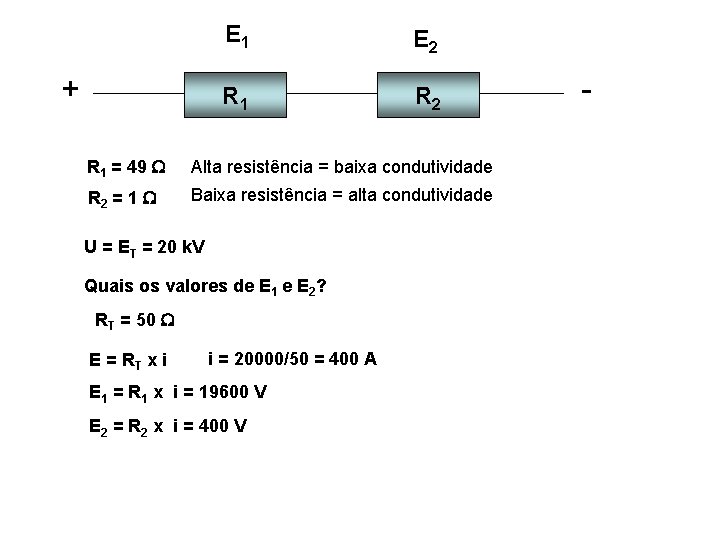
+ E 1 E 2 R 1 R 2 R 1 = 49 Alta resistência = baixa condutividade R 2 = 1 Baixa resistência = alta condutividade U = ET = 20 k. V Quais os valores de E 1 e E 2? RT = 50 E = RT x i i = 20000/50 = 400 A E 1 = R 1 x i = 19600 V E 2 = R 2 x i = 400 V -

+ Água Solução Na. Cl 0, 1 mol/L Qual das duas regiões acima tem maior resistência? Qual das duas regiões acima terá maior campo elétrico? -

Stacking Campo elétrico alto + + + + + Campo elétrico baixo + + ++ ++ Stacking velocidade = E -

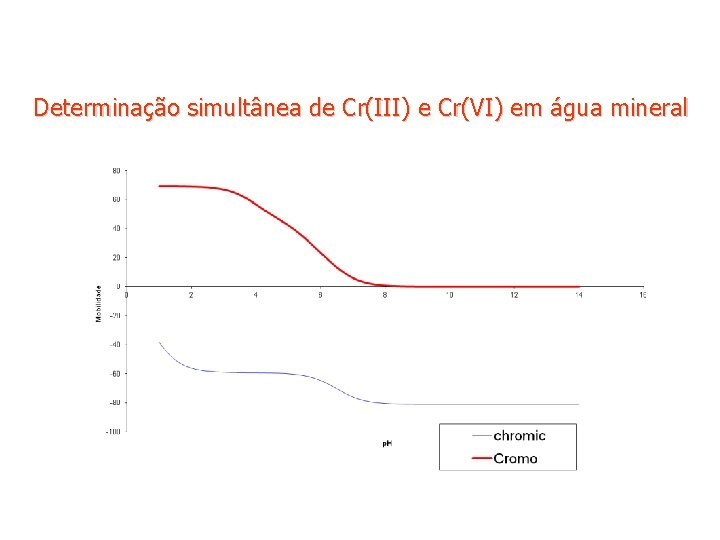
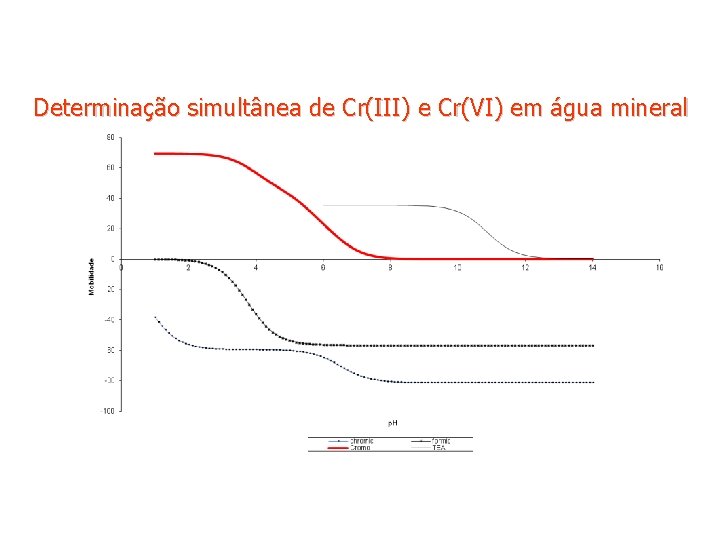
Determinação simultânea de Cr(III) e Cr(VI) em água mineral

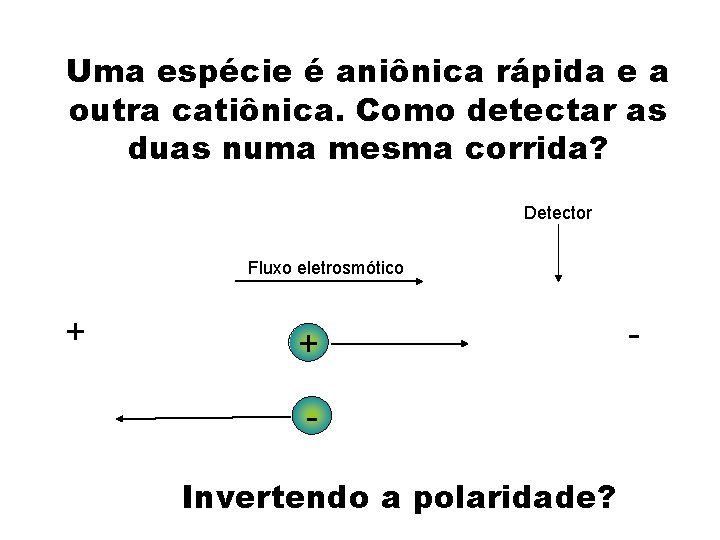
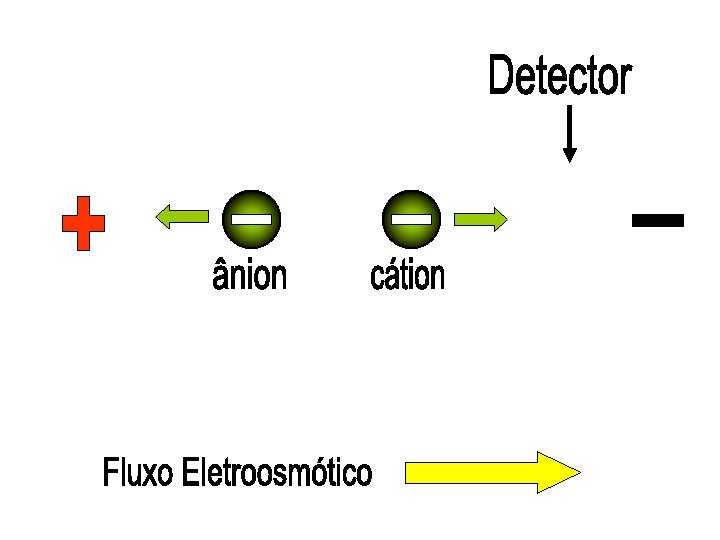
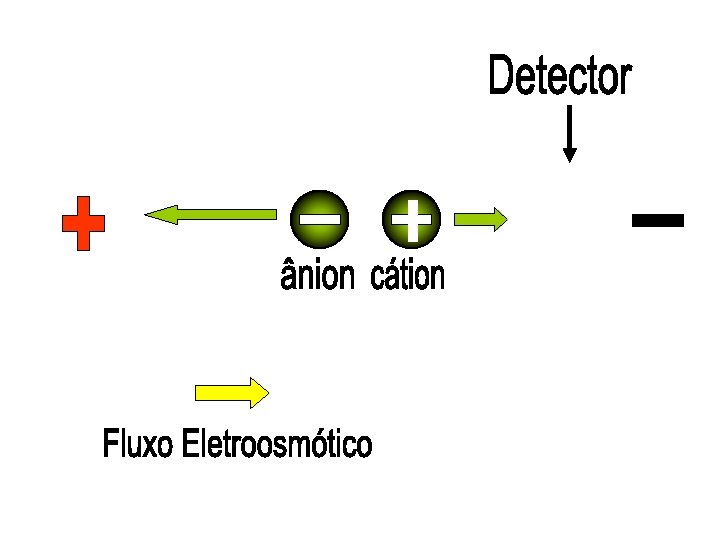
Uma espécie é aniônica rápida e a outra catiônica. Como detectar as duas numa mesma corrida? Detector Fluxo eletrosmótico + + Invertendo a polaridade? -

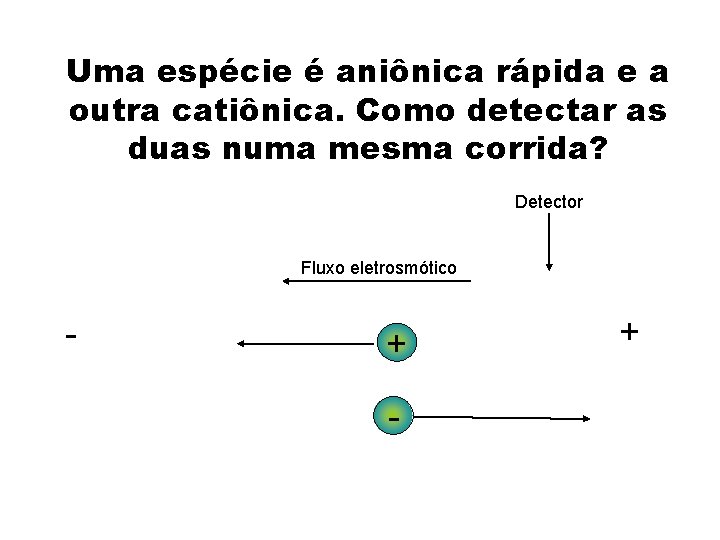
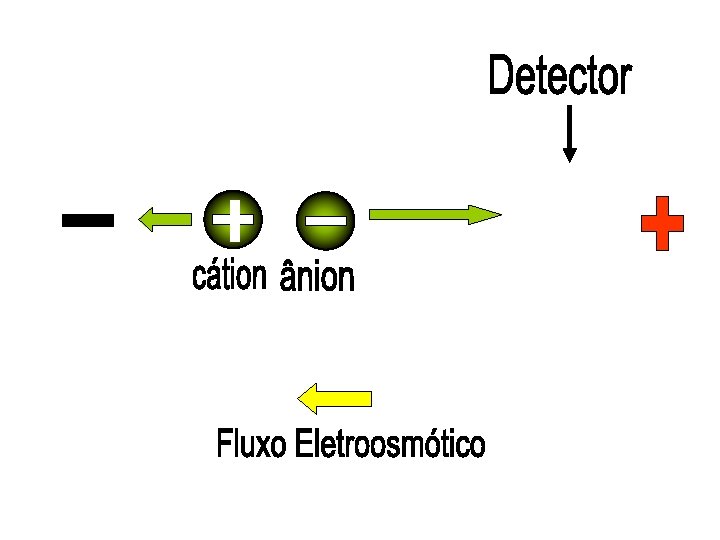
Uma espécie é aniônica rápida e a outra catiônica. Como detectar as duas numa mesma corrida? Detector Fluxo eletrosmótico - +

Determinação simultânea de Cr(III) e Cr(VI) em água mineral

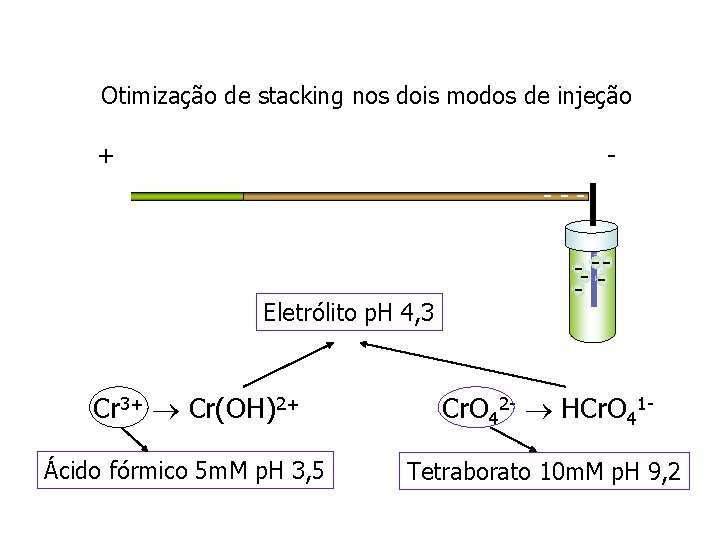
Otimização de stacking nos dois modos de injeção + --- Eletrólito p. H 4, 3 Cr 3+ Cr(OH)2+ Ácido fórmico 5 m. M p. H 3, 5 -- ---- - - Cr. O 42 - HCr. O 41 Tetraborato 10 m. M p. H 9, 2

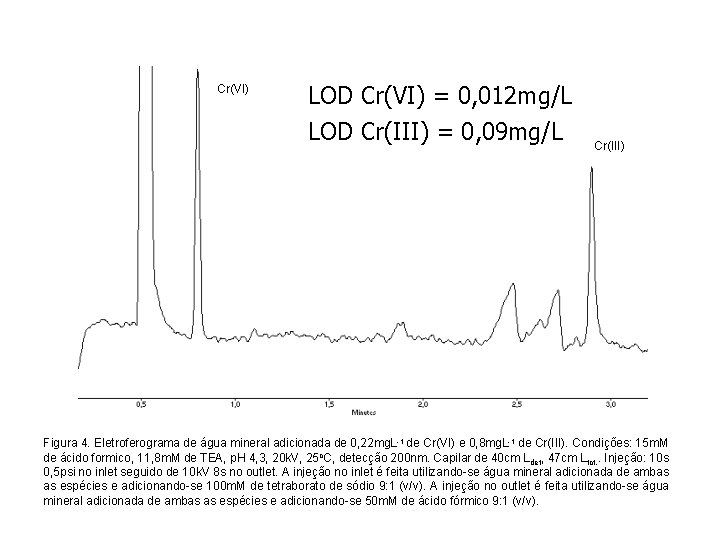
Cr(VI) LOD Cr(VI) = 0, 012 mg/L LOD Cr(III) = 0, 09 mg/L Cr(III) Figura 4. Eletroferograma de água mineral adicionada de 0, 22 mg. L-1 de Cr(VI) e 0, 8 mg. L-1 de Cr(III). Condições: 15 m. M de ácido formico, 11, 8 m. M de TEA, p. H 4, 3, 20 k. V, 25 o. C, detecção 200 nm. Capilar de 40 cm Ldet, 47 cm Ltot. . Injeção: 10 s 0, 5 psi no inlet seguido de 10 k. V 8 s no outlet. A injeção no inlet é feita utilizando-se água mineral adicionada de ambas as espécies e adicionando-se 100 m. M de tetraborato de sódio 9: 1 (v/v). A injeção no outlet é feita utilizando-se água mineral adicionada de ambas as espécies e adicionando-se 50 m. M de ácido fórmico 9: 1 (v/v).

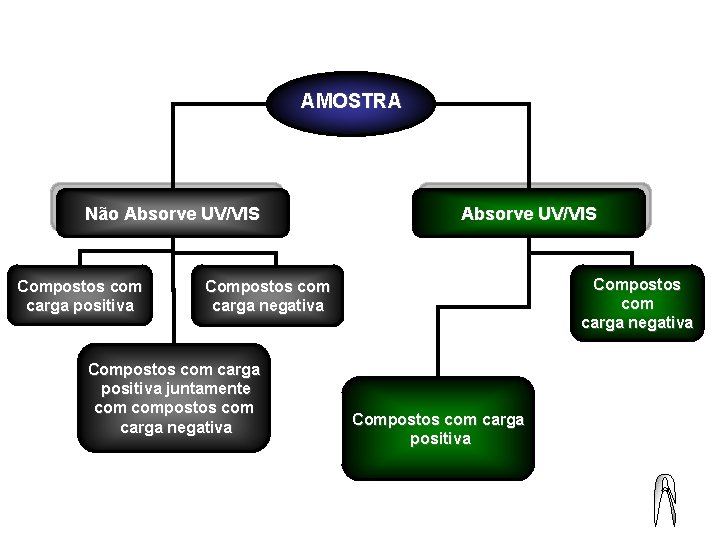
AMOSTRA Não Absorve UV/VIS Compostos com carga positiva Absorve UV/VIS Compostos com carga negativa Compostos com carga positiva juntamente compostos com carga negativa Compostos com carga positiva

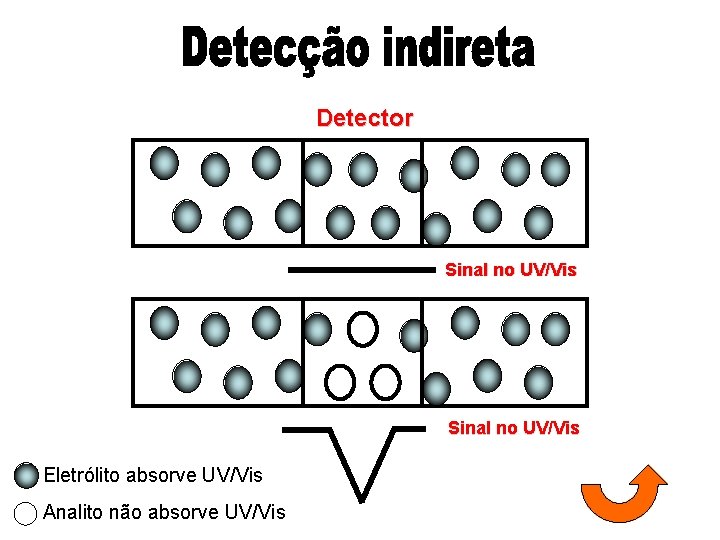
Detector Sinal no UV/Vis Eletrólito absorve UV/Vis Analito não absorve UV/Vis




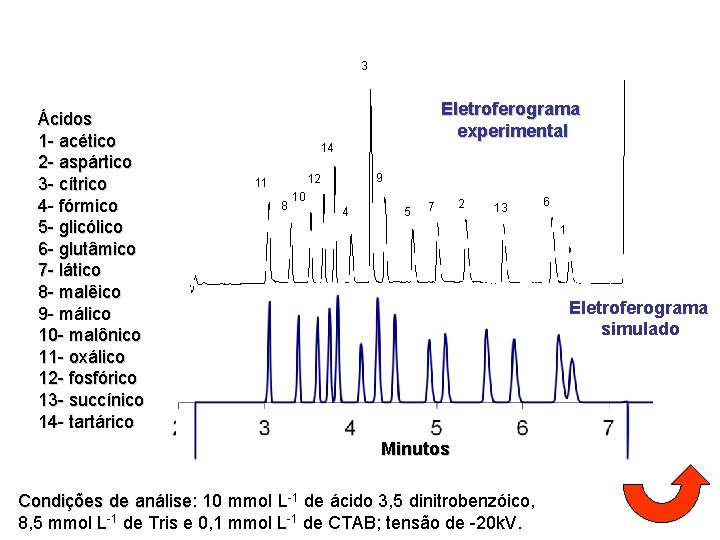
3 Ácidos 1 - acético 2 - aspártico 3 - cítrico 4 - fórmico 5 - glicólico 6 - glutâmico 7 - lático 8 - malêico 9 - málico 10 - malônico 11 - oxálico 12 - fosfórico 13 - succínico 14 - tartárico Eletroferograma experimental 14 9 12 11 8 10 4 5 7 2 13 6 1 Eletroferograma simulado Minutos Condições de análise: 10 mmol L-1 de ácido 3, 5 dinitrobenzóico, 8, 5 mmol L-1 de Tris e 0, 1 mmol L-1 de CTAB; tensão de -20 k. V.


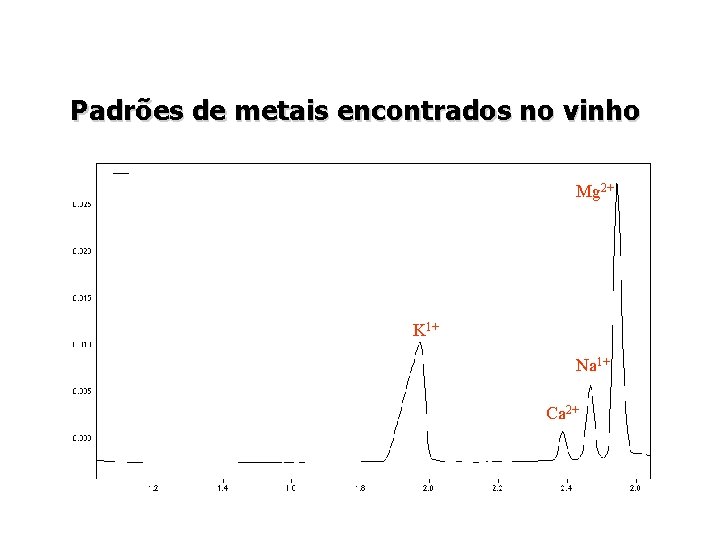
Padrões de metais encontrados no vinho Mg 2+ K 1+ Na 1+ Ca 2+

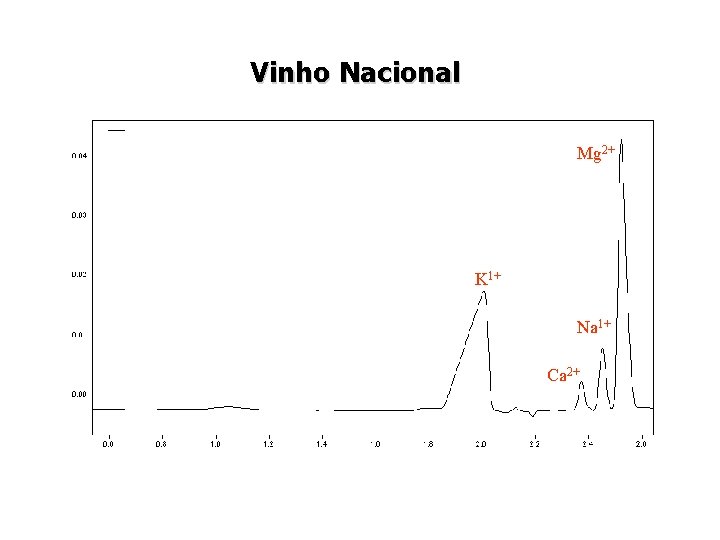
Vinho Nacional Mg 2+ K 1+ Na 1+ Ca 2+

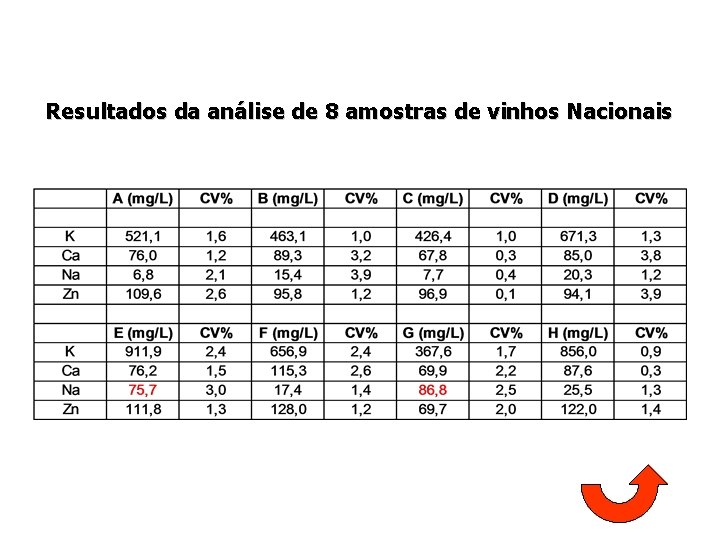
Resultados da análise de 8 amostras de vinhos Nacionais



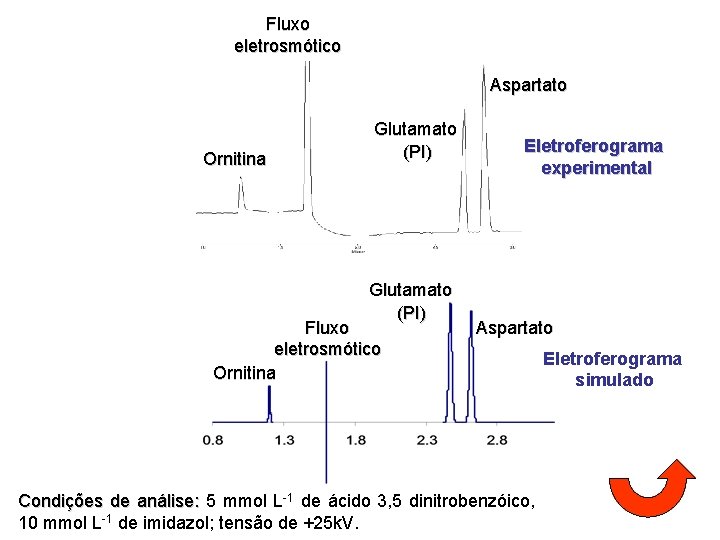
Fluxo eletrosmótico Aspartato Ornitina Glutamato (PI) Fluxo eletrosmótico Ornitina Eletroferograma experimental Aspartato Condições de análise: 5 mmol L-1 de ácido 3, 5 dinitrobenzóico, 10 mmol L-1 de imidazol; tensão de +25 k. V. Eletroferograma simulado

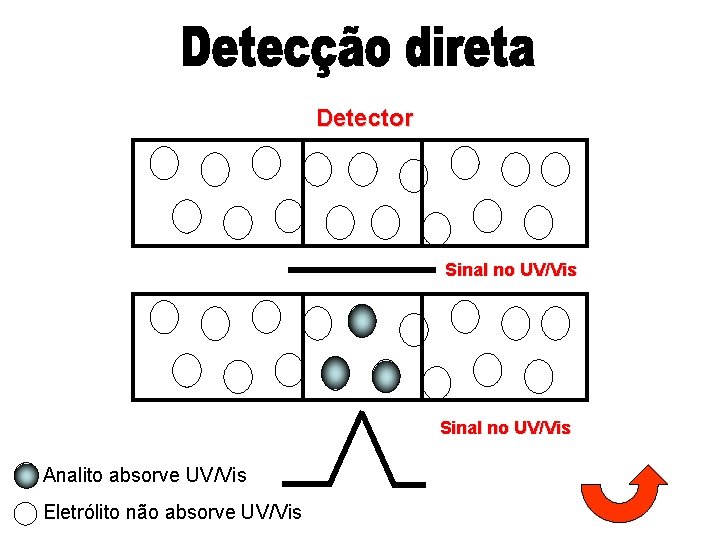
Detector Sinal no UV/Vis Analito absorve UV/Vis Eletrólito não absorve UV/Vis



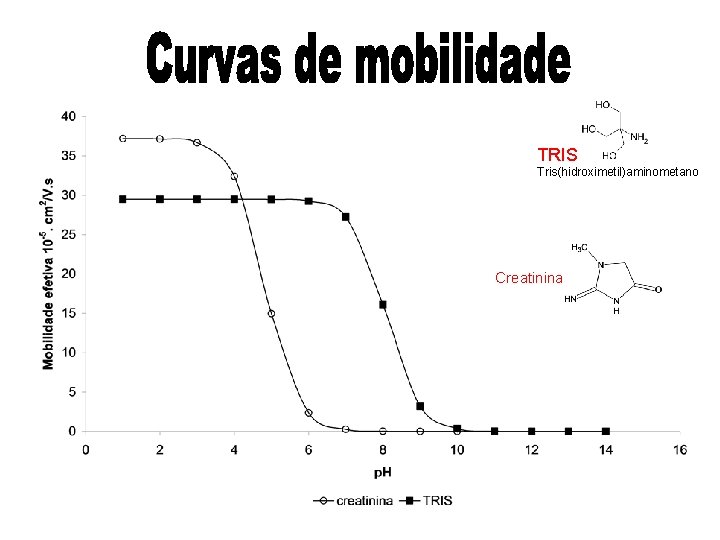
TRIS Tris(hidroximetil)aminometano Creatinina

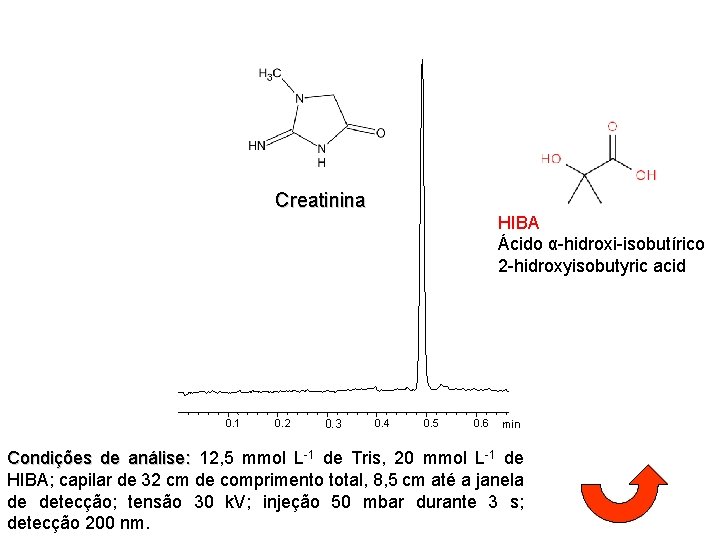
Creatinina HIBA Ácido α-hidroxi-isobutírico 2 -hidroxyisobutyric acid 0. 1 0. 2 0. 3 0. 4 0. 5 0. 6 min Condições de análise: 12, 5 mmol L-1 de Tris, 20 mmol L-1 de HIBA; capilar de 32 cm de comprimento total, 8, 5 cm até a janela de detecção; tensão 30 k. V; injeção 50 mbar durante 3 s; detecção 200 nm.


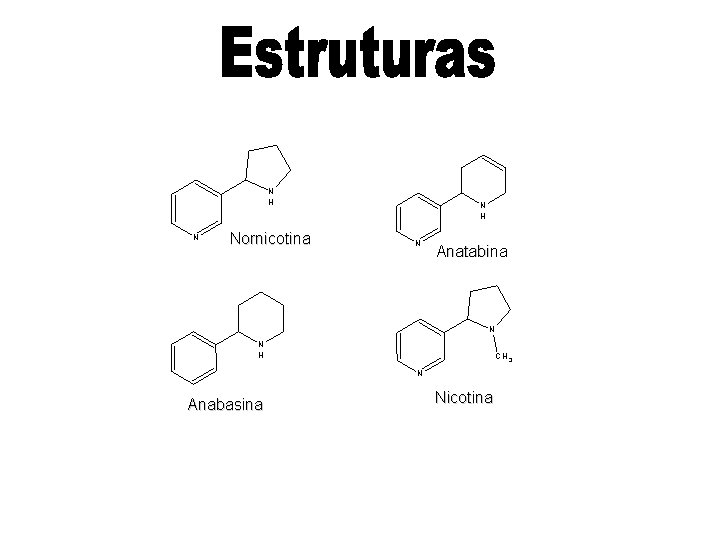
N H N Nornicotina N H N Anatabina N N H CH 3 N Anabasina Nicotina



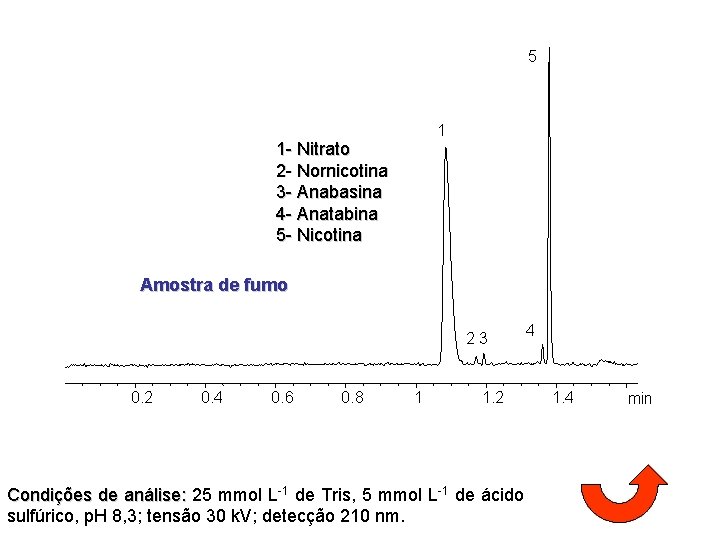
5 1 1 - Nitrato 2 - Nornicotina 3 - Anabasina 4 - Anatabina 5 - Nicotina Amostra de fumo 23 0. 2 0. 4 0. 6 0. 8 1 1. 2 Condições de análise: 25 mmol L-1 de Tris, 5 mmol L-1 de ácido sulfúrico, p. H 8, 3; tensão 30 k. V; detecção 210 nm. 4 1. 4 min

A A osm B B Mobilidades muito próximas osm

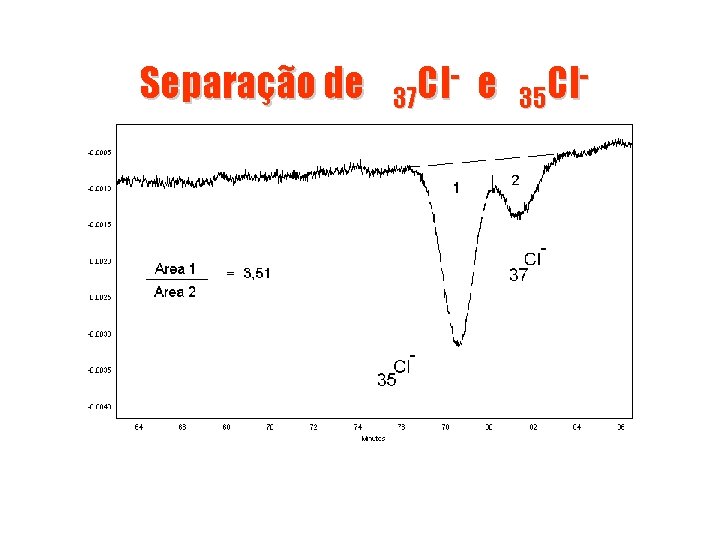
Separação de - e Cl 37 Cl 35

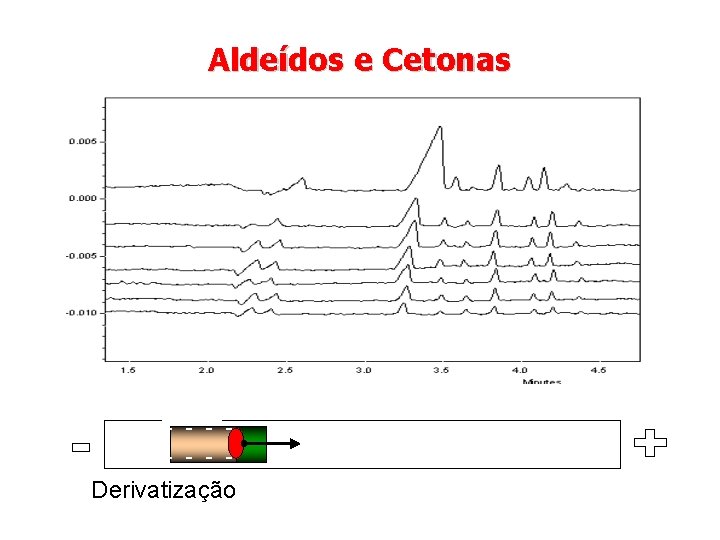
Aldeídos e Cetonas - - - -- - - Derivatização