Equilibrio Qumico Velocidade V 2 Velocidade V 1

Equilibrio Químico

Velocidade V 2 Velocidade V 1

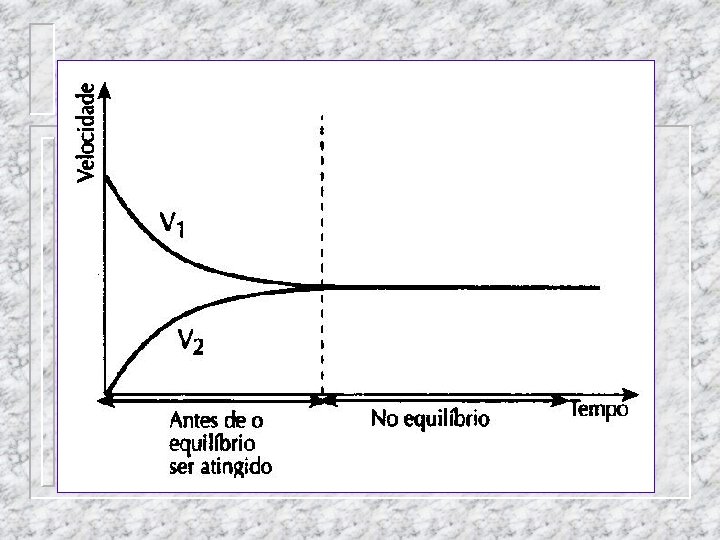
O equilíbrio é o resultado final de dois processos opostos com velocidades iguais A Reação direta Reação inversa B V 1 = V 2 Esse tipo de processo reversível é chamado de Equilíbrio Químico e este equilíbrio pode ser deslocado para qualquer um dos lados.
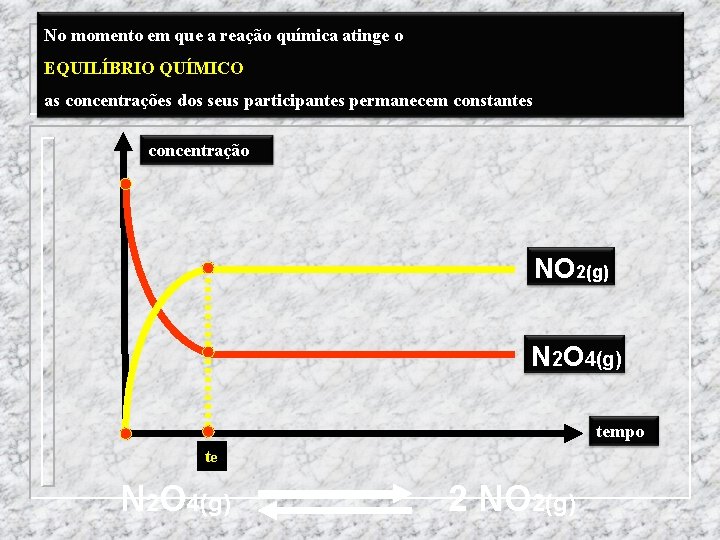
No momento em que a reação química atinge o EQUILÍBRIO QUÍMICO as concentrações dos seus participantes permanecem constantes concentração NO 2(g) N 2 O 4(g) tempo te N 2 O 4(g) 2 NO 2(g)

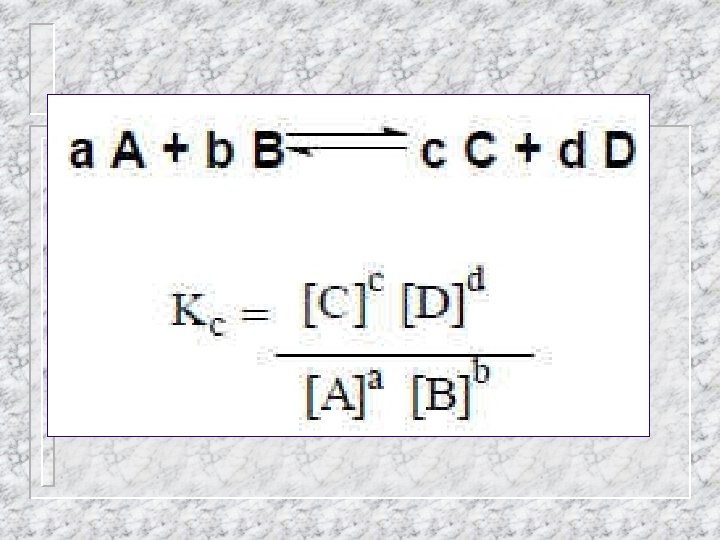

Ex. 1 - O gás fosgênio (COCl 2) foi utilizado como arma química na 1ª Guerra Mundial; em seguida, na Etiópia durante o seu conflito com a Itália. Esse gás foi abandonado como arma em razão de sua baixa toxicidade e por apresentar odor característico. O fosgênio pode ser obtido pela reação CO(g) + Cl 2(g) ⇌ COCl 2(g) a) Represente a expressão da constante de equilíbrio da reação e a sua unidade. b) Represente o gráfico da concentração de CO(g) e COCl 2(g) em função do tempo, considerando que a concentração do reagente é maior que a concentração do produto no equilíbrio. c) A expressão da constante de equilíbrio para uma reação hipotética é K(eq) = ([B][C])/[A]2 Calcule a constante de equilíbrio. (As concentrações no equilíbrio, em mol/L, são: [A] = 0, 1 , [B] = 0, 2 e [C] = 0, 8)
![a) K = [COCl 2]/([CO]. [Cl 2]) (mol/. L)-1. c) K = (0, 2 a) K = [COCl 2]/([CO]. [Cl 2]) (mol/. L)-1. c) K = (0, 2](http://slidetodoc.com/presentation_image_h2/44469ecad04e9ead80429ec60d3800b5/image-9.jpg)
a) K = [COCl 2]/([CO]. [Cl 2]) (mol/. L)-1. c) K = (0, 2 x 0, 8)/(0, 1)2 = 16. b)
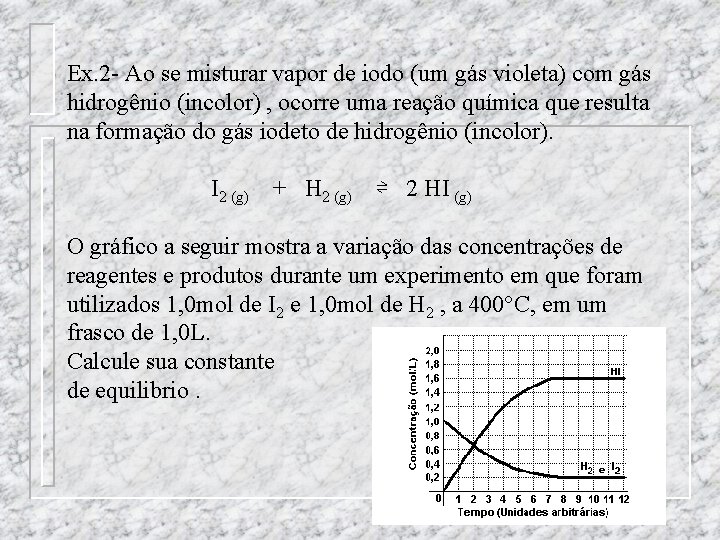
Ex. 2 - Ao se misturar vapor de iodo (um gás violeta) com gás hidrogênio (incolor) , ocorre uma reação química que resulta na formação do gás iodeto de hidrogênio (incolor). I 2 (g) + H 2 (g) ⇌ 2 HI (g) O gráfico a seguir mostra a variação das concentrações de reagentes e produtos durante um experimento em que foram utilizados 1, 0 mol de I 2 e 1, 0 mol de H 2 , a 400°C, em um frasco de 1, 0 L. Calcule sua constante de equilibrio.
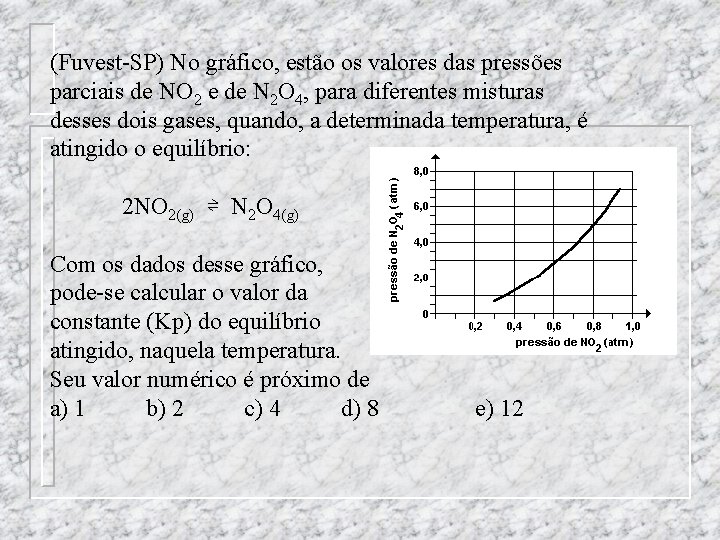
(Fuvest-SP) No gráfico, estão os valores das pressões parciais de NO 2 e de N 2 O 4, para diferentes misturas desses dois gases, quando, a determinada temperatura, é atingido o equilíbrio: 2 NO 2(g) ⇌ N 2 O 4(g) Com os dados desse gráfico, pode-se calcular o valor da constante (Kp) do equilíbrio atingido, naquela temperatura. Seu valor numérico é próximo de a) 1 b) 2 c) 4 d) 8 e) 12
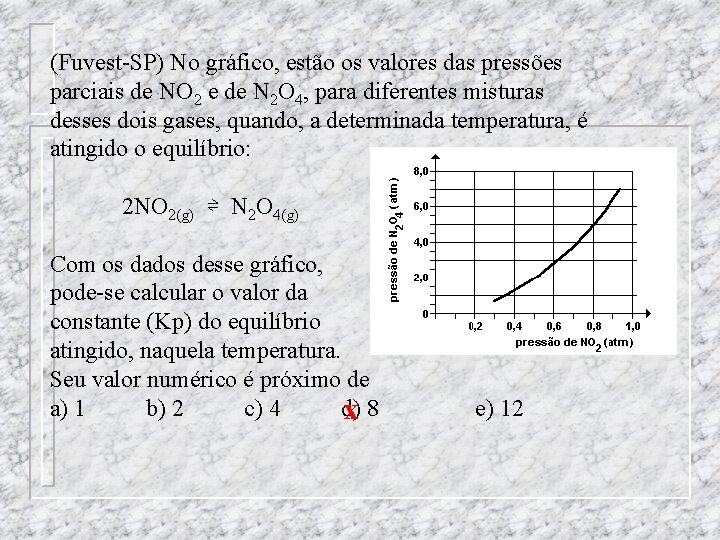
(Fuvest-SP) No gráfico, estão os valores das pressões parciais de NO 2 e de N 2 O 4, para diferentes misturas desses dois gases, quando, a determinada temperatura, é atingido o equilíbrio: 2 NO 2(g) ⇌ N 2 O 4(g) Com os dados desse gráfico, pode-se calcular o valor da constante (Kp) do equilíbrio atingido, naquela temperatura. Seu valor numérico é próximo de a) 1 b) 2 c) 4 d) x 8 e) 12
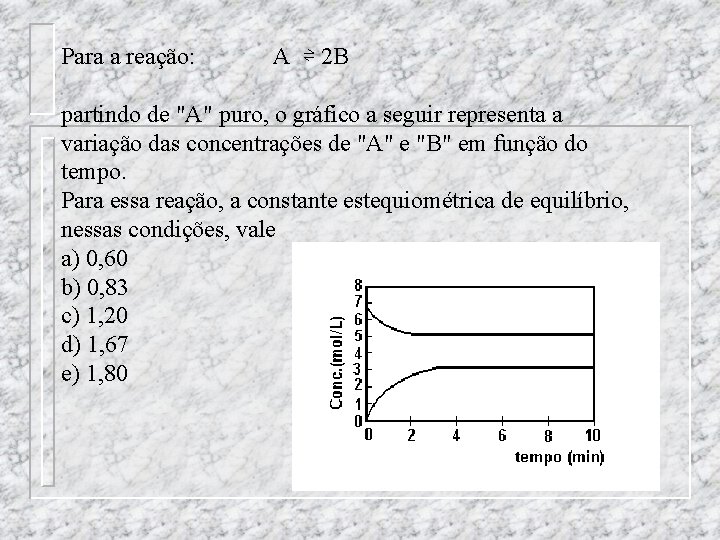
Para a reação: A ⇌ 2 B partindo de "A" puro, o gráfico a seguir representa a variação das concentrações de "A" e "B" em função do tempo. Para essa reação, a constante estequiométrica de equilíbrio, nessas condições, vale a) 0, 60 b) 0, 83 c) 1, 20 d) 1, 67 e) 1, 80
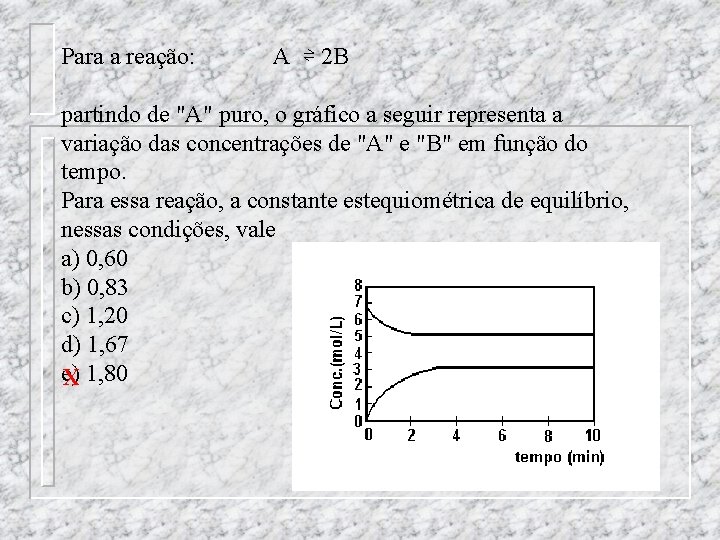
Para a reação: A ⇌ 2 B partindo de "A" puro, o gráfico a seguir representa a variação das concentrações de "A" e "B" em função do tempo. Para essa reação, a constante estequiométrica de equilíbrio, nessas condições, vale a) 0, 60 b) 0, 83 c) 1, 20 d) 1, 67 e) X 1, 80
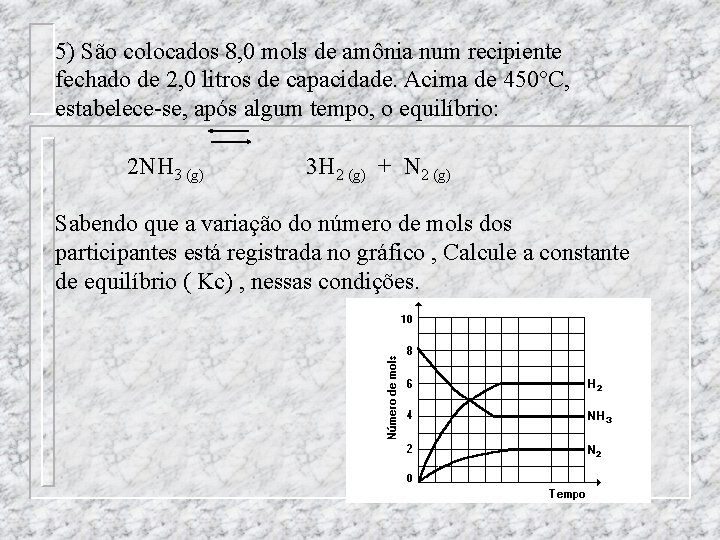
5) São colocados 8, 0 mols de amônia num recipiente fechado de 2, 0 litros de capacidade. Acima de 450°C, estabelece-se, após algum tempo, o equilíbrio: 2 NH 3 (g) 3 H 2 (g) + N 2 (g) Sabendo que a variação do número de mols dos participantes está registrada no gráfico , Calcule a constante de equilíbrio ( Kc) , nessas condições.

Ex. 6) Considerar o equilíbrio Fe 3 O 4 (s) + 4 H 2 (g) 3 Fe (s) + 4 H 2 O(g) a 150°C em recipiente fechado. Escrever a expressão da constante de equilíbrio (Kc) da reação.

Deslocando o equilíbrio Um equilíbrio não se desloca por vontade própria. Fatores externos forçarão o deslocamento para um dos lados. Obs. : Deslocar para direita aumentar Produtos Deslocar para esquerda aumentar reagentes Os fatores são: Temperatura Concentração e Pressão

Principio de Le Chatelier Em 1888, Henry Louis Le Chatelier enunciou um princípio que permite prever o sentido em que o equilíbrio será deslocado Princípio de Le Chatelier: Quando um equilibrio é alterado por um fator externo, ocorre um deslocamento no sentido de anular a alteração

Influência da Temperatura Um aumento da temperatura desloca o equilíbrio no sentido da reação endotérmica, e uma diminuição da temperatura desloca o equilíbrio no sentido da reação exotérmica. Ex. : Abaixamento da temperatura 2 H 2(g) + O 2(g) exotérmica 2 H 2 O(g) H < 0 endotérmica Elevação da temperatura

Deslocamento do Equilíbrio pela temperatura Frio 2 NO 2(g) castanho exotérmica endotérmica Quente N 2 O 4(g) incolor H = - 14, 5 KJ/mol
![Influência da Concentração A B Alteração Aumentando [A] ou diminuindo [B] Diminuindo [A] ou Influência da Concentração A B Alteração Aumentando [A] ou diminuindo [B] Diminuindo [A] ou](http://slidetodoc.com/presentation_image_h2/44469ecad04e9ead80429ec60d3800b5/image-21.jpg)
Influência da Concentração A B Alteração Aumentando [A] ou diminuindo [B] Diminuindo [A] ou aumentando [B] Deslocamento Direita Esquerda

Co. Cl 2 + 6 H 2 O Azul Co. Cl 2. 6 H 2 O Rosa

Influência da pressão O aumento de pressão desloca o equilíbrio do lado com menor número de moléculas( menor volume) e uma diminuição da pressão desloca o equilíbrio para o lado de maior número de moléculas (maior volume) Ex. : N 2 O 4(g) 2 NO 2(g) incolor 1 volume Castanho-escuro 2 volumes

Ação do catalisador : substância que diminui a Energia de ativação No caso dos equilíbrios, o catalisador diminui igualmente as energias de ativação nos dois sentidos. Com isso, ele aumenta a velocidade da reação direta e também da reação inversa. Podemos concluir, portanto, que o catalisador não afeta um equilíbrio. Ele apenas faz com que o equilíbrio seja atingido em menor tempo.
- Slides: 24