AINE EHITUS MRGAMINE MRGAMINE JA MITTEMRGAMINE KAPILLAARSUS DIFUSIOON
























- Slides: 52

AINE EHITUS

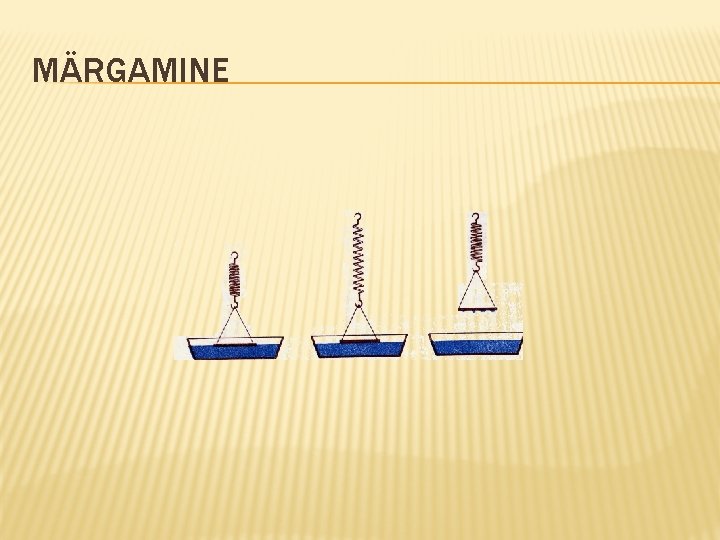
MÄRGAMINE

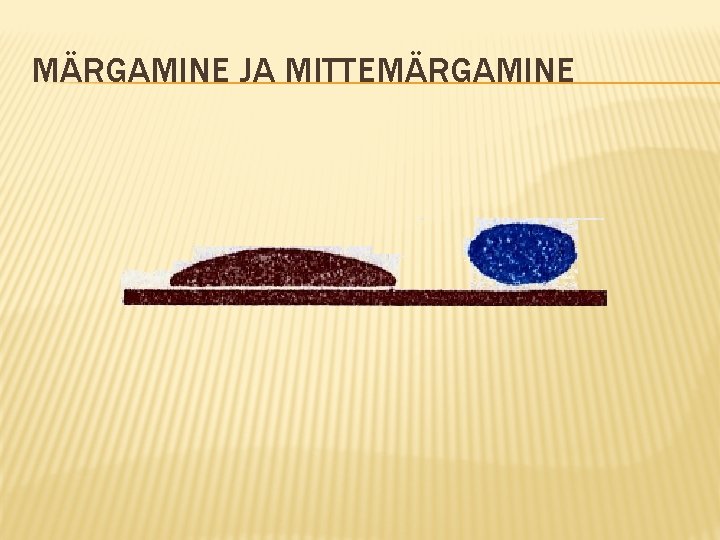
MÄRGAMINE JA MITTEMÄRGAMINE

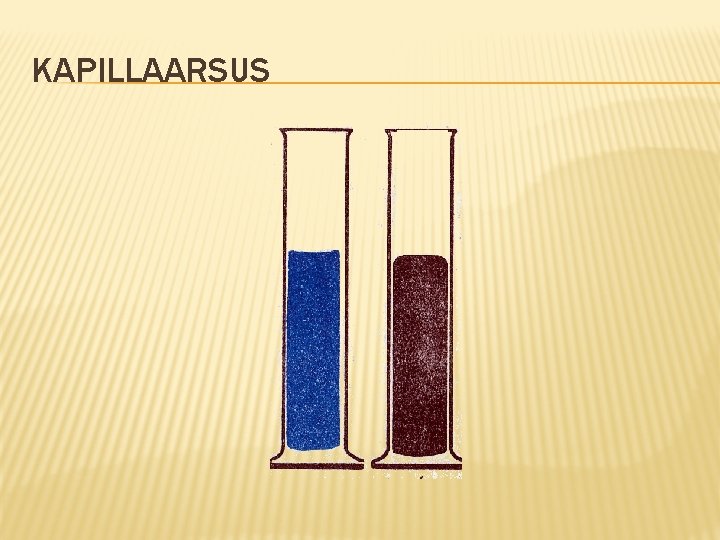
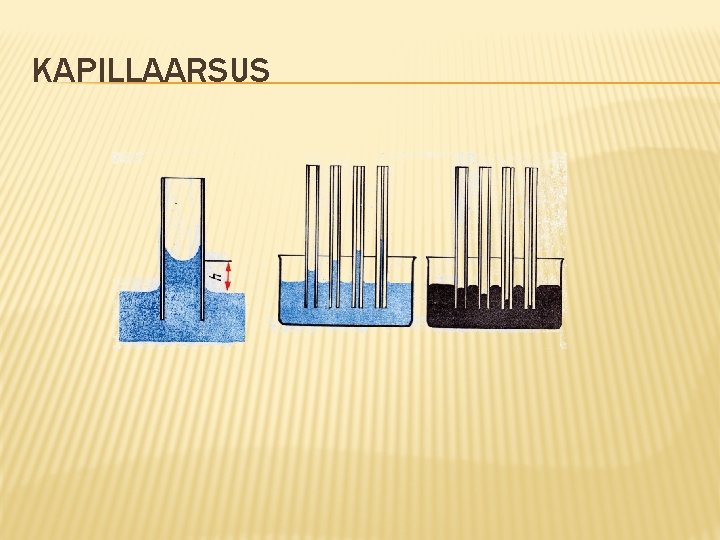
KAPILLAARSUS

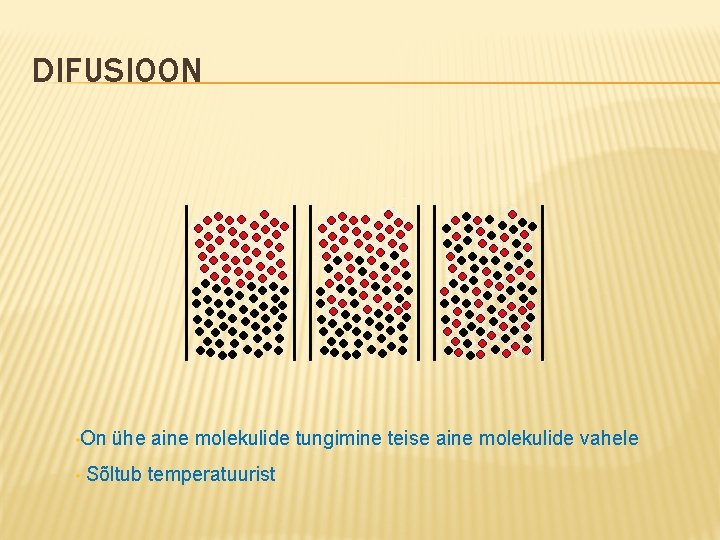
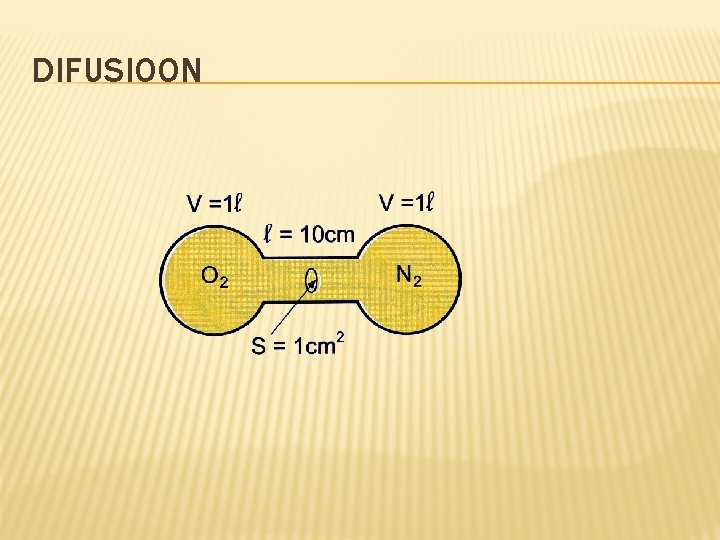
DIFUSIOON • On • ühe aine molekulide tungimine teise aine molekulide vahele Sõltub temperatuurist

DIFUSIOON

KAPILLAARSUS

DIFUSIOON VEDELIKES

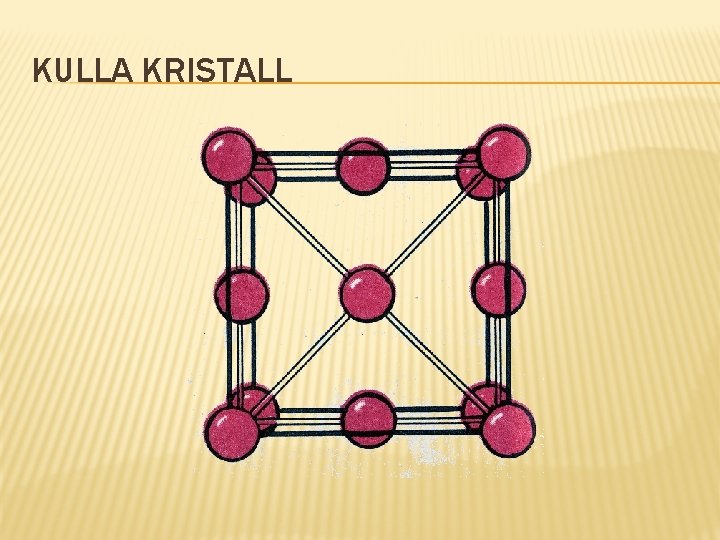
KULLA KRISTALL

KULLA KRISTALL ELEKTROMMIKROSKOOBIS

KULLA MOLEKULID

VEDELIKU SOOJENDAMINE

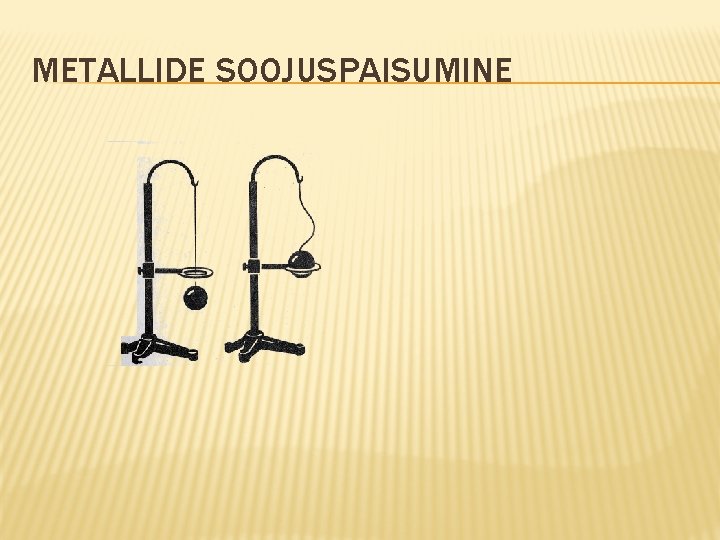
METALLIDE SOOJUSPAISUMINE

SOOJENDADES GAASI RUUMALA SUURENEB

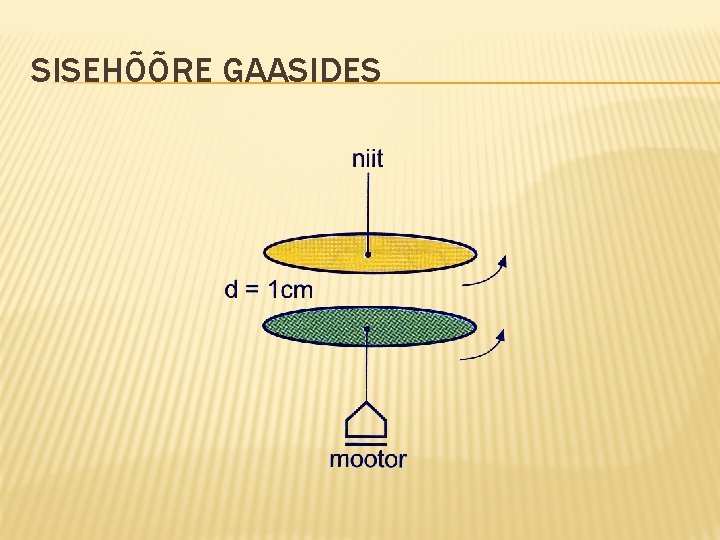
SISEHÕÕRE GAASIDES

KATSE TAHKE AINEGA

GAAS

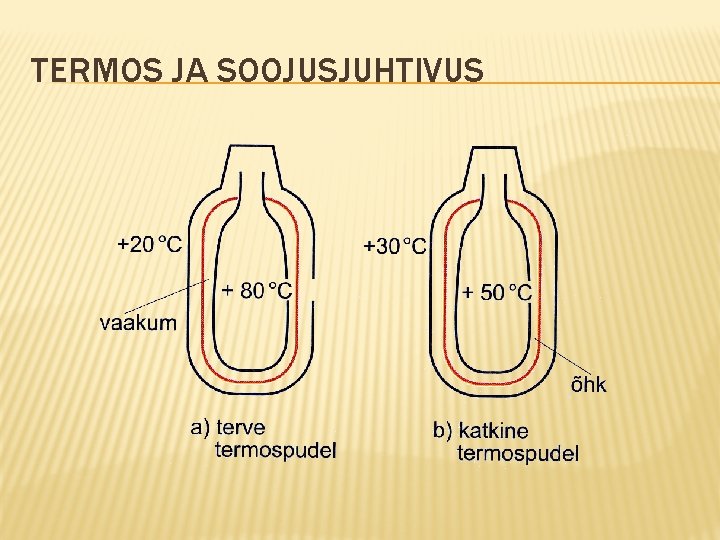
TERMOS JA SOOJUSJUHTIVUS

DIFUSIOON ÕHUS

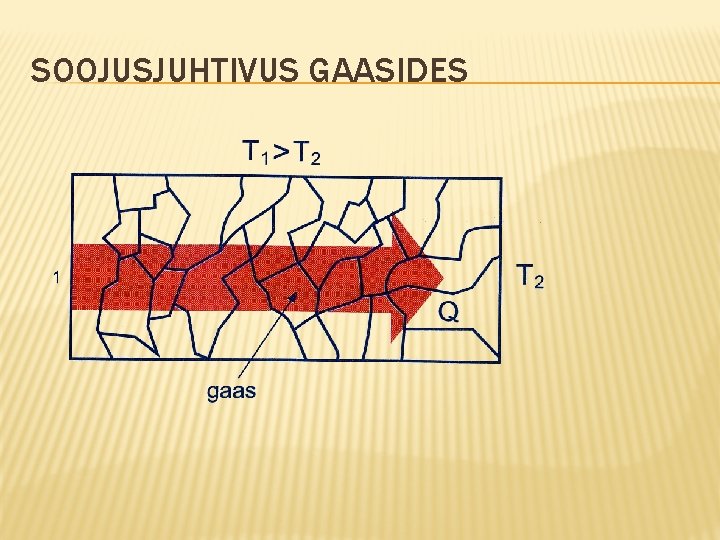
SOOJUSJUHTIVUS GAASIDES

KÄRGTELLIS – HEA SOOJUSE ISOLATSIOON

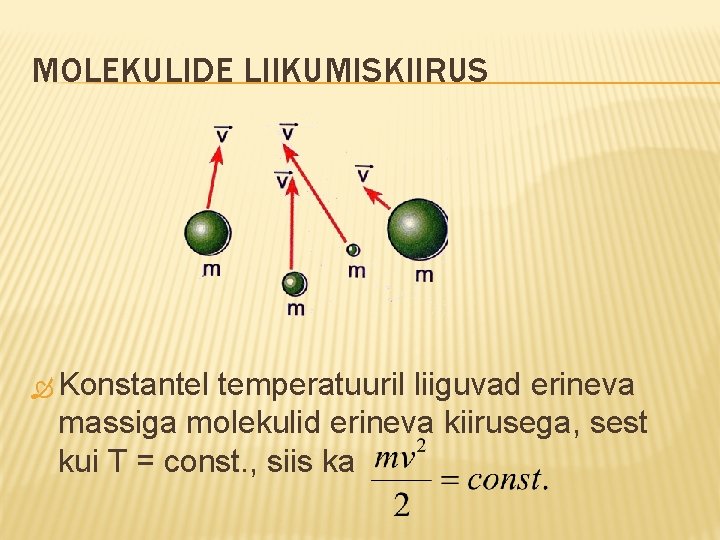
MOLEKULIDE LIIKUMISKIIRUS Konstantel temperatuuril liiguvad erineva massiga molekulid erineva kiirusega, sest kui T = const. , siis ka

DIFUSIOON

KASUKAS HOIAB SOOJUST

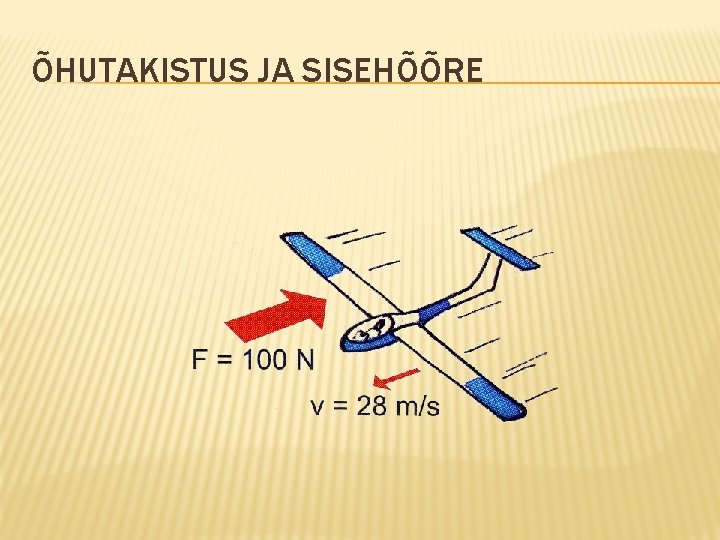
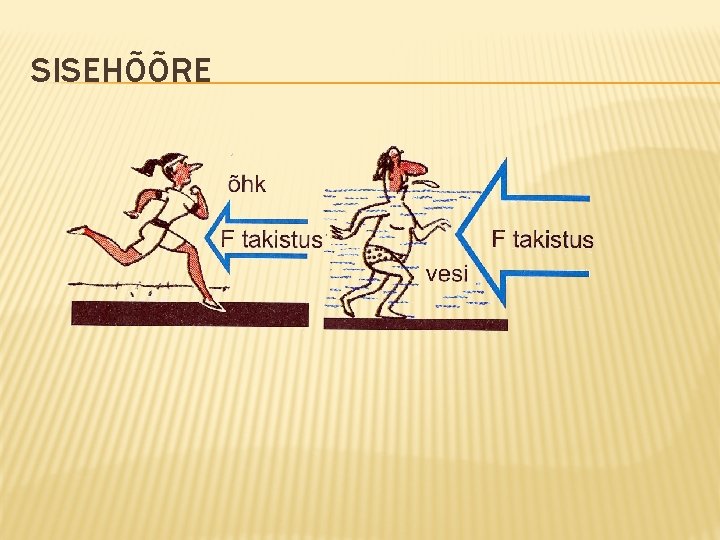
ÕHUTAKISTUS JA SISEHÕÕRE

ÕHUTAKISTUS JA SISEHÕÕRE

SISEHÕÕRE JA TEHNIKA Concorde Ty 144 Tupolev

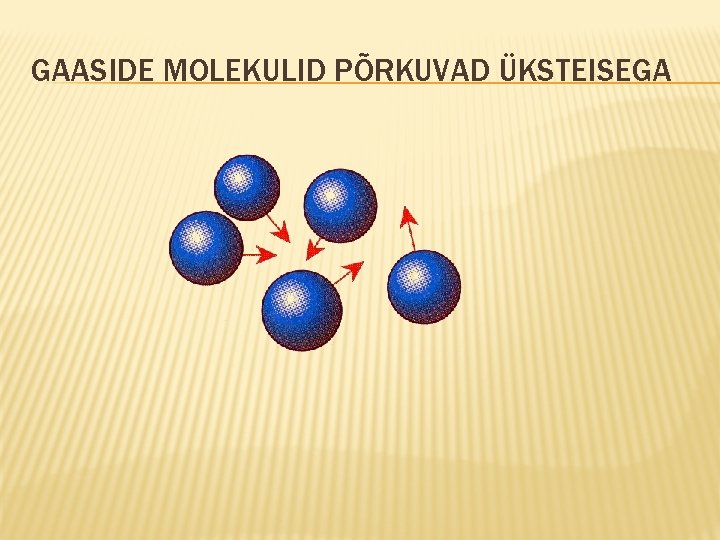
GAASIDE MOLEKULID PÕRKUVAD ÜKSTEISEGA

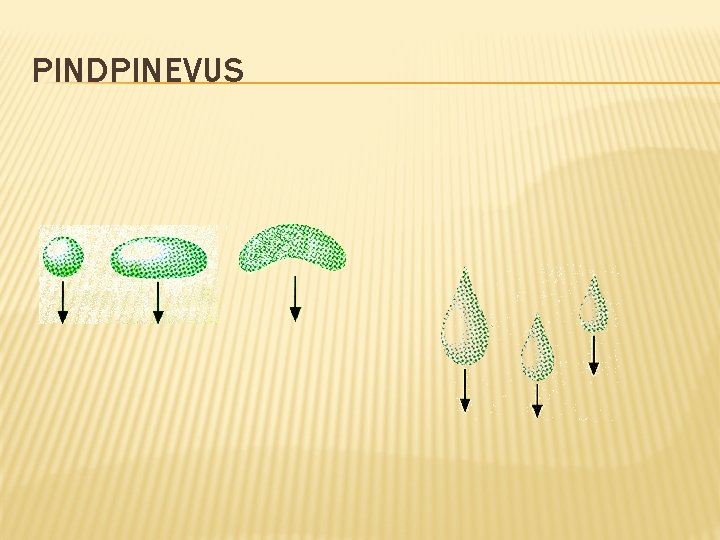
PINDPINEVUS

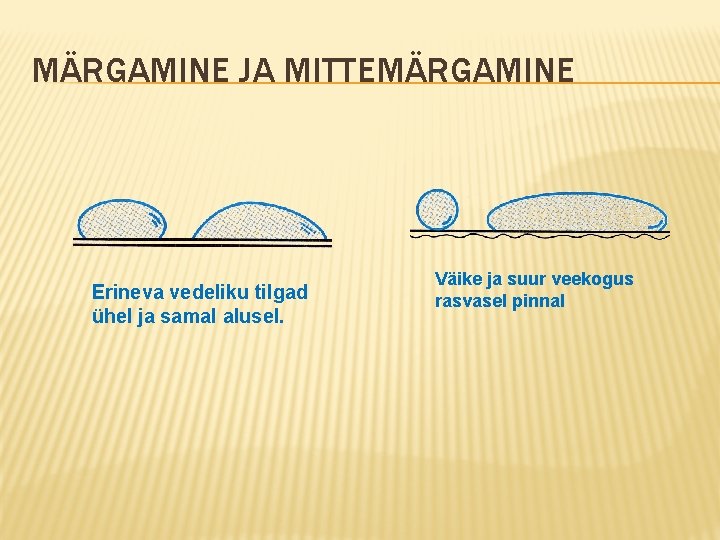
MÄRGAMINE JA MITTEMÄRGAMINE Erineva vedeliku tilgad ühel ja samal alusel. Väike ja suur veekogus rasvasel pinnal

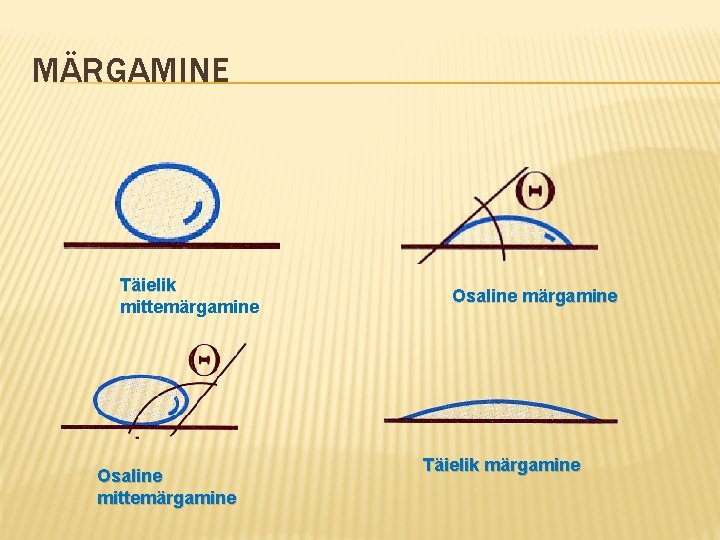
MÄRGAMINE Täielik mittemärgamine Osaline märgamine Täielik märgamine

SISEHÕÕRE

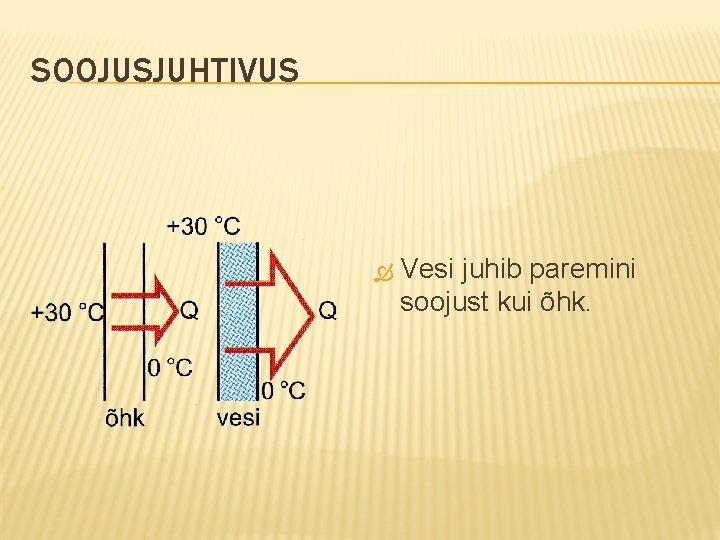
SOOJUSJUHTIVUS Vesi juhib paremini soojust kui õhk.

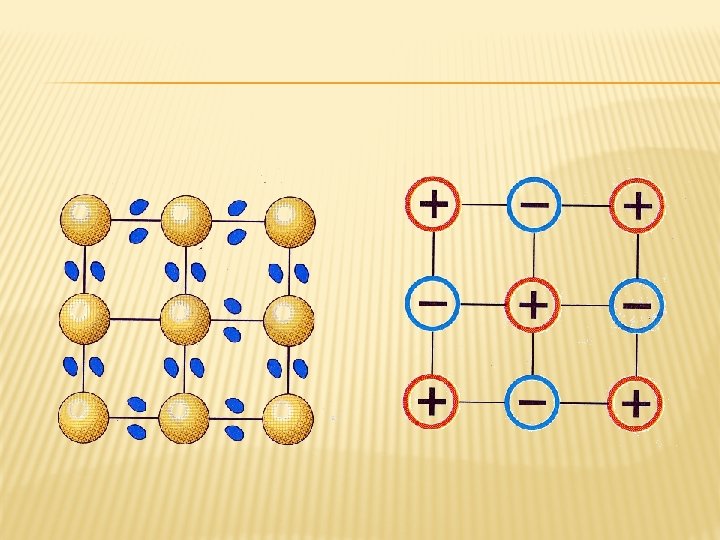
TAHKE AINE STRUKTUUR

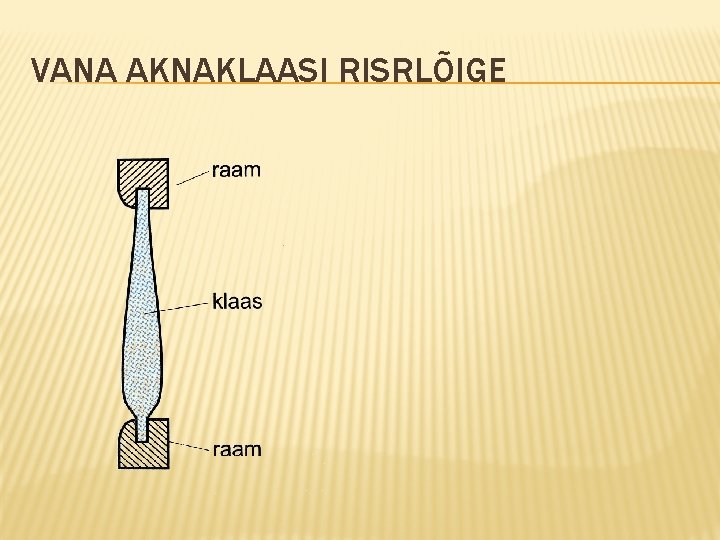
VANA AKNAKLAASI RISRLÕIGE



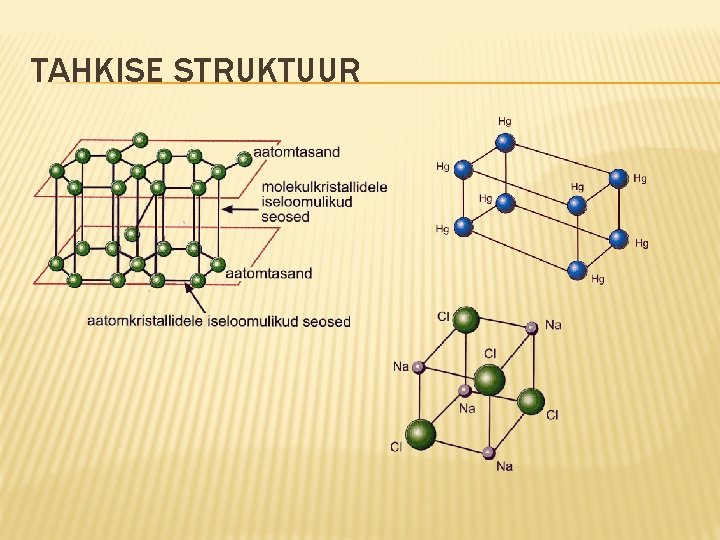
TAHKISE STRUKTUUR


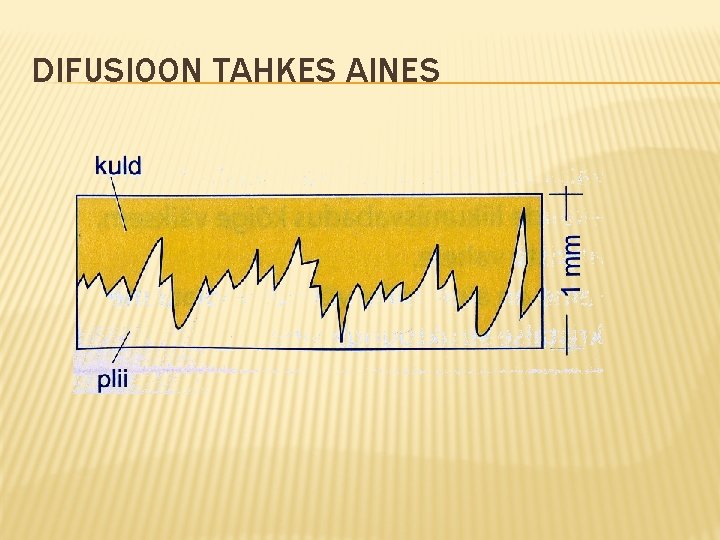
DIFUSIOON TAHKES AINES

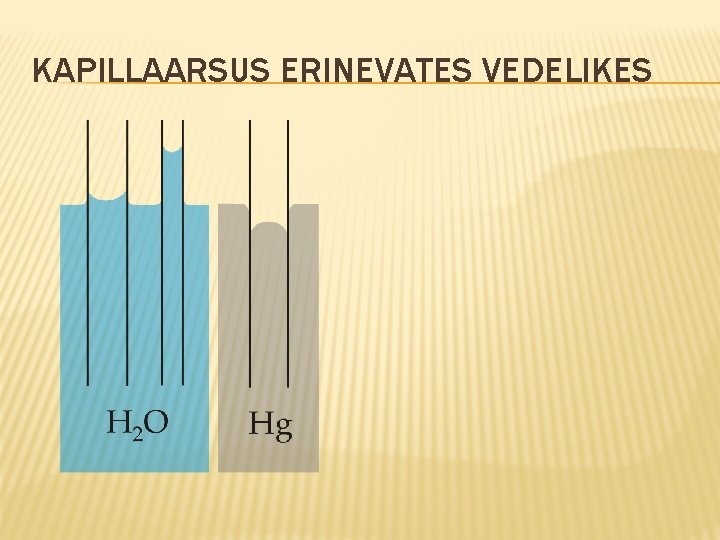
KAPILLAARSUS ERINEVATES VEDELIKES

ÜLEKANDENÄHTUSED GAASIDES Soojusjuhtivus. Soojusülekanne molekulide omavaheliste põrgete kaudu. Toimub väga aeglaselt, sest gaasid on väga halva soojusjuhtivusega. Sellel põhineb poorsete materjalide kasutamine soojusisolatsioonis.

ÜLEKANDENÄHTUSED GAASIDES Sisehõõre. See on tingitud gaasimolekulide kaasahaaramisest gaasis liikuva keha poolt. Osa keha impulsist kandub üle gaasi molekulidele, keha impulss väheneb. Takistusjõud sõltub Keha kujust Keha kiirusest Teadusharu, mis tegeleb kehade liikumisega gaasides nimetatakse aerodünaamikaks

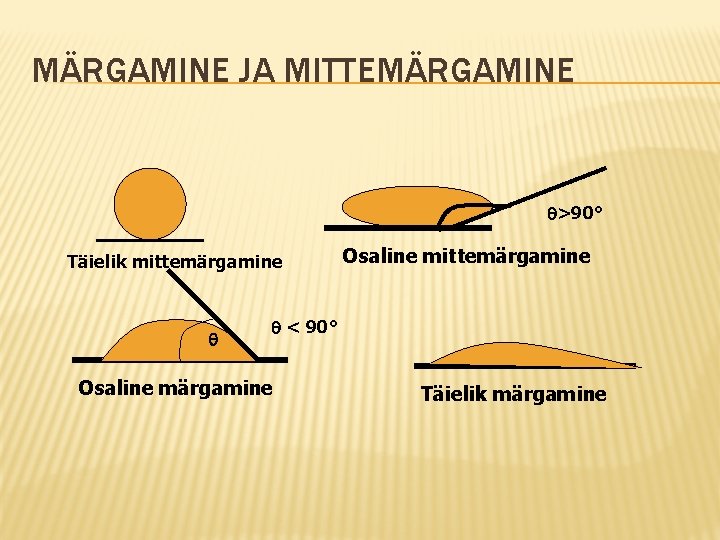
MÄRGAMINE JA MITTEMÄRGAMINE >90° Täielik mittemärgamine Osaline mittemärgamine < 90° Osaline märgamine Täielik märgamine

VEDELIKUD Tiheduselt lähemal tahkele kui gaasilisele olekule Vedeliku omaduseks on voolata, kuju on kergelt muudetav. Vedelik on raskesti kokku surutav Molekulid saavad liikuda vaid molekulide mõõtmetega võrreldavates piirides Molekulid paiknevad enamasti korrapäratult(v. a. vedelkristallid) Vedelikele on omane pindpinevus

PINDPINEVUS Vedeliku omadus kokku tõmbuda ja omandada võimalikult väikest pindala. Selle tulemusena üritab vedelik võtta kera kuju. Pindpinevusjõud F = l, kus l on pinna pikkus ja pindpinevustegur, pindpinevusjõud on suunatud piki vedeliku pinda Pindpinevusega on seotud märgamine ja mittemärgamine.

ÜLEKANDENÄHTUSED VEDELIKES Difusioon vedelikes on aeglasem kui gaasides. Soojusjuhtivus. Vedelikud on paremad soojusjuhid kui gaasid. Sisehõõre on vedelikes tunduvalt suurem kui gaasides.

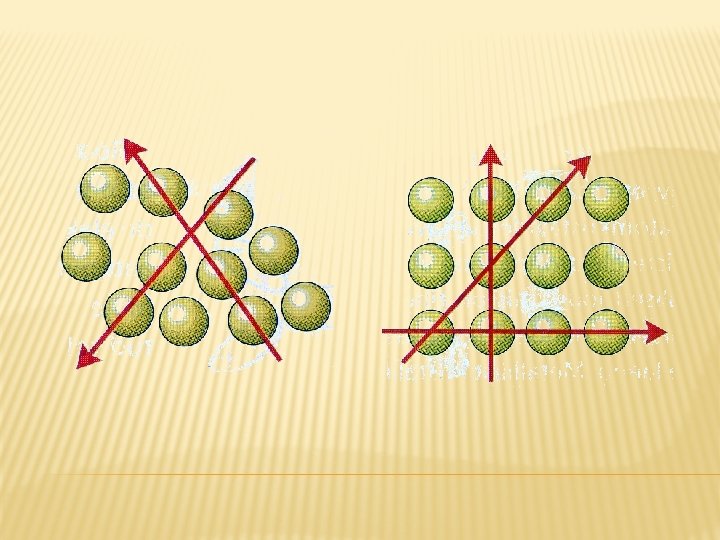
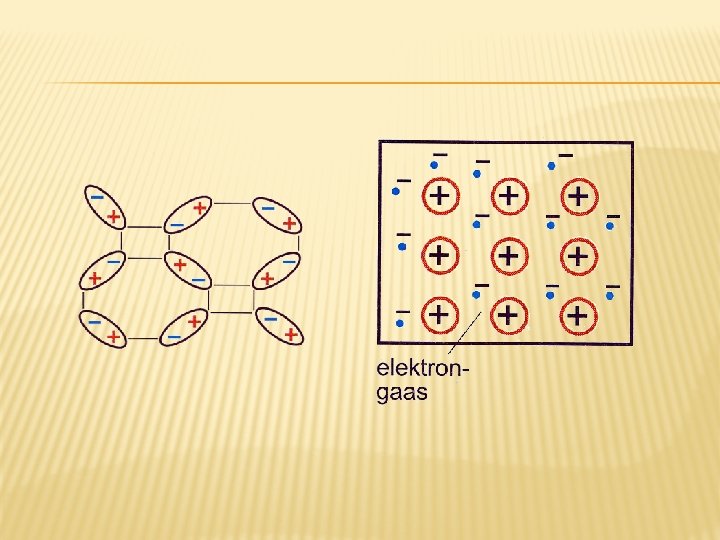
TAHKED KEHAD Tahkised. Tahked ained millel on korrapärane e. kristallstruktuur. (süsinik, jää jne) On mono- ja polükristallid. Kristallid on anisotroopsed(omadused sõltuvad suunast) Amorfsed ained. Tahked ained millel kristallstruktuur puudub. (klaas, pigi, plastmassid) Voolavad Isotroopsed

ÜLEKANDENÄHTUSED TAHKISTES Difusioon. Esineb ka tahkistes, kuid vähesel määral. Soojusjuhtivus. Tahkised on head soojusjuhid, eriti metallid. Sõltub suunast. Sisehõõrdumisest tahkiste puhul rääkida ei saa. Amorfsed kehad aga on voolavad ja nende puhul saame sisehõõrdest rääkida.

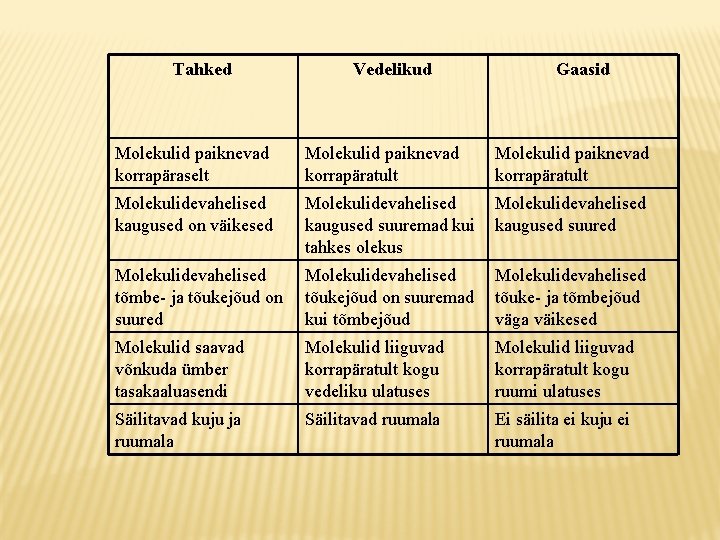
Tahked Vedelikud Gaasid Molekulid paiknevad korrapäraselt Molekulid paiknevad korrapäratult Molekulidevahelised kaugused on väikesed Molekulidevahelised kaugused suuremad kui tahkes olekus Molekulidevahelised kaugused suured Molekulidevahelised tõmbe- ja tõukejõud on suured Molekulidevahelised tõukejõud on suuremad kui tõmbejõud Molekulidevahelised tõuke- ja tõmbejõud väga väikesed Molekulid saavad võnkuda ümber tasakaaluasendi Molekulid liiguvad korrapäratult kogu vedeliku ulatuses Molekulid liiguvad korrapäratult kogu ruumi ulatuses Säilitavad kuju ja ruumala Säilitavad ruumala Ei säilita ei kuju ei ruumala

FAASID Aine võib esineda kolmes olekus – tahkes, vedelas ja gaasilises. Neid olekuid nimetatakse aine agregaatolekuteks. Ühes ja samas agregaatolekus võivad aine omadused olla erinevad. Erinevate omadustega olekuid nimetatakse faasideks. Faase on rohkem kui agregaatolekuid. Üleminekut ühest faasist teise nimetatakse faasisiirdeks.

Tänan tähelepanu eest! ©anmet. rtg 2010