Universit degli Studi di Perugia Corso di Laurea










![NH 3 + H 2 O Kb = NH 4+ + OH- [NH 4+] NH 3 + H 2 O Kb = NH 4+ + OH- [NH 4+]](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-30.jpg)


![2 H 2 O Kc = H 3 + OH [H 3 O+] · 2 H 2 O Kc = H 3 + OH [H 3 O+] ·](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-42.jpg)
![[H 3 O+] = [OH-] = 1· 10 -7 M Nell'acqua pura, solo una [H 3 O+] = [OH-] = 1· 10 -7 M Nell'acqua pura, solo una](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-43.jpg)

![+ p. H = - log [H ] = - log [H 3 + + p. H = - log [H ] = - log [H 3 +](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-45.jpg)
![p. H dell’acqua [H 3 O+] = [OH-] = 1· 10 -7 M - p. H dell’acqua [H 3 O+] = [OH-] = 1· 10 -7 M -](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-46.jpg)
![Kw = [H 3 O+] · [OH-] = 1· 10 -14 M 2 Kw Kw = [H 3 O+] · [OH-] = 1· 10 -14 M 2 Kw](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-47.jpg)
![[H 3 O+] > 1· 10 -7 M p. H = 0 [H 3 [H 3 O+] > 1· 10 -7 M p. H = 0 [H 3](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-48.jpg)


![[H 3 O+] = 3, 2 · 10 -12 p. H = - log [H 3 O+] = 3, 2 · 10 -12 p. H = - log](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-51.jpg)
![[H 3 O+] = 1, 1 · 10 -4 p. H = - log [H 3 O+] = 1, 1 · 10 -4 p. H = - log](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-52.jpg)

- Slides: 53

Università degli Studi di Perugia Corso di Laurea in Medicina e Chirurgia Corso di Chimica e Biochimica I Modulo di Chimica Generale e Chimica Organica EQUILIBRIO ACIDO-BASE Pier Luigi Orvietani Dipartimento di Medicina Sperimentale - Sezione di Biochimica Email: pier. orvietani@unipg. it A. A: 2017 -2018

I soluti delle soluzioni acquose (soluzioni liquide) possono essere divisi in due grandi categorie: - elettroliti: sostanze che, una volta disciolte in acqua, danno luogo a soluzioni che conducono la corrente elettrica (dissociandosi in ioni positivi e negativi) negativi - non-elettroliti: sostanze che, in acqua, non producono ioni e quindi le loro soluzioni non conducono corrente elettrica

ELETTROLITI FORTI completamente ionizzati in soluzione Na. Cl Na+aq + Cl-aq Na 3 PO 4 + 3 Na + HCl H aq + PO 4 aq aq + Na. OH Na 3 - + Cl aq aq + OH aq

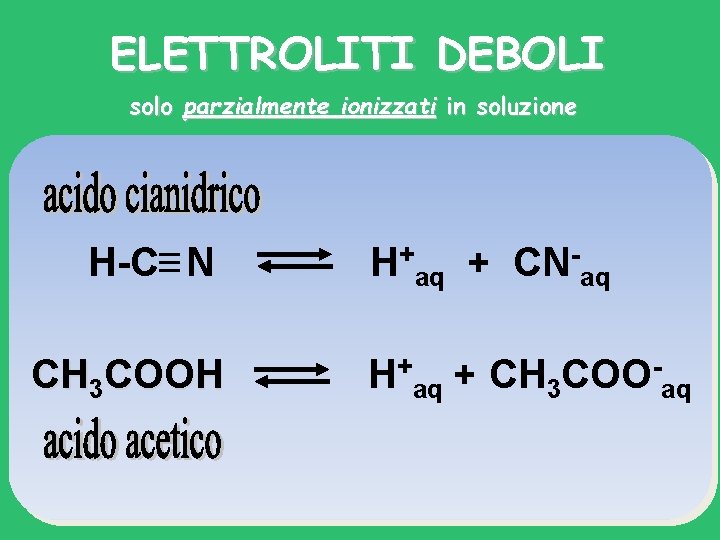
ELETTROLITI DEBOLI solo parzialmente ionizzati in soluzione H-C N H+aq + CN-aq + + CH COOCH 3 COOH H COOH aq 3 aq

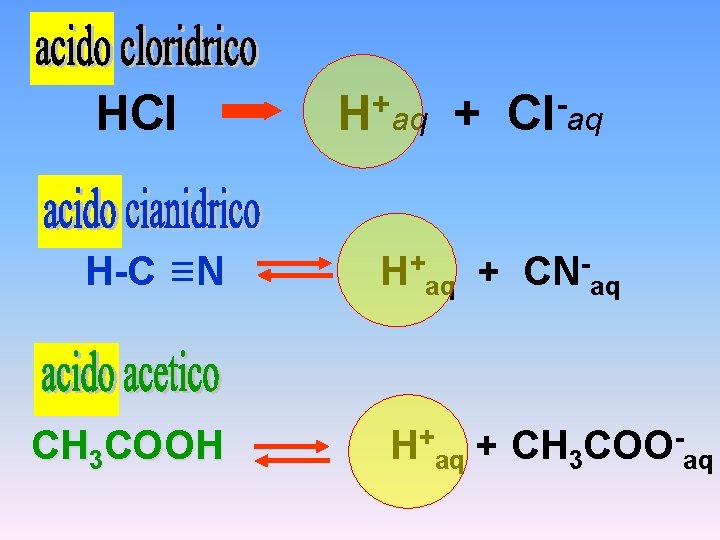
+ HCl H aq + Cl aq H-C N H+aq + CN-aq + + CH COOCH 3 COOH H COOH aq 3 aq

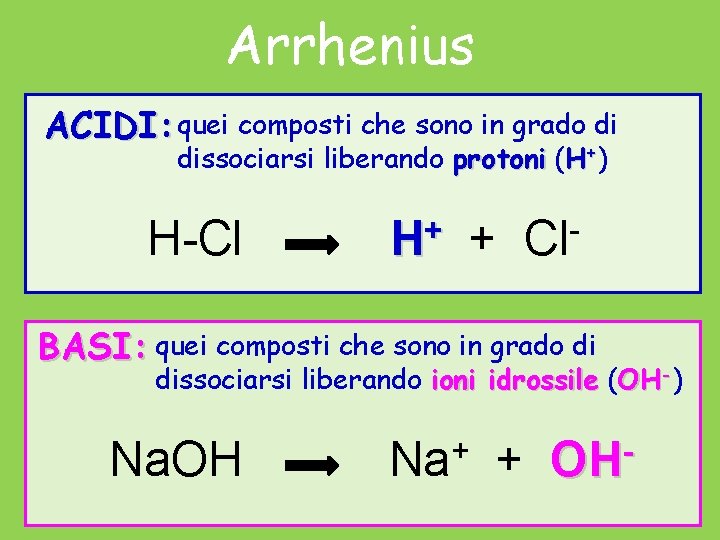
Arrhenius ACIDI: quei composti che sono in grado di dissociarsi liberando protoni (H+) H-Cl H+ + Cl- BASI: quei composti che sono in grado di dissociarsi liberando ioni idrossile (OH-) Na. OH + Na + OH

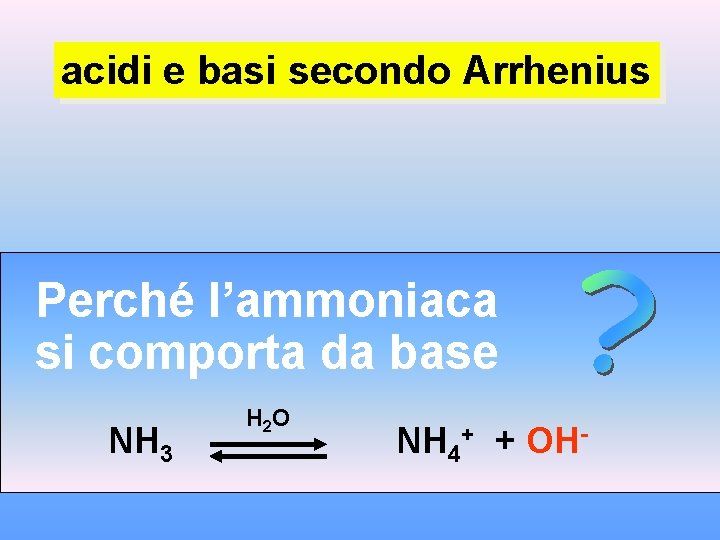
acidi e basi secondo Arrhenius Perché l’ammoniaca si comporta da base NH 3 H 2 O NH 4+ + OH-

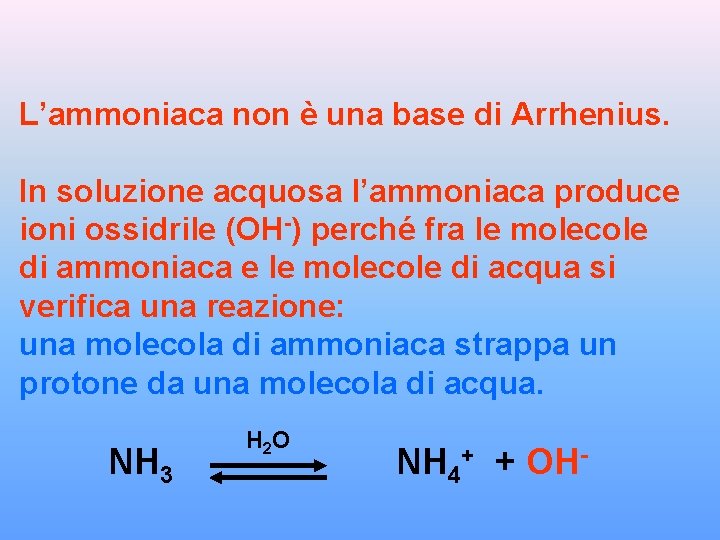
L’ammoniaca non è una base di Arrhenius. In soluzione acquosa l’ammoniaca produce ioni ossidrile (OH-) perché fra le molecole di ammoniaca e le molecole di acqua si verifica una reazione: una molecola di ammoniaca strappa un protone da una molecola di acqua. NH 3 H 2 O NH 4+ + OH-

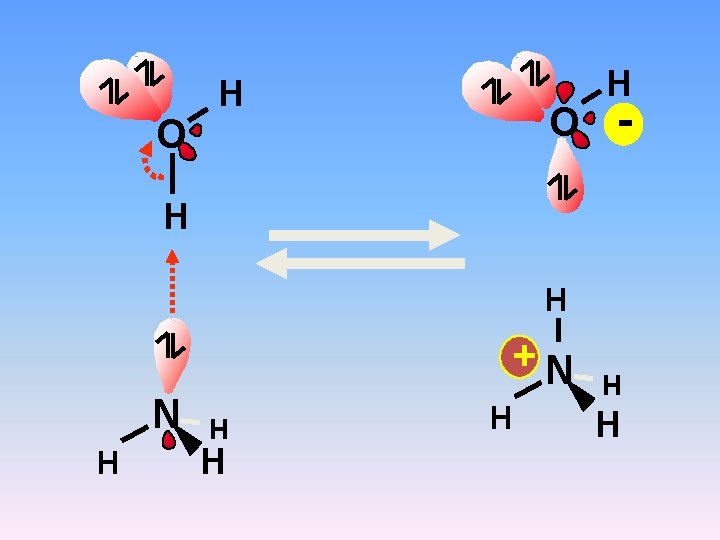
O H - H H N H +N H H H

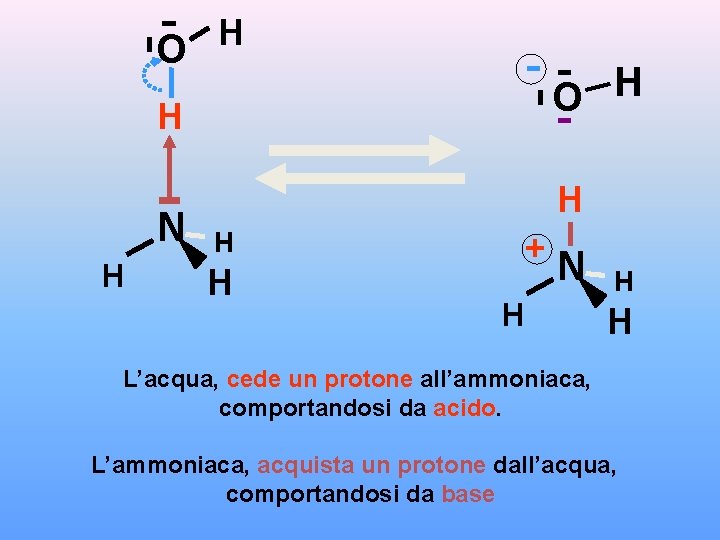
O H - H N H O H H + N H H H L’acqua, cede un protone all’ammoniaca, comportandosi da acido. L’ammoniaca, acquista un protone dall’acqua, comportandosi da base

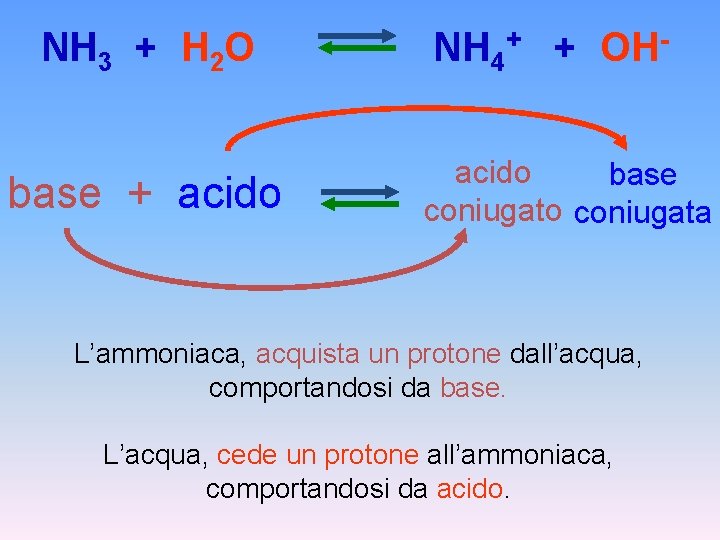
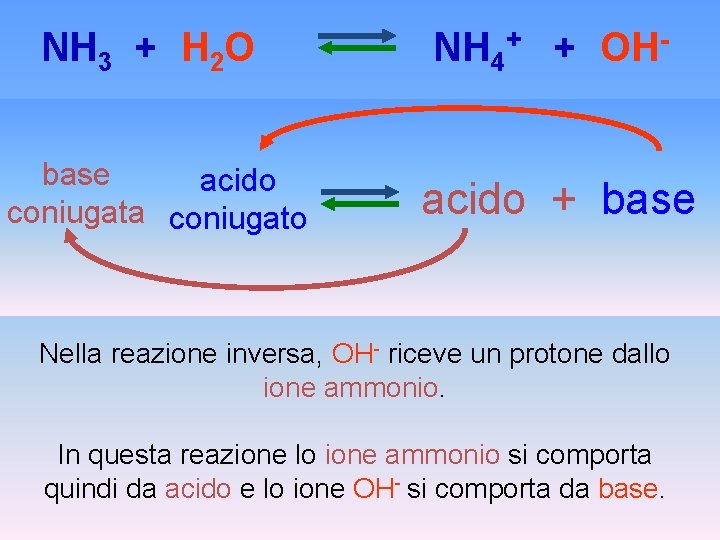
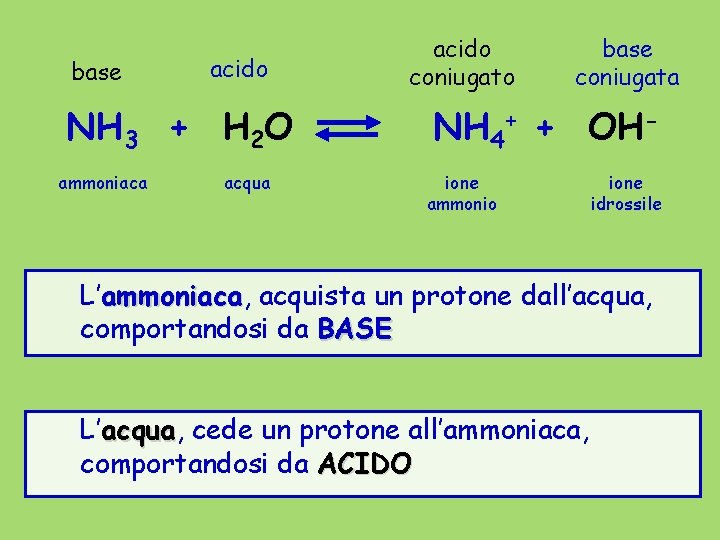
NH 3 + H 2 O NH 4+ + OH- base + acido base coniugato coniugata L’ammoniaca, acquista un protone dall’acqua, comportandosi da base. L’acqua, cede un protone all’ammoniaca, comportandosi da acido.

NH 3 + H 2 O NH 4+ + OHbase acido coniugata coniugato acido + base Nella reazione inversa, OH- riceve un protone dallo ione ammonio. In questa reazione lo ione ammonio si comporta quindi da acido e lo ione OH- si comporta da base.

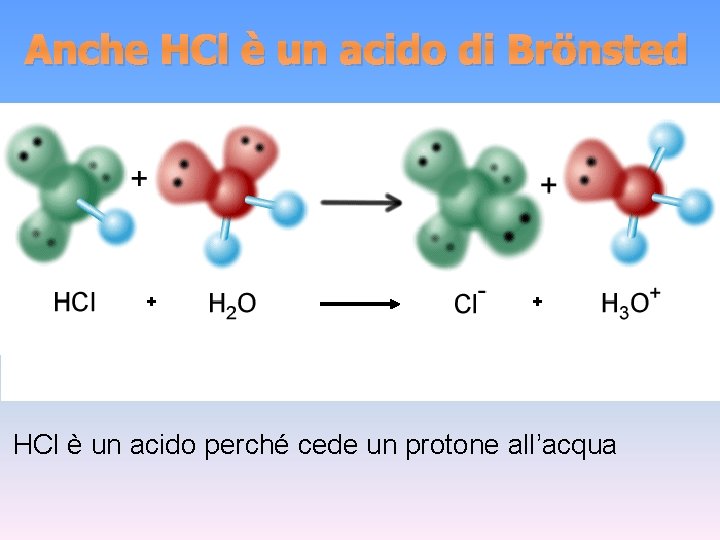
Anche HCl è un acido di Brönsted + + HCl è un acido perché cede un protone all’acqua

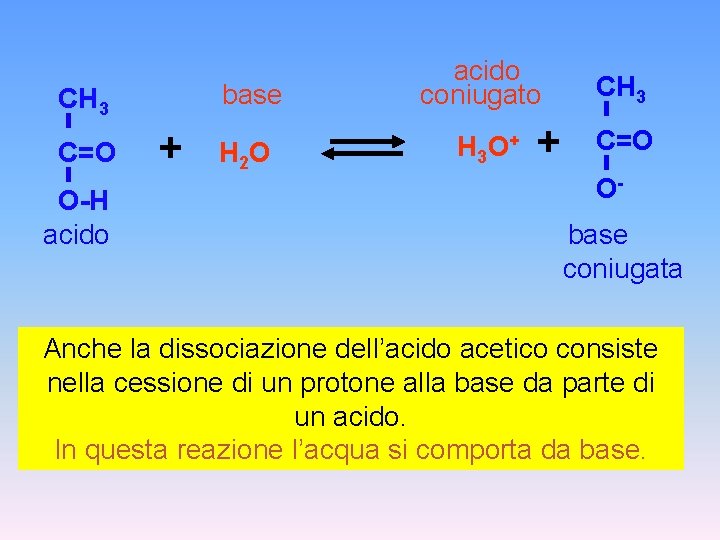
base CH 3 C=O O-H acido + H 2 O acido coniugato H 3 O+ + CH 3 C=O Obase coniugata Anche la dissociazione dell’acido acetico consiste nella cessione di un protone alla base da parte di un acido. In questa reazione l’acqua si comporta da base.

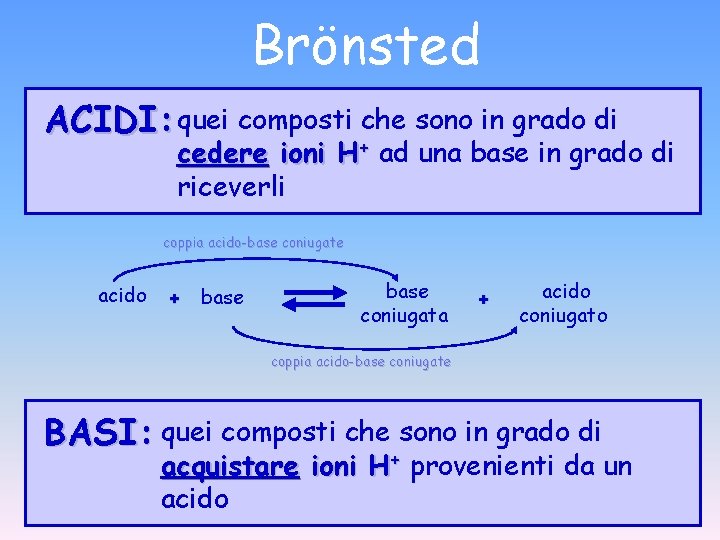
. . Bronsted ACIDI: quei composti che sono in grado di cedere ioni H+ ad una base in grado di riceverli coppia acido-base coniugate acido + base coniugata + acido coniugato coppia acido-base coniugate BASI: quei composti che sono in grado di acquistare ioni H+ provenienti da un acido

base acido NH 3 + H 2 O ammoniaca acqua acido coniugato base coniugata NH 4+ + OHione ammonio ione idrossile L’ammoniaca, ammoniaca acquista un protone dall’acqua, comportandosi da BASE L’acqua, acqua cede un protone all’ammoniaca, comportandosi da ACIDO

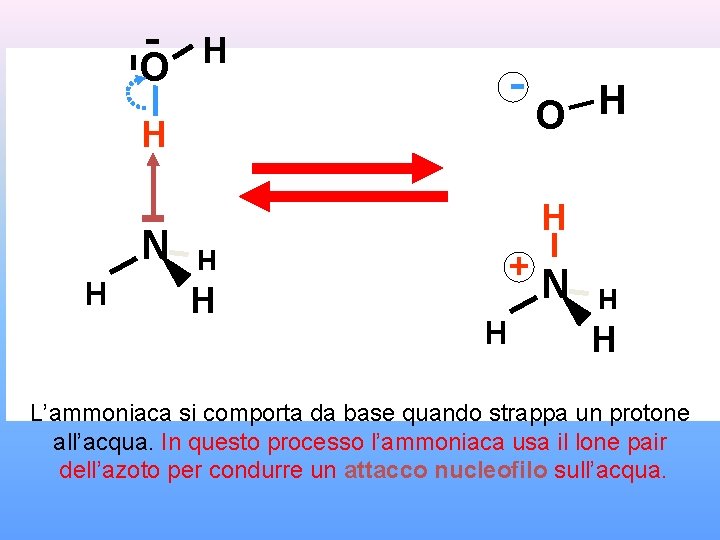
O H - H N H H O H H H + H N H H L’ammoniaca si comporta da base quando strappa un protone all’acqua. In questo processo l’ammoniaca usa il lone pair dell’azoto per condurre un attacco nucleofilo sull’acqua.

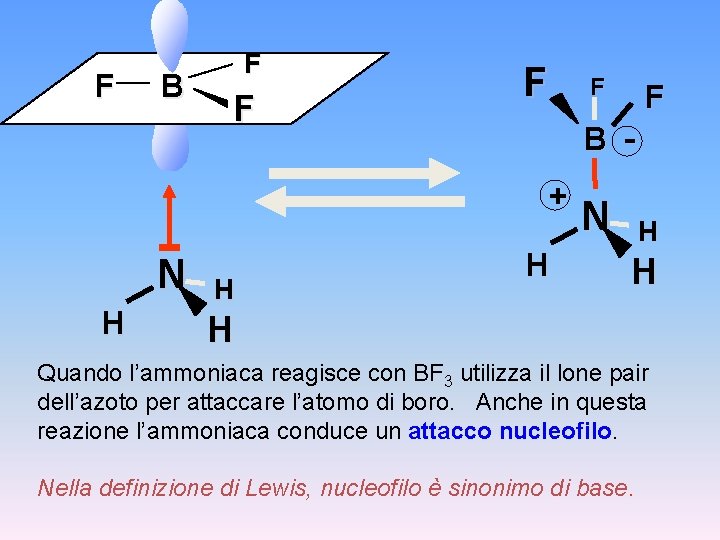
F B F F B + N H H F H N H H H Quando l’ammoniaca reagisce con BF 3 utilizza il lone pair dell’azoto per attaccare l’atomo di boro. Anche in questa reazione l’ammoniaca conduce un attacco nucleofilo. Nella definizione di Lewis, nucleofilo è sinonimo di base.

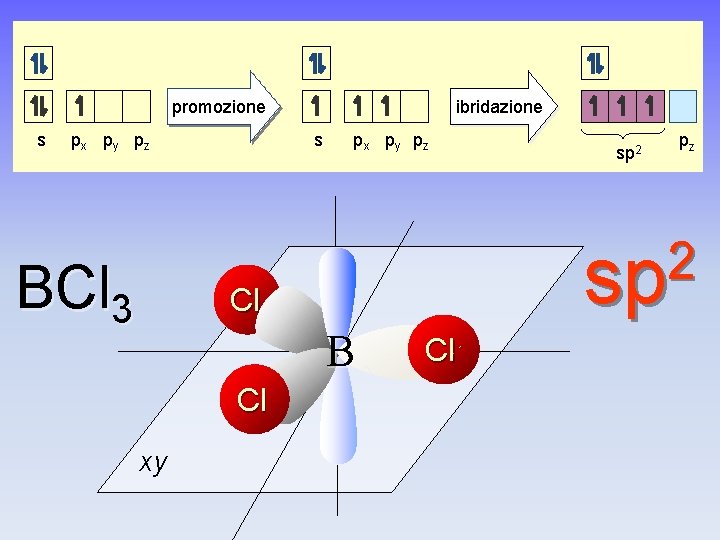
promozione s p x py p z BCl 3 ibridazione s p x p y pz B xy pz 2 sp Cl Cl sp 2 Cl

Lewis ACIDI: quei composti che sono in grado di accettare un doppietto elettronico Es: BF 3 Al. Cl 3 Zn. Cl 2 BASI: quei composti che sono in grado di donare un doppietto elettronico Una base di Lewis è anche un NUCLEOFILO Es: NH 3 N(CH 3)3


Forza relativa di acidi e basi La forza relativa di un acido (o di una base) base può essere considerata in funzione della loro tendenza a perdere (o accettare) accettare un protone Gli acidi più forti sono quelli che perdono più facilmente i loro protoni Le basi più forti sono quelle che accettano più facilmente un protone

Acidi e basi FORTI Un acido forte è una sostanza che in acqua è completamente ionizzatato: HCl(aq) H 2 O(l) H+ (aq) + Cl-(aq) Le reazioni sono spostate completamente verso destra Una base forte è una sostanza che in acqua è completamente ionizzatata: Na. OH(aq) H 2 O(l) Na+ (aq) + OH-(aq)

Acidi e basi DEBOLI L’ acido acetico è un ACIDO DEBOLE : CH 3 C=O + H 2 O O-H H 3 O + + CH 3 C=O O- Gli acidi e le basi deboli non si dissociano completamente in acqua, ma danno luogo a un equilibrio L’ ammoniaca è una BASE DEBOLE : NH 3 + H 2 O OH- + NH 4+

L’Equilibrio Chimico Nella maggior parte delle reazioni chimiche i reagenti non vengono convertiti completamente in prodotti a. A+b. B reagenti v 1 c. C+d. D v 2 prodotti • la velocità delle reazioni diretta e inversa è costante • la concentrazione delle varie specie è costante All’equilibrio, ad una data temperatura, è costante il rapporto fra il prodotto delle concentrazioni dei prodotti e il prodotto delle concentrazioni dei reagenti, ciascuno elevato al proprio coefficiente stechiometrico.

a A + b B c. C+d. D reagenti prodotti Legge di azione delle masse Esprime il rapporto tra prodotti e reagenti quando una reazione ha raggiunto l’equilibrio Keq= [C]c [D]d [A]a [B]b Keq= costante di equilibrio è funzione solo di T La parentesi [ ] indica la concentrazione molare dei componenti

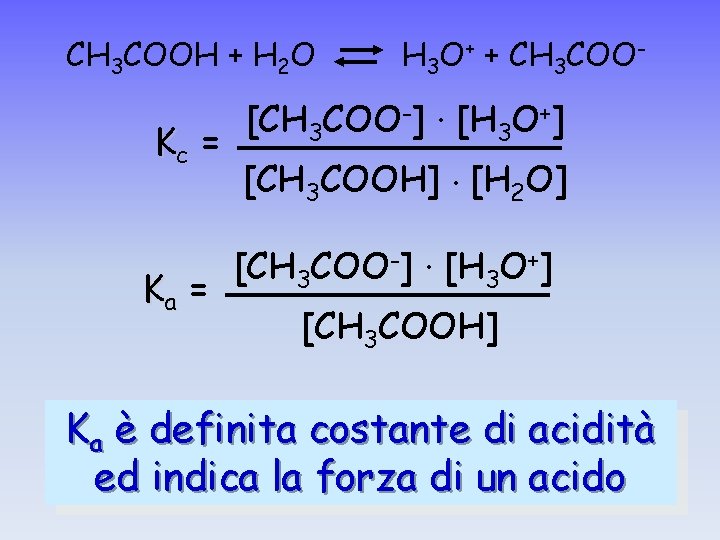
CH 3 COOH + H 2 O H 3 O+ + CH 3 COO- [CH 3 COO-] · [H 3 O+] Kc = [CH 3 COOH]. [H O] 2 Ka = [CH 3 COO-] · [H 3 O+] [CH 3 COOH] Ka è definita costante di acidità ed indica la forza di un acido

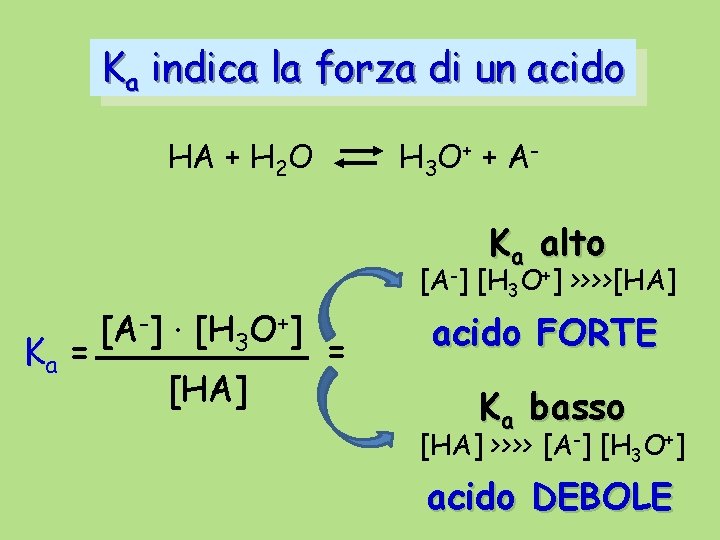
Ka indica la forza di un acido HA + H 2 O H 3 O + + A - Ka alto Ka = [A-] · [H 3 O+] [HA] [A-] [H 3 O+] >>>>[HA] = acido FORTE Ka basso [HA] >>>> [A-] [H 3 O+] acido DEBOLE

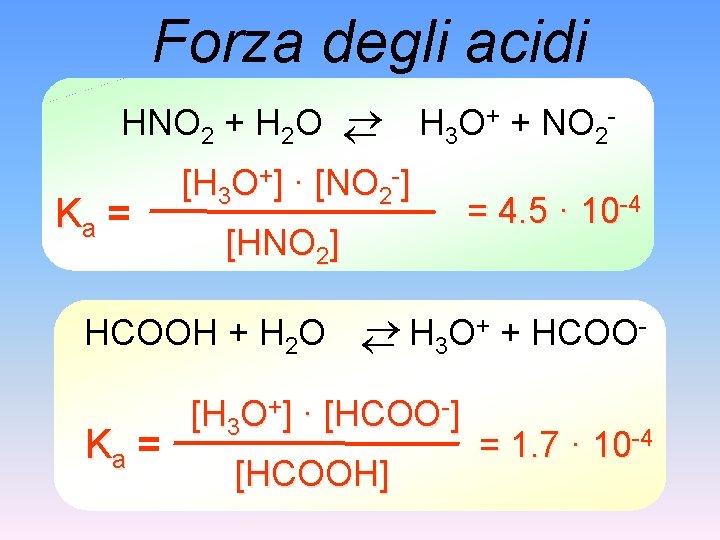
Forza degli acidi H 3 O+ + NO 2 HNO 2 + H 2 O [H 3 O+] · [NO 2 -] = 4. 5 · 10 -4 Ka = [HNO 2] H 3 O+ + HCOOH + H 2 O Ka = [H 3 O+] · [HCOO-] [HCOOH] = 1. 7 · 10 -4
![NH 3 H 2 O Kb NH 4 OH NH 4 NH 3 + H 2 O Kb = NH 4+ + OH- [NH 4+]](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-30.jpg)
NH 3 + H 2 O Kb = NH 4+ + OH- [NH 4+] · [OH-] [NH 3] La Kb è definita costante di basicità indica la forza di una base

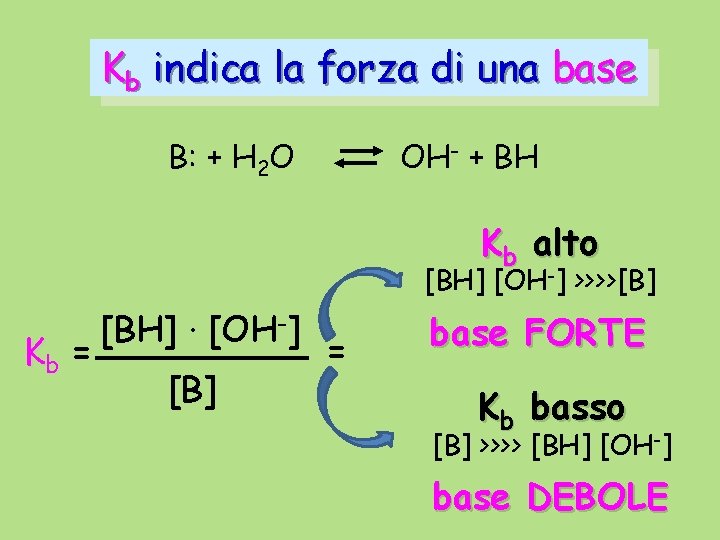
Kb indica la forza di una base B: + H 2 O OH- + BH Kb alto [BH] [OH-] >>>>[B] Kb = [BH] · [OH-] [B] = base FORTE Kb basso [B] >>>> [BH] [OH-] base DEBOLE

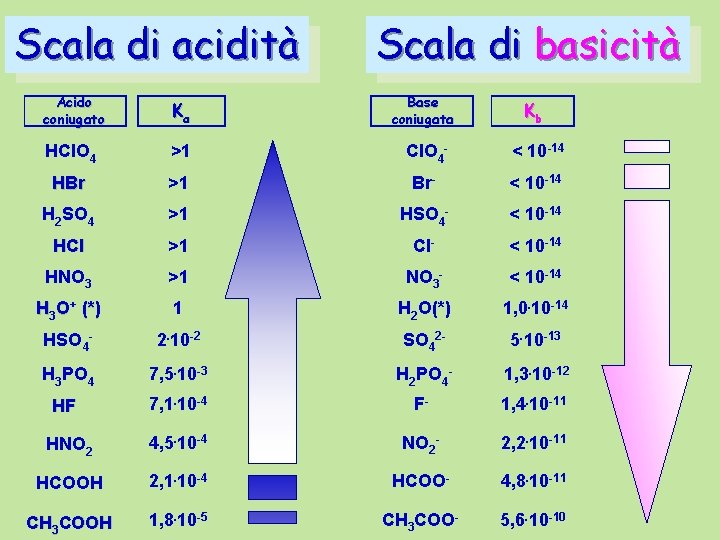
Scala di acidità Scala di basicità Acido coniugato Ka Base coniugata Kb HCl. O 4 >1 Cl. O 4 - < 10 -14 HBr >1 Br- < 10 -14 H 2 SO 4 >1 HSO 4 - < 10 -14 HCl >1 Cl- < 10 -14 HNO 3 >1 NO 3 - < 10 -14 H 3 O+ (*) 1 H 2 O(*) 1, 0. 10 -14 HSO 4 - 2. 10 -2 SO 42 - 5. 10 -13 H 3 PO 4 7, 5. 10 -3 H 2 PO 4 - 1, 3. 10 -12 HF 7, 1. 10 -4 F- 1, 4. 10 -11 HNO 2 4, 5. 10 -4 NO 2 - 2, 2. 10 -11 HCOOH 2, 1. 10 -4 HCOO- 4, 8. 10 -11 CH 3 COOH 1, 8. 10 -5 CH 3 COO- 5, 6. 10 -10

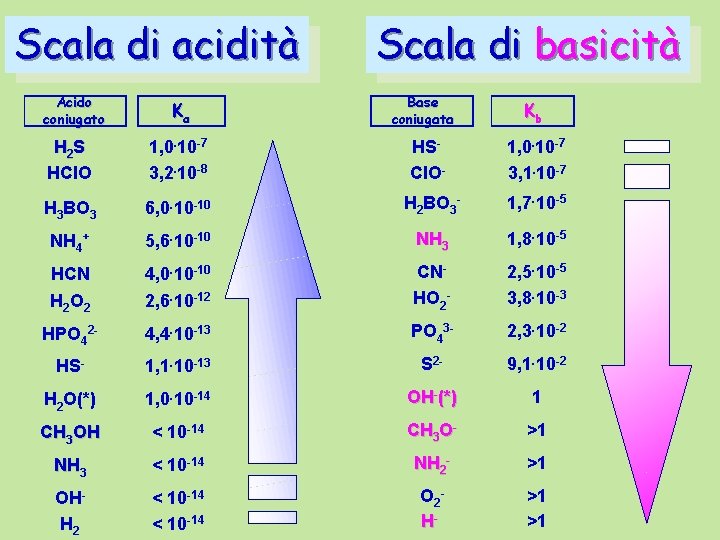
Scala di acidità Scala di basicità Acido coniugato Ka Base coniugata Kb H 2 S HCl. O 1, 0. 10 -7 3, 2. 10 -8 HSCl. O- 1, 0. 10 -7 3, 1. 10 -7 H 3 BO 3 6, 0. 10 -10 H 2 BO 3 - 1, 7. 10 -5 NH 4+ 5, 6. 10 -10 NH 3 1, 8. 10 -5 HCN H 2 O 2 4, 0. 10 -10 2, 6. 10 -12 CNHO 2 - 2, 5. 10 -5 3, 8. 10 -3 HPO 42 - 4, 4. 10 -13 PO 43 - 2, 3. 10 -2 HS- 1, 1. 10 -13 S 2 - 9, 1. 10 -2 H 2 O(*) 1, 0. 10 -14 OH-(*) 1 CH 3 OH < 10 -14 CH 3 O- >1 NH 3 < 10 -14 NH 2 - >1 OHH 2 < 10 -14 O 2 H- >1 >1

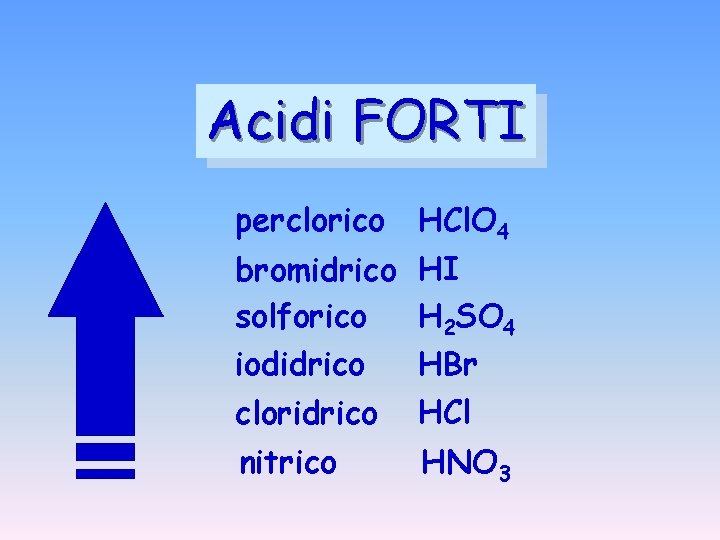
Acidi FORTI perclorico HCl. O 4 bromidrico HI H 2 SO 4 solforico HBr iodidrico cloridrico HCl nitrico HNO 3

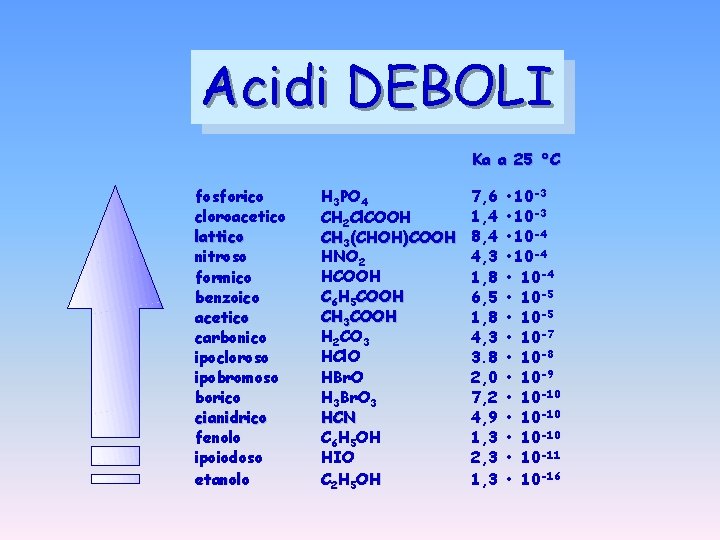
Acidi DEBOLI Ka a 25 °C fosforico cloroacetico lattico nitroso formico benzoico acetico carbonico ipocloroso ipobromoso borico cianidrico fenolo ipoiodoso etanolo H 3 PO 4 CH 2 Cl. COOH CH 3(CHOH)COOH HNO 2 HCOOH C 6 H 5 COOH CH 3 COOH H 2 CO 3 HCl. O HBr. O H 3 Br. O 3 HCN C 6 H 5 OH HIO C 2 H 5 OH 7, 6 1, 4 8, 4 4, 3 1, 8 6, 5 1, 8 4, 3 3. 8 2, 0 7, 2 4, 9 1, 3 2, 3 1, 3 • 10 -3 • 10 -4 • 10 -5 • 10 -7 • 10 -8 • 10 -9 • 10 -10 • 10 -11 • 10 -16

Basi FORTI Ione idruro ione metossi HCH 3 O- idrossido di Na Na. OH ione ossidrile OH-

Basi DEBOLI Kb a 25°C dimetilammina (CH 3)2 NH 5, 4 • 10 -4 metilammina CH 3 NH 2 3, 6 • 10 -4 trimetilammina (CH 3)3 N 6, 5 • 10 -5 ammoniaca NH 3 1, 8 • 10 -5 idrazina NH 2 1, 7 • 10 -6 morfina C 17 H 19 O 3 N 1, 6 • 10 -6 nicotina C 10 H 14 N 2 1, 0 • 10 -8 idrossilammina piridina anilina urea HONH 2 C 5 H 5 N C 6 H 5 NH 2 CO(NH 2)2 1, 1 • 10 -8 1, 8 • 10 -9 4, 3 • 10 -10 1, 3 • 10 -14

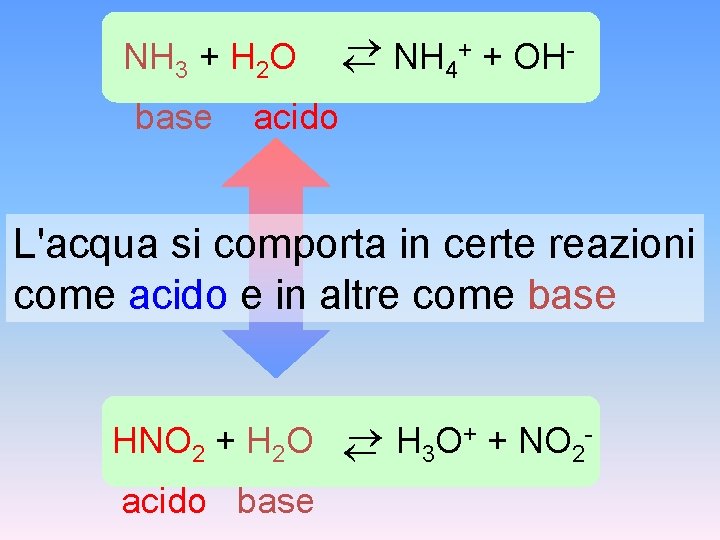
NH 3 + H 2 O base + + OHNH 4 acido L'acqua si comporta in certe reazioni come acido e in altre come base H 3 O+ + NO 2 HNO 2 + H 2 O acido base

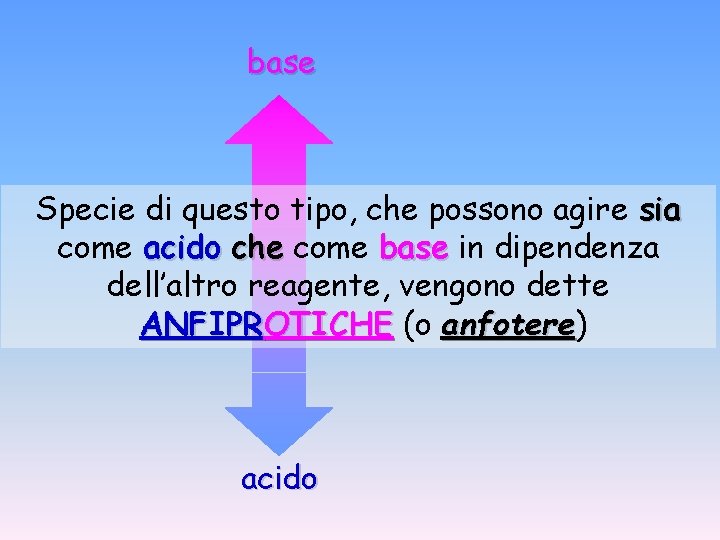
base Specie di questo tipo, che possono agire sia come acido che come base in dipendenza dell’altro reagente, vengono dette ANFIPROTICHE (o anfotere) anfotere acido

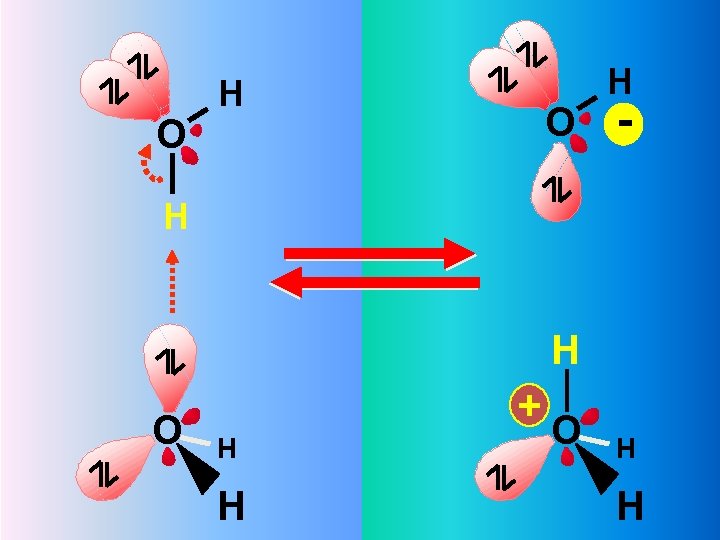
L’acqua è un conduttore elettrico di seconda specie perché è dissociata parzialmente in ioni idronio (H 3 O+) ed idrossilioni (OH-)

O H - H H O + H H O H H
![2 H 2 O Kc H 3 OH H 3 O 2 H 2 O Kc = H 3 + OH [H 3 O+] ·](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-42.jpg)
2 H 2 O Kc = H 3 + OH [H 3 O+] · [OH-] [H 2 O]2(55. 5 M) + -14 Kw = [H 3 O ] · [OH ] = 1· 10 M 2 [H 3 O+] = [OH-] = 1· 10 -7 M (prodotto ionico dell’acqua) a 25°C
![H 3 O OH 1 10 7 M Nellacqua pura solo una [H 3 O+] = [OH-] = 1· 10 -7 M Nell'acqua pura, solo una](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-43.jpg)
[H 3 O+] = [OH-] = 1· 10 -7 M Nell'acqua pura, solo una molecola ogni 500 milioni è dissociata in H+ e OH-. In questa pagina sono rappresentate 357 molecole di acqua, di cui una sola dissociata. Si dovranno esaminare circa 1 milione e mezzo di pagine come questa (circa 3000 libri di 500 pagine) prima di trovare un'altra molecola di acqua dissociata

Ka acido acetico = 1, 8 · -5 10 M Ka acido nitroso = 4, 5 · -4 10 M Ka acido formico = 1, 7 · 10 -4 M Kw = 1, 0 · 10 -14 M 2 [H 3 O+] = 1, 3 · 10 -6 M Odio gli esponenziali!
![p H log H log H 3 + p. H = - log [H ] = - log [H 3 +](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-45.jpg)
+ p. H = - log [H ] = - log [H 3 + O]
![p H dellacqua H 3 O OH 1 10 7 M p. H dell’acqua [H 3 O+] = [OH-] = 1· 10 -7 M -](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-46.jpg)
p. H dell’acqua [H 3 O+] = [OH-] = 1· 10 -7 M - log (1· 10 -7 ) = - log 10 -7 = 7 p. H = - log·[10 -7 ]= 7
![Kw H 3 O OH 1 10 14 M 2 Kw Kw = [H 3 O+] · [OH-] = 1· 10 -14 M 2 Kw](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-47.jpg)
Kw = [H 3 O+] · [OH-] = 1· 10 -14 M 2 Kw = [H 3 O+] · [OH-] = 1· 10 -7· 1· 10 -7 M a 25°C p. H = -log [H 3 O+] = 7 p. OH = -log [OH-] = 7 p. Kw = p. H + p. OH = 14
![H 3 O 1 10 7 M p H 0 H 3 [H 3 O+] > 1· 10 -7 M p. H = 0 [H 3](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-48.jpg)
[H 3 O+] > 1· 10 -7 M p. H = 0 [H 3 O+] < 1· 10 -7 M p. H = 14 p. H = 7 [H 3 O+] = 1· 10 -7 M 0 p. H < 7 Soluzione ACIDA p. H = 7 p. H > 7 Soluzione BASICA Soluzione NEUTRA p. H = 0 [OH-] < 1· 10 -7 M [OH-] = 1· 10 -7 M p. H = 7 p. H = 14 [OH-] > 1· 10 -7 M 14

Ka acido acetico = 1, 8 · 10 -5 p. Ka = - log (1, 8 · -5 10 ) p. Ka = - log 1, 8 - log -5 10 ) p. Ka = - 0, 25527 + 5 = 4, 74473

Ka alto p. Ka basso Acido FORTE Ka basso p. Ka alto Acido DEBOLE
![H 3 O 3 2 10 12 p H log [H 3 O+] = 3, 2 · 10 -12 p. H = - log](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-51.jpg)
[H 3 O+] = 3, 2 · 10 -12 p. H = - log 3, 2· 10 -12 = - log 3, 2 - log 10 -12 = - 0, 505 + 12 = 11, 495 p. Kw = p. H + p. OH = 14 – 11, 5 = 3, 5
![H 3 O 1 1 10 4 p H log [H 3 O+] = 1, 1 · 10 -4 p. H = - log](https://slidetodoc.com/presentation_image/376b96971d09382c04005c4265cb6f4d/image-52.jpg)
[H 3 O+] = 1, 1 · 10 -4 p. H = - log 1, 1· 10 -4 = - log 1, 1 - log 10 -4 = - 0, 0413 + 4 = 3, 958 p. OH = 14 - 3, 96 = 10, 04
