Universit degli Studi di Perugia Corso di Laurea











- Slides: 46

Università degli Studi di Perugia Corso di Laurea in Medicina e Chirurgia Corso di Chimica e Biochimica I Modulo di Chimica Generale e Chimica Organica STATO LIQUIDO Pier Luigi Orvietani Dipartimento di Medicina Sperimentale - Sezione di Biochimica Email: pier. orvietani@unipg. it A. A: 2017 -2018

uno stato intermedio fra lo stato solido e lo stato gassoso nello stato liquido, tra le molecole animate da moto caotico agiscono forze attrattive di entità sufficiente a non consentirne la separazione, ma insufficiente a bloccare le molecole nelle posizioni fisse di un reticolo cristallino tipico di un solido le molecole di un liquido sono in continuo movimento reciproco, e, a differenza di quanto succede in un gas, scorrono le une sulle altre senza separarsi presentano un volume proprio, assumono la forma del recipiente che li contiene e sono praticamente incomprimibili esistono infine liquidi con una struttura cristallina così definita da essere indicati col nome di cristalli liquidi.


Tensione Superficiale

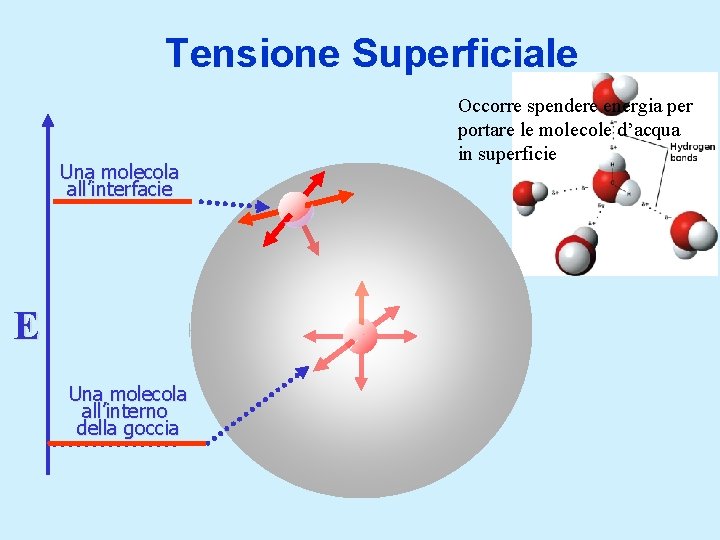
Tensione Superficiale Una molecola all’interfacie E Una molecola all’interno della goccia Occorre spendere energia per portare le molecole d’acqua in superficie

Tensione Superficiale Energia specifica superficiale Il lavoro che occorre compiere per aumentare di 1 cm 2 la superficie di una massa liquida L/S erg/cm 2

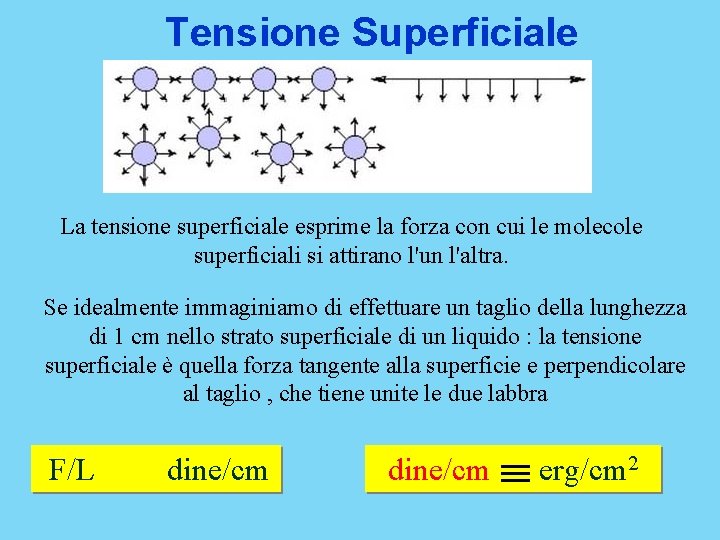
Tensione Superficiale La tensione superficiale esprime la forza con cui le molecole superficiali si attirano l'un l'altra. Se idealmente immaginiamo di effettuare un taglio della lunghezza di 1 cm nello strato superficiale di un liquido : la tensione superficiale è quella forza tangente alla superficie e perpendicolare al taglio , che tiene unite le due labbra F/L dine/cm erg/cm 2

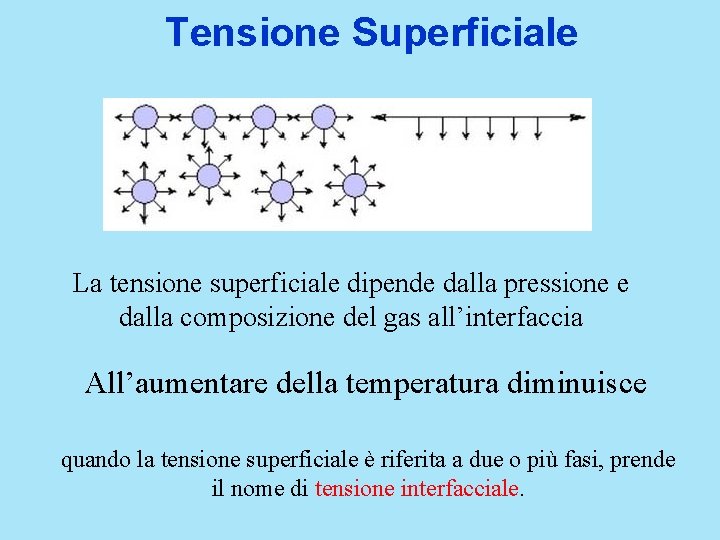
Tensione Superficiale La tensione superficiale dipende dalla pressione e dalla composizione del gas all’interfaccia All’aumentare della temperatura diminuisce quando la tensione superficiale è riferita a due o più fasi, prende il nome di tensione interfacciale.

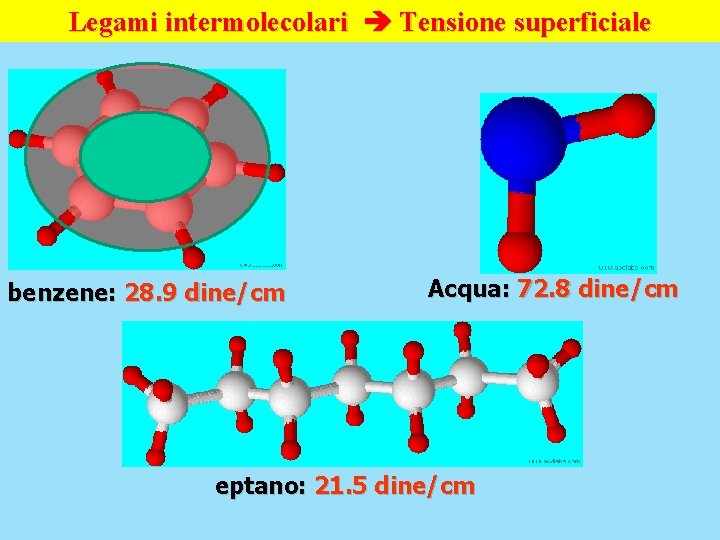
Legami intermolecolari Tensione superficiale benzene: 28. 9 dine/cm Acqua: 72. 8 dine/cm eptano: 21. 5 dine/cm

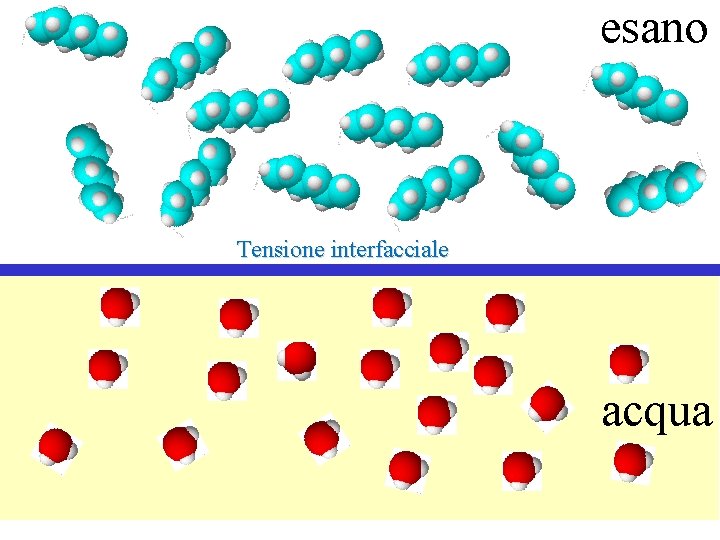
esano Tensione interfacciale acqua

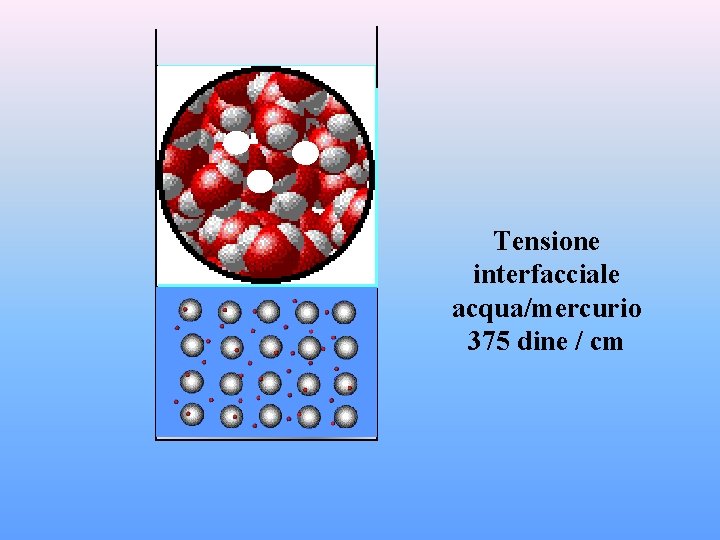
Hg Tensione interfacciale acqua/mercurio 375 dine / cm

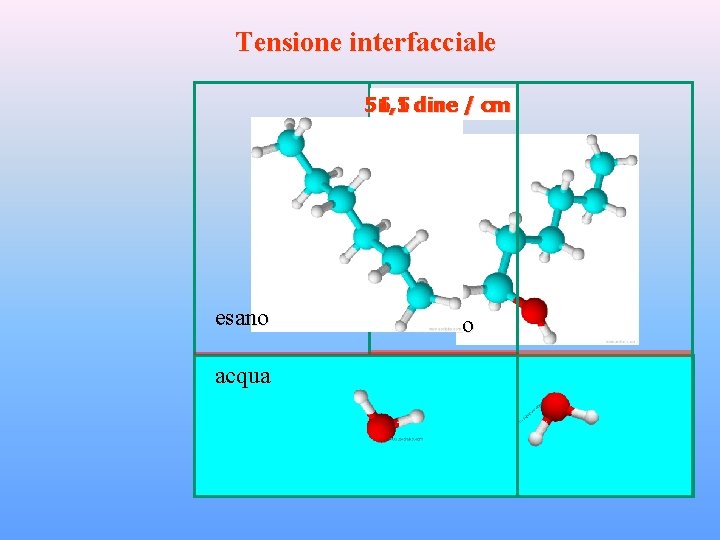
Tensione interfacciale 51, 1 6, 5 dine / cm esano 1 -esanolo acqua

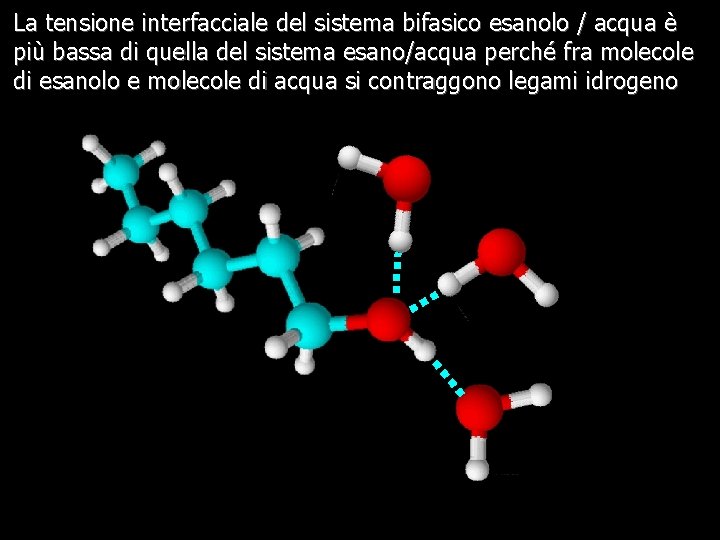
La tensione interfacciale del sistema bifasico esanolo / acqua è più bassa di quella del sistema esano/acqua perché fra molecole di esanolo e molecole di acqua si contraggono legami idrogeno

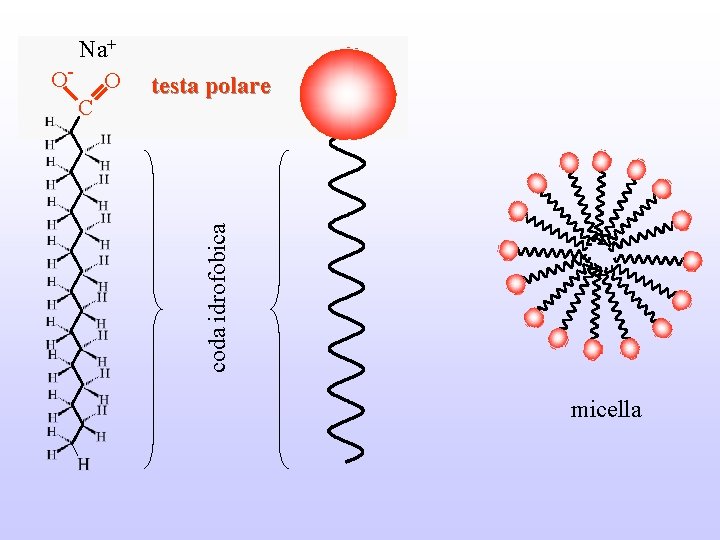
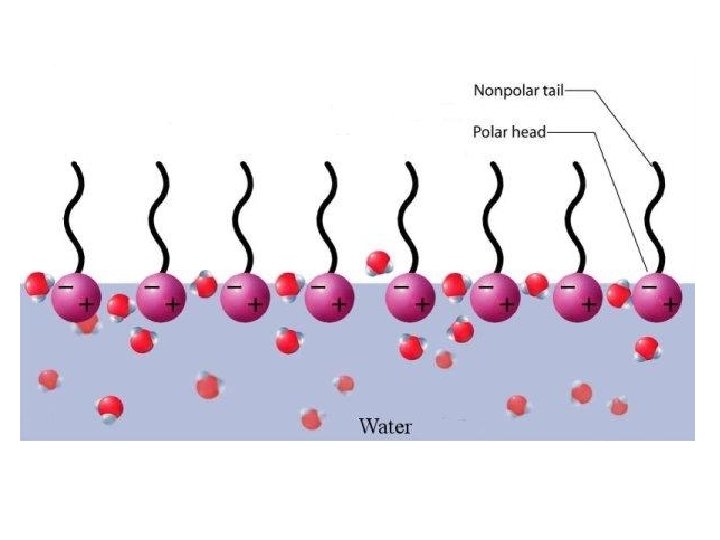
testa polare coda idrofobica Na+ O- O C micella

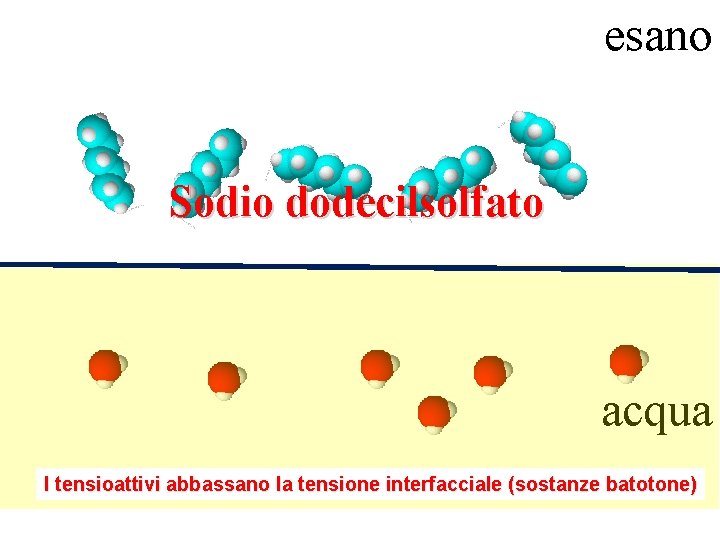
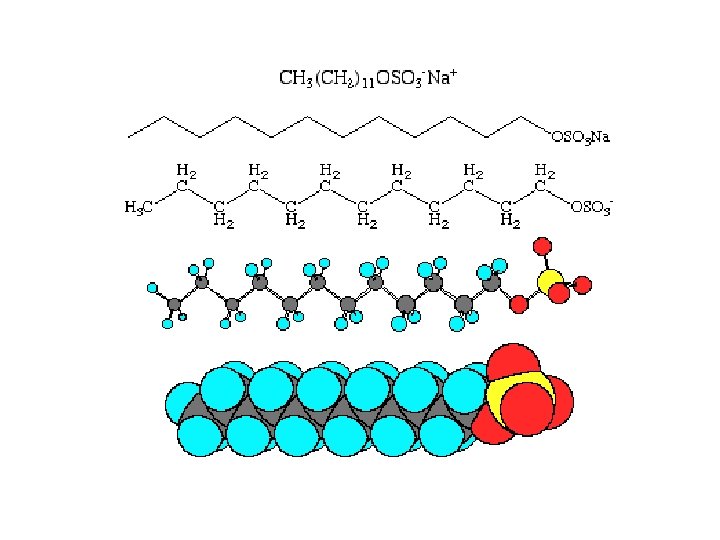
esano Sodio dodecilsolfato acqua I tensioattivi abbassano la tensione interfacciale (sostanze batotone)

TG I saponi portano i grassi in sospensione acquosa agendo da batotoni






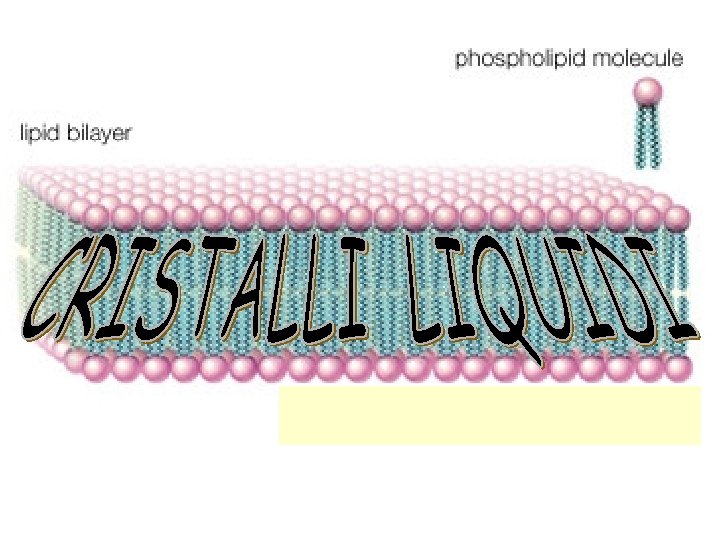
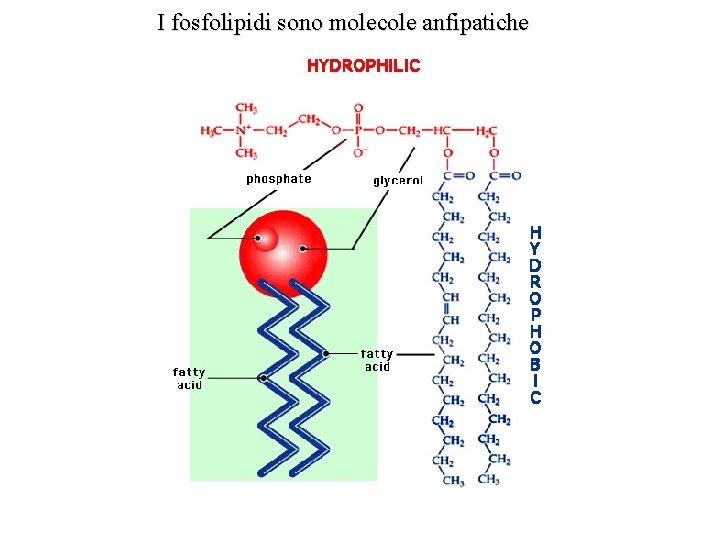
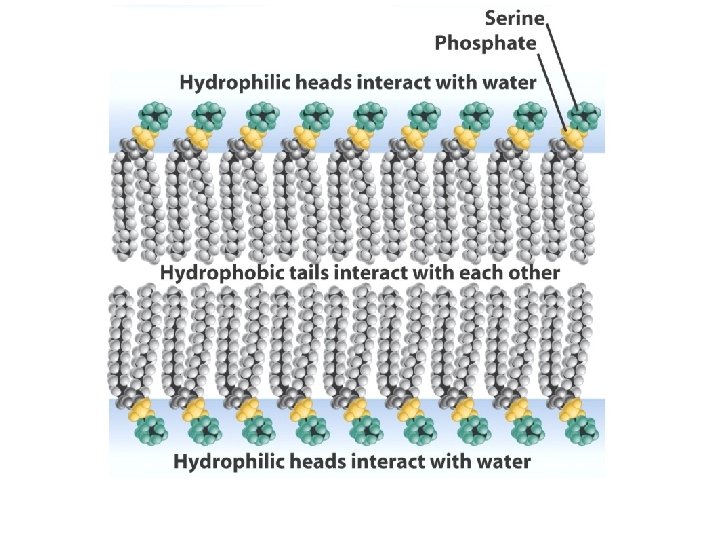
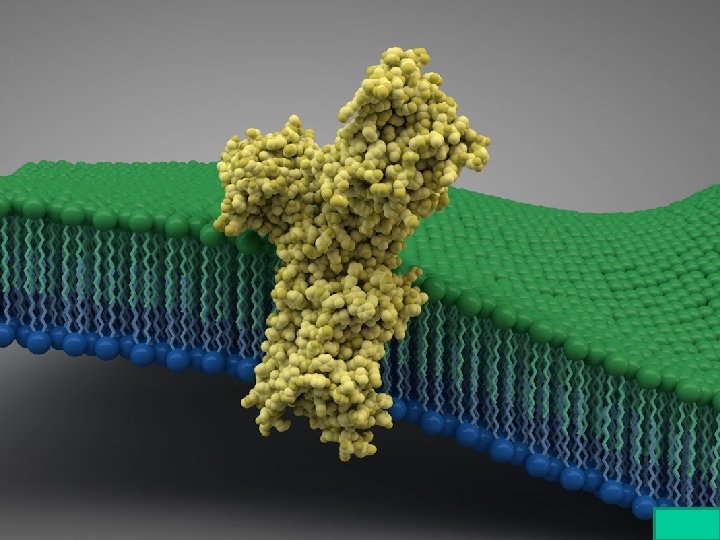
I fosfolipidi sono molecole anfipatiche

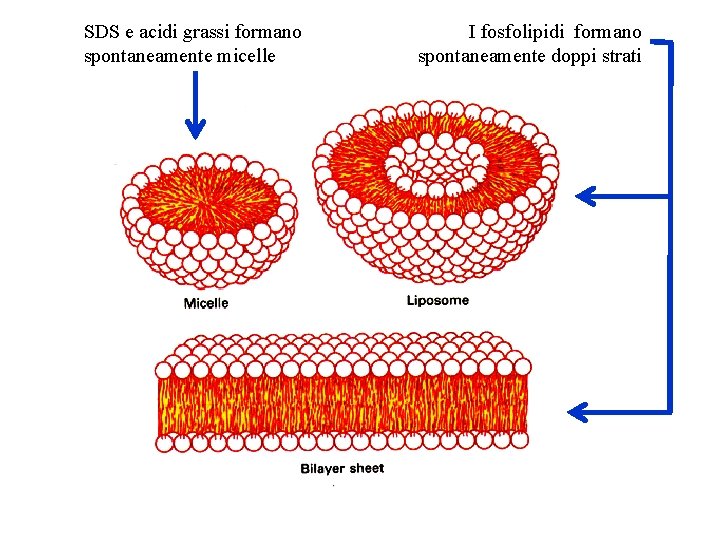
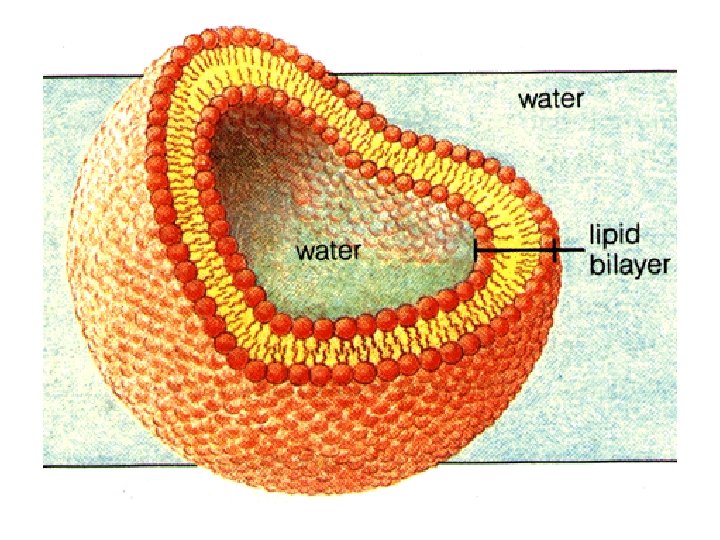
SDS e acidi grassi formano spontaneamente micelle I fosfolipidi formano spontaneamente doppi strati



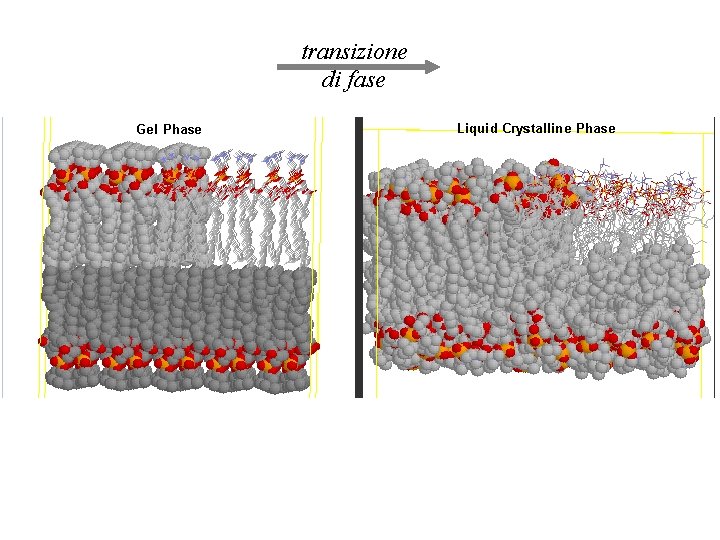
transizione di fase


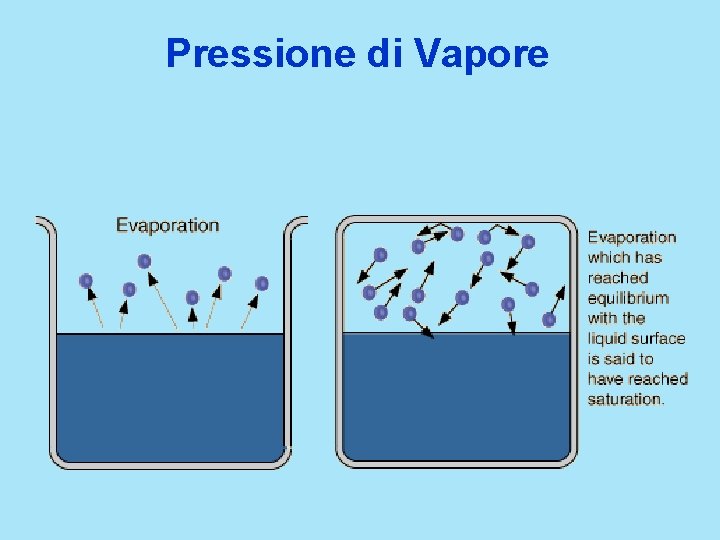
Pressione di Vapore

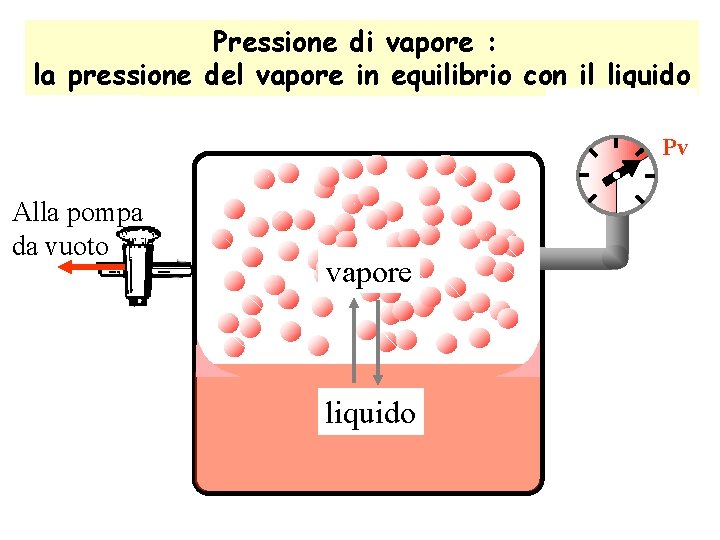
Pressione di vapore : la pressione del vapore in equilibrio con il liquido P=0 Pv Alla pompa da vuoto vapore liquido

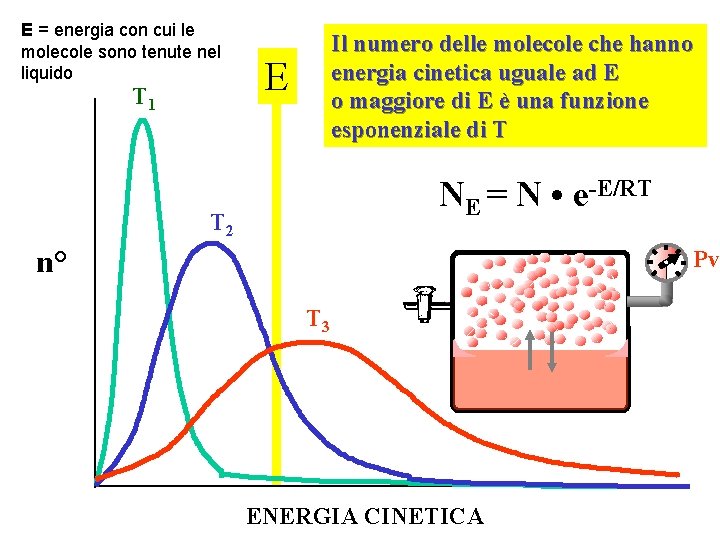
E = energia con cui le molecole sono tenute nel liquido T 1 Il numero delle molecole che hanno energia cinetica uguale ad E o maggiore di E è una funzione esponenziale di T E NE = N • e-E/RT T 2 n° Pv T 3 ENERGIA CINETICA

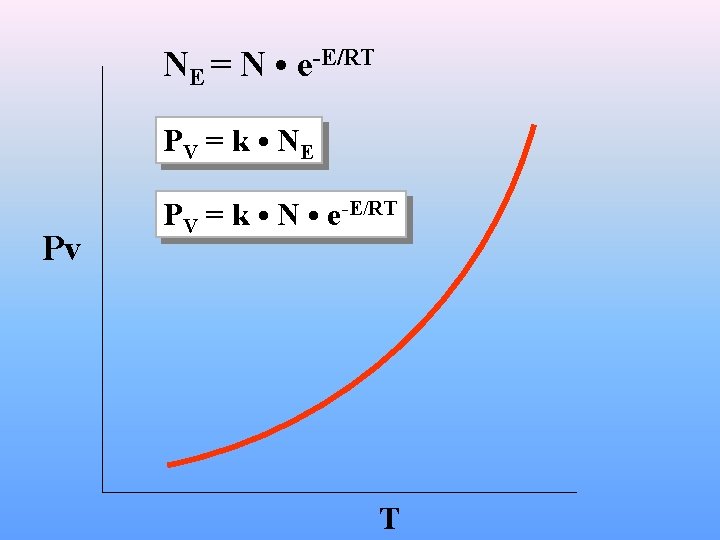
NE = N • e-E/RT PV = k • N E Pv PV = k • N • e-E/RT T


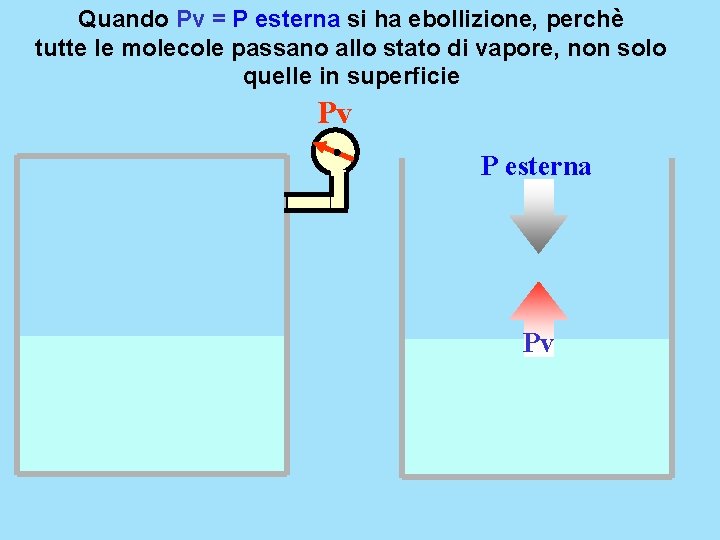
Quando Pv = P esterna si ha ebollizione, perchè tutte le molecole passano allo stato di vapore, non solo quelle in superficie Pv P esterna Pv

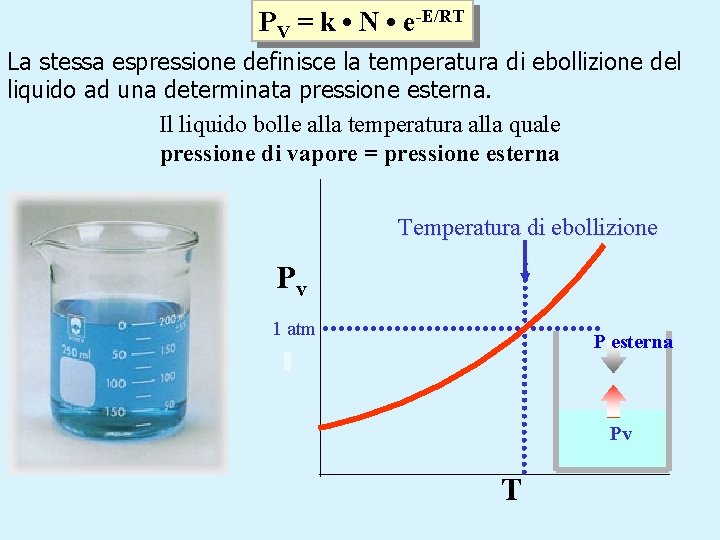
PV = k • N • e-E/RT La stessa espressione definisce la temperatura di ebollizione del liquido ad una determinata pressione esterna. Il liquido bolle alla temperatura alla quale pressione di vapore = pressione esterna Temperatura di ebollizione Pv 1 atm P esterna Pv T

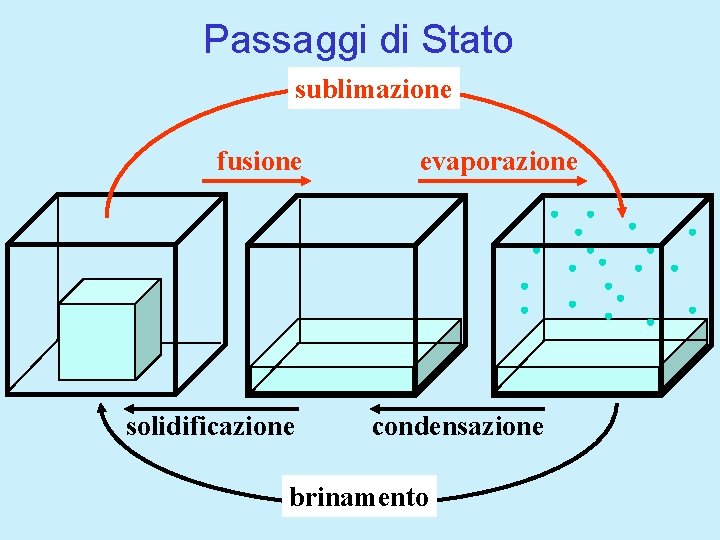
Passaggi di Stato sublimazione fusione solidificazione evaporazione condensazione brinamento

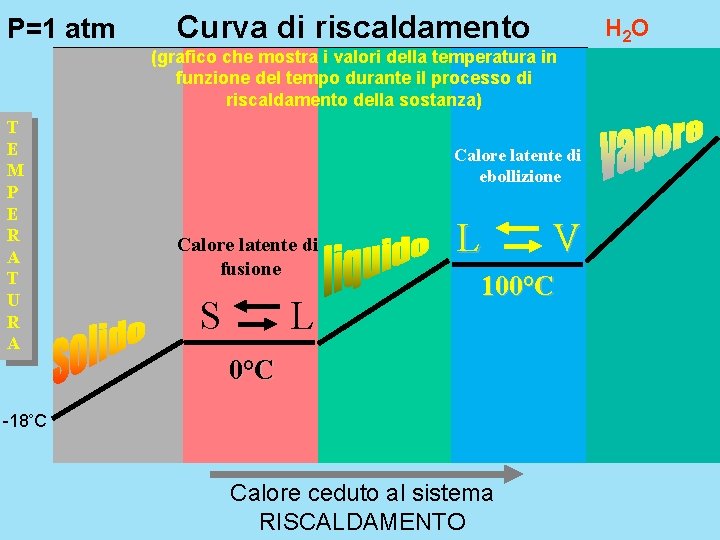
P=1 atm Curva di riscaldamento H 2 O (grafico che mostra i valori della temperatura in funzione del tempo durante il processo di riscaldamento della sostanza) T E M P E R A T U R A Calore latente di ebollizione Calore latente di fusione S L L V 100°C -18 C Calore ceduto al sistema RISCALDAMENTO

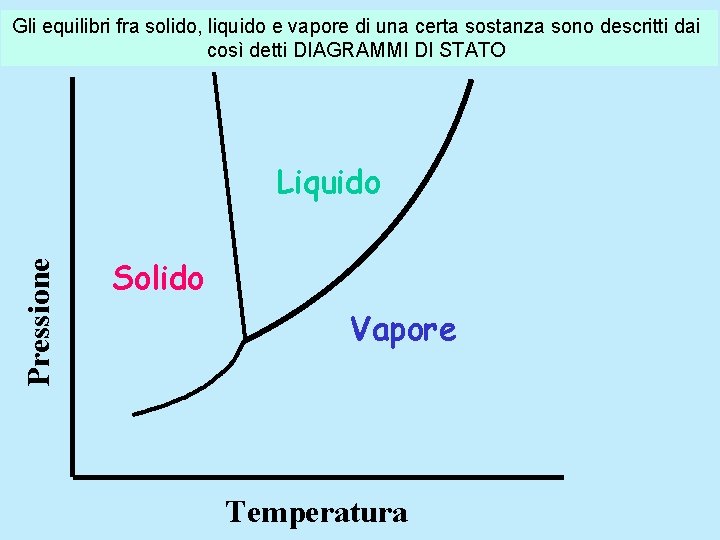
Gli equilibri fra solido, liquido e vapore di una certa sostanza sono descritti dai così detti DIAGRAMMI DI STATO Pressione Liquido Solido Vapore Temperatura

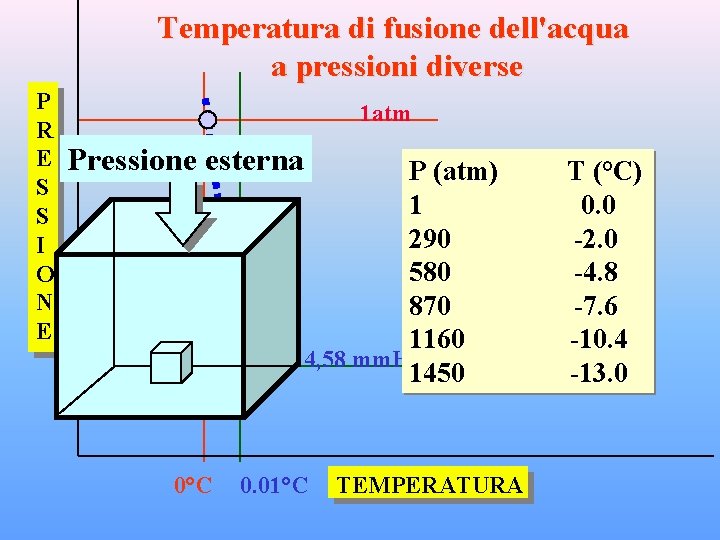
Temperatura di fusione dell'acqua a pressioni diverse Pressione esterna P (atm) 1 290 580 870 1160 1450 T (°C) 0. 0 -2. 0 -4. 8 -7. 6 -10. 4 -13. 0

Temperatura di fusione dell'acqua a pressioni diverse P R E S S I O N E 1 atm Pressione esterna P (atm) 1 290 580 870 1160 4, 58 mm. Hg 1450 0°C 0. 01°C TEMPERATURA T (°C) 0. 0 -2. 0 -4. 8 -7. 6 -10. 4 -13. 0

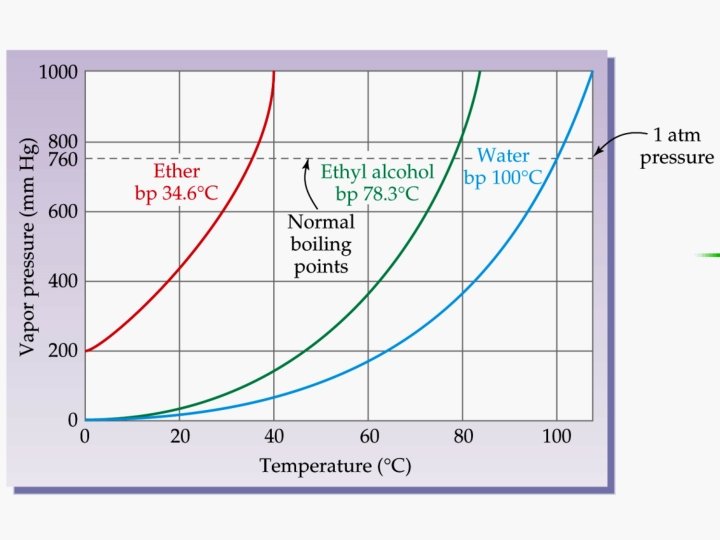
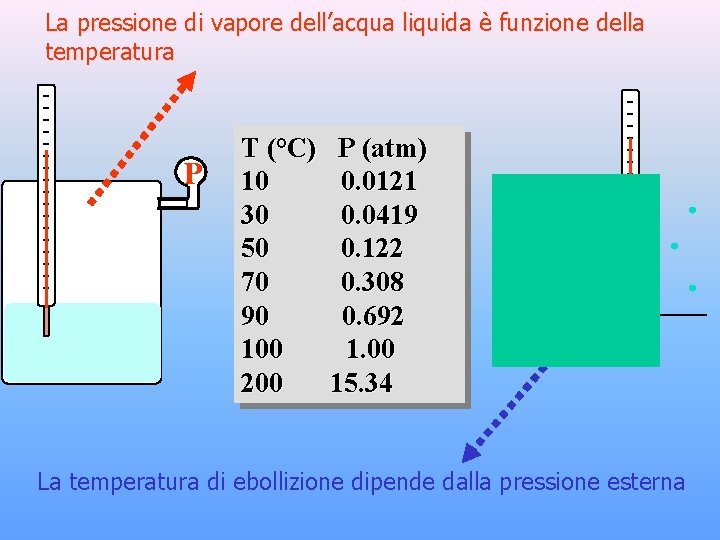
La pressione di vapore dell’acqua liquida è funzione della temperatura P T (°C) 10 30 50 70 90 100 200 P (atm) 0. 0121 0. 0419 0. 122 0. 308 0. 692 1. 00 15. 34 La temperatura di ebollizione dipende dalla pressione esterna

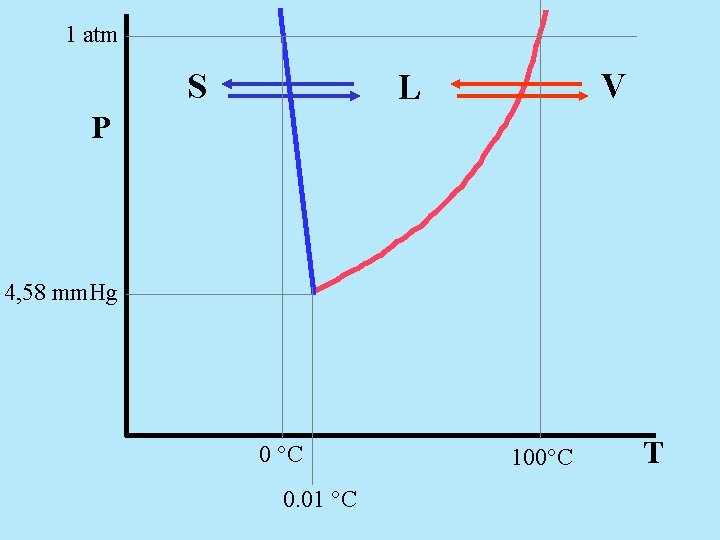
1 atm S V L P 4, 58 mm. Hg 0 °C 0. 01 °C 100°C T

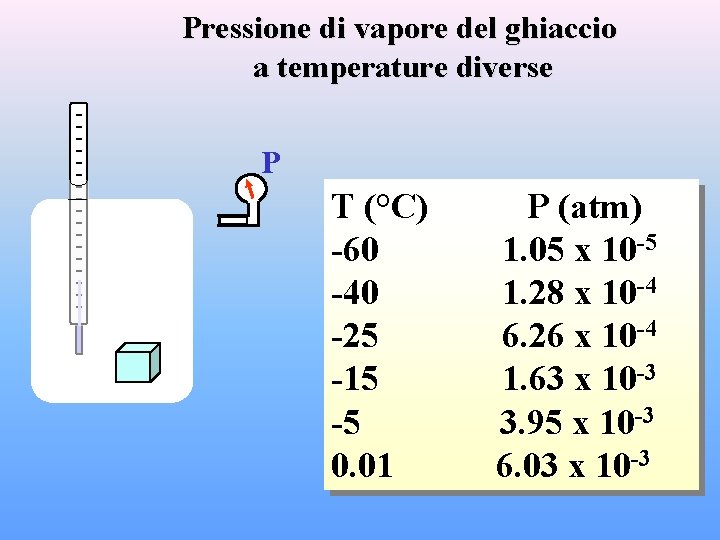
Pressione di vapore del ghiaccio a temperature diverse P T (°C) -60 -40 -25 -15 -5 0. 01 P (atm) 1. 05 x 10 -5 1. 28 x 10 -4 6. 26 x 10 -4 1. 63 x 10 -3 3. 95 x 10 -3 6. 03 x 10 -3

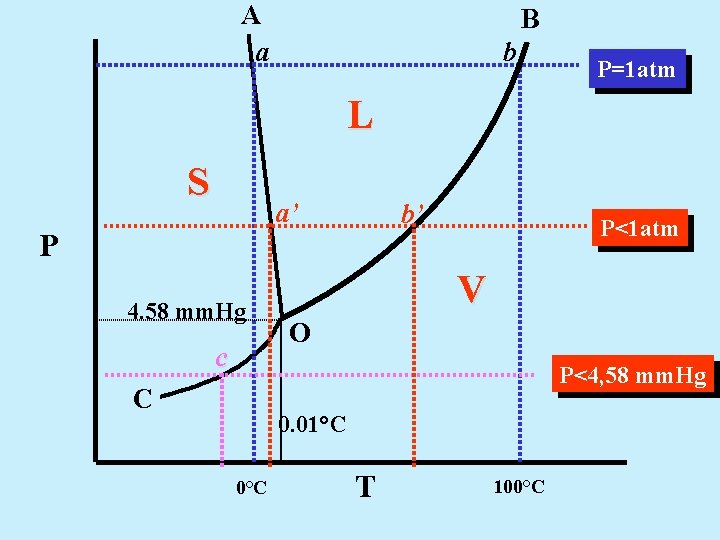
A a B b P=1 atm L S a’ P 4. 58 mm. Hg c b’ P<1 atm V O P<4, 58 mm. Hg C 0. 01°C 0°C T 100°C

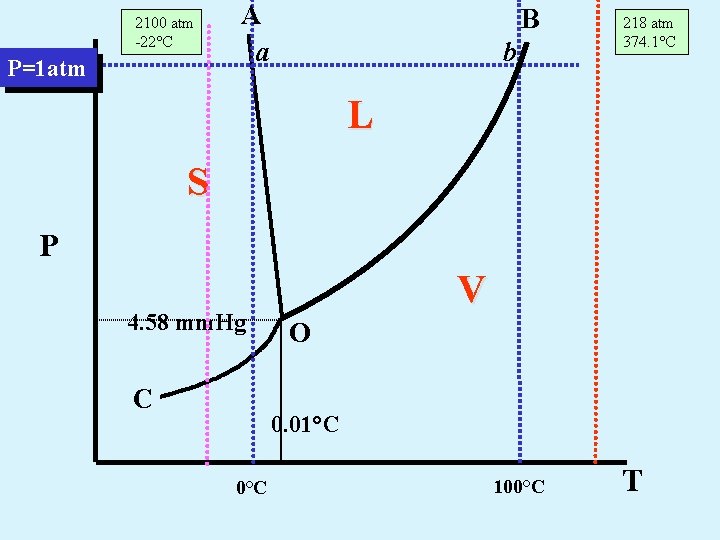
2100 atm -22°C P=1 atm A a B b 218 atm 374. 1°C L S P 4. 58 mm. Hg C V O 0. 01°C 0°C 100°C T

*Ad una temperatura inferiore alla temperatura critica l’areiforme viene chiamato vapore e può essere trasformato in liquido per sola compressione. *Per valori superiori di temperatura, la stessa sostanza si chiama gas e non può essere trasformata in liquido per sola compressione.

Viscosità La viscosità di un fluido è una misura della resistenza che, all’interno del fluido stesso, gli strati adiacenti oppongono allo scorrimento reciproco Per una corretta interpretazione di questo fenomeno, si deve ammettere che il movimento del fluido all'interno, per esempio, di un condotto cilindrico, sia dovuto al movimento di strati lamellari concentrici Fluido con viscosità minore Fluido con viscosità maggiore