Paula Costallat Canto Protenas Componentes fundamentais de todos





















- Slides: 30

Paula Costallat Cantão

Proteínas • Componentes fundamentais de todos os seres vivos, inclusive dos vírus; • Formam várias estruturas das células; • Controlam a entrada e saída de substâncias das células pela membrana plasmática; • Conferem sustentação a muitos tecidos do corpo; • Responsáveis pela contração dos músculos e; • Responsáveis pelo transporte de oxigênio no sangue de muitos animais.

Proteínas Composição Molecular: Moléculas relativamente grandes, formadas pela união sequencial de dezenas ou centenas de moléculas menores, denominadas aminoácidos. É uma sequência de aminoácidos encadeados (cadeia de aminoácidos). Aminoácidos: moléculas orgânicas formadas por átomos de C, H, O e N, unidos de maneira característica. (S)

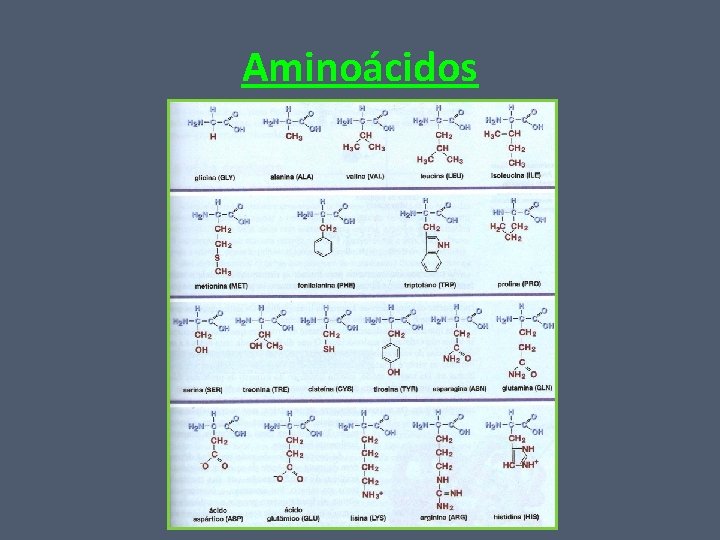
Aminoácidos Todos os 20 tipos de aminoácidos, diferem quanto ao radical (grupo –R); grupo este que os caracteriza.

Aminoácidos

Ligações Peptídicas São ligações entre dois aminoácidos vizinhos, formando uma molécula de proteína (síntese por desidratação). O grupamento Hidroxila do Grupo Carboxila de um dos aminoácidos une-se ao Hidrogênio do Grupo Amina do outro, formando uma molécula de água.

Ligações Peptídicas Peptídios = moléculas resultantes da união de aminoácidos. • Dipeptídio = dois aminoácidos unidos; • Tripeptídio = três aminoácidos unidos; • Tetrapeptídio = quatro aminoácidos unidos; • Oligopeptídio = (oligo = pouco) moléculas formadas por poucos aminoácidos; • Polipeptídio = (poli = muito) moléculas formadas por muitos aminoácidos.

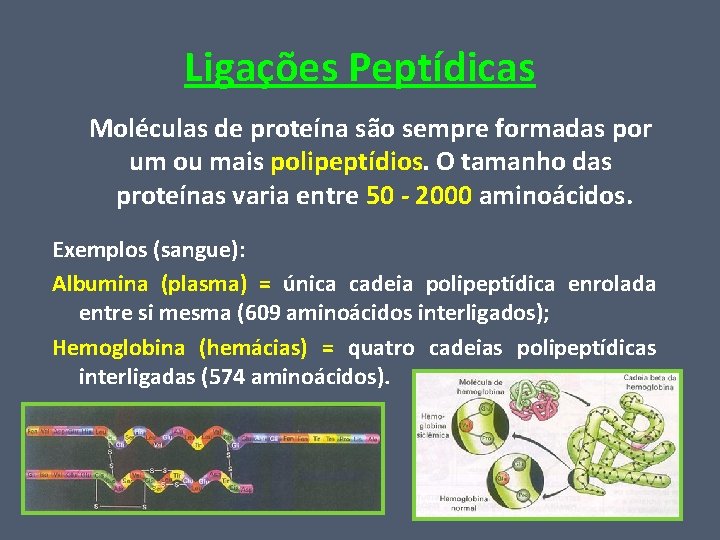
Ligações Peptídicas Moléculas de proteína são sempre formadas por um ou mais polipeptídios. O tamanho das proteínas varia entre 50 - 2000 aminoácidos. Exemplos (sangue): Albumina (plasma) = única cadeia polipeptídica enrolada entre si mesma (609 aminoácidos interligados); Hemoglobina (hemácias) = quatro cadeias polipeptídicas interligadas (574 aminoácidos).


Arquitetura das Proteínas Calcula-se que no corpo humano, existam entre 100 a 200 mil tipos diferentes de proteínas. Diferem umas das outras nos seguintes aspectos: a) Pela quantidade de aminoácidos da cadeia polipeptídica; b) Pelos tipos de aminoácidos presentes na cadeia; c) Pela sequência em que os aminoácidos se dispõem na cadeia polipeptídica.

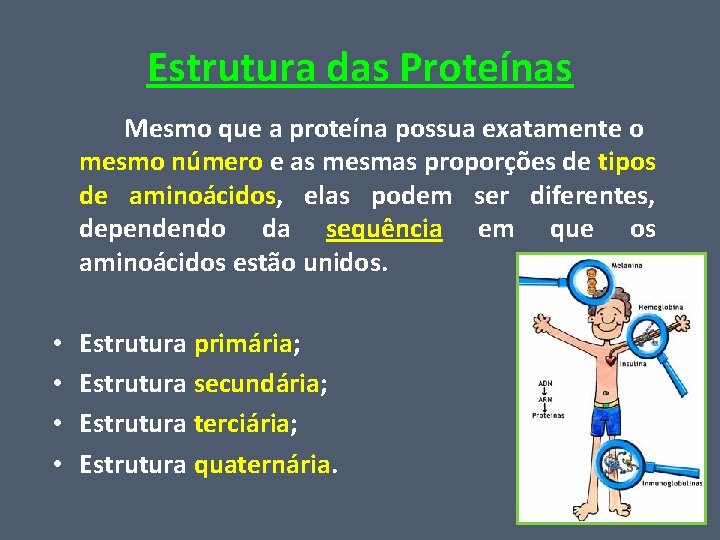
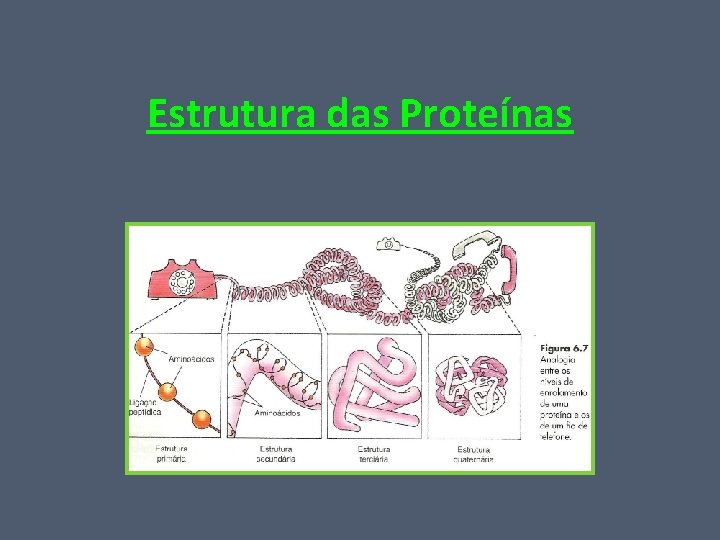
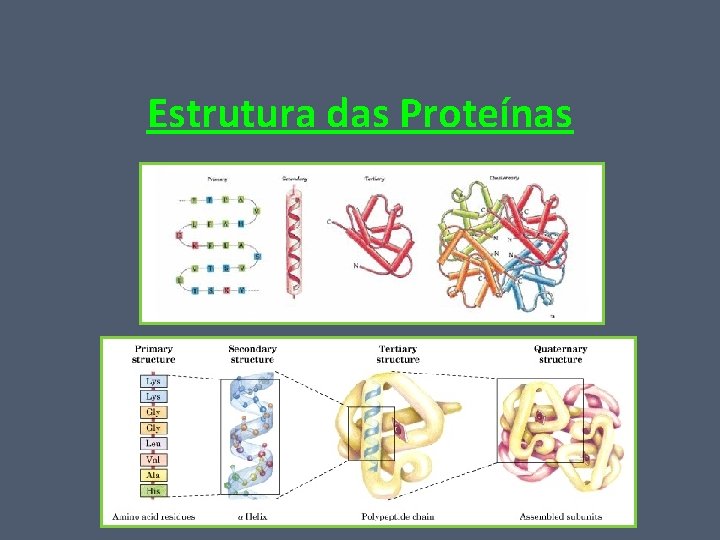
Estrutura das Proteínas Mesmo que a proteína possua exatamente o mesmo número e as mesmas proporções de tipos de aminoácidos, elas podem ser diferentes, dependendo da sequência em que os aminoácidos estão unidos. • • Estrutura primária; Estrutura secundária; Estrutura terciária; Estrutura quaternária.

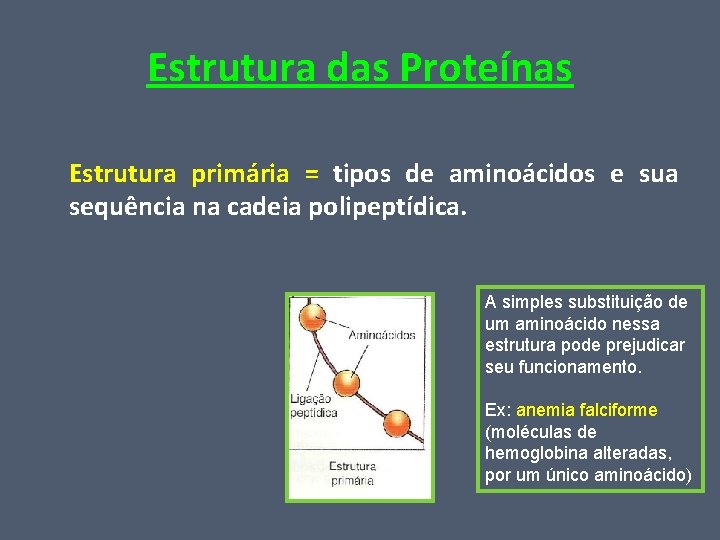
Estrutura das Proteínas Estrutura primária = tipos de aminoácidos e sua sequência na cadeia polipeptídica. A simples substituição de um aminoácido nessa estrutura pode prejudicar seu funcionamento. Ex: anemia falciforme (moléculas de hemoglobina alteradas, por um único aminoácido)

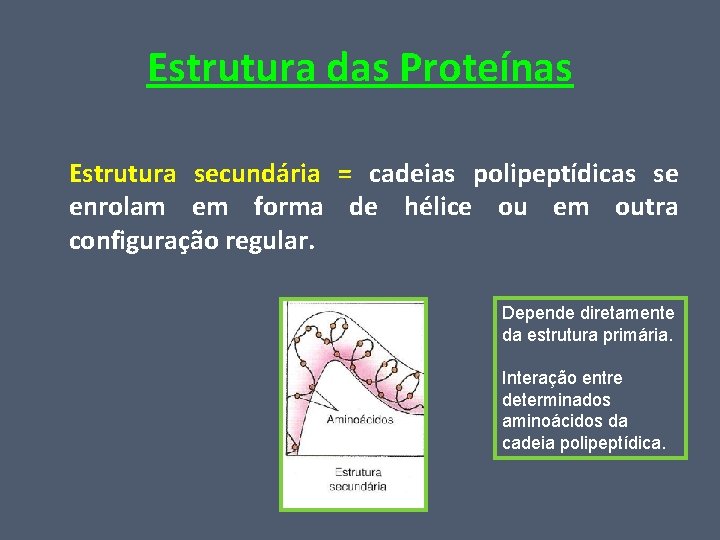
Estrutura das Proteínas Estrutura secundária = cadeias polipeptídicas se enrolam em forma de hélice ou em outra configuração regular. Depende diretamente da estrutura primária. Interação entre determinados aminoácidos da cadeia polipeptídica.

Estrutura das Proteínas Estrutura terciária = segundo nível de enrolamento. Decorre da atração entre diferentes partes da molécula já enrolada em estrutura secundária. Resulta da atração e da repulsão entre os aminoácidos da cadeia polipeptídica e a água circundante.

Estrutura das Proteínas Estrutura quaternária = cadeias polipeptídicas em estruturas terciárias associadas.

Estrutura das Proteínas

Estrutura das Proteínas

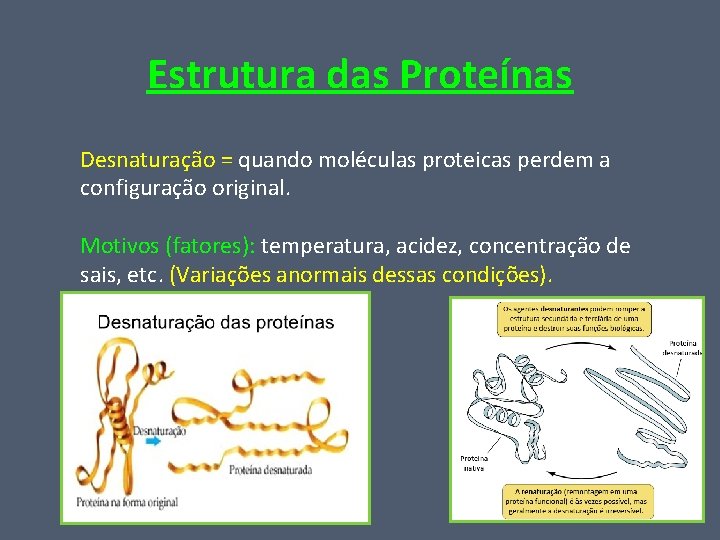
Estrutura das Proteínas Desnaturação = quando moléculas proteicas perdem a configuração original. Motivos (fatores): temperatura, acidez, concentração de sais, etc. (Variações anormais dessas condições).

Estrutura das Proteínas Desnaturação da Albumina

Funções das Proteínas São importantes tanto na estrutura das células quanto no funcionamento. - Ponto de vista estrutural: Formam o Citoesqueleto (esqueleto interno das células, constituído por filamentos protéicos, dando forma e movimento a célula); Fazem parte da estrutura das membranas celulares; Conferem consistência ao citoplasma; -Ponto de vista funcional: Participam de praticamente todas as reações químicas vitais, através de proteínas especiais, denominadas enzimas.

Enzimas São proteínas que atuam como catalisadores biológicos. Catalisador = participa de uma reação química, acelerando-a, porém se desgastar ou se alterar no curso da reação, podendo ser reutilizado. • Catalisam reações de quebra de molécula; • Favorecem a união entre moléculas de substratos; • Atuam modificando certas ligações químicas em uma molécula, transformando-a em outra.

Enzimas Nomenclatura = nome do substrato enzimático + sufixo ase. Exemplos: Protease = enzimas que digerem proteínas; Lipases = enzimas que digerem lipídios; Lactase = enzimas quebram lactose em galactose e glicose; Amilase salivar (ptialina) = enzimas quebram moléculas de amido em maltose ; Sacarase = enzima quebra sacarose em glicose e frutose.

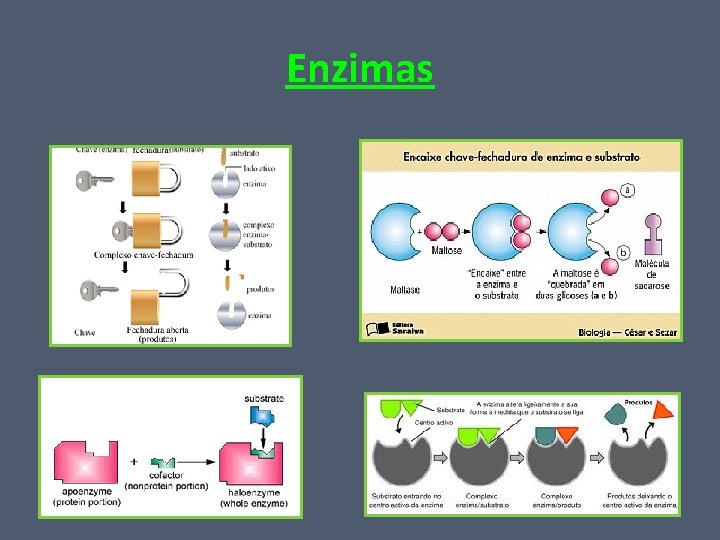
Enzimas São altamente específicas. (Determinada enzima catalisa, em geral, um único tipo de reação. ) Proteína Enzimática: apresenta “encaixes” que se adaptam as moléculas sobre as quais ela atua (substratos enzimáticos). Parte da enzima responsável pelo encaixe com o substrato: CENTRO ATIVO. Grande especificidade: CHAVE – FECHADURA Catalisadores Biológicos: não sofrem alterações moleculares e não são consumidas.

Enzimas

Cofatores e coenzimas Proteínas Simples = enzimas constituídas apenas por cadeias polipeptídicas. Proteínas Conjugadas = enzimas constituídas por: Uma parte proteica (uma ou mais cadeias polipeptídicas) – Apoenzima + Uma parte não-proteica (íons de Cobre, Zinco, . . . ) – Cofator Apoenzima (inativa) + Cofator (inativo) = Holoenzima (ativa) Cofatores de certas enzimas: substâncias orgânicas (Coenzimas). Ex: Vitaminas

Inibição da atividade enzimática Inibição Competitiva: atividades das enzimas inibidas por algumas substâncias. Essas estruturas tem estrutura semelhante à do substrato e competem com ele pela ligação com a enzima. Ligação = é permanente (a molécula de enzima associada ao inibidor deixa de funcionar). Exemplos de inibidores competitivos de ação enzimática: Íon cianeto (CN) = INIBE = Citocromo oxidase (respiração celular) = morte da célula Penicilina = INIBE = Transpeptidase (produção da parede bacteriana) = célula não se reproduz pois não possui a parede da célula.

Fatores que afetam a atividade da enzima Temperatura: cada enzima atua melhor em uma faixa de temperatura característica, chamada temperatura ótima (velocidade da reação catalisada é máxima, sem desnaturação). Maioria das enzimas humanas = 37ºC Bactérias de fontes termais = 80ºC p. H: Grau de acidez do meio, em que a enzima tem seu poder de atuação, chamado de p. H ótimo (no qual sua atividade é máxima). Maioria das enzimas = p. H 7, próximo ao neutro Enzima pepsina (estômago) = p. H 2, fortemente ácido Enzima Tripsina (intestino) = p. H 8, ambiente alcalino



FIM!