SEMANA 30 2010 Lic Sofa Tobas PROTENAS PROTENAS
SEMANA 30 -2010 Lic. Sofìa Tobìas PROTEÍNAS

PROTEÍNAS Compuestos de masa molar elevada, formados en su mayor parte o totalmente de cadenas de amino ácidos. PROTEIOS=primero.

• El ser humano no puede sobrevivir sin proteínas en la dieta. • Generan tejido y mantienen los ya formados. • Forman parte de nervios, anticuerpos, hormonas, enzimas. • Contienen: C, H, O, N, P y S. • Son polímeros de alfa a. a. de alto peso molecular.

CLASIFICACIÓN: I. Por su composición: 1. SIMPLES: formadas por alfa a. a. 2. CONJUGADAS: alfa a. a. y grupo no protéico.

1. SIMPLES • Albuminas: Son las mas comunes y mas abundantes. Estan presentes en clara de huevo (ovoalbúmina), suero (seroalbúminas), leche(lactoalbúminas) Son solubles en agua y soluciones salinas. • Globulinas: anticuerpos en suero sanguíneo. Son insolubles en agua.

• Histonas: son básicas porque tienen a. a. básicos (lisina y/o arginina). Se encuentran asociadas en las nucleoproteínas, son solubles en agua. • Escleroproteínas: Tienen función estructural. Son insolubles en agua y casi todo solvente. Ejs. : queratina: en pelo, piel, uñas. Colágeno: en huesos, tendones y cartílagos. Elastina: fibras elásticas y tejido conectivo.

2. CONJUGADAS • Fosfoproteínas: Contienen α a. a. y ácido fosfórico. (caseína) • Glucoproteínas: contienen α a. a. y carbohidratos. (mucina)intervienen en procesos digestivos, gama globulina (interferón). • Cromoproteínas: contienen α a. a. y un pigmento. Ej. Hemoglobina (grupo hem)
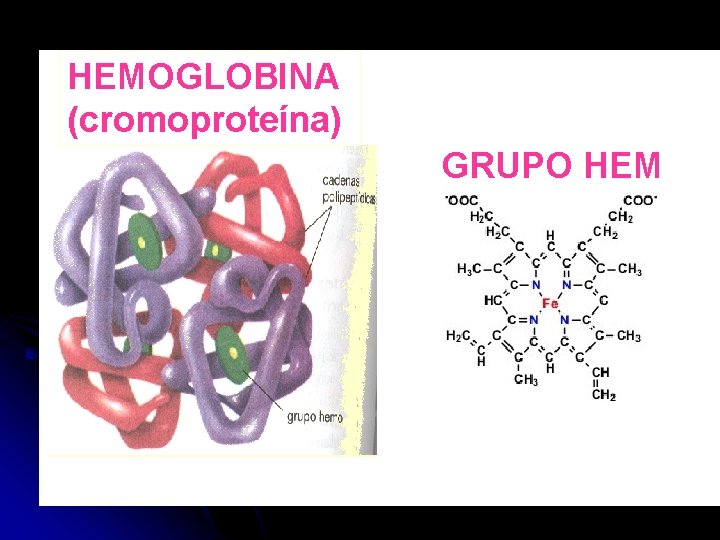
HEMOGLOBINA (cromoproteína) GRUPO HEM

• Nucleoproteínas: α a. a. y ácidos nucléicos (ADN, ARN). • Lipoproteínas: α a. a, esteres de colesterol y fosfolípidos. Están presentes en la yema de huevo, núcleo celuar, ribosomas. Intervienen en el transporte de lípidos en sangre y se clasifican por su densidad: VLDL, LDL Y HDL.
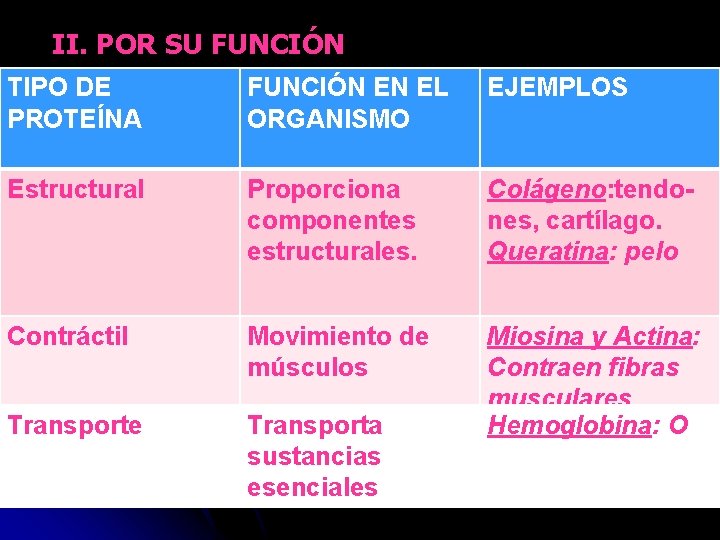
II. POR SU FUNCIÓN TIPO DE PROTEÍNA FUNCIÓN EN EL ORGANISMO EJEMPLOS Estructural Proporciona componentes estructurales. Colágeno: tendones, cartílago. Queratina: pelo Contráctil Movimiento de músculos Transporte Transporta sustancias esenciales Miosina y Actina: Contraen fibras musculares Hemoglobina: O

PROTEÍNA FUNCIÓN ALMACENAMIENTO Almacena nutrientes HORMONA Regula metabolismo corporal ENZIMA Cataliza reacciones PROTECCIÓN Reconoce y destruye sustancias extrañas EJEMPLOS Caseína Ferritina Insulina H. del crecimiento Sacarasa Tripsina Inmunoglobulinas : estimulan respuesta inmunológica.

Clasificación por Grupos Descriptivos 1. Globulares Albúminas: Seroalbúmina (sangre), ovoalbúmina (huevo), lactoalbúmina (leche) Hormonas: Insulina, hormona del crecimiento, prolactina, tirotropina 2. Fibrosas Colágenos: en tejidos conjuntivos, cartilaginosos Queratinas: En formaciones epidérmicas: pelos, uñas, plumas, cuernos. Elastinas: En tendones y vasos sanguíneos Fibroínas: En hilos de seda, (arañas, insectos)

ESTRUCTURA PRIMARIA La estructura primaria es la secuencia y número de aminoácidos de la proteína. Nos indica qué aminoácidos componen la cadena polipeptídica y el orden de aminoácidos. La función de una proteína depende de su secuencia y de la forma que ésta adopte. Enlace que la mantiene: Peptídico. Los cambios aunque sean pequeños en ésta estructura, tienen un efecto fundamental en las propiedades de las proteínas. Ej. Anemia de células falciformes.
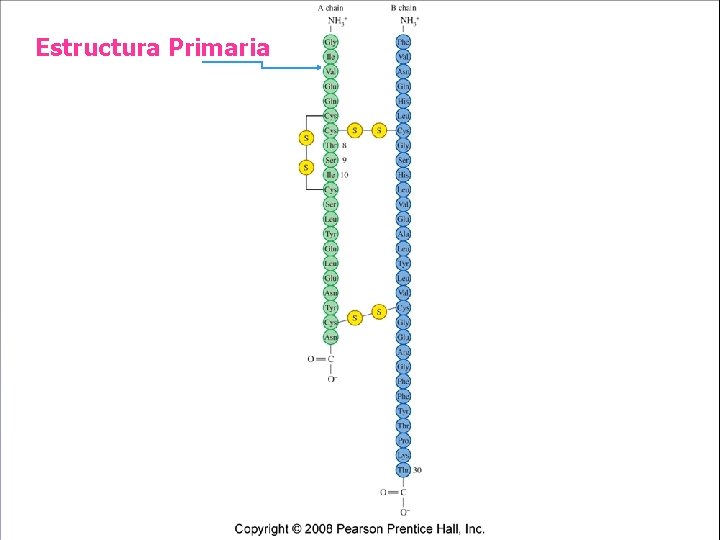
Estructura Primaria

Error en secuencia de aminoácidos

ESTRUCTURA SECUNDARIA La estructura secundaria es la disposición de la secuencia de aminoácidos en el espacio. Los aminoácidos, a medida que van siendo enlazados durante la síntesis protéica y gracias a la capacidad de giro de sus enlaces, adquieren una disposición espacial estable. Resulta de la interacción de los enlaces amídicos cercanos. Existen dos tipos de estructura secundaria:

1. Hélice α : Se forma al enrollarse helicoidalmente sobre sí misma la estructura primaria. Se debe a la formación de enlaces de hidrógeno entre el -C=O de un aminoácido y el -NH- del cuarto aminoácido que le sigue. Cada vuelta de la espiral tiene de 3 a 6 a. a. . Las cadenas laterales (R) , se proyectan hacia el exterior del esqueleto.
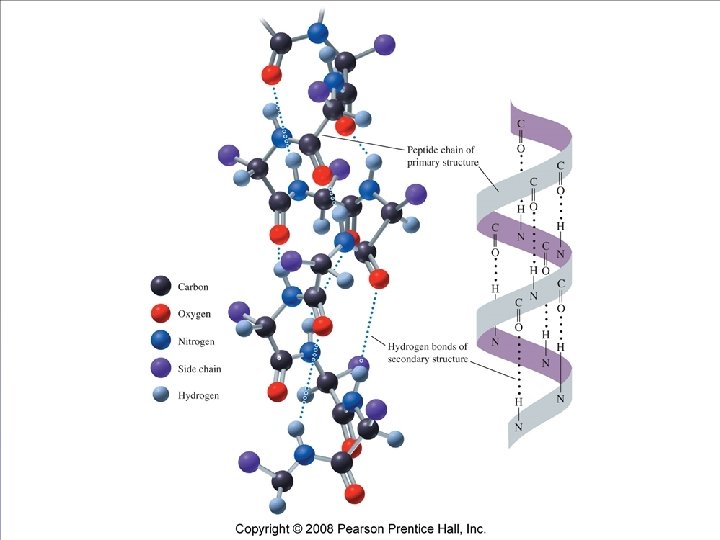
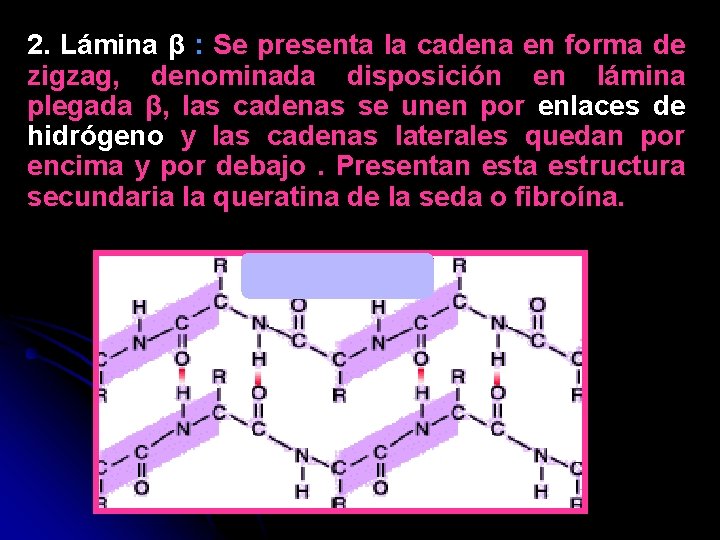
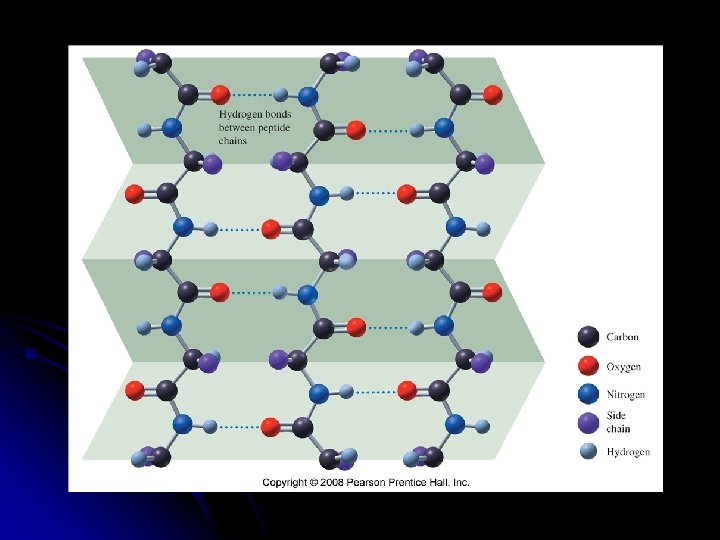
2. Lámina β : Se presenta la cadena en forma de zigzag, denominada disposición en lámina plegada β, las cadenas se unen por enlaces de hidrógeno y las cadenas laterales quedan por encima y por debajo . Presentan esta estructura secundaria la queratina de la seda o fibroína.
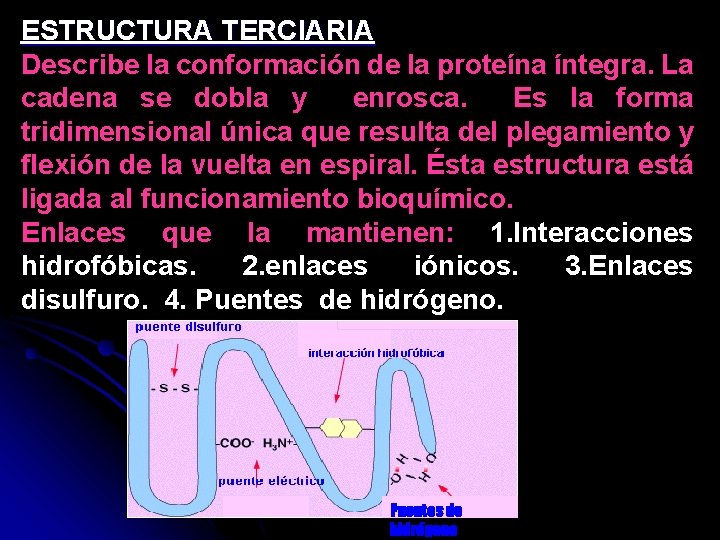
ESTRUCTURA TERCIARIA Describe la conformación de la proteína íntegra. La cadena se dobla y enrosca. Es la forma tridimensional única que resulta del plegamiento y flexión de la vuelta en espiral. Ésta estructura está ligada al funcionamiento bioquímico. Enlaces que la mantienen: 1. Interacciones hidrofóbicas. 2. enlaces iónicos. 3. Enlaces disulfuro. 4. Puentes de hidrógeno
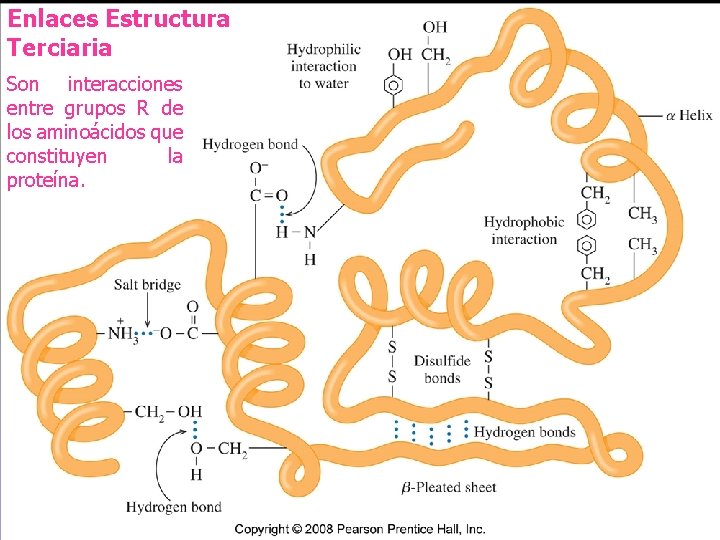
Enlaces Estructura Terciaria Son interacciones entre grupos R de los aminoácidos que constituyen la proteína.
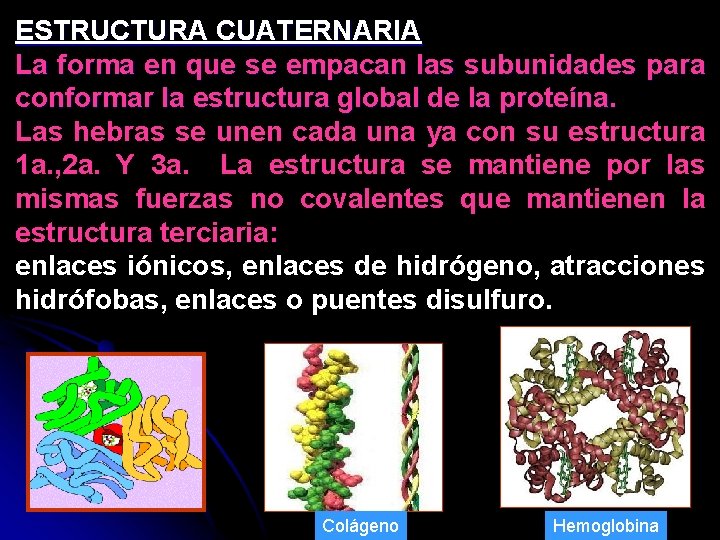
ESTRUCTURA CUATERNARIA La forma en que se empacan las subunidades para conformar la estructura global de la proteína. Las hebras se unen cada una ya con su estructura 1 a. , 2 a. Y 3 a. La estructura se mantiene por las mismas fuerzas no covalentes que mantienen la estructura terciaria: enlaces iónicos, enlaces de hidrógeno, atracciones hidrófobas, enlaces o puentes disulfuro. Colágeno Hemoglobina
Cuatro Niveles de Estructura Proteica Estructura Primaria Secuencia de Aminoácidos

Estructura Secundaria Hélice

Estructura Terciaria Péptido Individual Doblado

Estructura Cuaternaria (Agregado de Dos o Más Péptidos)

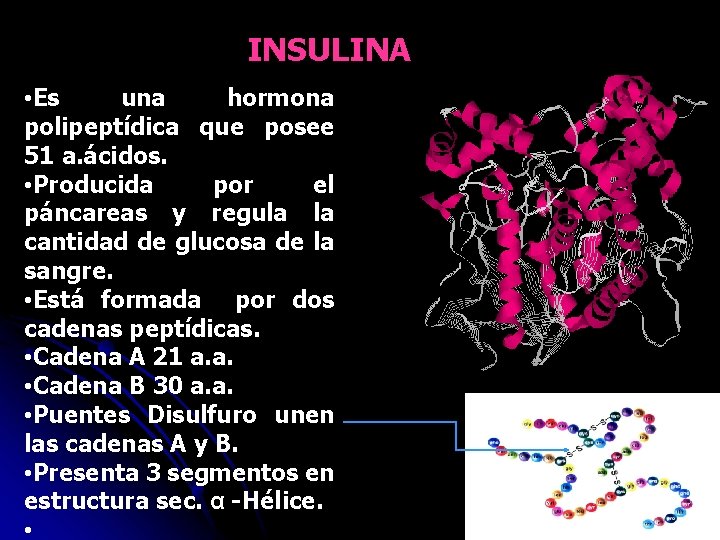
INSULINA • Es una hormona polipeptídica que posee 51 a. ácidos. • Producida por el páncareas y regula la cantidad de glucosa de la sangre. • Está formada por dos cadenas peptídicas. • Cadena A 21 a. a. • Cadena B 30 a. a. • Puentes Disulfuro unen las cadenas A y B. • Presenta 3 segmentos en estructura sec. α -Hélice. •
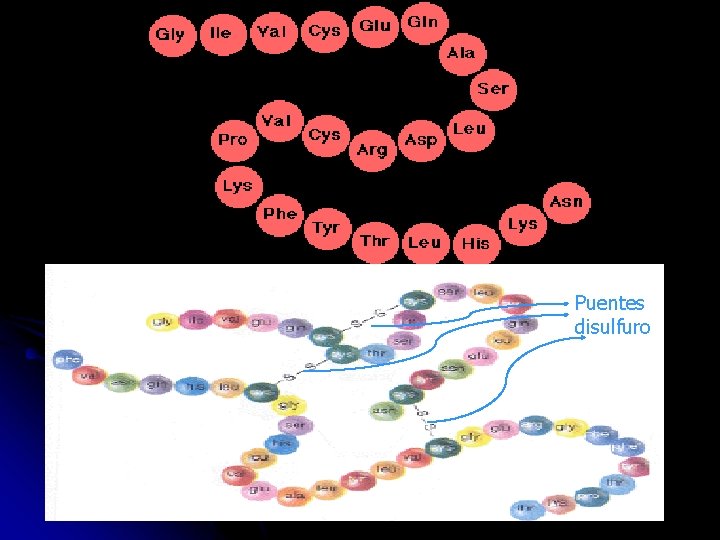
Puentes disulfuro
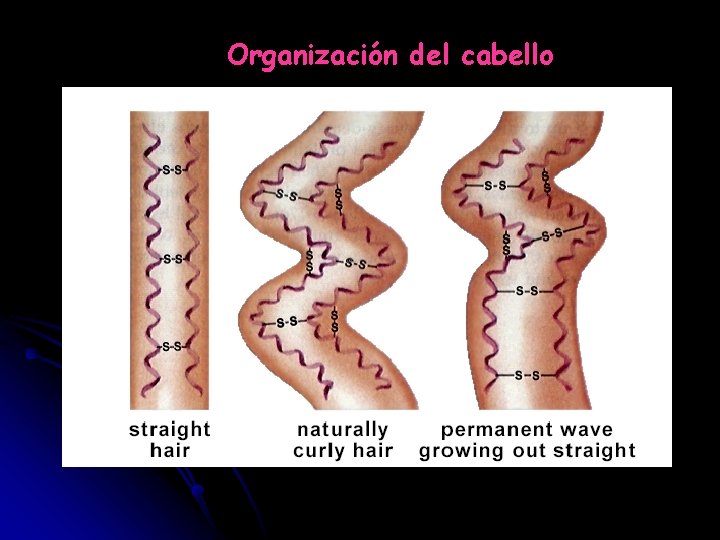
Organización del cabello

MIOGLOBINA La mioglobina es una proteína muscular, con estructura primaria formada por 153 unidades de residuos de aminoácidos, secundaria de espiral y estructura terciaria que forma una estructura compacta estable. Consta de una sola cadena polipeptídica.
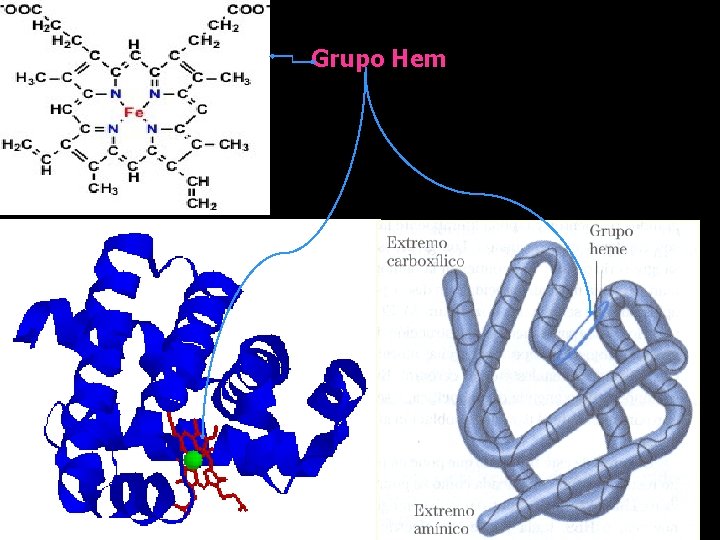
Grupo Hem

HEMOGLOBINA La hemoglobina consta de varias cadenas polipeptídicas. También es una proteína conjugada, compleja o plus, contiene el grupo hem. Está formada por 4 subunidades (dos subunidades y dos subunidades ). Presenta por lo tanto estructura cuaternaria.
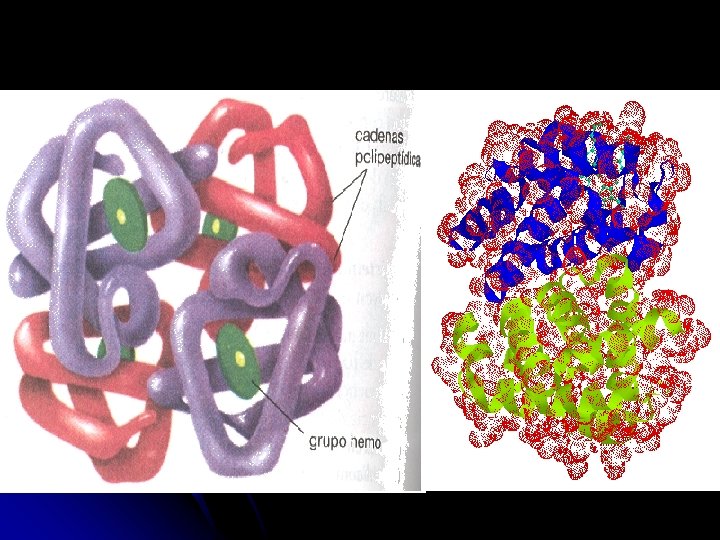

COLÁGENO • El colágeno es la proteína más abundante en los animales superiores, constituyendo un tercio de todas las proteínas del cuerpo. Se considera como el elemento estructural más importante en los seres vivos. • Está compuesto por tres cadenas que forman una triple hélice. • Cada cadena tiene unos 1400 aminoácidos de los cuales uno de cada tres es una glicina.

• Además se repiten regularmente otros aminoácidos, prolina e hidroxiprolina, poco frecuentes en otras proteínas. • La presencia de dichos aminoácidos permite que las tres cadenas se enrrollen una alrededor de la otra formando una fibra muy resistente. • Entre las cadenas se establecen puentes de hidrógeno que confieren al colágeno una gran estabilidad


• Se utiliza en cirugía cosmética en terapia de sustitución de colágeno, el cuál consiste en inyectar subcutáneamente colágeno natural o sintético en las áreas en las que se quiere que desaparezcan arrugas, cicatrices u otras imperfecciones de la piel. • Además se está utilizando como soporte en cultivos de células cartilaginosas para implantar posteriormente a pacientes que han sufrido lesiones, con una nueva tecnología denominada ingeniería de tejidos.

DESNATURALIZACIÓN Todo cambio que altere la configuración tridimensional única de una molécula de proteína sin causar una ruptura simultánea de los enlaces peptídicos.

Al destruirse la estructura secundaria y terciaria se da un cambio drástico en la naturaleza física y bioquímica de la molécula. Las proteínas se transforman en filamentos lineales y delgados que se entrelazan hasta formar compuestos fibrosos e insolubles en agua.

DESNATURALIZACIÓN REVERSIBLE

La desnaturalización puede ser reversible (renaturalización) pero en muchos casos es irreversible. Los agentes que pueden desnaturalizar a una proteina pueden ser: calor excesivo; sustancias que modifican el p. H; alteraciones en la concentración; alta salinidad; agitación molecular; etc. . .

1. Calor y Radiación UV: rompen las fuerzas de dispersión y los enlaces de H. (Exposición intensa al sol desnaturaliza las proteínas de la piel. ) 2. Ácidos y bases: rompen enlaces iónicos y puentes de H. Alteran el estado de ionización del grupo amino y carboxilo, por lo que producen la coagulación. 3. Solventes orgánicos: rompen los enlaces de H intermoleculares e intramoleculares, formando nuevos enlaces de H. Por ejemplo el alcohol, forman puentes de H con el OH. Etanol y a. isopropílico son antisépticos porque desnaturalizan las proteínas de las bacterias.

4. Sales de metales pesados: (Pb, Hg, Ag) Se combinan con los aniones carboxilato y puentes disulfuro, precipitando las proteínas como complejo metal-proteína. El nitrato de plata se usa como antiséptico en ojos de recien nacidos. Leche y clara de huevo se usan como antídotos en intoxicaciones por metales pesados.

ENZIMAS Todas las enzimas son proteínas. Algunas son simples (pepsina, ribonucleasa) y otras conjugadas (llamadas holoenzimas). Apoenzima: segmento polipeptídico de la enzima. Coenzima: porción orgánica no proteíca. Es una creencia general que todas las reacciones catalíticas ocurren por lo menos en dos etapas. E +S E-S PRODUC. + ENZIMA

Toda enzima tiene un sitio activo que es su porción funcional. Ésto incluye el sitio de unión, que es el que atrae al sustrato y el sitio catalítico que es el encargado de llevar a cabo la catálisis.


CLASE EJEMPLOS I. II. Deshidrogenasa, peroxidasa, oxidas a Transaminasa, cinasa, transacetilasa

III. IV. Lipasa, fosfata sa, amilasa, amidasa, peptidasa. Descarboxilasa, fumarasa, aldolasa.

5. Isomerasas V. VI Isomerasa, racemasa, epimerasa, mutasa Sintetasa, tiocinasa

N I F
- Slides: 52