PROTENAS CONJUGADAS MIOGLOBINA HEMOGLOBINA ANEMIA FERROPRIVA 1 PROTENAS
PROTEÍNAS CONJUGADAS MIOGLOBINA HEMOGLOBINA ANEMIA FERROPRIVA 1

PROTEÍNAS CONJUGADAS São aquelas que através de hidrólise liberam outro componente além dos aminoácidos. APOPROTEÍNA GRUPO PROSTÉTICO - Nucleoproteínas Ácidos Nucleicos - Lipoproteínas Lipídeos - Glicoproteínas Glicídica/ carboidrato - Metaloproteínas Metal - Fosfoproteínas Ácido Fosfórico - Porfirinoproteínas/ Hemoproteínas Porfirina 2
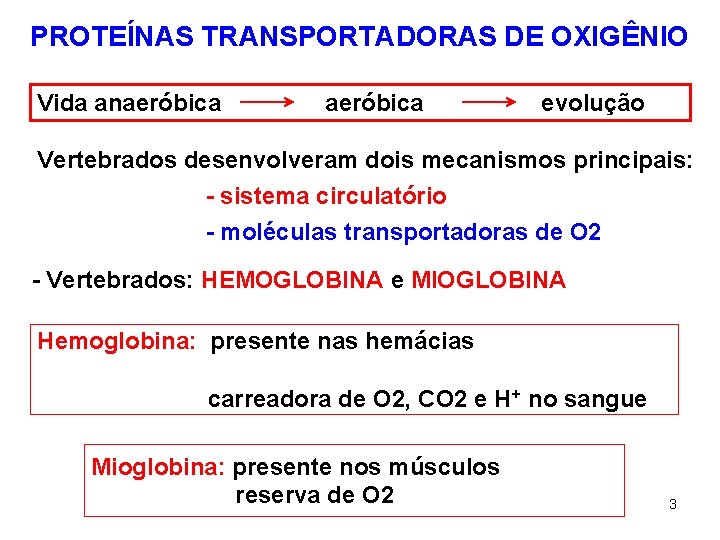
PROTEÍNAS TRANSPORTADORAS DE OXIGÊNIO Vida anaeróbica evolução Vertebrados desenvolveram dois mecanismos principais: - sistema circulatório - moléculas transportadoras de O 2 - Vertebrados: HEMOGLOBINA e MIOGLOBINA Hemoglobina: presente nas hemácias carreadora de O 2, CO 2 e H+ no sangue Mioglobina: presente nos músculos reserva de O 2 3

HEMÁCIAS Quase todo oxigênio transportado pelo sangue está ligado à Hemoglobina. Os eritrócitos são discos bicôncavos pequenos (6 -9 μm). São especializados no transporte de oxigênio. 600 litros de oxigênio dos pulmões aos tecidos por dia. 4

HEMÁCIAS No processo de maturação, perdem as organelas intracelulares e sintetizam grandes quantidades de Hb. Duram cerca de 120 dias. A Hb que deixa os pulmões está 96% saturada com oxigênio. 5

PROTEÍNAS CONJUGADAS são aquelas que através de hidrólise liberam outro componente além dos aminoácidos. APOPROTEÍNA GRUPO PROSTÉTICO - Porfirinoproteínas/ Porfirina Hemoproteínas 6
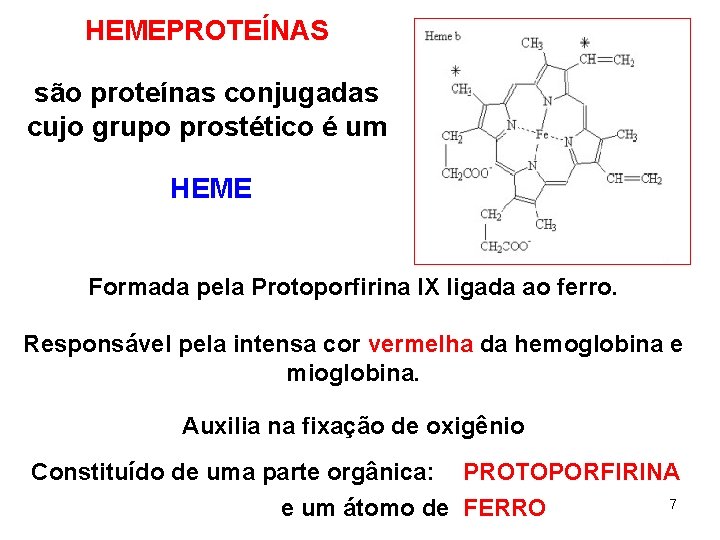
HEMEPROTEÍNAS são proteínas conjugadas cujo grupo prostético é um HEME Formada pela Protoporfirina IX ligada ao ferro. Responsável pela intensa cor vermelha da hemoglobina e mioglobina. Auxilia na fixação de oxigênio Constituído de uma parte orgânica: PROTOPORFIRINA 7 e um átomo de FERRO
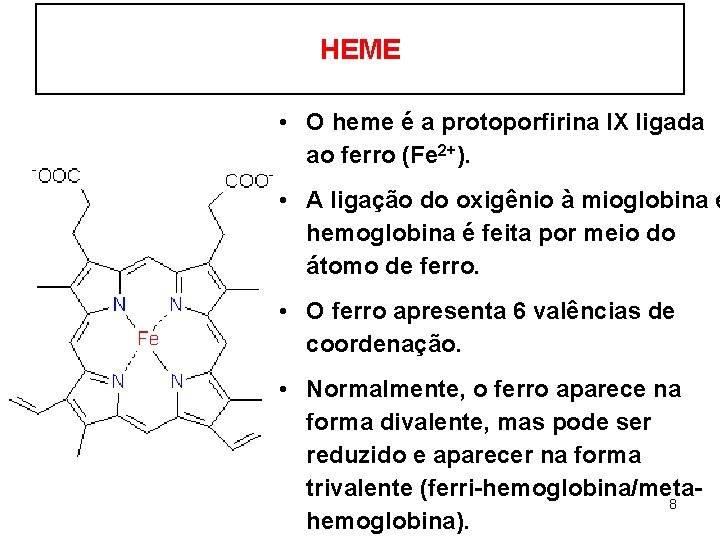
HEME • O heme é a protoporfirina IX ligada ao ferro (Fe 2+). • A ligação do oxigênio à mioglobina e hemoglobina é feita por meio do átomo de ferro. • O ferro apresenta 6 valências de coordenação. • Normalmente, o ferro aparece na forma divalente, mas pode ser reduzido e aparecer na forma trivalente (ferri-hemoglobina/meta 8 hemoglobina).
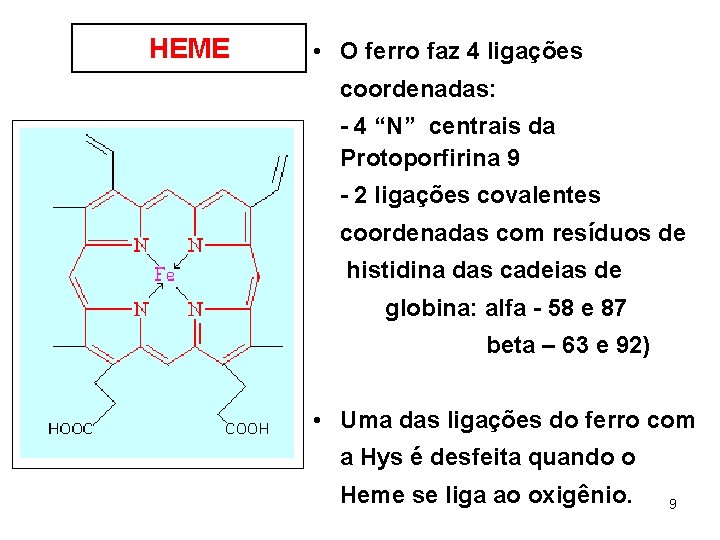
HEME • O ferro faz 4 ligações coordenadas: - 4 “N” centrais da Protoporfirina 9 - 2 ligações covalentes coordenadas com resíduos de histidina das cadeias de globina: alfa - 58 e 87 beta – 63 e 92) • Uma das ligações do ferro com a Hys é desfeita quando o Heme se liga ao oxigênio. 9
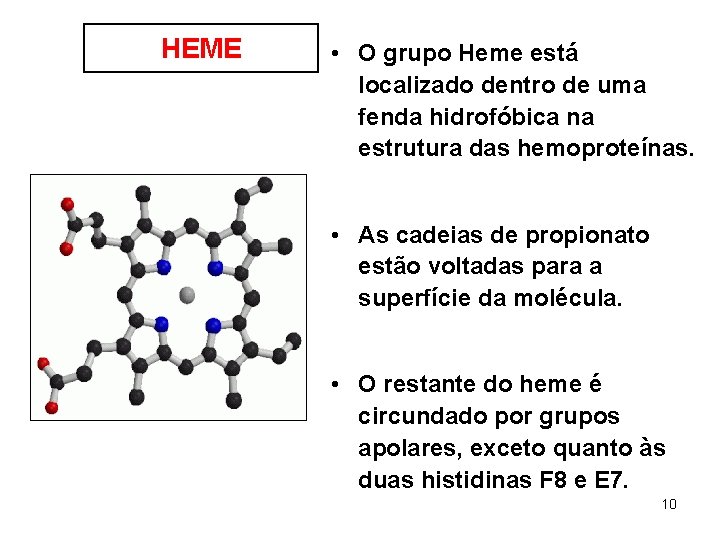
HEME • O grupo Heme está localizado dentro de uma fenda hidrofóbica na estrutura das hemoproteínas. • As cadeias de propionato estão voltadas para a superfície da molécula. • O restante do heme é circundado por grupos apolares, exceto quanto às duas histidinas F 8 e E 7. 10
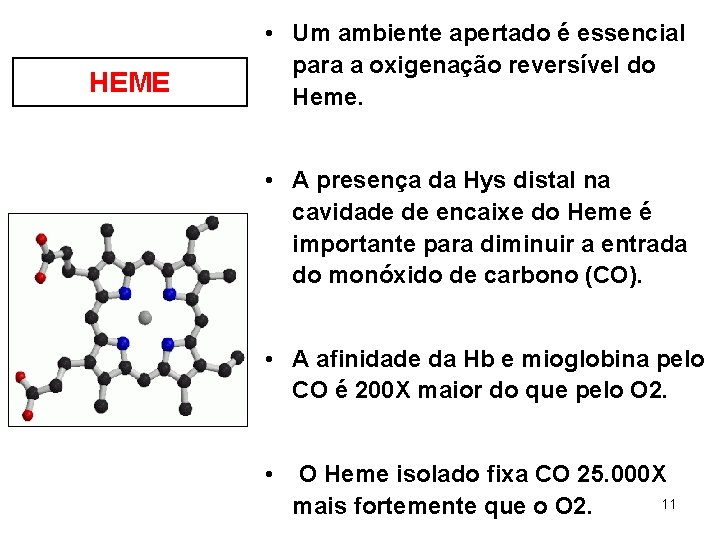
HEME • Um ambiente apertado é essencial para a oxigenação reversível do Heme. • A presença da Hys distal na cavidade de encaixe do Heme é importante para diminuir a entrada do monóxido de carbono (CO). • A afinidade da Hb e mioglobina pelo CO é 200 X maior do que pelo O 2. • O Heme isolado fixa CO 25. 000 X 11 mais fortemente que o O 2.
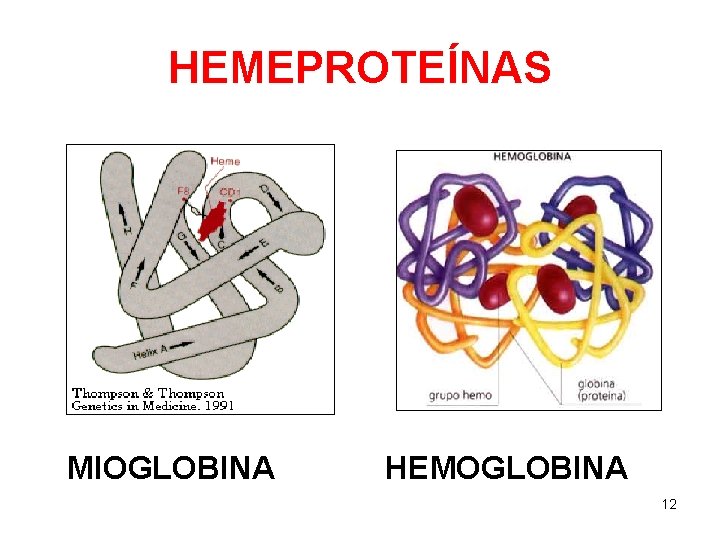
HEMEPROTEÍNAS MIOGLOBINA HEMOGLOBINA 12

MIOGLOBINA • Funciona como um reservatório de oxigênio nos músculos. • Apresenta uma cadeia de globina e um grupo heme. • 80% em alfa-hélice. • 8 segmentos separados por dobras e curvas. • PM : 16. 700 daltons. • 153 aa • É abundante nos músculos dos mamíferos marinhos como a baleia e o golfinho. 13

• Estrutura tridimensional: John Kendrew, 1957. MIOGLOBINA • A estrutura da mioglobina é compacta. • Aa com grupos R apolares no interior da molécula e aa com grupos R polares na parte externa. • Quatro resíduos de Pro ocorrem nas curvas, além de Ser, Thr e Asn. 14

MIOGLOBINA • O grupo Heme localiza-se numa fenda, cercado por aa apolares, exceto 2 resíduos de Hys. • Hys proximal liga-se diretamente ao ferro. • Hys distal estabiliza a ligação do Heme com o oxigênio. • Mioglobinas de diferentes espécies tem estruturas primárias homólogas e estrutura terciária semelhante. • A mioglobina apresenta alta afinidade pelo oxigênio. 15

HEMOGLOBINA Marx Perutz, 1962. Análises com difração de raios X. A molécula de Hb é esférica, com diâmetro aproximado de 5, 5 nm. Segmentos em α-hélice, separados por curvaturas. Grupos Heme localizados em uma fenda. Cada cadeia polipeptídica liga-se a um grupo Heme. Cada Heme liga-se à globina por meio de um resíduo de Hys. 16
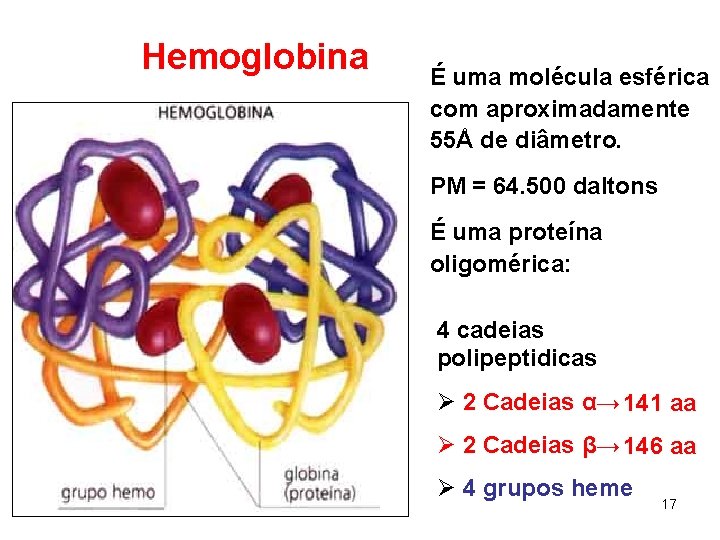
Hemoglobina É uma molécula esférica com aproximadamente 55Å de diâmetro. PM = 64. 500 daltons É uma proteína oligomérica: 4 cadeias polipeptidicas Ø 2 Cadeias α→ 141 aa Ø 2 Cadeias β→ 146 aa Ø 4 grupos heme 17

Hemoglobina As cadeias alfa e beta apresentam estruturas semelhantes. As cadeias da Hemoglobina são semelhantes à cadeia única da mioglobina. 70% das cadeias estão em α- hélice. Os dobramentos e ângulos de cada cadeia são semelhantes. Cadeias α e β estão enoveladas. Cada cadeia de globina se liga a um grupo Heme. 18

Hemoglobina Poucos pontos de contato entre α 1α 2 e entre β 1β 2. As cadeias se encaixam formando pares α 1β 1 e α 2β 2. Estrutura quaternária característica. A estrutura do tetrâmero é mantida por pontes de H e ligações salinas. A hemoglobina é uma proteína alostérica. 19
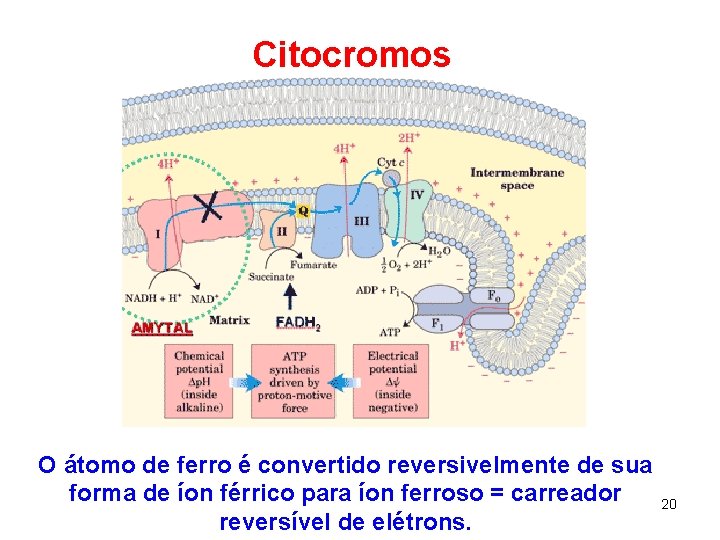
Citocromos O átomo de ferro é convertido reversivelmente de sua forma de íon férrico para íon ferroso = carreador reversível de elétrons. 20
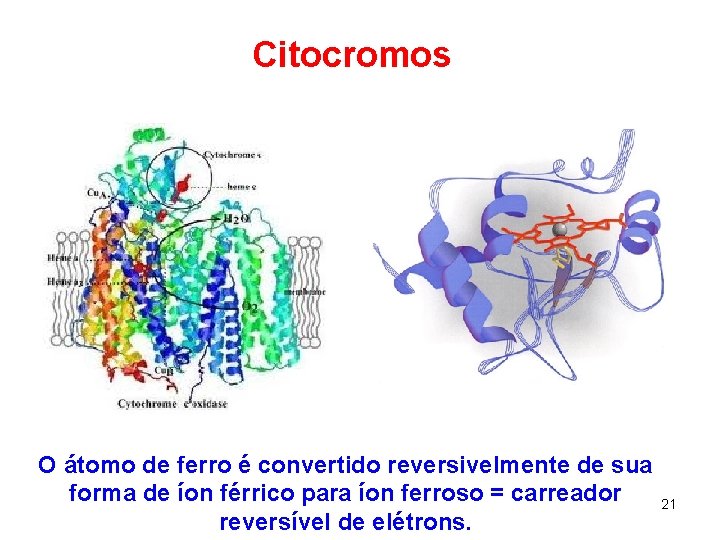
Citocromos O átomo de ferro é convertido reversivelmente de sua forma de íon férrico para íon ferroso = carreador reversível de elétrons. 21

Anemia é uma condição na qual a capacidade das células vermelhas de transportar oxigênio é insuficiente para suprir as necessidades fisiológicas, as quais variam com a idade, gênero, altitude, hábito de fumar e gravidez. OMS - condição na qual o conteúdo de hemoglobina no sangue está abaixo do normal como resultado da carência de um ou mais nutrientes essenciais, seja qual for a causa dessa deficiência. 22 22

Anemia Causas: deficiência de vários nutrientes como ferro, zinco, vitamina B 12 e proteínas. Anemia Ferropriva: causada por deficiência de ferro. Comum - 90% das anemias - carência de Ferro. Nutriente essencial para a vida e atua principalmente na síntese das células vermelhas do sangue e no transporte do oxigênio para todas as células do corpo. Crianças, gestantes, lactantes, meninas adolescentes e mulheres adultas em fase de reprodução são os grupos mais afetados pela anemia. Homens (adolescentes/ adultos/ idosos) - podem ser afetados 23 pela anemia.
- Slides: 23