MINISTRIO DA EDUCAO SECRETARIA DE EDUCAO PROFISSIONAL E


























- Slides: 36

MINISTÉRIO DA EDUCAÇÃO SECRETARIA DE EDUCAÇÃO PROFISSIONAL E TECNOLÓGICA INSTITUTO FEDERAL DE EDUCAÇÃO, CIÊNCIA E TECNOLOGIA DE SANTA CATARINA CAMPUS LAGES Soluções e Expressão das concentrações Prof. Marcel Piovezan marcel. piovezan@ifsc. edu. br Curso Técnico concomitante em Análises Química Unidade Curricular: Química Analítica Módulo 2

BRIAN SYTNYK/ MASTERFILE/OTHER-IMAGES Introdução às expressões de concentração das soluções aquosas X SAIR

Os conceitos de solução, solvente e soluto HIGHRES PRESS STOCK/CID Solução: mistura homogênea (soluto + solvente) Soluto: dissolvido pelo solvente Solvente: substância utilizada para dissolver outra Grande parte das soluções é líquida, mas, como vemos aqui, existem soluções sólidas, como o ouro, e gasosas, como o ar atmosférico. 1 Introdução às expressões de concentração das soluções aquosas X SAIR

"Solutos diferentes apresentam solubilidades diferentes“ - Solução diluída - quantidade grande de solvente em relação ao soluto Ex: 2 g de Na. Cl em 100 m. L de H 2 O a 18ºC - Solução concentrada - quantidade grande de soluto em relação ao solvente Ex: 30 g de Na. Cl em 100 m. L de H 2 O a 18ºC X SAIR

- Solução saturada - contém a máxima quantidade de sal que se dissolve em 100 m. L de H 2 O a uma determinada temperatura. Ex: 36 g de Na. Cl em 100 m. L de H 2 O a 18 ºC -Solução supersaturada - apresenta uma maior quantidade de soluto do que o solvente consegue dissolver. Essa solução apresenta corpo de chão, corpo de fundo ou precipitado. Ex: 40 g de Na. Cl em 100 m. L de H 2 O a 18ºC X SAIR

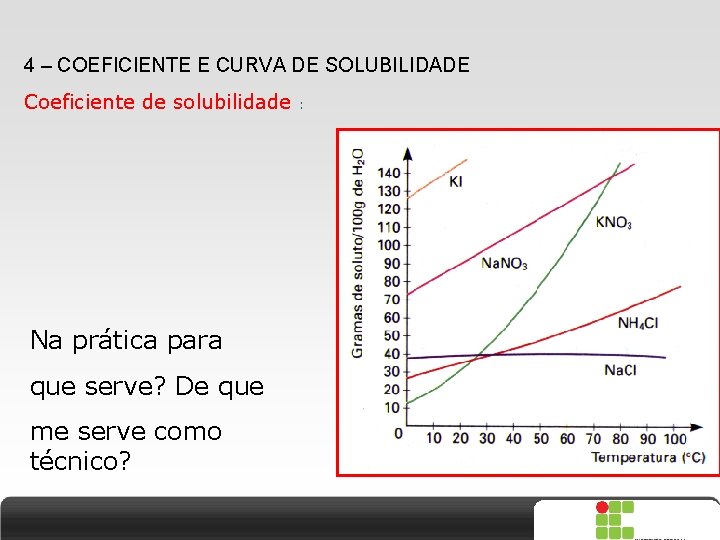
4 – COEFICIENTE E CURVA DE SOLUBILIDADE Coeficiente de solubilidade : Na prática para que serve? De que me serve como técnico? X SAIR

O preparo de uma solução aquosa em laboratório THE NEXT/CID Solução aquosa de Na. OH O soluto é transferido para o frasco e, em seguida, adiciona-se um pouco de água destilada e agita-se até que todo o sólido se dissolva. Massa do soluto = 80 g M(Na. OH) = 40 g • mol– 1 Finalmente, acrescenta- se água com auxílio de uma pisseta até atingir a marca de 1. 000 m. L. 1 Introdução às expressões de concentração das soluções aquosas Massa do soluto = 80 g Volume da solução = 1 L X SAIR

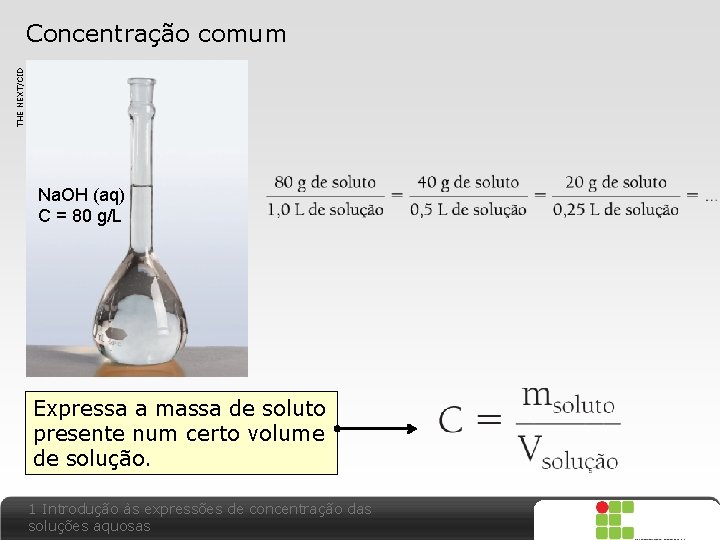
Concentração comum THE NEXT/CID Relação entre massa de soluto e volume de sua solução Na. OH (aq) C = 80 g/L A solução preparada contém 80 g de soluto dissolvidos em 1, 0 L de solução. 1 Introdução às expressões de concentração das soluções aquosas X SAIR

THE NEXT/CID Concentração comum Na. OH (aq) C = 80 g/L Expressa a massa de soluto presente num certo volume de solução. 1 Introdução às expressões de concentração das soluções aquosas X SAIR

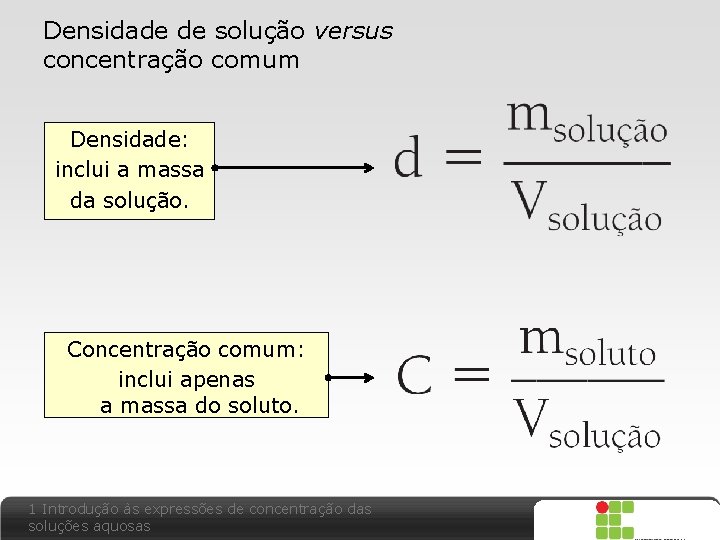
Densidade de solução versus concentração comum Densidade: inclui a massa da solução. Concentração comum: inclui apenas a massa do soluto. 1 Introdução às expressões de concentração das soluções aquosas X SAIR

BRIAN SYTNYK/ MASTERFILE/OTHER-IMAGES Concentração em quantidade de matéria e outras expressões de concentração X SAIR

Concentração em quantidade de matéria e outras expressões de concentração THE NEXT/CID Concentração em quantidade de matéria X SAIR

Relembrando. . . Mol É a quantidade de uma espécie química que contém 6, 02 x 1023 partículas (átomos, moléculas, íons, elétrons, etc). Massa Molar (M ou MM) A massa em g de 1 mol da espécie química. Massa molar atômica Peso atômico Ex: 1 mol de H = 1, 0079 g de H, 1 mol de Fe = 55, 847 g de Fe Massa molar molecular Ex: 1 mol de CO 2 = 44, 01 g de CO 2 1 mol de H 2 O = 18, 0158 g de H 2 O X SAIR

Concentração da solução Concentração Molar (Molaridade) Concentração da solução expressa em mols do soluto por litros do solvente. Solução 1 molar = 1 mol da substância / 1 L de solução ou 1 molar = 1 mmol da substância / 1 m. L de solução X SAIR

Densidade = massa da substância / volume Unidades: (g/m. L) ou (g/cm 3) ou (kg/L) Expressões de resultados analíticos: Relação m/m Amostras sólidas % analito = massa (g) analito x 100 massa (g) amostra Relação m/v % analito = massa (g) analito Amostras líquidas x 100 volume (m. L) amostra Relação v/v % analito = volume (m. L) analito x 100 volume (m. L) amostra X SAIR

Título em massa Expressa a relação entre a massa de soluto e a massa de solução. 2 Concentração em quantidade de matéria e outras expressões de concentração X SAIR

Título em volume Expressa a relação entre o volume de soluto e o volume de solução. 2 Concentração em quantidade de matéria e outras expressões de concentração X SAIR

Porcentagem em massa e em volume Quando o título em massa é expresso em porcentagem, tem-se a porcentagem em massa do soluto na solução. 2 Concentração em quantidade de matéria e outras expressões de concentração X SAIR

Porcentagem em volume Quando o título em volume é expresso em porcentagem, tem-se a porcentagem em volume do soluto na solução. 2 Concentração em quantidade de matéria e outras expressões de concentração X SAIR

Exercícios 1. Calcular a massa em gramas em 1 mol de Ca. SO 4. 7 H 2 O (Ca = 40, 08; S = 32, 06; O = 15, 99; H = 1, 01) R: 262, 14 g/mol 2. Calcular o número de mols em 500 mg de Na 2 CO 3. (Na = 22, 990; C = 12, 011) R: 0, 0047 mol ou 4, 7 x 10 -3 mol 3. Quantos miligramas estão contidos em 0, 250 mmol de Fe 2 O 3? (Fe = 55, 847) R: 39, 923 mg 4. Calcule a concentração , em g/L da solução obtida ao dissolver cloreto de sódio em 50 cm 3 de água? R: 80 g/L 4 g de 5. O soro fisiológico contém 0, 900 g de Na. Cl, em 100 m. L de solução aquosa. Calcule a concentração do sal expressa em mol L -1 ? R: 0, 15 mol L-1 X SAIR

Vamos exercitar mais. . X SAIR

1. Um técnico de análises químicas precisa preparar uma solução de concentração 0, 1 mol/L de Na. OH em um balão volumétrico de 50 m. L a) Qual a massa molar da base (g/mol) M = 0, 1 mol/L b) Qual a massa a ser pesada da base em gramas e em miligramas para preparar essa solução. V = 50 m. L ou 0, 05 L c) Será necessário preparar mais volume de solução (500 m. L), quanto de base devo pesar para obter a mesma concentração de 0, 1 mol/L Na. OH X SAIR

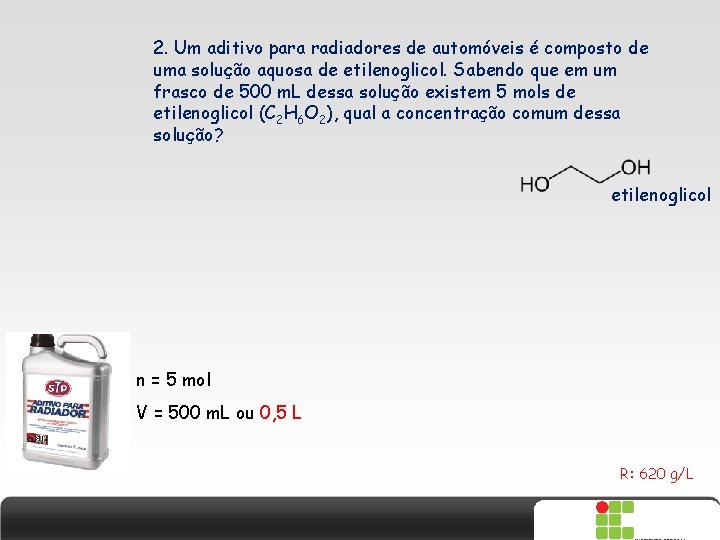
2. Um aditivo para radiadores de automóveis é composto de uma solução aquosa de etilenoglicol. Sabendo que em um frasco de 500 m. L dessa solução existem 5 mols de etilenoglicol (C 2 H 6 O 2), qual a concentração comum dessa solução? etilenoglicol n = 5 mol V = 500 m. L ou 0, 5 L R: 620 g/L X SAIR

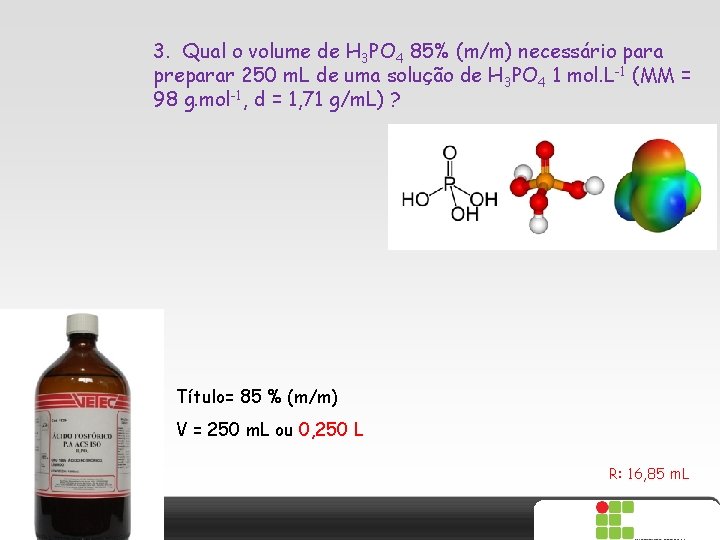
3. Qual o volume de H 3 PO 4 85% (m/m) necessário para preparar 250 m. L de uma solução de H 3 PO 4 1 mol. L-1 (MM = 98 g. mol-1, d = 1, 71 g/m. L) ? Título= 85 % (m/m) V = 250 m. L ou 0, 250 L R: 16, 85 m. L X SAIR

4. Qual a massa de iodeto de potássio para preparar 2 L de uma solução de KI 10% (m/v)? R: 0, 2 kg ou 200 g X SAIR

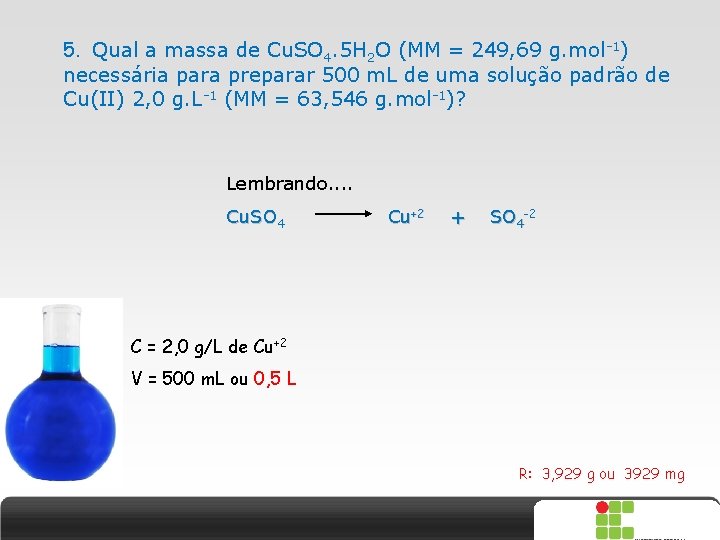
5. Qual a massa de Cu. SO 4. 5 H 2 O (MM = 249, 69 g. mol-1) necessária para preparar 500 m. L de uma solução padrão de Cu(II) 2, 0 g. L-1 (MM = 63, 546 g. mol-1)? Lembrando. . Cu. SO 4 Cu+2 + SO 4 -2 C = 2, 0 g/L de Cu+2 V = 500 m. L ou 0, 5 L R: 3, 929 g ou 3929 mg X SAIR

6. Uma solução de ácido Nítrico tem concentração igual a 126 g/L e densidade igual a 1, 008 g/m. L. Quai as frações molares do soluto e do solvente nessa solução? C = 126 g/L d = 1, 008 g/m. L R: XHNO 3 = 0, 035 ou 3, 5 % XH 2 O = 0, 965 ou 96, 5 % X SAIR

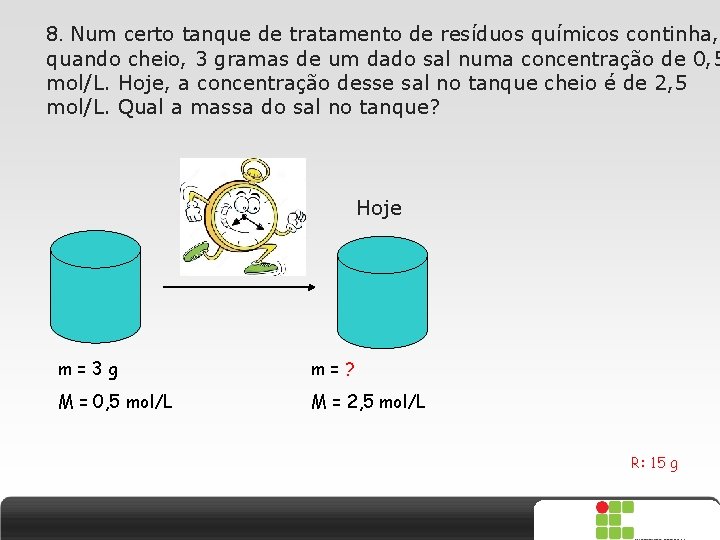
8. Num certo tanque de tratamento de resíduos químicos continha, quando cheio, 3 gramas de um dado sal numa concentração de 0, 5 mol/L. Hoje, a concentração desse sal no tanque cheio é de 2, 5 mol/L. Qual a massa do sal no tanque? Hoje m=3 g m=? M = 0, 5 mol/L M = 2, 5 mol/L R: 15 g X SAIR

9. O soro fisiológico utilizado para limpar lentes de contato é uma solução aquosa de Na. Cl 0, 9 %. Se, em um frasco contendo 100 m. L desse soro, forem adicionados 10, 8 g de Na. Cl, qual será a concentração molar da solução preparada? m = 10, 8 g de Na. Cl M=? Título = 0, 9 % (m/m) V = 100 m. L ou 0, 1 L R: massa final = 10, 8 g M = 1, 85 mol/L X SAIR

Diluição e mistura de soluções X SAIR BRIAN SYTNYK/ MASTERFILE/OTHER-IMAGES

Diluição de soluções Adição de solvente a uma solução I II O pó dissolvido em água. Muito concentrado Acrescenta-se mais água: diluição. Menos concentrado ou mais diluído Diluição de pó em solvente água 3 Diluição e mistura de soluções X SAIR

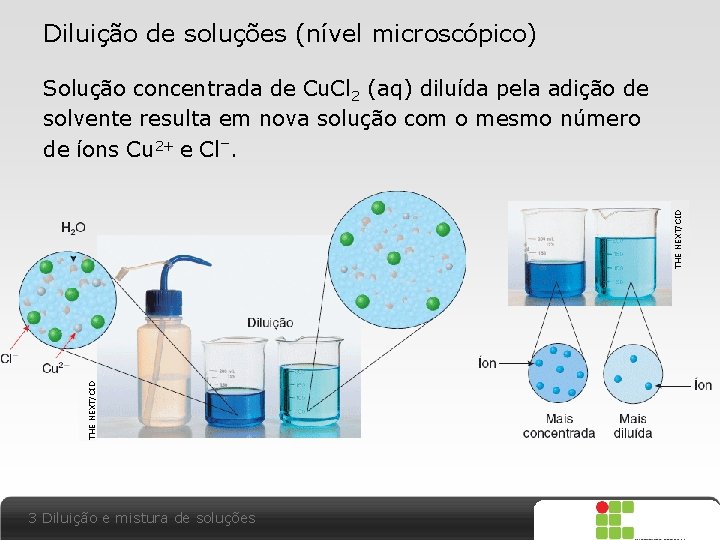
Diluição de soluções (nível microscópico) THE NEXT/CID Solução concentrada de Cu. Cl 2 (aq) diluída pela adição de solvente resulta em nova solução com o mesmo número de íons Cu 2+ e Cl–. 3 Diluição e mistura de soluções X SAIR

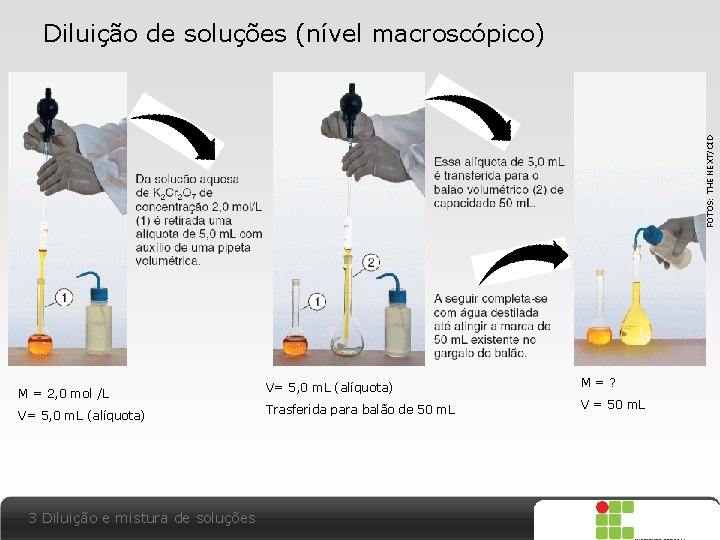
FOTOS: THE NEXT/CID Diluição de soluções (nível macroscópico) M = 2, 0 mol /L V= 5, 0 m. L (alíquota) M=? V= 5, 0 m. L (alíquota) Trasferida para balão de 50 m. L V = 50 m. L 3 Diluição e mistura de soluções X SAIR

Cálculos envolvendo diluição A quantidade de soluto permanece a mesma. 3 Diluição e mistura de soluções X SAIR

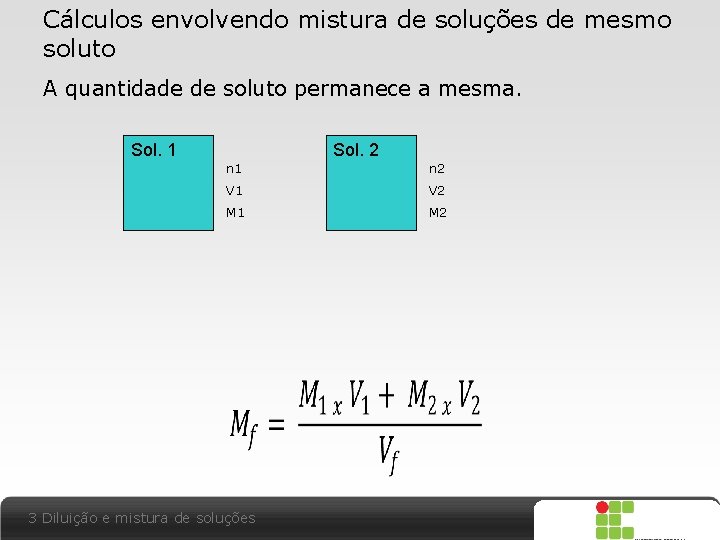
Cálculos envolvendo mistura de soluções de mesmo soluto A quantidade de soluto permanece a mesma. Sol. 1 Sol. 2 n 1 n 2 V 1 V 2 M 1 M 2 3 Diluição e mistura de soluções X SAIR

Cálculos envolvendo mistura de soluções de mesmo soluto 1) Diluição é uma operação muito utilizada no nosso dia-a-dia, quando, por exemplo, preparamos um refresco a partir do suco concentrado. Considere 100 m. L de determinado suco em que a concentração do soluto seja de 0, 4 mol/L. Qual o volume em m. L de água, que deverá ser acrescentado para que a concentração do soluto caia para 0, 04 mol/L? 1) Um volume de 200 m. L de uma solução aquosa de glicose (C 5 H 12 O 6) de concentração igual a 60 g/L foi misturada a 300 m. L de uma solução de glicose de concentração igual a 120 g/L. Determine a concetração em g/L da solução final. 1) Uma solução aquosa 2 mol/L de Na. Cl de volume 50 m. L foi misturada a 100 m. L de uma solução aquosa de Na. Cl 0, 5 mol/L. Calcule a nova concentração da solução. 3 Diluição e mistura de soluções X SAIR