Enstrmantal Analiz II Prof Dr Hasan Cesur Ondokuz

















- Slides: 48

Enstrümantal Analiz II Prof. Dr. Hasan Cesur Ondokuz Mayıs Üniversitesi Fen Edebiyat Fakültesi, Kimya Bölümü, 5139 -Kurupelit Samsun 1

Enstrümantal analiz II Konular: Kütle spektroskopisi Atomik Absorpsiyon Spektroskopisi Atomik Emisyon Spektroskopisi Elektrokimyasal yöntemler Potansiyometri Voltametri Konduktometri Kulometri Ekstraksiyon Teorisi Kromatografik yöntemler Otomatikleştirilmiş yöntemler (Akışa enjeksiyon) Termal analiz yöntemleri 2

Kütle spektroskopisi ile ilgili tanımlar İyonlaştırma yöntemleri Kütle ayırıcıları Dedektörler Atomik Kütle spektroskopisi ile analiz Moleküler Kütle spektroskopisi ile analiz 3

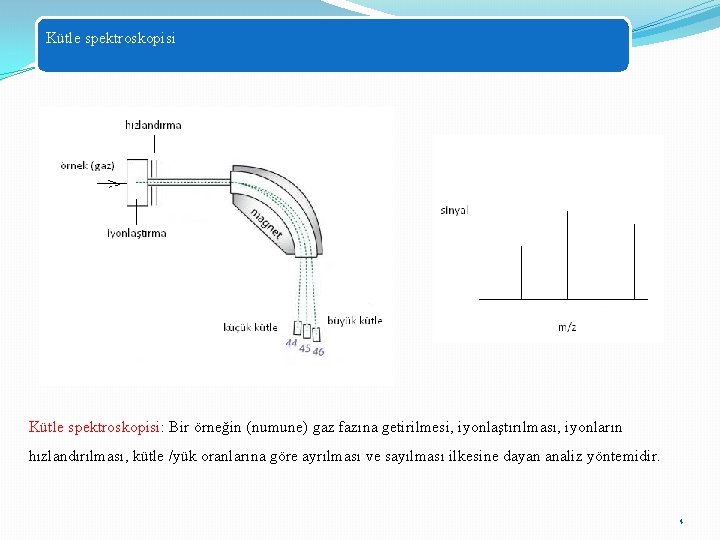
Kütle spektroskopisi: Bir örneğin (numune) gaz fazına getirilmesi, iyonlaştırılması, iyonların hızlandırılması, kütle /yük oranlarına göre ayrılması ve sayılması ilkesine dayan analiz yöntemidir. 4

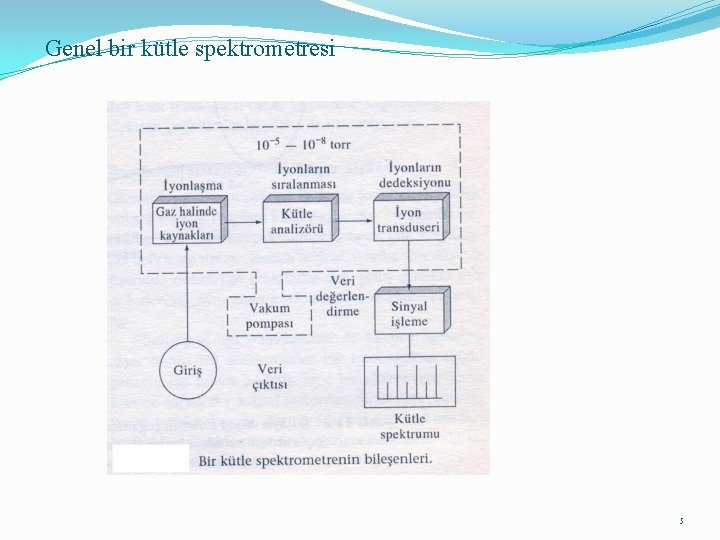
Genel bir kütle spektrometresi 5

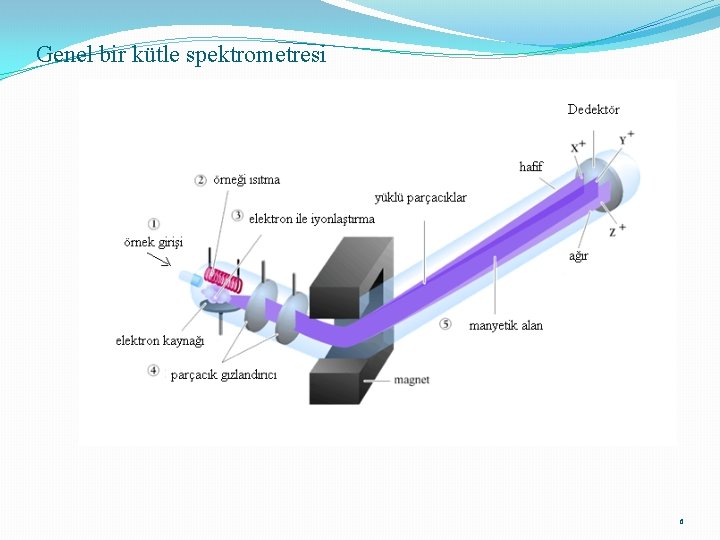
Genel bir kütle spektrometresi 6

Kütle spektroskopisi ile ilgili tanımlar Kütle spektroskopisi Atomik Kütle Spektroskopisi Moleküler kütle spektroskopisi Atomik Kütle Spektroskopisi : Örnek, atomlarına kadar parçalanır ve atomik düzeyde iyonlar oluşturulur. (Na+, Mg+, S+, Fe+ vs) Bir madde içinde hangi elementlerin ne oranda bulunduğunu tayin etmede kullanılır. Periyodik cetveldeki bütün elementler bu yöntemle tayin edilebilir. Moleküler kütle spektroskopisi : Örnek, molekül veya molekül bölümleri düzeyinde parçalanır ve moleküler düzeyde iyonlar oluşturulur. (C 2 H 5 OH+, CH 3+, C 2 H 5+ vs) Bir maddenin molekül yapısı (açık formülü ) tayininde kullanılır. Genel bir kütle spektrometresi (atomik veya moleküler) kütle/yük (kütle) ölçümünü temel alır. 7

Kütle spektroskopisinde atom kütleleri Kütle spektrometreleri izotopların kütleleri arasında fark gözetirken, diğer cihazlar genellikle bunu yapmaz. Atom ve molekül kütlelerinin birimleri genellikle atomik kütle birimi (akb) veya dalton (Da)dur. Bunlar 12 C izotopunu referans kabul eden bağıl bir ölçeğe dayalıdır. kesinlikle 12 C izotopunun kütlesi 12 akb olarak belirtilir. Yani akb veya Da nötral 126 C atomunun kütlesinin 1/12 'si olarak tanımlanır. CH 4 molekülünün kütlesi izotoplara göre farklı olur 12 C 1 H 4 için m=12, 000 x 1+1, 007825 x 4=16, 031 Da 13 C 1 H 4 için m=13, 00335 x 1+1, 007825 x 4=17, 035 Da 12 C 1 H 2 H 3 1 için m=12, 000 x 1+ 1, 007825 x 3+ 2, 0140 x 1=17, 037 Da Kütle spektrometride kütleler, virgülden sonra 3 ya da 4 basamaklı olarak verilir. 8

Kütle spektrometresi Genel bir kütle spektrometresi dört kısımdan oluşur. Örneği gaz hale getirme (gazlaştırma ) İyonlaştırma ve hızlandırma İyonları Kütle /yük oranlarına göre ayırma (kütle ayırıcısı) Ayrılan iyonları sayma (Dedektör) Gazlaştırma: ısıtma ile yapılır. Bazen iyonlaştırma basamağı ile birlikte gerçekleştirilir. 9

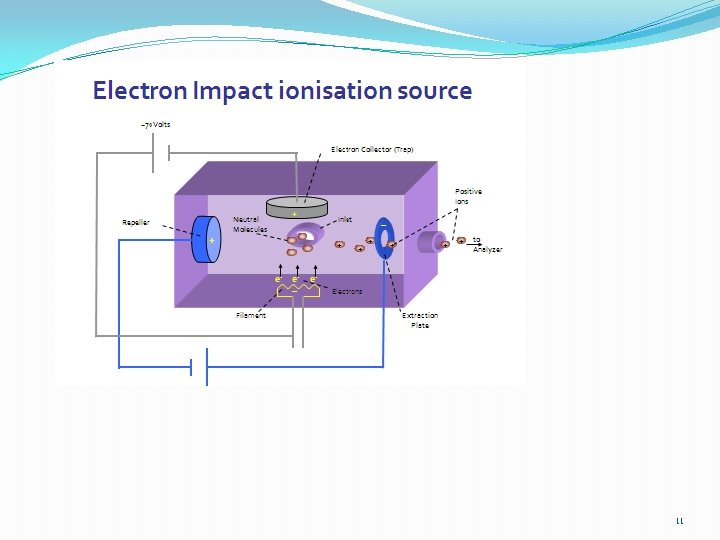
İyonlaştırma Elektron çarpması: Isıtılmış bir flamandan yayılan ve elektrik alanından geçirilerek hızlandırılan 50 -80 e. V enerjiye sahip elektronlar ile gaz fazındaki örnek bombardıman edilir. M(g) + e → M+(g) + 2 e Ark boşalım tekniği: Gaz halimdeki örnek elektrik arkı içinden geçirilir. Bu yöntemle çok fazla iyonlar oluşur. Kıvılcım iyonlaşma tekniği: katı örnek elektrot olarak kullanılır ve ark oluşturulur. Bu sırada katı yüzeyinden kopan moleküller iyon haline gelir. Işınla iyonlaştırma: (foto iyonlaştırma) Örnek yüksek enerjili ışınlarla bombardıman edilir. Bu yöntemde parçalanma az olur ve düşük enerjili iyonlar elde edilir. Isı ile iyonlaştırma: (termal iyonlaştırma) Örnek tungsten bir flaman üzerine konulur ve ısıtılır. Bu sırada hem gazlaşma hem de iyonlaşma işlemi gerçekleştirilir. Flaman olarak platin, Renyum, Tantal kullanılabilir. Kimyasal iyonlaştırma: Örnek yüksek basınçtaki reaktif gaz ile çarpıştırılarak iyonlaşma sağlanır. Reaktif gaz olarak metan, propan, bütan , izobütan, amonyak… 10

11

Bu yöntemde elektron bombardımanı ile önce reaktif gaz iyonlaştırılır ve iyonlaşan reaktif gaz ile örnek çarpıştırılır. RH + e → RH+ + 2 e MH + RH+ → MH + + RH Bu yöntemde farklı reaksiyonlar ve iyonlar da oluşabilir. RH + RH+ → RH 2 + R+ MH + R+ → M + + RH RH+2 + M → RH + MH + R+ → M + + RH Aynı zamanda negatif iyonlar da oluşabilir XCl + e → X + Cl. Cl - + MH 2 → MH- + HCl M + e → M+ 12

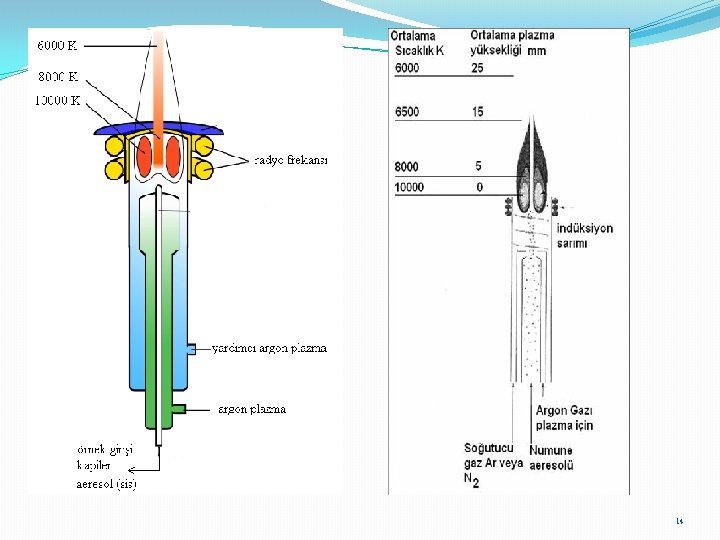
Alan iyonlaştırma: iki elektrot arasında 107 -108 V/cm lik bir elektrik alanı bulunan bir ortamdan gaz halindeki örnek geçirilir. İyonlaşan örnek anot üzerinde tutunur. Anoda elktriksel alan uygulanırsa tekrar serbest hale gelir. Lazer ışıması: lazer ışın demeti katı örnek yüzeyine düşürülür ve gaz halinde iyonlar elde edilir. Hızlı atom bombardımanı: Ne Ar, He gibi hızlandırılmış gaz halindeki atomlar kat örnek yüzeyine çarptırılır. Plazma desorpsiyonu: Radyoaktif Cf -252 izotop atomunun parçalanmasından oluşan ürünler katı örnek yüzeyine çarptırılır ve iyonlar elde edilir. İnduktif eşleşmiş plazma : (ICP) Doğru akım plazma: (DCP) Mikro dalga uyarımlı plazma: (MIP) Kıvılcım Kaynağı: Radyo frakansı –elektrik kıvılcımı 13

14

Atomik ve moleküler kütle spektroskopisinde iyonlaştırma Atomik kütlede iyonlaştırma Örnek atomlarına kadar parçalanır. Atom halinde iyonlar oluşturulması sağlanır. Bu yöntemler, plazma elektrik arkı Moleküler kütle spektroskopisinde ise parçalanmanın mümkün olduğu kadar az olması sağlanır. Moleküler düzeyde iyonlar oluşturulur. 15

İyonlaşma kaynağı ve atomik kütle spektroskopisi İyonlaşma kaynağı isim İndüktif eşleşmiş plazma ICP-MS Doğru akım plazma DCP-MS Mikrodalga uyarımlı plazma MIP-MS Kıvılcım kaynağı SS-MS Termal iyonlaşma TIMS Akkor boşalımı GDMS Lazer mikroprobu LMMS İkincil iyon SIMS 16

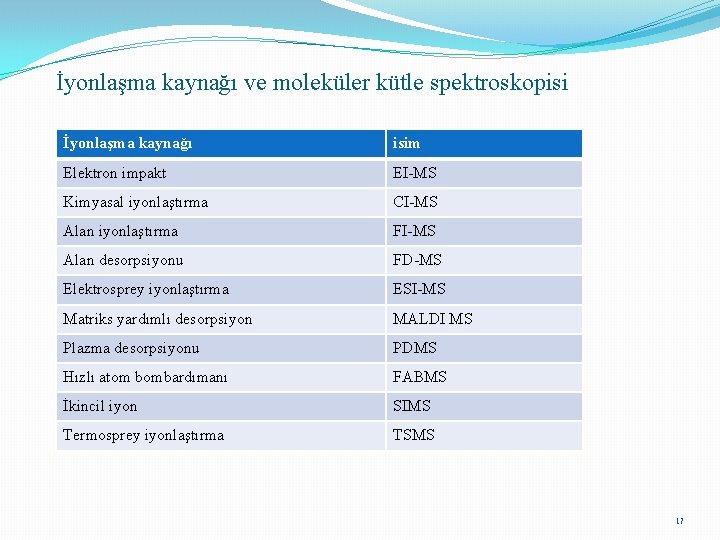
İyonlaşma kaynağı ve moleküler kütle spektroskopisi İyonlaşma kaynağı isim Elektron impakt EI-MS Kimyasal iyonlaştırma CI-MS Alan iyonlaştırma FI-MS Alan desorpsiyonu FD-MS Elektrosprey iyonlaştırma ESI-MS Matriks yardımlı desorpsiyon MALDI MS Plazma desorpsiyonu PDMS Hızlı atom bombardımanı FABMS İkincil iyon SIMS Termosprey iyonlaştırma TSMS 17

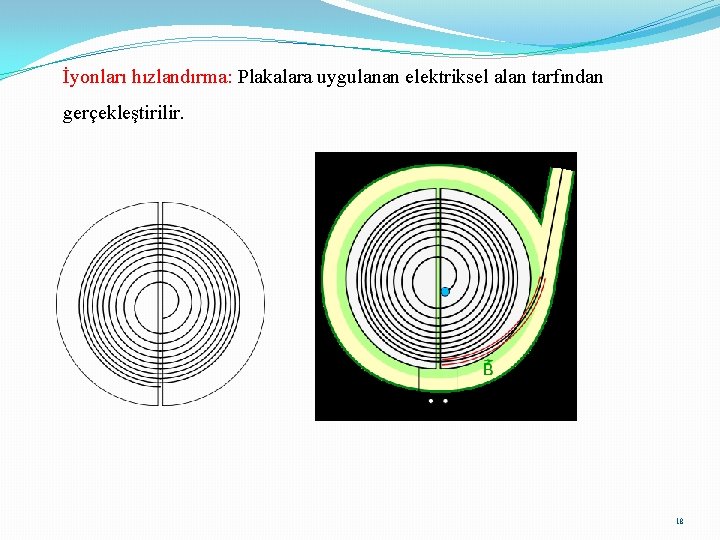
İyonları hızlandırma: Plakalara uygulanan elektriksel alan tarfından gerçekleştirilir. 18

Kütle ayırıcıları İyon haline getirilen örnek hızlandırıcılardan geçerek kütle ayırıcısına gelir. Kütle ayırıcılarının çalışma ilkesi farklıdır; Magnetik kütle ayırıcıları: Hızlandırılarak magnetik kütle ayırıcıına gelen iyonların kinetik enerjisi ile hızlandırma potansiyeli arsında mv 2 /2 = e. V gibi bağıntı vardır m: iyonun kütlesi v : iyonun hızı V: hızlandırma potansiyeli e: iyonun yükü Yüklü bir parçacık magnetik alana girdiğinde doğrusal yolundan saparak daire çizmeye zorlanır. Magnetik sapmayı sağlayan kuvvet: F 1 = Hev H: magnetik alan şiddeti İyona dairesel hareket için etkiyen kuvvet (merkezcil kuvvet) F 2 = mv 2 / r 19

Bu iki kuvvet eşitlenirse F 1 = F 2 Hev = mv 2 / r m / e = Hrv/v 2 = Hr/v v’yi kinetik enerji eşitliğinden bulursak, mv 2 /2 = e. V → v 2 = 2 e. V/m → v = √ 2 e. V/m m / e = Hr/v → Hr / √ 2 e. V/m m / e = H 2 r 2/2 V m arttıkça r yarıçap artar (magnetik alanda daha az sapar) m azaldıkça r azalır (magnetik alanda daha fazla sapar) Magnetik kütle ayırıcısı ile 2000 -5000 arasında ayırıcılık elde edilir. 20

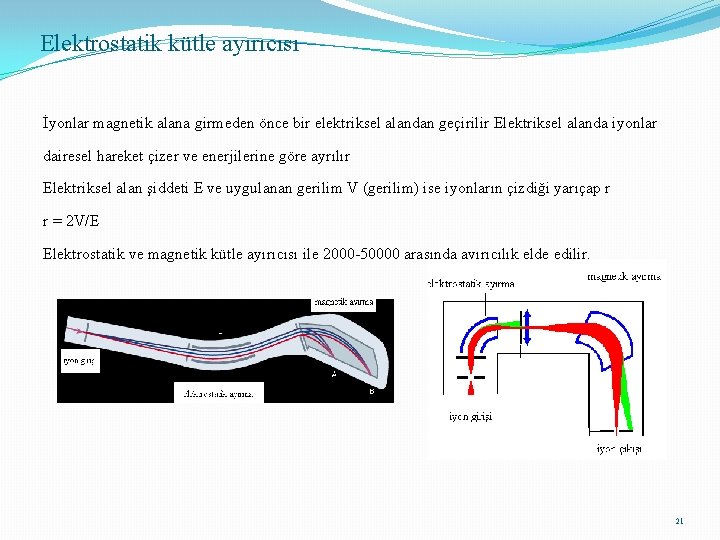
Elektrostatik kütle ayırıcısı İyonlar magnetik alana girmeden önce bir elektriksel alandan geçirilir Elektriksel alanda iyonlar dairesel hareket çizer ve enerjilerine göre ayrılır Elektriksel alan şiddeti E ve uygulanan gerilim V (gerilim) ise iyonların çizdiği yarıçap r r = 2 V/E Elektrostatik ve magnetik kütle ayırıcısı ile 2000 -50000 arasında ayırıcılık elde edilir. 21

Uçuş zamanlı kütle ayırıcısı İyon kaynağından gelen iyonlar uçuş tüpüne alınır. Uçuş tüpü 1 -2 m uzunluğunda, camdan yapılmış, vakum ortamı ve çıkışında dedektör bulunan bir sistemdir. Değişik kütleli iyonlar aynı gerilimle hızlandırıldıkları için e. V =mv 2/2 eşitliğine göre farklı hızlara sahip olur. m ↗ v ↘ küçük kütleli iyonlar dedektöre daha çabuk büyük kütleli iyonlar ise daha geç ulaşır. Ayırıcılık 500 civarındadır. 22

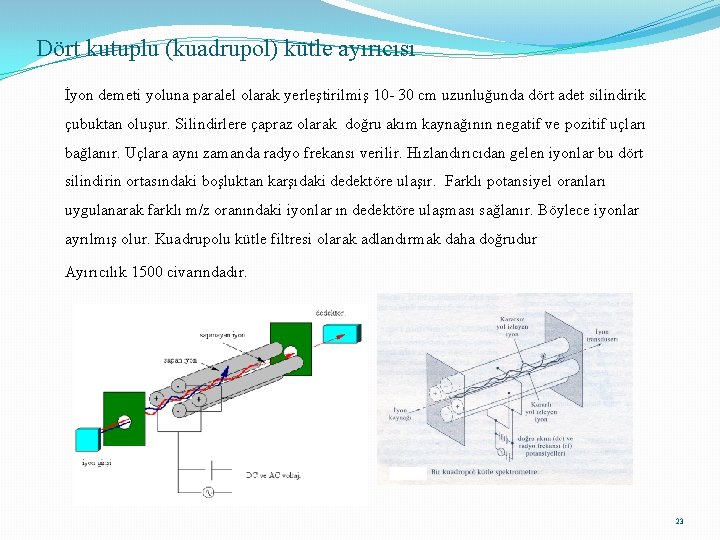
Dört kutuplu (kuadrupol) kütle ayırıcısı İyon demeti yoluna paralel olarak yerleştirilmiş 10 - 30 cm uzunluğunda dört adet silindirik çubuktan oluşur. Silindirlere çapraz olarak doğru akım kaynağının negatif ve pozitif uçları bağlanır. Uçlara aynı zamanda radyo frekansı verilir. Hızlandırıcıdan gelen iyonlar bu dört silindirin ortasındaki boşluktan karşıdaki dedektöre ulaşır. Farklı potansiyel oranları uygulanarak farklı m/z oranındaki iyonlar ın dedektöre ulaşması sağlanır. Böylece iyonlar ayrılmış olur. Kuadrupolu kütle filtresi olarak adlandırmak daha doğrudur Ayırıcılık 1500 civarındadır. 23

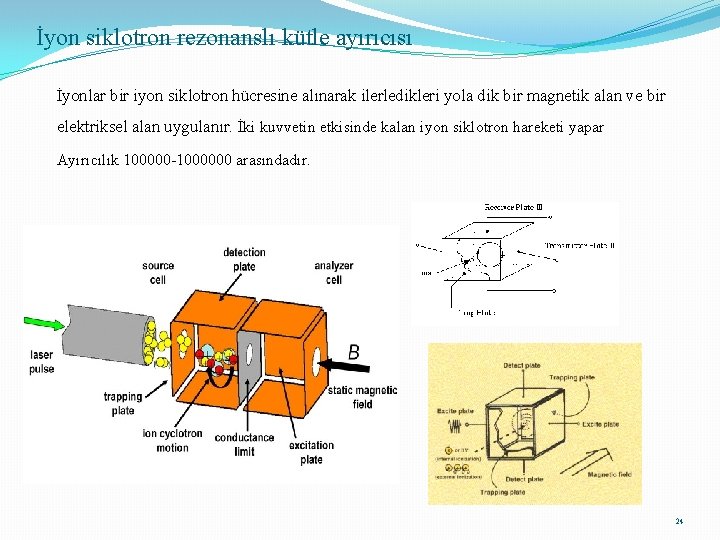
İyon siklotron rezonanslı kütle ayırıcısı İyonlar bir iyon siklotron hücresine alınarak ilerledikleri yola dik bir magnetik alan ve bir elektriksel alan uygulanır. İki kuvvetin etkisinde kalan iyon siklotron hareketi yapar Ayırıcılık 100000 -1000000 arasındadır. 24

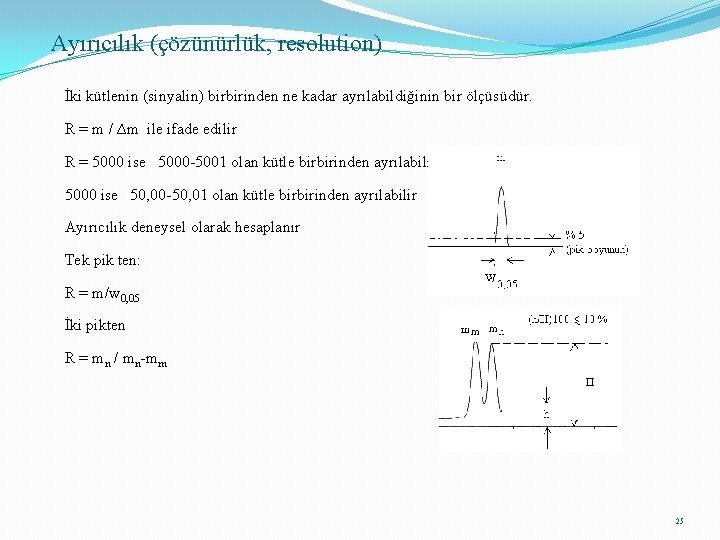
Ayırıcılık (çözünürlük, resolution) İki kütlenin (sinyalin) birbirinden ne kadar ayrılabildiğinin bir ölçüsüdür. R = m / ∆m ile ifade edilir R = 5000 ise 5000 -5001 olan kütle birbirinden ayrılabilir veya 5000 ise 50, 00 -50, 01 olan kütle birbirinden ayrılabilir Ayırıcılık deneysel olarak hesaplanır Tek pik ten: R = m/w 0, 05 İki pikten R = mn / mn-mm 25

26

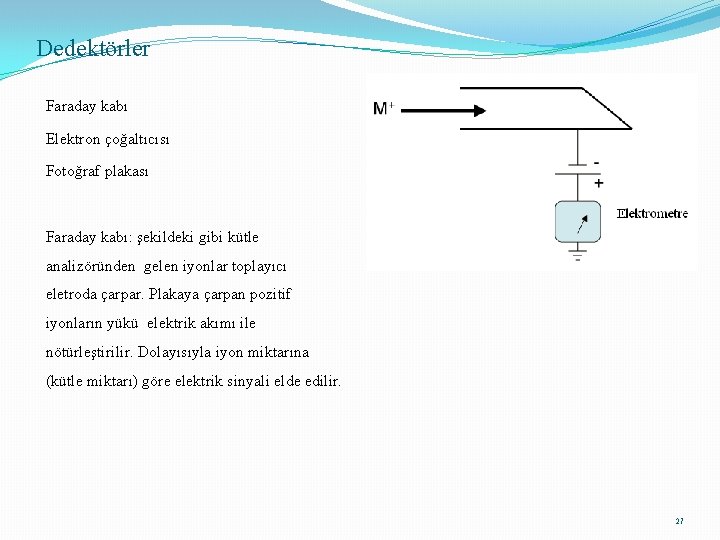
Dedektörler Faraday kabı Elektron çoğaltıcısı Fotoğraf plakası Faraday kabı: şekildeki gibi kütle analizöründen gelen iyonlar toplayıcı eletroda çarpar. Plakaya çarpan pozitif iyonların yükü elektrik akımı ile nötürleştirilir. Dolayısıyla iyon miktarına (kütle miktarı) göre elektrik sinyali elde edilir. 27

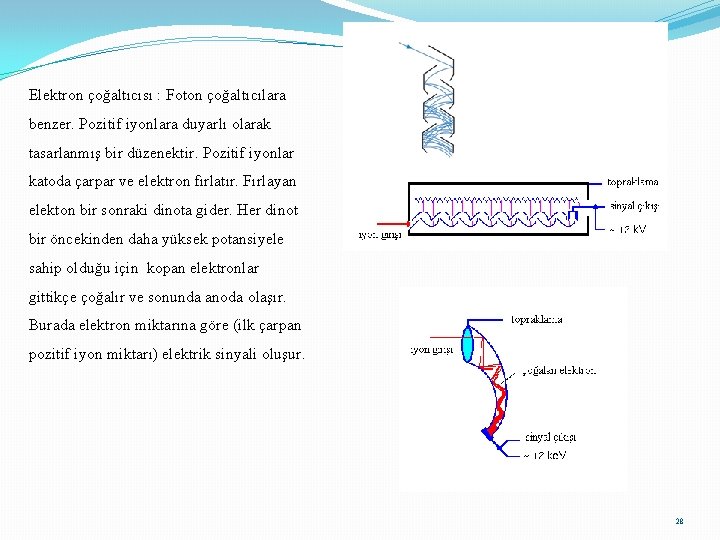
Elektron çoğaltıcısı : Foton çoğaltıcılara benzer. Pozitif iyonlara duyarlı olarak tasarlanmış bir düzenektir. Pozitif iyonlar katoda çarpar ve elektron fırlatır. Fırlayan elekton bir sonraki dinota gider. Her dinot bir öncekinden daha yüksek potansiyele sahip olduğu için kopan elektronlar gittikçe çoğalır ve sonunda anoda olaşır. Burada elektron miktarına göre (ilk çarpan pozitif iyon miktarı) elektrik sinyali oluşur. 28

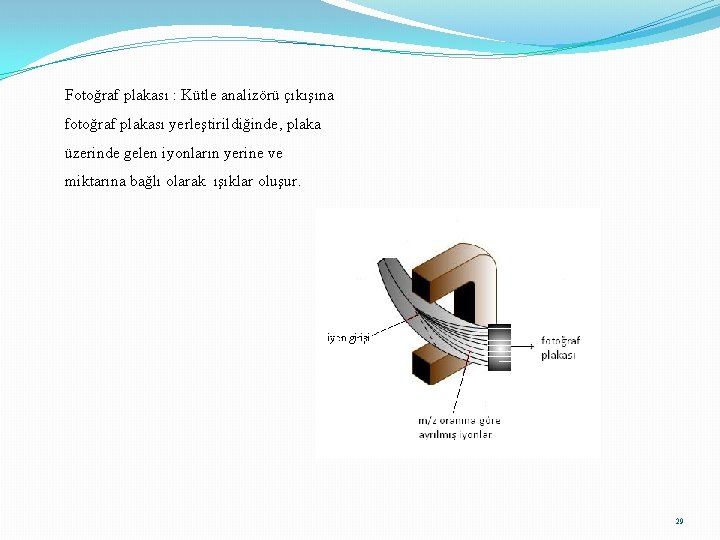
Fotoğraf plakası : Kütle analizörü çıkışına fotoğraf plakası yerleştirildiğinde, plaka üzerinde gelen iyonların yerine ve miktarına bağlı olarak ışıklar oluşur. 29

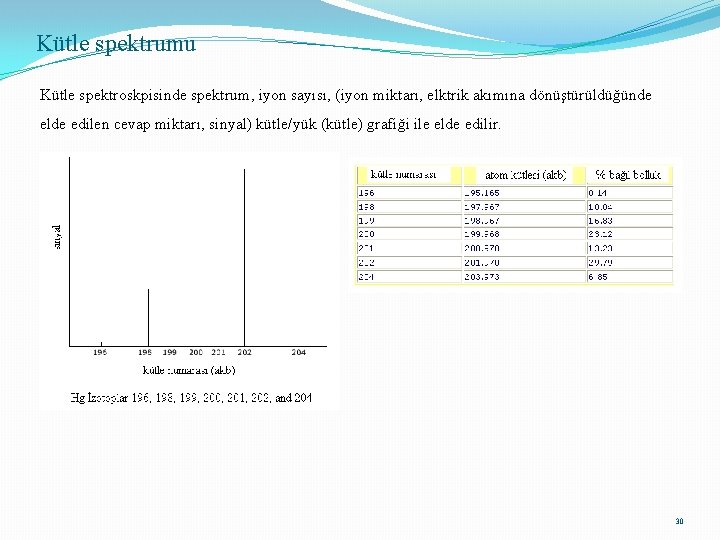
Kütle spektrumu Kütle spektroskpisinde spektrum, iyon sayısı, (iyon miktarı, elktrik akımına dönüştürüldüğünde elde edilen cevap miktarı, sinyal) kütle/yük (kütle) grafiği ile elde edilir. 30

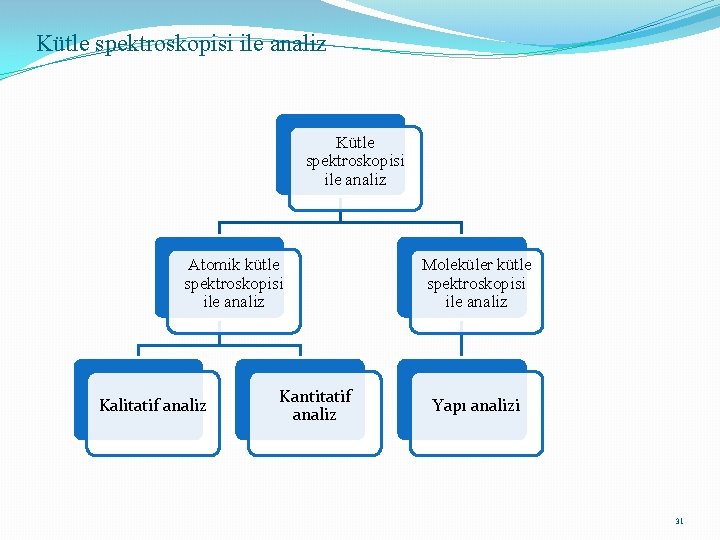
Kütle spektroskopisi ile analiz Atomik kütle spektroskopisi ile analiz Kalitatif analiz Kantitatif analiz Moleküler kütle spektroskopisi ile analiz Yapı analizi 31

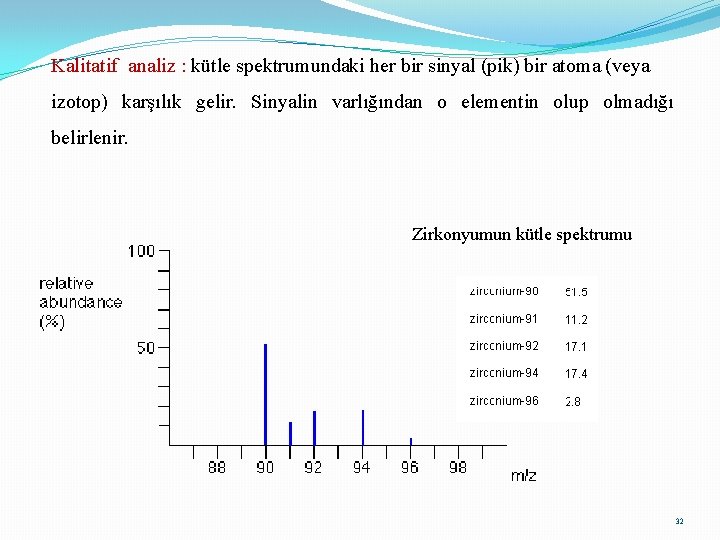
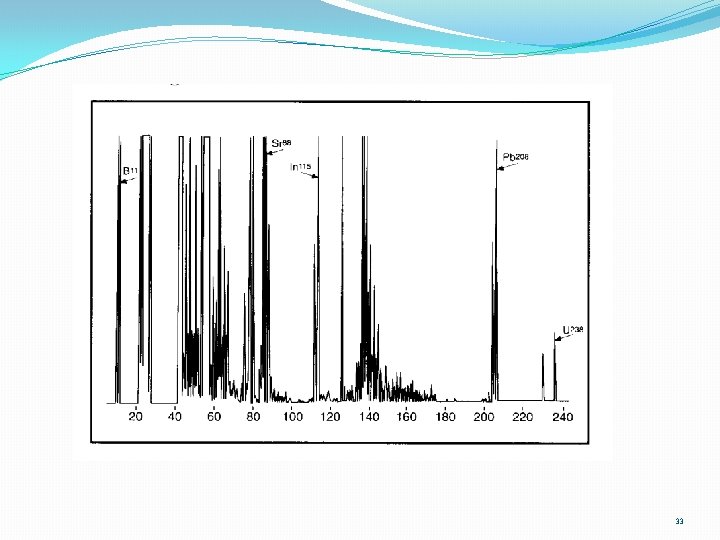
Kalitatif analiz : kütle spektrumundaki her bir sinyal (pik) bir atoma (veya izotop) karşılık gelir. Sinyalin varlığından o elementin olup olmadığı belirlenir. Zirkonyumun kütle spektrumu 32

33

34

35

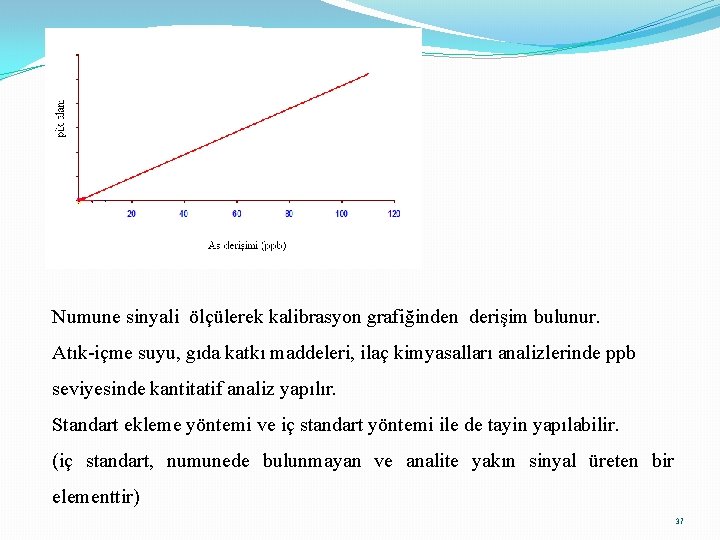
Kantitatif analiz: Kalibrasyon Yöntemi: En çok ICP-MS'de kullanılır. Önce kalibrasyon eğrisi hazırlamak üzere, bir dizi standart çözeltiler hazırlanır. Eğer numunedeki toplam çözünmüş katı derişimi 2000 g/m. L'nin altında ise, yani yeterince seyreltikse basit sulu standartlar genellikle uygundur. Derişime karşı sinyal grafiği çizilir. 36

Numune sinyali ölçülerek kalibrasyon grafiğinden derişim bulunur. Atık-içme suyu, gıda katkı maddeleri, ilaç kimyasalları analizlerinde ppb seviyesinde kantitatif analiz yapılır. Standart ekleme yöntemi ve iç standart yöntemi ile de tayin yapılabilir. (iç standart, numunede bulunmayan ve analite yakın sinyal üreten bir elementtir) 37

Kantitatif analizde girişimler 1 - Spektroskopik girişimler 2 - Diğer girişimler (optik ve atomik absorpsiyon ya da emisyondaki girişimlerle aynı) Spektroskopik girişimler İzobarik girişimler (aynı kütle) 113 In+ = 40 Ar+ 58 Ni+ = = 113 Cd+ 115 Sn+ = 115 In+ 40 Ca+ 58 Fe+ düzeltmek için elementin başka izotopu ölçülür (56 Fe+ ) Çok atomlu iyon girişimleri Ar. OH+ = 14 N + 2 = NOH+ = 16 O + 2 40 Ar + 2 = = 56 Fe+ 28 Si+ 31 P+ 32 S+ 80 Se+ 38

Oksit ve hidroksit türlerinin girişimi: oksit ve hidroksit iyonlarının kütlesi başka metalin kütlesi ile aynı olabilir. MO+ MOH+ = M’ Ti : 46, 47, 48, 49, 50 izotopları Ti. O+ : 62 62 Ni+ 63 63 Cu+ 64 65 64 Zn+ 65 Cu+ 66 66 Zn+ Çift yüklü iyon oluşumu m/z oranlarına göre (z = 1) ancak z = 2, 3 olabilir M+ M+2 M+3 gibi iyonlar oluşur 40 Ar+ = 80 Se+2 39

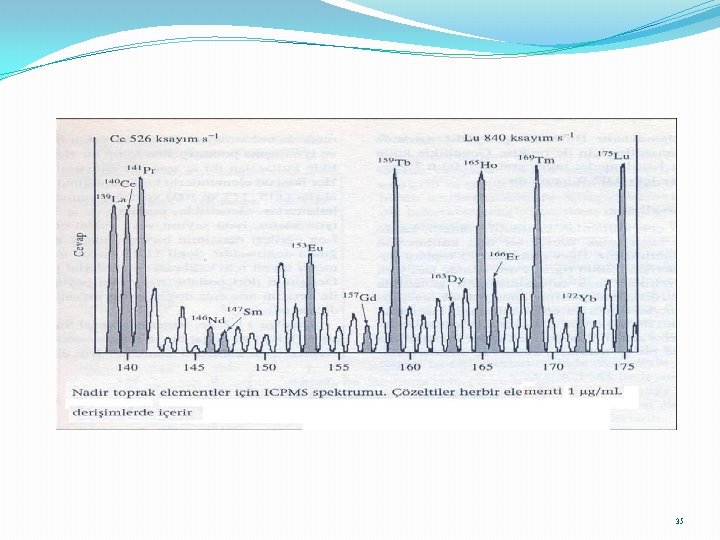
Atomik kütle ve atomik spektroskopisinin karşılaştırılması Üstteki şeklide, 100 ppm Ce içeren çözeltinin optik emisyon spektrumu Alttaki şekilde 100 ppm Ce çözeltisinin kütle spektrumun İkincisinde Ce izotoplarının pikleri ayrılmış olarak görülmektedir. Plazmalı atomik kütle spektroskopisinde plazmadaki iyonik türle (Ar+) analit iyonu aynı m/z oranına sahipse spektral girişim gözlenir. ICPMS de bozucu madde derişimleri 500 -1000 g/ml den fazla ise matriks etkisi gözlenir. 40

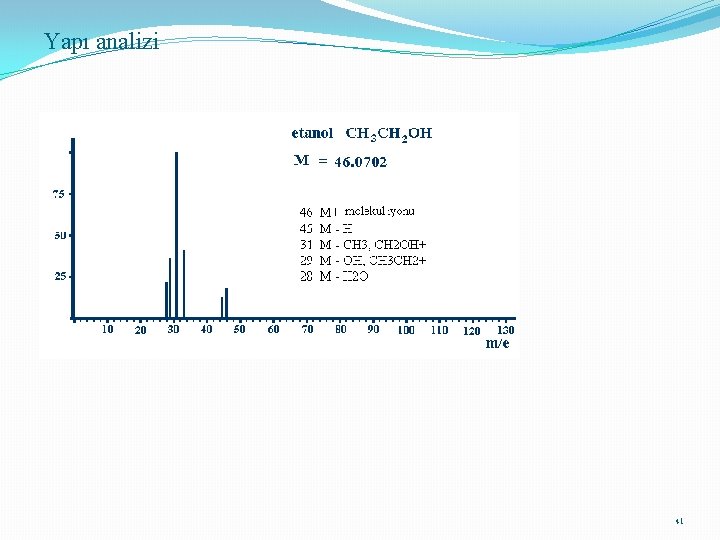
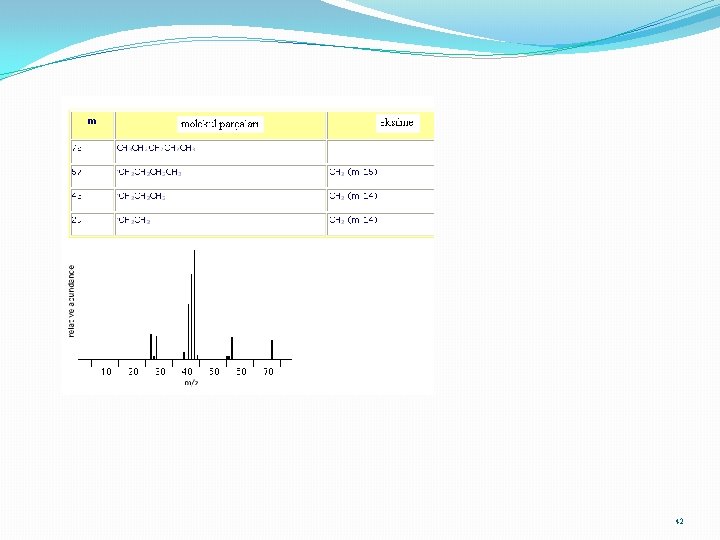
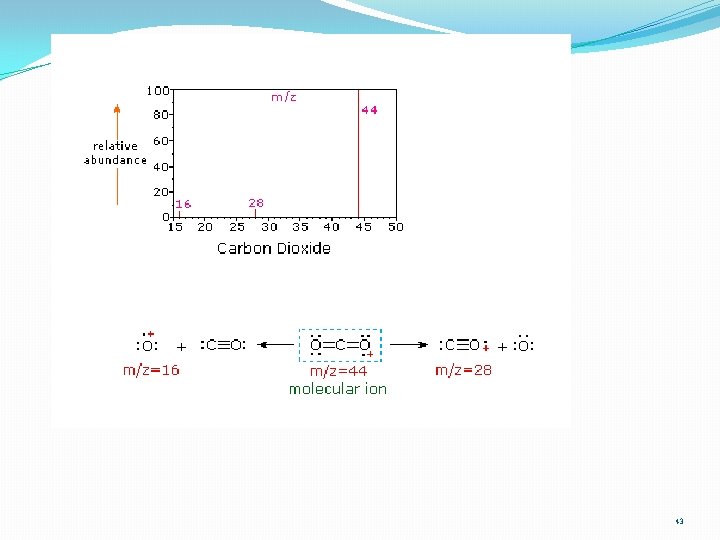
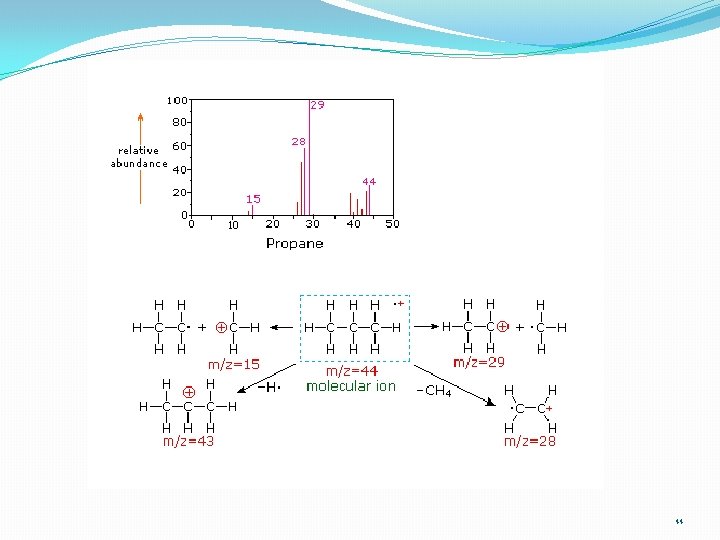
Yapı analizi 41

42

43

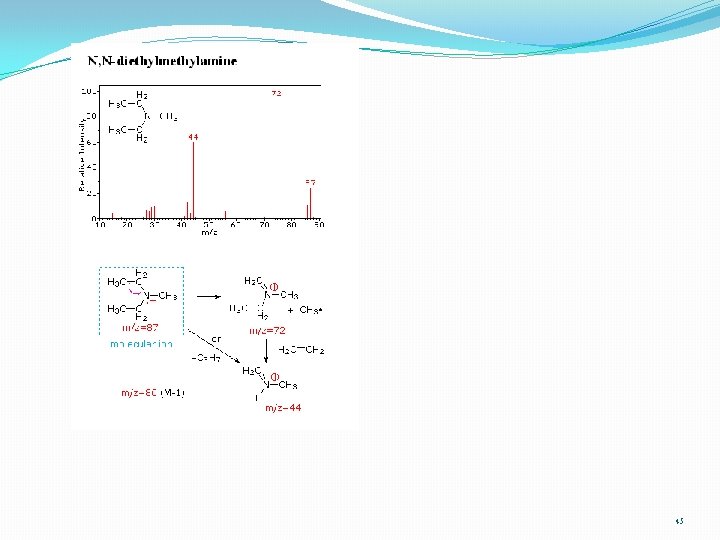
44

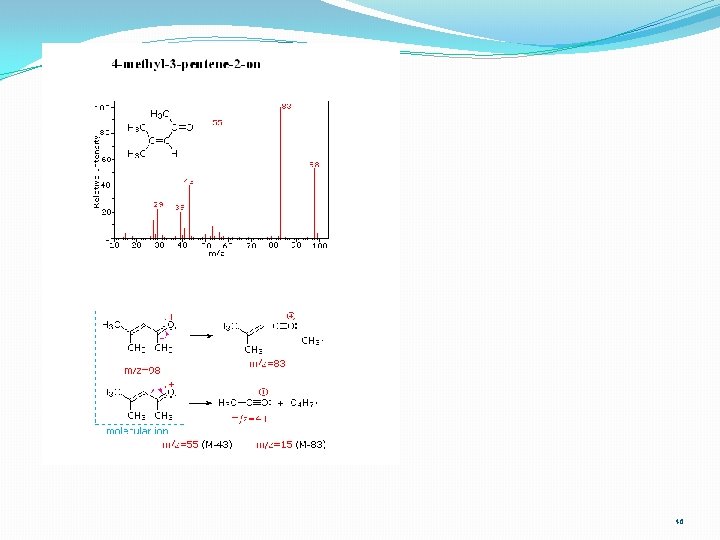
45

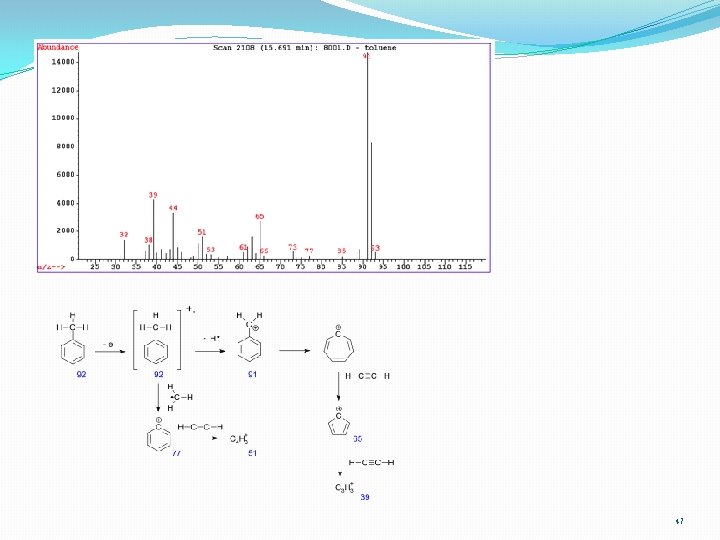
46

47

Yaygın molekül parçaları m/z composition 15 CH 3 17 OH 18 H 2 O 19 H 3 O, F 26 C 2 H 2, CN 27 C 2 H 3 28 C 2 H 4, CO, H 2 CN 29 C 2 H 5, CHO 30 CH 2 NH 2 31 CH 3 O 33 SH, CH 2 F 34 H 2 S 35(37) Cl 36(38) HCl 39 C 3 H 3 41 C 3 H 5, C 2 H 3 N 48