Associazione Italiana Oncologia Medica Il contributo di AIOM

Associazione Italiana Oncologia Medica Il contributo di AIOM nella ricerca in oncologia Stefania Gori Presidente eletto AIOM U. O. C. Oncologia Medica Ospedale “Sacro Cuore-Don Calabria” Negrar- VR Presidio Ospedaliero Accreditato- Regione Veneto

Associazione Italiana di Oncologia Medica Art. 2 – Scopo istituzionale • L'Associazione non ha fini di lucro, ed ha lo scopo di riunire i cultori dell’Oncologia Medica al fine di promuoverne il progresso nel campo clinico, sperimentale, e socio-assistenziale, di favorire i rapporti tra gli oncologi medici, i medici di medicina generale e gli specialisti di altre discipline, di stabilire relazioni scientifiche e di collaborazione con analoghe Associazioni italiane ed estere, ed altre società e organismi scientifici, nonché di partecipare e collaborare con organismi istituzionali nazionali, regionali e locali, compresi il Ministero della Salute, le Regioni, le Aziende Sanitarie, ed ogni altro organismo e istituzione sanitaria pubblica. • L'Associazione ha, inoltre, lo scopo di promuovere la ricerca sperimentale e clinica, i trials di studio e le ricerche scientifiche finalizzate, la prevenzione primaria, la prevenzione secondaria (screening e diagnosi precoce e tempestiva), la qualità delle cure oncologiche, la continuità terapeutica del paziente oncologico mediante Linee Guida elaborate anche in collaborazione con l’Agenzia per i Servizi Sanitari Regionali e con la Federazione delle Società Medico-Scientifiche Italiane, la interdisciplinarietà, la riabilitazione, le terapie palliative, le cure domiciliari e di incentivare campagne di educazione rivolte alla popolazione. In particolare, l’Associazione Italiana di Oncologia Medica si propone di operare per contribuire alla formazione e all’aggiornamento tecnicoprofessionale e manageriale di oncologi medici e di operatori sanitari, alla attività di formazione permanente nei confronti degli associati con programmi annuali di attività formativa E. C. M. (Educazione Continua in Medicina), ed alla formazione di strutture accreditate intra ed extraospedaliere per l'assistenza al paziente con neoplasia.

Associazione Italiana Oncologia Medica A- Attività di AIOM nell’ultimo decennio nell’ambito della ricerca

Linee Guida AIOM Associazione Italiana Oncologia Medica Valutazione dell’implementazione nella pratica clinica RIGHT-1 RIGHT-2 RIGHT-3 Adherence to 2009 AIOM guidelines in lung cancer clinical practice in Italy: results from the RIGHT-3 (Research for the Identification of the most effective and h. IGHly accepted clinical guidelines for cancer Treatment) study Barni S, et al Lung Cancer 2015 RIGHT-4 Adherence to 2012 guidelines AIOM in renal cancer clinical practice in Italy …ongoing…
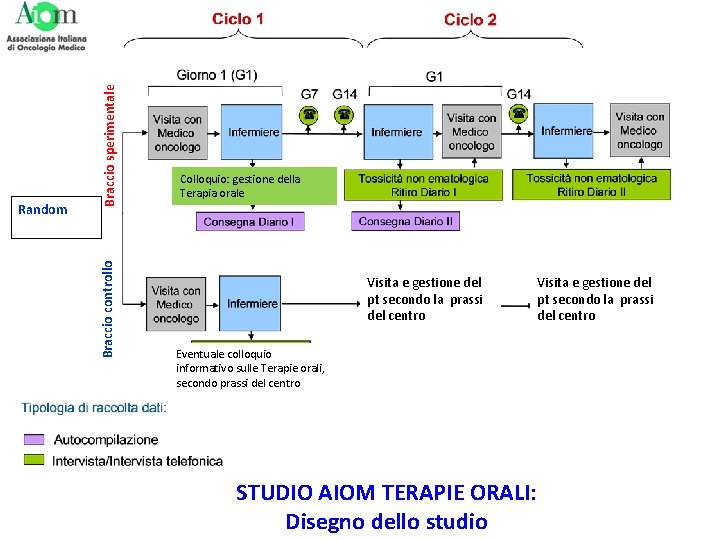
Braccio sperimentale Braccio controllo Random Colloquio: gestione della Terapia orale Visita e gestione del pt secondo la prassi del centro Eventuale colloquio informativo sulle Terapie orali, secondo prassi del centro STUDIO AIOM TERAPIE ORALI: Disegno dello studio Visita e gestione del pt secondo la prassi del centro

Studio AIOM Terapie orali • Obiettivo primario: – proporzione di pazienti con accessi ‘impropri’ Per accessi impropri si intende gli accessi al centro oncologico dovuti: - a scarsa comprensione del piano terapeutico, - alla necessità di rassicurazioni da parte del personale sanitario - a tossicità di grado ≤ 2
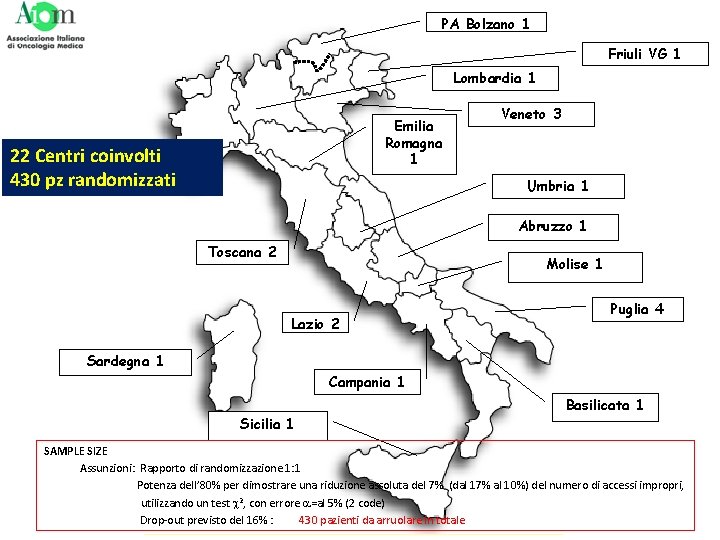
PA Bolzano 1 Friuli VG 1 Lombardia 1 Emilia Romagna 1 22 Centri coinvolti 430 pz randomizzati Veneto 3 Umbria 1 Abruzzo 1 Toscana 2 Molise 1 Lazio 2 Puglia 4 Sardegna 1 Campania 1 Sicilia 1 Basilicata 1 SAMPLE SIZE Assunzioni: Rapporto di randomizzazione 1: 1 Potenza dell’ 80% per dimostrare una riduzione assoluta del 7% (dal 17% al 10%) del numero di accessi impropri, utilizzando un test c 2, con errore a=al 5% (2 code) Drop-out previsto del 16% : 430 pazienti da arruolare in totale

Oral Anticancer Therapy Project: clinical utility of a specific home care nursing program M. Cirillo, L. Carlucci, I. Pacchetti, E. Rulli, C. Sacco, V. Zagonel, E. Baldini, FL. Rojas-Llimpe, G. Tonini, S. Leo, M. Meacci, A. Tartarone, G. Tortora, M. Zaninelli, VM. Valori, A. Quaranta, E. Cretella, G. Lunardi, C. Pinto, S. Gori Ospedale Sacro Cuore-Don Calabria, Negrar; IRCCS - Mario Negri Institute for Pharmacological Research, Milano; Azienda Ospedaliero-Universitaria, Udine; Istituto Oncologico Veneto IRCCS, Padova; Campo di Marte Hospital, Lucca; Policlinico S. Orsola-Malpighi, Bologna; Univ Campus Bio-Medico, Roma; Ospedale Vito Fazzi, Lecce; S Maria della Misericordia Hospital, Perugia; IRCCS Centro di Riferimento Oncologico della Basilicata, Rionero in Vulture; AO Universitaria Integrata, Verona; ULSS 22, Bussolengo; IRCCS Casa Sollievo della Sofferenza, San Giovanni Rotondo; A. Perrino Hospital, Brindisi; Ospedale di Bolzano; IRCCS-Arcispedale S. Maria Nuova, OECI Clinical Cancer Center, Reggio Emilia; ITALY Introduction: In recent years oral chemotherapy is an expanding option for cancer treatment. Despite more convenient, an home-based therapy makes patients and caregivers responsible for dose adjustments and exact drug intake particularly in the case of side effects onset. Patient education has a key role in the successful treatment with oral chemotherapy. Therefore an accurate attention must be paid to develop educational strategies to ensure patient understanding about administration, potential side effects and self-care measure particularly concerning the early detection and management of toxicities. The Italian Association of Medical Oncology (AIOM) sponsored a prospective randomized study aimed to assess the effectiveness and clinical impact of a specific home care nursing program (HCNP) (in addition to standard care) in a large and multi-institutional study Methods: representative of different practices in the management of oral chemotherapy. A randomized controlled trial was designed. The study gained the approval by every local Ethics Committees related to the Oncology Units involved. The study was registered in the Italian observational studies registry [AIOM TO -1(ID 637)] Sample and setting The sample consisted of patients aged 18 years or older receiving treatment for a neoplastic disease. They were eligible if: - they had to receive a regimen containing cytotoxic drugs and/or target therapies as oral form without past experience of oral treatment - they were able to communicate answering phone calls and they were able to register toxicity and drug intake in specific form. Concomitant use of Radiotherapy, intravenous drugs or metronomic therapies were not allowed. Patients unable to self care were excluded. Consecutive patients were recruited and were allocated to receive either standard care (control arm) or HCNP (experimental arm). Random assignment was centrally carried out by an independent statistician by a computer-generated program. Experimental Arm During the medical visit physicians discuss chemotherapy and its adverse effects providing patient all information related to the prescribe treatment. Only in the experimental arm after the medical visit, dedicated nurses provided: - Accurate information to the patients for self management of therapy at home; - A daily record on which patients check off the pills consumption for each day and a specific form to collect toxicity; - A telephone monitoring by means of phone calls on day 7 and 14 of cycle 1 and on day 14 of cycle 2. Patients were monitored for the first two cycles independently from the treatment schedule (3, 4 or 6 weeks). Statistical analysis Data were reported as absolute difference between the two proportions and relative risk. Data were statistically compared by Mantel-Haenszel chi-squared test stratified by center. A P value < 0. 05 was considered statistically significant. Outcome measure Primary endpoint was to verify if this HMP could reduce unplanned hospital admissions. We consider as unplanned hospital admission any admission to Oncology Unit or to Emergency Unit due to grade 12 toxicities according to CTC-AE scale v 4. 0 or to solve patient’s doubts and questions of clarification. The population for primary endpoint includes all randomized patients without major violation of eligibility criteria or study contact, who received at least one dose of treatment and with at least one access. Table 1 - Baseline and socio-demographic characteristics Table 3 - Anticancer therapy prescribed at randomization Table 4 - Compliance to treatment Number of patients - n (%) Age (years) Results: Overall 430 pts were randomized in 18 Italian Oncology Units. 44 pts were excluded for major violation (9 pts) or for never starting treatment (35 pts). We included in the analysis 386 pts (188 pts in arm A and 198 in arm B). Baseline and socio-demographic patient characteristics are listed in Table 1. Arms were comparable as regard the origin of neoplasia (Table 2). As regard treatment no significant differences were registered between arms. Anticancer treatment consisted of cytotoxic drugs in 110/188 pts in arm A and 120/198 pts in arm B (58% and 60%, respectively). Antiangiogenic or target therapies were prescribed in the remaining cases (84 pts in arm A and 79 in arm B) Capecitabine was the most prescribed drug (88/386 pts corresponding to 22%). Anticancer therapy prescribed at randomization is listed in Table 3. Compliance to treatment was comparable between arms since 144/188 pts in arm A (76. 6%) and 154/198 pts in arm B (77. 8%) completed treatment as planned during the period of monitoring program. 39 pts in both arms interrupted treatment before planned corresponding to 20. 7% in arm A and 19. 7% in arm B. Reasons of interruptions are listed in Table 4 At least one access to hospital was observed in 40 pts in arm A and 42 pts in arm B (21. 3% vs 21. 2% respectively) Primary end point was unmet as no difference was detected in the proportion of pts with improper accesses between arm A and arm B (27. 5% vs 23. 8% respectively, ) Table 5 shows difference between arms of pts with at least one access (proper and improper accesses). Table 6 shows number of proper and improper accesses between arms. Arm A Arm B 188 (48. 7) 198 (51. 3) 69. 0 69. 8 Mean (SD) (11. 1) (10. 2) 71. 9 (60. 5 72. 2 (63. 7 Median (Q 1 - Q 3) -77. 9) -77. 7) 31. 0 - Min - Max 43. 1 - 85. 7 88. 2 Missing 0 0 Sex - n (%) Male 94 (50. 0) 101 (51. 0) Female 94 (50. 0) 97 (49. 0) ECOG-PS - n (%) 0 100 (53. 2) 102 (51. 5) 1 79 (42. 0) 87 (43. 9) 2 9 (4. 8) 9 (4. 5) Educational - n (%) Illiterate 11 (5. 9) 4 (2. 0) Primary school 51 (27. 3) 63 (32. 1) Middle school 56 (29. 9) 59 (30. 1) High school 37 (19. 8) 39 (19. 9) University degree 9 (4. 8) 8 (4. 1) Table 2 - Baseline tumor characteristics Other 23 (12. 3) 23 (11. 7) Missing 1 2 Arm A Arm B Number of patients - n (%) Months from diagnosis to random Mean (SD) 188 (48. 7) 198 (51. 3) Median (Q 1 - Q 3) Min - Max Missing Primary site - n (%) Colon Kidney Breast Lung Liver Pancreas Stomach Bile ducts Skin Brain Other Stage - n (%) 0 I II IV Missing 25. 1 (44. 6) 5. 1 (1. 823. 6) 0. 0 - 239. 7 3 55 (29. 3) 31 (16. 5) 27 (14. 4) 25 (13. 3) 18 (9. 6) 7 (3. 7) 2 (1. 1) 3 (1. 6) 4 (2. 1) 9 (4. 8) 2 (1. 1) 9 (4. 8) 25 (13. 4) 40 (21. 4) 111 (59. 4) 1 21. 5 (42. 6) 4. 0 (1. 517. 8) 0. 0 - 276. 8 4 51 (25. 8) 35 (17. 7) 31 (15. 7) 23 (11. 6) 18 (9. 1) 12 (6. 1) 7 (3. 5) 5 (2. 5) 2 (1. 0) 7 (3. 5) 1 (0. 5) 7 (3. 5) 26 (13. 1) 41 (20. 7) 123 (62. 1) 0 Therapy - n (%) Arm A Arm B Capecitabine Sunitinib Sorafenib Vinorelbine Pazopanib Erlotinib Everolimus Gefitinib Temozolomide Capecitabina + Vinorealbine Capecitabina + Lapatinib Vemurafenib Afatinib Imatinib Others 81 (43. 1) 19 (10. 1) 22 (11. 7) 14 (7. 4) 9 (4. 8) 6 (3. 2) 5 (2. 7) 88 (43. 4) 23 (11. 6) 18 (9. 1) 17 (8. 6) 9 (4. 5) 5 (2. 5) 7 (3. 5) 5 (2. 5) Arm A Number of patients - 188 n (%) (48. 7) Treatment 144 completed (76. 6) Treatment 39 (20. 7) interrupted Reasons: Medical 22 (56. 4) decision Death 6 (15. 4) 2 (1. 1) 5 (2. 5) Disease 6 (15. 4) progression 6 (3. 2) 1 (0. 5) Lost to follow 2 (5. 1) 2 (1. 1) 3 (1. 5) up 1 (0. 5) 3 (1. 5) Consent 2 (5. 1) 1 (0. 5) 2 (1. 0) withdrawal 5 (2. 6) 7 (3. 5 Subject refusal 1 (2. 6) 0 Table 5 - Number of subjects who have had at least one access Missing Treatment ongoing 5 (2. 7) Number of patients - n (%) Number of patients with at least one access - n (%) Improper access - n (%) Proper access - (%) Arm A Arm B Number of patients with at least one access - n (%) 0 improper accesses - n (%) 1 improper access - n (%) 2 improper accesses - n (%) Number of accesses - n Proper - n (%) Improper - n (%) ASCO 2016 RR (CI 95%) 188 (48. 7) 40 (21. 3) 198 (51. 3) 42 (21. 2) 11 (27. 5) 29 (72. 5) 10 (23. 8) 32 (76. 2) 3. 7 1. 00 198 (51. 3) 154 (77. 8) 39 (19. 7) 19 (50. 0) 7 (18. 4) 4 (10. 5) 3 (7. 9) 1 (2. 6) 1 5 (2. 5) Mantel. Haenszel Chi-Square Test* 0. 999 (0. 51 Conclusions: 1. 98) Table 6 - Number of subjects /accesses Difference % Arm B Arm A Arm B 40 (21. 3) 42 (21. 2) 29 (72. 5) 11 (27. 5) 0 (0. 0) 60 49 (81. 7) 11 (18. 3) 32 (76. 2) 8 (19. 0) 2 (4. 8) 67 55 (82. 1) 12 (17. 9) Our experience failed to support the role of a specific HCNP for patients taking oral anticancer therapy. During recent years implementation of recommendations for oral treatments, an improved attention to specific educational practice and an increasing use of prescription writings with accurate information given to all pts receiving oral therapies may explain these results.
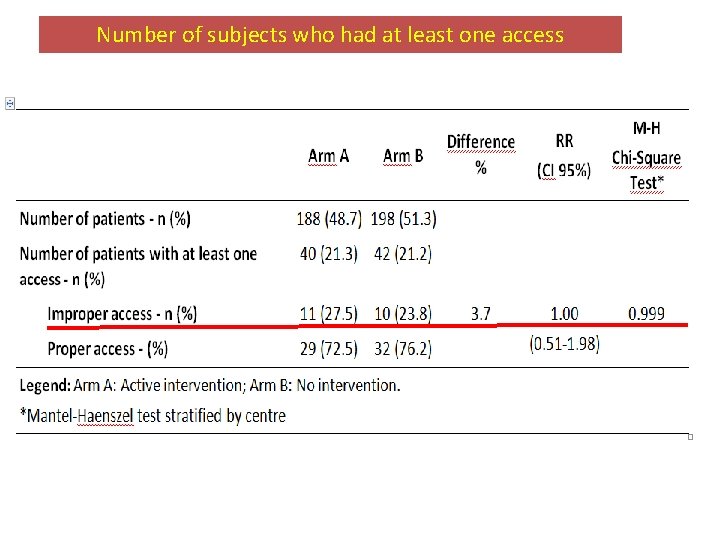
Number of subjects who had at least one access

Associazione Italiana Oncologia Medica B- Ricerca clinica oncologica in Italia: PROBLEMATICHE


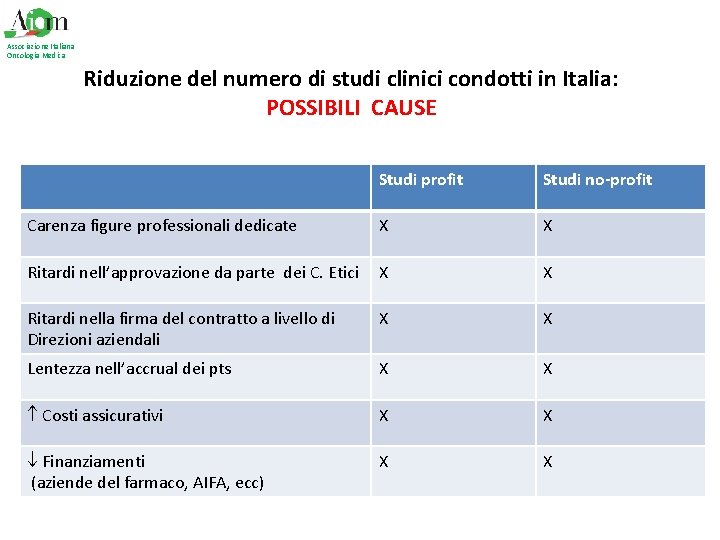
Associazione Italiana Oncologia Medica Riduzione del numero di studi clinici condotti in Italia: POSSIBILI CAUSE Studi profit Studi no-profit Carenza figure professionali dedicate X X Ritardi nell’approvazione da parte dei C. Etici X X Ritardi nella firma del contratto a livello di Direzioni aziendali X X Lentezza nell’accrual dei pts X X Costi assicurativi X X ¯ Finanziamenti (aziende del farmaco, AIFA, ecc) X X
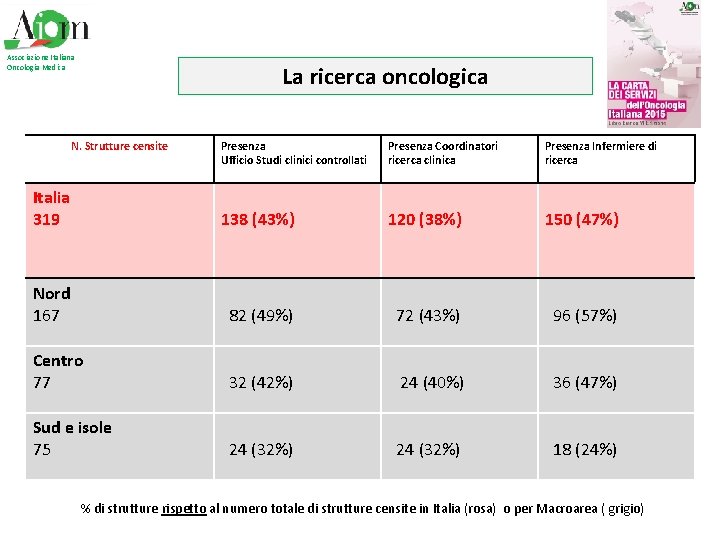
Associazione Italiana Oncologia Medica La ricerca oncologica N. Strutture censite Presenza Ufficio Studi clinici controllati Presenza Coordinatori ricerca clinica Presenza Infermiere di ricerca Italia 319 138 (43%) 120 (38%) 150 (47%) Nord 167 82 (49%) 72 (43%) 96 (57%) Centro 77 32 (42%) 24 (40%) 36 (47%) Sud e isole 75 24 (32%) 18 (24%) % di strutture rispetto al numero totale di strutture censite in Italia (rosa) o per Macroarea ( grigio)

Time required to start multicentre clinical trials within the Italian Medicine Agency programme of support for independent research. De Feo G , Frontini L, Rota S, Pepe A, Signoriello S, Labianca R, Sobrero A, De Placido S, Perrone F. J Med Ethics 2015 RESULTS: 106 centres applied to participate in FATA-GIM 3 and 137 in TOSCA. An IEC opinion was issued by 100/106 (1 negative opinion) and 137/137 (2 negative opinions) centres, with a median time from submission of 3. 6 months (range 0. 160. 2). After a positive IEC opinion, the median time before signing the trial contract was 3. 3 months (0. 1 -59. 2). Contracts were signed with 93/99 and 135/135 centres, with a median time from submission of study documentation of 8. 4 months (0. 5 -61. 1). Times for NAS trials were not substantially different. CONCLUSIONS: FATA-GIM 3 and TOSCA centres were opened after a median of 8 months, consisting of nearly 4 months each for IEC opinion and administrative signature, similar to the NAS trials. The process of trial activation in Italy remains inefficient and takes far longer than legally allowed.

La Direttiva europea 2001 sulla sperimentazione clinica 15 anni di esperienza. . L’obiettivo di un approccio armonizzato è stato raggiunto solo in parte, conseguenti difficoltà a condurre trial clinici nei diversi Stati membri Miglioramenti in materia di: • sicurezza • validità etica • affidabilità dei dati In Europa, dal 2007 al 2011: • numero di domande diminuito del 25% (da 5. 109 a 4. 127) • costi aumentati (per gli sponsor non profit fino al 98%) • personale da dedicare più che raddoppiato (107%) • premi assicurativi aumentati dell’ 800% per gli sponsor industriali • tempo medio d’attesa aumentato del 90%, attestandosi a 152 giorni di media Fonte: Report Commissione europea, 17 luglio 2012)

Conseguenza …. Negli ultimi anni i clinical trial hanno effettuato una vera migrazione … Crescita (o diminuzione) annuale degli investimenti in ricerca, sviluppo e innovazione … verso Paesi a più alta attrattività, che sono riusciti ad investire sempre di più in R&S.
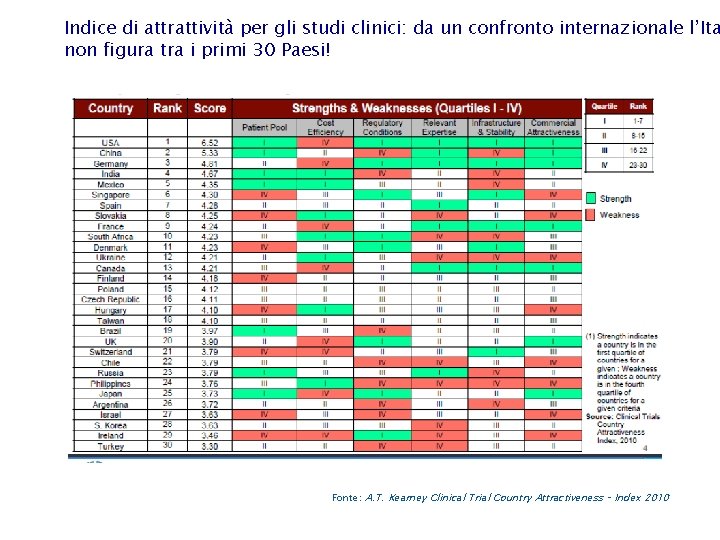
Indice di attrattività per gli studi clinici: da un confronto internazionale l’Ita non figura tra i primi 30 Paesi! Fonte: A. T. Kearney Clinical Trial Country Attractiveness – Index 2010

Associazione Italiana Oncologia Medica C- Ricerca oncologica in Italia e l’impegno di AIOM: organizzazione formazione comunicazione

Milano, 16 aprile 2015: Costituzione “FICOG” Associazione Italiana Oncologia Medica FEDERATION ITALIAN COOPERATIVE ONCOLOGY GROUPS Gruppi cooperativi oncologici italiani fondatori della FICOG AIOM (Associazione Italiana di Oncologia Medica) GOIRC (Gruppo Oncologico Italiano di Ricerca Clinica) GONO (Gruppo Oncologico Nord Ovest) ITMO (Italian Trials in Medical Oncology) GOIM (Gruppo Oncologico Italia Meridionale) GISCAD (Gruppo Italiano Studio Carcinomi App. Digerente) ISG (Italian Sarcoma Group, 1997) ) MITO (Multicenter Italian Trials in Ovarian Cancer) IMI (Intergruppo Melanoma Italiano) APRIC – CTPG (Clinical Trials Promoting Group) GIM-ONCOTECH (Gruppo Italiano Mammella) IGCCG (Italian Germ Cell Cancer Group) ASTRO (Association for Traslation Research in Oncology) Fondazione NIBIT (Network Italiano per la bioimmunoterapia dei tumori) APRIC (Associazione per la promozione Ricerca Clinica)

Associazione Italiana Oncologia Medica Obiettivi • Implementazione della ricerca clinica oncologica • Accreditamento dei Gruppi aderenti e dei centri oncologici • Proposte di legge e lobby per la definizione : -di un network italiano riconosciuto da AIFA e dal SSN; -delle figure professionali impegnate nella ricerca clinica (infermiere di ricerca, data manager. . ) • Collaborazione internazionale con altri gruppi e con l’industria.

Associazione Italiana Oncologia Medica Working Group AIOM Clinical Study Coordinator (CSC) Costituito a Milano, in Via E. Nöe 23, il 12 marzo 2015 Motivazioni: -importanza crescente della ricerca oncologica in Italia, -necessità della presenza del CSC nelle strutture oncologiche, -assenza di un riconoscimento amministrativo/burocratico di questa figura. Obiettivi : 1 - identificare una formazione specifica (Master, Laurea breve, etc. ). 2 - identificare le competenze del CSC; 3 - intraprendere azioni per ottenere il riconoscimento burocratico/amministrativo;

Associazione Italiana Oncologia Medica Working Group AIOM Clinical Study Coordinator (CSC)

Associazione Italiana Oncologia Medica Convegni 2015 e 2016 sulla ricerca clinica alla luce del nuovo Regolamento Europeo 2014 FORMAZIONE

Associazione Italiana Oncologia Medica FORMAZIONE

FORMAZIONE Associazione Italiana Oncologia Medica

La buona informazione produce salute. Dalle informazioni che diamo derivano: -stili di vita -prevenzione/diagnosi precoce -modalità di cura Luciano Onder ETICA DEL DARE LA NOTIZIA

www. aiom. it STUDI CLINICI
Per individuare studi clinici sia su criteri geografici, sia in base a caratteristiche come la sede del tumore o i farmaci utilizzati

Associazione Italiana Oncologia Medica D- Ricerca oncologica in Italia e l’impegno di AIOM: COSTRUIRE QUALITA’


Progetto per la caratterizzazione bio-molecolare in funzione terapeutica dei tumori solidi • Garantire per ogni paziente nell’intero territorio nazionale la possibilità di accesso a test molecolari validati • Appropriatezza delle indicazioni cliniche per il test • Appropriatezza del test di biologia molecolare per la singola neoplasia • Appropriatezza metodologica

Associazione Italiana Oncologia Medica D- Ricerca oncologica in Italia e l’impegno di AIOM: REPERIRE FONDI

Associazione Italiana Oncologia Medica Borse di studio 2015 AIOM-Fondazione AIOM Progetti supportati da 30 borse di studio da 25. 000€ finanziate da MSD Italia. Presentazione dei progetti inviata alla Segreteria Nazionale AIOM entro il 20 settembre 2014 da parte di Oncologi iscritti all’AIOM, di età inferiore a 40 anni. Commissione giudicatrice, individuata dal Consiglio Direttivo Nazionale AIOM (Iacono C, Pinto C, Del Mastro L, Cinieri S, Tonini G, Perrone F): ha esaminato 85 progetti. Comunicazione ufficiale sull’esito della selezione pubblicata il 12 dicembre 2014 attraverso il sito ufficiale www. AIOM. it

Associazione Italiana Oncologia Medica Bando AIOM Progetti di ricerca 2016 - Progetti totali esaminati: 83 - La valutazione degli 83 progetti pervenuti è stata effettuata da Reviewers stranieri - Progetti selezionati: 3

Associazione Italiana Oncologia Medica CONCLUDENDO…. .

Ricerca clinica oncologica in Italia Considerando la ricerca biomedica nel suo complesso, i ricercatori italiani risultano peraltro sempre ai primi posti per numero e qualità delle pubblicazioni scientifiche, testimoniando l’esistenza di una competenza consolidata che rappresenta quindi una notevole opportunità da cogliere e sviluppare.

La qualità della ricerca oncologica in Italia Associazione Italiana Oncologia Medica 2 5 1 0 t e nc La 0 A 2 11 JAM 6 A M JA 1 20

La qualità della ricerca oncologica in Italia Associazione Italiana Oncologia Medica 2014 Carboplatin plus paclitaxel once a week versus every 3 weeks in patients with advanced ovarian cancer (MITO-7): a randomised, multicentre, openlabel, phase 3 trial Pignata S et al, on behalf of the Multicentre Italian Trials in Ovarian cancer (MITO-7) 2014

2015 Erlotinib versus docetaxel as second-line treatment of patients with advanced nonsmall-cell lung cancer and wild-type EGFRtumours (TAILOR): a randomised controlled trial Marina Chiara Garassino, et al, on behalf of the TAILOR trialists

Nuovo Regolamento UE: una risposta per incrementare la ricerca clinica e migliorare la competitività La forma giuridica del Regolamento: • garantisce una procedura coerente per la presentazione delle domande e le loro modifiche sostanziali; • evita misure di recepimento nazionali divergenti; • semplifica sulla base di un unico quadro normativo, (non a mosaico degli Stati membri). La nuova norma, tuttavia: • non incide né interferisce sull’organizzazione degli Stati membri, in riferimento alle strutture incaricate di autorizzare una sperimentazione clinica; • non regolamenta né armonizza nel dettaglio il funzionamento dei Comitati etici, né impone una cooperazione sistematica a livello operativo tra i Comitati etici nella UE; • non si applica agli studi non interventistici (osservazionali).

Riorganizzazione strutturale e funzionale del sistema della ricerca clinica in Italia Condizione indispensabile in vista dell’attuazione del nuovo Regolamento UE per: • dare l’opportunità ai pazienti di accedere a terapie innovative • sviluppare ricerca e sviluppo presso i numerosi centri di eccellenza riconosciuti a livello internazionale • incrementare la capacità e la crescita professionale dei ricercatori • far aumentare gli investimenti in ricerca e sviluppo da parte delle imprese • trasferire risorse al SSN (costi diretti e indiretti a carico dello sponsor) • accrescere i livelli di competitività del sistema nel contesto internazionale di ricerca

Cosa CHIEDE AIOM Associazione Italiana Oncologia Medica Collaborazione: • Istituzioni: AIFA; Ministero Salute, ISS, AGENAS • Società scientifiche, • Direzioni Generali, • IRCCS, • FIASO, • COMU, • Farmindustria, • FADOI, • Comitati Etici, • Associazioni pazienti • EUPATI • Risorse economiche dedicate e adeguate • Implementazione degli organici nelle strutture oncologiche • Creazione di uffici studi clinici controllati • Sistemi informatizzati • Interazione ottimale con i Comitati etici, per assicurare un efficiente e tempestivo processo di valutazione e autorizzazione • Progetto ongoing: -Identificazione di metodi per quantificare l’impatto della ricerca in termini di ricaduta economica sulle strutture ove viene condotta e sul SSN(Progetto AIOM- Fondazione AIOMBocconi).
- Slides: 43



































































