2 Enlace qumico e interacciones no covalentes Estructura














- Slides: 28

2. Enlace químico e interacciones no covalentes

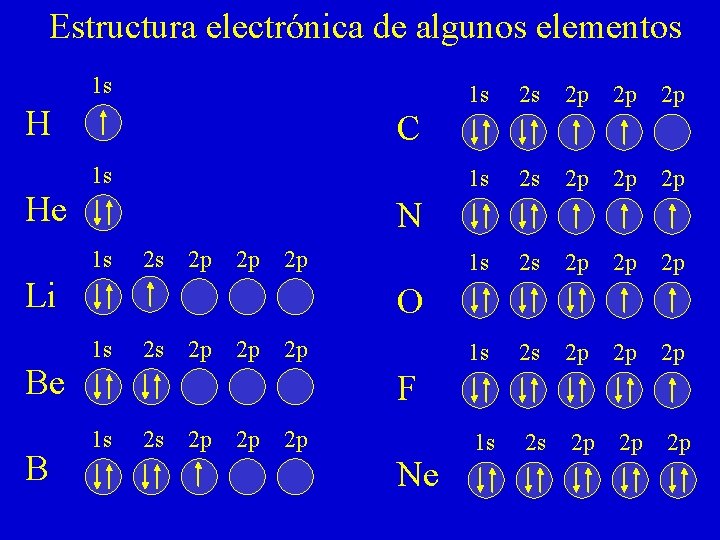
Estructura electrónica de algunos elementos 1 s H He 2 p 2 p 2 p 1 s 2 s 2 p 2 p 2 p N 1 s 2 s 2 p 2 p 2 p Li B 2 s C 1 s Be 1 s O 1 s 2 s 2 p 2 p 2 p F 1 s 2 s 2 p 2 p 2 p Ne

Enlaces iónicos A • + B • A+ + : B- 1. Fuertes (>50 kcal/mol) 2. Propios del estado cristalino 3. Elementos extremos en la Tabla Periódica

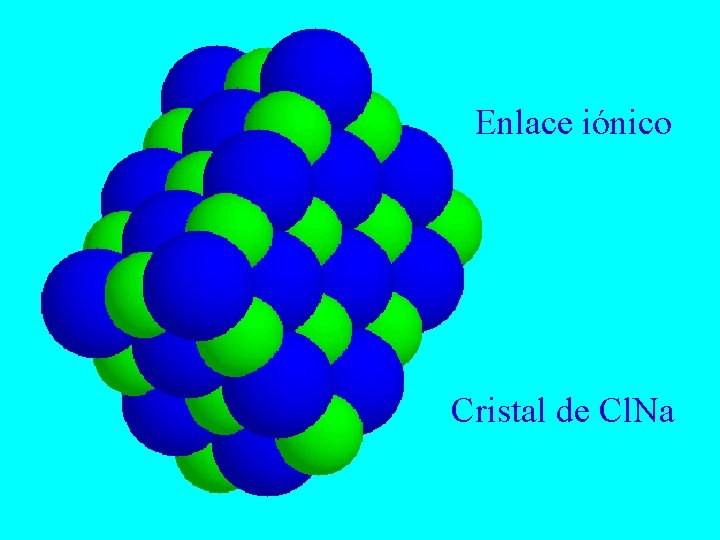
Enlace iónico Cristal de Cl. Na

Enlaces covalentes 1. Compartición de electrones en orbitales moleculares 2. Estado sólido, líquido y gas 3. Fuertes (>50 kcal/mol) 4. Tantos como orbitales con electrones desapareados

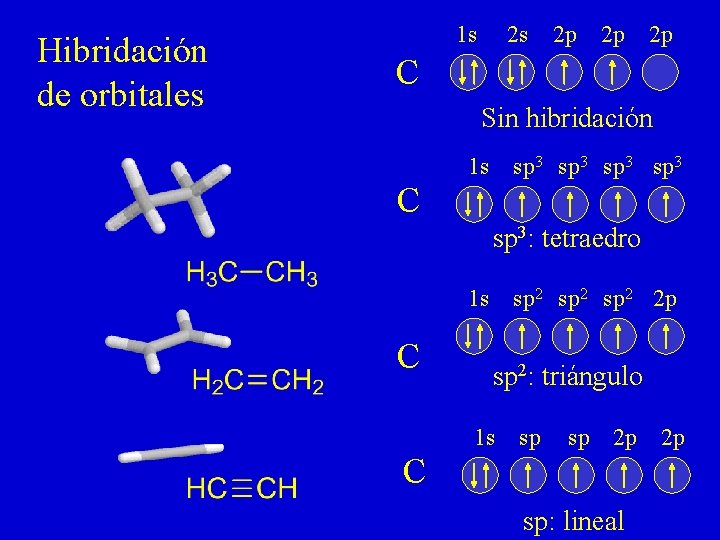
Hibridación de orbitales 1 s 2 s 2 p 2 p 2 p C Sin hibridación 1 s sp 3 C sp 3: tetraedro 1 s C sp 2 2 p sp 2: triángulo 1 s sp sp 2 p 2 p C sp: lineal

Energía de enlaces covalentes, kcal/mol H-H H-Cl 102 HO-H H 2 N-H H 3 C-H 103 119 107 102

Enlaces de coordinación Orbital molecular formado por: - Un orbital vacío - Un par electrónico Dador: átomos con pares electrónicos: N, O Aceptor: orbital vacío (átomos metálicos)

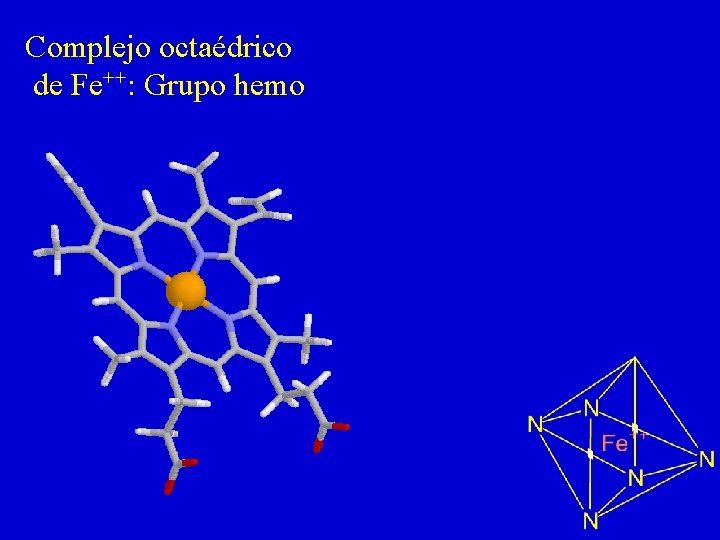
Complejo octaédrico de Fe++: Grupo hemo

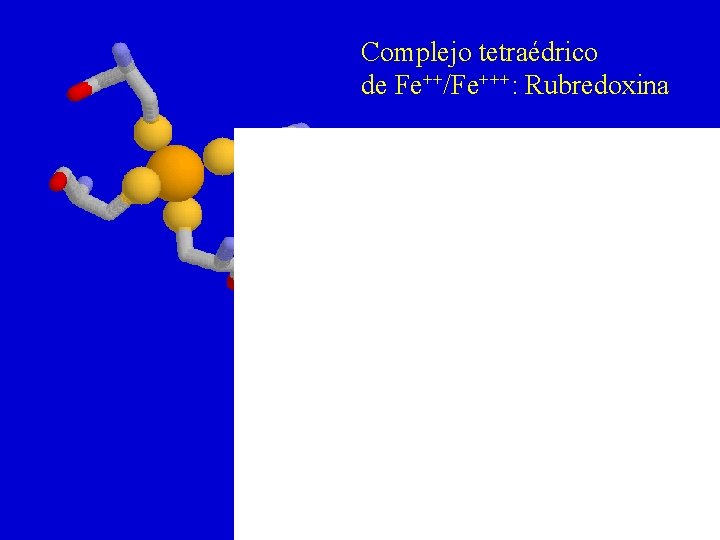
Complejo tetraédrico de Fe++/Fe+++: Rubredoxina

Interacciones débiles 1. Fuerzas de van der Waals 2. Enlaces de hidrógeno 3. Interacciones iónicas o salinas

Fuerzas de van der Waals n. RT = PV n. RT = (P + a/V 2)(V- b) (Gas perfecto) (Gas real) a: Atracción intermolecular b: Volumen de la molécula 1. Dipolos transitorios 2. Dipolos inducidos 3. Dipolos permanentes

Momento dipolar, m H 2 Cl 2 HF HCl H 2 O NH 3 CH 4 0 0 1. 91 1. 08 1. 85 1. 47 0

Fuerzas de van der Waals - Son interacciones muy débiles - En el medio biológico tienen importancia en ausencia de agua - Rotas por detergentes

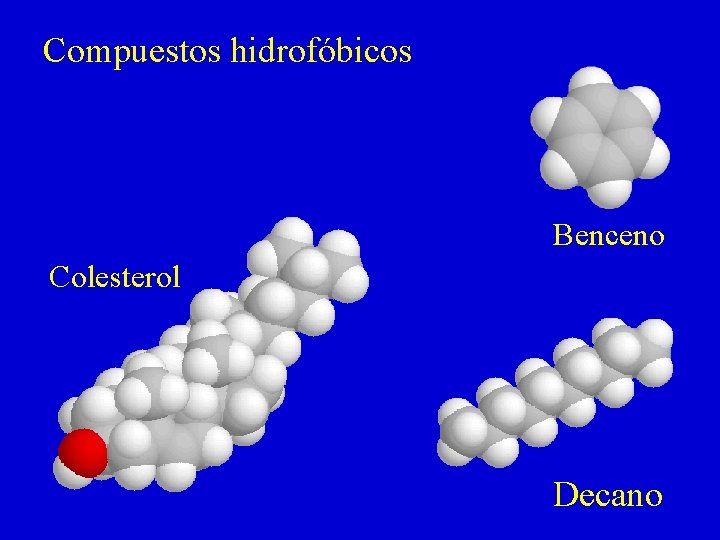
Compuestos hidrofóbicos Benceno Colesterol Decano

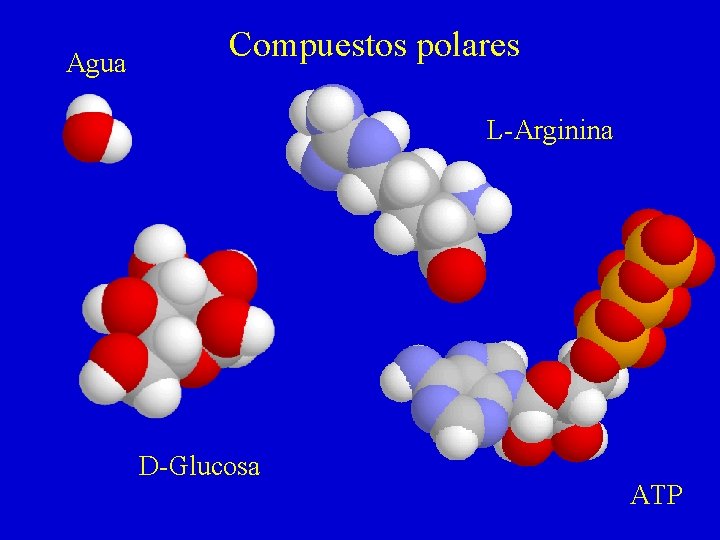
Agua Compuestos polares L-Arginina D-Glucosa ATP

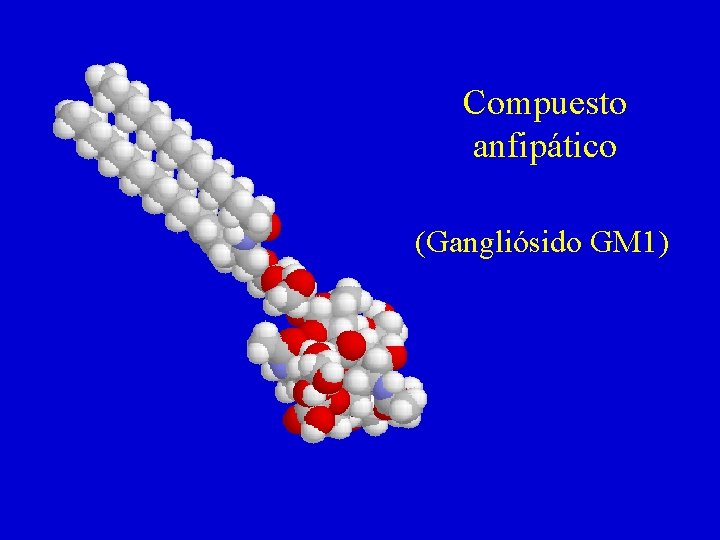
Compuesto anfipático (Gangliósido GM 1)

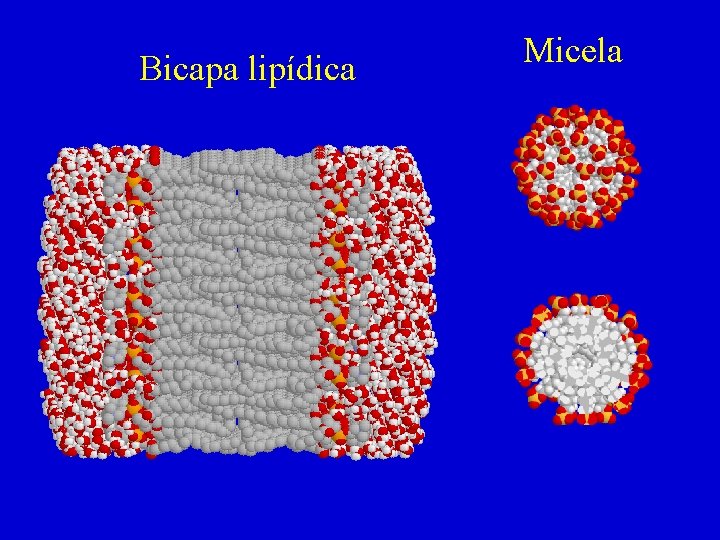
Bicapa lipídica Micela

Enlaces de hidrógeno - Compartición de un protón entre dos pares electrónicos - Dador: Grupo X-H con cierto momento dipolar - Aceptor: Grupo Y: con un par electrónico - Débil (mucho más fuerte que int. de van der Waals) - Rotas por urea 6 M, guanidina 8 M

Algunos enlaces de hidrógeno

DNA conformación B Estructura mantenida por enlaces de H

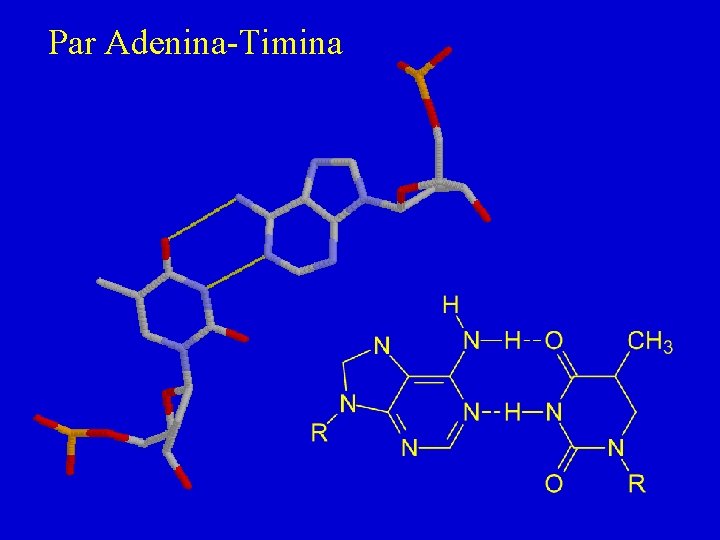
Par Adenina-Timina

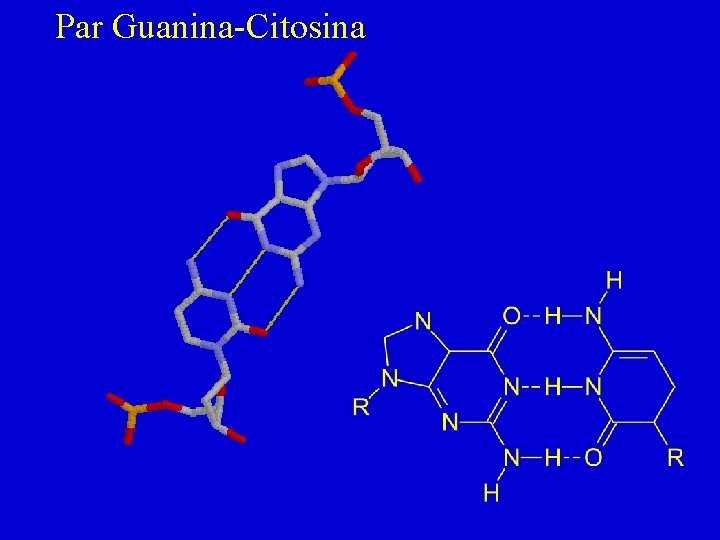
Par Guanina-Citosina

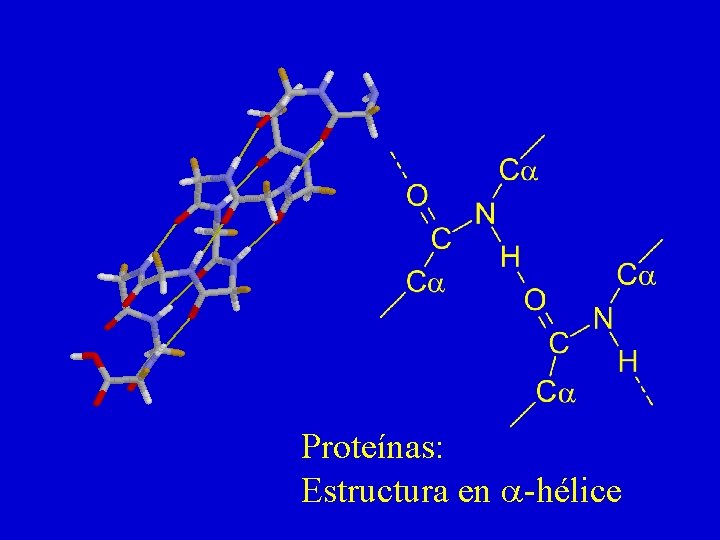
Proteínas: Estructura en a-hélice

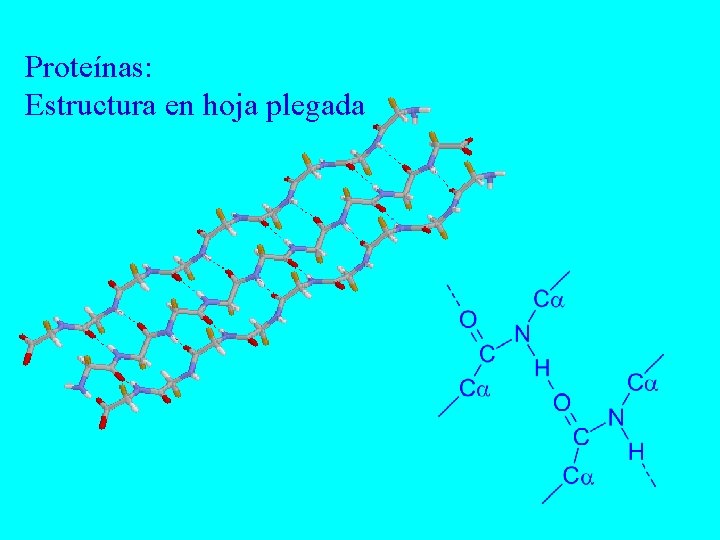
Proteínas: Estructura en hoja plegada

Interacciones iónicas o salinas (No confundir con enlace iónico) - Entre grupos de carga opuesta en solución - Débiles (más fuertes que int. de van der Waals) - Los iones participantes aparecen solvatados - Rotas por altas concentraciones salinas, extremos de p. H

Solvatación de iones en solución

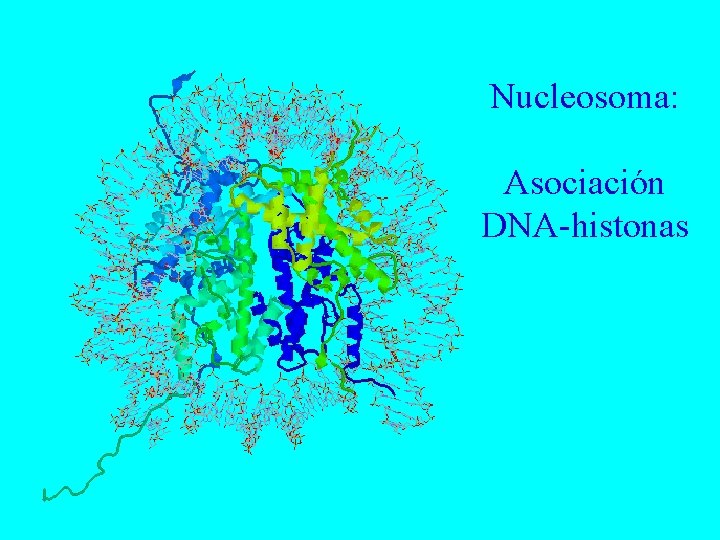
Nucleosoma: Asociación DNA-histonas