Qumica 2 BAC U 2 Enlace Qumico Enlace

Química 2º BAC U. 2 Enlace Químico Enlace de hidrógeno
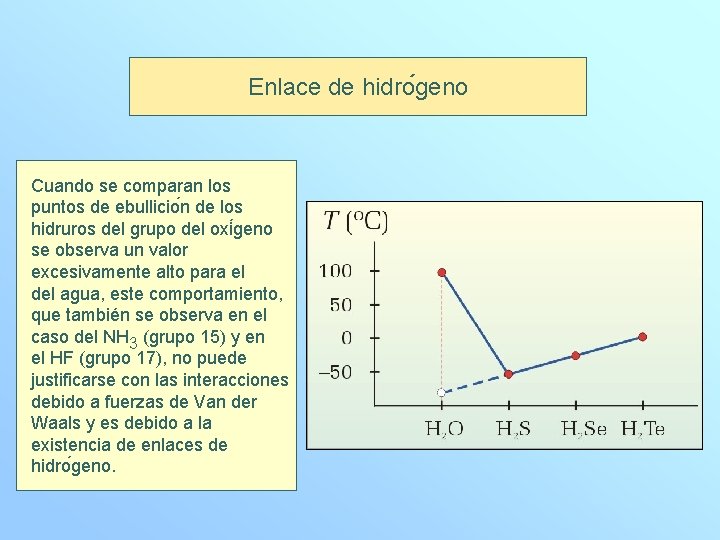
Enlace de hidro geno Cuando se comparan los puntos de ebullicio n de los hidruros del grupo del oxi geno se observa un valor excesivamente alto para el del agua, este comportamiento, que también se observa en el caso del NH 3 (grupo 15) y en el HF (grupo 17), no puede justificarse con las interacciones debido a fuerzas de Van der Waals y es debido a la existencia de enlaces de hidro geno.
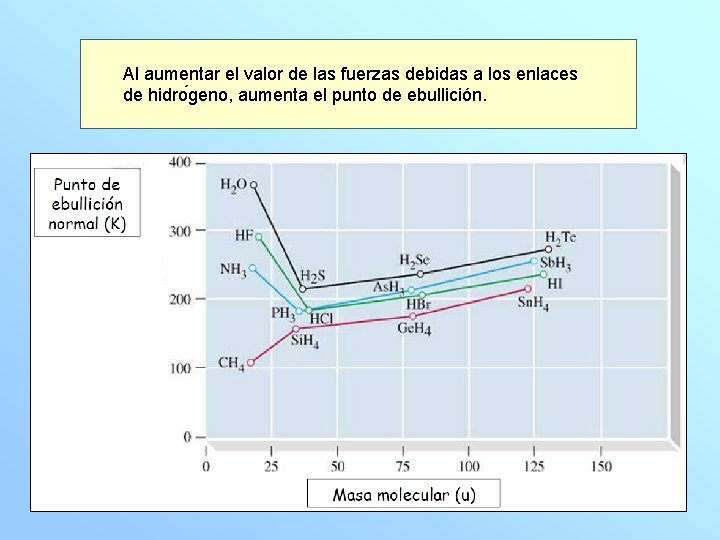
Al aumentar el valor de las fuerzas debidas a los enlaces de hidro geno, aumenta el punto de ebullición.
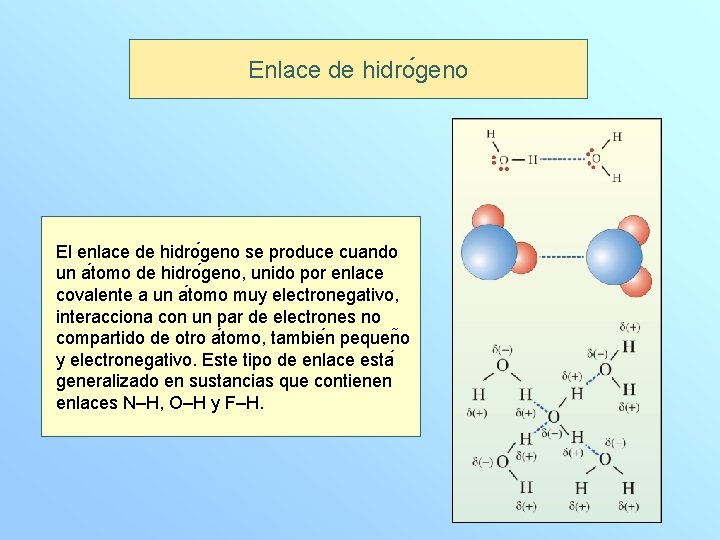
Enlace de hidro geno El enlace de hidro geno se produce cuando un a tomo de hidro geno, unido por enlace covalente a un a tomo muy electronegativo, interacciona con un par de electrones no compartido de otro a tomo, tambie n pequen o y electronegativo. Este tipo de enlace esta generalizado en sustancias que contienen enlaces N–H, O–H y F–H.
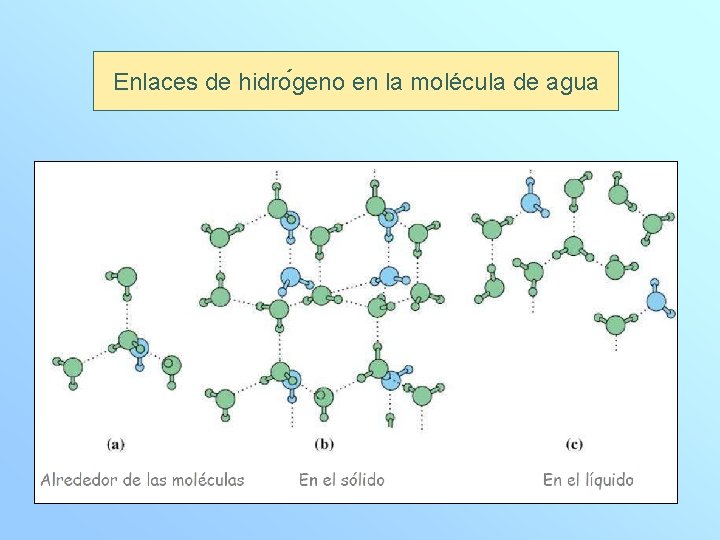
Enlaces de hidro geno en la molécula de agua
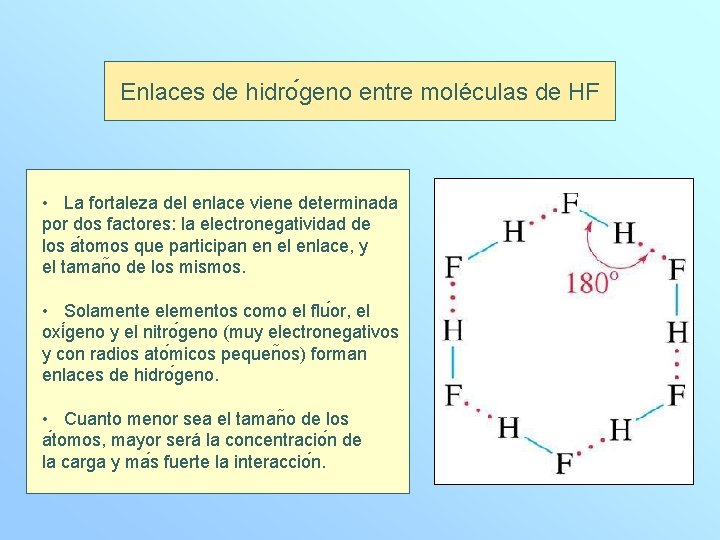
Enlaces de hidro geno entre moléculas de HF • La fortaleza del enlace viene determinada por dos factores: la electronegatividad de los a tomos que participan en el enlace, y el taman o de los mismos. • Solamente elementos como el flu or, el oxi geno y el nitro geno (muy electronegativos y con radios ato micos pequen os) forman enlaces de hidro geno. • Cuanto menor sea el taman o de los a tomos, mayor será la concentracio n de la carga y ma s fuerte la interaccio n.
- Slides: 6