Enlace qumico II Geometra molecular e hibridacin de
Enlace químico II: Geometría molecular e hibridación de orbitales atómicos Unidad 4 Copyright © The Mc. Graw-Hill Companies, Inc. Química, R. Chang, Séptima Edición.
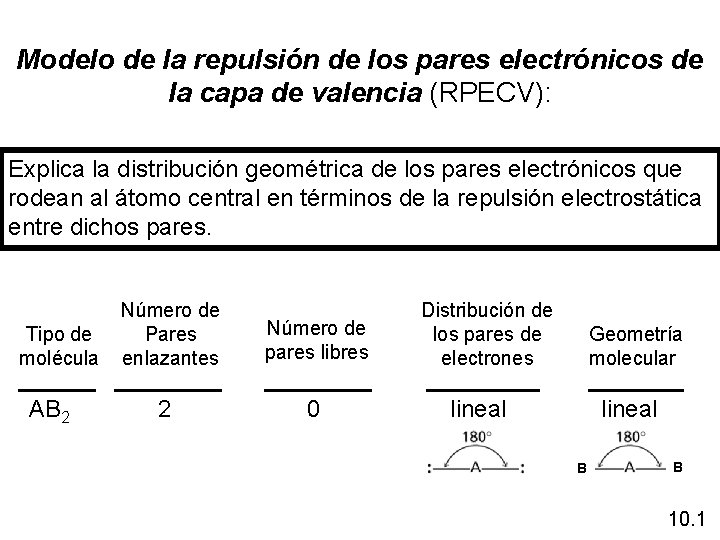
Modelo de la repulsión de los pares electrónicos de la capa de valencia (RPECV): Explica la distribución geométrica de los pares electrónicos que rodean al átomo central en términos de la repulsión electrostática entre dichos pares. Tipo de molécula AB 2 Número de Pares enlazantes Número de pares libres 2 0 Distribución de los pares de electrones Geometría molecular lineal B B 10. 1
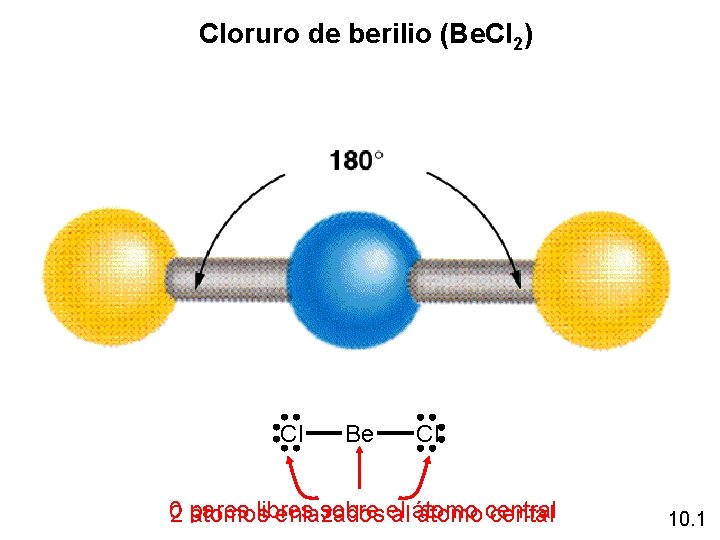
Cloruro de berilio (Be. Cl 2) Cl Be Cl 0 pares libres sobre el átomo central 2 átomos enlazados al átomo cental 10. 1
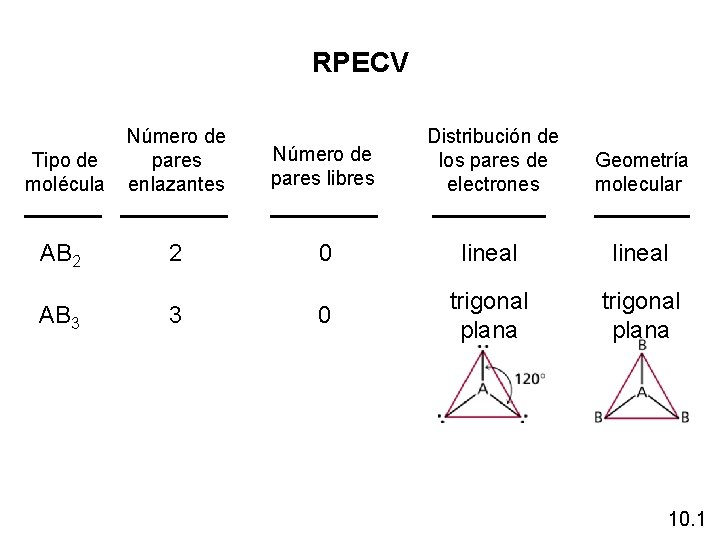
RPECV Tipo de molécula Número de pares enlazantes Número de pares libres Distribución de los pares de electrones Geometría molecular AB 2 2 0 lineal AB 3 3 0 trigonal plana 10. 1
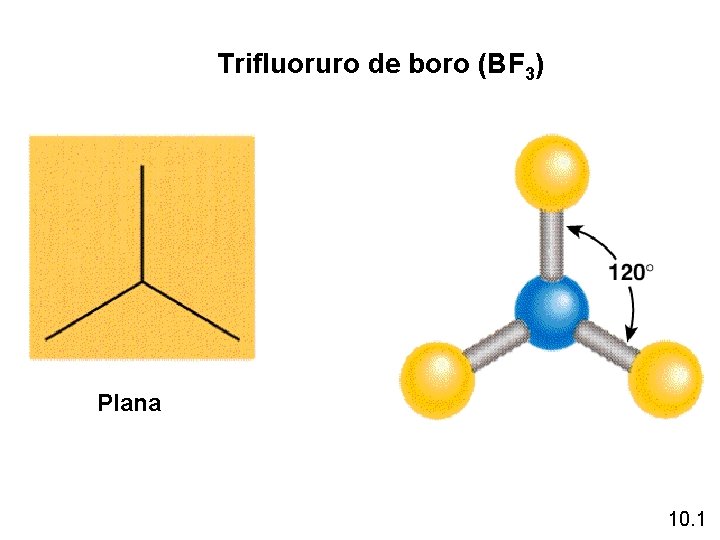
Trifluoruro de boro (BF 3) Plana 10. 1
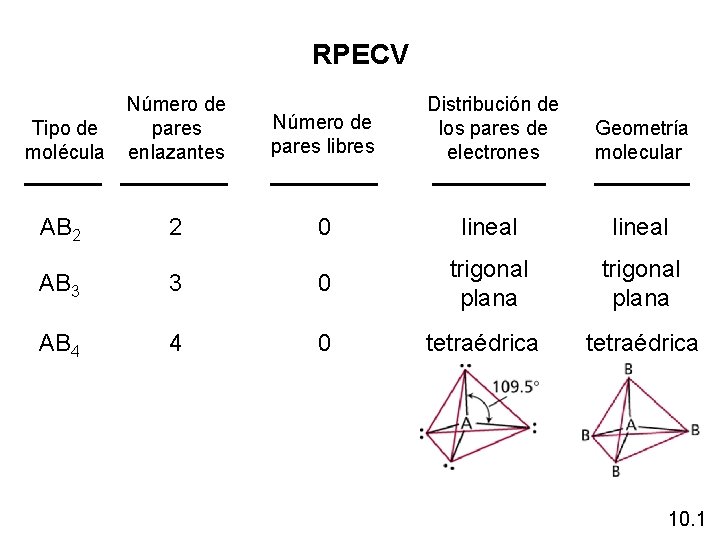
RPECV Tipo de molécula Número de pares enlazantes Número de pares libres Distribución de los pares de electrones Geometría molecular AB 2 2 0 lineal AB 3 3 0 trigonal plana AB 4 4 0 tetraédrica 10. 1
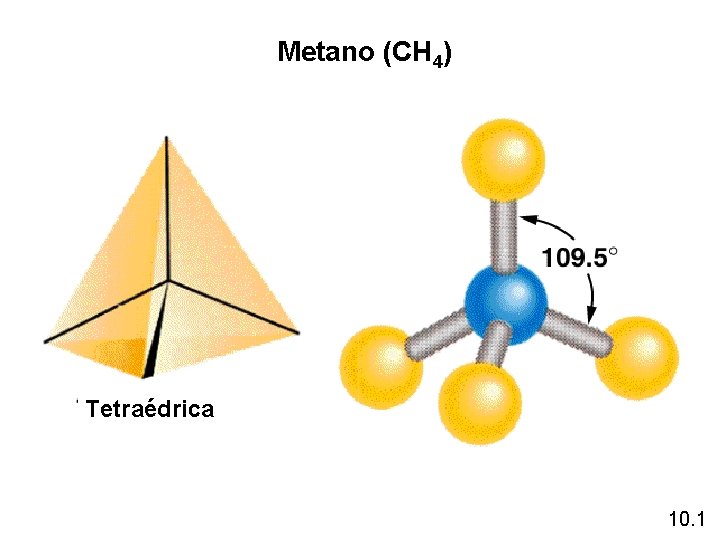
Metano (CH 4) Tetraédrica 10. 1
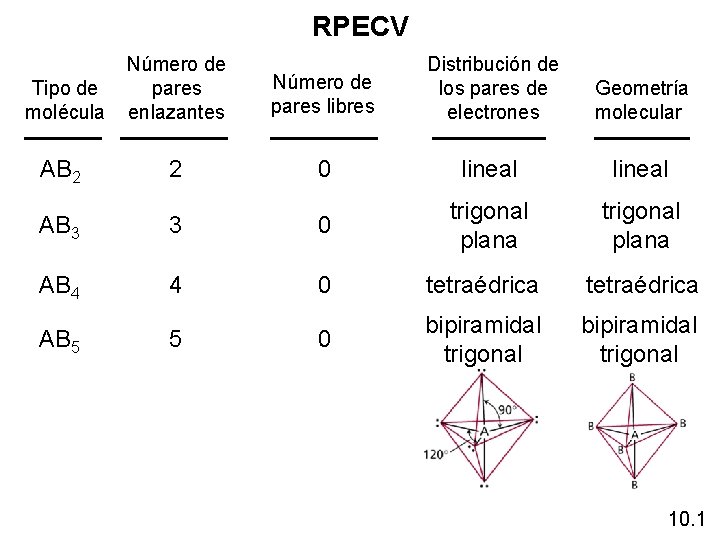
RPECV Tipo de molécula Número de pares enlazantes AB 2 2 Número de pares libres Distribución de los pares de electrones Geometría molecular 0 lineal trigonal plana AB 3 3 0 trigonal plana AB 4 4 0 tetraédrica AB 5 5 0 bipiramidal trigonal 10. 1
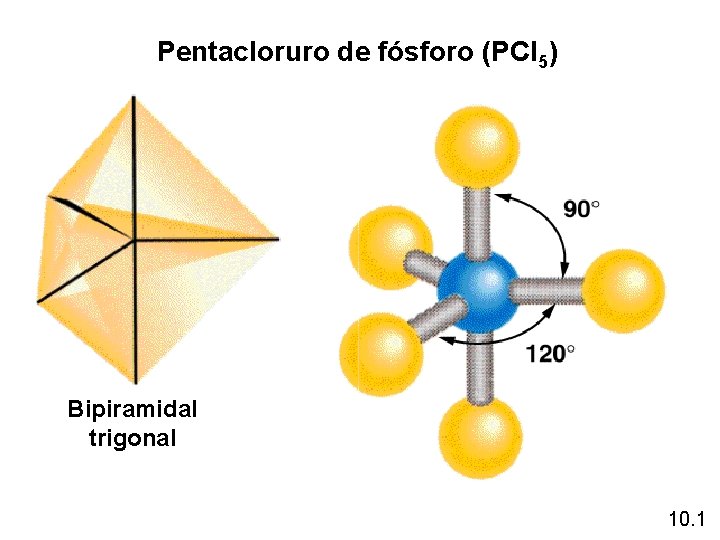
Pentacloruro de fósforo (PCl 5) Bipiramidal trigonal 10. 1
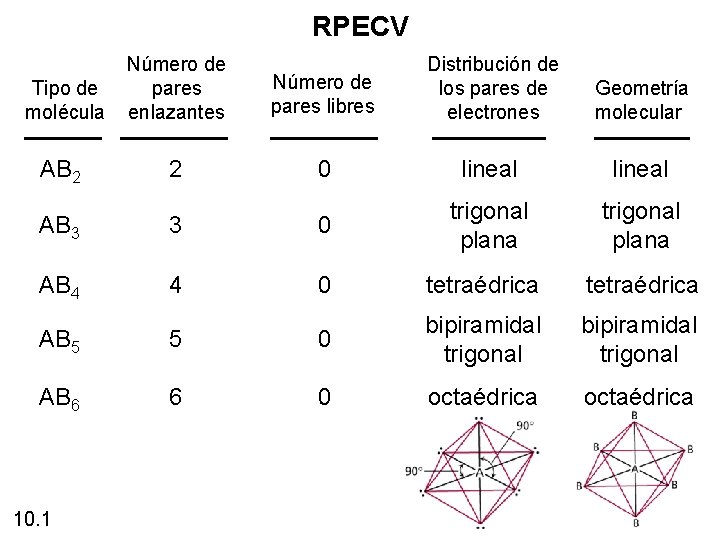
RPECV Tipo de molécula Número de pares enlazantes AB 2 2 Número de pares libres Distribución de los pares de electrones Geometría molecular 0 lineal trigonal plana AB 3 3 0 trigonal plana AB 4 4 0 tetraédrica AB 5 5 0 bipiramidal trigonal AB 6 6 0 octaédrica 10. 1
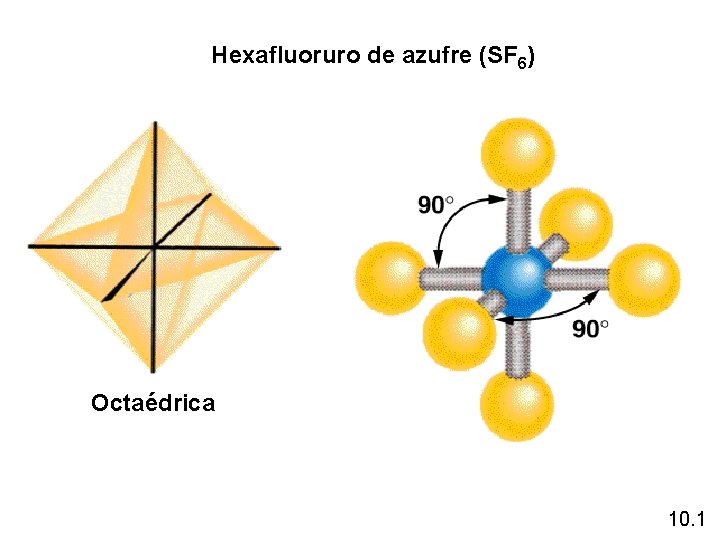
Hexafluoruro de azufre (SF 6) Octaédrica 10. 1
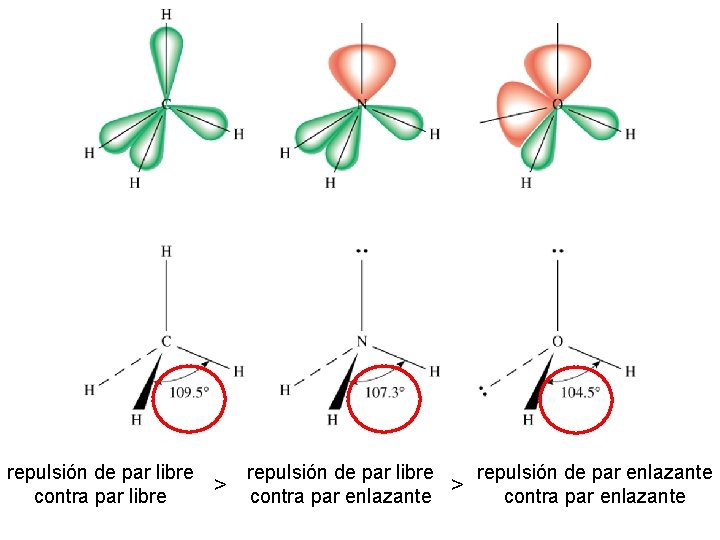
repulsión de par libre contra par libre > repulsión de par libre contra par enlazante > repulsión de par enlazante contra par enlazante
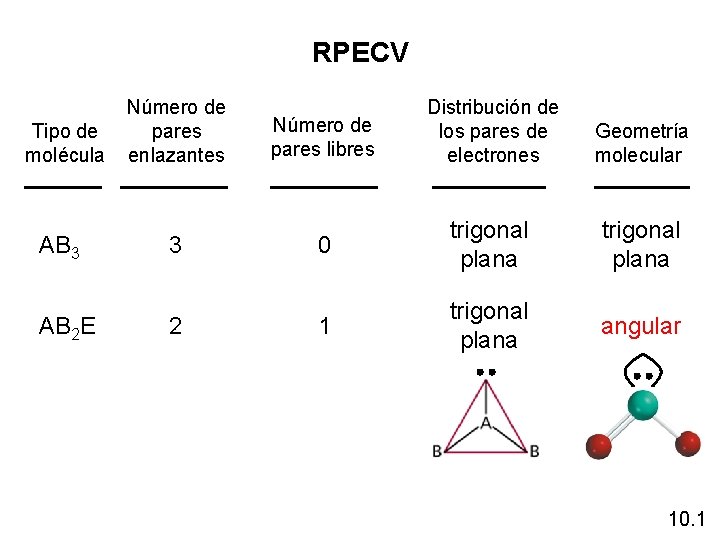
RPECV Tipo de molécula AB 3 AB 2 E Número de pares enlazantes 3 2 Número de pares libres Distribución de los pares de electrones Geometría molecular 0 trigonal plana 1 trigonal plana angular 10. 1
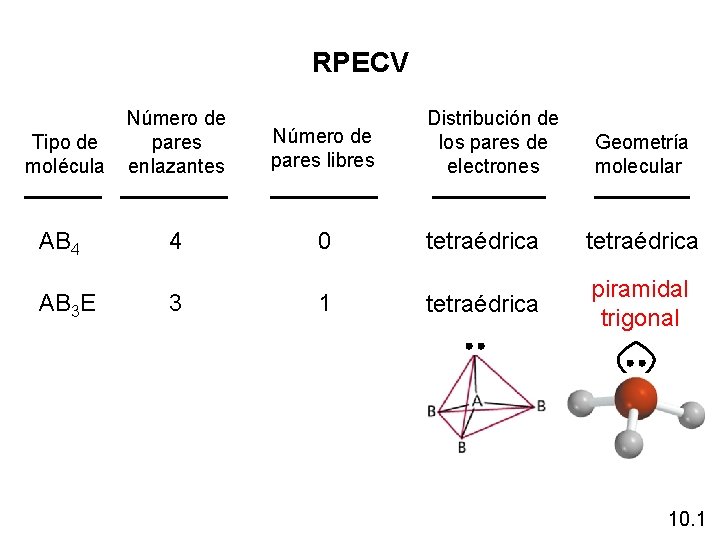
RPECV Tipo de molécula Número de pares enlazantes Distribución de los pares de electrones Número de pares libres AB 4 4 0 tetraédrica AB 3 E 3 1 tetraédrica piramidal trigonal Geometría molecular 10. 1
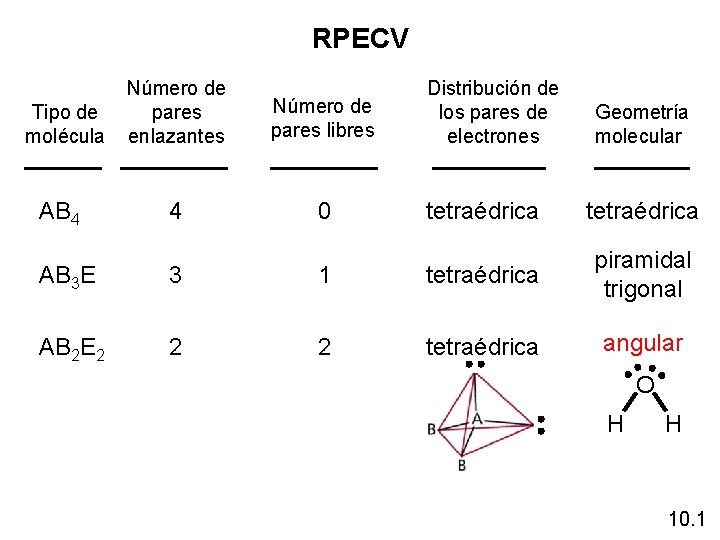
RPECV Tipo de molécula Número de pares enlazantes Distribución de los pares de electrones Número de pares libres AB 4 4 0 tetraédrica AB 3 E 3 1 tetraédrica piramidal trigonal AB 2 E 2 2 2 tetraédrica angular Geometría molecular O H H 10. 1
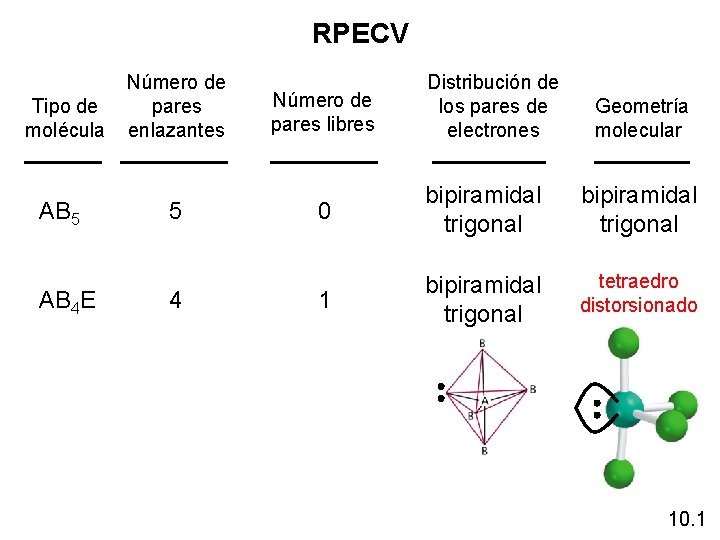
RPECV Tipo de molécula AB 5 AB 4 E Número de pares enlazantes 5 4 Número de pares libres Distribución de los pares de electrones Geometría molecular 0 bipiramidal trigonal 1 bipiramidal trigonal tetraedro distorsionado 10. 1
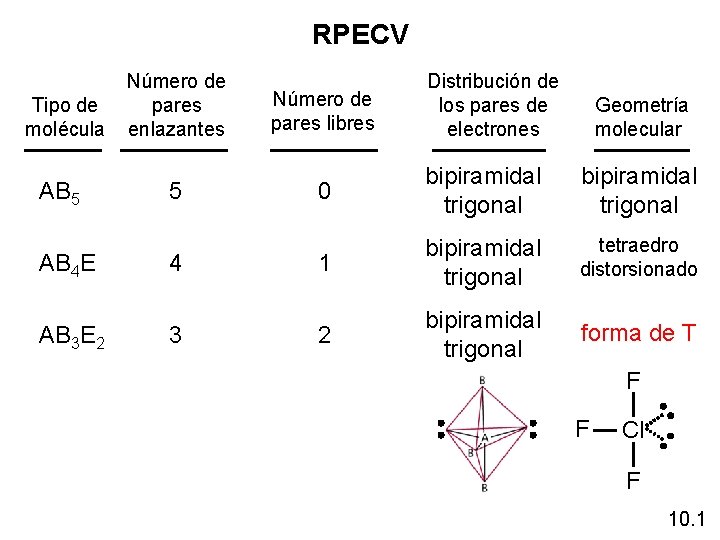
RPECV Tipo de molécula Número de pares enlazantes Distribución de los pares de electrones Número de pares libres AB 5 5 0 bipiramidal trigonal tetraedro distorsionado forma de T AB 4 E 4 1 bipiramidal trigonal AB 3 E 2 3 2 bipiramidal trigonal Geometría molecular F F Cl F 10. 1
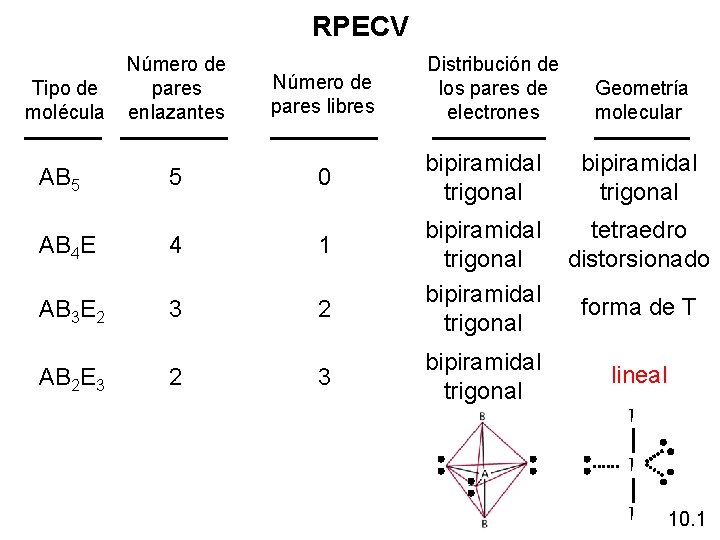
RPECV Tipo de molécula AB 5 Número de pares enlazantes 5 Número de pares libres 0 AB 4 E 4 1 AB 3 E 2 3 2 AB 2 E 3 2 3 Distribución de los pares de electrones Geometría molecular bipiramidal trigonal tetraedro distorsionado bipiramidal trigonal forma de T lineal I I I 10. 1
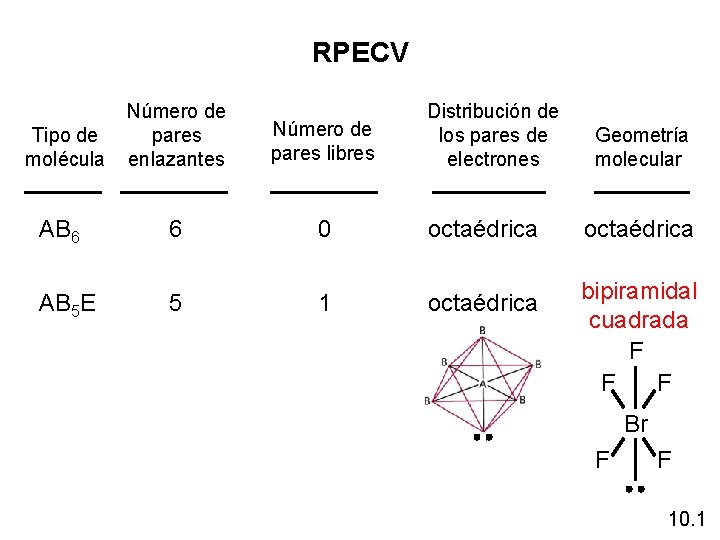
RPECV Tipo de molécula Número de pares enlazantes Distribución de los pares de electrones Número de pares libres AB 6 6 0 octaédrica AB 5 E 5 1 octaédrica bipiramidal cuadrada F F F Geometría molecular Br F F 10. 1
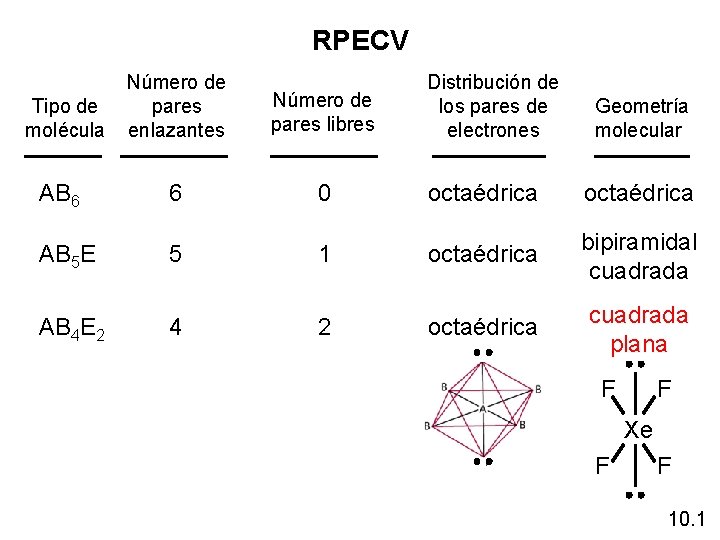
RPECV Tipo de molécula Número de pares enlazantes Distribución de los pares de electrones Número de pares libres AB 6 6 0 octaédrica AB 5 E 5 1 octaédrica bipiramidal cuadrada AB 4 E 2 4 2 octaédrica cuadrada plana Geometría molecular F F Xe F F 10. 1
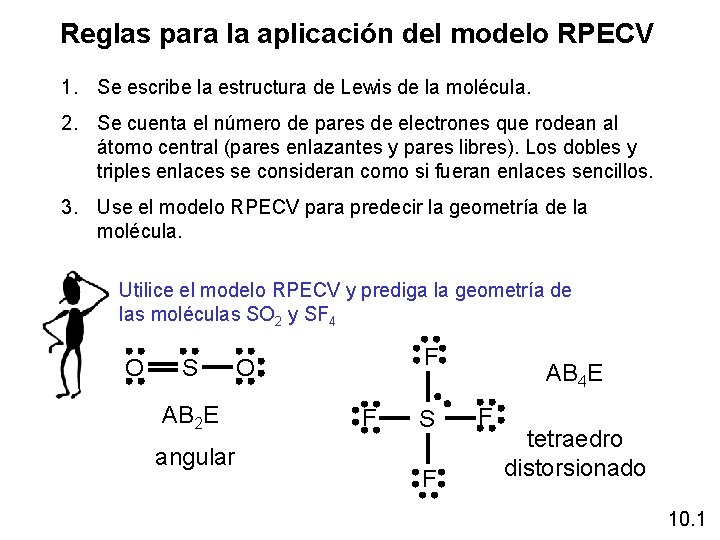
Reglas para la aplicación del modelo RPECV 1. Se escribe la estructura de Lewis de la molécula. 2. Se cuenta el número de pares de electrones que rodean al átomo central (pares enlazantes y pares libres). Los dobles y triples enlaces se consideran como si fueran enlaces sencillos. 3. Use el modelo RPECV para predecir la geometría de la molécula. Utilice el modelo RPECV y prediga la geometría de las moléculas SO 2 y SF 4 O S AB 2 E angular F O F S F AB 4 E F tetraedro distorsionado 10. 1
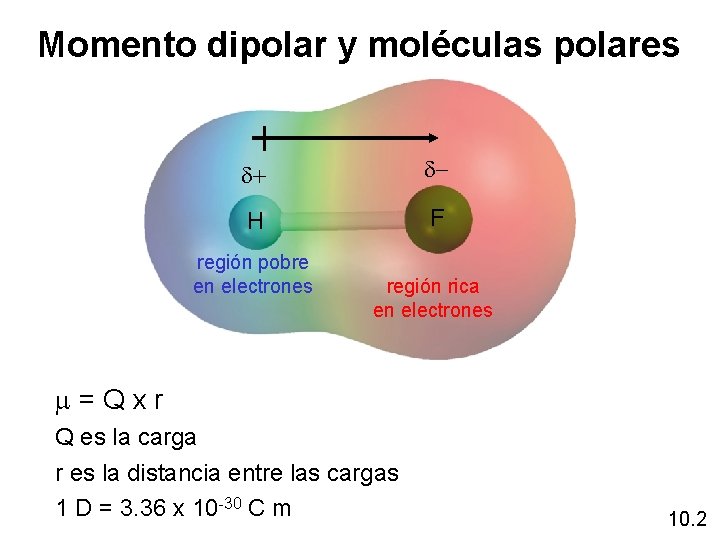
Momento dipolar y moléculas polares d+ d- H F región pobre en electrones región rica en electrones m = Q x r Q es la carga r es la distancia entre las cargas 1 D = 3. 36 x 10 -30 C m 10. 2
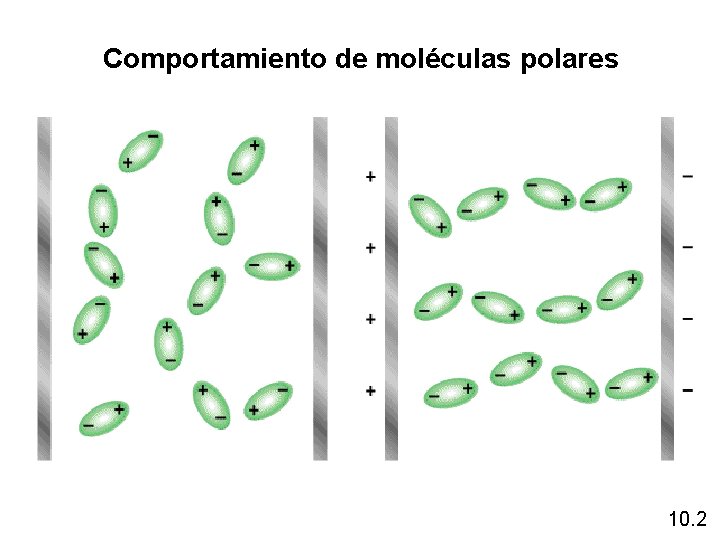
Comportamiento de moléculas polares 10. 2
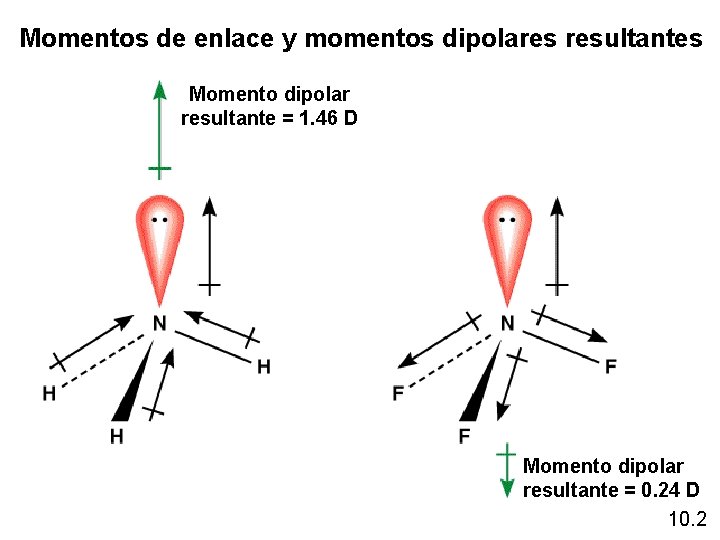
Momentos de enlace y momentos dipolares resultantes Momento dipolar resultante = 1. 46 D Momento dipolar resultante = 0. 24 D 10. 2
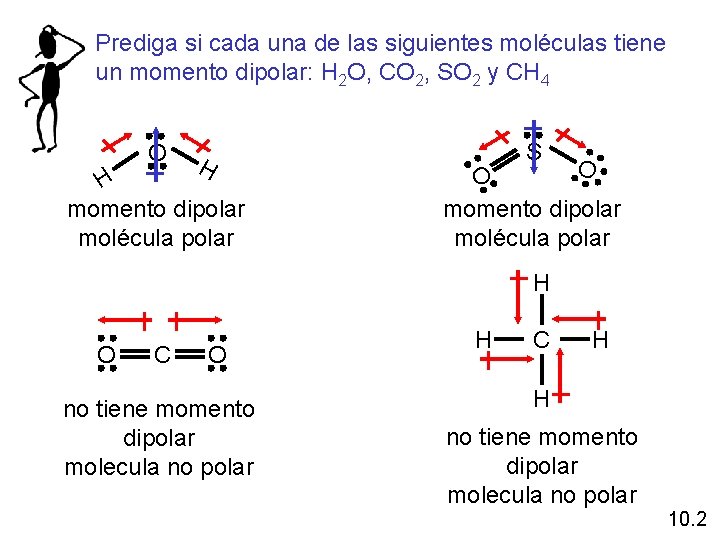
Prediga si cada una de las siguientes moléculas tiene un momento dipolar: H 2 O, CO 2, SO 2 y CH 4 O H H momento dipolar molécula polar S O O momento dipolar molécula polar H O C O no tiene momento dipolar molecula no polar H C H H no tiene momento dipolar molecula no polar 10. 2
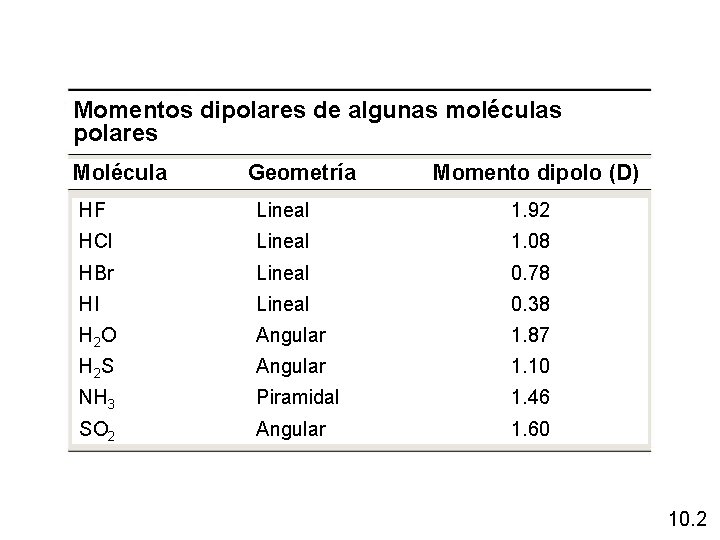
Momentos dipolares de algunas moléculas polares Molécula Geometría Momento dipolo (D) HF Lineal 1. 92 HCl Lineal 1. 08 HBr Lineal 0. 78 HI Lineal 0. 38 H 2 O Angular 1. 87 H 2 S Angular 1. 10 NH 3 Piramidal 1. 46 SO 2 Angular 1. 60 10. 2

¿Cómo describe la teoría de Lewis los enlaces en H 2 y F 2? Como el apareamiento de los dos electrones de los átomos Energías de disociación de enlace Longitudes de enlace Solapamiento de H 2 436. 4 k. J/mol 74 pm 2 1 s F 2 150. 6 k. J/mol 142 pm 2 2 p Teoría del enlace valencia – los enlaces son formados por el apareamiento de e- a partir del solapamiento de los orbitales atómicos. 10. 3
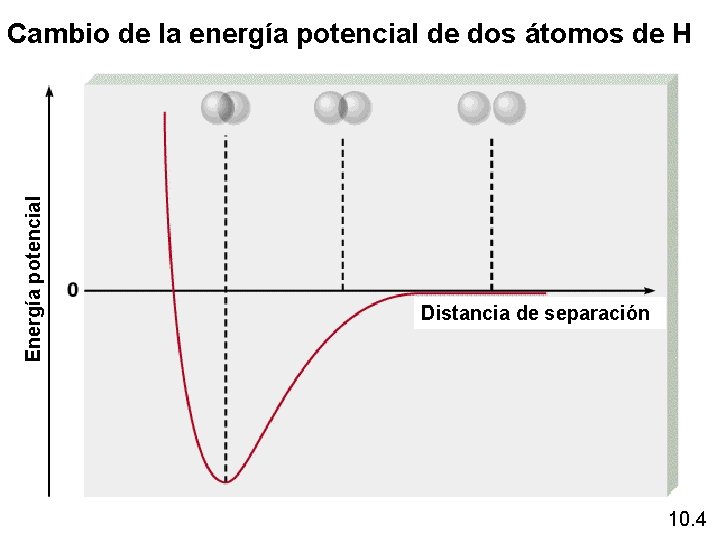
Energía potencial Cambio de la energía potencial de dos átomos de H Distancia de separación 10. 4
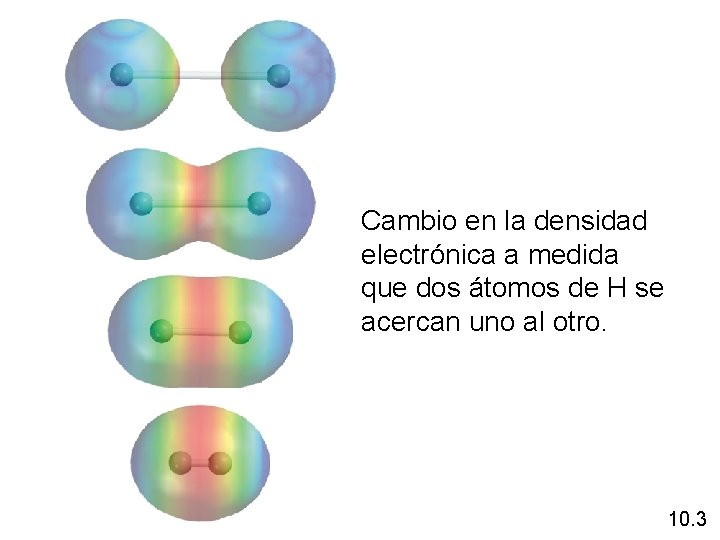
Cambio en la densidad electrónica a medida que dos átomos de H se acercan uno al otro. 10. 3
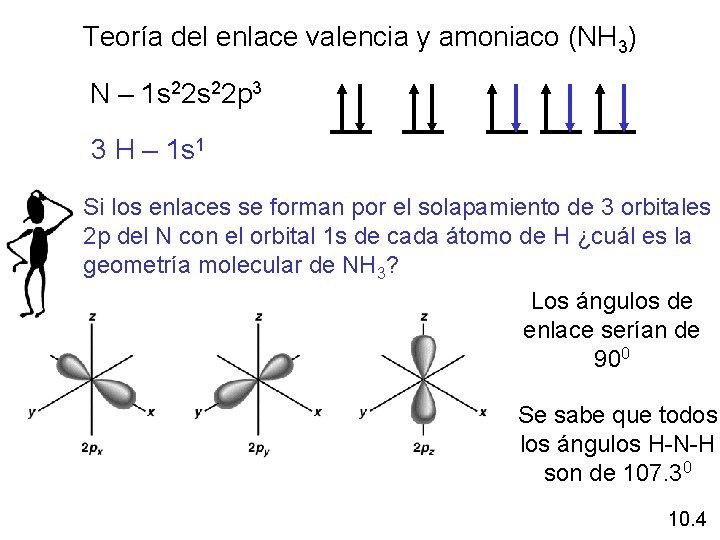
Teoría del enlace valencia y amoniaco (NH 3) N – 1 s 22 p 3 3 H – 1 s 1 Si los enlaces se forman por el solapamiento de 3 orbitales 2 p del N con el orbital 1 s de cada átomo de H ¿cuál es la geometría molecular de NH 3? Los ángulos de enlace serían de 900 Se sabe que todos los ángulos H-N-H son de 107. 30 10. 4

Hibridación – mezcla de los orbitales atómicos en un átomo (por lo general el átomo central) para generar un conjunto de orbitales híbridos. 1. La hibridación es la mezcla de, por lo menos, dos orbitales atómicos no equivalentes, por ejemplo orbitales s y p. Como consecuencia, un orbital híbrido no es un orbital atómico puro. 2. El número de orbitales híbridos generados es igual al número de orbitales atómicos puros que participan en el proceso de hibridación. 3. Los enlaces covalentes se forman por el solapamiento de: a. Orbitales híbridos con orbitales atómicos puros. b. Orbitales híbridos con otros orbitales híbridos. 10. 4
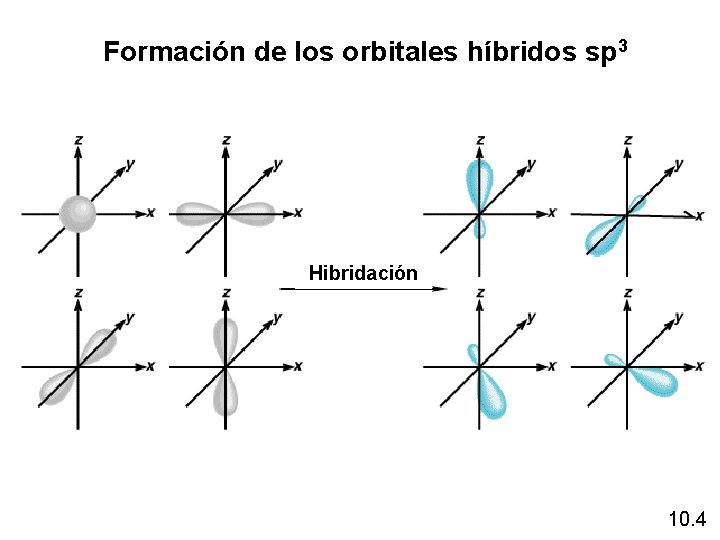
Formación de los orbitales híbridos sp 3 Hibridación 10. 4
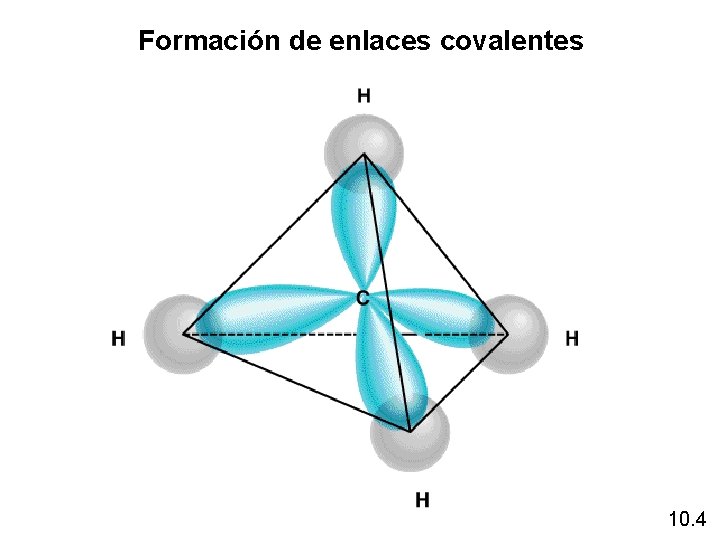
Formación de enlaces covalentes 10. 4
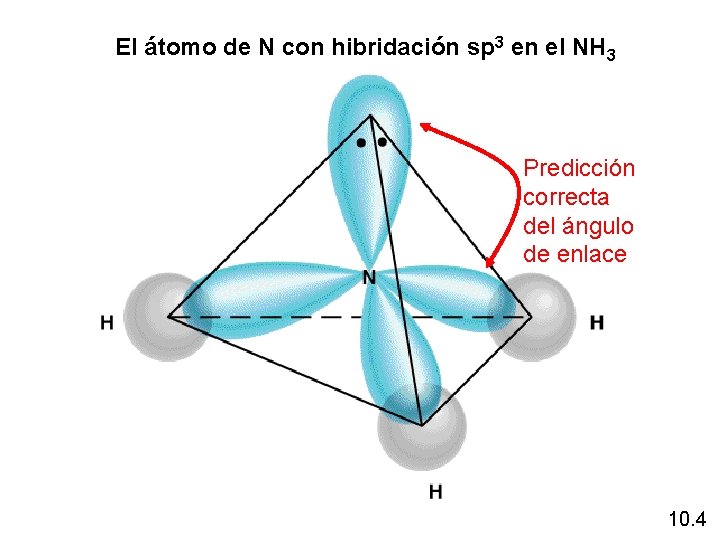
El átomo de N con hibridación sp 3 en el NH 3 Predicción correcta del ángulo de enlace 10. 4
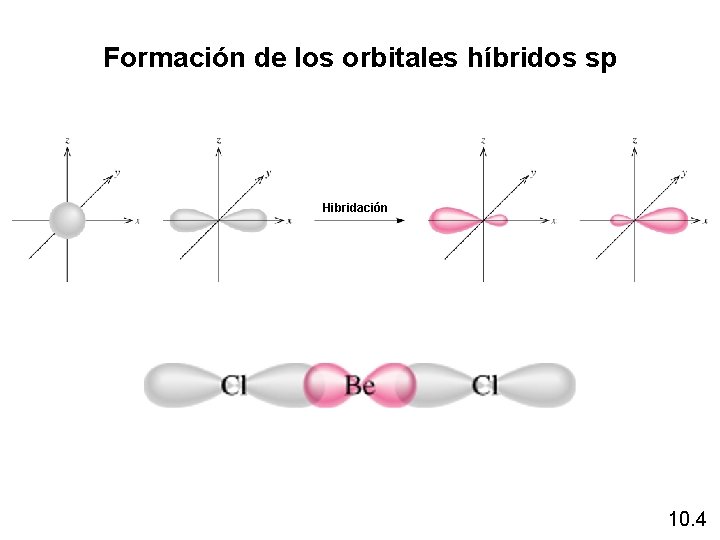
Formación de los orbitales híbridos sp sp Hibridación 10. 4
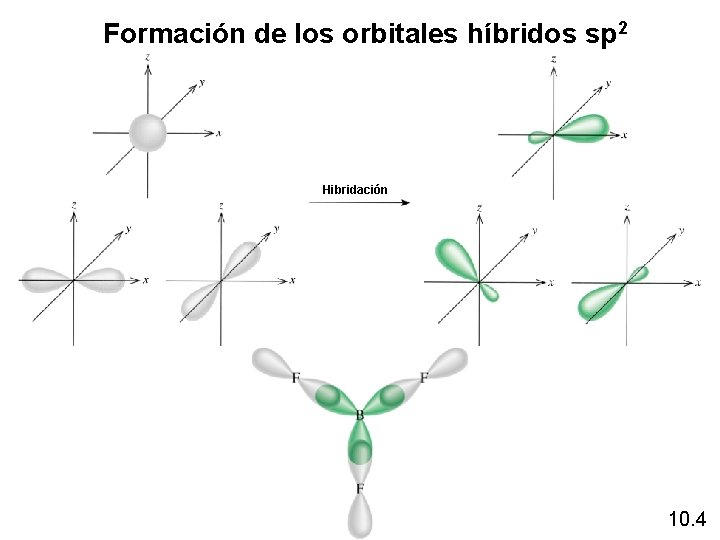
Formaciónde delos orbitales híbridos sp 2 Formación orbitales híbridos Hibridación 10. 4

¿Cómo predecir la hibridación del átomo central? Cuente el número de pares libres Y el número de átomos enlazados al átomo central # de pares libres + # de átomos enlazados Hibridación Ejemplos 2 sp Be. Cl 2 3 sp 2 BF 3 4 sp 3 CH 4, NH 3, H 2 O 5 sp 3 d PCl 5 6 sp 3 d 2 SF 6 10. 4
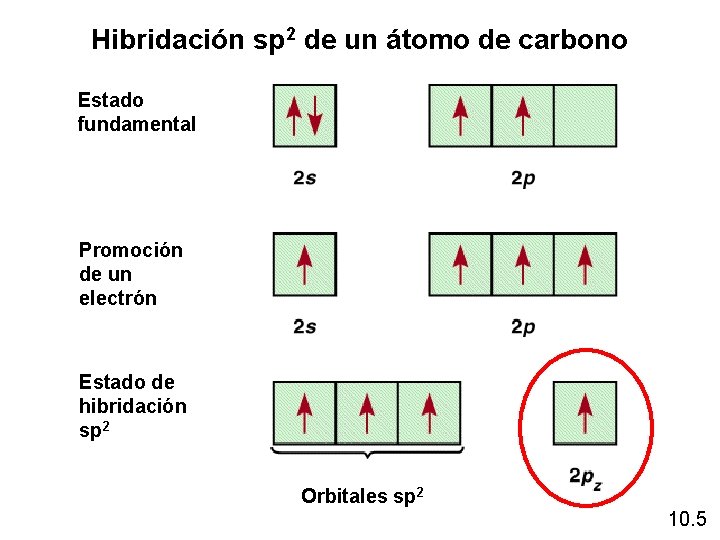
Hibridación sp 2 de un átomo de carbono Estado fundamental Promoción de un electrón Estado de hibridación sp 2 Orbitales sp 2 10. 5
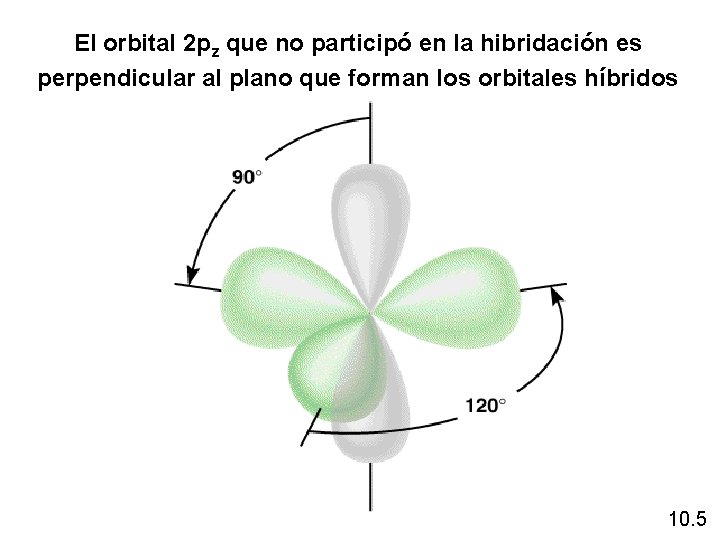
El orbital 2 pz que no participó en la hibridación es perpendicular al plano que forman los orbitales híbridos 10. 5
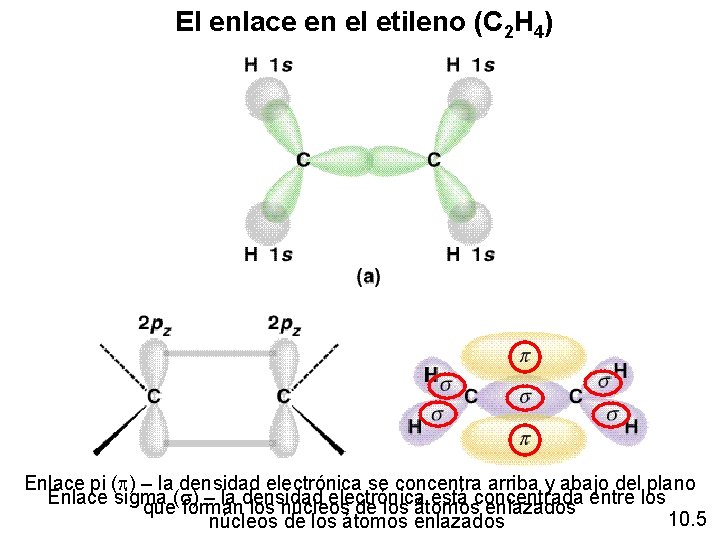
El enlace en el etileno (C 2 H 4) Enlace pi (p) – la densidad electrónica se concentra arriba y abajo del plano Enlace sigma (s) – la densidad electrónica está concentrada entre los que forman los núcleos de los átomos enlazados 10. 5 núcleos de los átomos enlazados
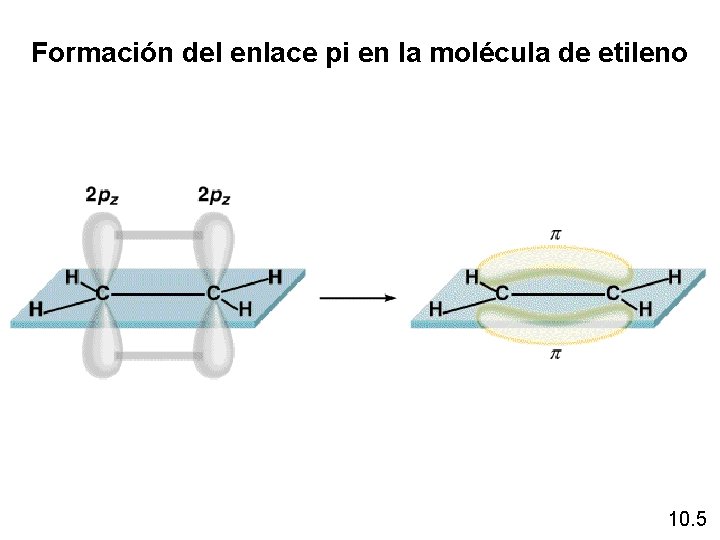
Formación del enlace pi en la molécula de etileno 10. 5
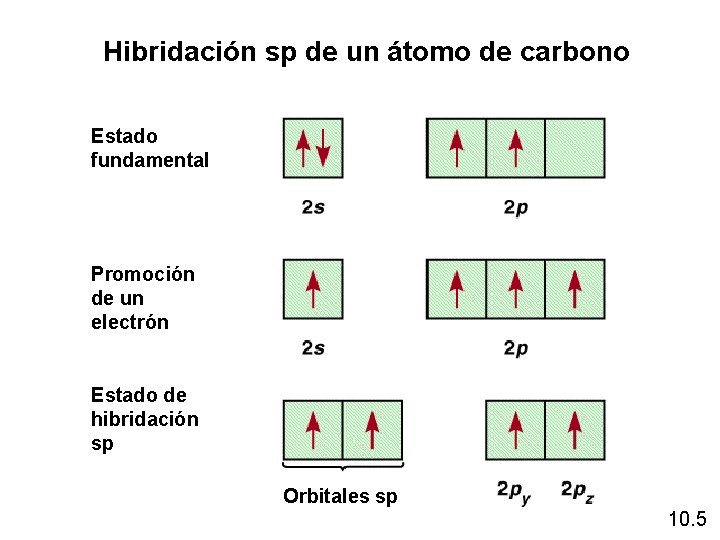
Hibridación sp de un átomo de carbono Estado fundamental Promoción de un electrón Estado de hibridación sp Orbitales sp 10. 5
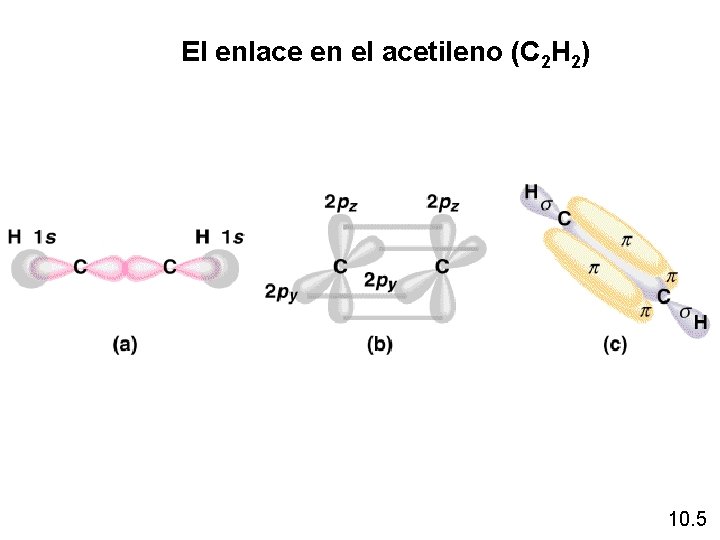
El enlace en el acetileno (C 2 H 2) 10. 5
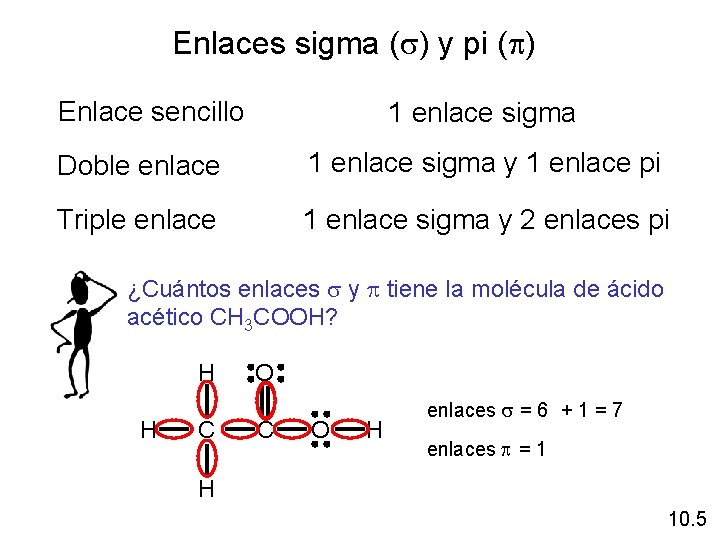
Enlaces sigma (s) y pi (p) Enlace sencillo 1 enlace sigma Doble enlace 1 enlace sigma y 1 enlace pi Triple enlace 1 enlace sigma y 2 enlaces pi ¿Cuántos enlaces s y p tiene la molécula de ácido acético CH 3 COOH? H C O H enlaces s = 6 + 1 = 7 enlaces p = 1 H 10. 5
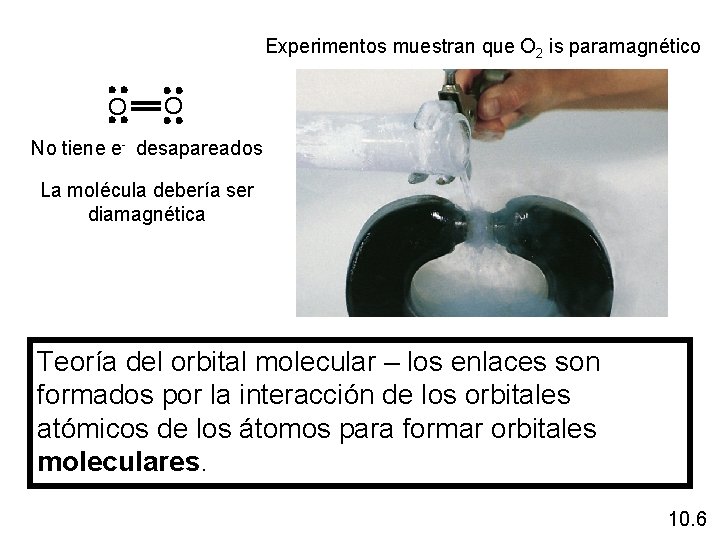
Experimentos muestran que O 2 is paramagnético O O No tiene e- desapareados La molécula debería ser diamagnética Teoría del orbital molecular – los enlaces son formados por la interacción de los orbitales atómicos de los átomos para formar orbitales moleculares. 10. 6
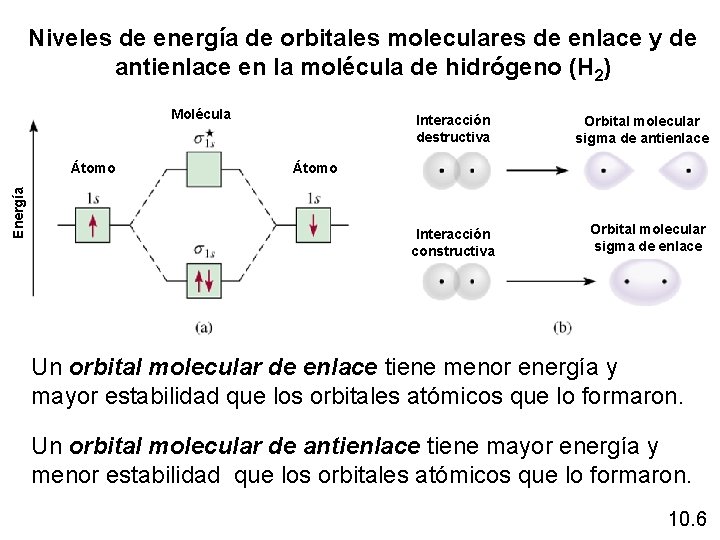
Niveles de energía de orbitales moleculares de enlace y de antienlace en la molécula de hidrógeno (H 2) Molécula Energía Átomo Interacción destructiva Orbital molecular sigma de antienlace Átomo Interacción constructiva Orbital molecular sigma de enlace Un orbital molecular de enlace tiene menor energía y mayor estabilidad que los orbitales atómicos que lo formaron. Un orbital molecular de antienlace tiene mayor energía y menor estabilidad que los orbitales atómicos que lo formaron. 10. 6
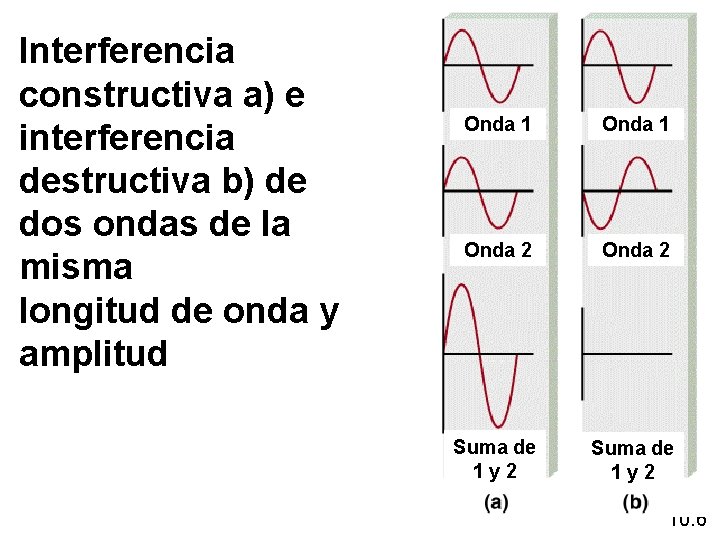
Interferencia constructiva a) e interferencia destructiva b) de dos ondas de la misma longitud de onda y amplitud Onda 1 Onda 2 Suma de 1 y 2 10. 6
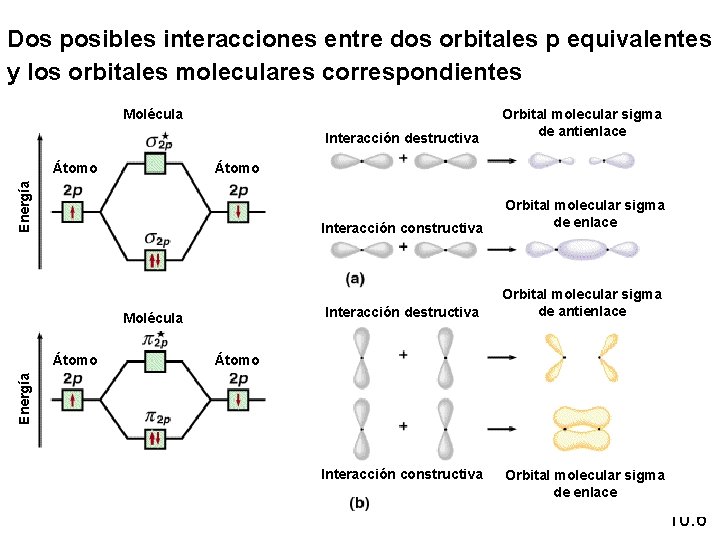
Dos posibles interacciones entre dos orbitales p equivalentes y los orbitales moleculares correspondientes Molécula Interacción destructiva Átomo Energía Átomo Molécula Interacción constructiva Orbital molecular sigma de enlace Interacción destructiva Orbital molecular sigma de antienlace Átomo Energía Átomo Orbital molecular sigma de antienlace Interacción constructiva Orbital molecular sigma de enlace 10. 6

Configuraciones de orbitales moleculares 1. El número de orbitales moleculares que se forman siempre es igual al número de orbitales atómicos que se combinan. 2. Cuanto más estable es el orbital molecular de enlace, menos estable será el orbital molecular de antienlace correspondiente. 3. El llenado de los orbitales moleculares procede de menor a mayor energía. 4. Al igual que un orbital atómico, cada orbital molecular puede aceptar dos electrones con espín opuesto, de acuerdo con el Principio de exclusión de Pauli. 5. Cuando se agregan electrones a orbitales moleculares con la misma energía, la regla de Hund predice la distribución más estable; es decir, los electrones ocupan estos orbitales moleculares con espines paralelos. 6. El número de electrones en los orbitales moleculares es igual a la suma de todos los electrones de los átomos que se enlazan. 10. 7
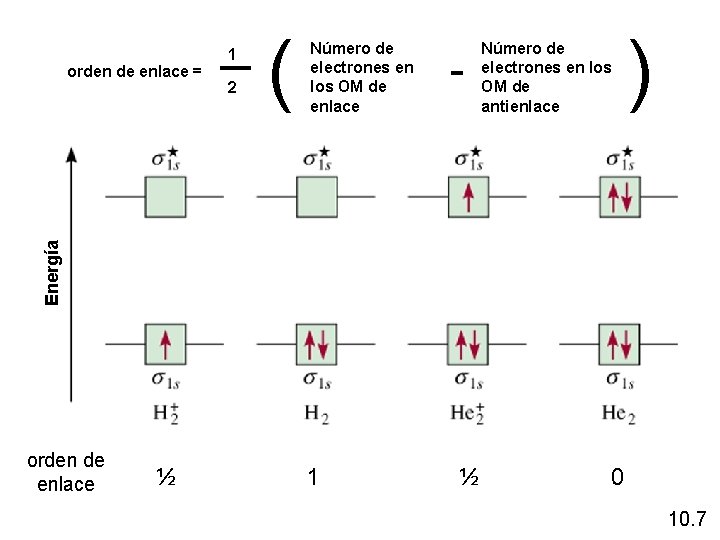
2 ( Número de electrones en los OM de enlace - Número de electrones en los OM de antienlace ) Energía orden de enlace = 1 orden de enlace ½ 1 ½ 0 10. 7
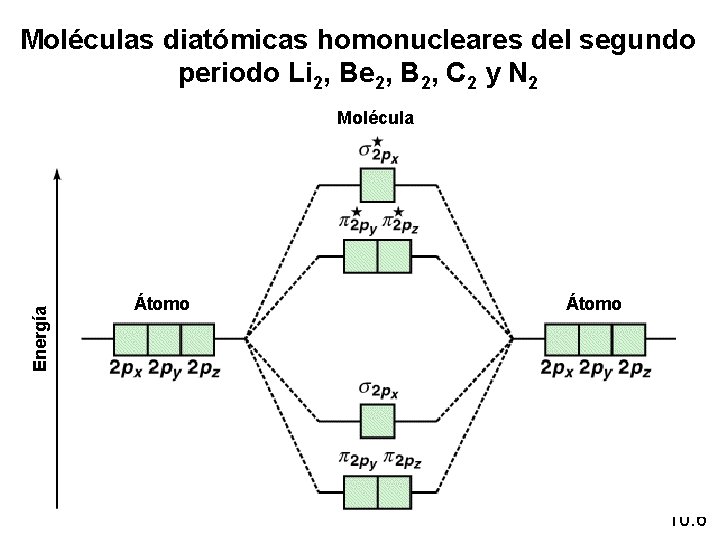
Moléculas diatómicas homonucleares del segundo periodo Li 2, Be 2, B 2, C 2 y N 2 Energía Molécula Átomo 10. 6
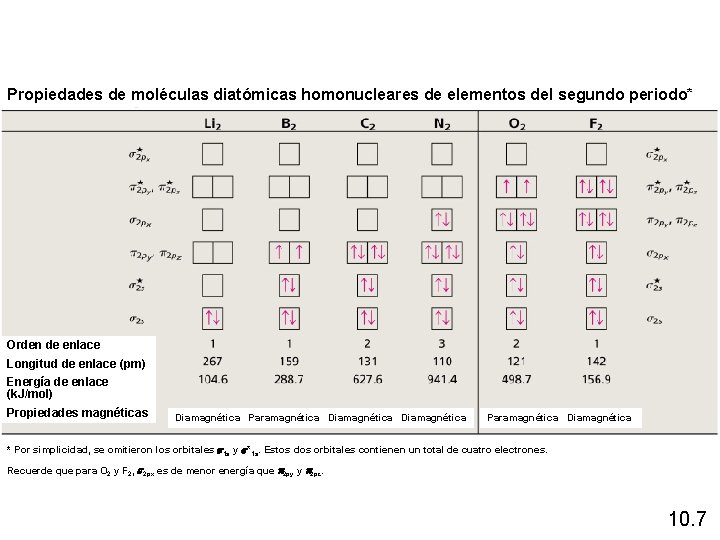
Propiedades de moléculas diatómicas homonucleares de elementos del segundo periodo* Orden de enlace Longitud de enlace (pm) Energía de enlace (k. J/mol) Propiedades magnéticas Diamagnética Paramagnética Diamagnética * Por simplicidad, se omitieron los orbitales s 1 s y s*1 s. Estos dos orbitales contienen un total de cuatro electrones. Recuerde que para O 2 y F 2, s 2 px es de menor energía que p 2 py y p 2 pz. 10. 7
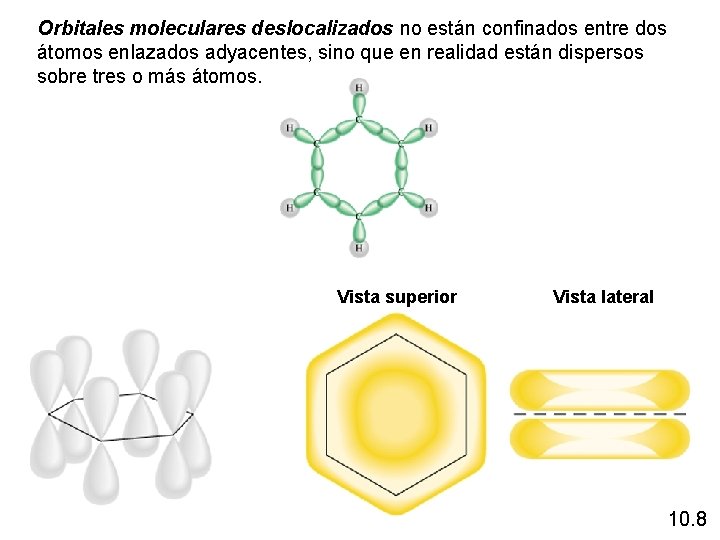
Orbitales moleculares deslocalizados no están confinados entre dos átomos enlazados adyacentes, sino que en realidad están dispersos sobre tres o más átomos. Vista superior Vista lateral 10. 8
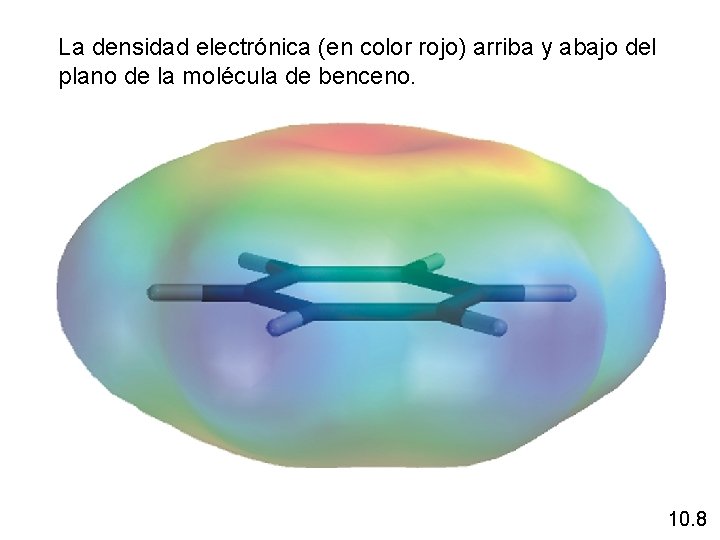
La densidad electrónica (en color rojo) arriba y abajo del plano de la molécula de benceno. 10. 8
- Slides: 54