Themenschwerpunkte 1 TherapieStart 2 Antiretrovirale Therapie 3 BegleiterkrankungenKomplikationen


Themenschwerpunkte 1. Therapie-Start 2. Antiretrovirale Therapie 3. Begleiterkrankungen/Komplikationen 4. Prävention 5. Neue Substanzen www. hivandmore. de

1. Therapiestart und -strategien 1. 1. When to start - Hintergrund: Neaton; MOSY 202 und Robbins; WEPEB 080 1. 1. 1. SMART/ACTG 384: Emery; WEPEB 018, Robbins; WEPEB 080 1. 1. 2. ATHENA: van Sighem et al. ; WEPEB 016 1. 1. 3. HOPS: Lichtenstein, MOPEB 016 1. 1. 4. INSIGHT (Startdesign): Neaton; MOSY 202 1. 2. SMART: weitere Ergebnisse www. hivandmore. de

When to Start § Warum früher anfangen? § In Kohortenstudien Hinweis auf erhöhtes Risiko von AIDS/Tod auch im CD 4 Stratum 350 -500/µl (UKCHIC, CASCADE) § Erhöhtes Risiko von schwerwiegenden Non-AIDS Ereignissen auch in hohen CD 4 Strata § Reduktion des Transmissionsrisikos § Bessere Verträglichkeit und Convenience aktueller Therapieregime § ACTG 384: Normalisierung der CD 4/CD 8 Ratio nur bei Therapiestart >350/µl mod. nach Neaton; MOSY 202 und Robbins; WEPEB 080; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Klinische Ereignisse bei verzögertem Therapiebeginn (CD 4<250/µl) § Subanalyse der SMART Studie § Einschlusskriterium: Patienten ART-naiv (n=251) oder ART -Pause >6 Monate (n=227) bei Baseline § Endpunkte: Opportunistische Infektionen, schwerwiegende Non-AIDS Ereignisse, Tod mod. nach Emery; WEPEB 018; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
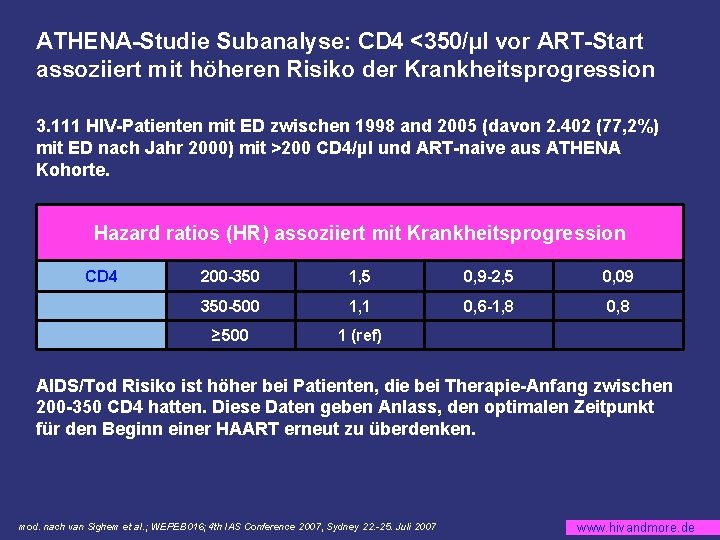
ATHENA-Studie Subanalyse: CD 4 <350/µl vor ART-Start assoziiert mit höheren Risiko der Krankheitsprogression 3. 111 HIV-Patienten mit ED zwischen 1998 and 2005 (davon 2. 402 (77, 2%) mit ED nach Jahr 2000) mit >200 CD 4/µl und ART-naive aus ATHENA Kohorte. Hazard ratios (HR) assoziiert mit Krankheitsprogression CD 4 200 -350 1, 5 0, 9 -2, 5 0, 09 350 -500 1, 1 0, 6 -1, 8 0, 8 ≥ 500 1 (ref) AIDS/Tod Risiko ist höher bei Patienten, die bei Therapie-Anfang zwischen 200 -350 CD 4 hatten. Diese Daten geben Anlass, den optimalen Zeitpunkt für den Beginn einer HAART erneut zu überdenken. mod. nach van Sighem et al. ; WEPEB 016; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
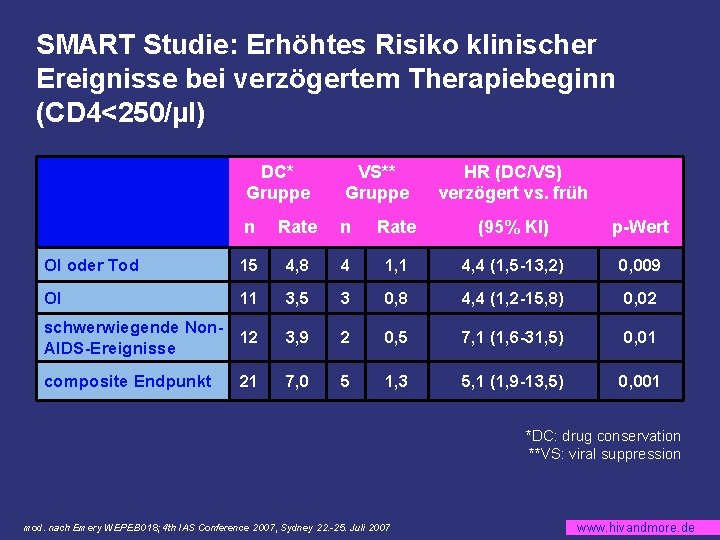
SMART Studie: Erhöhtes Risiko klinischer Ereignisse bei verzögertem Therapiebeginn (CD 4<250/µl) DC* Gruppe VS** Gruppe n Rate (95% KI) p-Wert OI oder Tod 15 4, 8 4 1, 1 4, 4 (1, 5 -13, 2) 0, 009 OI 11 3, 5 3 0, 8 4, 4 (1, 2 -15, 8) 0, 02 schwerwiegende Non 12 AIDS-Ereignisse 3, 9 2 0, 5 7, 1 (1, 6 -31, 5) 0, 01 composite Endpunkt 7, 0 5 1, 3 5, 1 (1, 9 -13, 5) 0, 001 21 HR (DC/VS) verzögert vs. früh *DC: drug conservation **VS: viral suppression mod. nach Emery WEPEB 018; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

. . . mehr Evidenz für den früheren Therapiestart § Aktivierung des Gerinnungssystems (D-Dimere) mit viraler Replikation und erhöhter AIDS- und Non-AIDS-Ereignisrate assoziiert (SMART-Substudie 1) § Weniger Nuke-Toxizität bei Therapiestart mit höherer CD 4 -Zellzahl 2 mod. nach. 1 Neaton, MOSY 202 und 2 Lichtenstein, MOPEB 016; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Rationale für eine randomisierte Studie zum Therapiestart § Non-AIDS Endpunkte in weniger als 30% der großen Kohorten erfasst 1 § Nicht messbarer Bias und Confounder in Kohorten § Unvollständige Erfassung und Verifikation der Endpunkte durch passives Follow-Up in Kohorten § Laufende randomisierte Studien erfassen meist keine Non-AIDS Endpunkte 1 Ledergerber, INSIGHT-DAIDS Workshop, July 2007 mod. nach Neaton; MOSY 202; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Brauchen wir eine prospektive randomisierte Studie zum Therapiestart? HIV-infizierte Patienten CD 4 -Zellzahl >500/µl Frühe ART-Gruppe Verzögerte ART-Gruppe sofortiger ART-Start ART erst bei CD 4 -Zellzahl <350/µl oder Symptomatik n=600 für initiale Studienphase n=1. 500 (ca. ) für Hauptstudie Studienbeginn 2008 Multinationale Studie (auch Deutschland) INSIGHT Study Team, Copenhagen mod. nach. Neaton; Mo. Sy 202; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Weitere Ergebnisse der SMART-Studie § Pneumonie: Erhöhtes Risiko in DC Arm (drug conservation) vs. VS Arm (viral suppression)1 § HIV koinfizierte Patienten (HBV u. /o. HCV) haben eine erhöhte Sterblichkeit durch non-OIs in DC Arm (drug conservation) vs. nicht koinfizierte HIV Patienten 2 mod. nach. 1 Gordin et al. , MOPEP 100 und 2 Tedaldi et al. , TUAB 20; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

2. Klinische Studien 2. 1. PREDICT-1: 2. 2. SHARE: 2. 3. BICOMBO: 2. 4. TITAN: 2. 5. ALERT: 2. 6. BOLD 100: 2. 7. Blips: Mallal et al. ; WESS 101 Elion et al. ; WEPE 033 Martinez et al. ; WESS 102 Valdez-Madruga et al. ; TUAB 101 Smith et al. ; WEPEB 023 Blick et al. ; WEPEB 040 Garcia-Gasco et al. ; WEPEB 083 www. hivandmore. de
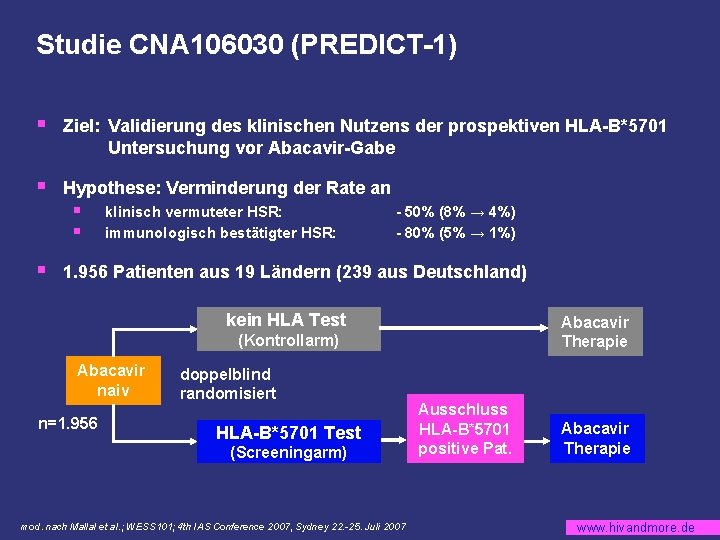
Studie CNA 106030 (PREDICT-1) § Ziel: Validierung des klinischen Nutzens der prospektiven HLA-B*5701 Untersuchung vor Abacavir-Gabe § Hypothese: Verminderung der Rate an § § § klinisch vermuteter HSR: immunologisch bestätigter HSR: - 50% (8% → 4%) - 80% (5% → 1%) 1. 956 Patienten aus 19 Ländern (239 aus Deutschland) kein HLA Test Abacavir Therapie (Kontrollarm) Abacavir naiv n=1. 956 doppelblind randomisiert HLA-B*5701 Test (Screeningarm) mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 Ausschluss HLA-B*5701 positive Pat. Abacavir Therapie www. hivandmore. de

Co-primäre Endpunkte § Inzidenz klinisch vermuteter Abacavir HSR (90% Power) § Inzidenz immunologisch bestätigter (klinische Diagnose plus positiver epikutaner Patch-Test) Abacavir HSR (>90% Power) Im Falle eines signifikanten Unterschieds für die co-primären Endpunkte zwischen den Armen wird davon ausgegangen, dass die Studie definitiv den klinischen Nutzen des HLA-B*5701 Screenings als Maßnahme zur Identifizierung von Patienten mit erhöhtem HSR Risiko belegt. mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
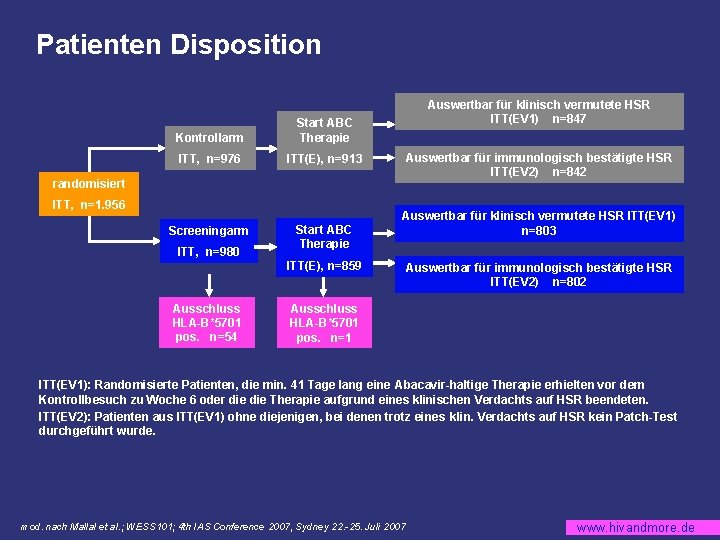
Patienten Disposition Kontrollarm Start ABC Therapie ITT, n=976 ITT(E), n=913 Screeningarm Start ABC Therapie Auswertbar für klinisch vermutete HSR ITT(EV 1) n=847 Auswertbar für immunologisch bestätigte HSR ITT(EV 2) n=842 randomisiert ITT, n=1. 956 ITT, n=980 Auswertbar für klinisch vermutete HSR ITT(EV 1) n=803 ITT(E), n=859 Ausschluss HLA-B*5701 pos. n=54 Auswertbar für immunologisch bestätigte HSR ITT(EV 2) n=802 Ausschluss HLA-B*5701 pos. n=1 ITT(EV 1): Randomisierte Patienten, die min. 41 Tage lang eine Abacavir-haltige Therapie erhielten vor dem Kontrollbesuch zu Woche 6 oder die Therapie aufgrund eines klinischen Verdachts auf HSR beendeten. ITT(EV 2): Patienten aus ITT(EV 1) ohne diejenigen, bei denen trotz eines klin. Verdachts auf HSR kein Patch-Test durchgeführt wurde. mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
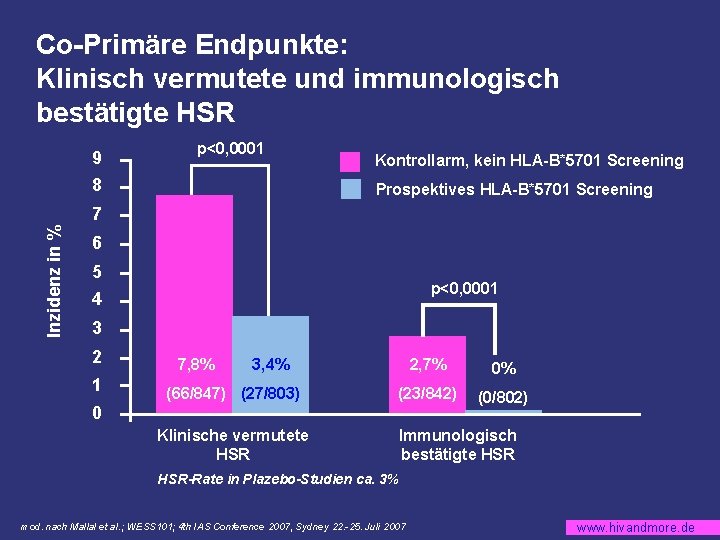
Co-Primäre Endpunkte: Klinisch vermutete und immunologisch bestätigte HSR 9 p<0, 0001 8 Kontrollarm, kein HLA-B*5701 Screening Prospektives HLA-B*5701 Screening Inzidenz in % 7 6 5 p<0, 0001 4 3 2 1 7, 8% 2, 7% 0% (23/842) (0/802) 3, 4% (66/847) (27/803) 0 Klinische vermutete HSR Immunologisch bestätigte HSR-Rate in Plazebo-Studien ca. 3% mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Co-Primäre Endpunkte: Immunologisch bestätigte HSR Multivariate Analyse Odds Ratio (95% KI) p-Wert Prospektive Testung vs. Kontrolle 0, 03 (0, 00 -0, 18) p<0, 000001 Kaukasisch vs. nicht-kaukasisch 4, 21 (0, 67 -175, 5) p=0, 1139 ART naiv vs. vorbehandelt 1, 20 (0, 31 -3, 82) p=0, 6637 Start neuer NNRTI (ja vs. nein) 1, 45 (0, 22 -6, 49) p=0, 5693 Gleichzeitige PI Tx (ja vs. nein) 1, 05 (0, 39 -2, 79) p=0, 9123 mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
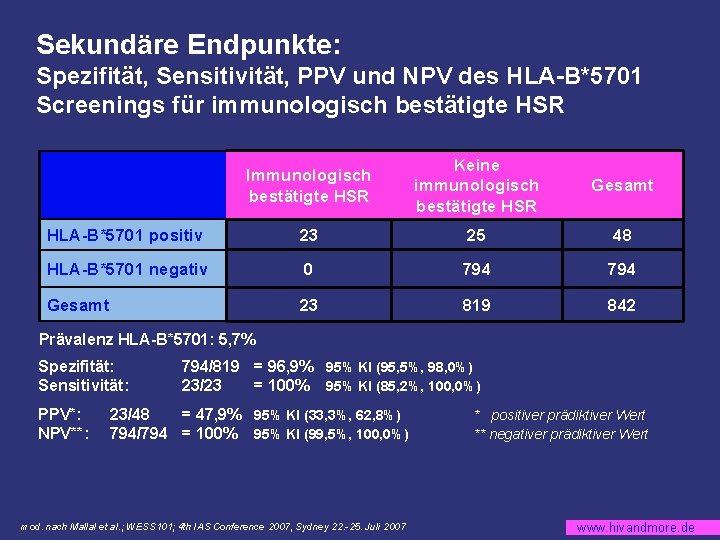
Sekundäre Endpunkte: Spezifität, Sensitivität, PPV und NPV des HLA-B*5701 Screenings für immunologisch bestätigte HSR Immunologisch bestätigte HSR Keine immunologisch bestätigte HSR Gesamt HLA-B*5701 positiv 23 25 48 HLA-B*5701 negativ 0 794 Gesamt 23 819 842 Prävalenz HLA-B*5701: 5, 7% Spezifität: Sensitivität: PPV*: NPV**: 794/819 = 96, 9% 95% KI (95, 5%, 98, 0%) 23/23 = 100% 95% KI (85, 2%, 100, 0%) 23/48 = 47, 9% 95% KI (33, 3%, 62, 8%) 794/794 = 100% 95% KI (99, 5%, 100, 0%) mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 * positiver prädiktiver Wert ** negativer prädiktiver Wert www. hivandmore. de
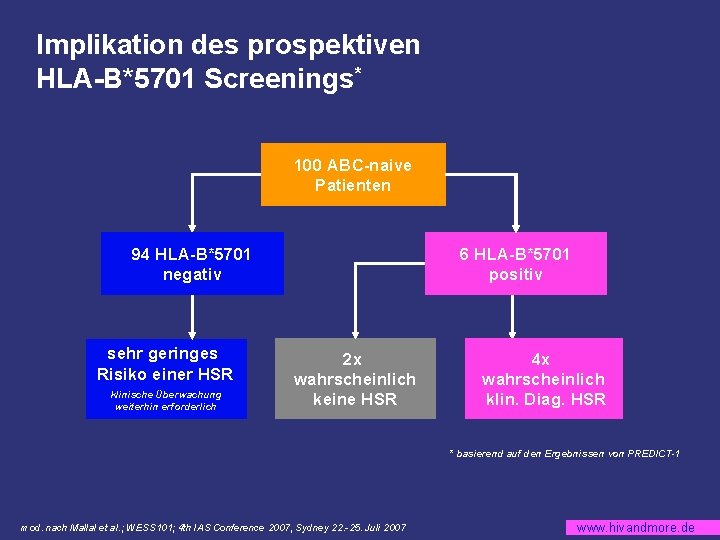
Implikation des prospektiven HLA-B*5701 Screenings* 100 ABC-naive Patienten 94 HLA-B*5701 negativ sehr geringes Risiko einer HSR klinische Überwachung weiterhin erforderlich 6 HLA-B*5701 positiv 2 x wahrscheinlich keine HSR 4 x wahrscheinlich klin. Diag. HSR * basierend auf den Ergebnissen von PREDICT-1 mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Schlussfolgerungen und Implikationen I § In PREDICT-1 resultierte prospektives HLA-B*5701 Screening in einer signifikanten Reduktion des Risikos einer klinisch vermuteten HSR § HLA-B*5701 Screening in PREDICT-1 eliminierte vollständig das Risiko einer im Patch-Test bestätigten HSR § Angesichts dieser Ergebnisse empfiehlt GSK, dass alle ABC-naiven Patienten auf HLA-B*5701 untersucht werden, sofern dazu die Möglichkeit besteht mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Schlussfolgerungen und Implikationen II § Wenn ein HLA-B*5701 Screening nicht möglich ist, können Ärzte weiterhin eine ABC-Therapie unter angemessener klinischer Überwachung initiieren § HLA-B*5701 positive Patienten haben ein hohes Risiko eine ABC HSR zu entwickeln; GSK empfiehlt, dass diese Patienten kein ABC einnehmen sollten § GSK weist weiterhin auf die Notwendigkeit angemessener klinischer Vigilanz im Rahmen der HIV-Behandlung hin, unabhängig von unterstützenden diagnostischen Verfahren mod. nach Mallal et al. ; WESS 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
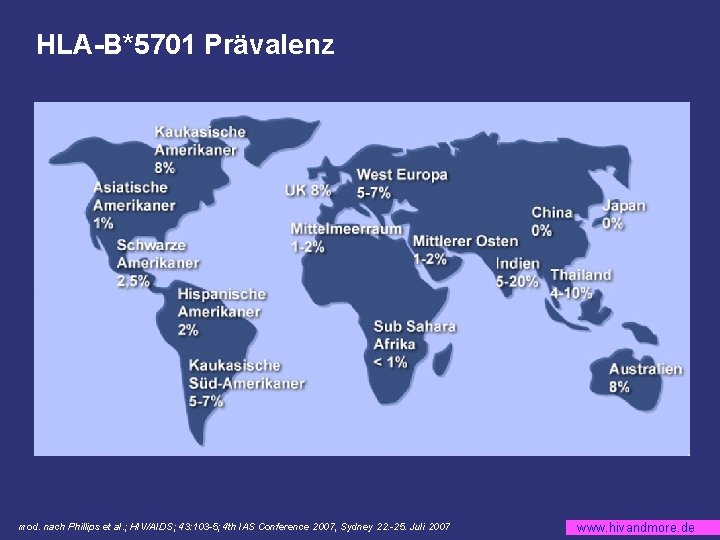
HLA-B*5701 Prävalenz mod. nach Phillips et al. ; HIV/AIDS; 43: 103 -5; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
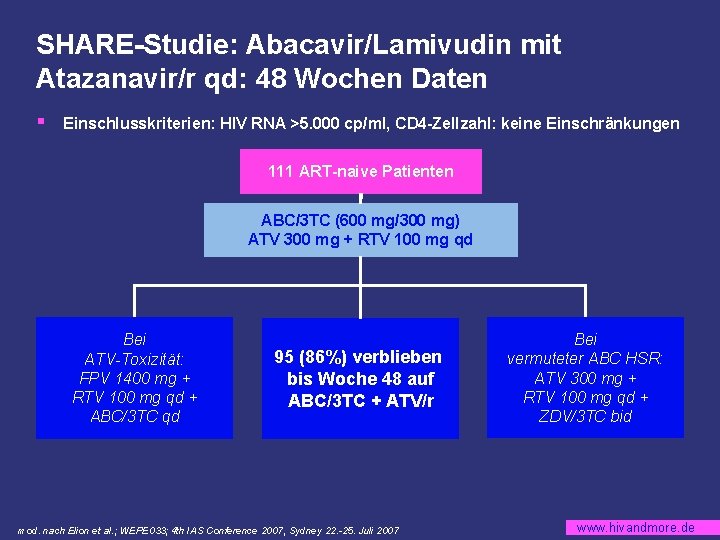
SHARE-Studie: Abacavir/Lamivudin mit Atazanavir/r qd: 48 Wochen Daten § Einschlusskriterien: HIV RNA >5. 000 cp/ml, CD 4 -Zellzahl: keine Einschränkungen 111 ART-naive Patienten ABC/3 TC (600 mg/300 mg) ATV 300 mg + RTV 100 mg qd Bei ATV-Toxizität: FPV 1400 mg + RTV 100 mg qd + ABC/3 TC qd 95 (86%) verblieben bis Woche 48 auf ABC/3 TC + ATV/r mod. nach Elion et al. ; WEPE 033; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 Bei vermuteter ABC HSR: ATV 300 mg + RTV 100 mg qd + ZDV/3 TC bid www. hivandmore. de
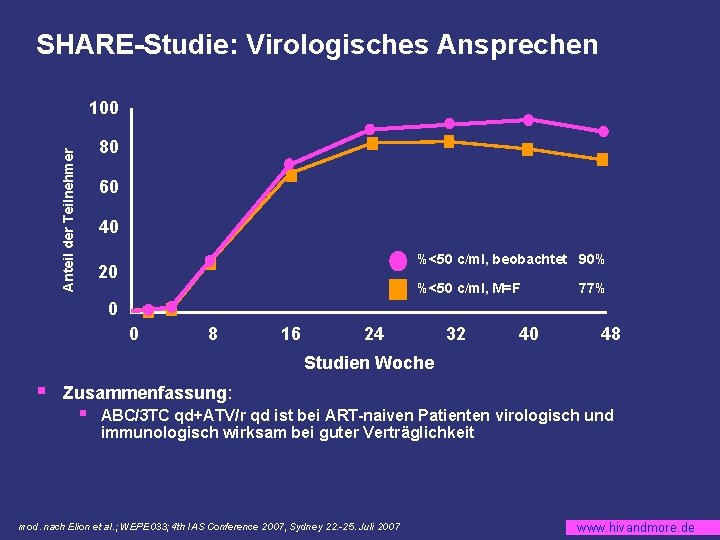
SHARE-Studie: Virologisches Ansprechen 100 Anteil der Teilnehmer 80 60 40 %<50 c/ml, beobachtet 90% 20 %<50 c/ml, M=F 77% 0 0 8 16 24 32 40 48 Studien Woche § Zusammenfassung: § ABC/3 TC qd+ATV/r qd ist bei ART-naiven Patienten virologisch und immunologisch wirksam bei guter Verträglichkeit mod. nach Elion et al. ; WEPE 033; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

BICOMBO: Umstellung virologisch stabiler Patienten auf ABC/3 TC bzw. TDF/FTC • Stabile 3 TC-haltige HAART (<50 cp/ml für >6 Monate) • 96 Wochen, geplante 48 Wochen Analyse • 18% 1 st Line, 82% ≥ 2 nd Line n=166 § § n=167 Umstellung auf ABC/3 TC Umstellung auf TDF/FTC 7% zu Baseline auf ABC/3 TC 34% zu Baseline auf TDF/3 TC Primärer Endpunkt: Therapieversagen Sekundäre Endpunkte (u. a. ): virologisches Versag immunologisches Ansprechen mod. nach Martinez et al. ; WESS 102; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
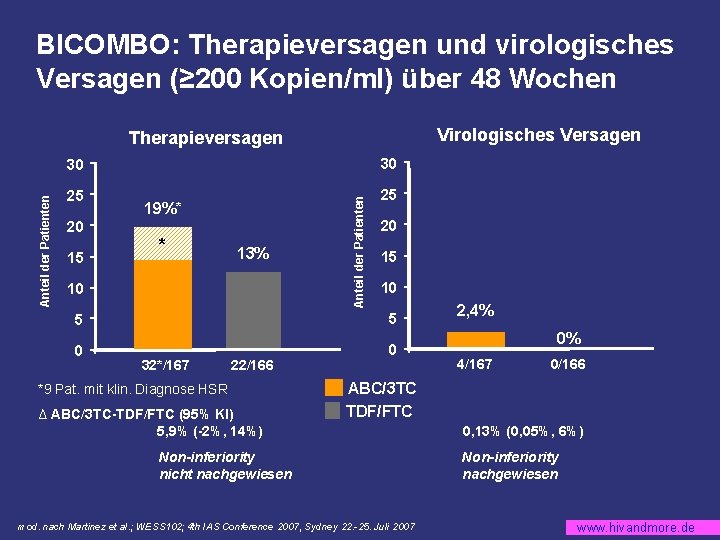
BICOMBO: Therapieversagen und virologisches Versagen (≥ 200 Kopien/ml) über 48 Wochen Virologisches Versagen 30 30 25 25 19%* 20 15 * 13% 10 Anteil der Patienten Therapieversagen 20 15 10 5 5 0 0 32*/167 22/166 *9 Pat. mit klin. Diagnose HSR ∆ ABC/3 TC-TDF/FTC (95% KI) 5, 9% (-2%, 14%) 2, 4% 0% 4/167 0/166 ABC/3 TC TDF/FTC Non-inferiority nicht nachgewiesen mod. nach Martinez et al. ; WESS 102; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 0, 13% (0, 05%, 6%) Non-inferiority nachgewiesen www. hivandmore. de
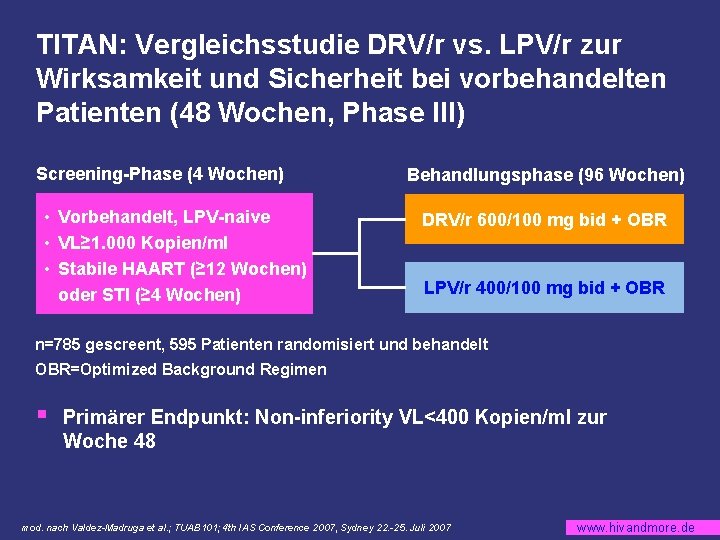
TITAN: Vergleichsstudie DRV/r vs. LPV/r zur Wirksamkeit und Sicherheit bei vorbehandelten Patienten (48 Wochen, Phase III) Screening-Phase (4 Wochen) • Vorbehandelt, LPV-naive • VL≥ 1. 000 Kopien/ml • Stabile HAART (≥ 12 Wochen) oder STI (≥ 4 Wochen) Behandlungsphase (96 Wochen) DRV/r 600/100 mg bid + OBR LPV/r 400/100 mg bid + OBR n=785 gescreent, 595 Patienten randomisiert und behandelt OBR=Optimized Background Regimen § Primärer Endpunkt: Non-inferiority VL<400 Kopien/ml zur Woche 48 mod. nach Valdez-Madruga et al. ; TUAB 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
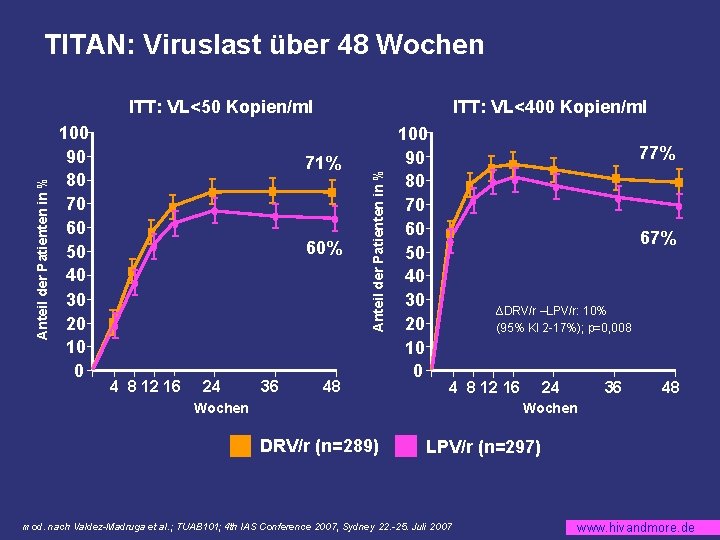
TITAN: Viruslast über 48 Wochen 100 90 80 70 60 50 40 30 20 10 0 ITT: VL<400 Kopien/ml 71% 60% 4 8 12 16 24 36 Anteil der Patienten in % ITT: VL<50 Kopien/ml 48 100 90 80 70 60 50 40 30 20 10 0 77% 67% ∆DRV/r –LPV/r: 10% (95% KI 2 -17%); p=0, 008 4 8 12 16 Wochen 24 36 48 Wochen DRV/r (n=289) LPV/r (n=297) mod. nach Valdez-Madruga et al. ; TUAB 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
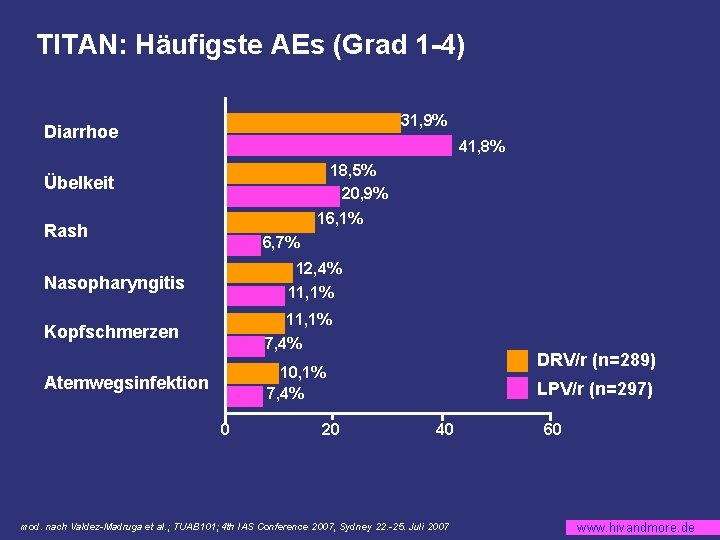
TITAN: Häufigste AEs (Grad 1 -4) 31, 9% Diarrhoe 41, 8% 18, 5% 20, 9% Übelkeit 16, 1% Rash 6, 7% 12, 4% Nasopharyngitis 11, 1% Kopfschmerzen 11, 1% 7, 4% Atemwegsinfektion 10, 1% 7, 4% 0 20 DRV/r (n=289) LPV/r (n=297) 40 mod. nach Valdez-Madruga et al. ; TUAB 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 60 www. hivandmore. de
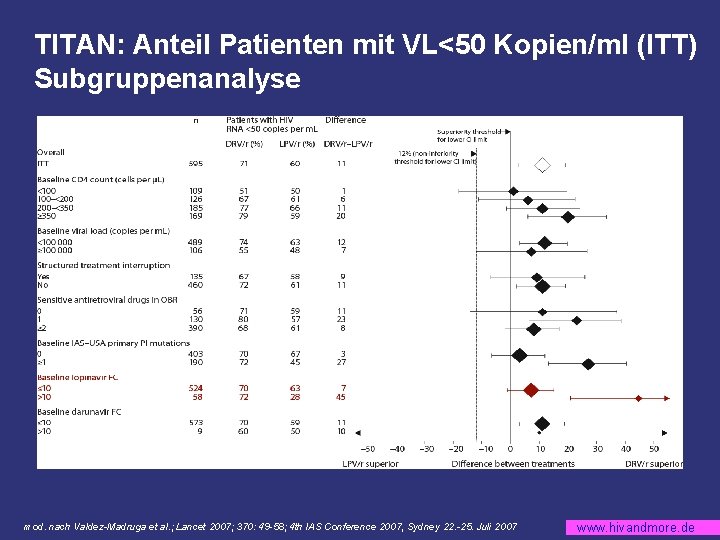
TITAN: Anteil Patienten mit VL<50 Kopien/ml (ITT) Subgruppenanalyse mod. nach Valdez-Madruga et al. ; Lancet 2007; 370: 49 -58; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

TITAN: Zusammenfassung Bei vorbehandelten HIV Patienten, LPV-naive: § DRV/r ist non-inferior und superior gegenüber LPV/r hinsichtlich des primären Endpunkts (VL<400 Kopien/ml zur Woche 48) § DRV/r: Gute Verträglichkeit und Sicherheit § Bei LPV/r Empfindlichkeit (FC<10) keine Überlegenheit von DRV/r Poster WEPEB 038 mod. nach Valdez-Madruga et al. ; TUAB 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
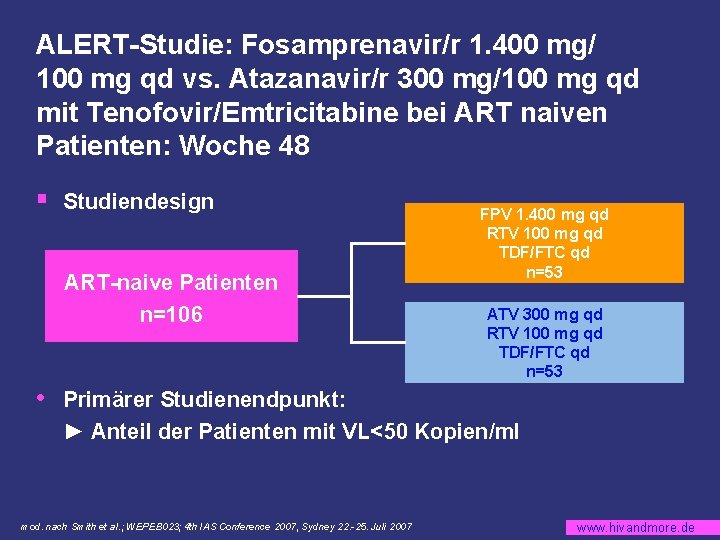
ALERT-Studie: Fosamprenavir/r 1. 400 mg/ 100 mg qd vs. Atazanavir/r 300 mg/100 mg qd mit Tenofovir/Emtricitabine bei ART naiven Patienten: Woche 48 § Studiendesign ART-naive Patienten n=106 • FPV 1. 400 mg qd RTV 100 mg qd TDF/FTC qd n=53 ATV 300 mg qd RTV 100 mg qd TDF/FTC qd n=53 Primärer Studienendpunkt: ► Anteil der Patienten mit VL<50 Kopien/ml mod. nach Smith et al. ; WEPEB 023; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
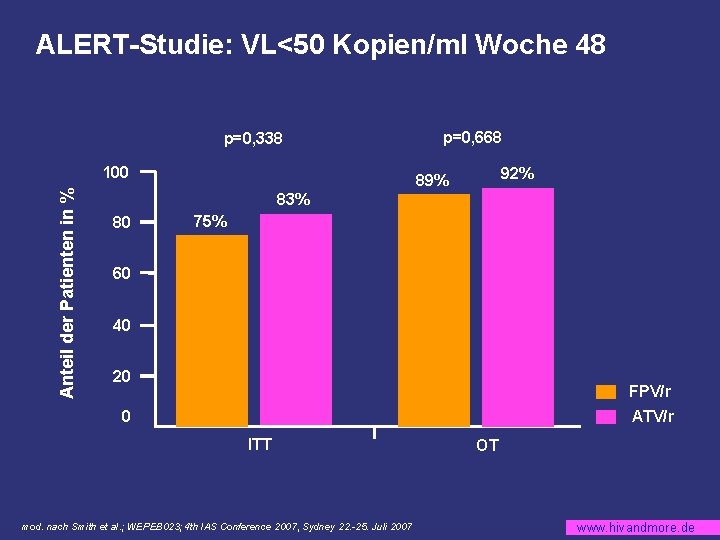
ALERT-Studie: VL<50 Kopien/ml Woche 48 p=0, 338 Anteil der Patienten in % 100 p=0, 668 92% 89% 83% 80 75% 60 40 20 FPV/r 0 ATV/r ITT mod. nach Smith et al. ; WEPEB 023; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 OT www. hivandmore. de
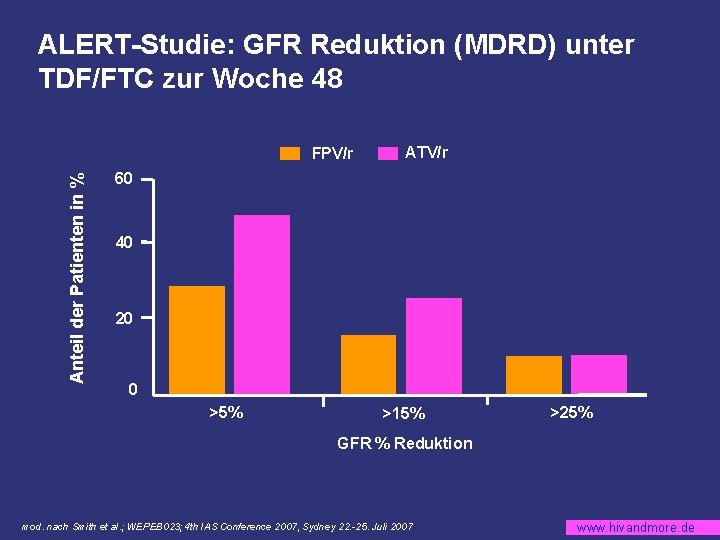
ALERT-Studie: GFR Reduktion (MDRD) unter TDF/FTC zur Woche 48 Anteil der Patienten in % FPV/r ATV/r 60 40 20 0 >5% >15% >25% GFR % Reduktion mod. nach Smith et al. ; WEPEB 023; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

ALERT-Studie: Zusammenfassung § FPV/r qd und ATV/r qd jeweils mit TDF/FTC zeigen vergleichbares virologisches und immunologisches Therapieansprechen § Lipidveränderungen waren vergleichbar § Engmaschige Kontrolle der GFR bei Kombination mit TDF/FTC empfohlen mod. nach Smith et al. ; WEPEB 023; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
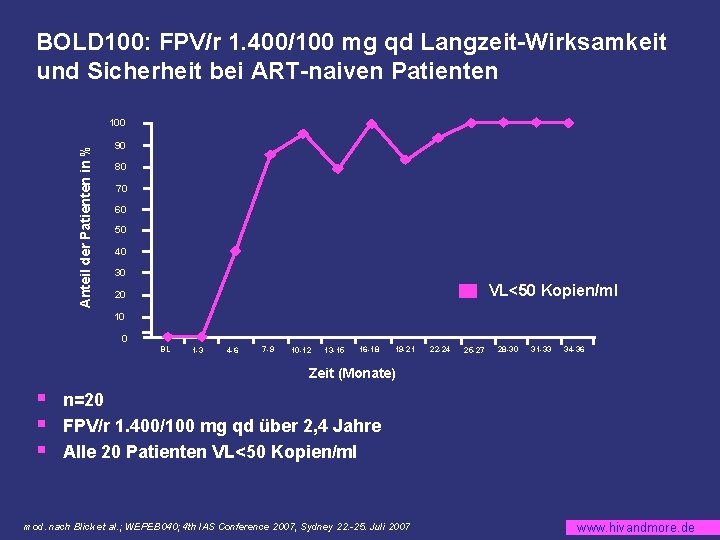
BOLD 100: FPV/r 1. 400/100 mg qd Langzeit-Wirksamkeit und Sicherheit bei ART-naiven Patienten Anteil der Patienten in % 100 90 80 70 60 50 40 30 VL<50 Kopien/ml 20 10 0 BL 1 -3 4 -6 7 -9 10 -12 13 -15 16 -18 19 -21 22 -24 25 -27 28 -30 31 -33 34 -36 Zeit (Monate) § § § n=20 FPV/r 1. 400/100 mg qd über 2, 4 Jahre Alle 20 Patienten VL<50 Kopien/ml mod. nach Blick et al. ; WEPEB 040; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Prävalenz, Prädiktoren und Outcome bei geringgradiger viraler Replikation § Spanische Kohorte (1999 -2006), retrospektive Auswertung aller Patienten mit Viruslast-Rebound bei niedriger VL (>50 -500 Kopien/ml) unter HAART § Follow-Up nach 12 Wochen § Virologisches Versagen definiert als VL >500 Kopien/ml in zwei konsekutiven Messungen mod. nach Garcia-Gasco et al. ; WEPEB 083; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Höhe des viralen Rebounds (51 -500 Kopien/ml) und Risiko des virologisches Versagens Virologisches Versagen (%) 20 18 16 14 12 10 8 6 4 2 0 Plasma HIV-RNA Anzahl an Patienten 51 -100 101 -300 301 -500 452 324 83 mod. nach Garcia-Gasco et al. ; WEPEB 083; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Prävalenz, Prädiktoren und Outcome bei geringgradiger viraler Replikation unter HAART § Niedrig virämische Rebounds waren in den meisten Fällen Blips (71%) und ohne prognostische Konsequenz § Beibehaltung der aktuellen HAART kam es bei 10% der Patienten zum virologischen Versagen § Ab einer Viruslast von über 120 Kopien/ml war virologisches Versagen signifikant häufiger mod. nach Garcia-Gasco et al. ; WEPEB 083; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

3. Begleiterkrankungen/Komplikationen 3. 1. HIV & Malignome: Grulich et al. ; MOPEB 080 3. 2. HIV & Leber: 3. 2. 1. Hep. B Impfung: Bortan et al. ; MOPEB 055 3. 2. 2. HEALTH: Valantin MA et al. ; MOPEB 062 3. 2. 3. RVR als Prädictor: Pagani et al; MOPEB 047 3. 3. NVP-HSR Risiko: Wit et al. ; MOPEB 008 3. 4. Lipide: Benett et al. ; TUPEB 075 und Klibanov et al. ; TUPEB 076 3. 5. EFV & Schwangerschaft: Joao et al. ; TUPEB 113 www. hivandmore. de

Metaanalyse: HIV-assoziierte Malignome Virus-assoziierte Malignome § Kohortenstudien: Krebsregister in Industrieländern § HIV-infizierte (7 Studien: n=444. 172, 1980 -2002) § Organtransplantatempfänger (5 Studien: n=31. 977, 1964 -2003) § Vergleich der Malignom-spezifischen standardisierten Inzidenzratio SIR (Malignominzidenz in der jeweiligen Risikogruppe bezogen auf die Inzidenz in der Normalbevölkerung) ► Malignominzidenz erhöht unabhängig von Ursache der Immunsuppression ► Erhöhte Inzidenz auch von nicht AIDS-definierenden Malignomen bei HIV-Infizierten mod. nach Grulich et al. ; MOPEB 080; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
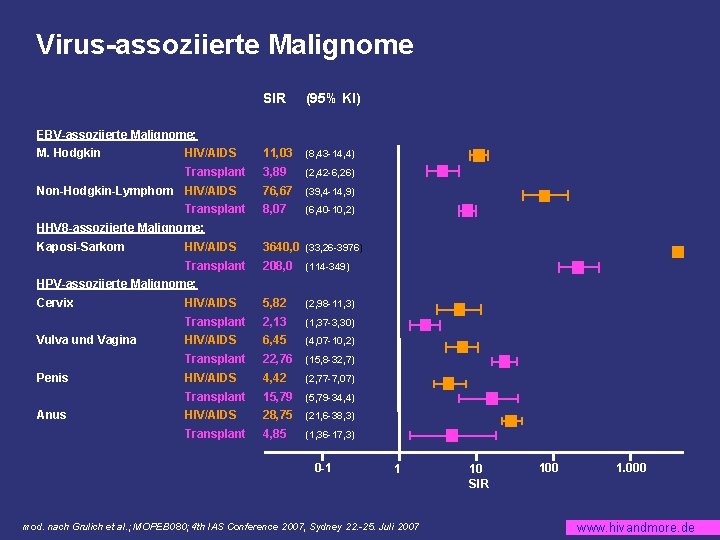
Virus-assoziierte Malignome SIR (95% KI) HIV/AIDS 11, 03 (8, 43 -14, 4) Transplant 3, 89 (2, 42 -6, 26) 76, 67 (39, 4 -14, 9) 8, 07 (6, 40 -10, 2) EBV-assoziierte Malignome: M. Hodgkin Non-Hodgkin-Lymphom HIV/AIDS Transplant HHV 8 -assoziierte Malignome: Kaposi-Sarkom HIV/AIDS 3640, 0 (33, 26 -3976) Transplant 208, 0 (114 -349) HIV/AIDS 5, 82 (2, 98 -11, 3) Transplant 2, 13 (1, 37 -3, 30) HIV/AIDS 6, 45 (4, 07 -10, 2) Transplant 22, 76 (15, 8 -32, 7) HIV/AIDS 4, 42 (2, 77 -7, 07) Transplant 15, 79 (5, 79 -34, 4) HIV/AIDS 28, 75 (21, 6 -38, 3) Transplant 4, 85 (1, 36 -17, 3) HPV-assoziierte Malignome: Cervix Vulva und Vagina Penis Anus 0 -1 1 mod. nach Grulich et al. ; MOPEB 080; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 10 SIR 100 1. 000 www. hivandmore. de
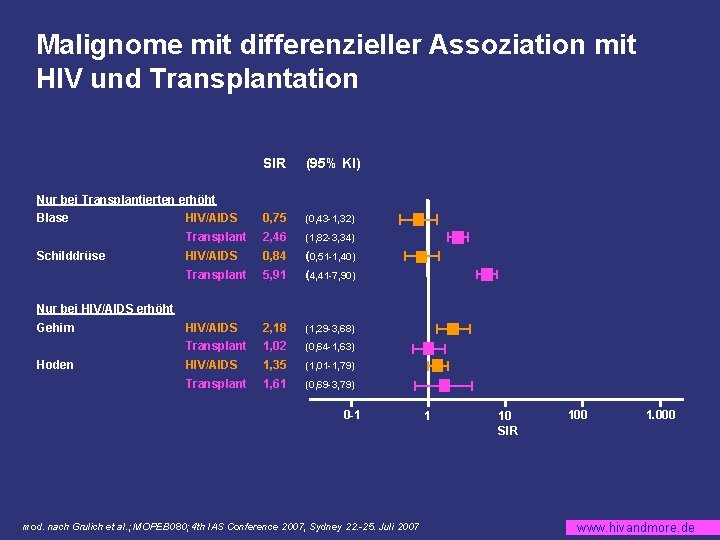
Malignome mit differenzieller Assoziation mit HIV und Transplantation SIR (95% KI) HIV/AIDS 0, 75 (0, 43 -1, 32) Transplant 2, 46 (1, 82 -3, 34) HIV/AIDS 0, 84 (0, 51 -1, 40) Transplant 5, 91 (4, 41 -7, 90) HIV/AIDS 2, 18 (1, 29 -3, 68) Transplant 1, 02 (0, 64 -1, 63) HIV/AIDS 1, 35 (1, 01 -1, 79) Transplant 1, 61 (0, 69 -3, 79) Nur bei Transplantierten erhöht Blase Schilddrüse Nur bei HIV/AIDS erhöht Gehirn Hoden 0 -1 mod. nach Grulich et al. ; MOPEB 080; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 1 10 SIR 100 1. 000 www. hivandmore. de

Effektivität der 40µg HBV Impfung (Hochdosis) bei HIV infizierten Patienten § Problem: Die Ansprechrate der HBV Impfung bei HIV Patienten ist signifikant geringer als bei HIV negativen Individuen. § Impfschemata: 0 – 1 – 6 Monate § Retrospektive Kohortenstudie § Primärer Endpunkt der Studie: positiver Anti-HBs-Titer (>10 IU/l) mod. nach Bortan et al. ; MOPEB 055; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
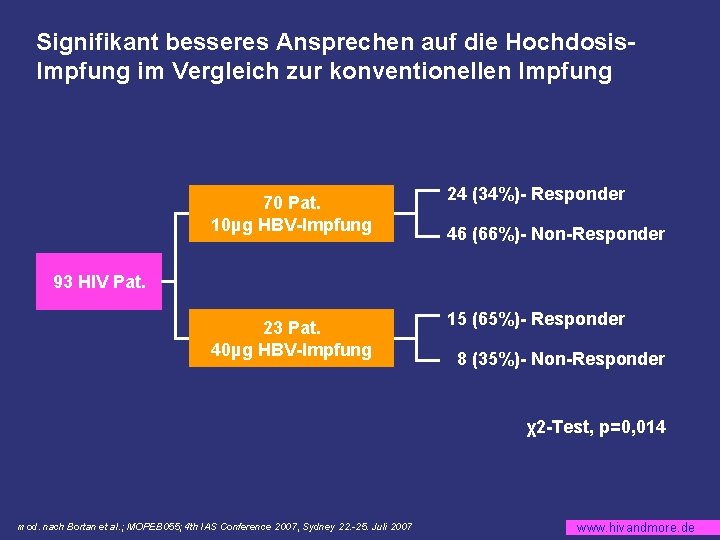
Signifikant besseres Ansprechen auf die Hochdosis. Impfung im Vergleich zur konventionellen Impfung 70 Pat. 10µg HBV-Impfung 24 (34%)- Responder 46 (66%)- Non-Responder 93 HIV Pat. 23 Pat. 40µg HBV-Impfung 15 (65%)- Responder 8 (35%)- Non-Responder χ2 -Test, p=0, 014 mod. nach Bortan et al. ; MOPEB 055; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Evaluation des Leberschadens bei vorbehandelten HIV Patienten mit chronisch erhöhten Transaminasen (HEALTH Studie) § 33 Patienten mit unklarer Transaminasenerhöhung § Medianes Alter 46 Jahre § Mediane Therapiedauer 118 Monate § Ausschlusskriterien: HBV, HCV, Autoimmunhepatitis, Alkoholabusus, hereditäre Lebererkrankungen § Diagnostik erfolgte ausschließlich durch Leberbiopsie mod. nach Valantin MA et al. ; MOPEB 062; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
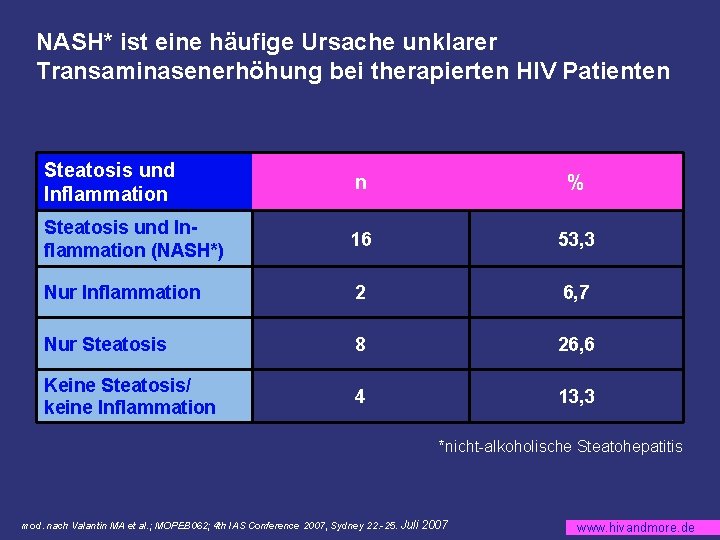
NASH* ist eine häufige Ursache unklarer Transaminasenerhöhung bei therapierten HIV Patienten Steatosis und Inflammation n % Steatosis und Inflammation (NASH*) 16 53, 3 Nur Inflammation 2 6, 7 Nur Steatosis 8 26, 6 Keine Steatosis/ keine Inflammation 4 13, 3 *nicht-alkoholische Steatohepatitis mod. nach Valantin MA et al. ; MOPEB 062; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
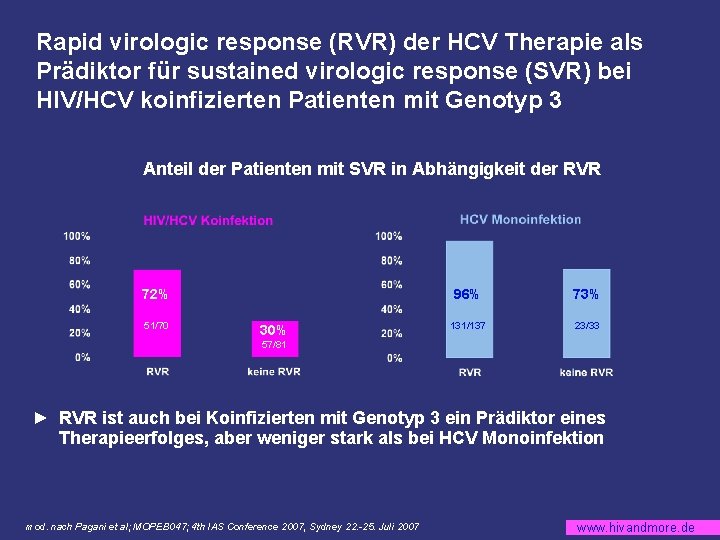
Rapid virologic response (RVR) der HCV Therapie als Prädiktor für sustained virologic response (SVR) bei HIV/HCV koinfizierten Patienten mit Genotyp 3 Anteil der Patienten mit SVR in Abhängigkeit der RVR 72% 51/70 30% 96% 73% 131/137 23/33 57/81 ► RVR ist auch bei Koinfizierten mit Genotyp 3 ein Prädiktor eines Therapieerfolges, aber weniger stark als bei HCV Monoinfektion mod. nach Pagani et al; MOPEB 047; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

ATHENA Kohorte: Nevirapin assoziierte HSR bei Therapie-naiven und vorbehandelten Patienten § Analyse von drei Gruppen auf durch NVP-haltige Kombinationstherapie (NVPc) induzierte HSR Geschlecht Ethnizität Therapie-naive Patienten - NL - NH NL = Naiv, Low CD 4+ NH = Naiv, High CD 4+ PLL = Pretreated, Low nadir, Low current CD 4+ PLH = Pretreated, Low nadir, High current CD 4+ PHL = Pretreated, High nadir, Low current CD 4+ PHH = Pretreated, High nadir, High current CD 4+ Vorbehandelte Patienten - PLL* - PLH - PHL - PHH *niedrige CD 4 -Zellzahl =Frauen mit CD 4≤ 250/µl =Männer mit CD 4≤ 400/µl mod. nach Wit et al. ; MOPEB 008; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
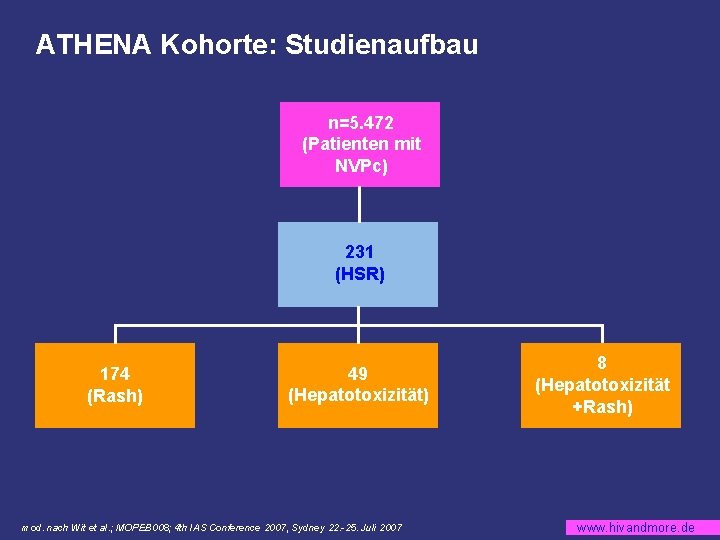
ATHENA Kohorte: Studienaufbau n=5. 472 (Patienten mit NVPc) 231 (HSR) 174 (Rash) 49 (Hepatotoxizität) mod. nach Wit et al. ; MOPEB 008; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 8 (Hepatotoxizität +Rash) www. hivandmore. de

ATHENA Kohorte: NVP-HSR Risiko § Vorbehandelte Patienten mit niedrigem CD 4 -Nadir und aktuell hoher CD 4 -Zellzahl sowie VL<50 cp/ml haben ein vergleichbares HSR-Risiko wie unbehandelte Patienten mit niedriger CD 4 Zellzahl § Vorbehandelte Patienten mit niedrigem CD 4 -Nadir und aktuell hoher CD 4 -Zellzahl sowie nachweisbarer Viruslast haben ein höheres HSR-Risiko als unbehandelte Patienten mit niedriger CD 4 -Zellzahl § Weibliches Geschlecht und asiatische Herkunft sind unabhängige Risikofaktoren mod. nach Wit et al. ; MOPEB 008; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Ezetimibe add-on bei HIV-Patienten § 33 Patienten aus Vancouver (24 mit PI-Therapie)1 § Zu Baseline max. tolerierte Lipid-senkende Therapie (kein Zeitrahmen) ► Keine AEs § 20 Patienten aus Philadelphia mit PI-Therapie 2 § § Zu Baseline Pravastatin 20 mg oder Atorvastatin 10 mg Diät und Einnahmeberatung in Wo 6, Ergebnisse nach Wo 6 -12 -18 ► 1 x CK-Erhöhung Wo 18, reversibel nach Absetzen mod. nach 1 Benett et al. ; TUPEB 075 und 2 Klibanov et al. ; TUPEB 076; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
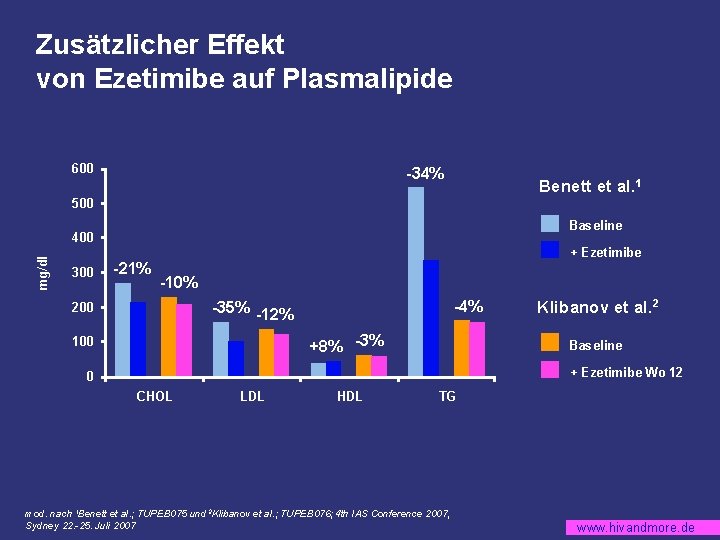
Zusätzlicher Effekt von Ezetimibe auf Plasmalipide 600 -34% Benett et al. 1 500 Baseline mg/dl 400 300 -21% + Ezetimibe -10% -4% -35% -12% 200 +8% -3% 100 Klibanov et al. 2 Baseline + Ezetimibe Wo 12 0 CHOL LDL HDL TG mod. nach 1 Benett et al. ; TUPEB 075 und 2 Klibanov et al. ; TUPEB 076; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
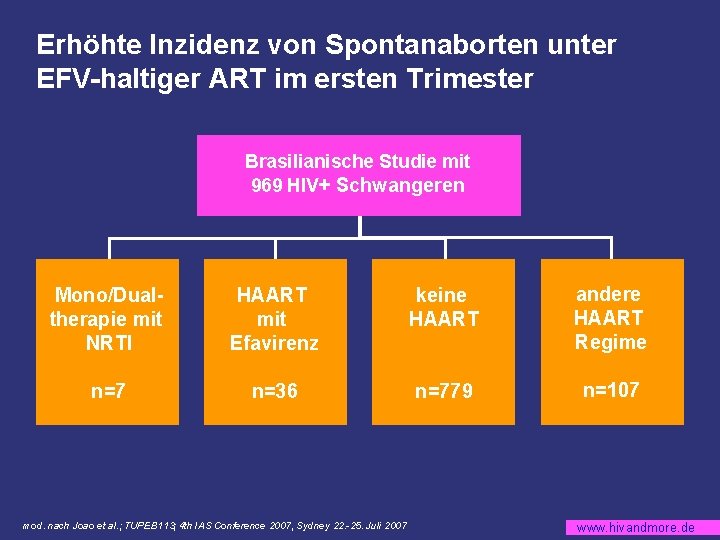
Erhöhte Inzidenz von Spontanaborten unter EFV-haltiger ART im ersten Trimester Brasilianische Studie mit 969 HIV+ Schwangeren Mono/Dualtherapie mit NRTI HAART mit Efavirenz keine HAART andere HAART Regime n=7 n=36 n=779 n=107 mod. nach Joao et al. ; TUPEB 113; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
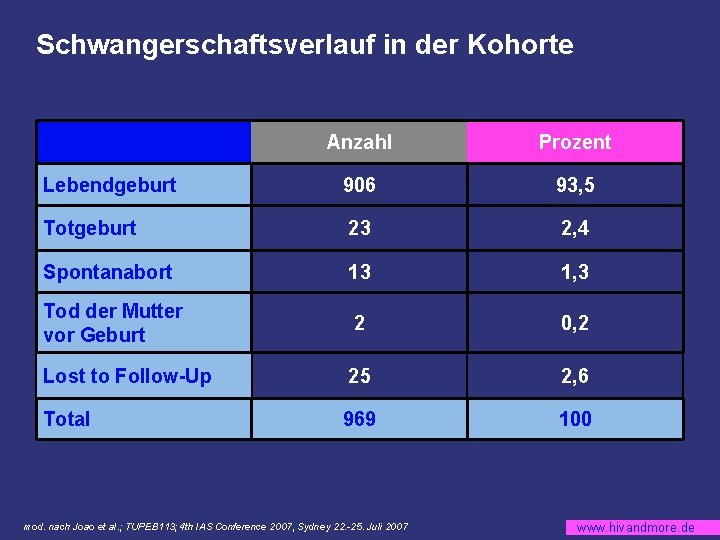
Schwangerschaftsverlauf in der Kohorte Anzahl Prozent Lebendgeburt 906 93, 5 Totgeburt 23 2, 4 Spontanabort 13 1, 3 Tod der Mutter vor Geburt 2 0, 2 Lost to Follow-Up 25 2, 6 Total 969 100 mod. nach Joao et al. ; TUPEB 113; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
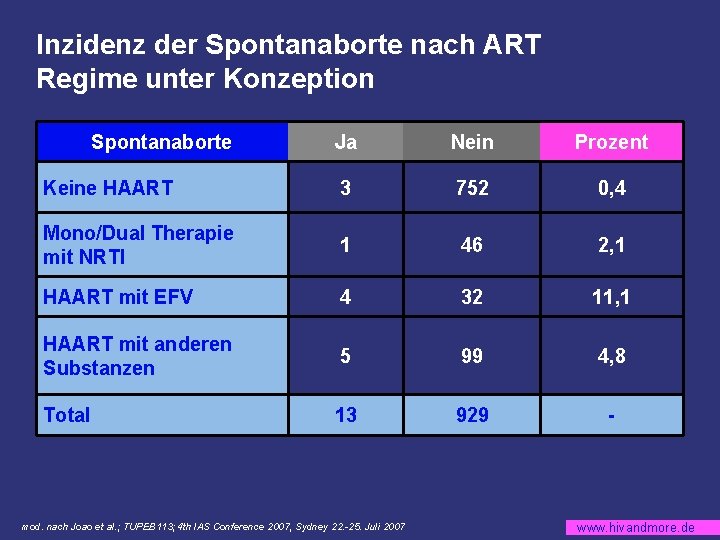
Inzidenz der Spontanaborte nach ART Regime unter Konzeption Spontanaborte Ja Nein Prozent Keine HAART 3 752 0, 4 Mono/Dual Therapie mit NRTI 1 46 2, 1 HAART mit EFV 4 32 11, 1 HAART mit anderen Substanzen 5 99 4, 8 Total 13 929 - mod. nach Joao et al. ; TUPEB 113; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

EFV im ersten Trimenon § Vor geplanter Schwangerschaft Wechsel auf EFV freie ART anstreben § Bei EFV-haltiger Therapie zuverlässige Kontrazeptionsmaßnahmen vornehmen § Erhöhte Rate von Spontanaborten unter EFV könnte durch frühe kongenitale Malformationen bedingt sein mod. nach Joao et al. ; TUPEB 113; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

4. Prävention 4. 1. CHER-Studie: 4. 2. PREP: 4. 3. Zirkumzision: 4. 3. 1. Chirurgische Risiken: 4. 3. 2. Modelle: 4. 4. Cellulosesulfat: 4. 5 Mikrobizide: Violari et al. ; WESS 103 Vernazza et al. ; MOPDC 01 Bailey et al. ; TUPL 101 Kigozi et al. ; WEAC 103 Londish et al. ; WEAC 104 van Damme et al. ; WESS 301 Cates et al. ; WESS 302 Hillier; http: //www. mtnstopshiv. org/ downloads/core/presentations/ Hillier%20 Regional%203. pdf www. hivandmore. de

CHER-Studie: ART-Beginn vor der 12. Lebenswoche senkt die Mortalität bei HIV-infizierten Kindern in Südafrika Diagnose HIV vor Woche 12, CD 4 >25% Arm 1 Späterer Therapiebeginn (nach Indikation) n=125 Arm 2 Frühe Therapie: bis zum 1. Geburtstag n=125 Arm 3 Frühe Therapie: bis zum 2. Geburtstag n=125 ART-Beginn, bzw. Re-Start bei CD 4 <20% oder klinischem Ereignis Follow-Up: Minimum 3, 5 Jahr mod. nach Violari et al. ; WESS 103; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

CHER-Studie: § Einschlusskriterien § HIV PCR positiv, CD 4 >25% § ART-naiv, außer p. MTCT § Alter <12 Wochen § § Gewählte ART: AZT+3 TC+LPV/r § Endpunkte § Tod, Therapieversagen, Krankheitsprogression, Pneumokokkenimpfung und Cotrim-Prophylaxe aller Kinder Hospitalisierung, Grad 3+4 Ereignisse mod. nach Violari et al. ; WESS 103; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
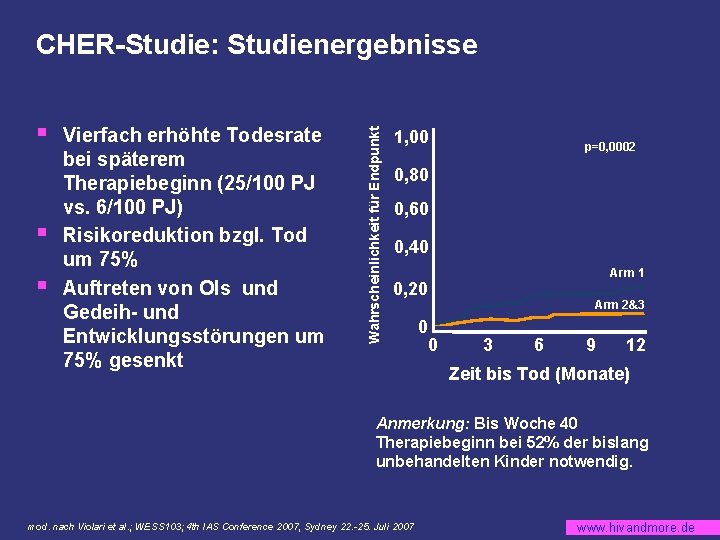
§ § § Vierfach erhöhte Todesrate bei späterem Therapiebeginn (25/100 PJ vs. 6/100 PJ) Risikoreduktion bzgl. Tod um 75% Auftreten von OIs und Gedeih- und Entwicklungsstörungen um 75% gesenkt Wahrscheinlichkeit für Endpunkt CHER-Studie: Studienergebnisse 1, 00 p=0, 0002 0, 80 0, 60 0, 40 Arm 1 0, 20 0 0 Arm 2&3 3 6 9 12 Zeit bis Tod (Monate) Anmerkung: Bis Woche 40 Therapiebeginn bei 52% der bislang unbehandelten Kinder notwendig. mod. nach Violari et al. ; WESS 103; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Präexpositionsprophylaxe bei serodiskordanten Paaren mit Kinderwunsch § 22 Serodiskordante Paare mit Kinderwunsch (Mann HIV-infiziert, Frau HIV-negativ) § Geschlechtsverkehr zum Zeitpunkt der Ovulation (Bestimmung über Urin LH-Peak) § Ausschluss asymptomatischer STD § HAART bei Mann mit VL<50 Kopien/ml in Blut und Sperma § Ausführliche Aufklärung des Paares Intervention: 1 x TDF bei LH-Peak und 24 Std. später, 12 Std. danach ungeschützter Verkehr mod. nach Vernazza; MOPDC 01; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
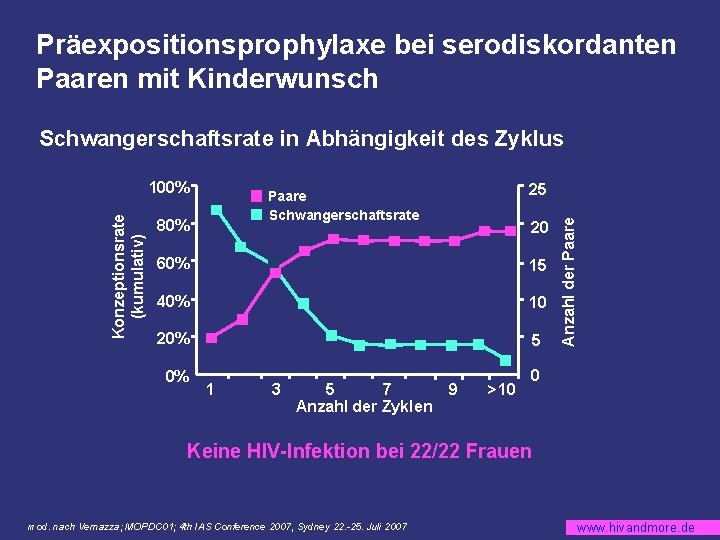
Präexpositionsprophylaxe bei serodiskordanten Paaren mit Kinderwunsch Schwangerschaftsrate in Abhängigkeit des Zyklus 25 Paare Schwangerschaftsrate 80% 20 60% 15 40% 10 20% 5 0% 1 3 5 7 Anzahl der Zyklen 9 >10 Anzahl der Paare Konzeptionsrate (kumulativ) 100% 0 Keine HIV-Infektion bei 22/22 Frauen mod. nach Vernazza; MOPDC 01; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Zirkumzision von Männern: 57% Risikoreduktion § Auswirkung der Zirkumzision auf die HIV-Inzidenz § Metaanalyse von Beobachtungsstudien und 3 prospektiven randomisierten Studien (RCT) in Afrika Relatives Risiko (95% KI) Beobachtungsstudien 0, 42 (0, 34 -0, 52) Südafrika 0, 40 (0, 24 -0, 68) Kenia 0, 41 (0, 24 -0, 70) Uganda 0, 49 (0, 2 -0, 84) Alle RCT (95% KI) 0, 43 (0, 32 -0, 58) 0, 15 0, 2 0, 3 0, 4 0, 5 1 1, 5 Relatives Risiko mod. nach Bailey; TUPL 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Offene Fragen zur Zirkumzision § Auswirkungen auf Risikoverhalten? § Bisher keine sicheren Hinweise auf Zunahme des Risikoverhaltens § Wege zur Implementierung offen: Dringende Empfehlung von WHO und UNAIDS (Mai 2007) § Kosteneffektivität abhängig von HIV-Prävalenz § § Bei HIV-Prävalenz von 25% Kosten pro verhinderter Infektion US$ 181 über 20 Jahre Effektivität in Populationen mit nicht heterosexuellem Übertragungsweg (IVDU, MSM) unklar mod. nach Bailey; TUPL 101; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
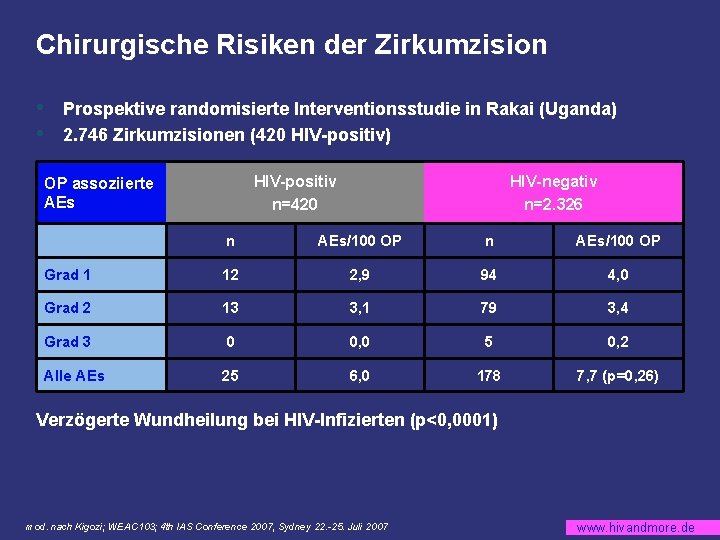
Chirurgische Risiken der Zirkumzision • • Prospektive randomisierte Interventionsstudie in Rakai (Uganda) 2. 746 Zirkumzisionen (420 HIV-positiv) HIV-positiv n=420 OP assoziierte AEs HIV-negativ n=2. 326 n AEs/100 OP Grad 1 12 2, 9 94 4, 0 Grad 2 13 3, 1 79 3, 4 Grad 3 0 0, 0 5 0, 2 Alle AEs 25 6, 0 178 7, 7 (p=0, 26) Verzögerte Wundheilung bei HIV-Infizierten (p<0, 0001) mod. nach Kigozi; WEAC 103; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
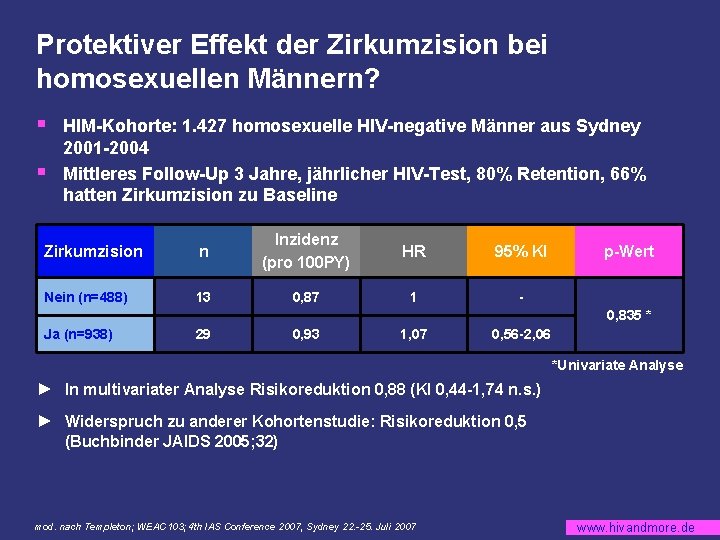
Protektiver Effekt der Zirkumzision bei homosexuellen Männern? § § HIM-Kohorte: 1. 427 homosexuelle HIV-negative Männer aus Sydney 2001 -2004 Mittleres Follow-Up 3 Jahre, jährlicher HIV-Test, 80% Retention, 66% hatten Zirkumzision zu Baseline Zirkumzision n Inzidenz (pro 100 PY) HR 95% KI Nein (n=488) 13 0, 87 1 - p-Wert 0, 835 * Ja (n=938) 29 0, 93 1, 07 0, 56 -2, 06 *Univariate Analyse ► In multivariater Analyse Risikoreduktion 0, 88 (KI 0, 44 -1, 74 n. s. ) ► Widerspruch zu anderer Kohortenstudie: Risikoreduktion 0, 5 (Buchbinder JAIDS 2005; 32) mod. nach Templeton; WEAC 103; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
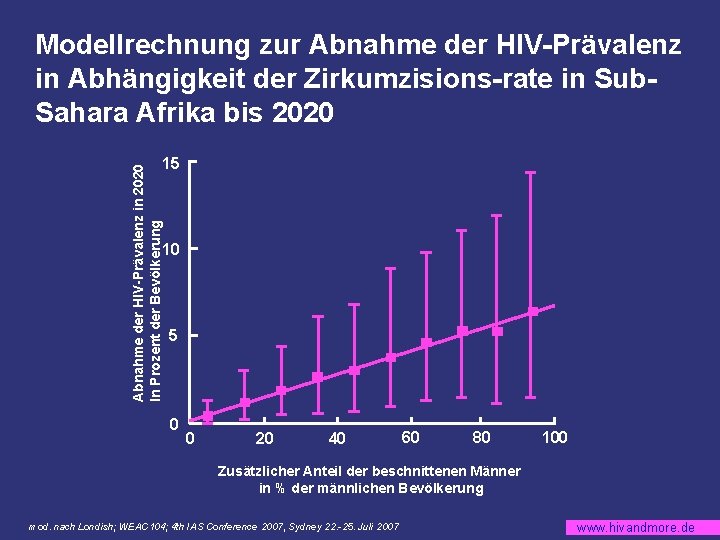
Modellrechnung zur Abnahme der HIV-Prävalenz in Abhängigkeit der Zirkumzisions-rate in Sub. Sahara Afrika bis 2020 Abnahme der HIV-Prävalenz in 2020 In Prozent der Bevölkerung 15 10 5 0 0 20 40 60 80 100 Zusätzlicher Anteil der beschnittenen Männer in % der männlichen Bevölkerung mod. nach Londish; WEAC 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
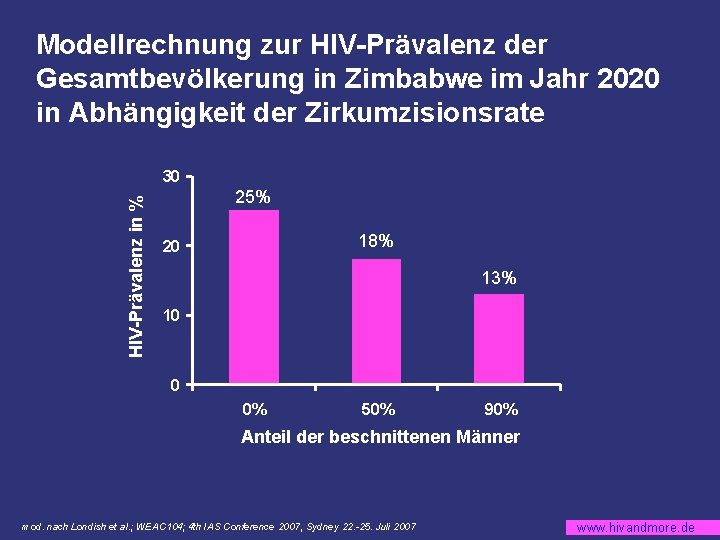
Modellrechnung zur HIV-Prävalenz der Gesamtbevölkerung in Zimbabwe im Jahr 2020 in Abhängigkeit der Zirkumzisionsrate HIV-Prävalenz in % 30 25% 18% 20 13% 10 0 0% 50% 90% Anteil der beschnittenen Männer mod. nach Londish et al. ; WEAC 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

CONRAD: Na-Cellulosesulfat 6% Vaginalgel (CS) § 5 Länder, Einschluss von 2. 574 Frauen geplant § CS+Kondome vs. Plazebo + Kondome § Geplante Interimsanalyse 1/2007: Studienabbruch § HIV Serokonversionen: CS 24/717 vs. Plazebo 11/708 RR 2, 23 (p=0, 022) ► Signifikant höhere HIV-Infektionsrate unter CS ► Ursache noch unklar mod. nach Van Damme et al. ; WESS 301; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

FHI: Na-Cellulosesulfat 6% Vaginalgel (CS) § Nigeria, Einschluss von 2. 160 Frauen geplant § CS+Kondome vs. Plazebo + Kondome § 1/2007: Studienabbruch wg. CONRAD § HIV Serokonversionen: CS 10/820 vs. Plazebo 13/823 RR 0, 8 (p=0, 56) ► Kein signifikanter Effekt von CS mod. nach Cates et al. ; WESS 302; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
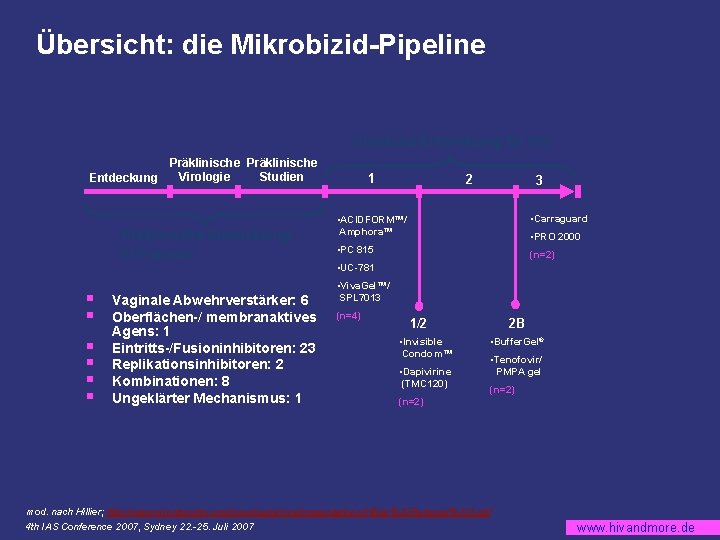
Übersicht: die Mikrobizid-Pipeline Klinische Entwicklung für HIV Präklinische Virologie Studien Entdeckung Präklinische Entwicklung: 51 Präparate 1 2 3 • ACIDFORM™/ Amphora™ • Carraguard • PC 815 (n=2) • PRO 2000 • UC-781 § § § Vaginale Abwehrverstärker: 6 Oberflächen-/ membranaktives Agens: 1 Eintritts-/Fusioninhibitoren: 23 Replikationsinhibitoren: 2 Kombinationen: 8 Ungeklärter Mechanismus: 1 • Viva. Gel™/ SPL 7013 (n=4) 2 B 1/2 • Invisible Condom™ • Dapivirine (TMC 120) • Buffer. Gel® • Tenofovir/ PMPA gel (n=2) mod. nach Hillier; http: //www. mtnstopshiv. org/downloads/core/presentations/Hillier%20 Regional%203. pdf 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

5. Neue Substanzen 5. 1. Integrasehemmer: 5. 1. 1. RAL vs. EFV: 5. 1. 2. RAL vs. EVG: 5. 2. Vicriviroc: ACTG 5211: 5. 3. NNRTI: 5. 3. 1. DUET 1 und 2: Markowitz et al. ; TUAB 104 de Jesus et al. ; TUPEB 032 Gulick et al. ; TUAB 102 Mills et al. ; WESS 203 Katlama et al. ; WESS 204 5. 3. 2. TMC 278: Ruxrungtham et al. ; TUAB 105 5. 5. Maraviroc: MERIT Studie: Saag et al. ; WESS 104 5. 6. PIPELINE www. hivandmore. de

Raltegravir (RAL) vs. Efavirenz (EFV) in der Initialtherpie Therapie-Outcome nach 48 Wochen § Studiendesign § Randomisiert, kontrolliert, doppelblind, Phase II § RAL in unterschiedlichen Dosierungen (100 -200 -400 -600 mg bid) vs. EFV, jeweils kombiniert mit TDF/3 TC § Studienziel § VL, CD 4, AEs zu Woche 48 § Studienpopulation (n=198) § ART-naiv § VL>5. 000 Kopien/ml § CD 4>100/µl mod. nach Markowitz; TUAB 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
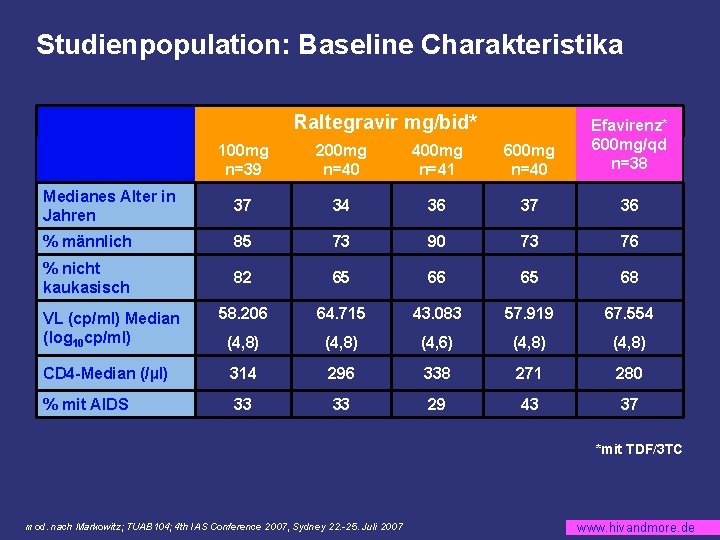
Studienpopulation: Baseline Charakteristika Raltegravir mg/bid* 100 mg n=39 200 mg n=40 400 mg n=41 600 mg n=40 Efavirenz* 600 mg/qd n=38 Medianes Alter in Jahren 37 34 36 37 36 % männlich 85 73 90 73 76 % nicht kaukasisch 82 65 66 65 68 58. 206 64. 715 43. 083 57. 919 67. 554 (4, 8) (4, 6) (4, 8) CD 4 -Median (/µl) 314 296 338 271 280 % mit AIDS 33 33 29 43 37 VL (cp/ml) Median (log 10 cp/ml) *mit TDF/3 TC mod. nach Markowitz; TUAB 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
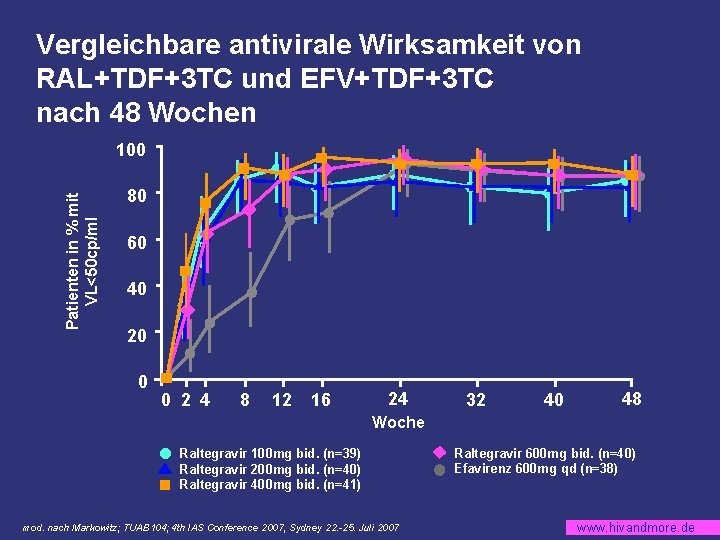
Vergleichbare antivirale Wirksamkeit von RAL+TDF+3 TC und EFV+TDF+3 TC nach 48 Wochen Patienten in % mit VL<50 cp/ml 100 80 60 40 20 0 0 2 4 8 12 16 24 32 40 48 Woche Raltegravir 100 mg bid. (n=39) Raltegravir 200 mg bid. (n=40) Raltegravir 400 mg bid. (n=41) mod. nach Markowitz; TUAB 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 Raltegravir 600 mg bid. (n=40) Efavirenz 600 mg qd (n=38) www. hivandmore. de

Zusammenfassung § VL<50 Kopien/ml bei 87 -95% unter RAL vs. 92% unter EFV § Im Vergleich zum EFV-Arm signifikant schnellerer Abfall der VL (Murray et al. ; TUAB 103) § Weniger NW in den RAL-Armen (ZNS NW selten, kein signifikanter Anstieg der Serumlipide) mod. nach Markowitz; TUAB 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Kreuzresistenz zwischen Raltegravir (RAL) und Elvitegravir (EVG) § Einsatz von RAL nach versagender EVG Therapie bei 2 Patienten § Genotyp bei Umstellung von EVG auf RAL § § Patient 1: A 91 Q, Q 59 Q/K, T 97 T/A, N 155 H Patient 2: H 51 Y, E 138 E/K, P 145 P/S, S 174 G, Q 148 R ► Nichtansprechen nach Therapieumstellung wegen Kreuzresistenzen mod. nach de Jesus et al. ; TUPEB 032; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

Kreuzresistenz zwischen Raltegravir (RAL) und Elvitegravir (EVG) § Hintergrund § § § RAL: bisher 2 Resistenzpfade beschrieben (N 155 H oder Q 148 R) EVG: bisher häufigste Mutationen bei versagender Therapie: E 92 Q, E 138 K, Q 148 R/H/K, N 155 H Hochgradige Resistenz für RAL und EVG bei Q 148 H/R+G 140 S Fazit § § § Kreuzresistenz zwischen RAL und EVG möglich Integrasehemmer-Resistenz bereits bei singulärer Integrase. Mutation möglich In vivo neue Resistenzmuster unter EVG mod. nach de Jesus et al. ; TUPEB 032; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
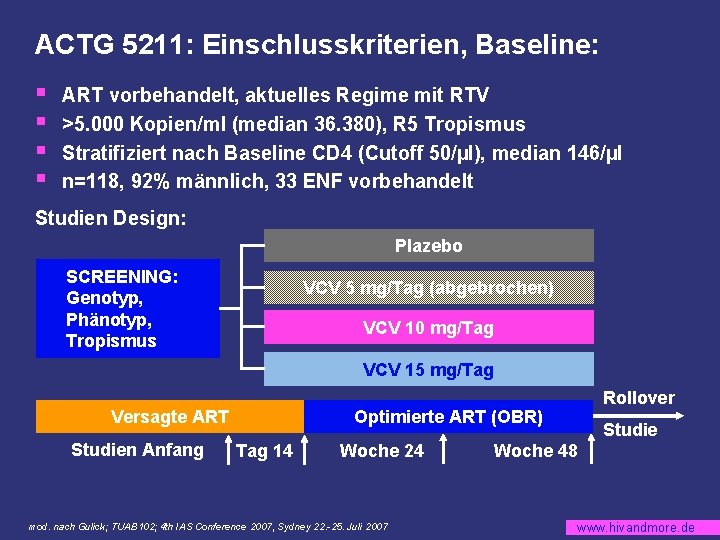
ACTG 5211: Einschlusskriterien, Baseline: § § ART vorbehandelt, aktuelles Regime mit RTV >5. 000 Kopien/ml (median 36. 380), R 5 Tropismus Stratifiziert nach Baseline CD 4 (Cutoff 50/µl), median 146/µl n=118, 92% männlich, 33 ENF vorbehandelt Studien Design: Plazebo SCREENING: Genotyp, Phänotyp, Tropismus VCV 5 mg/Tag (abgebrochen) VCV 10 mg/Tag VCV 15 mg/Tag Versagte ART Studien Anfang Rollover Optimierte ART (OBR) Tag 14 Woche 24 mod. nach Gulick; TUAB 102; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 Studie Woche 48 www. hivandmore. de
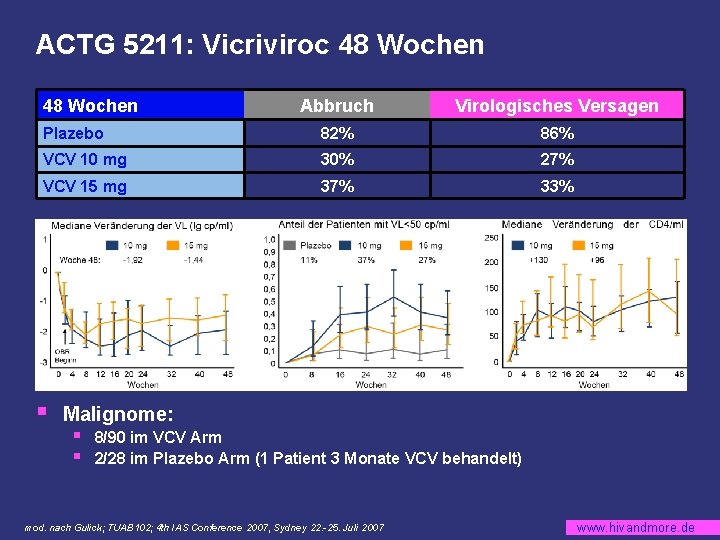
ACTG 5211: Vicriviroc 48 Wochen Abbruch Virologisches Versagen Plazebo 82% 86% VCV 10 mg 30% 27% VCV 15 mg 37% 33% § Malignome: § § 8/90 im VCV Arm 2/28 im Plazebo Arm (1 Patient 3 Monate VCV behandelt) mod. nach Gulick; TUAB 102; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

ACTG 5211: Zusammenfassung CCR 5 Tropismus § 10% Veränderung Tropismus zwischen Screening und Baseline § § Shift zu X 4 tropem Virus (dual/mixed): § § § Minorvarianten <10% werden von Tropismustests nicht sicher erfasst Auftreten bei 9/26 (35%) der Patienten mit virologischem Versagen 3 x im Plazeboarm (2 x nach Crossover zu VCV), 15 x in VCV Arm Alternativer Resistenzmechanismus: gp 120 Mutation ermöglicht Bindung von HIV an den CCR 5 -Rezeptor/Inhibitor Komplex mod. nach Gulick; TUAB 102; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
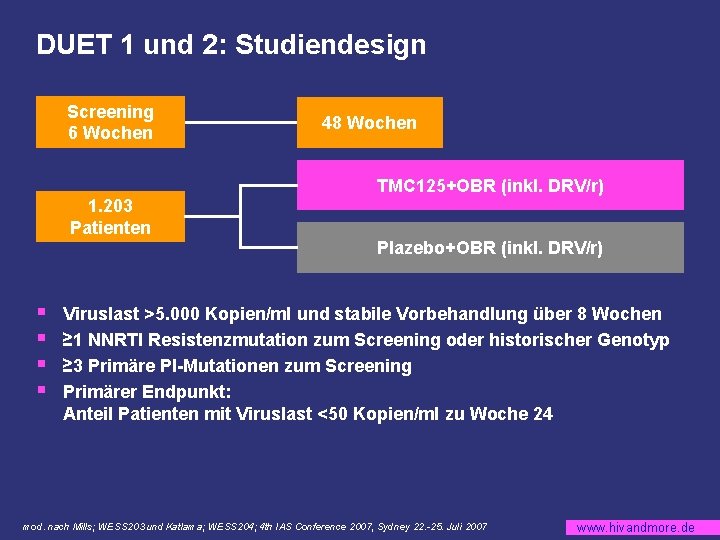
DUET 1 und 2: Studiendesign Screening 6 Wochen 48 Wochen TMC 125+OBR (inkl. DRV/r) 1. 203 Patienten Plazebo+OBR (inkl. DRV/r) § § Viruslast >5. 000 Kopien/ml und stabile Vorbehandlung über 8 Wochen ≥ 1 NNRTI Resistenzmutation zum Screening oder historischer Genotyp ≥ 3 Primäre PI-Mutationen zum Screening Primärer Endpunkt: Anteil Patienten mit Viruslast <50 Kopien/ml zu Woche 24 mod. nach Mills; WESS 203 und Katlama; WESS 204; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
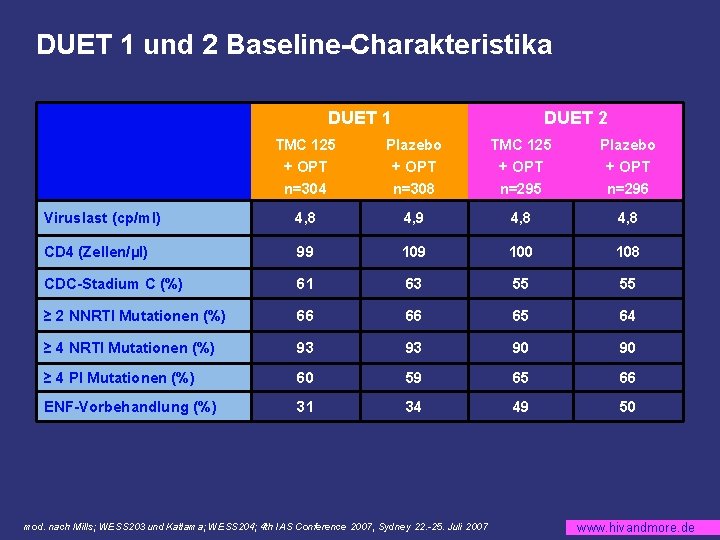
DUET 1 und 2 Baseline-Charakteristika DUET 1 DUET 2 TMC 125 + OPT n=304 Plazebo + OPT n=308 TMC 125 + OPT n=295 Plazebo + OPT n=296 Viruslast (cp/ml) 4, 8 4, 9 4, 8 CD 4 (Zellen/µl) 99 100 108 CDC-Stadium C (%) 61 63 55 55 ≥ 2 NNRTI Mutationen (%) 66 66 65 64 ≥ 4 NRTI Mutationen (%) 93 93 90 90 ≥ 4 PI Mutationen (%) 60 59 65 66 ENF-Vorbehandlung (%) 31 34 49 50 mod. nach Mills; WESS 203 und Katlama; WESS 204; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
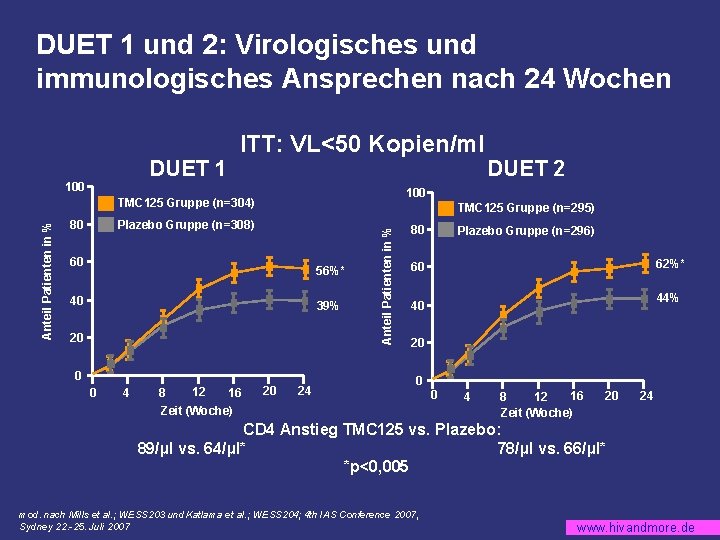
DUET 1 und 2: Virologisches und immunologisches Ansprechen nach 24 Wochen DUET 1 ITT: VL<50 Kopien/ml 100 TMC 125 Gruppe (n=295) Plazebo Gruppe (n=308) 60 56%* 40 39% 20 0 0 4 12 16 8 Zeit (Woche) 20 24 Anteil Patienten in % TMC 125 Gruppe (n=304) 80 DUET 2 80 Plazebo Gruppe (n=296) 62%* 60 44% 40 20 0 0 4 16 8 12 Zeit (Woche) 20 24 CD 4 Anstieg TMC 125 vs. Plazebo: 89/µl vs. 64/µl* 78/µl vs. 66/µl* *p<0, 005 mod. nach Mills et al. ; WESS 203 und Katlama et al. ; WESS 204; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
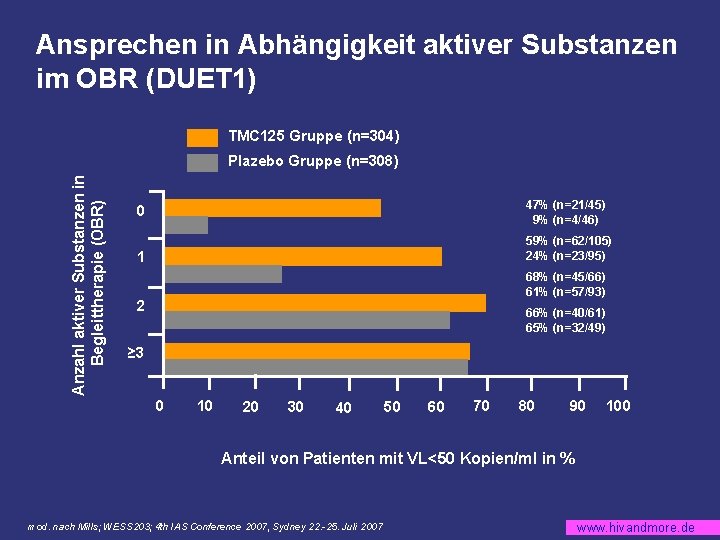
Ansprechen in Abhängigkeit aktiver Substanzen im OBR (DUET 1) TMC 125 Gruppe (n=304) Anzahl aktiver Substanzen in Begleittherapie (OBR) Plazebo Gruppe (n=308) 47% (n=21/45) 9% (n=4/46) 0 59% (n=62/105) 24% (n=23/95) 1 68% (n=45/66) 61% (n=57/93) 2 66% (n=40/61) 65% (n=32/49) ≥ 3 0 10 20 30 40 50 60 70 80 90 100 Anteil von Patienten mit VL<50 Kopien/ml in % mod. nach Mills; WESS 203; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
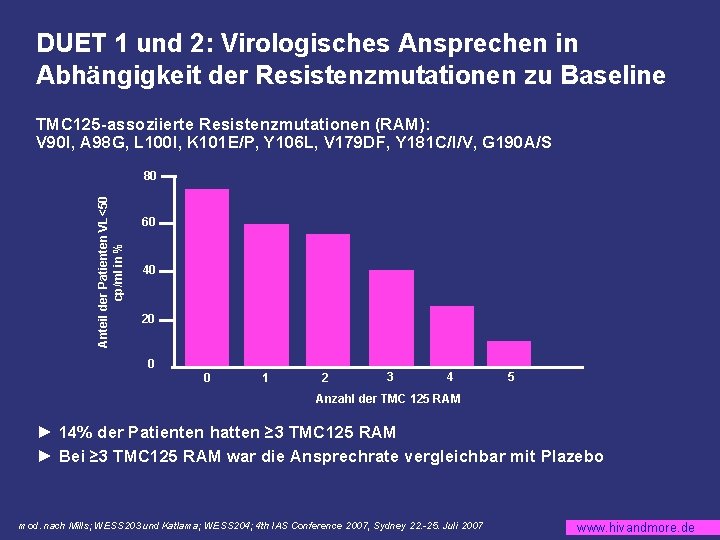
DUET 1 und 2: Virologisches Ansprechen in Abhängigkeit der Resistenzmutationen zu Baseline TMC 125 -assoziierte Resistenzmutationen (RAM): V 90 I, A 98 G, L 100 I, K 101 E/P, Y 106 L, V 179 DF, Y 181 C/I/V, G 190 A/S Anteil der Patienten VL<50 cp/ml in % 80 60 40 20 0 0 1 2 3 4 5 Anzahl der TMC 125 RAM ► 14% der Patienten hatten ≥ 3 TMC 125 RAM ► Bei ≥ 3 TMC 125 RAM war die Ansprechrate vergleichbar mit Plazebo mod. nach Mills; WESS 203 und Katlama; WESS 204; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
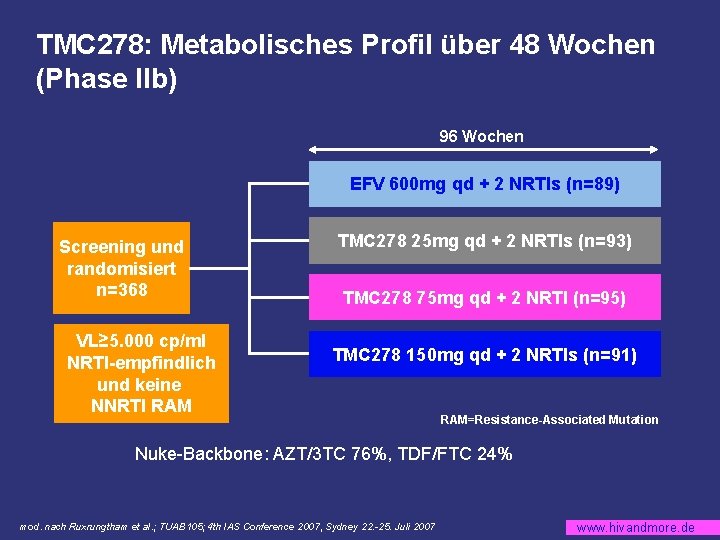
TMC 278: Metabolisches Profil über 48 Wochen (Phase IIb) 96 Wochen EFV 600 mg qd + 2 NRTIs (n=89) Screening und randomisiert n=368 VL≥ 5. 000 cp/ml NRTI-empfindlich und keine NNRTI RAM TMC 278 25 mg qd + 2 NRTIs (n=93) TMC 278 75 mg qd + 2 NRTI (n=95) TMC 278 150 mg qd + 2 NRTIs (n=91) RAM=Resistance-Associated Mutation Nuke-Backbone: AZT/3 TC 76%, TDF/FTC 24% mod. nach Ruxrungtham et al. ; TUAB 105; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
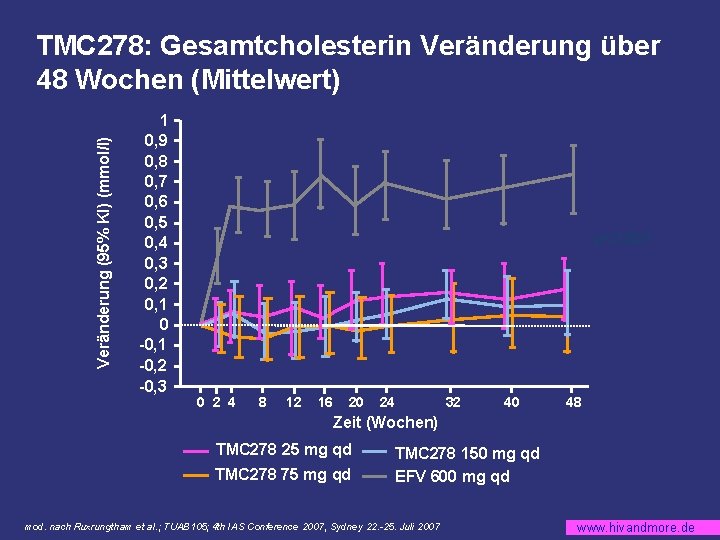
Veränderung (95% KI) (mmol/l) TMC 278: Gesamtcholesterin Veränderung über 48 Wochen (Mittelwert) 1 0, 9 0, 8 0, 7 0, 6 0, 5 0, 4 0, 3 0, 2 0, 1 0 -0, 1 -0, 2 -0, 3 p<0, 001 0 2 4 8 12 16 20 24 32 40 48 Zeit (Wochen) TMC 278 25 mg qd TMC 278 75 mg qd TMC 278 150 mg qd EFV 600 mg qd mod. nach Ruxrungtham et al. ; TUAB 105; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
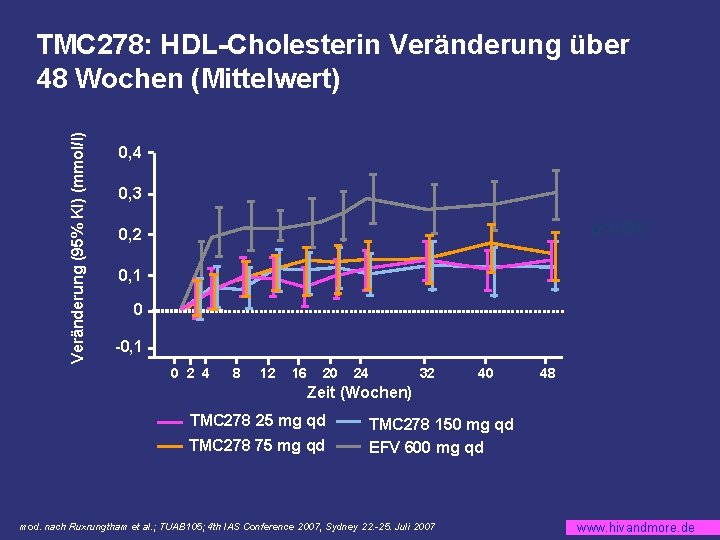
Veränderung (95% KI) (mmol/l) TMC 278: HDL-Cholesterin Veränderung über 48 Wochen (Mittelwert) 0, 4 0, 3 p<0, 001 0, 2 0, 1 0 -0, 1 0 2 4 8 12 16 20 24 32 40 48 Zeit (Wochen) TMC 278 25 mg qd TMC 278 75 mg qd TMC 278 150 mg qd EFV 600 mg qd mod. nach Ruxrungtham et al. ; TUAB 105; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
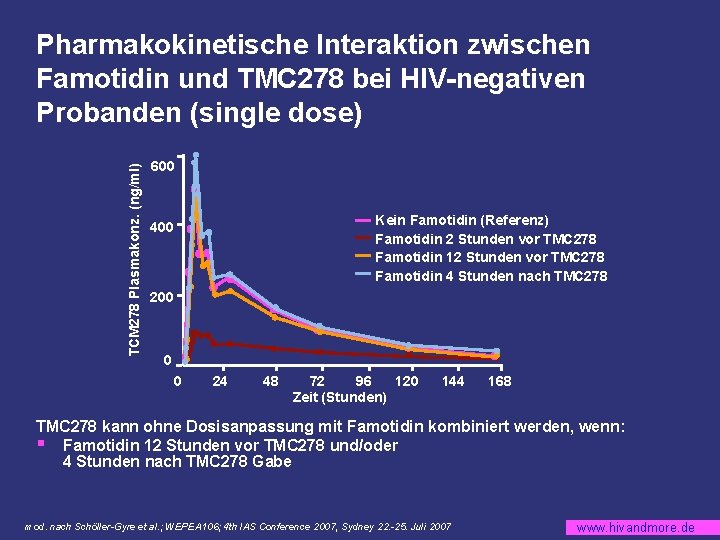
TCM 278 Plasmakonz. (ng/ml) Pharmakokinetische Interaktion zwischen Famotidin und TMC 278 bei HIV-negativen Probanden (single dose) 600 Kein Famotidin (Referenz) Famotidin 2 Stunden vor TMC 278 Famotidin 12 Stunden vor TMC 278 Famotidin 4 Stunden nach TMC 278 400 200 0 0 24 48 72 96 120 Zeit (Stunden) 144 168 TMC 278 kann ohne Dosisanpassung mit Famotidin kombiniert werden, wenn: § Famotidin 12 Stunden vor TMC 278 und/oder 4 Stunden nach TMC 278 Gabe mod. nach Schöller-Gyre et al. ; WEPEA 106; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
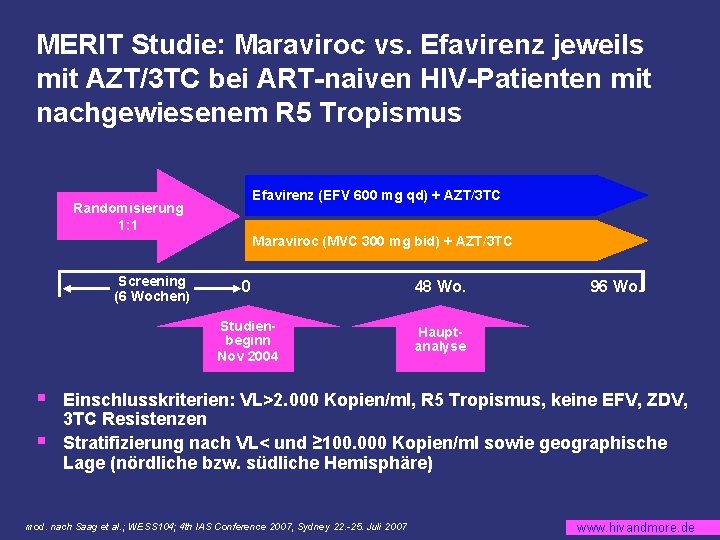
MERIT Studie: Maraviroc vs. Efavirenz jeweils mit AZT/3 TC bei ART-naiven HIV-Patienten mit nachgewiesenem R 5 Tropismus Efavirenz (EFV 600 mg qd) + AZT/3 TC Randomisierung 1: 1 Maraviroc (MVC 300 mg bid) + AZT/3 TC Screening (6 Wochen) § § 0 48 Wo. Studienbeginn Nov 2004 Hauptanalyse 96 Wo. Einschlusskriterien: VL>2. 000 Kopien/ml, R 5 Tropismus, keine EFV, ZDV, 3 TC Resistenzen Stratifizierung nach VL< und ≥ 100. 000 Kopien/ml sowie geographische Lage (nördliche bzw. südliche Hemisphäre) mod. nach Saag et al. ; WESS 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
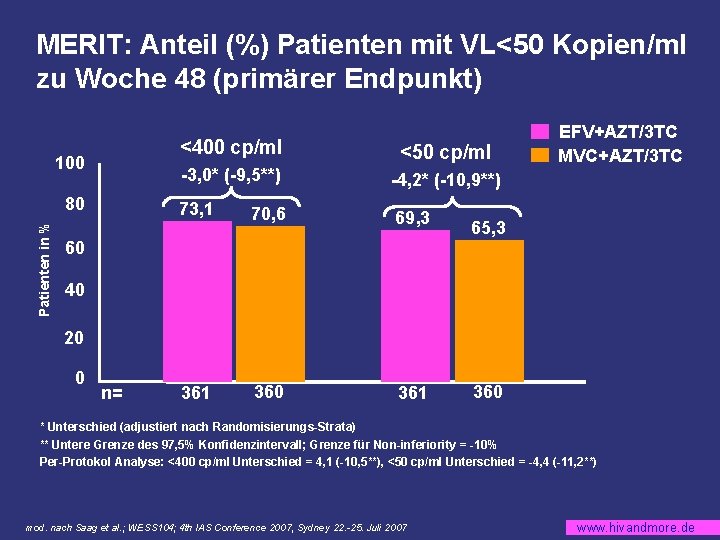
MERIT: Anteil (%) Patienten mit VL<50 Kopien/ml zu Woche 48 (primärer Endpunkt) 100 Patienten in % 80 <400 cp/ml <50 cp/ml -3, 0* (-9, 5**) -4, 2* (-10, 9**) 73, 1 70, 6 69, 3 361 360 361 60 EFV+AZT/3 TC MVC+AZT/3 TC 65, 3 40 20 0 n= 360 * Unterschied (adjustiert nach Randomisierungs-Strata) ** Untere Grenze des 97, 5% Konfidenzintervall; Grenze für Non-inferiority = -10% Per-Protokol Analyse: <400 cp/ml Unterschied = 4, 1 (-10, 5**), <50 cp/ml Unterschied = -4, 4 (-11, 2**) mod. nach Saag et al. ; WESS 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
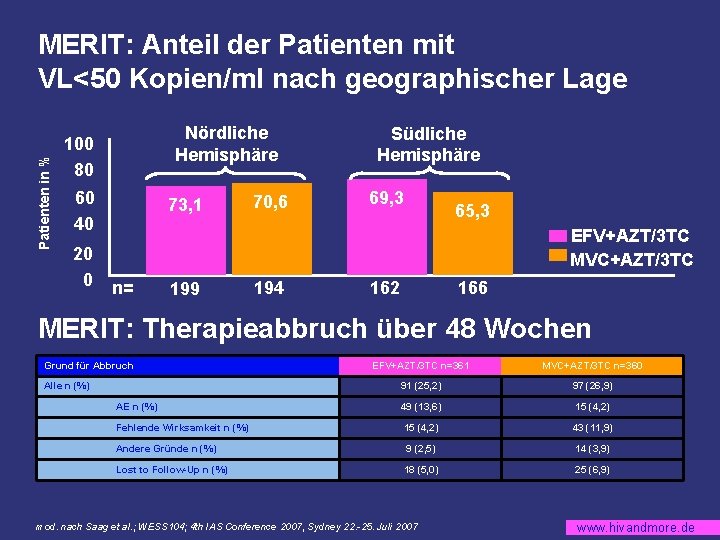
Patienten in % MERIT: Anteil der Patienten mit VL<50 Kopien/ml nach geographischer Lage Nördliche Hemisphäre 100 80 60 40 20 0 73, 1 70, 6 Südliche Hemisphäre 69, 3 65, 3 EFV+AZT/3 TC MVC+AZT/3 TC n= 199 194 162 166 MERIT: Therapieabbruch über 48 Wochen Grund für Abbruch EFV+AZT/3 TC n=361 MVC+AZT/3 TC n=360 91 (25, 2) 97 (26, 9) AE n (%) 49 (13, 6) 15 (4, 2) Fehlende Wirksamkeit n (%) 15 (4, 2) 43 (11, 9) Andere Gründe n (%) 9 (2, 5) 14 (3, 9) Lost to Follow-Up n (%) 18 (5, 0) 25 (6, 9) Alle n (%) mod. nach Saag et al. ; WESS 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de

MERIT: Zusammenfassung § Non-inferiority von MVC konnte bei VL<400 Kopien/ml, nicht aber bei < 50 Kopien/ml (primärer Endpunkt) nachgewiesen werden § Anteil der Patienten mit Therapieabbruch vor Woche 48 in beiden Armen vergleichbar [MVC 26, 9% EFV 25, 2%] § § Fehlende Wirksamkeit: MVC 11, 9% >EFV 4, 2% AE: MVC (4, 2%) <EFV (13, 6%) § Anstieg der CD 4 -Zellzahl bei MVC vs. EFV (+170 vs. +144 CD 4/µl) § Unterschiedliches Ansprechen von MVC nach geographischer Lage (nördliche vs. südliche Hemisphäre) mod. nach Saag et al. ; WESS 104; 4 th IAS Conference 2007, Sydney 22. -25. Juli 2007 www. hivandmore. de
Phase I & II Daten zu neuen Substanzen beim IAS 2007 Name Kürzel / Code Klasse Hersteller Phase Apricitabine AVX 754 NRTI Avexa IIb INCB 009471 CCR 5 Inhibitor Incyte II Elvitegravir EVG Integraseinhibitor Gilead I (+2 Pt. ) Bevirimat BVM Maturationsinhibitor Panacos I PRO 140 CCR 5 m. Ab Progenics I UK-453, 061 NNRTI Pfizer I www. hivandmore. de
- Slides: 96










































