Regenerative Kraftstoffe Experimentalvortrag von Jan Grosse Austing SS



















![• Bestimmung des Ethanolanteils mithilfe einer Dichtetabelle Dichte (20 °C) [g/m. L] 3. • Bestimmung des Ethanolanteils mithilfe einer Dichtetabelle Dichte (20 °C) [g/m. L] 3.](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-26.jpg)
![3. Bioethanol Erträge von Ethanol [L/ha] 3. Bioethanol Erträge von Ethanol [L/ha]](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-28.jpg)















![5. Kurzes Fazit • Herstellungskosten der Kraftstoffe [in €/L Kraftstoffäquivalent] *Nettopreis bei 61 Dollar 5. Kurzes Fazit • Herstellungskosten der Kraftstoffe [in €/L Kraftstoffäquivalent] *Nettopreis bei 61 Dollar](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-49.jpg)








- Slides: 65

Regenerative Kraftstoffe Experimentalvortrag von Jan Grosse Austing SS 07

Gliederung 1. Einleitung 2. Biodiesel 3. Bioethanol 4. Bt. L-Kraftstoffe (Fischer-Tropsch) 5. kurzes Fazit 6. Schulrelevanz

1. Einleitung Regenerative Energien zurzeit kontrovers diskutiert 1) Erdölverknappung 2) Klimawandel

1. Einleitung Anteil Verkehr an Emissionen von Treibhausgasen Kraftwerke (43 %) Verkehr (20 %) Gewerbe, Handel, Dienstleistungen (7 %) Haushalte (15 %) Industriefeuerungen (15%)

1. Einleitung • Interesse an Regenerativen Kraftstoffen („Biosprit“) groß • dazu zählen: Biodiesel, Bioethanol, Bt. L-Kraftstoffe, Biowasserstoff, Biomethanol, Biogas u. a.

2. Biodiesel

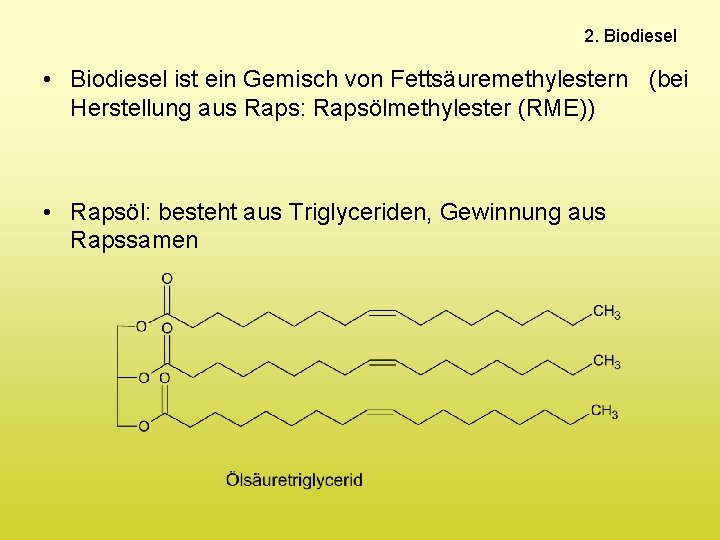
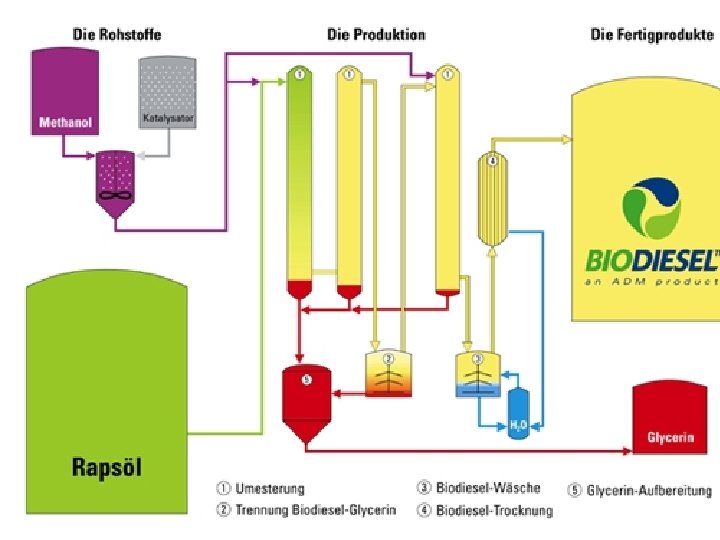
2. Biodiesel • Biodiesel ist ein Gemisch von Fettsäuremethylestern (bei Herstellung aus Raps: Rapsölmethylester (RME)) • Rapsöl: besteht aus Triglyceriden, Gewinnung aus Rapssamen

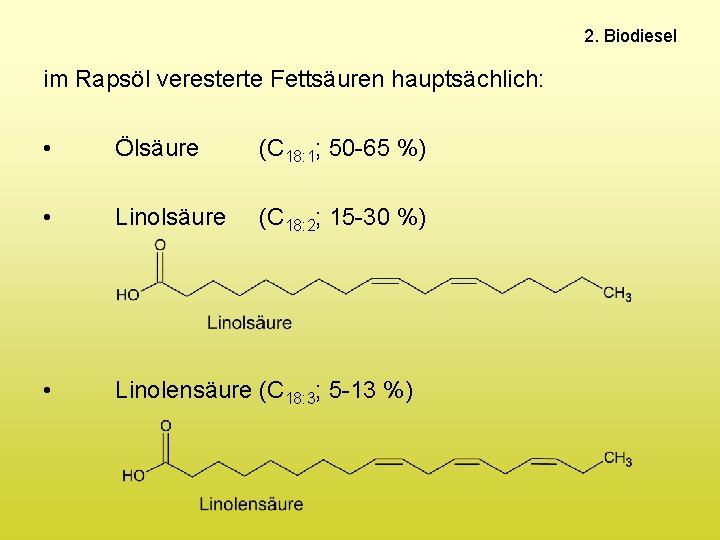
2. Biodiesel im Rapsöl veresterte Fettsäuren hauptsächlich: • Ölsäure (C 18: 1; 50 -65 %) • Linolsäure (C 18: 2; 15 -30 %) • Linolensäure (C 18: 3; 5 -13 %)

Versuch 1 Herstellung von Biodiesel

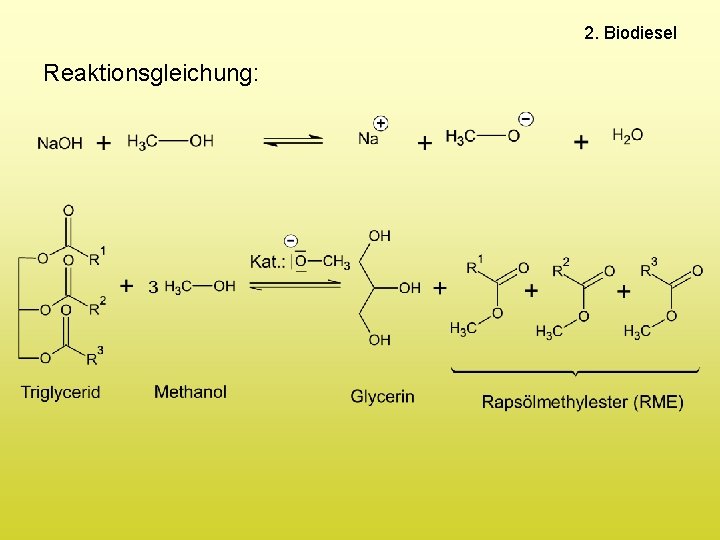
2. Biodiesel Reaktionsgleichung:

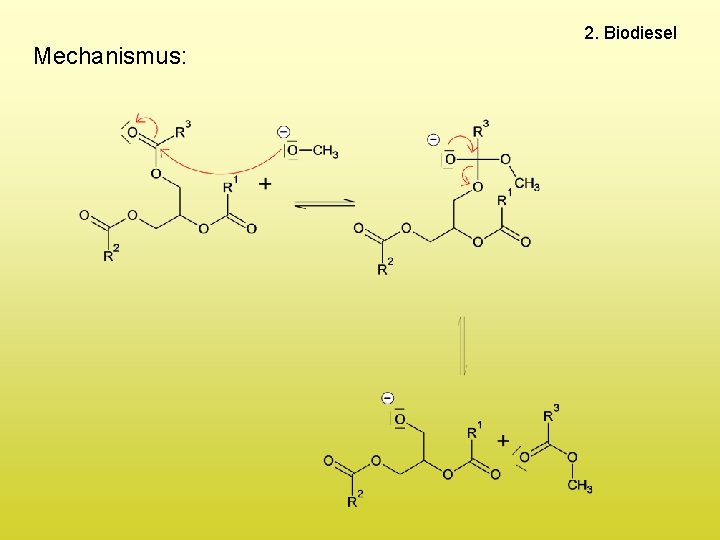
Mechanismus: 2. Biodiesel

2. Biodiesel

2. Biodiesel • Umesterung ist eine Gleichgewichtsreaktion (ca. 25 % nicht-umgesetztes Rapsöl in Versuch 1) • industriell: CD-Verfahren (continuously deglycerolizing)

2. Biodiesel Warum Umesterung? - Absenkung der Cetanzahl (Maß für die Zündwilligkeit) - RME hat geringere Viskosität als Rapsöl

Demo 1 Vergleich der Viskositäten

2. Biodiesel • Literaturwerte: Kraftstoff Diesel Biodiesel Rapsöl kinematische Viskosität [ in mm 2/s, bei 40 °C] 2, 0 -4, 5 3, 5 -5, 0 38

Demo 2 Verbrennung von Diesel bzw. Biodiesel

2. Biodiesel Zwischenbilanz Vorteile Biodiesel gegenüber Diesel 1. regenerativ (je nach Quelle 30 -80 % CO 2 Verringerung) 2. Verringerung Ruß-Emissionen (bis zu 50 %) 3. Biodiesel ist schwefelarm 4. Biodiesel besser umweltverträglich

2. Biodiesel Nachteile Biodiesel gegenüber Diesel 1. geringerer Heizwert als Diesel 2. in Biodiesel kann sich Wasser lösen → Korrosionsprobleme 3. teure Herstellung

3. Bioethanol

3. Bioethanol • Verwendung von Bioethanol als Treibstoff - rein - in Gemischen mit Benzin, z. B. a) bis 5 Vol. -% schon heute in Deutschland im Otto. Kraftstoff möglich b) E 85 (85 Vol-% Et. OH, 15 Vol-% Benzin)

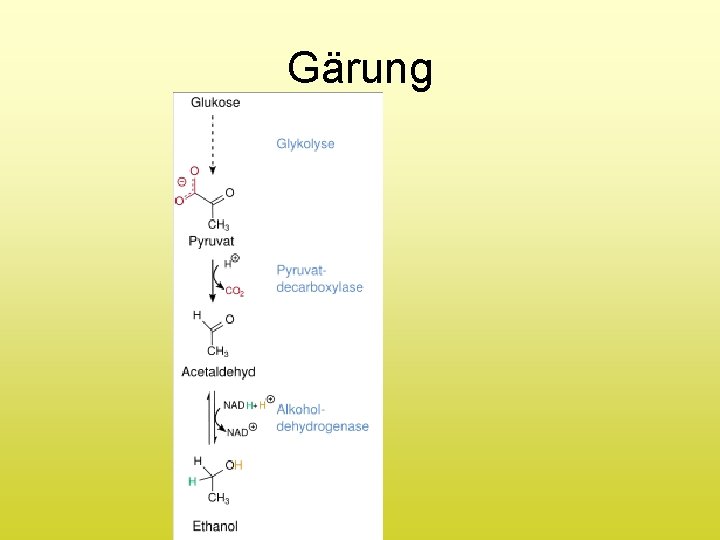
3. Bioethanol Ethanol-Produktion 1. Vergärung von zucker- bzw. stärkehaltigen Pflanzen - evtl. Spaltung der Stärke - Vergärung

3. Bioethanol 2. Destillation → hochprozentiges Ethanol (bis max. 97 Vol - % Et. OH, azeotropes Gemisch mit Wasser)

3. Bioethanol 3. Absolutierung als Treibstoff wird 99, 5 -99, 8 %iger Alkohol benötigt, letzter Wasserentzug durch a) Schleppmittelverfahren b) Membranverfahren c) Molekularsiebverfahren

3. Bioethanol Versuch 2 Wasserentzug durch Molekularsieb
![Bestimmung des Ethanolanteils mithilfe einer Dichtetabelle Dichte 20 C gm L 3 • Bestimmung des Ethanolanteils mithilfe einer Dichtetabelle Dichte (20 °C) [g/m. L] 3.](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-26.jpg)
• Bestimmung des Ethanolanteils mithilfe einer Dichtetabelle Dichte (20 °C) [g/m. L] 3. Bioethanol Vol-% Ethanol 0, 81942 0, 81674 0, 81401 93, 2 94 94, 7 0, 81127 0, 80848 0, 80567 0, 8028 0, 79988 0, 79688 0, 79383 0, 79074 95, 4 96, 1 96, 7 97, 4 98, 1 98, 7 99, 3 100

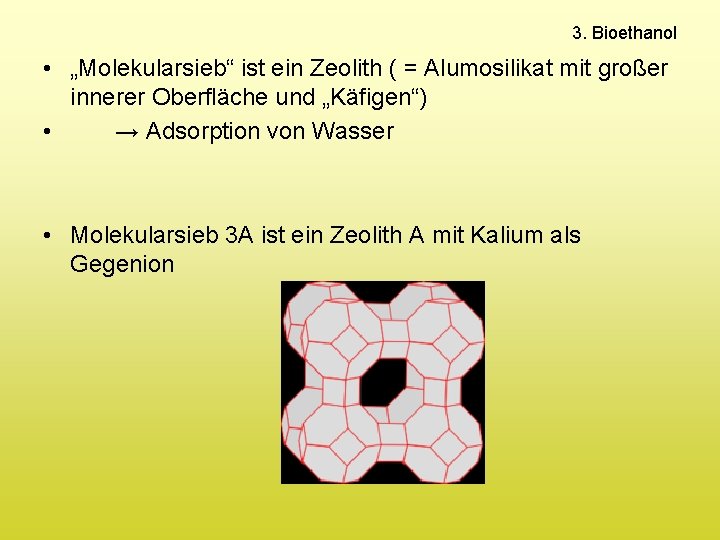
3. Bioethanol • „Molekularsieb“ ist ein Zeolith ( = Alumosilikat mit großer innerer Oberfläche und „Käfigen“) • → Adsorption von Wasser • Molekularsieb 3 A ist ein Zeolith A mit Kalium als Gegenion
![3 Bioethanol Erträge von Ethanol Lha 3. Bioethanol Erträge von Ethanol [L/ha]](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-28.jpg)
3. Bioethanol Erträge von Ethanol [L/ha]

3. Bioethanol 2. -größter Bioethanol-Produzent: Brasilien - 34 % der Weltproduktion (2006) - 40 % des Kraftstoffbedarfs durch Ethanol gedeckt - 50 % aller PKW fahren mit E 85

Versuch 3 Explosion eines E 85 Luftgemisches

3. Bioethanol analoge Explosion findet im Otto-Motor statt: Benzin (Hautbestandteil Alkane, n ≈ 5 -11): Ethanol:

4. Bt. L-Kraftstoffe

4. Bt. L-Kraftstoffe • Bt. L (Biomass to Liquid) -Kraftstoffe: - synthetische Kraftstoffe - ausgehend von Synthesegas (Gemisch von CO/H 2, aus Kohle oder Holz, neuerdings auch Biomasse aller Art) • Synthese von Kohlenwasserstoffen nach der Fischer. Tropsch-Synthese (1925)

4. Bt. L-Kraftstoffe • bereits im 2. Weltkrieg zur Treibstoffversorgung angewendet, Synthesegas aus Kohle • heutige Bestrebungen: Synthesegas aus nachwachsenden Rohstoffen (Holz, andere Biomasse)

Versuch 4 Holzvergasung

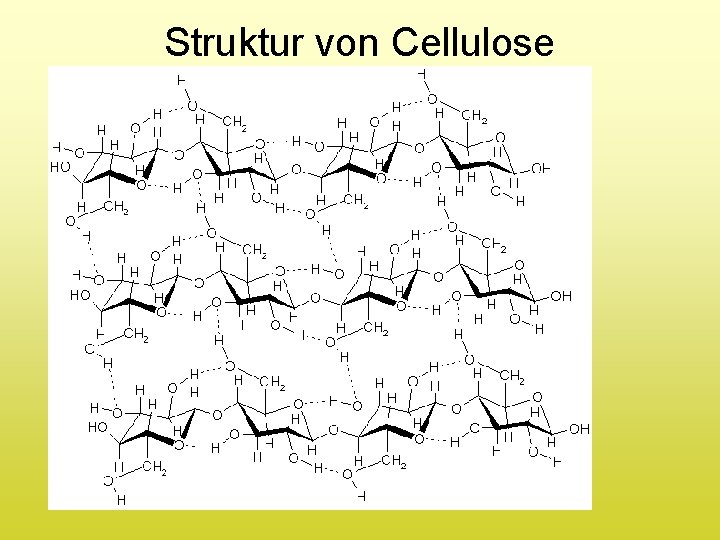
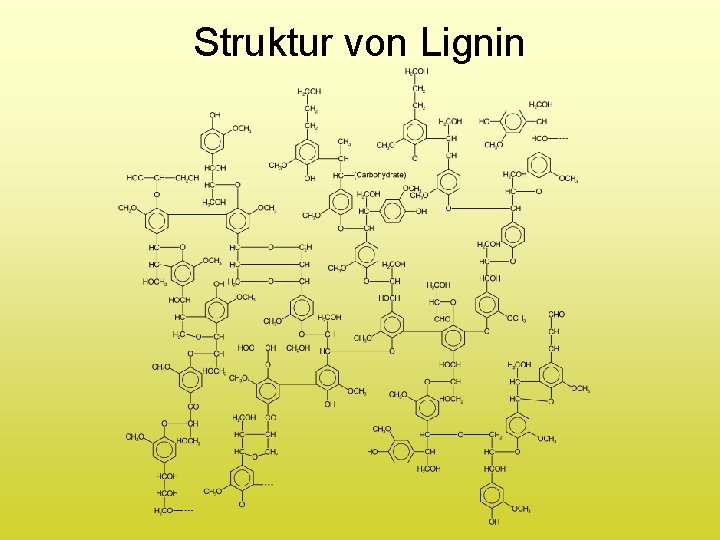
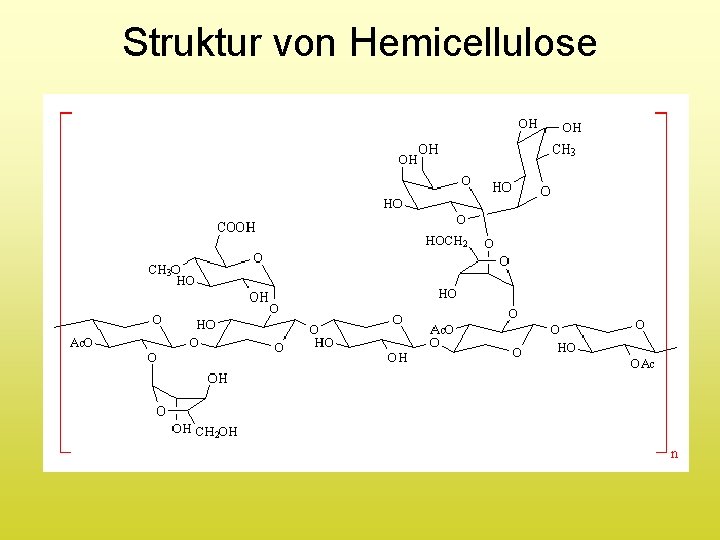
4. Bt. L-Kraftstoffe wichtigste Holzbestandteile 1. Cellulose (35 %) Polysaccharide 2. Hemicellulose (20 %) 3. Lignin (20 %) 4. Wasser (25 %) (unregelmäßiges Phenol-Polymer)


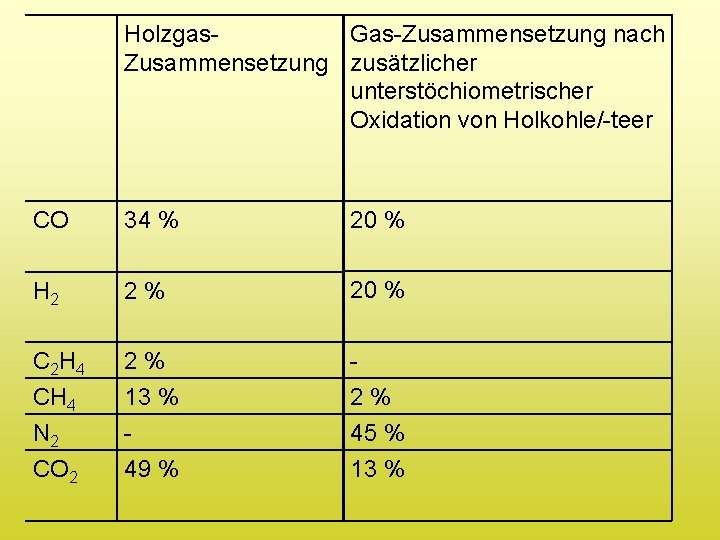
4. Bt. L-Kraftstoffe • unter Luftausschluss wird Holz zu a) Holzgas (gasförmig) b) Holzgeist (flüssig) c) Holzkohle/Holzteer (fest) pyrolysiert • die Holzvergasung kann wie folgt beschrieben werden:

Holzgas. Gas-Zusammensetzung nach Zusammensetzung zusätzlicher unterstöchiometrischer Oxidation von Holkohle/-teer CO 34 % 20 % H 2 2% 20 % C 2 H 4 CH 4 N 2 CO 2 2% 13 % 49 % 2% 45 % 13 %

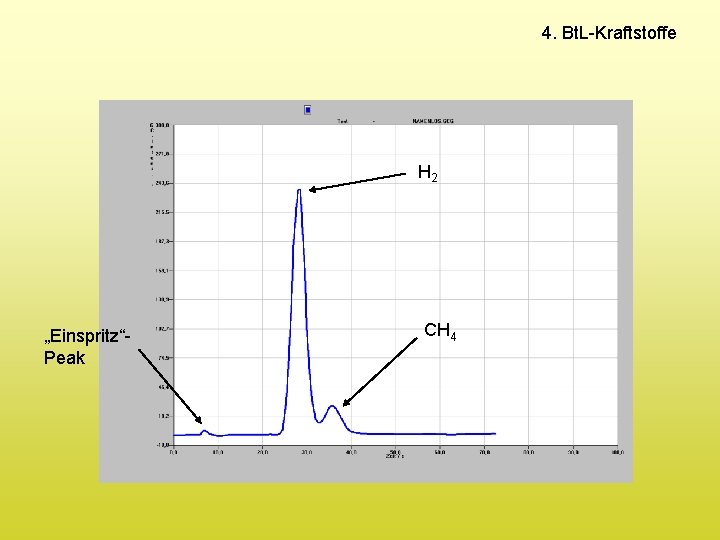
Versuch 5 Fischer-Tropsch-Synthese

4. Bt. L-Kraftstoffe H 2 „Einspritz“Peak CH 4

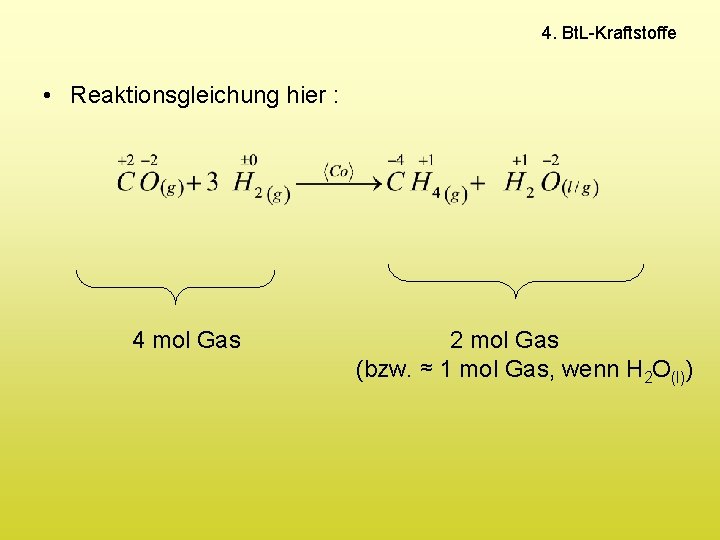
4. Bt. L-Kraftstoffe • Reaktionsgleichung hier : 4 mol Gas 2 mol Gas (bzw. ≈ 1 mol Gas, wenn H 2 O(l))

4. Bt. L-Kraftstoffe • allgemeine Reaktionsgleichung der Fischer-Tropsch. Synthese (Hauptprodukt: n-Alkane): • hier eigentlich nur Vorgänger-Reaktion der FTS, da kein Kettenwachstum

4. Bt. L-Kraftstoffe (möglicher) Mechanismus der Reaktion:

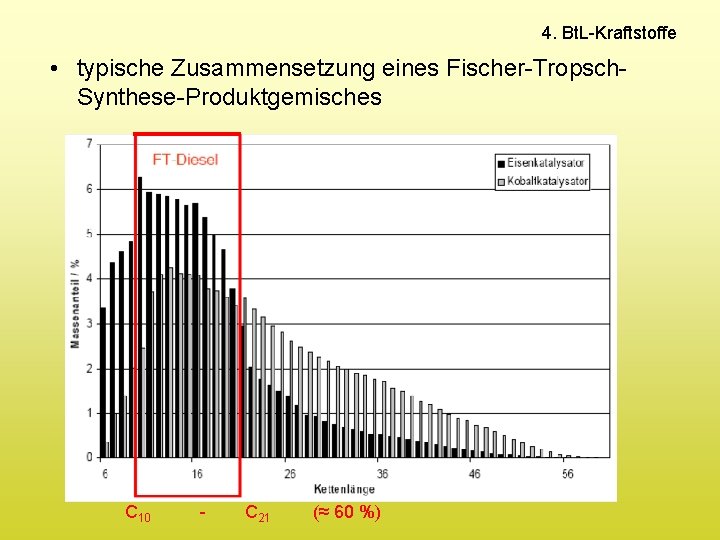
4. Bt. L-Kraftstoffe • typische Zusammensetzung eines Fischer-Tropsch. Synthese-Produktgemisches C 10 - C 21 (≈ 60 %)

4. Bt. L-Kraftstoffe Franz Fischer in seinem Labor (1918)

5. Kurzes Fazit • fossile Kraftstoffe werden mittel- bis längerfristig knapper • Biokraftstoffe besserer CO 2 -Gesamthaushalt als fossile Kraftstoffe, gewisse Emissionen vorteilhafter als bei fossilen Kraftstoffe • aber kein „geschlossener“ CO 2 -Kreislauf

5. Kurzes Fazit
![5 Kurzes Fazit Herstellungskosten der Kraftstoffe in L Kraftstoffäquivalent Nettopreis bei 61 Dollar 5. Kurzes Fazit • Herstellungskosten der Kraftstoffe [in €/L Kraftstoffäquivalent] *Nettopreis bei 61 Dollar](https://slidetodoc.com/presentation_image_h2/6763c189b072dfe9d7c61a7067cb5086/image-49.jpg)
5. Kurzes Fazit • Herstellungskosten der Kraftstoffe [in €/L Kraftstoffäquivalent] *Nettopreis bei 61 Dollar je Barrel Rohöl (Brent)

5. Kurzes Fazit • Biotreibstoffe oft mit Nahrungsmittelproduktion eng verkettet (z. B. Anstieg des Weltmarktpreises von Mais um 80 % in 2006 → Massendemonstrationen in Mexiko wegen Preisanstieg für Zutat Maismehl für Volksspeise Tortilla)

5. Kurzes Fazit • teilweise ökologische Aspekte sehr fragwürdig (z. B. Abholzung des Regenwaldes zum Anbau von Ölpalmen für Palmöl-Produktion in Indonesien)

6. Schulrelevanz • allgemein Regenerative Energien sehr aktuell • praxisnahes Thema • Behandlung von Ökobilanzen ermöglicht Hinterfragen von Umweltschutz-Konzepten • schöne fächerübergreifende Zusammenhänge zwischen Geschichte, Politik, Chemie (Fischer-Tropsch)

6. Schulrelevanz Hessischer Lehrplan G 8 • 9 G. 3: - Erdöl etc. • 10 G: - Alkanole - fakultativ: Alkohole als Treibstoffzusatz

6. Schulrelevanz • 11 G. 1: - Mechanismus der Esterbildungund -verseifung, mehrwertige Alkohole (Glycerin) • 11 G. 2: - Fette • 12 G. 2: - Wahlthema Angewandte Chemie (u. a. „Vom Raps zum Biodiesel“)

„Drink the best and drive the rest!“ Danke für Ihre Aufmerksamkeit!


Gärung

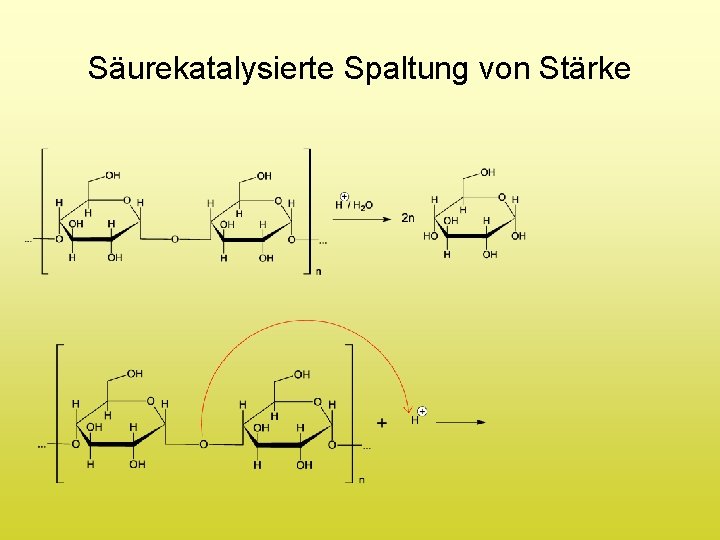
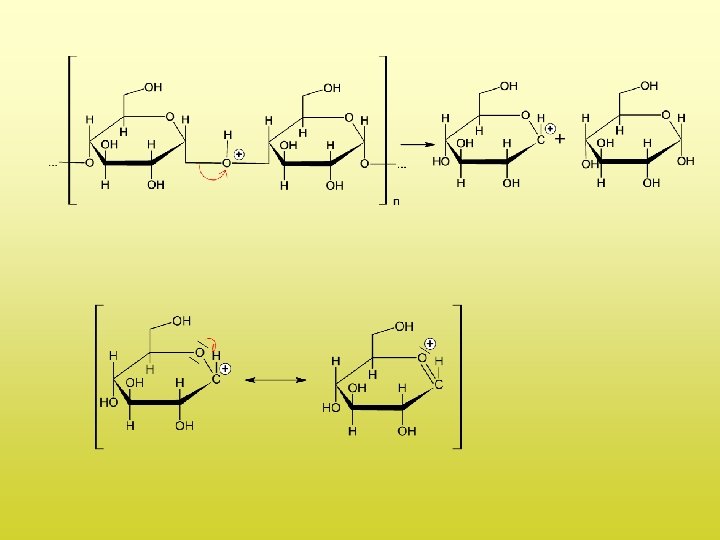
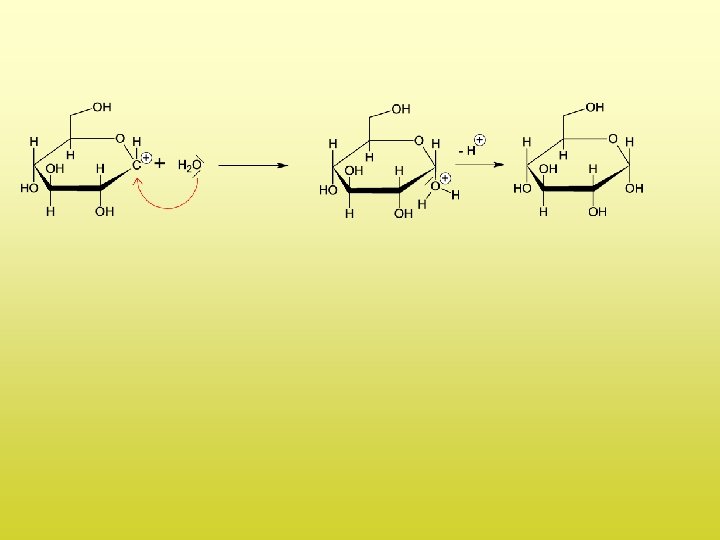
Säurekatalysierte Spaltung von Stärke



Struktur von Cellulose

Struktur von Lignin

Struktur von Hemicellulose

