Preinvazif Endometrial Patolojiler Dr Tayfun GNGR Hitit niversitesi





























![D skoru D=0, 6229+(0, 0439 x. VPS)-[3, 9934 xln(SDSNA)]- (0, 1592 x. OSD) VPS D skoru D=0, 6229+(0, 0439 x. VPS)-[3, 9934 xln(SDSNA)]- (0, 1592 x. OSD) VPS](https://slidetodoc.com/presentation_image_h2/69e32971fbcbc9b353bd253c61a4df73/image-40.jpg)






- Slides: 49

Preinvazif Endometrial Patolojiler Dr. Tayfun GÜNGÖR Hitit Üniversitesi Kadın Hastalıkları ve Doğum & Zekai Tahir Burak Kadın Sağlığı EAH Jinekolojik Onkoloji

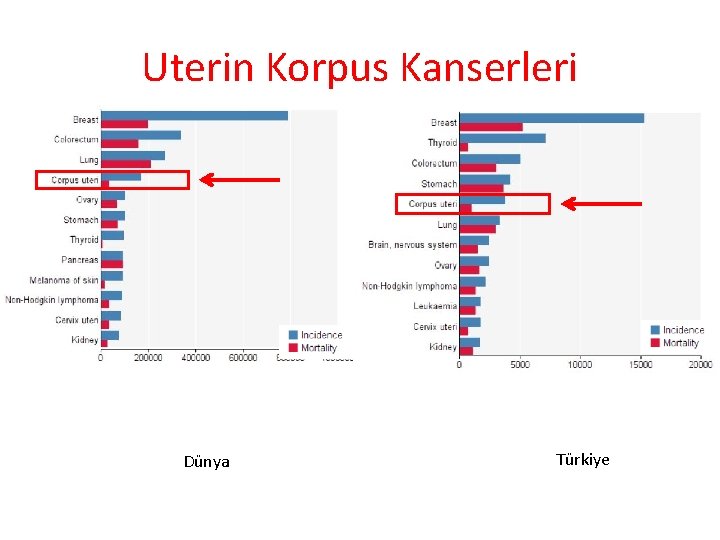
Uterin Korpus Kanserleri Dünya Türkiye

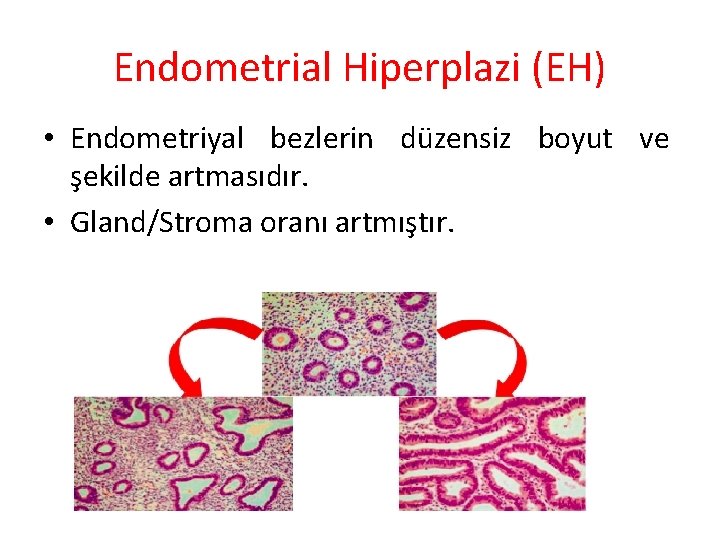
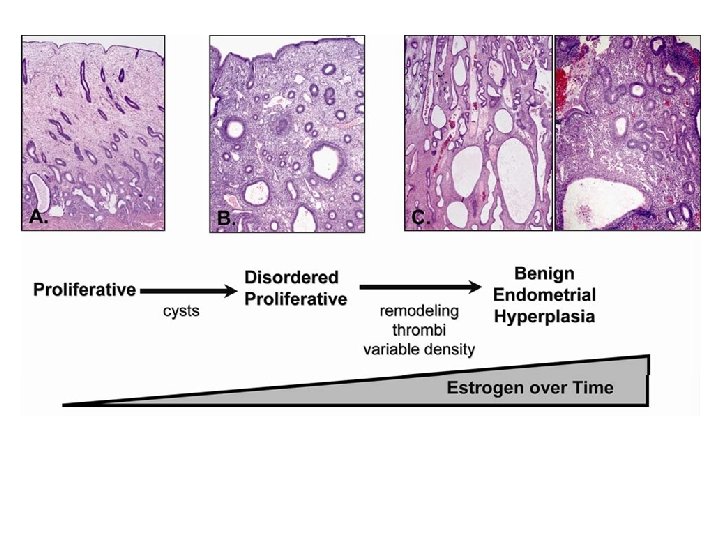
Endometrial Hiperplazi (EH) • Endometriyal bezlerin düzensiz boyut ve şekilde artmasıdır. • Gland/Stroma oranı artmıştır.

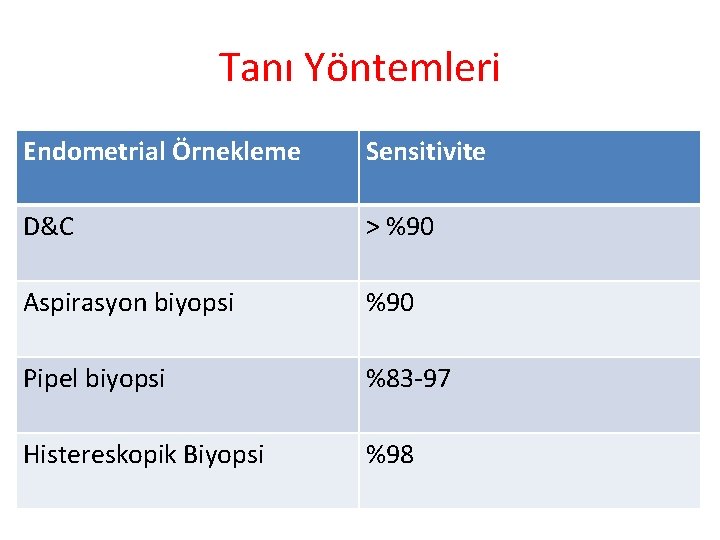
Tanı Yöntemleri Endometrial Örnekleme Sensitivite D&C > %90 Aspirasyon biyopsi %90 Pipel biyopsi %83 -97 Histereskopik Biyopsi %98

Tanı • İki ofiste yetersiz materyalde D&C • İlk yetersiz materyalde ofis veya D&C • Benign bulgularda kanama sürerse 3 -6 ay sonra tekrar D&C • Persiste kanamalarda Ca riski %4 -21 Twu NF 2000 Runghe R 2010


Endometrial Hiperplazi • Semptomatik (AUK) – Menoraji ve/veya metroraji – Post menapozal kanama • Prevalans ? • 133/100. 000 kadın yılı – AUK’lı hastalarda %1, 5 -15 – Histerektomide %5 • Atipisiz EH 50 -54 yaş • Atipili EH 60 -64 yaş • Risk faktörleri Tip I End. Ca ile aynı

EH Risk Faktörleri • Karşılanmamış östrojenli menopozda hormon tedavisi • Anovulasyon • Obezite • Östrojen salgılayan tümörler • Tamoksifen tedavisi • Diabet • Nulliparite

EH Koruyucu Faktörleri • • • Multiparite Normal BMI Kombine oral kontraseptif kullanımı Progesteron tedavisi 49 yaşından önce menopoz

EH açısından değerlendirilmesi gereken grup • >40 yaş AUK • <40 yaş AUK ve Hiperestrojenik durum (Anovulasyon, obezite, DM, PKOS) • Medikal tedaviye yanıtsız her tür AUK • Karşılanmamış postmenopozal östrojen replasman tedavisi • PAP Smear’da Atipik glandüler hücre • (%3 endometrial kanser riski) • >40 yaş pap smearde Endometrial hücre varlığı • Herediter non-polipozis kolorektal kanseri olan hastalar

EH Kullanılan Sınıflandırmalar • WHO 1994 • EİN 2000 • WHO 2014

WHO 1994 – En yaygın kullanılan sınıflama. – Endometriyal karsinomaya progresyon için uyumlu. • • Basit atipisiz Kompleks atipisiz Basit atipili Kompleks atipili (%1) (%3) (%8) (%29) Kurman RJ 1985

Hiperplazi- Kanser Progresyonu • Atipisiz hiperplazi – 10 yıl • Atipili hiperplazi – 4 yıl • Kansere progesyon: – premenapozal %3 – postmenapozal %25 • Atipisiz EH spontan regrese • Kompleks atipik hiperplazi persiste

Yönetimde Etkili Faktörler • Atipi ve ve buna bağlı malignite potansiyeli • Hastanın yaşı ve fertilite arzusu • Genel sağlık durumu • Over tümörüyle birlikteliği • Hastanın arzusu • Birlikte diğer jinekolojik patolojiler

Tedavi Seçenekleri • Ekspektan • Medikal • Cerrahi

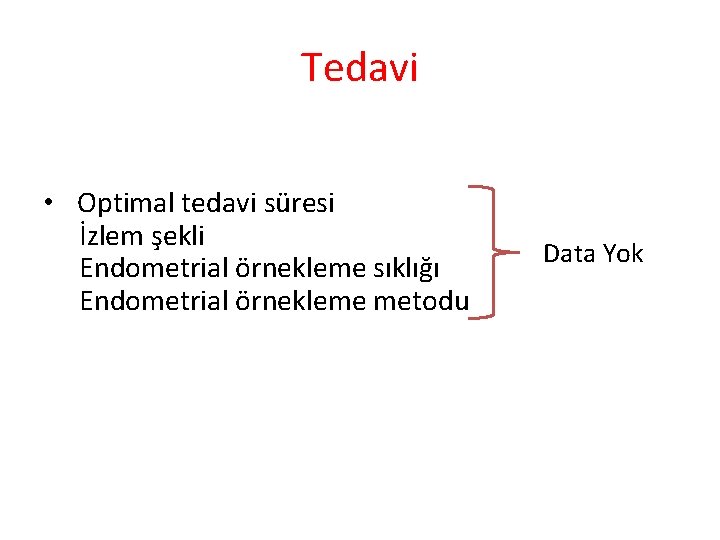
Tedavi • Optimal tedavi süresi İzlem şekli Endometrial örnekleme sıklığı Endometrial örnekleme metodu Data Yok

Ekspektan Yaklaşım • Endikasyonları: • Atipisiz • Asemptomatik hasta • Progesteron kontrendike • PR reseptör (+) meme Ca • Tromboz riski • Progesteronla yan etki • • Anksiyete, irritabilite, depresyon Tromboemboli Ciddi ödem, şişlik hissi Başağrısı • 6 -12 ayda kontrol USG ve Bx • %70 Regresyon Reed SD, Obstet Gynecol 2009

Medikal Yaklaşım • Progestinlerde etki mekanizması: • Östrojenin mitojenik etkilerini antagonize eder • Östrojen reseptörleri • Hidroksilaz aktivasyonu • Estradiol estron • Apoptozu indükler • Stromal desidüalizasyon • Endometrial atrofi • • Doz? Tedavi süresi? Tercih edilen progestin? Progestinin kullanım yolu?

Tedavi Seçenekleri (Medikal) • Progestinler • Medroksiprogesteron asetat (MPA); Farlutal® • Megesterol Asetat Megace® • Mikronize progesteron; – Oral Progestan® – Vaginal Cyclogest® • Oral Kontraseptifler (OK) • Ovulasyon indüksiyonu (OI) • Levonorgestrel içeren IU system • Danazol • Gn. RH analogları • Aromataz inhibitörleri

MPA • En sık tercih edilen preperat – 5 -10 mg oral (14 gün/ay) – Devamlı kullanım (siklik kanama yok) • 3 -6 ay tedavi • %80 -90 regresyon • Regresyon olana kadar 3 -6 ay aralıkla örnekleme • 3 -6 ay sonrası regresyon yoksa yüksek doz tedavi yada cerrahi

MPA • Siklik rejim (10 mg – 12/14 gün) • 7 gün tedavi %81 reg. • 10 gün tedavi %98 reg. • 13 gün tedavi %100 reg. En az 10 gün kullanılmalıdır Gambrel RD 1995

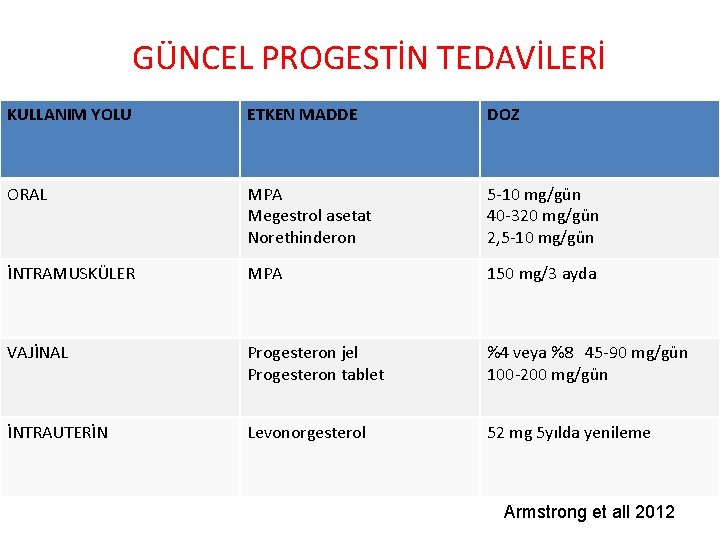
GÜNCEL PROGESTİN TEDAVİLERİ KULLANIM YOLU ETKEN MADDE DOZ ORAL MPA Megestrol asetat Norethinderon 5 -10 mg/gün 40 -320 mg/gün 2, 5 -10 mg/gün İNTRAMUSKÜLER MPA 150 mg/3 ayda VAJİNAL Progesteron jel Progesteron tablet %4 veya %8 45 -90 mg/gün 100 -200 mg/gün İNTRAUTERİN Levonorgesterol 52 mg 5 yılda yenileme Armstrong et all 2012

LNG içeren RİA • Sistemik verilenden daha düşük dozda progesteron ile daha potent etki sağlanır • Estrojen ve progesteron reseptörlerinde down regulasyon ile endometrial baskılama • Daha iyi hasta uyumu • 14 ve 20 mcg/gün salınım yapan tipleri var

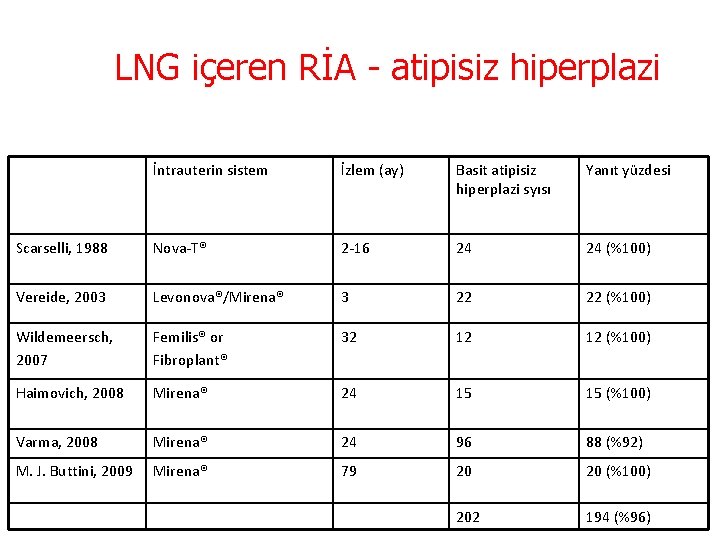
LNG içeren RİA - atipisiz hiperplazi İntrauterin sistem İzlem (ay) Basit atipisiz hiperplazi syısı Yanıt yüzdesi Scarselli, 1988 Nova-T® 2 -16 24 24 (%100) Vereide, 2003 Levonova®/Mirena® 3 22 22 (%100) Wildemeersch, 2007 Femilis® or Fibroplant® 32 12 12 (%100) Haimovich, 2008 Mirena® 24 15 15 (%100) Varma, 2008 Mirena® 24 96 88 (%92) M. J. Buttini, 2009 Mirena® 79 20 20 (%100) 202 194 (%96)

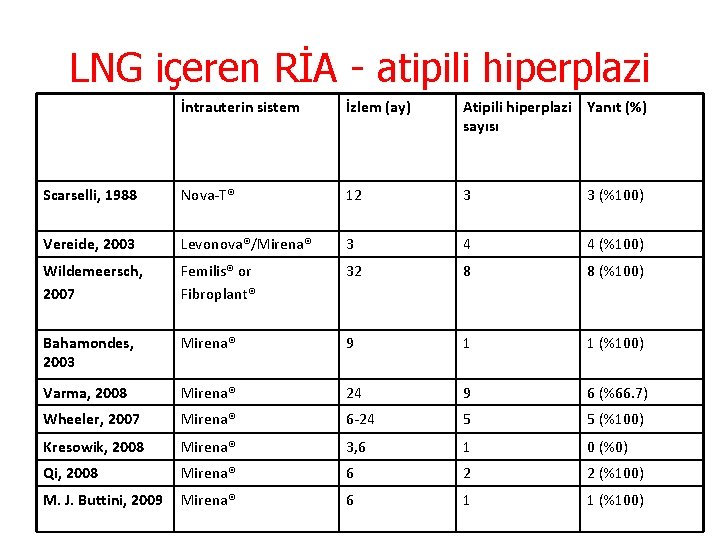
LNG içeren RİA - atipili hiperplazi İntrauterin sistem İzlem (ay) Atipili hiperplazi Yanıt (%) sayısı Scarselli, 1988 Nova-T® 12 3 3 (%100) Vereide, 2003 Levonova®/Mirena® 3 4 4 (%100) Wildemeersch, 2007 Femilis® or Fibroplant® 32 8 8 (%100) Bahamondes, 2003 Mirena® 9 1 1 (%100) Varma, 2008 Mirena® 24 9 6 (%66. 7) Wheeler, 2007 Mirena® 6 -24 5 5 (%100) Kresowik, 2008 Mirena® 3, 6 1 0 (%0) Qi, 2008 Mirena® 6 2 2 (%100) M. J. Buttini, 2009 Mirena® 6 1 1 (%100)

TAKİP • • Örnekleme için Tedavi başladıktan 3 ay sonra ilk bx. 3 ayda bir end bx. Biyopsi için geri çekilme kanaması beklenebilir. (2 -6 hf) • Progesteron reseptör düzeyi önemlidir. • Regresyon sonrası idame tedavi verilir. YÖNTEM: – Ofis prosedürü (pipel) – D&C (LNG-IUD yerinde iken örnek alınabilir. ) Scorselli G 2011 Gunderson CC 2012

Tedavi Seçenekleri (Cerrahi) • Özellikle atipili olgularda tercih edilir • Atipili Endometrial hiperplazi olgularında kanser oranı % 17 -62 • Frozen patoloji imkanı olan yer tercih edilmeli (%75) • Evreleme cerrahisi yapılabilen yerlerde tedavi yapılmalıdır.

Tedavi Seçenekleri (Cerrahi) • Histerektomi (Tip I) – Subtotal histerektomi önerilmez – İntraoperatif değerlendirme ve frozen • Endometrial ablasyon veya rezeksiyon önerilmez. • Tedavi sonrası takip gerektirmez.

BSO Postmenopozal • • Tartışmalı %17 -52 eşlik eden end. Ca %5 over tutulumu Ameliyatta kesin değerlendirme yapılamaz İkinci operasyonu önler. Yaklaşık %50 -80 gereksizdir. Uzun süreli riskler. Creasman WT 1987 Indermaur MD 2007 Attard MS 2008

BSO Premenopozal • Senkron primer veya metastatik durumlar daha sık (%25) • Menopozal yakınmalar • HRT tartışmalı Indermaur MD 2007

Önleyici Tedavi • Kronik anovulasyon – PCOS • Kombine OK, • Intemittant veya sürekli progesteron – MPA – Mikrojenize progesteron – Depo MPA – LNG

WHO Sınıflaması Limitasyonları • Subjektif diagnostik kriterler • Tanıda zorluklar • Belirgin intraobserver değişkenlikler ve interobserver – Atipi mevcudiyeti – Kompleks ve iyi diff. End. Ca ayrımı Usubutun A, 2000

Endometrial İntraepitelyal Hiperplazi (EIN) • Tip I Endomerial kanser prekürsör lezyonu – Karşılanmamış E 2 • • Görülme insidansı %1. 4 Ortalama tanı yaşı 53 EIN tanısı sonrası Ca. gelişme süresi : 4 yıl Histerektomi dışı tedavilerde eş zamanlı endometrial kanser varlığı ekarte edilmelidir.

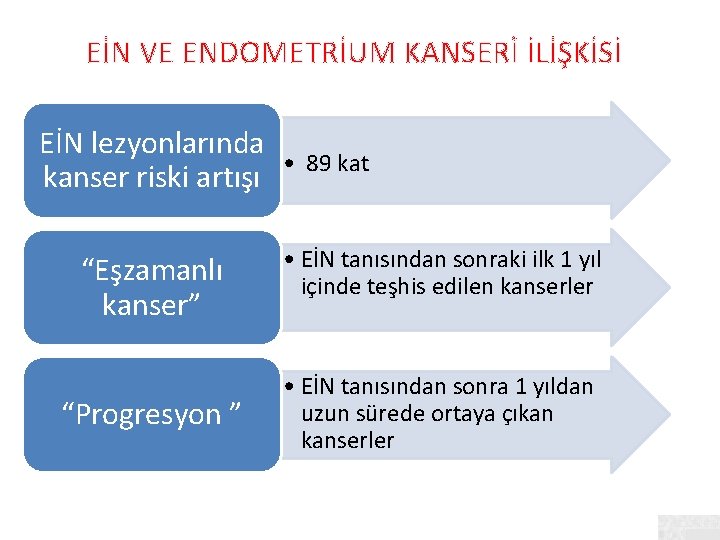
EİN VE ENDOMETRİUM KANSERİ İLİŞKİSİ EİN lezyonlarında kanser riski artışı “Eşzamanlı kanser” “Progresyon ” • 89 kat • EİN tanısından sonraki ilk 1 yıl içinde teşhis edilen kanserler • EİN tanısından sonra 1 yıldan uzun sürede ortaya çıkan kanserler

EIN • Bazı merkezler dışında kullanılmıyor. • Ölçüm ve uygulama için tecrübe ve eğitim. • WHO’ya göre interobserver varyans daha azdır. intraobserver • Interobserver %75 • Intraobserver %93 • EIN kanser progresyonunu WHO ya göre daha iyi tahmin eder.

EIN sistemine göre EH’lerde farklı yaklaşım gerektiren iki kategori 1. Anormal hormonal uyarıya diffüz yanıt veren NORMAL POLİKLONAL endometriyum. ØEH (benign EH) 2. Artmış adenokanser riski ile ilişkili olan ve fokal gelişen MONOKLONAL lezyon ØEIN

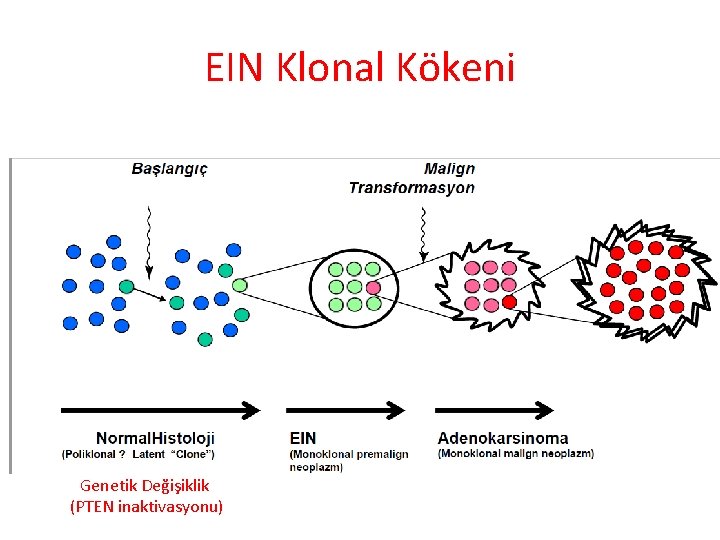
Endometrial Karsinogenez Ø PTEN geni (10. kromozom) Ø Östrojenden zengin mitotik ortamda en fazla ekspresyon Ø Hücre bölünmesinin kontrolü Ø PTEN mutasyonu Ø Sık (endometrioid tipte en sık genetik değişiklik) Ø Erken (endometrial karsinogenezde en erken aşama PTEN negatif glandlar) Ø Östrojen ile PTEN mutant hücrelerde klonal genişleme Ø EH EIN Ø EIN’de 2/3 PTEN mutasyonu Ø Premalign lezyon belirteci olarak kullanılabilir

EIN Klonal Kökeni Genetik Değişiklik (PTEN inaktivasyonu)

EIN Tanı Yöntemleri Moleküler testler – Monoklonalite – X kromozomu inaktivasyonu – Mikrosatellit instabilitesi – PTEN mutasyonu (10. kromozom) – Endometrial karsinogenezde en erken aşama PTEN negatif glandlar Bilgisayar sistemleri – Yapısal ve hücresel özellikler – D skoru
![D skoru D0 62290 0439 x VPS3 9934 xlnSDSNA 0 1592 x OSD VPS D skoru D=0, 6229+(0, 0439 x. VPS)-[3, 9934 xln(SDSNA)]- (0, 1592 x. OSD) VPS](https://slidetodoc.com/presentation_image_h2/69e32971fbcbc9b353bd253c61a4df73/image-40.jpg)
D skoru D=0, 6229+(0, 0439 x. VPS)-[3, 9934 xln(SDSNA)]- (0, 1592 x. OSD) VPS = Volume percentage stroma – Gland ve stroma oranı – %55’in altı anormal olup glandlar artmıştır OSD = Outer surface density – Glandların dallanma derecesini gösterir SDSNA = Standard deviation of shortest nuclear axis – Nükleer varyasyon

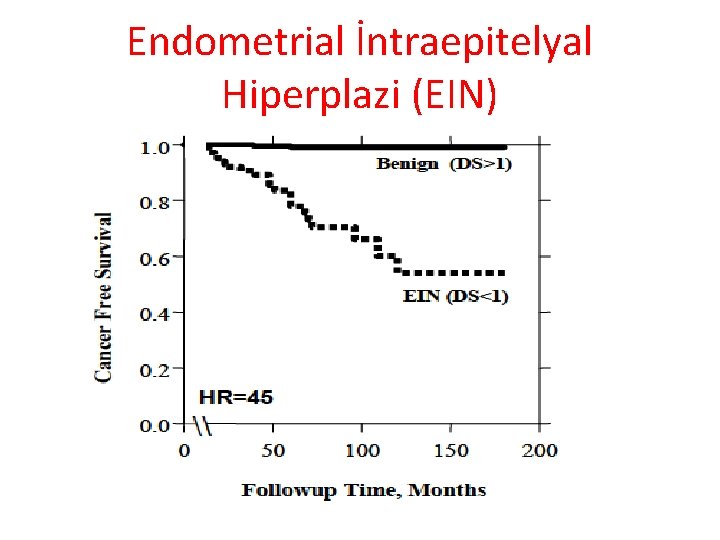
D skoru • D-skoru; (-4, +4) – ≥ 1 Benign EH (düşük Ca riski) – <1 EIN (yüksek Ca riski) Sensitivite ve NPV %100 Bu skorlama klonalite analizi ile de oldukça paralel sonuçlar verir. • D-skoru ≥ 1 %5 monoklonal • D-skoru <1 %75 monoklonal

Endometrial İntraepitelyal Hiperplazi (EIN)

EIN • Daha objektif ve daha prognostik • Lezyonun prekanser olması ile ilişkili en önemli bulgu atipinin varlığıdır. • D-skorlama özel ekipman ve çok iyi eğitilmiş personel gerektirmektedir. • Tecrübeli jinekopatolog gerektirir. • Objektif ve subjektif EIN kriterleri arasında yüksek derecede uyum vardır.

EIN Subjektif Tanı Kriterleri Kriter Yapı Yorum Gland/stroma oranı >1 • EIN’in subjektif tanı kriterleri Sitoloji Glandların yoğunlaştığı alanla geri kalan endometrium arasında hücresel farklılık (sitolojik demarkasyon) Boyut Tek bir odakta maksimum lineer çap >1 mm Benzer lezyonların Disordered proliferatif endometrium, sekretuar endometrium, bazal ekartasyonu endometrium, alt uterin segment, polipler ve onarım ayırdedilir Kanserin ekartasyonu İleri derecede dallanmış glandlar, solid alanlar ve belirgin kribriform yapı varsa kanser tanısı konur Tanı için tamamı mevcut olmalıdır. Progesteron kullanımı belirtilmelidir. Mutter GL, 2007

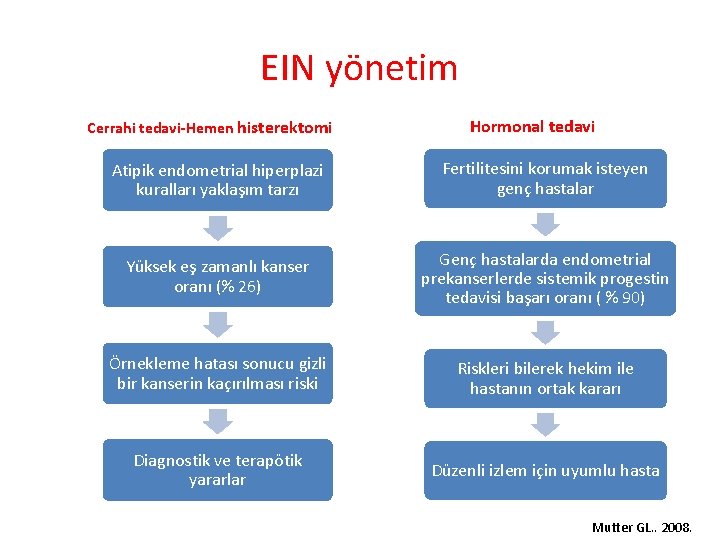
EIN yönetim Cerrahi tedavi-Hemen histerektomi Hormonal tedavi Atipik endometrial hiperplazi kuralları yaklaşım tarzı Fertilitesini korumak isteyen genç hastalar Yüksek eş zamanlı kanser oranı (% 26) Genç hastalarda endometrial prekanserlerde sistemik progestin tedavisi başarı oranı ( % 90) Örnekleme hatası sonucu gizli bir kanserin kaçırılması riski Riskleri bilerek hekim ile hastanın ortak kararı Diagnostik ve terapötik yararlar Düzenli izlem için uyumlu hasta Mutter GL. . 2008.

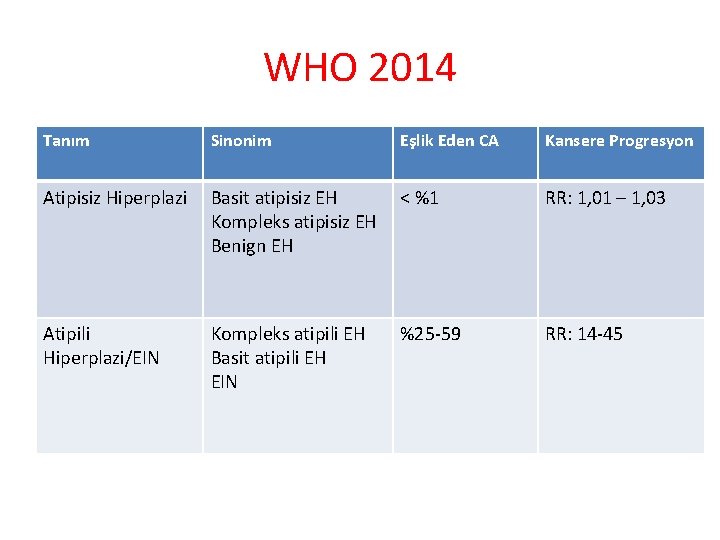
WHO 2014 Tanım Sinonim Eşlik Eden CA Kansere Progresyon Atipisiz Hiperplazi Basit atipisiz EH Kompleks atipisiz EH Benign EH < %1 RR: 1, 01 – 1, 03 Atipili Hiperplazi/EIN Kompleks atipili EH Basit atipili EH EIN %25 -59 RR: 14 -45

ACOG ÖNERİLERİ (2015) • EIN terminolojisi atipili endometrial hiperplazi terminolojisi yerine tercih edilmelidir. • Doku örneklemesi için histereskopi ile örnekleme tercih edilmelidir (Gör ve yönet) • Supraservikal histerektomi, morselasyon, endometrial ablasyon tedavi seçeneği olarak kabul edilmez.

ACOG ÖNERİLERİ (2015) • Cerrahi için kontraendikayon durumunda sistemik ya da lokal progesteron tedavisi kanıtlanmamış ancak alternatif tedavi seçeneğidir. • Cerrahisiz tedavide 3 -6 ay aralıklarla endometrial örnekleme gereklidir (uygun sıklık kesin olarak bilinmemektedir. )

Teşekkürler