LAJU REAKSI Menyatakan besarnya perubahan konsentrasi pereaksi atau
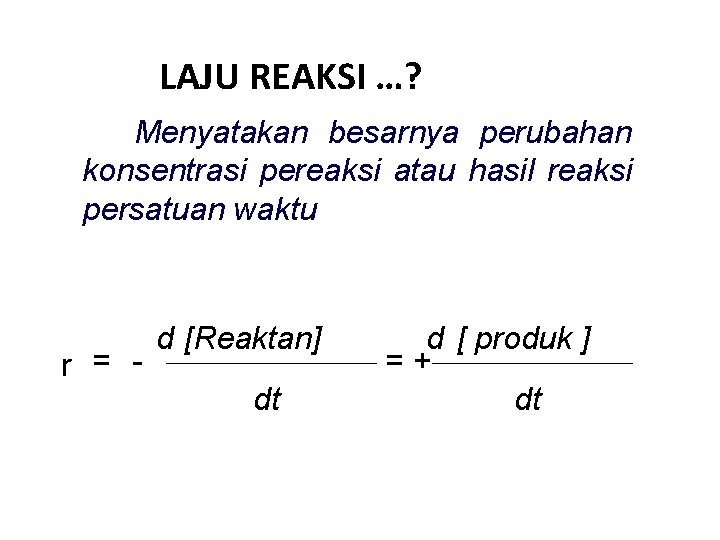
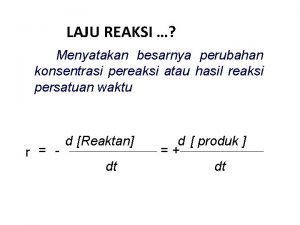
LAJU REAKSI …? Menyatakan besarnya perubahan konsentrasi pereaksi atau hasil reaksi persatuan waktu r = - d [Reaktan] dt d [ produk ] = + dt

2 A + B 3 C + D VA = Laju berkurangnya konsentrasi A persatuan waktu. VB = Laju berkurangnya konsentrasi B persatuan waktu. VC = Laju bertambahnya konsentrasi C persatuan waktu. VD = Laju bertambahnya konsentrasi D persatuan waktu.

SYARAT TERJADINYA REAKSI Reaksi kimia dapat terjadi bila ada tumbukan antara partikel reaktan yang satu dengan yang lain. Tetapi tidak semua tumbukan dapat menghasilkan reaksi. Tumbukan yang menghasilkan reaksi adalah tumbukan efektif.

TEORI TUMBUKAN Reaksi kimia berlangsung sebagai hasil tumbukan antar partikel pereaksi Tumbukan yang menghasilkan reaksi adalah tumbukan yang efektif Ø arah yang tepat Ø energi tumbukan > Ea

Tumbukan efektif memiliki kriteria energi dan posisi tumbukan. Kriteria energi untuk tumbukan efektif adalah memiliki energi cukup atau minimal sama dengan energi aktivasi (pengaktifan / Ea), sedangkan kriteria posisi tumbukan memiliki posisi tumbukan yang menguntungkan untuk terbentuknya suatu produk.

Energi aktivasi, Ea merupakan energi minimal yang dibutuhkan untuk berlangsungnya suatu reaksi (untuk membentuk molekul / kompleks aktif). Energi aktivasi ditafsirkan sebagai energi penghalang (barier) antara pereaksi dan produk. Tumbukan efektif = Tumbukan antar partikel pereaksi yang memiliki energi aktivasi.

Energi aktivasi = energi minimum yang harus dimiliki pereaksi agar tumbukannya dapat menghasilkan reaksi (Tumbukan antar partikel pereaksi yang dapat membentuk komplek teraktivasi). Komplek teraktivasi (intermediate species) = keadaan molekul-molekul yang siap menjadi zat hasil reaksi.

Energi aktivasi tanpa katalis Energi Aktivasi dengan katalis Produk Reaktan Reaksi endoterm ∆H = (+)
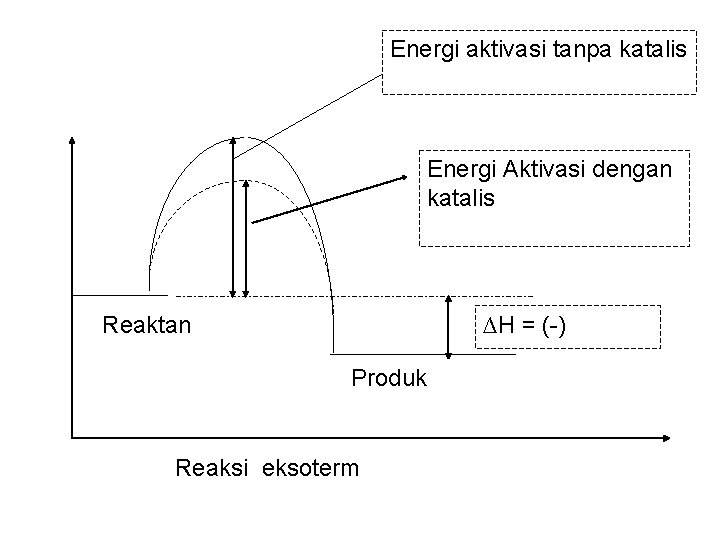
Energi aktivasi tanpa katalis Energi Aktivasi dengan katalis Reaktan ∆H = (-) Produk Reaksi eksoterm
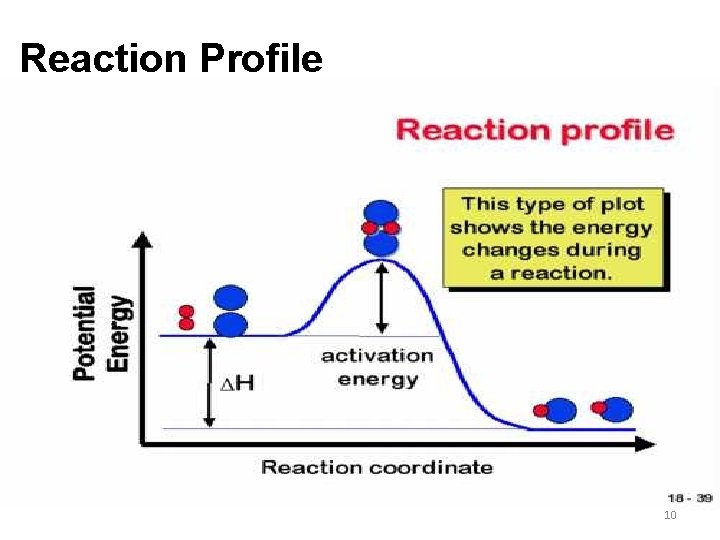
Reaction Profile 10
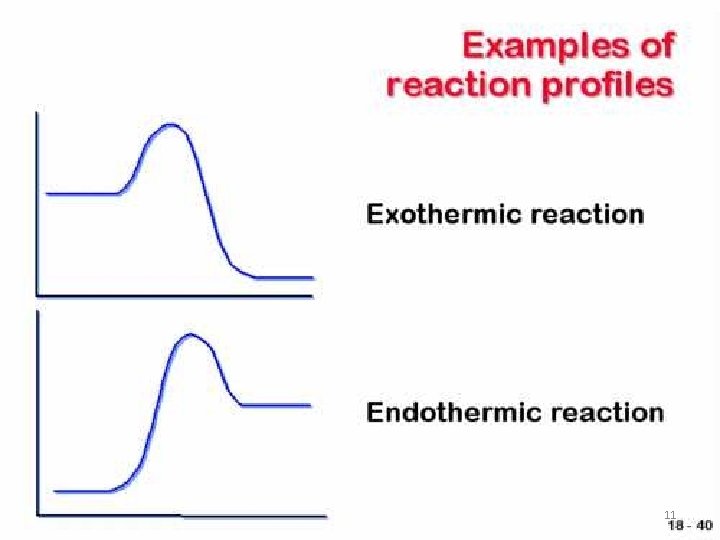
11
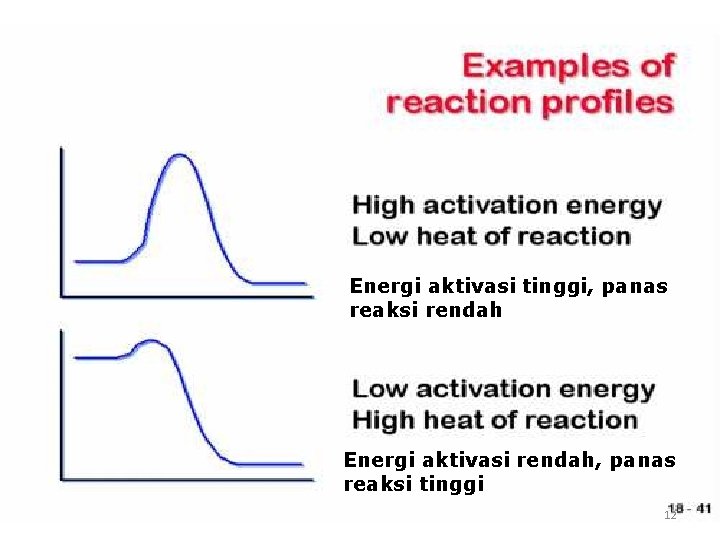
Energi aktivasi tinggi, panas reaksi rendah Energi aktivasi rendah, panas reaksi tinggi 12

PENENTUAN LAJU REAKSI Laju reaksi ditentukan melalui percobaan, yaitu dengan mengukur banyaknya pereaksi yang dihabiskan atau banyaknya produk yang dihasilkan pada selang waktu tertentu. Contoh : Laju reaksi antara Mg dengan HCl dapat ditentukan dengan mengukur jumlah satu produknya, yaitu gas hydrogen Mg (s) + HCl(aq) Mg. Cl 2 (aq) + H 2 (g)
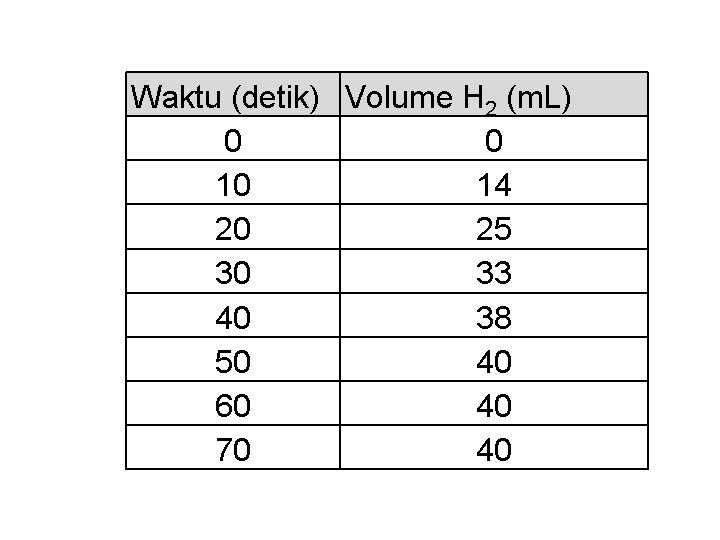
Waktu (detik) Volume H 2 (m. L) 0 0 10 14 20 25 30 33 40 38 50 40 60 40 70 40
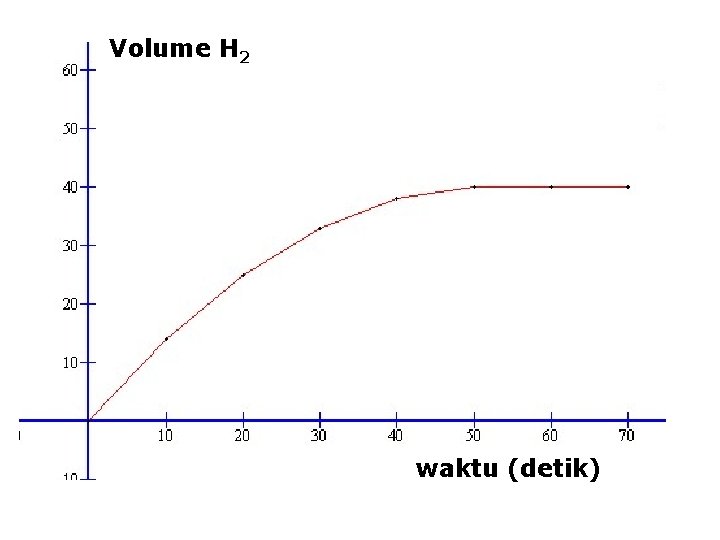
Volume H 2 waktu (detik)

45 Volum H 2 Y 40 35 30 25 Y 20 15 10 5 Waktu (detik) 0 0 2 4 6 8

Keterangan: • Pada 10 detik pertama dihasilkan 14 m. L gas H 2, jadi laju reaksi pada 10 detik pertama adalah 1, 4 m. L hydrogen perdetik. Pada detik ke 20 dihasilkan 11 m. L (25 -14). Jadi laju reaksi pada detik ke 20 adalah 1, 1 m. L perdetik • Kemiringan kurva berubah setiap saat. Kemiringan berkurang seiring dengan berkurangnya laju reaksi. • Kemiringan (gradient) terbesar terjadi pada 10 detik pertama dan makin kecil pada detik-detik berikutnya.

• Volume total gas hydrogen yang dihasilkan adalah 40 m. L, yaitu dalam waktu 50 detik. Laju reaksi rata-rata adalah 40 m. L/50 detik = 0, 8 m. L gas H 2 perdetik Laju Rerata = rerata laju untuk selang waktu tertentu.

Laju Sesaat = laju reaksi pada saat tertentu hal ini karena laju reaksi berubah dari waktu ke waktu. Pada umumnya laju reaksi makin kecil seiring dengan bertambahnya waktu reaksi. Sehingga plot laju terhadap waktu berbentuk garis lengkung. Laju sesaat pada waktu t dapat ditentukan dari kemiringan (gradien) tangen pada saat t tersebut.
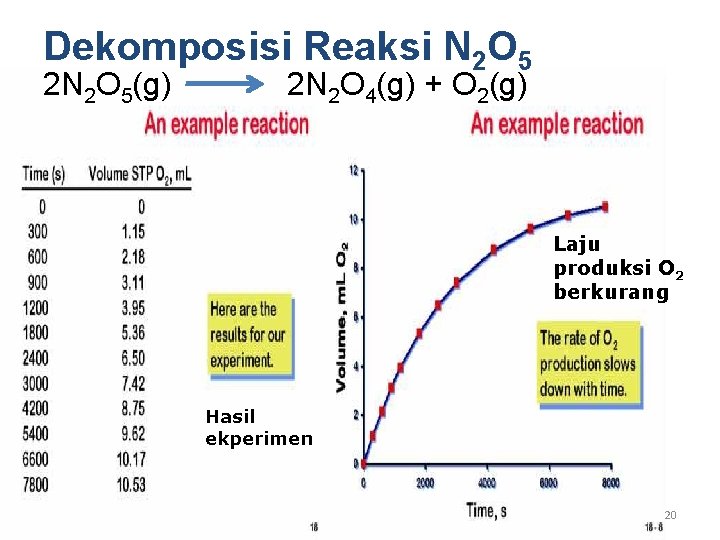
Dekomposisi Reaksi N 2 O 5 2 N 2 O 5(g) 2 N 2 O 4(g) + O 2(g) Laju produksi O 2 berkurang Hasil ekperimen 20
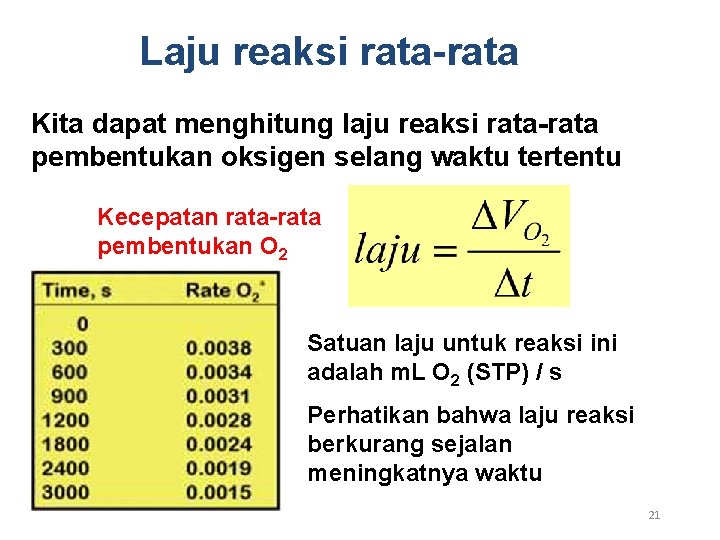
Laju reaksi rata-rata Kita dapat menghitung laju reaksi rata-rata pembentukan oksigen selang waktu tertentu Kecepatan rata-rata pembentukan O 2 Satuan laju untuk reaksi ini adalah m. L O 2 (STP) / s Perhatikan bahwa laju reaksi berkurang sejalan meningkatnya waktu 21

22
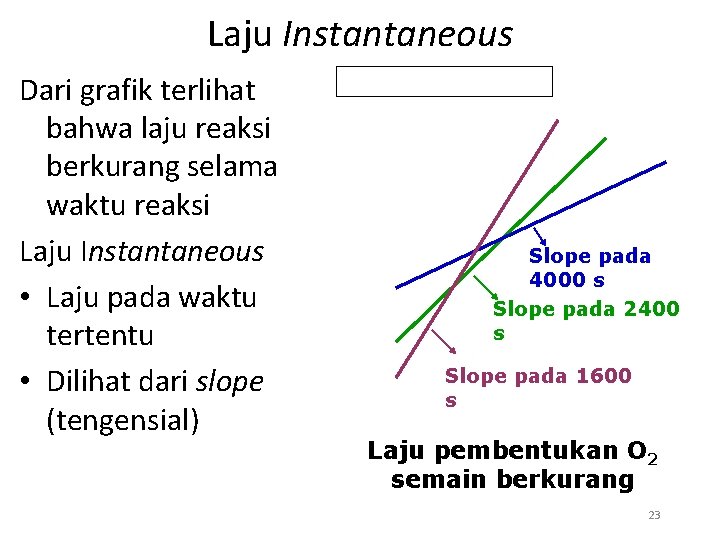
Laju Instantaneous Dari grafik terlihat bahwa laju reaksi berkurang selama waktu reaksi Laju Instantaneous • Laju pada waktu tertentu • Dilihat dari slope (tengensial) Slope pada 4000 s Slope pada 2400 s Slope pada 1600 s Laju pembentukan O 2 semain berkurang 23
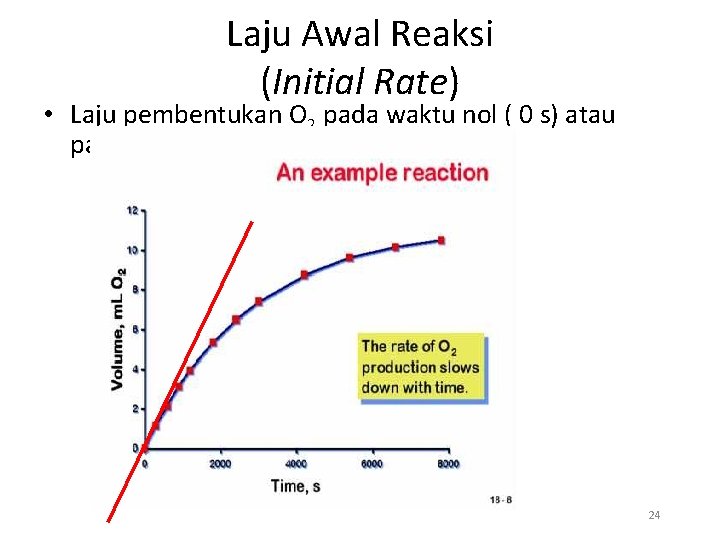
Laju Awal Reaksi (Initial Rate) • Laju pembentukan O 2 pada waktu nol ( 0 s) atau pada saat reaksi tepat akan dimulai 24
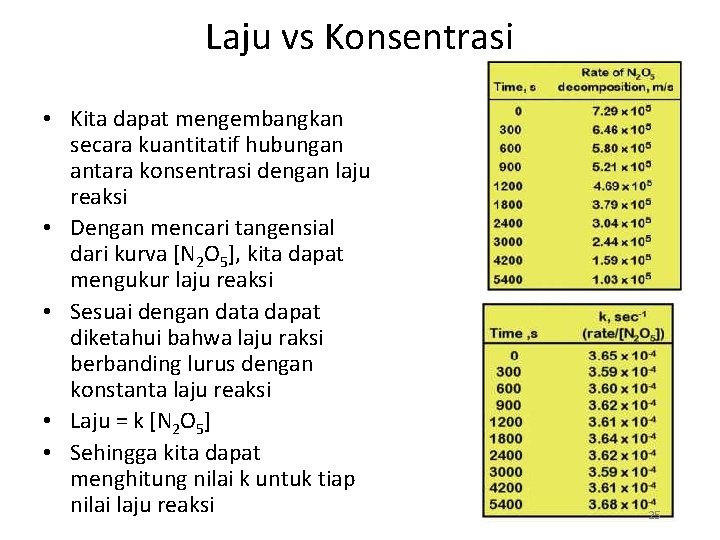
Laju vs Konsentrasi • Kita dapat mengembangkan secara kuantitatif hubungan antara konsentrasi dengan laju reaksi • Dengan mencari tangensial dari kurva [N 2 O 5], kita dapat mengukur laju reaksi • Sesuai dengan data dapat diketahui bahwa laju raksi berbanding lurus dengan konstanta laju reaksi • Laju = k [N 2 O 5] • Sehingga kita dapat menghitung nilai k untuk tiap nilai laju reaksi 25
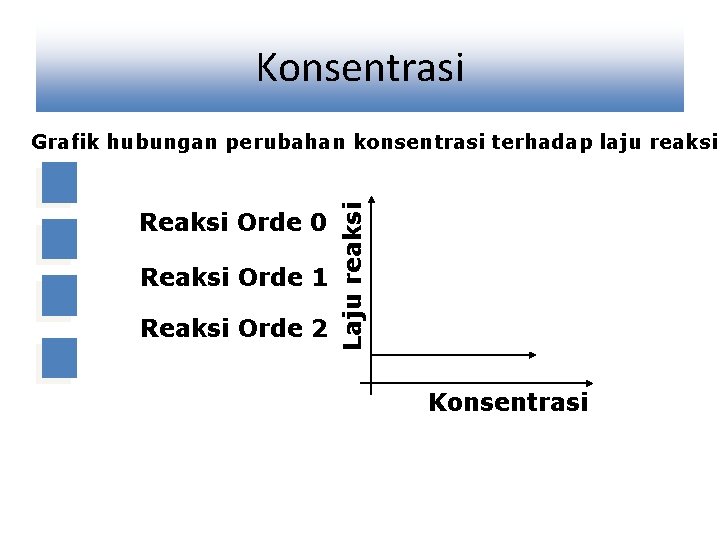
Konsentrasi Reaksi Orde 0 Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Grafik hubungan perubahan konsentrasi terhadap laju reaksi Konsentrasi
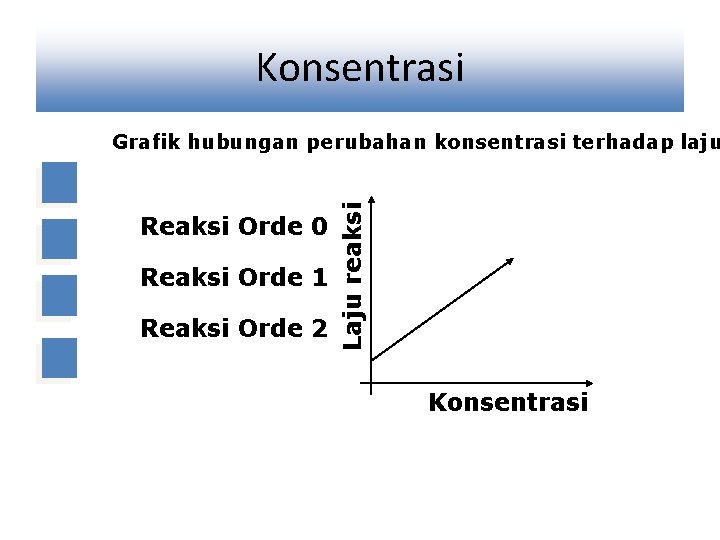
Konsentrasi Reaksi Orde 0 Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Grafik hubungan perubahan konsentrasi terhadap laju Konsentrasi
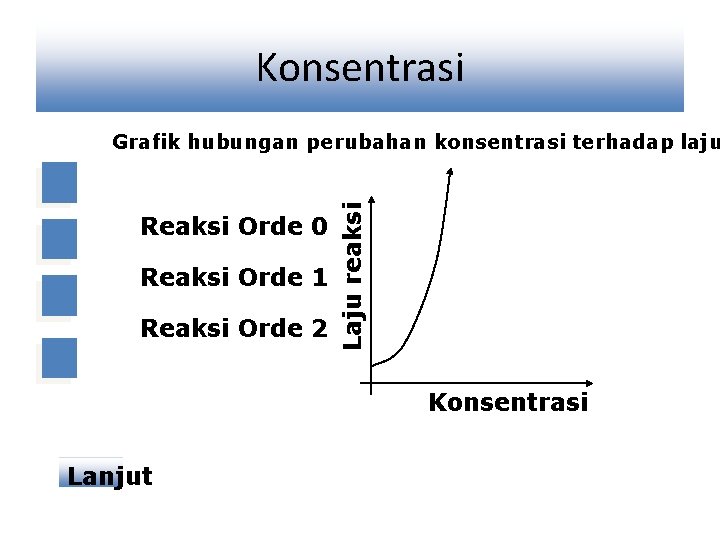
Konsentrasi Reaksi Orde 0 Reaksi Orde 1 Reaksi Orde 2 Laju reaksi Grafik hubungan perubahan konsentrasi terhadap laju Konsentrasi Lanjut

FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI • • • Konsentrasi Suhu Tekanan Luas permukaan Katalis

Faktor Luas Permukaan Bagaimana pengaruh luas permukaan bidang sentuh terhadap laju reaksi. . . ? Mg(s) + 2 HCl Mg. Cl 2(aq) + H 2(g) No Logam Mg (2 gram) HCl Waktu (sekon) 1 Lempeng 1 M 60 2 Butiran 1 M 40 3 Serbuk 1 M 20

Faktor Katalis Apa itu katalis ? ? Bagaimana pengaruh katalis terhadap laju reaksi ? Bagaimana cara kerja katalis . . . ?

Evaluasi 1. Sebutkan faktor-faktor yang mempengaruhi laju reaksi ! 2. Jelaskan mengapa bila konsentrasi diperbesar laju reaksi makin besar ? 3. Setiap kenaikan suhu 10 o. C, laju reaksi menjadi 2 kali semula. Bila pada suhu 25 o. C reaksi berlangsung dengan laju x M/det, tentukan laju reaksi pada suhu 55 o. C 4. Bagaimana cara kerja konsentrasi diperbesar laju reaksi makin besar ?
- Slides: 32