LAJU REAKSI Laju reaksi Berkurangnya konsentrasi pereaksi persatuan

LAJU REAKSI

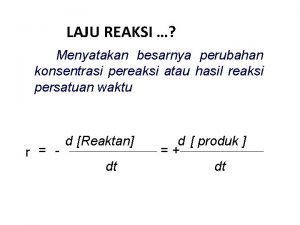
Laju reaksi: Berkurangnya konsentrasi pereaksi persatuan waktu atau bertambahnya konsentrasi hasil reaksi persatuan waktu.

Secara umum untuk reaksi: p. A + q. B r C + s. D V = k[A]x [B]y x = orde reaksi terhadap A y = orde reaksi terhadap B

Teori tumbukan: Suatu reaksi dapat dihasilkan apabila pada saat terjadinya tumbukan antara partikel-partikel zat yang bereaksi pada posisi yang tepat dan memiliki energi yang cukup.

Faktor-Faktor Yang Mempengaruhi Laju Reaksi 1. Konsentrasi 2. Luas Permukaan 3. Kereaktifan zat pereaksi 4. Suhu 5. Katalis

1. Konsentrasi Semakin banyak partikel atom / molekul berarti semakin banyak peluang terjadinya tumbukan efektif sehingga terjadi reaksi

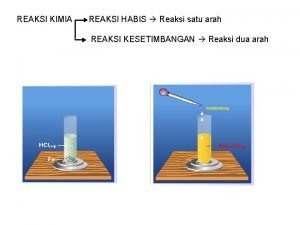
Contoh: Kalsium karbonat (Ca. CO 3) direaksikan dengan asam klorida (HCl) 1 M, 2 M, 3 M. Maka HCl 3 M akan lebih cepat bereaksi Ca. CO 3 1 M HCl 2 M HCl 3 M HCl

2. Luas Permukaan Semakin luas permukaan bidang sentuh berarti semakin banyak peluang terjadinya tumbukan efektif. 1 2 3

Contoh: Asam klorida (HCl) di reaksikan dengan Besi (Fe) bongkahan, lempengan, dan serbuk dengan massa yang sama. Fe serbuk akan lebih cepat bereaksi 1 2 3

3. Kereaktifan zat pereaksi Semakin reaktif suatu zat berarti semakin mudah melepaskan elektron sehingga dapat terjadi reaksi.

Contoh: Mereaksikan logam Natrium dengan logam Magnesium ke dalam Gelas kimia yang berisi air Na + air Mg + air Logam Na lebih reaktif dari Mg

4. Suhu Panas menyediakan energi untuk mengubah partikel yang tidak aktif menjadi aktif. Partikel aktif dapat merusak ikatannya pada saat tumbukan sehingga dapat terjadi reaksi.

Contoh: Mereaksikan logam magnesium (Mg) dengan asam klorida, maka pada suhu yang lebih tinggi logam Mg akan lebih cepat habis bereaksi 25°C 1 35°C 2 45°C 3
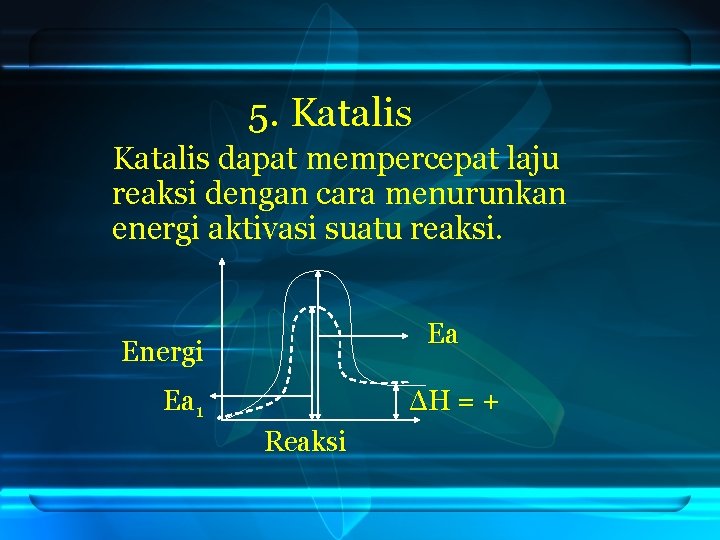
5. Katalis dapat mempercepat laju reaksi dengan cara menurunkan energi aktivasi suatu reaksi. Ea Energi Ea 1 ΔH = + Reaksi

Penentuan Orde Reaksi Orde persamaan laju reaksi hanya dapat ditentukan secara eksperimen dan tidak dapat diturunkan dari koefisien persamaan reaksi.
![Grafik laju reaksi: 1. Grafik laju reaksi orde 0 V = k [A]0 V Grafik laju reaksi: 1. Grafik laju reaksi orde 0 V = k [A]0 V](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-16.jpg)
Grafik laju reaksi: 1. Grafik laju reaksi orde 0 V = k [A]0 V [A]
![2. Grafik laju reaksi orde 1: V = k [A]1 V [A] 2. Grafik laju reaksi orde 1: V = k [A]1 V [A]](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-17.jpg)
2. Grafik laju reaksi orde 1: V = k [A]1 V [A]
![3. Grafik laju reaksi orde 2: V= k [A]2 V [A] 3. Grafik laju reaksi orde 2: V= k [A]2 V [A]](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-18.jpg)
3. Grafik laju reaksi orde 2: V= k [A]2 V [A]

Contoh: 1. Diketahui data percobaan laju reaksi 2 NO + Cl 2 2 NOCl No [NO]M [Cl 2]M Waktu / s 1 0, 01 0, 1 72 2 0, 01 0, 2 18 3 0, 02 0, 3 2 Tentukan orde reaksi NO dan Cl 2!
![Jawab: a. Mencari orde Cl 2 bandingkan data [NO] yang sama ( data nomor Jawab: a. Mencari orde Cl 2 bandingkan data [NO] yang sama ( data nomor](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-20.jpg)
Jawab: a. Mencari orde Cl 2 bandingkan data [NO] yang sama ( data nomor 1 dan 2 )
![b. Mencari orde NO bandingkan data [Cl 2] ( data nomor 1 dan 3 b. Mencari orde NO bandingkan data [Cl 2] ( data nomor 1 dan 3](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-21.jpg)
b. Mencari orde NO bandingkan data [Cl 2] ( data nomor 1 dan 3 )
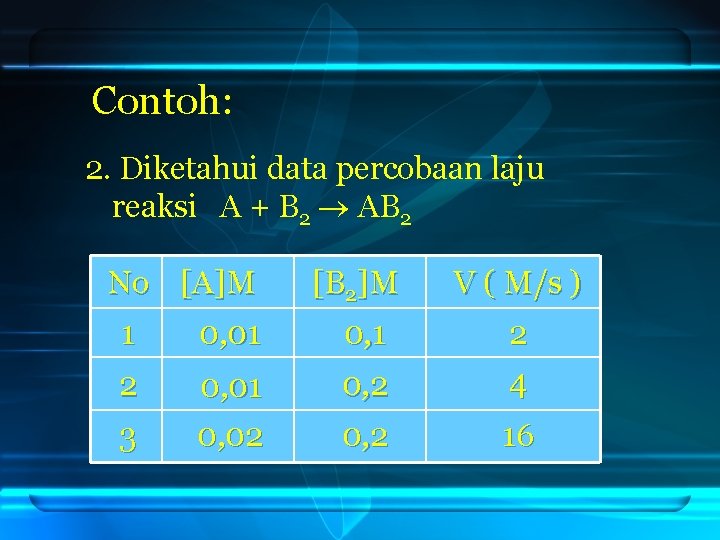
Contoh: 2. Diketahui data percobaan laju reaksi A + B 2 AB 2 No [A]M [B 2]M V ( M/s ) 1 0, 01 0, 1 2 0, 01 0, 02 0, 2 2 4 0, 2 16 3

Tentukan: a. b. c. d. e. Orde reaksi terhadap A Orde reaksi terhadap B 2 Orde reaksi total Harga tetapan k Persamaan laju reaksi
![Jawab: a. Mencari orde A bandingkan data [B 2] yang sama (data nomor 2 Jawab: a. Mencari orde A bandingkan data [B 2] yang sama (data nomor 2](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-24.jpg)
Jawab: a. Mencari orde A bandingkan data [B 2] yang sama (data nomor 2 dan 3)

b. Mencari orde B bandingkan data A yang sama (data nomor 1 dan 2)

c. Orde reaksi total = x + y = 2+1 = 3 d. Harga tetapan k

e. Persamaan laju reaksi

Katalis Zat yang dapat mempercepat reaksi tanpa mengalami perubahan kekal (komposisi kimia katalis tidak berubah pada akhir reaksi) dengan menurunkan energi aktivasi (energi minimum yang dibutuhkan untuk terjadinya tumbukan efektif)
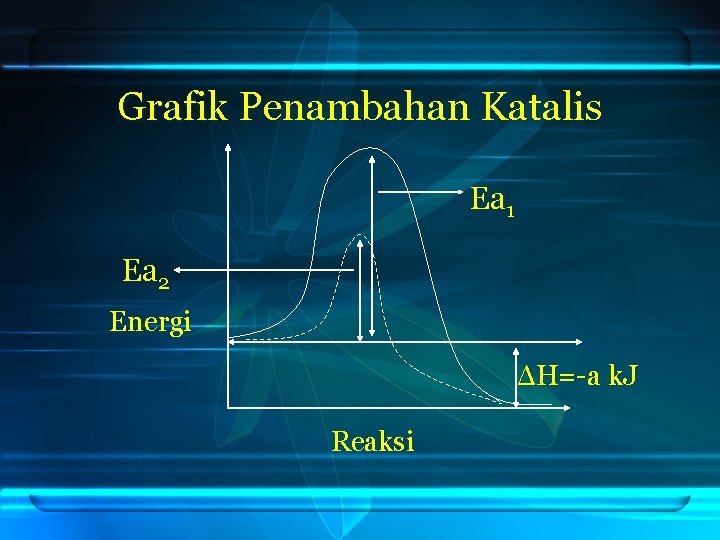
Grafik Penambahan Katalis Ea 1 Ea 2 Energi ΔH=-a k. J Reaksi

Peran katalis 1. Dalam tubuh diantaranya enzim pencernaan. 2. Enzim papain untuk melunakkan daging. 3. Pembuatan NH 3 4. Pembuatan H 2 SO 4 baik dengan proses kontak maupun bilik timbal.

Sifat katalis 1. Komposisi kimia katalis tidak berubah pada akhir reaksi 2. Katalis tidak memulai suatu reaksi, tetapi mempengaruhi laju reaksi. 3. Katalis bekerja secara spesifik untuk reaksi tertentu.

4. Katalis bekerja pada temperatur optimum. 5. Katalis dapat diracuni oleh zat lain yang disebut racun katalis. 6. Keaktifan katalis dapat diperbesar oleh promotor. 7. Katalis yang memperlambat reaksi disebut katalis negatif (inhibitor)

8. Salah satu hasil reaksi dapat berfungsi sebagai katalis untuk reaksi berikutnya disebut autokatalisis. 9. Katalis yang terdapat pada makhluk hidup disebut enzim.

Pertanyaan: 1. Zat yang dapat menurunkan energi aktifasi disebut … Katalisator
![2. Grafik laju reaksi berikut termasuk orde… V [A] Satu 2. Grafik laju reaksi berikut termasuk orde… V [A] Satu](http://slidetodoc.com/presentation_image_h/b06dfbdff7ae104344cf91144344c934/image-35.jpg)
2. Grafik laju reaksi berikut termasuk orde… V [A] Satu

- Slides: 36