Bab 3 LAJU REAKSI Kemolaran atau molaritas adalah

Bab 3 LAJU REAKSI

Kemolaran atau molaritas adalah besaran yang menyatakan jumlah mol zat yang terlarut tiap liter larutan. Kemolaran atau molaritas dilambangkan dengan huruf M. Keterangan: M = kemolaran larutan (M atau mol/liter atau mmol/ml) n = jumlah mol zat terlarut (mol) V = volume larutan (liter)

Kegunaan Kemolaran ü Melarutkan Zat Padat ü Pengenceran ü Mencampurkan Larutan yang Mempunyai Konsentrasi Berbeda

Laju Reaksi Laju reaksi adalah laju pengurangan konsentrasi molar salah satu pereaksi atau laju pertambahan konsentrasi salah satu produk dalam satuan waktu. Perhatikan reaksi berikut! A B Keterangan: A = pereaksi B = produk Laju reaksi dapat diukur dengan menghitung pengurangan konsentrasi A tiap satuan waktu atau pertambahan konsentrasi B tiap satuan waktu.

Faktor-Faktor yang Memengaruhi Laju Reaksi Pengaruh Konsentrasi terhadap Laju Reaksi Pengaruh Luas Bidang Sentuh terhadap Laju Reaksi Pengaruh Suhu terhadap Laju Reaksi Pengaruh Kasalisator terhadap Laju Reaksi

Teori Tumbukan Suatu zat jika berinteraksi dengan zat lain akan membuat partikel - partikel antara kedua zat itu saling bertumbukan. Akan tetapi, tidak semua tumbukan mampu menghasilkan reaksi kimia. Energi aktivasi adalah energi minimum yang harus dimiliki oleh partikel pereaksi untuk menghasilkan tumbukan yang efektif.

Hubungan Faktor-Faktor yang Memengaruhi Laju Reaksi dengan Teori Tumbukan ü Konsentrasi ü Luas Permukaan Bidang Sentuh ü Suhu ü Katalisator

Persamaan Laju Reaksi dan Orde Reaksi a. Persamaan Laju Reaksi Persamaan laju reaksi hanya dapat dinyatakan berdasarkan data percobaan. Bentuk persamaan laju reaksi itu adalah sebagai berikut. Reaksi: p. A + q. B g r. C + s. D v = k. [A]x. [B]y Keterangan: v = laju reaksi k = tetapan jenis reaksi [A] = konsentrasi zat A [B] = konsentrasi zat B x = orde (tingkat) reaksi terhadap pereaksi A y = orde (tingkat) reaksi terhadap pereaksi B x + y = orde reaksi total

b. Orde Reaksi Orde reaksi adalah bilangan pangkat dari besarnya konsentrasi pereaksi pada persamaan laju reaksi. Berikut ini contoh-contoh dari beberapa persamaan laju reaksi dari beberapa reaksi.

Grafik perubahan konsentrasi versus laju reaksi. Jika nilai konsentrasi pereaksi dilipatduakan, maka laju reaksi = 21 = 2 kali lebih besar. Jika nilai konsentrasi pereaksi dilipatduakan, maka laju reaksi 22 = 4 kali lebih besar.
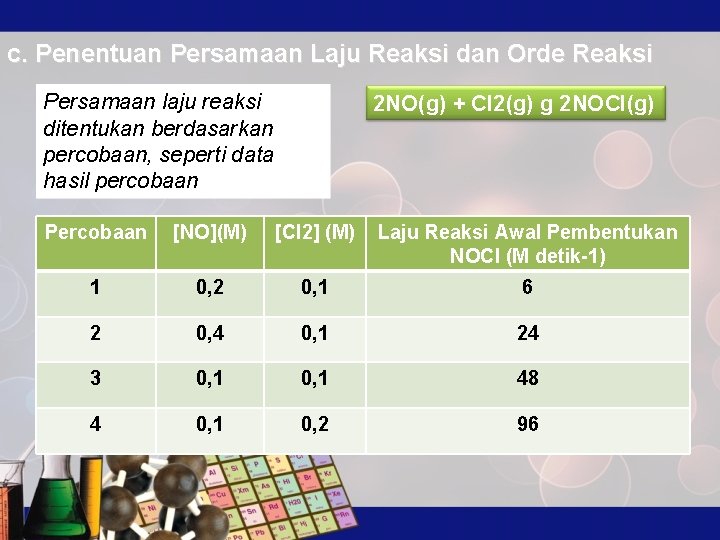
c. Penentuan Persamaan Laju Reaksi dan Orde Reaksi Persamaan laju reaksi ditentukan berdasarkan percobaan, seperti data hasil percobaan 2 NO(g) + Cl 2(g) g 2 NOCl(g) Percobaan [NO](M) [Cl 2] (M) Laju Reaksi Awal Pembentukan NOCl (M detik-1) 1 0, 2 0, 1 6 2 0, 4 0, 1 24 3 0, 1 48 4 0, 1 0, 2 96

Dari persamaan reaksi 2 NO(g)+Cl 2(g) g 2 NOCl(g) dapat dibuat persamaan laju reaksi sebagai berikut. v = k. [NO]x. [Cl 2]y Orde reaksi terhadap NO adalah x. Cara menentukan x, yaitu dengan membandingkan data percobaan 1 dan 2. Orde reaksi terhadap Cl 2 adalah y. Cara menentukan y, yaitu dengan membandingkan data percobaan 3 dan 4. Orde reaksi total = x + y = 2 + 1 = 3.

Terapan Laju Reaksi dalam Kehidupan Sehari-Hari 1. Pengaruh Luas Permukaan Bidang Sentuh terhadap Laju Reaksi Aktivitas sehari-hari yang kita lakukan secara sadar atau tidak, sebenarnya merupakan upaya untuk mempercepat laju reaksi.

a. Jika seseorang membuat sambal, biasanya cabai dipotong terlebih dahulu sebelum dimasukkan dalam blender. b. Gula jawa supaya cepat larut dalam air pada pembuatan kolak, selalu diiris-iris terlebih dahulu. c. Jika memasak menggunakan kayu bakar, kayu yang digunakan adalah belahan dari kayu gelondongan. d. Pada industri semen, batu kapur dihancurkan dengan mesin penghancur untuk mempercepat proses selanjutnya. e. Pada industri kertas, bahan-bahan yang digunakan untuk membuat bubur kertas digerus terlebih dahulu supaya campuran menjadi homogen dan reaksi berlangsung sempurna.

2. Penggunaan Katalisator dalam Industri Katalisator banyak digunakan dalam industri. Hal ini karena katalisator dapat mempercepat reaksi. Dengan proses reaksi yang cepat, produksi dalam industri akan meningkat. Misalnya, pada industri asam sulfat menggunakan katalisator V 2 O 5, pada industri amonia menggunakan katalisator Fe dan Al 2 O 3, serta pada industri yang memproduksi metanol menggunakan katalisator Zn. O/Cr 2 O 3.
- Slides: 15