REAKSI REDOKS Reaksi Reduksi 1 Reaksi yang mengalami



















- Slides: 22

REAKSI REDOKS

Reaksi Reduksi 1. Reaksi yang mengalami penurunan bilangan oksidasi 2. Oksidator 3. Reaksi yang menerima elektron 4. Reaksi pelepasan oksigen

Reaksi Oksidasi 1. Reaksi yang mengalami kenaikan bilangan oksidasi 2. Reduktor 3. Reaksi yang menyerahkan elektron 4. Reaksi pengikatan oksigen

ATURAN BILOKS 1. Unsur bebas dan molekul unsur biloksnya = 0 Contoh : 4 K + O 2 → 2 K 2 O P 4 + 6 I 2 → 4 PI 3 Ba + Cl 2 → Ba. Cl 2

2. Logam dalam senyawa biloksnya selalu positif (+) Contoh : 2 K + Cl 2 → 2 KCl K = +1 Mg + Cl 2 → Mg. Cl 2 Mg =+2 3 Fe + 3 Cl 2 → 3 Fe. Cl 2 Fe = +2 2 Fe + 3 Cl 2 → 2 Fe. Cl 3 Fe = +3

3. Hidrogen dalam senyawa biloksnya = +1 Kecuali : bersenyawa langsung dengan logam, hidrogen = -1 Contoh : 2 H 2 + O 2 → 2 H 2 O H=+1 H 2 + 2 K → 2 KH H 2 + Mg → Mg. H 2 H=-1

4. Oksigen dalam senyawa biloksnya=-2 Kecuali : a. peroksida = -1 b. superoksida = -1/2 c. OF 2 = +2 Contoh : 2 H 2 + O 2 → 2 H 2 O O=-2 H 2 + O 2 → H 2 O 2 O=-1 K + O 2 → KO 2 O=-1/2

5. Biloks ion = muatannya a. monoatomik b. poliatomik Contoh : O 2 - = -2 Na+ = +1 Cl- = -1 NH 4+ = +1 NO 3 - = -1 Al 3+ = +3 Cr 2 O 72 - = -2 SO 42 - = -2

6. Total biloks senyawa = 0 Contoh : KCl. O 4 = 0 Mn. O 2 = 0 H 2 SO 4 = 0 H 2 O = 0 KO 2 = 0

CONTOH SOAL: 1. Tentukan biloks Cl dalam senyawa KCl. O 4 Jawab : 1 K + 1 Cl + 4 O = 0 1(+1) + 1(Cl) + 4(-2) = 0 +1 + Cl - 8 = 0 Cl = +7

2. Tentukan biloks Cr dalam senyawa Cr 2 O 72 - Jawab : 2 Cr + 7 O = -2 2(Cr) + 7(-2) = -2 2 Cr - 14 = -2 2 Cr = +12 Cr = +6

A. Penyetaraan Persamaan Reaksi Redoks 1. Metode Bilangan Oksidasi 2. Metode Ion Elektron

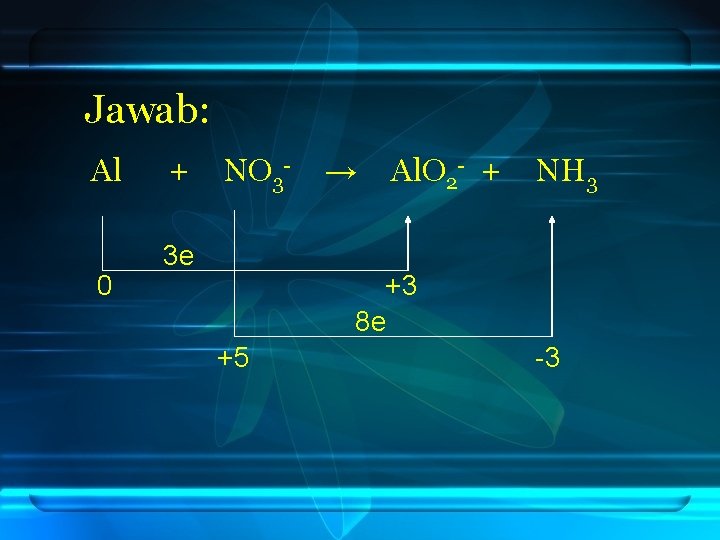
Contoh: 1. Tuliskan persamaan reaksi ion yang terjadi antara Al dan NO 3 - dalam suasana basa dengan cara perubahan biloks jika diketahui perubahan yang terjadi Al/Al. O 2 dan NO 3 -/NH 3

Jawab: Al 0 + NO 3 - 3 e → Al. O 2 - + NH 3 +3 8 e +5 -3

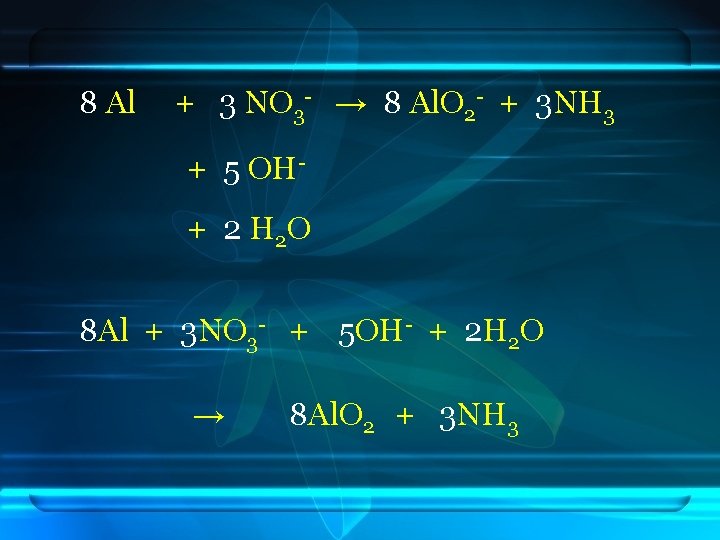
8 Al + 3 NO 3 - → 8 Al. O 2 - + 3 NH 3 + 5 OH+ 2 H 2 O 8 Al + 3 NO 3 - + 5 OH- + 2 H 2 O → 8 Al. O 2 + 3 NH 3

Contoh: 2. Tuliskan pers. reaksi ion yang terjadi antara KI + KOH + KMn. O 4 jika diketahui I-/I 2 dan Mn. O 4 - /Mn. O 2

Jawab: Langkah 1: oksidasi : I- → I 2 reduksi : Mn. O 4 - → Mn. O 2 Langkah 2: oksidasi : 2 I- → I 2 reduksi : Mn. O 4 - → Mn. O 2 + 4 OH-

Langkah 3: Oks : 2 I- → I 2 + 2 e ) x 3 Red : Mn. O 4 - +2 H 2 O + 3 e→Mn. O 2 +4 OH- ) x 2 Langkah 4: oksidasi : 6 I- → 3 I 2 + 6 e reduksi : 2 Mn. O 4 - +4 H 2 O + 6 e→ 2 Mn. O 2 + 8 OH-

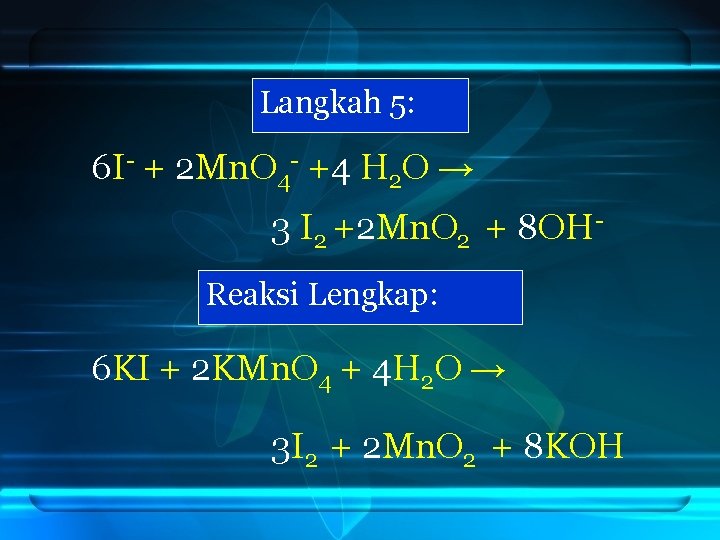
Langkah 5: 6 I- + 2 Mn. O 4 - +4 H 2 O → 3 I 2 +2 Mn. O 2 + 8 OHReaksi Lengkap: 6 KI + 2 KMn. O 4 + 4 H 2 O → 3 I 2 + 2 Mn. O 2 + 8 KOH

Pertanyaan: 1. Reaksi: 2 K + Cl 2 → 2 KCl Bilangan oksidasi K dalam senyawa KCl reaksi adalah … +1

2. Zat yang mengalami penurunan bilangan oksidasi dalam reaksi redoks disebut … oksidator
