Reaksi redoks Kelas X Semester 2 Oleh Musyarofah



















- Slides: 21

Reaksi redoks Kelas X Semester 2 Oleh : Musyarofah, S. Pd

Standar Kompetensi Memahami sifat-sifat larutan non elektrolit dan elektrolit, serta reaksi oksidasi reduksi Kompetensi Dasar 1. 2. Menganalisis perkembangan konsep reaksi oksidasi- reduksi serta menentukan bilangan oksidasi atom dalam molekul atau ion. Menerapkan aturan IUPAC untuk penamaan senyawa anorganik dan organik sederhana. Tujaan Pembelajaran 1. 2. 3. Siswa dapat membedakan konsep oksidasi reduksi ditinjau dari penggabungan dan pelepasan oksigen, pelepasan dan penerimaan elektron, serta peningkatan dan penurunan bilangan oksidasi. Siswa dapat menentukan bilangan oksidasi atom unsur dalam senyawa atau ion. Siswa dapat menentukan oksidator dan reduktor dalam reaksi redoks


Gunung Kelud Meletus Sumber: www. bacainfo. com


Sumber: www. bacainfo. com

Sumber: www. bacainfo. com

Contoh Reaksi Redoks • S 8 + 4 O 2 → 4 SO 2 • 2 SO 2 + O 2 → 2 SO 3 • 2 SO 3 + H 2 O → H 2 SO 4


Reaksi Kimia Dalam Kolam Renang

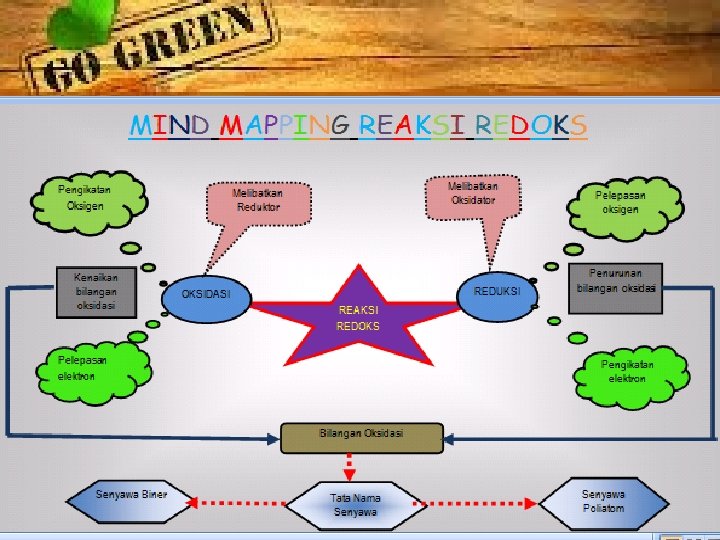
Reaksi Redoks itu apa ya? Reaksi Redoks adalah reaksi reduksi oksidasi.

KONSEP REDOKS 1. Berdasarkan Oksigen 2. Berdasarkan Elektron 3. BILANGAN OKSIDASI

1. Berdasarkan Oksigen Oksidasi Reduksi Sebagai Reaksi Pengikatan dan Pelepasan Oksigen Reaksi oksidasi adalah reaksi pengikatan oksigen oleh suatu zat. Sedangkan reduksi adalah pelepasan atau pengurangan oksigen dari suatu zat. Beberapa contoh reaksi oksidasi yaitu: Ø 4 Fe(s)+3 O 2(g) → 2 Fe 2 O 3(s) ØC 6 H 12 O 6(aq)+ 6 O 2→CO 2(g) + 2 H 2 O(g) Beberapa contoh reduksi yaitu: ØFe 2 O 3(s)+3 CO(g)→ 2 Fe(s)+3 CO 2(g) ØCr 2 O 3(s) + 2 Al(s) → Al 2 O 3(s) + 2 Cr

2. Berdasarkan Elektron

3. Berdasarkan Bilangan Oksidasi

OKSIDATOR adalah zat yang mengalami reaksi REDUKSI REDUKTOR adalah zat yang mengalami reaksi OKSIDASI

A. Cara Menentukan Biloks Unsur Dalam Senyawa Atau Ion Tentukan bilangan oksidasi Cr dalam (Cr 2 O 7)2– Biloks Cr dalam (Cr 2 O 7)-2, • biloks O = - 2, maka : • 2 x biloks Cr + 7 biloks O = -2 • 2 x biloks Cr + 7 x (-2) = -2 • 2 x biloks Cr = -2 + 14 • biloks Cr = = +6

Sekian dan terimakasih …………….

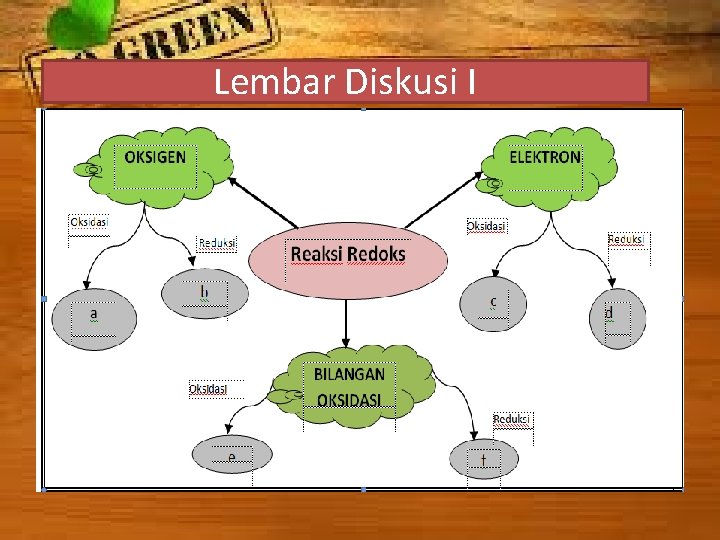
Lembar Diskusi I

QUIS 1. Aku merupakan hasil dari fotosintesis. Aku mempunyai biloks -2. Semua orang membutuhkan diriku untuk bernafas. Siapakah aku…? 2. Aku adalah suatu unsur. Aku mempunyai bilangan oksidasi +1 dan +3. Aku biasanya digunakan sebagai perhiasan. Siapakah aku……? 3. Aku merupakan unsur yang paling banyak dibumi. Biloks ku juga paling banyak diantara unsur lainnya. Siapakah aku…. ? Tebak Aku 4. Aku adalah zat yang ada pada reaksi redoks. Kehadiranku menyebabkan yang lain mengalami reaksi reduksi. Siapakah aku…. ?

“Jangan pernah berhenti belajar, karena hidup tak pernah berhenti mengajarkan” Semangat dan Salam Sukses