TITRASI REDOKS Titrimetri melibatkan rekasi oksidasi dan reduksi

TITRASI REDOKS Titrimetri melibatkan rekasi oksidasi dan reduksi yg berkaitan dg perpindahan elektron Perubahan e- � perubahan valensi atom / ion yang bersangkutan. Zat pengoksid mendapatkan e- dan tereduksi valensi atom / ion menurun Zat pereduksi kehilangan e- dan teroksidasi Valensi atom /ion meningkat
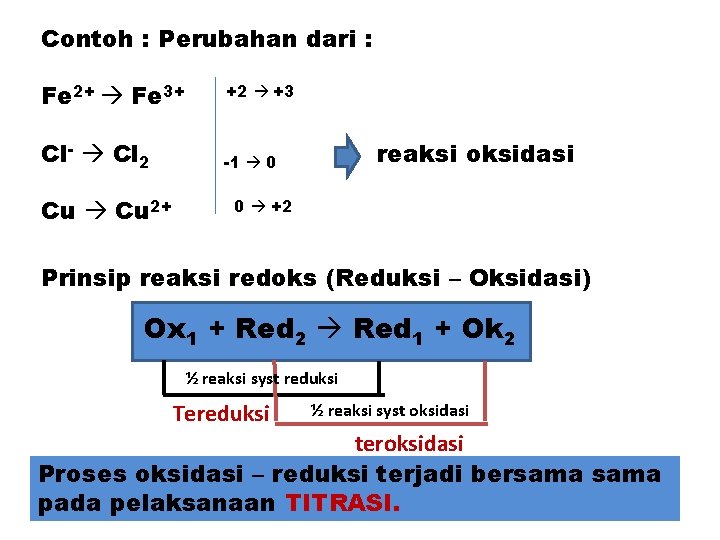
Contoh : Perubahan dari : Fe 2+ Fe 3+ +2 +3 Cl- Cl 2 -1 0 Cu 2+ reaksi oksidasi 0 +2 Prinsip reaksi redoks (Reduksi – Oksidasi) Ox 1 + Red 2 Red 1 + Ok 2 ½ reaksi syst reduksi Tereduksi ½ reaksi syst oksidasi teroksidasi Proses oksidasi – reduksi terjadi bersama pada pelaksanaan TITRASI.

Secara umum reaksi redoks digambarkan Ma+ + ne- M(a-n)+ Ox. 1 Red. 1 : Eo. V ½ reaksi tereduksi di katoda Ma+ M(a-n)+ + ne- : E 0 V Red. 2 Ox. 2 ½ reaksi teroksidasi di anoda Contoh: Fe 2+ + Ce 4+ Fe 3+ + Ce 3+ Fe 3+ + e- Fe 2+ Ce 4+ + e- Ce 3+ : Eo = 0, 771 Volt : Eo = 1, 61 Volt potensial reduksi

Zat pengoksid lemah cenderung kurang shg hanya dpt mengoksidai zat pereduksi yg plg siap menghasilkan e. Kekuatan zat pengoksidasi dan pereduksi di tunjukkan ole nilai potensial reduksi nya.
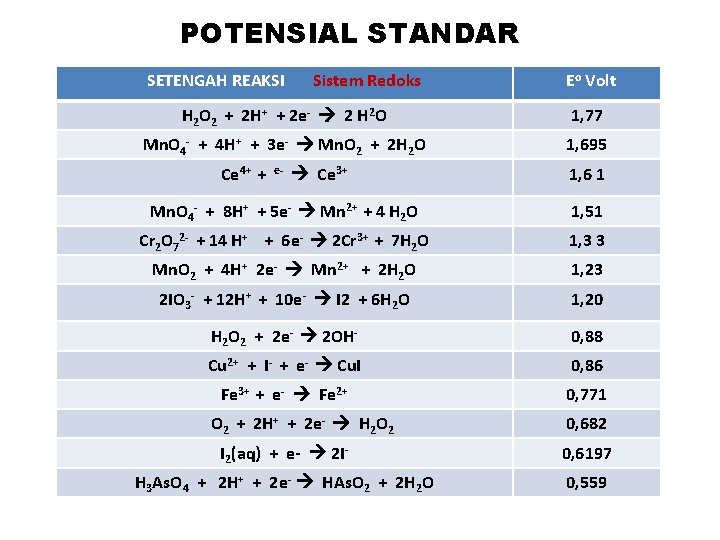
POTENSIAL STANDAR SETENGAH REAKSI Sistem Redoks Eo Volt H 2 O 2 + 2 H+ + 2 e- 2 H 2 O 1, 77 Mn. O 4 - + 4 H+ + 3 e- Mn. O 2 + 2 H 2 O 1, 695 Ce 4+ + e- Ce 3+ 1, 6 1 Mn. O 4 - + 8 H+ + 5 e- Mn 2+ + 4 H 2 O 1, 51 Cr 2 O 72 - + 14 H+ + 6 e- 2 Cr 3+ + 7 H 2 O 1, 3 3 Mn. O 2 + 4 H+ 2 e- Mn 2+ + 2 H 2 O 1, 23 2 IO 3 - + 12 H+ + 10 e- I 2 + 6 H 2 O 1, 20 H 2 O 2 + 2 e- 2 OH- 0, 88 Cu 2+ + I- + e- Cu. I 0, 86 Fe 3+ + e- Fe 2+ 0, 771 O 2 + 2 H+ + 2 e- H 2 O 2 0, 682 I 2(aq) + e- 2 I- 0, 6197 H 3 As. O 4 + 2 H+ + 2 e- HAs. O 2 + 2 H 2 O 0, 559
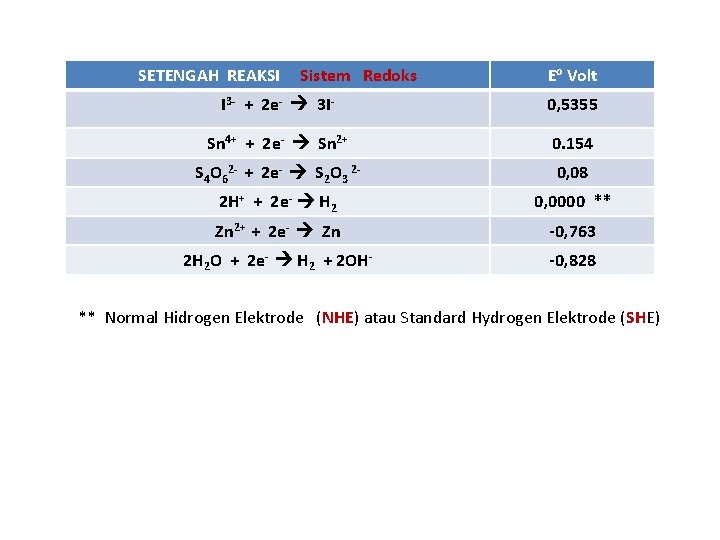
SETENGAH REAKSI Sistem Redoks Eo Volt I 3 - + 2 e- 3 I- 0, 5355 Sn 4+ + 2 e- Sn 2+ 0. 154 S 4 O 62 - + 2 e- S 2 O 3 2 - 0, 08 2 H+ + 2 e- H 2 0, 0000 ** Zn 2+ + 2 e- Zn -0, 763 2 H 2 O + 2 e- H 2 + 2 OH- -0, 828 ** Normal Hidrogen Elektrode (NHE) atau Standard Hydrogen Elektrode (SHE)

Reagen yang berperan sebagai Reduktor/Oksidator Reagen mengalami autooksidasi. Titrasi redoks merupakan bagian dr Titrasi Volumetri yang akan terlaksana dengan baik bila : • Kesetimbangan redoks tercapai dengan cepat setiap penambahan volume titran • Adanya indikator penunjuk TE. stokhiometri • ½ reaksi syst oksidasi dan ½ reaksi syst reduksi saat titrasi selalu terjadi kesetimbangan pada seluruh titik pengamatan

Pengaruh Konsentrasi & Reaksi dari medium Hubungan antara beda potensial (E) sistim redoks dan konsentrasi bentuk teroksidasi dan tereduksi ditunjukkan oleh pers NERNST sbg turunan dari HK. Termodinamika. RT [spesies tereduksi] E = Eo - ------- ln ----------------n. F [spesies teroksidasi] Eo R T F n (1) = potensial standard ln = 2, 303 log = konstante gas (8, 313 joule) = temperatur absolut = konstante Faraday (96500 coulomb) = banyaknya elektron yang ditransf dlm reaksi

Penentuan TAT atau TE. Kurve Titrasi Redoks Dalam titrasi redoks zat atau ion yang terlibat dlm reaksi berubah secara kontinyu, yang akan mempe ngaruhi perubahan potensial (E) larutan. Dengan mengalurkan potensial (E) thd perubahan Vol titran yg ditambahkan diperoleh kurve titrasi spt kurve titrasi netralisasi. Contoh : titrasi garam Fe 2+ dg KMn. O 4 dalam larutan asam teroksidasi Mn. O 4 - + 5 Fe 2+ + 8 H+ tereduksi Mn 2+ + Fe 3+ + 4 H 2 O

Reaksi yg terjadi reversibel, larutan akan selalu mengandung kedua ion awal dan ion yang terbentuk selama reaksi, dg kata lain pada tiap tahapan titrasi larutan akan mengandung dua redoks Fe 2+ /Fe 3+ dan Mn. O 4 -/Mn 2+ untuk menghitung E menggunakan pers 2 atau 3 0, 0591 [Fe 2+ ] Pers (2) E = 0, 771 – ------ log -----1 [Fe 3+ ] Pers (3) RT 0, 0591 [Mn 2+ ] E = 1, 51 - ------- log -----------n [Mn. O 4 -] [H+]8 ----- x 2, 303 = 0, 0591 pers (2) & pers (3) memberikan F hasil yg sama. F
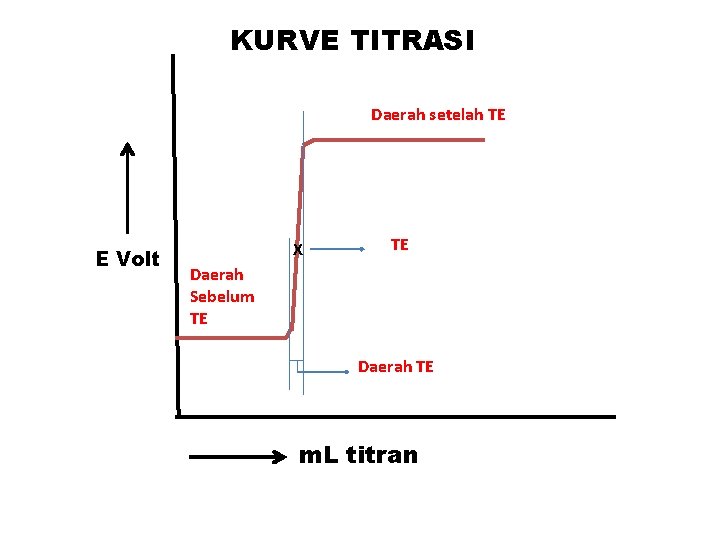
KURVE TITRASI Daerah setelah TE E Volt X TE Daerah Sebelum TE Daerah TE m. L titran

Pers (2) dan (3) dapat digunakan untuk perhitungan selanjutnya. Pers(2) akan lebih mudah untuk menghitung E besi ketika penambahan vol titran mendekati TE. Sedang pers (3) dipakai untuk menghitung E Mn. O 4 ketika terjadi kelebihan vol titran. Contoh: 50 m. L lrtn KMn. O 4 Nx 100 m. L Fe. SO 4 Nx Dicapai 50% Fe 2+ Fe 3+ Brp E pada keadaan sebelum TE, dan sesudah TE
![Maka dapat dituliskan 0, 0591 [50] E = 0, 771 - ----- log ------- Maka dapat dituliskan 0, 0591 [50] E = 0, 771 - ----- log -------](http://slidetodoc.com/presentation_image/2185f05cbea0ea9315925cb5b98ff093/image-13.jpg)
Maka dapat dituliskan 0, 0591 [50] E = 0, 771 - ----- log ------- = 0, 771 volt. 1 [50] Keadaan sebelum TE. E pada penambahan 0, 1 sebelum TE pada pe (+) 99, 9 m. L lrt KMn. O 4 0, 0591 [0, 1] E = 0, 771 - ------ log ----- = 0, 944 volt 1 [99, 9] Keadaan sesudah TE 0, 0591 ` [100] E = 1, 51 - ------ log --------- = 1, 475 volt 5 [0, 1] [H+]8
![Keadaan TE, diasumsikan [H+] = 1 M , 0, 0591 [Fe 2+] E = Keadaan TE, diasumsikan [H+] = 1 M , 0, 0591 [Fe 2+] E =](http://slidetodoc.com/presentation_image/2185f05cbea0ea9315925cb5b98ff093/image-14.jpg)
Keadaan TE, diasumsikan [H+] = 1 M , 0, 0591 [Fe 2+] E = 0, 771 - ------ log ------ ½ sel sist redoks 1 [Fe 3+] 0, 0591 [Mn 2+ ] E = 1, 51 - ------ log ------- ½ sel sist redoks 5 [Mn. O 4 -] ------------------------------- [+] 0, 0591 [Fe 2+ ] [Mn 2+ ] 6 E = 0, 771 + 5 x 1, 51 - ----- log ------------ (****) 1 [Fe 3+ ] [Mn. O 4 - ] Pada TE banyaknya eq titran = eq titrat.

Pada TE banyak ion Mn. O 4 - yang di (+) kan sesuai dg persamaan reakasi berikut : Mn. O 4 - + 5 Fe 2+ + 8 H+ Mn 2+ + 5 Fe 3+ + 4 H 2 O Pada kesetimbangan setiap 1 ion Mn. O 4 - harus ada 5 ion Fe 2+ Shg persamaan (****) harga log [ ] = 0 Maka ETE 0, 771 + (5 x 1, 51) = --------------- = 1, 387 volt 6
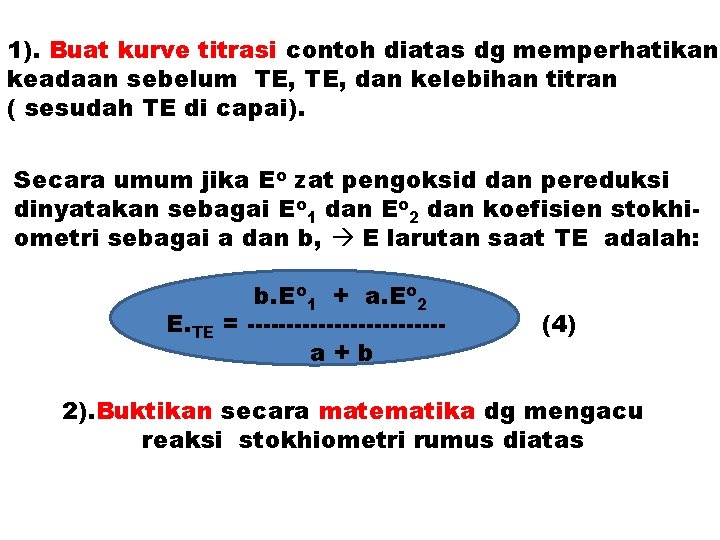
1). Buat kurve titrasi contoh diatas dg memperhatikan keadaan sebelum TE, dan kelebihan titran ( sesudah TE di capai). Secara umum jika Eo zat pengoksid dan pereduksi dinyatakan sebagai Eo 1 dan Eo 2 dan koefisien stokhiometri sebagai a dan b, E larutan saat TE adalah: E. TE b. Eo 1 + a. Eo 2 = ------------a+b (4) 2). Buktikan secara matematika dg mengacu reaksi stokhiometri rumus diatas

Kurve titrasi redoks secara umum sama dg kurve Titrasi netralisasi (asam-basa). E berubah tiba-tiba saat TE, dan berikutnya kurve tetap mendatar ini menunjukkan perubahan E sangat lambat selama titrasi. belokan pd kurve dapat digunakan utk penentu TE dg bantuan indikator. Besarnya perubahan E lrt tgt pada perbedaan E o dari kedua sistim redoks. Kurva oksidimetri biasanya tdk tgt pengenceran, krn Pers NERNST merupakan perbandingan [teroksidasi] [tereduksi], shg tdk berubah dg pengenceran. “Keadaan ini benar jika koefisien bentuk redoks kedua sistem sama”

Titik belok kurve titrasi redoks dapat diperlebar jika Salah satu ion yang terbentuk membentuk kompleks. Contoh : pada titrasi redoks penambahan PO 43 - , F bergabung dg Fe 3+ kompleks stabil [Fe(PO 4)2]= , [Fe. F 6]=

Indikator Reaksi Redoks. TE titrasi redoks dapat dilakukan dengan / tanpa Ind Tanpa indikator bisa dilakukan jika semua zat pereduksi teroksidasi oleh oksidator dan memberikan perubahan fisik (warna/tidak berwarna ) yang bisa teramati dg jelas. Contoh : Mn. O 4 - dlm suasana H+, warna ungu lemba yung ion Mn. O 4 - hilang krn tereduksi � Mn 2+ ketika Semua zat pereduksi telah dititrasi, kelebihan 0, 1 m. L permanganat larutan menjadi merah muda. Contoh lain: titrasi zat pereduksi dg lrt Iod, perubhn warna coklat gelap tak berwarna dr Iod I 2 I- , karena warna Iod krg tajam mk utk mempertajam digunakan indikator amilum biru kuat (I 2 <<)
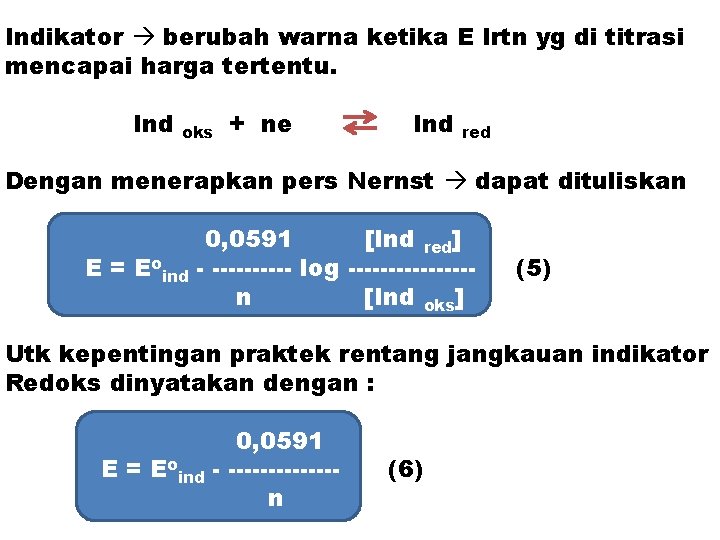
Indikator berubah warna ketika E lrtn yg di titrasi mencapai harga tertentu. Ind oks + ne Ind red Dengan menerapkan pers Nernst dapat dituliskan E = Eoind 0, 0591 [Ind red] - ----- log --------n [Ind oks] (5) Utk kepentingan praktek rentang jangkauan indikator Redoks dinyatakan dengan : E = Eoind 0, 0591 - -------n (6)

Contoh : Indikator Difenilamin Eo = +0, 76 volt , n = 2 Rentang E Indikator redoks : 0, 0591 E 1 = 0, 76 – ------ = 0, 73 volt. Rentang E 2 0, 73 0, 79 volt 0, 0591 E 2 = 0, 76 + ------ = 0, 79 volt. 2 E=0, 73 < Bentuk tereduksi tidak berwarna berubah bertahap < E=0, 79 bentuk teroksidasi ungu lembayung
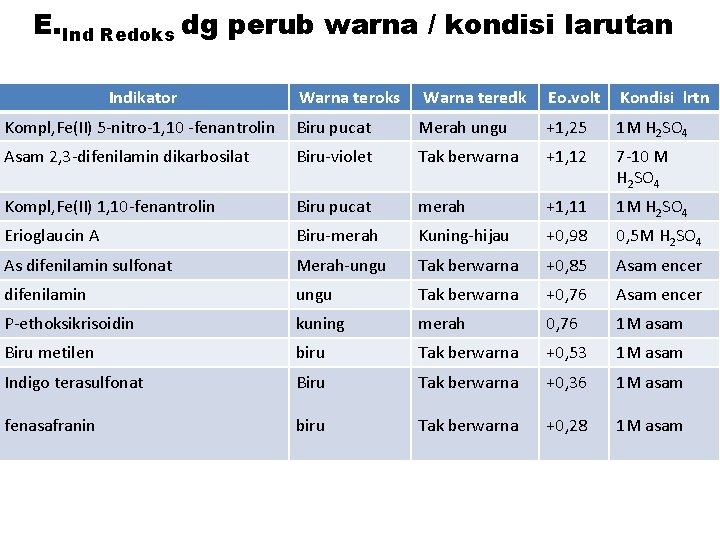
E. Ind Redoks dg perub warna / kondisi larutan Indikator Warna teroks Warna teredk Eo. volt Kondisi lrtn Kompl, Fe(II) 5 -nitro-1, 10 -fenantrolin Biru pucat Merah ungu +1, 25 1 M H 2 SO 4 Asam 2, 3 -difenilamin dikarbosilat Biru-violet Tak berwarna +1, 12 7 -10 M H 2 SO 4 Kompl, Fe(II) 1, 10 -fenantrolin Biru pucat merah +1, 11 1 M H 2 SO 4 Erioglaucin A Biru-merah Kuning-hijau +0, 98 0, 5 M H 2 SO 4 As difenilamin sulfonat Merah-ungu Tak berwarna +0, 85 Asam encer difenilamin ungu Tak berwarna +0, 76 Asam encer P-ethoksikrisoidin kuning merah 0, 76 1 M asam Biru metilen biru Tak berwarna +0, 53 1 M asam Indigo terasulfonat Biru Tak berwarna +0, 36 1 M asam fenasafranin biru Tak berwarna +0, 28 1 M asam

Reaksi samping dalam Titrasi Redoks Salah satu kesukaran dalam titrasi Redoks adalah terjadinya reaksi samping, sehingga akan mem pengaruhi penggunaan titran anlisa menjadi tidak akurat. Contoh : pada penetapan Ferro dg permanganat. 5 Fe 2+ + Mn. O 4 - + 8 H+ 5 Fe 3+ + Mn 2+ + 4 H 2 O Dari persamaan reaksi ion H+ dibutuhkan harus dilakukan dalam suasana asam. Namun sifat dari asam yang menghasilkan H+ sangat berarti. Dalam praktek asam yang tepat dan benar digunakan Asam sulfat. Bagaimana kalau digunakan HCl?

Reaksi yang terjadi dg adanya HCl 10 Cl- + 2 Mn. O 4 - + 16 H+ 2 Mn 2+ + 8 H 2 O + 5 Cl 2 Terlihat kebutuhan permanganat menjadi lbh banyak karena dibutuhkan untuk reaksi samping. klor yang terbentuk dalam reaksi harus mengoksidasi Fe 2+ mengikuti reaksi 2 Fe 2+ + Cl 2 2 Fe 3+ + 2 Cl- Jika semua klor ada di larutan, banyaknay besi yang teroksidasi ekivalen dengan banyaknya permanganat yg diperlukan dlm pembentukan reaksi samping Cl 2. Namun dalam praktek beberapa klor menguap dan ini Mengakibatkan penggunaan permanganat menjadi lbh Banyak.

Beberapa sistim redoks CERIMETRI Lrt stand : Ce(IV) Sulfat (oksidator) dpt digunakan spt lrt std KMn. O 4 dg sistem Titrasi Kembali dg lrtn stand Na. Oksalat Ce 4+ Ce 3+ kuning tdk berwarna krg terdukung perlu indikator (NH 4)2 Ce(NO 3)6 / HCl. O 4 Amonium Heksa Nitro Serat dlm HCl. O 4 Indikator : α Penantroline , Feroin. Rentang Eind 1, 0 1, 2 volt /SHE
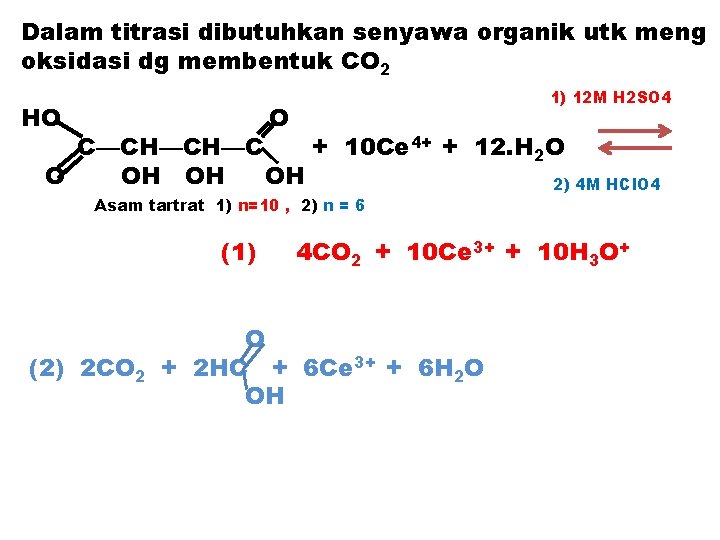
Dalam titrasi dibutuhkan senyawa organik utk meng oksidasi dg membentuk CO 2 HO 1) 12 M H 2 SO 4 O C—CH—CH—C + 10 Ce 4+ + 12. H 2 O O OH OH OH 2) 4 M HCl. O 4 Asam tartrat 1) n=10 , 2) n = 6 (1) (2) 2 CO 2 4 CO 2 + 10 Ce 3+ + 10 H 3 O+ O + 2 HC + 6 Ce 3+ + 6 H 2 O OH
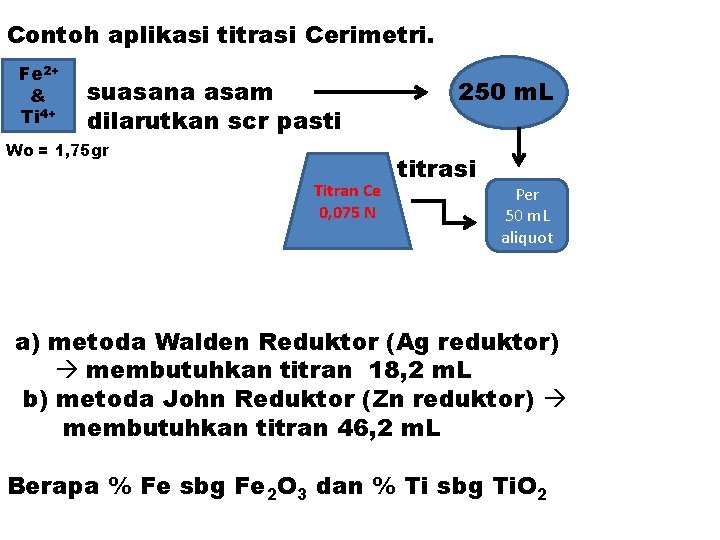
Contoh aplikasi titrasi Cerimetri. Fe 2+ & Ti 4+ suasana asam dilarutkan scr pasti Wo = 1, 75 gr Titran Ce 0, 075 N 250 m. L titrasi Per 50 m. L aliquot a) metoda Walden Reduktor (Ag reduktor) membutuhkan titran 18, 2 m. L b) metoda John Reduktor (Zn reduktor) membutuhkan titran 46, 2 m. L Berapa % Fe sbg Fe 2 O 3 dan % Ti sbg Ti. O 2

Reaksi yang terjadi pada Walder Reduktor. Walden Reduktor Ag(s) + Ce. Fe 3+ + e- Ag. Cl(s) + e- Fe 2+ Ti. O 2+ Reaksi yang terjadi pada John Reduktor Zn(s) Fe 2+ + e- Zn 2+ + 2 e- Fe 3+ Ti. O 2+ + 2 H 3 O+ + e- Ti 3+ + 3 H 2 O

Penyelesaian soal : Dari Walden R Fe 3+ Ti Fe 2+ n=1 meq Fe 2 O 3 setara meq titran Cerri meq Ce = 18, 2 x 0, 075 W Fe 2 O 3 (mg) ----------- = meq Fe 2 O 3 Mr Fe 2 O 3 / n WFe 2 O 3 = 0, 075 x 18, 2 x 100 = 136. 5 mg per 50 m. L W Fe 2 O 3 dalam sampel = 136, 5 x 250/50 = 682, 5 mg = 39 %

Dari John Red Fe dan Ti tereduksi Fe 3+ Fe 2+ Ti 4+ Ti 3+ meq titran = setara meq Fe 3+ + Ti 4+ W. Ti. O 2 (mg) 46, 2 x 0, 075 = ---------- + meq Fe 2 O 3 Mr. Ti. O 2 / n W. Ti. O 2 (mg) 3, 465 mg = ------- + 1, 365 mg 35/1 W. Ti. O 2 (mg) = (3, 465 – 1, 365) x 35 = 73, 5 mg`/ 50 m. L dlm sampel = 73, 5 x 5 =367, 5 mg =367, 5 / 1750 x 100 % = 21 %

PEMANGANOMETRI Metoda titrimetri dg larutan standard KMn. O 4 Titran KMn. O 4 oksidator kuat (+) * sbg self indikator titran * TE ditunjukkan oleh perubahan warnanya sendiri ungu jambon tidak berwarna. (-) * kekuatan oksidasi tergantung medium larutan, asam , netral, basa kuat. & reaksi yg terjadi * dlm medium HCl, KMn. O 4 teroksidasi oleh Cl* Kestabilan larutan terbatas * larutan standard sekunder (perlu standardisasi)

Penggunaan KMn. O 4 1. SUASANA ASAM 0, 1 N Mn. O 4 - + 8 H+ + 5 e. Mn. O 4 - + 8 H 3 O+ + 5 e. Mn 7+ Mn 2+ n=5 2. SUASANA NETRAL Mn. O 4 - + 4 H 3 O+ + 3 e. Mn 7+ Mn. O 2 n=3 3. SUASANA BASA KUAT Mn. O 4 - + e. Mn. O 42 - Mn 2+ + 4 H 2 O Mn 2+ + 12 H 2 O Eo = 1, 51 volt Mn. O 2 + 6 H 2 O Eo = 0, 1695 volt n = 1 Eo = 0, 564 volt

Larutan KMn. O 4 dlm air tdk stabil air teroksidasi 4. Mn. O 4 - + 2. H 2 O 4. Mn. O 2 + 3. O 2 + 4. OH- Perurian dikatalis adanya : cahaya, panas, asam, basa Mn 2+ Mn. O 2 dekomposisi sendiri bersifat auto katalitik S STANDARDISASI KMn. O 4 Larutan (standrd 1 o) utk standardisasi KMn. O 4 : Oksalat, Naoksalat (banyak digunakan), As 2 O 3, K 4[Fe(CN)6]3 H 2 O, logam besi dll

Lart stand primer hrs murni secara kimia, sesuai dg rumus mol, mudah dimurnikan. Na 2 C 2 O 4 mudah dimurnikan dg rekristalisasi dari air & pengeringan pada suhu 240 – 250 o. C. tdk higroscopis dan tdk berubah pd penyimpanan. Asam Oksalat agak lbh sukar dimurnikan krn mengandung air kristal bisa berkembang. Untuk mempersiapkan lrt stand KMn. O 4 harus bebas / dihindarkan dari Mn. O 2

Persamaan Reaksi standardiasi KMn. O 4 *) 2. Na 2 C 2 O 4 + 2. KMn. O 4 + 8. H 2 SO 4 2. Mn. SO 4 + K 2 SO 4 + 5. Na 2 SO 4 + 8. H 2 O + 10. CO 2 *) 5. H 2 C 2 O 4 + 2. KMn. O 4 + 3. H 2 SO 4 2. Mn. SO 4 + K 2 SO 4 + 8. H 2 O + 10. CO 2 Dari kedua reaksi ion C 2 O 42 - teroksidasi sbb C 2 O 42 - 2 CO 2 + 2 e- shg 1 grek as. Oksalat = 1 mol 1 grek Na. Oksalat = ½ mol [ lrt stnd ] = 0, 02 N

Contoh aplikasi analisa a. Lrt KMn. O 4 distandardisasi dg lrt sdt 1 o Na 2 C 2 O 4 Bila 282 mg Naoksalat membutuhkan 35, 87 m. L KMn. O 4 pada TE hitung berapa N KMn. O 4 b. Lrt KMn. O 4 (a) dipakai utk menentukan Mn 2+ Hitung % Mn dalam sampel mineral, bila 487, 4 mg sampel membutuhkan 45, 73 m. L lrt KMn. O 4 pd TE Pemecahan soal : dengan tinjauan Normalitas. a) Meq KMn. O 4 setara meq Na 2 C 2 O 4 pada TE W. Na 2 C 2 O 4 (mg) NKMn. O 4 x V = -------------Mr. Na 2 C 2 O 4 / n

Na 2 C 2 O 4 C 2 O 4 = 2 Na+ + C 2 O 4= 2 CO 2 + 2 e- 282, 0 N x 35, 87 = -------134, 0 / 2 n=2 [KMn. O 4] = 0, 1173. N Dalam suasana asam n = 5 [KMn. O 4] dalam Molar 0, 1173 / 5 = 0, 02347 M b) Meq Mn 2+ setara meq Mn. O 4 - pada TE Reaksi yg terjadi 2 Mn. O 4 - + 3 Mn 2+ + 4 OHn=3 5 Mn. O 2 + 2 H 2 O

Kekuatan oks KMn. O 4 3/5 x 0, 1173 N = 0, 0704 N W. Mn (mg) ---------- = N x m. L ------- = 0, 074 x 45, 73 Mr. Mn / n 54, 94/2 W. Mn (mg) 88, 44 = 88, 44 mg % = ------ x 100 % = 487, 4 = 18, 15 % 1) Coba selesaikan pemecahan soal dengan Tinjauan konsentrasi dalam mol (M) 2) Tugas materi Bikromatometri dan Iodo-iodimetri.

Pemecahan dg tinjauan molar. (M) Standardisasi mengikuti persamaan reaksi 2. Mn. O 4 - + 5. C 2 O 4 + 6. H 3 O+ 2. Mn 2+ + 10. CO 2 + 8. H 2 O mmol KMn. O 4 = mmol Na 2 C 2 O 4 x 2/5 = W. Na 2 C 2 O 4 2 282, 0 2 ---------- x ----- = ----- x ------- = 0, 8418 mmol Mr. Na 2 C 2 O 4 5 134, 0 5 0, 8418 mmol KMn. O 4 = [ ] M x V m. L = [ ] M x 35, 87 0, 8418 [KMn. O 4] M = ------- = 0, 02347 M 5 x 0, 02347 = 35, 87 0, 1173 N.

2 Mn. O 4 + 3. Mn+ + 4 OH- 5. Mn. O 2 + 2. H 2 O Sesuai stokhiometri mmol Mn dlm mineral setara mmol KMn. O 4 x 3/2 3 Mmol Mn = [ ] M x V m. L x -----2 = 0, 02347 x 45, 37 x 3/2 = 1, 610 mmol Kand Mn dlm mineral = 1, 610 mmol x 54, 94 mg/mol = 88, 44 mg % Mn = --------- x 100 % = 18, 5% 487, 4 mg

Aplikasi metoda permanganometri Beberapa contoh * Penentuan Ferro ( Ferro teroksidasi Ferri) Reaksi yg terjadi: 10. Fe. SO 4 + 2. KMn. O 4 + 8 H 2 SO 4 2 Mn. SO 4 + 5. Fe 2(SO 4)3 + K 2 SO 4 + 8. H 2 O Σ besi dihitung dari vol lrt KMn. O 4 yg diperlukan dg normalitasnya. * Penentuan H 2 O 2 Berdasar reaksi : 5 H 2 O 2 + 2. Mn. O 4 - + 6. H+ 5 O 2 +2. Mn 2+ + 8. H 2 O teroksidasi Pereduksi H 2 O 2 + 2 H+ + 2 e- 1 grek H 2 O 2 = ½ mol

H 2 O 2 perdagangan mengandung sekitar 3%, maka untuk penetapan hrs diencerkan dlm vol tertentu kira-kira 250 m. L). Titrasi dilakukan 3 kali per 25 m. L, diasamkam dg 5 – 10 m. L H 2 SO 4 (1: 4), Kadar H 2 O 2 berdasar rerata vol titran yg digunakan. • Penentuan Nitrit Berdasar reaksi : 5. NO 2 - + 2. Mn. O 4 - + 6 H+ Krn oks ion NO 2 - + H 2 O 5. NO 3 - + 2. Mn 2+ + 3. H 2 O NO 3 - + 2. H+ + 2 e- n = 2 1 grek NO 2 - = ½ mmol Ciri khusus penetapan ini, nitrit siap terurai oleh H + Nitrogen oksida. NO 2 - + 2 HNO 2 NO(g) + NO 2(g) + H 2 O
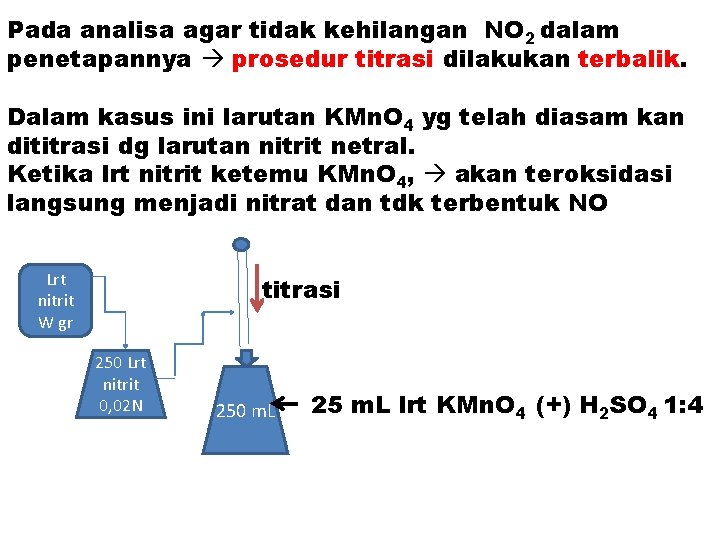
Pada analisa agar tidak kehilangan NO 2 dalam penetapannya prosedur titrasi dilakukan terbalik. Dalam kasus ini larutan KMn. O 4 yg telah diasam kan dititrasi dg larutan nitrit netral. Ketika lrt nitrit ketemu KMn. O 4, akan teroksidasi langsung menjadi nitrat dan tdk terbentuk NO Lrt nitrit W gr titrasi 250 Lrt nitrit 0, 02 N 250 m. L 25 m. L lrt KMn. O 4 (+) H 2 SO 4 1: 4

BIKROMATOMETRI Titran K 2 Cr 2 O 7 oksidator kuat. Eo = 1, 33 volt (+) • Lrt stnadard primer , Stabil, tdk perlu tempat glp. • Tidak terurai pada pemanasan, penguapan asam • Rekristalisasi dari lrt nya dan pengeringan t=200 o. C memungkinkan diperoleh dg kemurnian tinggi. (-) • Kekuatan oks lebih lemah dari KMn. O 4 dan Cerri • Reaksi lambat • Karsinogen perlu penanganan hati-hati. • Sbg zat pengoksid terjadi peningkatan Cr 3+ slm titrasi, orange warna hijau (sukar diamati pad TE) • Perlu indikator, indikator redoks yg biasa di pakai : as difenilamin-sulfnt Ba difenilamin-sulfnt
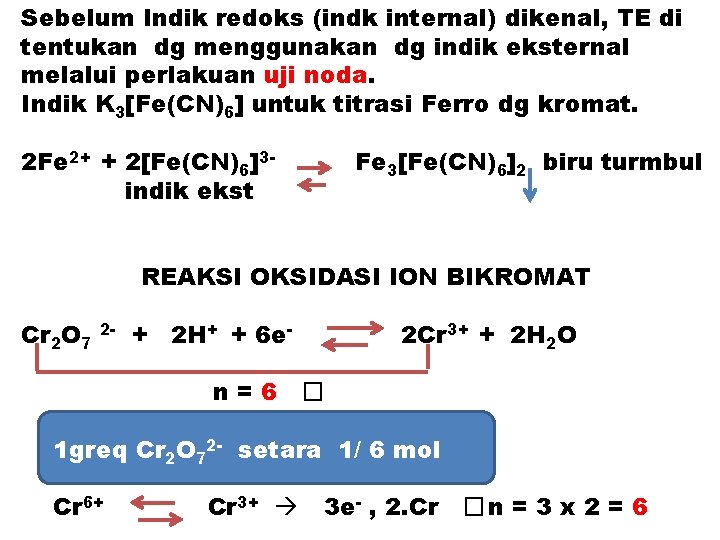
Sebelum Indik redoks (indk internal) dikenal, TE di tentukan dg menggunakan dg indik eksternal melalui perlakuan uji noda. Indik K 3[Fe(CN)6] untuk titrasi Ferro dg kromat. 2 Fe 2+ + 2[Fe(CN)6]3 indik ekst Fe 3[Fe(CN)6]2 biru turmbul REAKSI OKSIDASI ION BIKROMAT Cr 2 O 7 2 - + 2 H+ + 6 en=6 2 Cr 3+ + 2 H 2 O � 1 greq Cr 2 O 72 - setara 1/ 6 mol Cr 6+ Cr 3+ 3 e- , 2. Cr �n = 3 x 2 = 6

Aplikasi penting metoda bikromat penetapan besi Dalam bijih, slag (ampas bijih), dan alloy. Sampel dilarutkan besi diperoleh dlm bntk ion Fe 3 Shg perlu direduksi Fe 2+ dg Sn. Cl 2 dan dikuti menghilangkan kelebihan Sn. Cl 2 dg Hg. Cl 2 / dg amalgm Pereduksi yg sering digunakan adalah log seng. Reaksi yg terjadi 2. Fe 3+ + Zn 2. Fe 2+ + Zn 2+ Penentuan berikutnya ferro dititrasi dg lrt bikromat. Contoh aplikasi metoda bikromatometri Penentuan besi dalam bijih besi. Indk difenilamin Setelah besi direduksi Fe 2+, dititrasi dg bikromat Mengikuti reaksi : K 2 Cr 2 O 7 + 6. Fe. Cl 2 + 14 HCl 2 Cr. Cl 3 + 2 KCl + 6 Fe. Cl 3 + 7 H 2 O
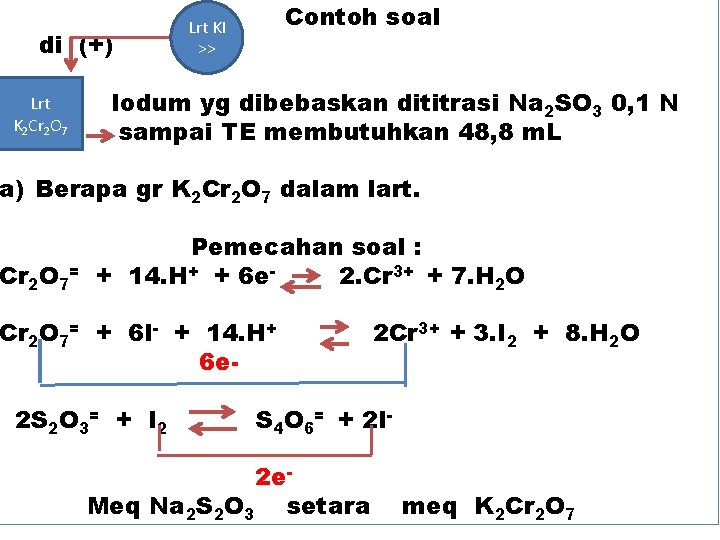
di (+) Lrt K 2 Cr 2 O 7 Contoh soal Lrt KI >> Iodum yg dibebaskan dititrasi Na 2 SO 3 0, 1 N sampai TE membutuhkan 48, 8 m. L a) Berapa gr K 2 Cr 2 O 7 dalam lart. Cr 2 O 7= Pemecahan soal : + 14. H+ + 6 e 2. Cr 3+ + 7. H 2 O Cr 2 O 7= + 6 I- + 14. H+ 6 e 2 S 2 O 3= + I 2 2 Cr 3+ + 3. I 2 + 8. H 2 O S 4 O 6= + 2 I- 2 e. Meq Na 2 S 2 O 3 setara meq K 2 Cr 2 O 7

V x Ntio setara meq K 2 Cr 2 O 7 294, 18 Mr, K 2 Cr 2 O 7 48, 8 x 0, 1 x ------ = W. K 2 Cr 2 O 7 6 0, 2393 gr = berat bikromat b) Bila berat bikromat di a) dilarutkan dalam volume 1 liter, berapa vol diperlukan utk menitrasi 3. 402 gr Fe. SO 47 H 2 O dalam suasana asam. Solusi : * cari N K 2 Cr 2 O 7, * TE meq K 2 Cr 2 O 7 setara meq Fe. SO 47 H 2 O
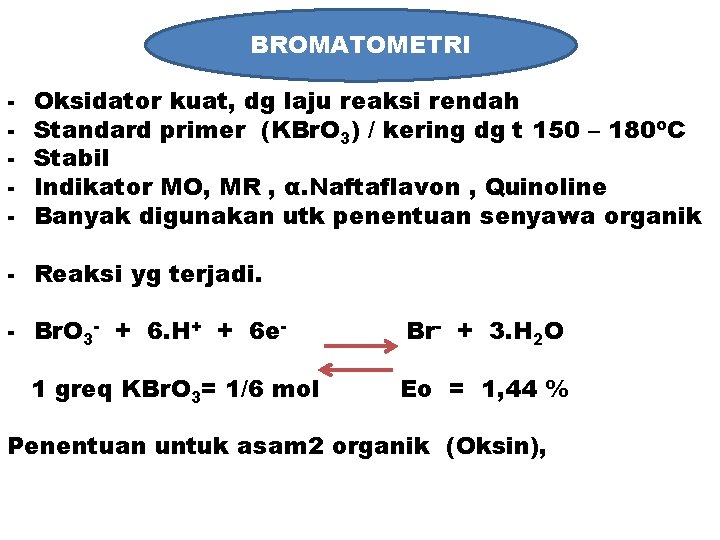
BROMATOMETR I KBr. O 3 BROMATOMETRI - Oksidator kuat, dg laju reaksi rendah Standard primer (KBr. O 3) / kering dg t 150 – 180 o. C Stabil Indikator MO, MR , α. Naftaflavon , Quinoline Banyak digunakan utk penentuan senyawa organik - Reaksi yg terjadi. - Br. O 3 - + 6. H+ + 6 e 1 greq KBr. O 3= 1/6 mol Br- + 3. H 2 O Eo = 1, 44 % Penentuan untuk asam 2 organik (Oksin),

Dari reaksi terlihat untuk konversi Br. O 3 - perlu H+ Untuk mempercepat reaksi konversi dilakukan pe manasan dalam asam kuat. Selama titrasi ion Br. O 3 - tereduksi Br 2 , kelebihan Ion ini menyebabkan warna kuning pucat, shg kurang Tegas pada penentuan TE perlu indikator z. warna MO atau MR (indikator ini tdk reversibel shg tdk ter masuk ind redoks) Aplikasi bromatometri banyak digunakan utk penentuan arsen dan antimon valensi III, penetapan dilaku kan dg adanya Sn val IV

Penentuan antimon dlm tartar emetic Tartar emetic tartar dr antimon trivalen dg rumol K(Sb. O)C 4 H 4 O 6. Ketika lrt garam ini dititrasi dg KBr. O 3 dg adanya HCl Terjadi reaksi : 3. K(Sb. O)C 4 H 4 O 6 + KBr. O 3 + 15. HCl 3. Sb. Cl 5 + KHC 4 H 4 O 6 + KBr + 6. H 2 O Dalam reaksi Sb (III) Sb (V) 2 e- tertransfer 1 greq Sb = ½ mol Indikator yg biasa digunakan Metil Jingga atau Metil merah.
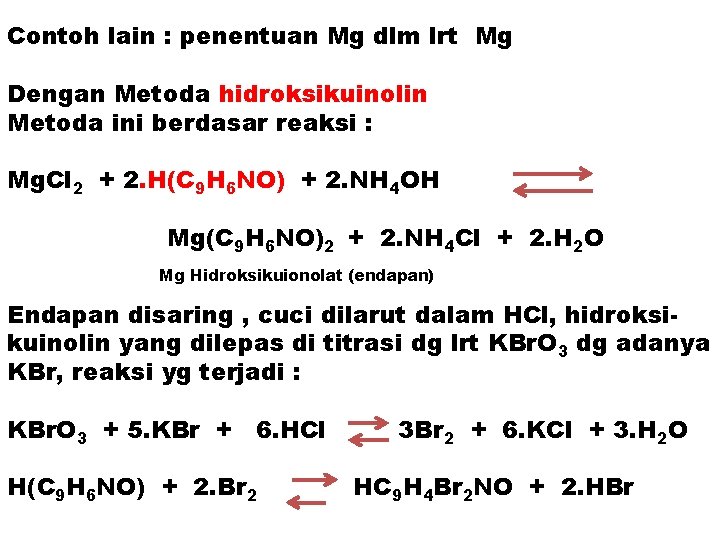
Contoh lain : penentuan Mg dlm lrt Mg Dengan Metoda hidroksikuinolin Metoda ini berdasar reaksi : Mg. Cl 2 + 2. H(C 9 H 6 NO) + 2. NH 4 OH Mg(C 9 H 6 NO)2 + 2. NH 4 Cl + 2. H 2 O Mg Hidroksikuionolat (endapan) Endapan disaring , cuci dilarut dalam HCl, hidroksikuinolin yang dilepas di titrasi dg lrt KBr. O 3 dg adanya KBr, reaksi yg terjadi : KBr. O 3 + 5. KBr + 6. HCl H(C 9 H 6 NO) + 2. Br 2 3 Br 2 + 6. KCl + 3. H 2 O HC 9 H 4 Br 2 NO + 2. HBr

Dari persamaan reaksi terlihat 1 atom Mg ekuivalen dg 2 mol hidroksikuinolin, yang masing-masing ekui valen dg 4 atom Br, 1 greq Mg = 1/8 mol Metoda ini mempunyai presisi analisis 0, 03 mg lbh tinggi dr metoda gravimetri sbg Mg 2 P 2 O 7 metoda ini dapat digunakan untuk penentuan Mg dengan adanya Al 3+ dan Fe 3+ , yg sebelumnya diubah dulu menjadi kompleks tartratnya.

IDO -IODIMETRI * Kalium iodat KIO 3 banyak dipakai dlm Kimia Analit IO 3 - + 5 I- + 6. H+ 3 I 2 + 3. H 2 O * Pemakaian iodium sbg reagen Redoks reduktor * Sistim iodium dapat berfungsi oksidator I 2(s) + 2 e. I 3 - + 2 e- 2 I 3 I- Eo = 0, 5345 volt Eo = 0, 536 volt * I 2 oksidator lemah , iodida reduktor lemah * Kelarutan KIO 3 dlm air cukup baik

* I 2 larut dalam KI * Perlu disimpan ditempat dingin gelap * Bukan standard primer perlu standardisasi dg *) As 2 O 3 dan *) Na 2 S 2 O 3. 5 H 2 O lrt thio sulfat perlu di standardisasi lebih dulu dg K 2 Cr 2 O 7 • indikator amilum / kanji • (I-) << 10 -5 M dapat ditekan dg mudah oleh amilum • Kelarutan I- -- Amilum << dlm air pe (+) nya dila kukan mendekati TE / TA.

Reaksi – reaksi yang terjadi a. Iodium – thiosulfat larutan iodium dalam KI dg suasana netral / asam I 3 - + 2. S 2 O 3= 3 I- + S 4 O 6= Selama titrasi S 2 O 3 I- terbentuk, Tahap reaksi yg terjadi : S 2 O 3 = + I 3 - S 2 O 3 I - + I - S 4 O 6 = + I 3 - S 2 O 3 I - + S 2 O 3 = p. H 5 S 4 O 6 = + larutan tidak ber warna titrasi I- berjalan warna indk muncul.

b. Reaksi dg Cu Kelebihan KI bereaksi dg Cu 2+ Cu. I + I 2 2. Cu 2+ + 4. I- 2. Cu. I + 4. I 2 2. Cu 2+ + 3. I- 2. Cu. I + 4 I 3 - I- sbg reduktor Cu 2+ + e- Cu+ Eo = 0, 15 volt I 2 + 2. e- 2 I- Eo = 0, 54 volt Cu 2+ + I- + e- Cu. I Eo = 0, 86 volt Hasil terbaik dilakukan pd p. H 4. dan 4% KI, suasana Basa Cu 2+ sulit dioksidasi.

Penmbahan lrt thio Na 2 S 2 O 3 dilakukan perlahan Lahan krn iodium yg teradsorbsi dilepas sedikit demi sedikit. Adanya Cl- akan mengganggu reaksi pada saat titrasi berlangsung. Iodida tdk mampu mereduksi Cu 2+ secara kuantitatif. c. Reaksi dengan O 2 terlarut. Metode ini pemanfaatan reaksi ini adalah metode Winkler diapakai untuk menentukan O 2 terlarut Dilakukan pd p. H 9. Dasar metoda winkler

Dasar metoda Winkler * * • • reaksi O 2 dengan Mn 2+ dalam media alkali pe (+) H+ Mn. OH berubah Mn. I eq Iodium dengan O 2 terlarut dititrasi dg Na 2 SO 3 Pada p. H 9 • Reaksi yang terjadi : • 2 Mn 2+ + 4. OH + O 2 • Mn. O 2 + 4 H+ + 2. I- 2. Mn. O 2 + 2. H 2 O I 2 + Mn 2+ + 2. H 2 O • Sumber kesalahan penentuan O 2 terlarut karena • Adanya reduktor SO 3=, S 2 O 3=, Fe 2+, Mn 2+ • Kesalahan ini dpt diatasi dengan membandingkan • Lrt blanko terutama anal lingkungan terpolusi.

- Slides: 60