LOGO Reaksi Redoks Konsep Redoks 1 Pengikatan dan






















- Slides: 26

L/O/G/O Reaksi Redoks

Konsep Redoks 1 Pengikatan dan pelepasan Oksigen 2 Pengikatan dan Pelepasan Elektron 3 4 Perubahan bilangan Oksidasi





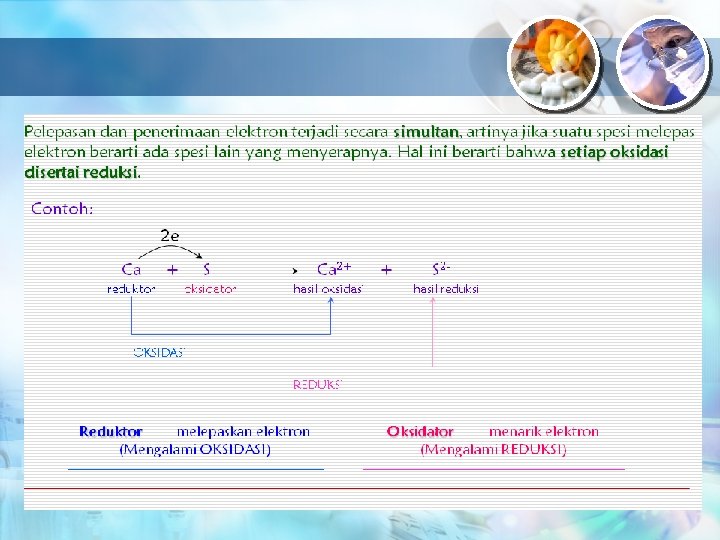
OKSIDATOR DAN REDUKTOR OKSIDATOR : Zat yang mengoksidasi zat lain, tetapi zat Tersebut mengalami reaksi reduksi (penurunan bilok) Ciri-ciri oksidator: § Memiliki bilok tinggi § Dalam bentuk molekul maupun ion mudah mengikat elek tron § Dalam sistim periodik unsur ada di sebelah kanan Contoh : KMNO 4 Mn bervalensi +7 K 2 Cr 2 O 7 Cr bervalensi +6 KCl. O 3 Cl bervalensi +5

OKSIDATOR DAN REDUKTOR Reduktor : zat yang mudah mereduksi zat lain, tetapi zat itu sendiri mengalami oksidasi (pening katan bilok) Ciri-ciri reduktor : § Memiliki bilok rendah § Dalam bentuk molekul maupun ion mudah melepaskan elektron § Dalam sistim periodik unsur, terletak di golongan : I, III, VI dan VII






Contoh Reaksi Redoks dalam Kehidupan

PENYETARAAN PERSAMAAN REDOKS Pengertian : Banyaknya elektron yang dilepaskan oleh reduktor harus sama dengan banyaknya elektron yang ditangkap oleh ok Sidator. 1. REAKSI SEDERHANA KCl K + Cl 2 Langkah-langkah : a. Cari perubahan bilok unsur-unsur b. Tulis reaksi oksidasi dan reduksi secara terpisah c. Kalikan masing-masing reaksi dengan bilangan tertentu untuk menyamakan elektron yang dilepas dan yang ditangkap

d. Jumlahkan kedua reaksi tersebut Penyelesaian contoh : K+ + 1 e ) x 2 K Cl 2 + 2 e 2 Cl- ) x 1 + 2 K Cl 2 + 2 e 2 K + Cl 2 2 K + 2 e 2 Cl+ 2 K + 2 Cl- 2 KCl

2. REAKSI DI LINGKUNGAN ASAM Syarat : harus diketahui perubahan biloknya. Contoh : Cu + HNO 3 Cu NO 3 - ? Cu 2+ (oksidasi) NO (reduksi) LANGKAH-LANGKAH : § § § Tulis masing-masing reaksi oksidasi dan reduksi secara terpisah, lengkapi dengan perubahan elektron Pihak yang kekurangan oksigen, ditambah H 2 O, yang kekurangan hidrogen tambahkan ion H+. Sempurnakan masing reaksi Kalikan masing-masing reaksi dengan bilangan tertentu untuk menyamakan jumlah elektron yang dilepas dan yang ditangkap

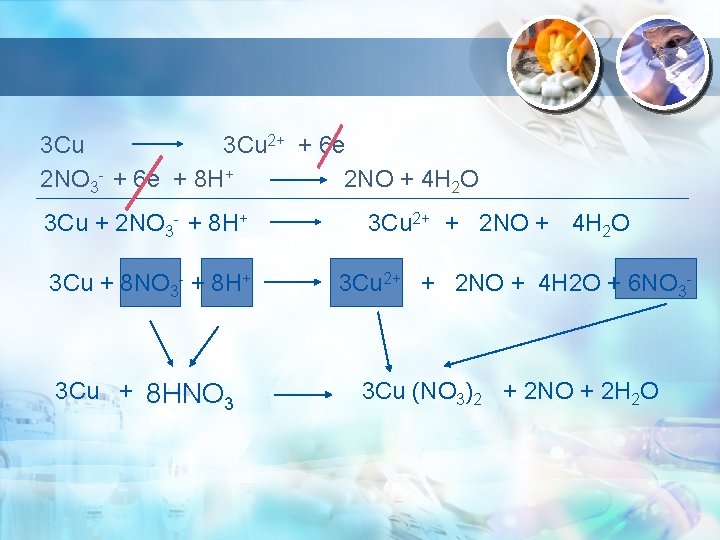
§ Jumlahkan kedua reaksi tersebut § Tulis hasil reaksi lengkap sesuai dengan zat yang bereaksi PENYELESAIAN CONTOH : Cu Cu 2+ + 2 e NO 3 - + 3 e NO Cu Cu 2+ + 2 e NO 3 - + 3 e + 4 H+ )x 3 NO + 2 H 2 O ) x 2 +

3 Cu 2+ + 6 e 2 NO 3 - + 6 e + 8 H+ 2 NO + 4 H 2 O 3 Cu + 2 NO 3 - + 8 H+ 3 Cu 2+ + 2 NO + 4 H 2 O 3 Cu + 8 NO 3 - + 8 H+ 3 Cu 2+ + 2 NO + 4 H 2 O + 6 NO 3 - 3 Cu + 8 HNO 3 3 Cu (NO 3)2 + 2 NO + 2 H 2 O

3. REAKSI DI LINGKUNGAN BASA Langkah –langkah : • Tulis masing-masing reaksi oksidasi dan reduksi secara terpisah, lengkapi dengan perubahan elektron • Pihak yang kekurangan oksigen, ditambah OH- yang kekurangan hidrogen tambahkan ion H 2 O. • Sempurnakan masing reaksi • Kalikan masing-masing reaksi dengan bilangan tertentu untuk menyamakan jumlah elektron yang dilepas dan yang ditangkap

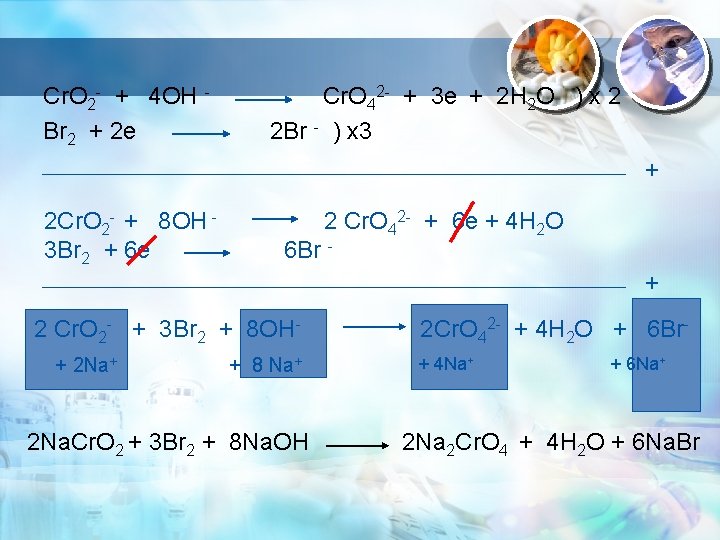
• Jumlahkan kedua reaksi tersebut • Tulis hasil reaksi lengkap sesuai dengan zat-zat yang bereaksi Contoh : Na. Cr. O 2 + Br 2 + Na. OH ? Diketahui : Cr. O 2 - Cr. O 42 - Br 2 Br- Penyelesaian : Cr. O 2 Br 2 + 2 e Cr. O 42 - + 3 e 2 Br -

Cr. O 2 - + 4 OH Br 2 + 2 e Cr. O 42 - + 3 e + 2 H 2 O ) x 2 2 Br - ) x 3 + 2 Cr. O 2 - + 8 OH 3 Br 2 + 6 e 2 Cr. O 42 - + 6 e + 4 H 2 O 6 Br - + 2 Cr. O 2 - + 3 Br 2 + 8 OH+ 2 Na+ + 8 Na+ 2 Na. Cr. O 2 + 3 Br 2 + 8 Na. OH 2 Cr. O 42 - + 4 H 2 O + 6 Br+ 4 Na+ + 6 Na+ 2 Na 2 Cr. O 4 + 4 H 2 O + 6 Na. Br

MENYEMPURNAKAN PERSAMAAN REDOKS (MENGISI KOEFISIEN REAKSI) Langkah-langkah : • Tentukan unsur-unsur yang mengalami perubahan bilok. Sertakan perubahan elektronnya. • Kalikan dengan bilangan tertentu untuk menyamakan jumlah elektron yang dilepas dan yang ditangkap. • Bilangan tersebut sebagai koefisien sementara. • Setarakan jumlah atom-atom, terutama H dan O di ruas kiri dan kanan.

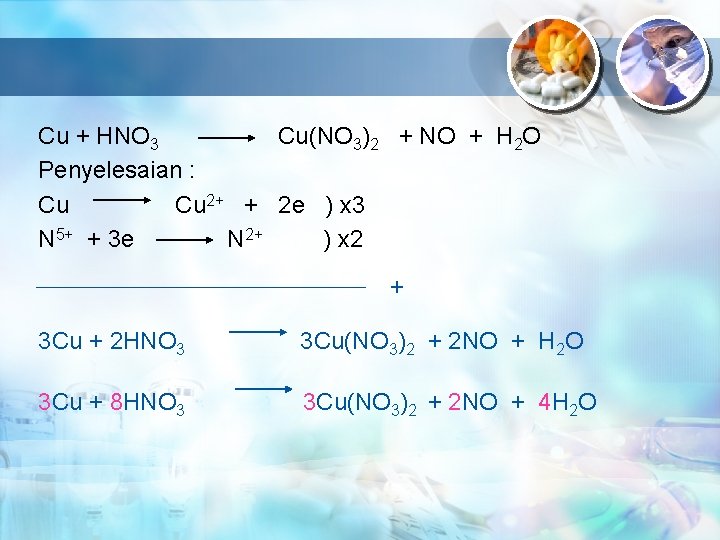
Cu + HNO 3 Cu(NO 3)2 + NO + H 2 O Penyelesaian : Cu Cu 2+ + 2 e ) x 3 N 5+ + 3 e N 2+ ) x 2 + 3 Cu + 2 HNO 3 3 Cu(NO 3)2 + 2 NO + H 2 O 3 Cu + 8 HNO 3 3 Cu(NO 3)2 + 2 NO + 4 H 2 O

LATIHAN SOAL : Isilah koefisien reaksi pada reaksi di bawah ini : KMn. O 4 + H 2 SO 4 + Fe. SO 4 KMn. O 4 + H 2 SO 4 + H 2 C 2 O 4 K 2 SO 4 + Mn. SO 4 + Fe 2(SO 4)3 + H 2 O K 2 SO 4 + Mn. SO 4 + CO 2 + H 2 O Catatan : pada reaksi pembakaran zat organik menghasilkan CO 2 dan H 2 O. Bilangan oksidasi C pada CO 2 adalah : +4. Tetapi bilangan oksidasi C dalam zat organik kebanyakan kurang dari 4. Misal pada H 2 C 2 O 4. Bilok C adalah +3

L/O/G/O Thank You!