REDOKS DAN SEL ELEKTROKIMIA PENYETARAN REAKSI REDOKS Dalam





















- Slides: 42

REDOKS DAN SEL ELEKTROKIMIA

PENYETARAN REAKSI REDOKS Dalam menyetarakan reaksi redoks JUMLAH ATOM dan MUATAN harus sama

Metode ½ Reaksi Langkah-langkah: 1. Tuliskan ½ reaksi reduksi / ½ reaksi oksidasi 2. Samakan jumlah atom-atom yang berubah biloksnya. 3. Samakan Jumlah O dan H dengan cara: a. Suasana Asam 4. 5. * Samakan O dengan menambahkan H 2 O 6. * Samakan jumlah H dengan Menambah H+ b. Suasana Basa 7. 8. 9. x * Samakan O dengan menambah OH- sebanyak 2 kekurangannya. * Samakan H dengan menambahkan H 2 O 10. 4. Samakan muatnnya dengan menambahkan elektron ( e- )

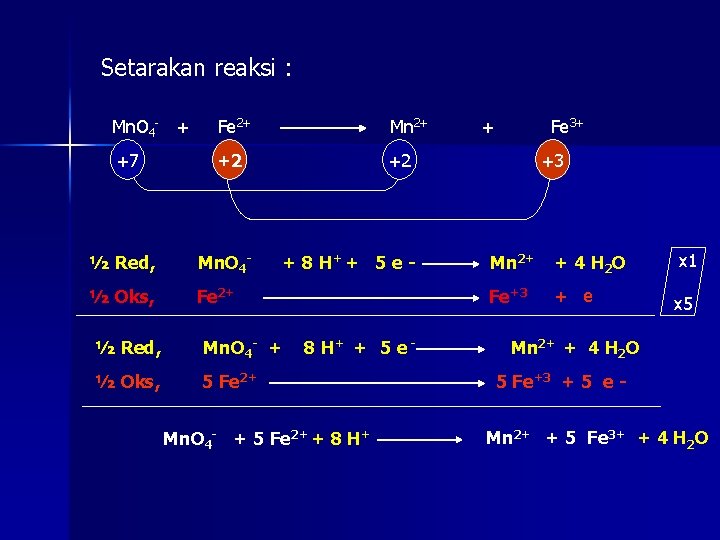
Setarakan reaksi : Mn. O 4 - + Fe 2+ Mn 2+ +7 +2 +2 ½ Red, Mn. O 4 - ½ Oks, Fe 2+ + 8 H+ + 5 e - ½ Red, Mn. O 4 - + ½ Oks, 5 Fe 2+ 8 H+ + 5 e - Mn. O 4 - + 5 Fe 2+ + 8 H+ + Fe 3+ +3 Mn 2+ + 4 H 2 O Fe+3 + e x 1 x 5 Mn 2+ + 4 H 2 O 5 Fe+3 + 5 e Mn 2+ + 5 Fe 3+ + 4 H 2 O

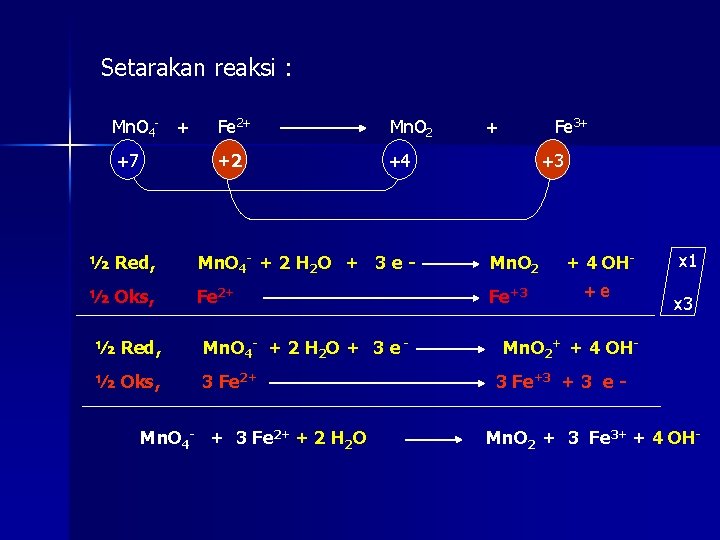
Setarakan reaksi : Mn. O 4 - + Fe 2+ Mn. O 2 +7 +2 +4 + Fe 3+ +3 ½ Red, Mn. O 4 - + 2 H 2 O + 3 e - Mn. O 2 ½ Oks, Fe 2+ Fe+3 ½ Red, Mn. O 4 - + 2 H 2 O + 3 e - ½ Oks, 3 Fe 2+ Mn. O 4 - + 3 Fe 2+ + 2 H 2 O + 4 OH+e x 1 x 3 Mn. O 2+ + 4 OH 3 Fe+3 + 3 e Mn. O 2 + 3 Fe 3+ + 4 OH-

Metode Bilangan Oksidasi 1. Tentukan reaksi ½ Reaksi redusi dan ½ Reaksi oksidasi’ 2. Samakan atom-atom yang berubah biloksnya. 3. Tentukan perubahan biloksnya. (dikalikan dengan jumlah atomnya) 4. Gunakan perubahan biloksnya sebagai koefisien dengan cara menyilangkan. 5. Setarakan muatanya, dalam suasana basa dengan OH-, dalam asam dengan H+ (sekaligus menyamakan H dan O )

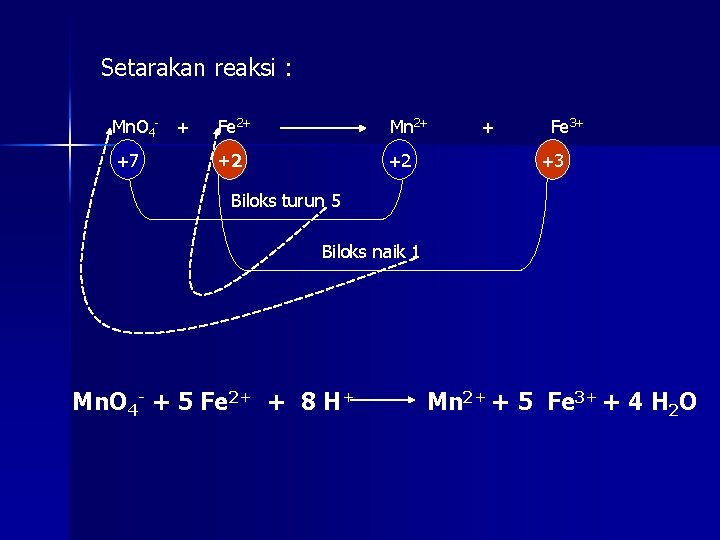
Setarakan reaksi : Mn. O 4 - + Fe 2+ Mn 2+ +7 +2 +2 + Fe 3+ +3 Biloks turun 5 Biloks naik 1 Mn. O 4 - + 5 Fe 2+ + 8 H+ Mn 2+ + 5 Fe 3+ + 4 H 2 O

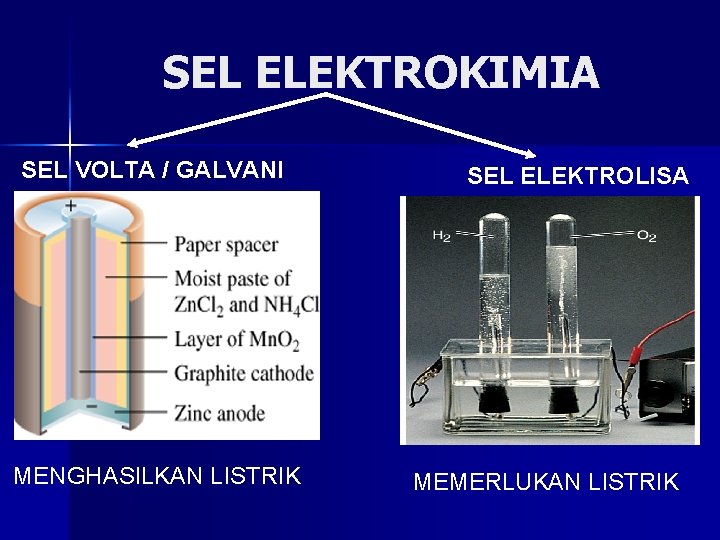
SEL ELEKTROKIMIA SEL VOLTA / GALVANI MENGHASILKAN LISTRIK SEL ELEKTROLISA MEMERLUKAN LISTRIK

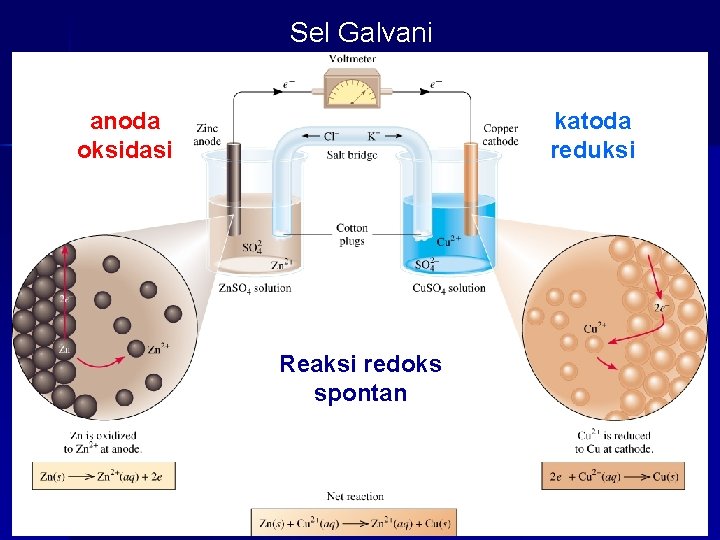
Sel Galvani anoda oksidasi katoda reduksi Reaksi redoks spontan 19. 2

PENULISAN PREAKSI PADA SEL VOLTA Ada 3 cara penulisan 1. Reaksi elektroda : menggambarkan reaksi pada masing -masing elektroda 2. Katoda : Cu 2+ + 2 e 3. Anoda : Zn Cu Zn 2+ + 2 e 2. Reaksi Sel: Merupakan penjumlahan dari reaksi elektroda. 3. Zn + Cu 2+ Zn 2+ + 3. Notasi Sel: Menggambarkan perubahan pada ion-ionnya. 4. Zn / Zn 2+ // Cu 2+/ Cu Cu

Standard Reduction Potentials Standard reduction potential (E 0) adalah potensial yang berkaitan dengan reaksi reduksi pada elektroda bila semua zat terlarut berkonsentrasi 1 M dan semua gas pada 1 atm. Reduction Reaction 2 e- + 2 H+ (1 M) E 0 = 0 V Standard hydrogen electrode (SHE) H 2 (1 atm)

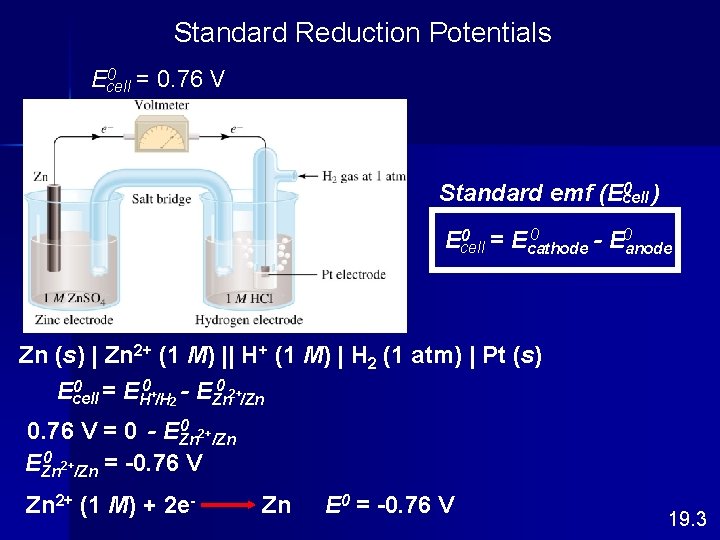
Potensial Reduksi Standar logam Zn Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) Anode (oxidation): Zn (s) Cathode (reduction): 2 e- + 2 H+ (1 M) Zn (s) + 2 H+ (1 M) Zn 2+ (1 M) + 2 e. H 2 (1 atm) Zn 2+ + H 2 (1 atm) 19. 3

Standard Reduction Potentials 0 = 0. 76 V Ecell 0 ) Standard emf (Ecell 0 0 = E 0 Ecell cathode - Eanode Zn (s) | Zn 2+ (1 M) || H+ (1 M) | H 2 (1 atm) | Pt (s) 0 = E 0 + - E 0 2+ Ecell H /H 2 Zn /Zn 0 2+ 0. 76 V = 0 - EZn /Zn 0 2+ EZn /Zn = -0. 76 V Zn 2+ (1 M) + 2 e- Zn E 0 = -0. 76 V 19. 3

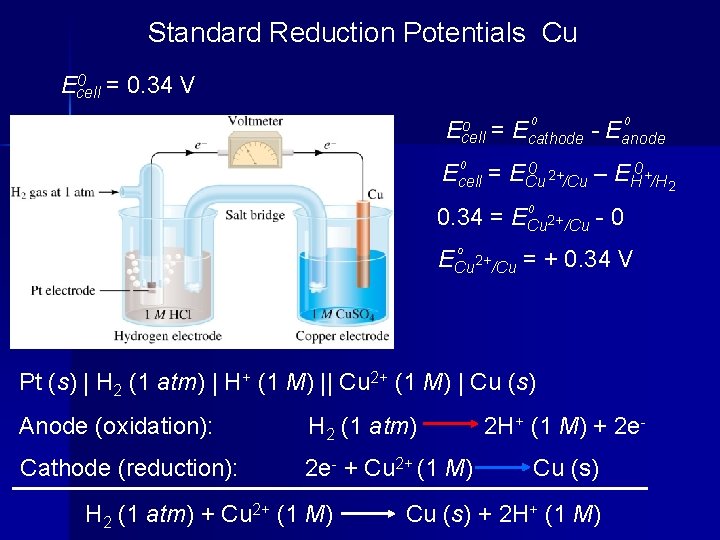
Standard Reduction Potentials Cu 0 = 0. 34 V Ecell 0 0 o = E Ecell cathode - Eanode 0 2+ 0 Ecell = ECu /Cu – EH +/H 2 0 0. 34 = ECu 2+ /Cu - 0 0 o ECu 2+/Cu = + 0. 34 V Pt (s) | H 2 (1 atm) | H+ (1 M) || Cu 2+ (1 M) | Cu (s) Anode (oxidation): H 2 (1 atm) Cathode (reduction): 2 e- + Cu 2+ (1 M) H 2 (1 atm) + Cu 2+ (1 M) 2 H+ (1 M) + 2 e. Cu (s) + 2 H+ (1 M)

Sel Galvani Perbedaan potensial listrik antara katoda dan anoda disebut: • cell voltage (potensial sel) • electromotive force (emf) (gaya gerak listrik • cell potential (potensial sel) Zn (s) + Cu 2+ (aq) Notasi Sel Cu (s) + Zn 2+ (aq) [Cu 2+] = 1 M & [Zn 2+] = 1 M Zn (s) | Zn 2+ (1 M) || Cu 2+ (1 M) | Cu (s) anoda katoda 19. 2

Berapa E sel yang tersusun atas elektroda Cd dalam 1, 0 M Cd(NO 3)2 dan elektroda Cr dalam 1, 0 M Cr(NO 3)3 ? (Data Eo lihat tabel Hal. 57. ) Cd 2+ (aq) + 2 e- Cd (s) E 0 = -0. 40 V Cd is the stronger oxidizer Cr 3+ (aq) + 3 e- Cr (s) Anode (oxidation): E 0 = -0. 74 V Cr 3+ (1 M) + 3 e- x 2 Cr (s) Cathode (reduction): 2 e- + Cd 2+ (1 M) 2 Cr (s) + 3 Cd 2+ (1 M) Cd will oxidize Cr Cd (s) x 3 3 Cd (s) + 2 Cr 3+ (1 M) 0 0 = E 0 Ecell cathode - Eanode 0 = -0. 40 – (-0. 74) Ecell 0 = 0. 34 V Ecell 19. 3

PERSMAAN NERNST Untuk kondisi larutan yang tidak standar (konsentrasi tidak 1 M ) maka Potensial sel ditentukan dengan persamaan Nernst. Esel = Eosel - 0, 0592 log K n EOsel pada keadaan standar (dicari dulu) n = Jumlah elektron yang terlibat dalam reaksi K = Tetapan kesetimbangan

n Soal No. 29 hal 60 Jawab: Esel = Eosel - 0, 0592 n log K n=2 Eosel= Eo. Cu - Eo. Zn Zn = +0, 34 – (-0, 76) Zn 2+ + 2 e Cu 2+ + 2 e = + 1, 10 Volt Esel = + 1, 10 - 0, 0592 2 = +1, 109 volt log 1 M 2 M Cu

n Soal No. 30 hal 60 Jawab: Esel = Eosel - 0, 0592 n Mg+2 log Ag+ n=2 Eosel= Eo. Ag - Eo. Mg = +0, 8 – (-2, 37) Mg Mg 2+ + 2 e 2 Ag+ + 2 e = + 3, 17 Volt Esel = + 3, 17 - 0, 0592 2 = + 3, 2292 volt log 0, 01 1 2 Ag

REAKSI AKAN BERLANGSUNG SPONTAN JIKA MEMILIKI HARGA EOSEL ( + ) REAKSI TIDAK AKAN BERLANGSUNG JIKA MEMILIKI HARGA EOSEL ( - )

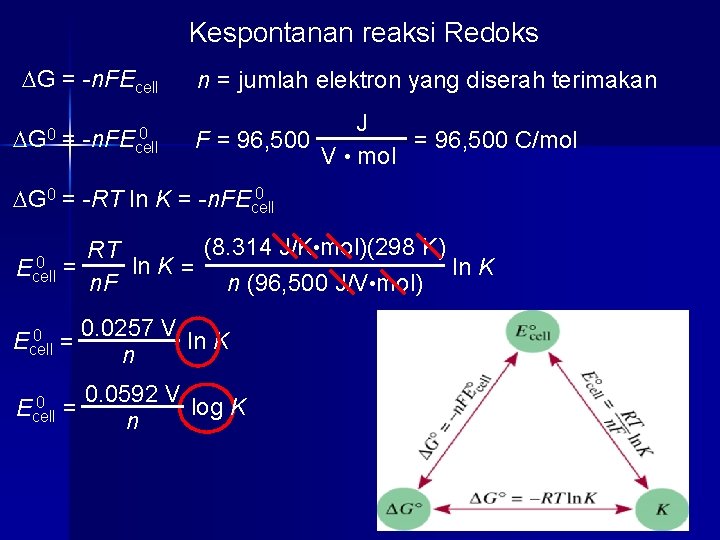
Kespontanan reaksi Redoks DG = -n. FEcell DG 0 = 0 -n. FEcell n = jumlah elektron yang diserah terimakan J F = 96, 500 C/mol V • mol 0 DG 0 = -RT ln K = -n. FEcell (8. 314 J/K • mol)(298 K) RT 0 = ln K Ecell n. F n (96, 500 J/V • mol) 0 Ecell = 0 Ecell 0. 0257 V ln K n 0. 0592 V log K = n

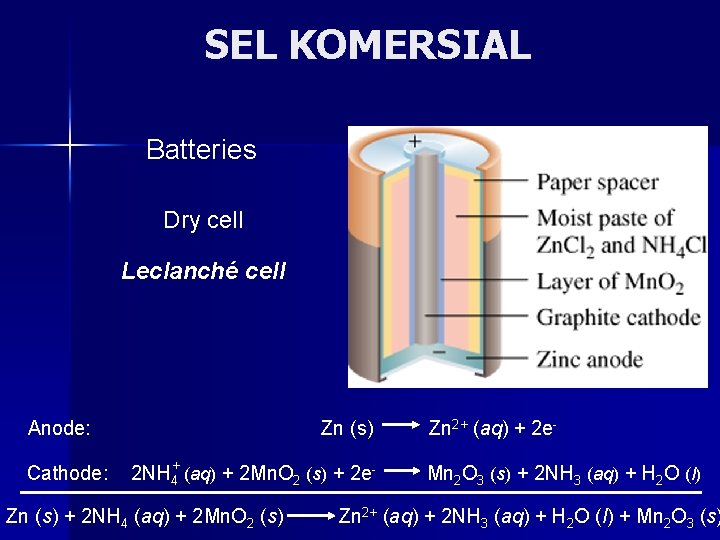
SEL KOMERSIAL Batteries Dry cell Leclanché cell Anode: Cathode: Zn (s) 2 NH 4+ (aq) + 2 Mn. O 2 (s) + 2 e- Zn (s) + 2 NH 4 (aq) + 2 Mn. O 2 (s) Zn 2+ (aq) + 2 e. Mn 2 O 3 (s) + 2 NH 3 (aq) + H 2 O (l) Zn 2+ (aq) + 2 NH 3 (aq) + H 2 O (l) + Mn 2 O 3 (s)

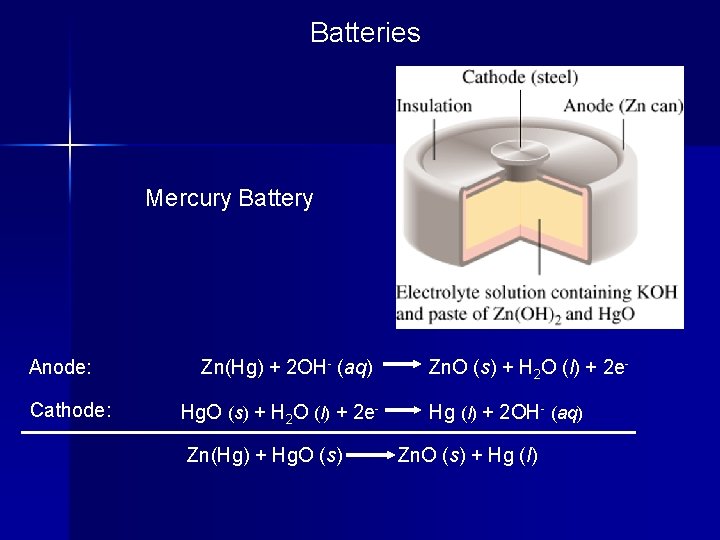
Batteries Mercury Battery Anode: Cathode: Zn(Hg) + 2 OH- (aq) Hg. O (s) + H 2 O (l) + 2 e. Zn(Hg) + Hg. O (s) Zn. O (s) + H 2 O (l) + 2 e. Hg (l) + 2 OH- (aq) Zn. O (s) + Hg (l)

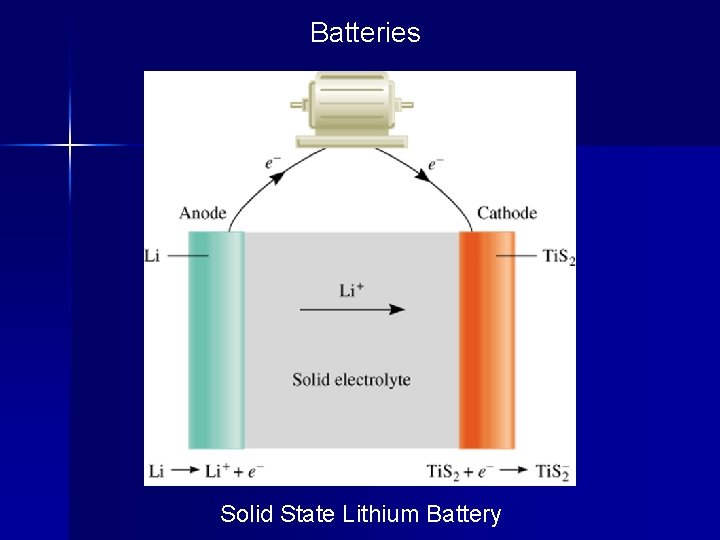
Batteries Solid State Lithium Battery

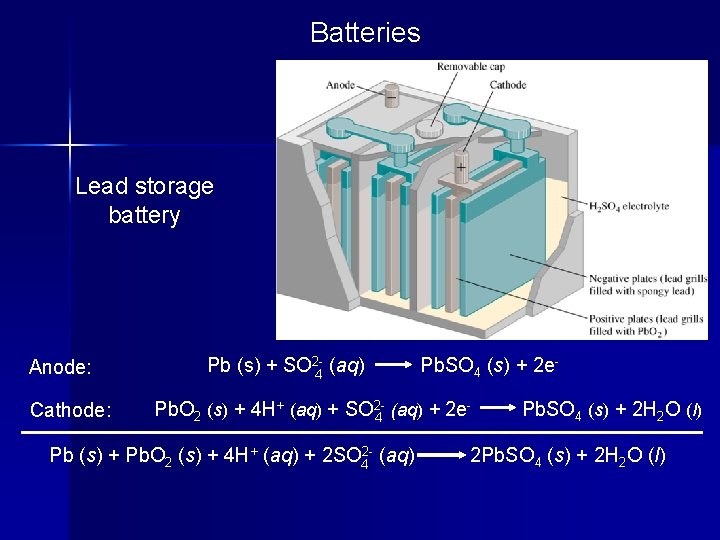
Batteries Lead storage battery Anode: Cathode: Pb (s) + SO 2 -4 (aq) Pb. SO 4 (s) + 2 e- Pb. O 2 (s) + 4 H+ (aq) + SO 24 (aq) + 2 e Pb (s) + Pb. O 2 (s) + 4 H+ (aq) + 2 SO 42 - (aq) Pb. SO 4 (s) + 2 H 2 O (l) 2 Pb. SO 4 (s) + 2 H 2 O (l)

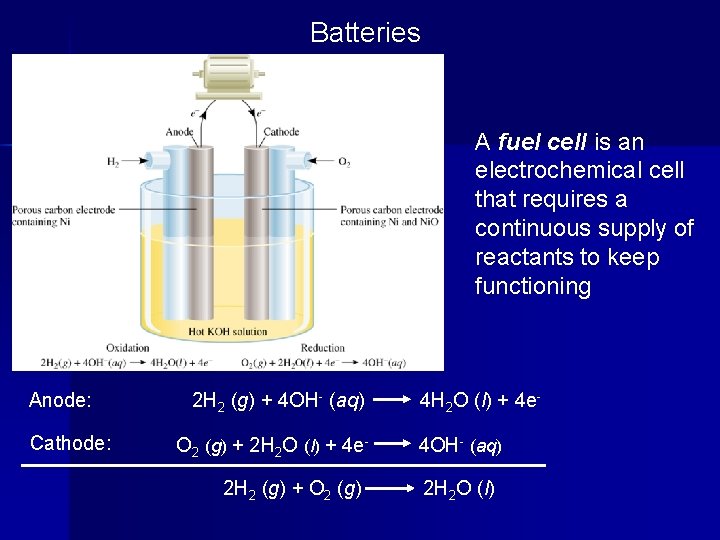
Batteries A fuel cell is an electrochemical cell that requires a continuous supply of reactants to keep functioning Anode: Cathode: 2 H 2 (g) + 4 OH- (aq) O 2 (g) + 2 H 2 O (l) + 4 e 2 H 2 (g) + O 2 (g) 4 H 2 O (l) + 4 e 4 OH- (aq) 2 H 2 O (l)

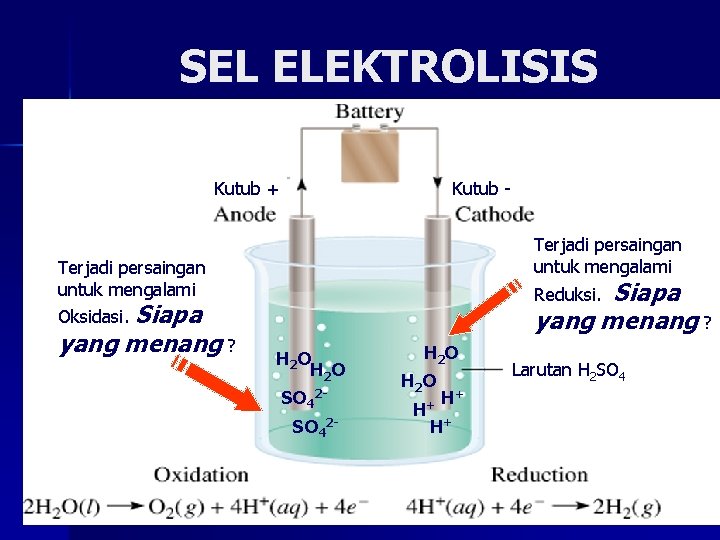
SEL ELEKTROLISIS Kutub + Kutub Terjadi persaingan untuk mengalami Siapa yang menang ? Reduksi. Oksidasi. H 2 O SO 42 - H 2 O H+ H+ H+ Larutan H 2 SO 4

REAKSI PADA ELEKTRODA Reaksi Pada Katoda ( - ) tergantung pada jenis kationnya (ion positif) * ion logam aktif (Gol I A, II A, Al dan Mn ) tidak direduksi yang direduksi air. 2 H 2 O + 2 e H 2 (g) + 2 OH- * Kation lain akan direduksi. Mx+ + x e M

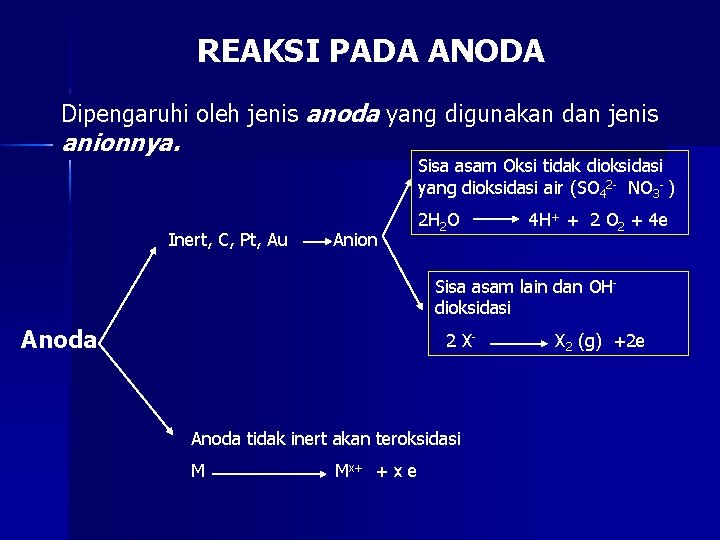
REAKSI PADA ANODA Dipengaruhi oleh jenis anoda yang digunakan dan jenis anionnya. Sisa asam Oksi tidak dioksidasi yang dioksidasi air (SO 42 - NO 3 - ) Inert, C, Pt, Au Anion 2 H 2 O 4 H+ + 2 O 2 + 4 e Sisa asam lain dan OHdioksidasi Anoda 2 X- Anoda tidak inert akan teroksidasi M Mx+ + x e X 2 (g) +2 e

Tuliskan reaksi yang terjadi di katoda dan anoda pada lektrolisis: a. Larutan KCl elektroda grafit. b. Larutan K 2 SO 4 elektroda grafit. c. Larutan Cu(NO 3)2 elektroda Cu d. Lelehan Mg. Cl 2 eletroda platina e. Larutan Na. OH elektroda grafit

Jawab A. Katoda (-) Reduksi 2 H 2 O + 2 e ----- H 2 + 2 OHB. Anoda (+) Anoda 2 Cl- ---- Cl 2 + 2 e B. Katoda (-) Reduksi 2 H 2 O + 2 e ----- H 2 + 2 OHAnoda (+) Anoda 2 H 2 O ---- O 2 + 4 H+ 4 e C. Katoda (-) Reduksi Cu 2+ + 2 e ------- Cu Anoda (+) Anoda Cu ------ Cu+2 + 2 e D. Katoda (-) Reduksi Mg 2+ + 2 e ------- Mg Anoda (+) Anoda 2 Cl- ---- Cl 2 + 2 e

HUKUM FARADAY Hukum Faraday I : Massa zat yang dibebaskan pada elektroda berbanding lurus dengan jumlah listrik ( Q ) yang digunakan. G ≈ Q Q = i. t G = i. t Kuat Arus Hukum Faraday II : Waktu (detik) Massa zat yang dibebaskan pada elektroda berbanding lurus dengan massa ekivalen zat itu. G ≈ ME Ar ME = Biloks k= 1 96500 C G = k. i. t. E G = i. t. E 96500 C

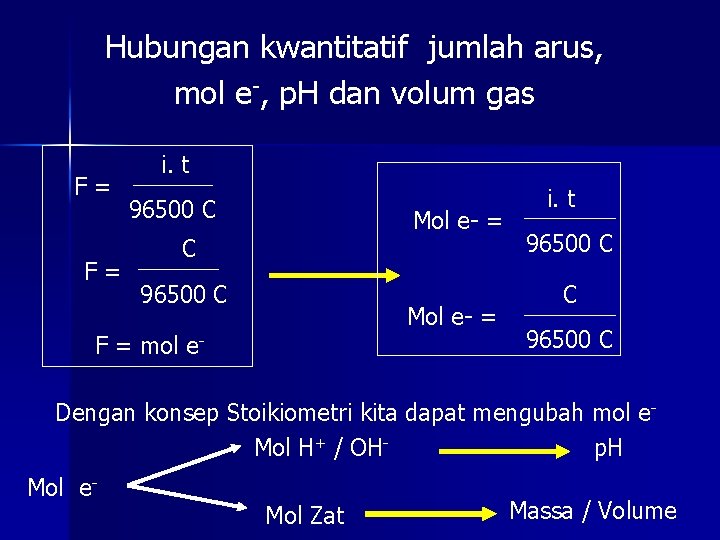
Hubungan kwantitatif jumlah arus, mol e-, p. H dan volum gas F= F= i. t 96500 C Mol e- = C 96500 C Mol e- = F = mol e- i. t 96500 C C 96500 C Dengan konsep Stoikiometri kita dapat mengubah mol e. Mol H+ / OHp. H Mol e- Mol Zat Massa / Volume

Soal: Jika kuat arus sebesar 5 Amper dilewatkan kedalam 1 liter larutan Cu. SO 4 selama 5 menit dengan menggunakan elektroda Pt. Maka tentukanlah : a. Reaksi elektrodanya b. Massa endapan yang terbentuk. Ar Cu 63, 5 c. Volume gas yang terbentuk. Diukur pada suhu 27 o. C tekanan 1 atm. d. p. H larutan setelah elektrolisis. (volume larutan dianggap idak berubah). Kerjakan soal-soal latihan yang ada pada buku ! No 45 s/d 50

Menurut Hukum Faraday II. Massa zat yang dihasilkan dalam elektrolisis berbanding lurus dengan Massa Ekivalen zat. Untuk beberapa sel yang disusun seri berlaku : G 1 : G 2 = E 1 : E 2

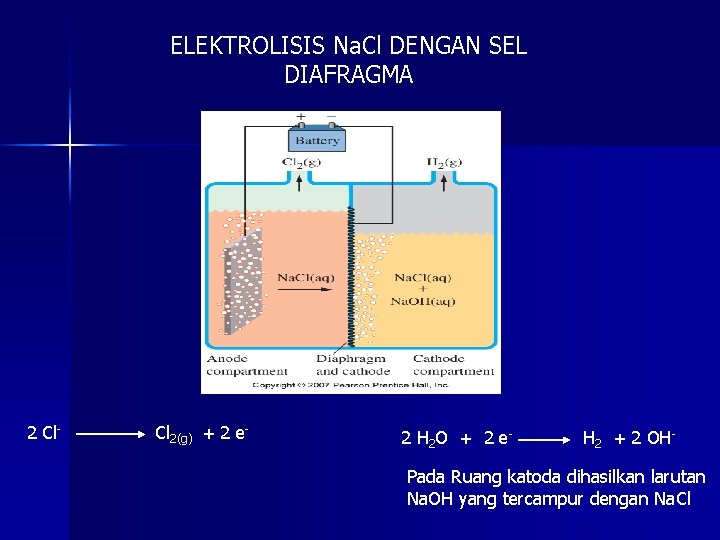
ELEKTROLISIS Na. Cl DENGAN SEL DIAFRAGMA 2 Cl- Cl 2(g) + 2 e- 2 H 2 O + 2 e - H 2 + 2 OH- Pada Ruang katoda dihasilkan larutan Na. OH yang tercampur dengan Na. Cl

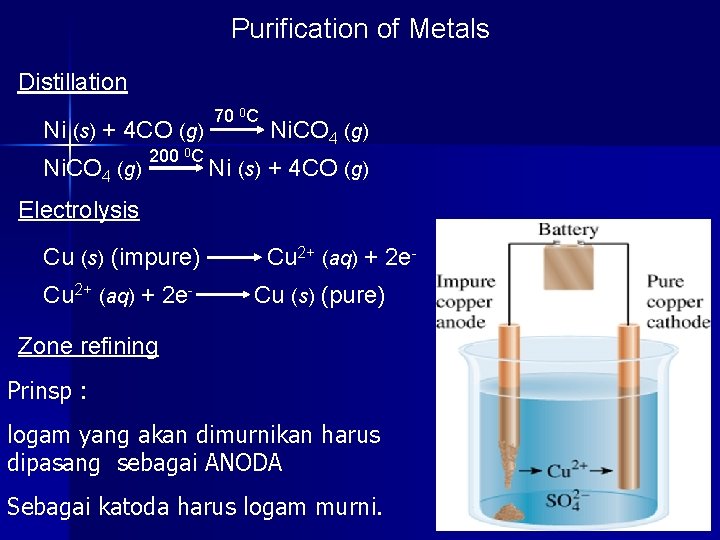
Purification of Metals Distillation Ni (s) + 4 CO (g) Ni. CO 4 (g) 200 0 C 70 0 C Ni. CO 4 (g) Ni (s) + 4 CO (g) Electrolysis Cu (s) (impure) Cu 2+ (aq) + 2 e- Cu 2+ (aq) + 2 e. Cu (s) (pure) Zone refining Prinsp : logam yang akan dimurnikan harus dipasang sebagai ANODA Sebagai katoda harus logam murni. 20. 2

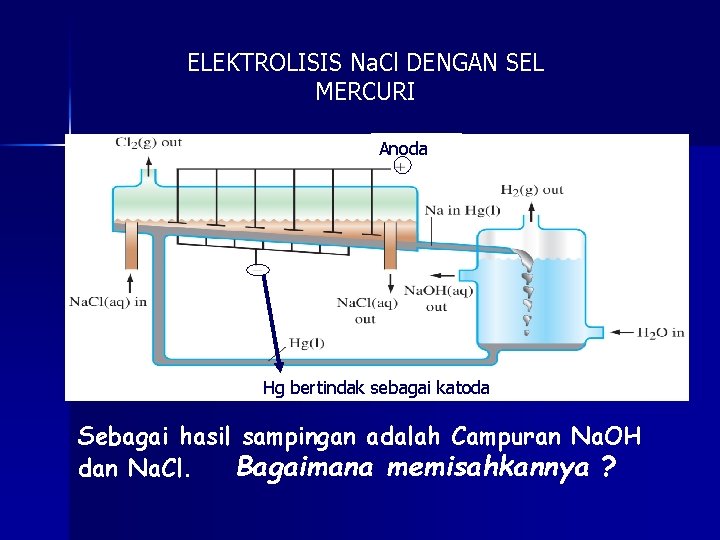
ELEKTROLISIS Na. Cl DENGAN SEL MERCURI Anoda Hg bertindak sebagai katoda Sebagai hasil sampingan adalah Campuran Na. OH dan Na. Cl. Bagaimana memisahkannya ?

Industrial Electrolysis Processes

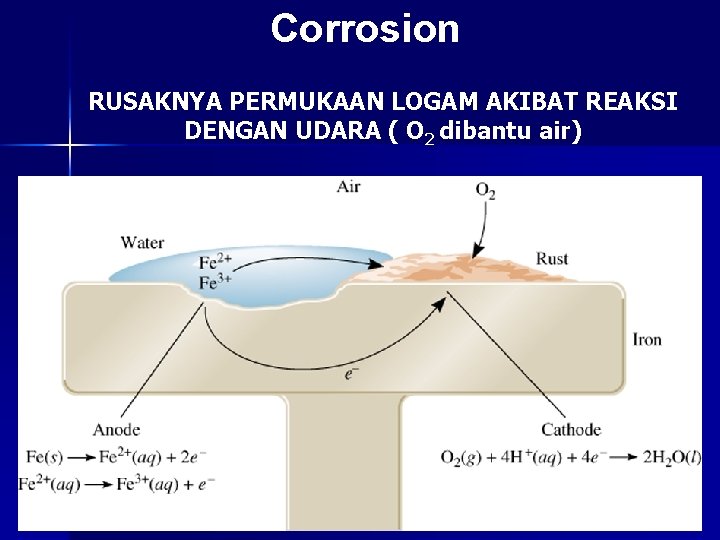
Corrosion RUSAKNYA PERMUKAAN LOGAM AKIBAT REAKSI DENGAN UDARA ( O 2 dibantu air)

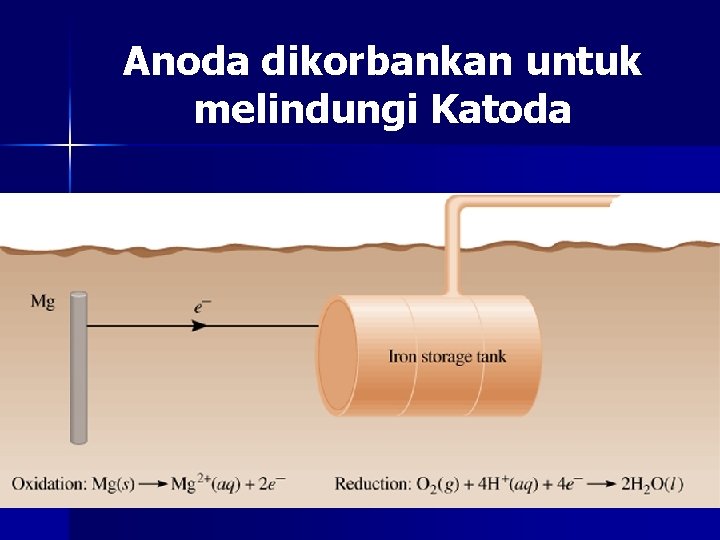
PERLINDUNGAN KATODA / PENGORBANAN ANODA Prinsip : Logam yang lebih reaktif (Eo kecil) akan lebih dahulu berkarat. Syarat : Logam yang akan digunakan untuk melindungi harus lebih reaktif

Anoda dikorbankan untuk melindungi Katoda