GEOMETRIJA U KRISTALIMA Prezentaciju pripremio Filip Korona uenik



















![2. Tetragonski sustav Vulfenit – Pb[Mo. O 4] 2. Tetragonski sustav Vulfenit – Pb[Mo. O 4]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-27.jpg)








![4. Heksagonski sustav Beril – Al 2 Be 3[Si 6 O 18] 4. Heksagonski sustav Beril – Al 2 Be 3[Si 6 O 18]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-38.jpg)





















![6. Monoklinski sustav Muskovit – KAl 2[(OH, F)2|Al Si 3 O 10] 6. Monoklinski sustav Muskovit – KAl 2[(OH, F)2|Al Si 3 O 10]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-62.jpg)
![6. Monoklinski sustav Adular – K[Al Si 3 O 8] 6. Monoklinski sustav Adular – K[Al Si 3 O 8]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-63.jpg)




![7. Triklinski sustav Albit - Na[Al. Si 3 O 8] 7. Triklinski sustav Albit - Na[Al. Si 3 O 8]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-69.jpg)


- Slides: 71

GEOMETRIJA U KRISTALIMA Prezentaciju pripremio: Filip Korona, učenik II razreda Gimnazije Jurja Barakovića Pripremio: Mentorica: Filip Korona , Gimnazija Jurja Barakovića u Zadru Ružica Milošević, profesorica kemije

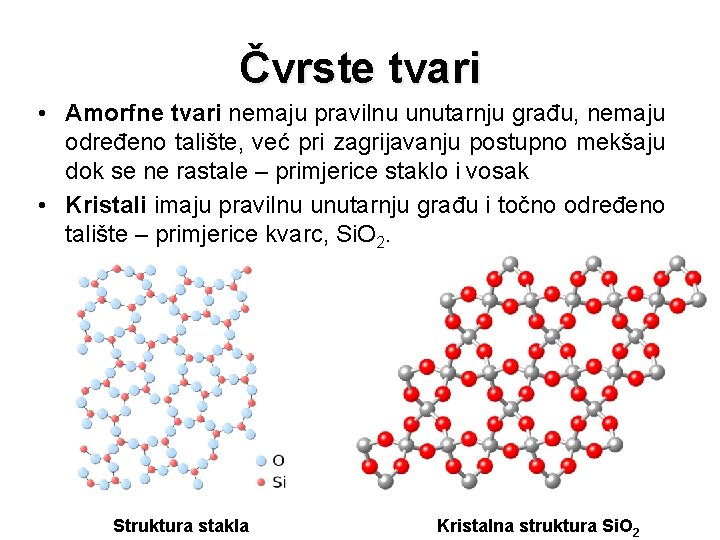
Čvrste tvari • Amorfne tvari nemaju pravilnu unutarnju građu, nemaju određeno talište, već pri zagrijavanju postupno mekšaju dok se ne rastale – primjerice staklo i vosak • Kristali imaju pravilnu unutarnju građu i točno određeno talište – primjerice kvarc, Si. O 2. Struktura stakla Kristalna struktura Si. O 2

Što je kristal? • Kristal je geometrijsko tijelo pravilne unutarnje građe, omeđeno plohama. • Kristali imaju tri vrste elemenata simetrije koje možemo zapaziti kako u njihovoj strukturi, tako i po vanjskom obliku. To su ravnina simetrije, os simetrije i središte simetrije.

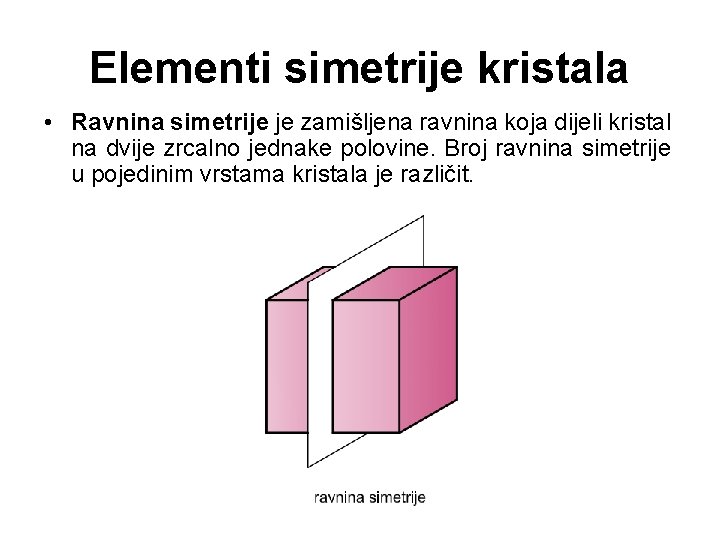
Elementi simetrije kristala • Ravnina simetrije je zamišljena ravnina koja dijeli kristal na dvije zrcalno jednake polovine. Broj ravnina simetrije u pojedinim vrstama kristala je različit.

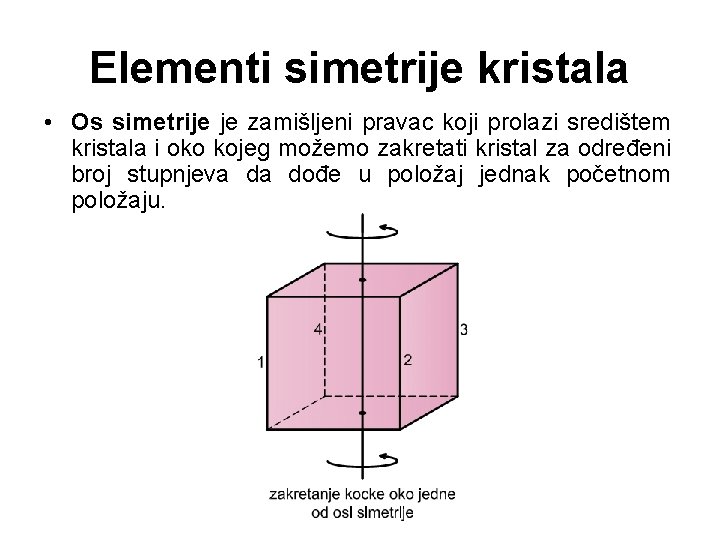
Elementi simetrije kristala • Os simetrije je zamišljeni pravac koji prolazi središtem kristala i oko kojeg možemo zakretati kristal za određeni broj stupnjeva da dođe u položaj jednak početnom položaju.

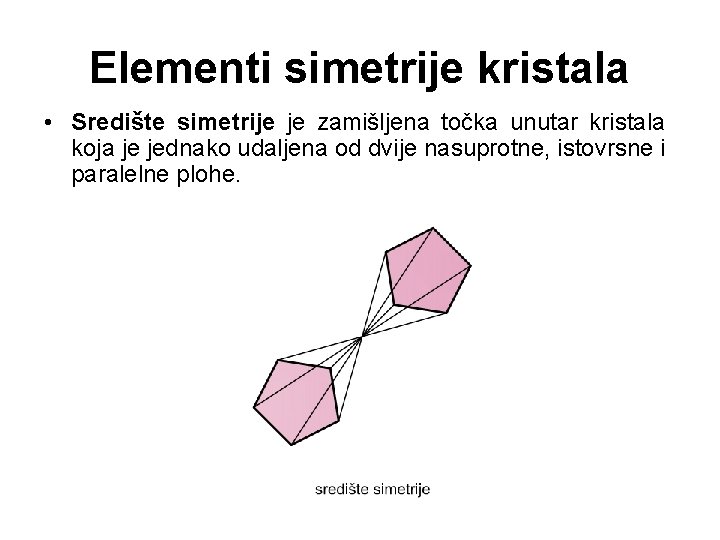
Elementi simetrije kristala • Središte simetrije je zamišljena točka unutar kristala koja je jednako udaljena od dvije nasuprotne, istovrsne i paralelne plohe.

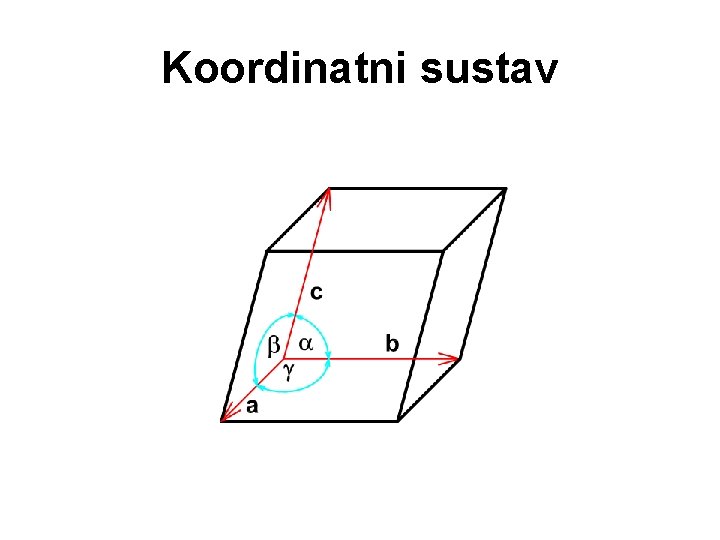
O kristalima • Pravilan raspored građevnih elemenata u kristalu možemo pokazati modelom prostorne rešetke • Za kristale je karakterističan najmanji dio koji se periodički ponavlja u prostoru i zove se elementarna ćelija kristalne rešetke • Svaka elementarna ćelija određena je bridovima i kutovima među njima • Bridovi elementarne ćelije predstavljaju koordinatni sustav koji je određen trima kristalografskim osima (a, b i c) i trima pripadnim kutovima između osi ( , i )

Koordinatni sustav

Kristalni sustavi 1. Odsječci na osima (ovisno o simetriji) mogu i ne moraju biti jednaki. 2. Sva tri kuta mogu biti prava 3. Dva kuta mogu biti prava, a jedan različit 4. Sva tri kuta mogu biti različita

Kristalni sustavi Danas je poznato oko 3000 minerala kristalne građe, ali po obliku elementarne ćelije svi oni se mogu svrstati u sedam kristalnih sustava: • Kubični sustav • Tetragonski sustav • Rompski sustav • Heksagonski sustav • Trigonski sustav/romboedarski • Monoklinski sustav • Triklinski sustav

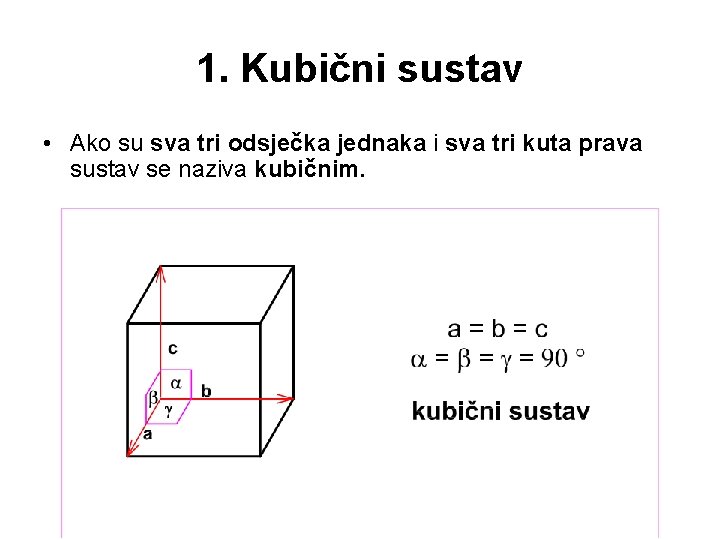
1. Kubični sustav • Ako su sva tri odsječka jednaka i sva tri kuta prava sustav se naziva kubičnim.

1. Kubični sustav Pirit - Fe. S 2

1. Kubični sustav Još jedan kristal pirita

1. Kubični sustav Srebro - Ag

1. Kubični sustav Zlato - Au

1. Kubični sustav Galenit - Pb. S

1. Kubični sustav Sfalerit - Zn. S

1. Kubični sustav Halit - Na. Cl

1. Kubični sustav još jedan kristal Na. Cl

1. Kubični sustav Fluorit – Ca. F 2

1. Kubični sustav Magnetit – Fe 2 O 3

1. Kubični sustav Analcim – Na. Al. Si 2 O 6·H 2 O

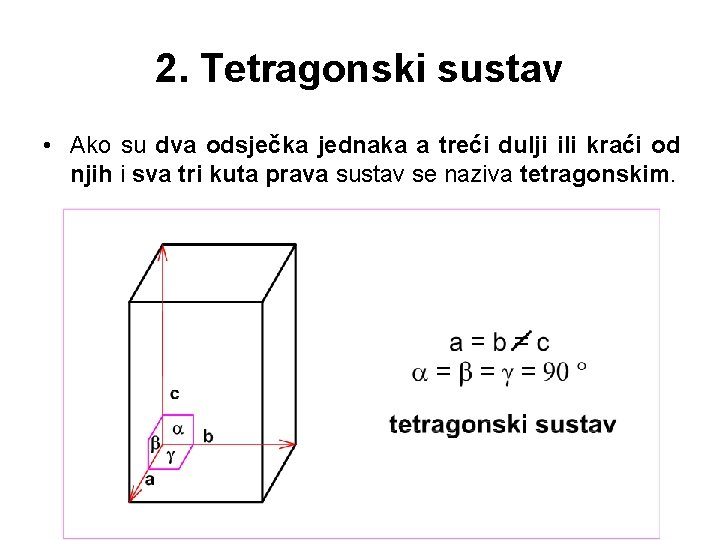
2. Tetragonski sustav • Ako su dva odsječka jednaka a treći dulji ili kraći od njih i sva tri kuta prava sustav se naziva tetragonskim.

2. Tetragonski sustav Cirkon – Zr. Si. O 4

2. Tetragonski sustav Halkopirit – Cu. Fe. S 2

2. Tetragonski sustav Urea – CO(NH 2)2
![2 Tetragonski sustav Vulfenit PbMo O 4 2. Tetragonski sustav Vulfenit – Pb[Mo. O 4]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-27.jpg)
2. Tetragonski sustav Vulfenit – Pb[Mo. O 4]

2. Tetragonski sustav Vezuvijan – Ca 10(Mg, Fe)2 Al 4[(OH)4|(Si. O 4)5(Si 2 O 7)2]

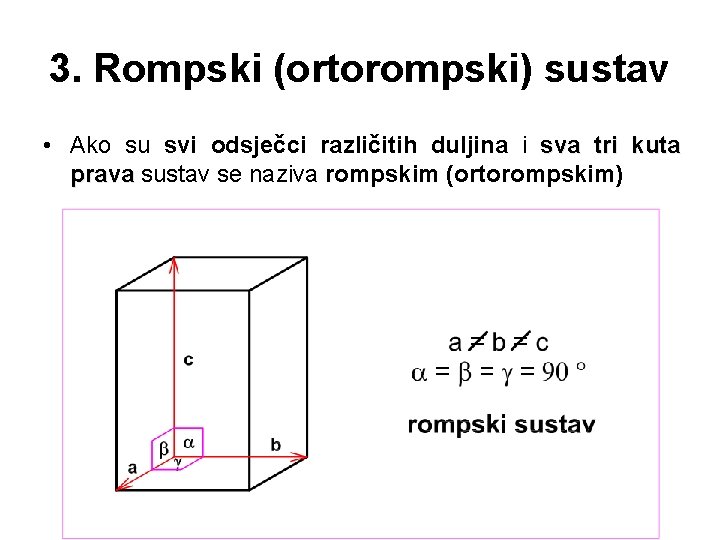
3. Rompski (ortorompski) sustav • Ako su svi odsječci različitih duljina i sva tri kuta prava sustav se naziva rompskim (ortorompskim)

3. Rompski sustav Aragonit –Ca. CO 3

3. Rompski sustav Rompski sumpor– S

3. Rompski sustav Jod – I 2

3. Rompski sustav Barit – Ba. SO 4

3. Rompski sustav Topaz – Al 2 Si. O 4 F 2

3. Rompski sustav Antimonit – Sb 2 S 3

3. Rompski sustav Bakrov(II) klorid dihidrat – Cu. Cl 2· 2 H 2 O

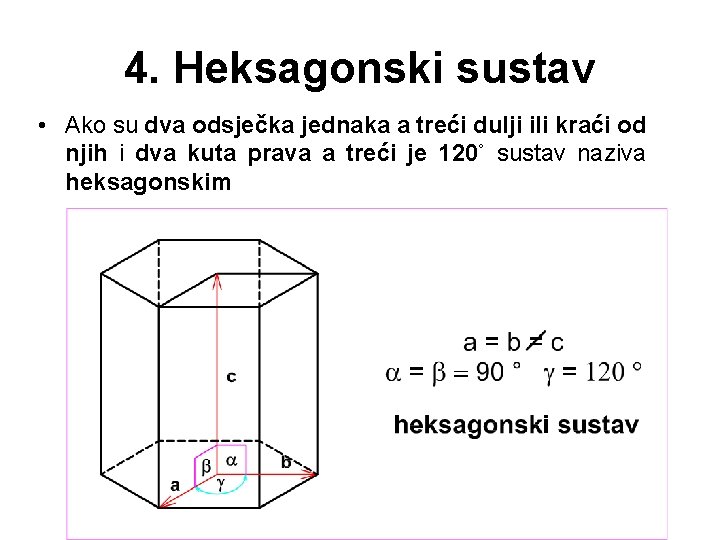
4. Heksagonski sustav • Ako su dva odsječka jednaka a treći dulji ili kraći od njih i dva kuta prava a treći je 120˚ sustav naziva heksagonskim
![4 Heksagonski sustav Beril Al 2 Be 3Si 6 O 18 4. Heksagonski sustav Beril – Al 2 Be 3[Si 6 O 18]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-38.jpg)
4. Heksagonski sustav Beril – Al 2 Be 3[Si 6 O 18]

4. Heksagonski sustav Korund – Al 2 O 3

4. Heksagonski sustav Apatit – Ca 5(PO 4)3 F

4. Heksagonski sustav Piromorfit - Pb 5(PO 4)3 Cl

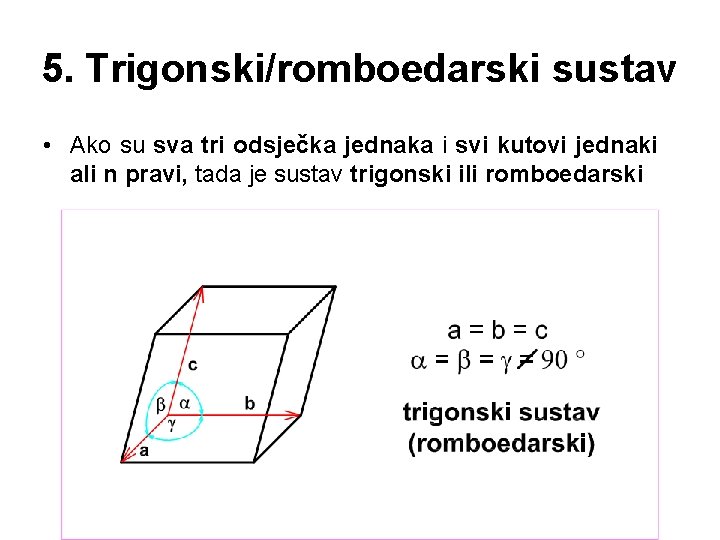
5. Trigonski/romboedarski sustav • Ako su sva tri odsječka jednaka i svi kutovi jednaki ali n pravi, tada je sustav trigonski ili romboedarski

5. Trigonski (romboedarski) sustav Kalcit– Ca. CO 3

5. Trigonski (romboedarski) sustav Prustit – Ag 3 As. S 3

5. Trigonski (romboedarski) sustav Hematit – Fe 2 O 3

5. Trigonski (romboedarski) sustav Kremen ili kvarc– Si. O 2

5. Trigonski (romboedarski) sustav još jedan kristal kvarca

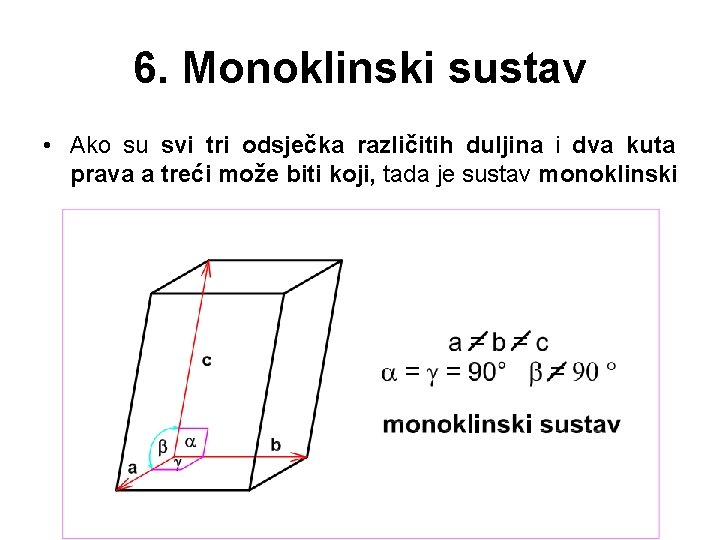
6. Monoklinski sustav • Ako su svi tri odsječka različitih duljina i dva kuta prava a treći može biti koji, tada je sustav monoklinski

6. Monoklinski sustav Gips – Ca. SO 4· 2 H 2 O

6. Monoklinski sustav monoklinski sumpor, S

6. Monoklinski sustav još jedan kristal gipsa

6. Monoklinski sustav Arsenopirit – Fe. As. S

6. Monoklinski sustav Auripigment – As. S 2

6. Monoklinski sustav Azurit – Cu 3 (CO 3)2 (OH)2

6. Monoklinski sustav Još jedan kristal azurita

6. Monoklinski sustav Malahitit – Cu 2 CO 3(OH)2

6. Monoklinski sustav još jedan kristal malahita

6. Monoklinski sustav Vivijanit – Fe 2 ( PO 4)2· 8 H 2 O

6. Monoklinski sustav Vavelit – Al 3(PO 4)2(OH)3· 5 H 2 O

6. Monoklinski sustav Volframit – (Fe, Mn)WO 4

6. Monoklinski sustav Epidot – Ca 2(Fe, Al)Al 2(Si. O 4)(Si 2 O 7)O(OH)
![6 Monoklinski sustav Muskovit KAl 2OH F2Al Si 3 O 10 6. Monoklinski sustav Muskovit – KAl 2[(OH, F)2|Al Si 3 O 10]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-62.jpg)
6. Monoklinski sustav Muskovit – KAl 2[(OH, F)2|Al Si 3 O 10]
![6 Monoklinski sustav Adular KAl Si 3 O 8 6. Monoklinski sustav Adular – K[Al Si 3 O 8]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-63.jpg)
6. Monoklinski sustav Adular – K[Al Si 3 O 8]

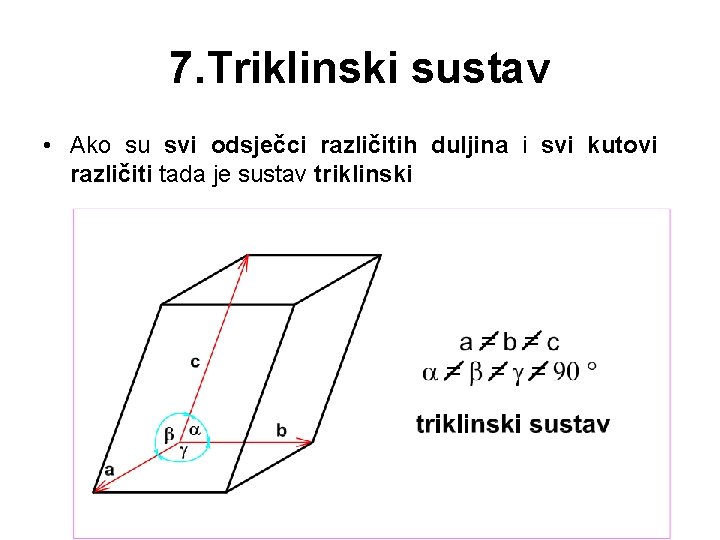
7. Triklinski sustav • Ako su svi odsječci različitih duljina i svi kutovi različiti tada je sustav triklinski

7. Triklinski sustav Modra galica – Cu. SO 4· 5 H 2 O

7. Triklinski sustav Još jedan kristal modre galice

7. Triklinski sustav Disten ili kianit - Al 2(Si. O 4)O

7. Triklinski sustav Još jedan kristal distena ili kianita
![7 Triklinski sustav Albit NaAl Si 3 O 8 7. Triklinski sustav Albit - Na[Al. Si 3 O 8]](https://slidetodoc.com/presentation_image/48fba746919e2aef6cc9bd7436a384d9/image-69.jpg)
7. Triklinski sustav Albit - Na[Al. Si 3 O 8]

7. Triklinski sustav Još jedan kristal albita

Literatura Martin Šoufek: Svijet minerala, Školska knjiga Zagreb i Hrvatski prirodoslovni muzej, 1991. Aleksandra Habuš - Vera Tomašić: OPĆA KEMIJA 1, udžbenik za prvi razred gimnazije, Profil International Zagreb, 6. izdanje, 2012. http: //webmineral. com/
 Miniprojekt
Miniprojekt św stanisław biskup i męczennik prezentacja
św stanisław biskup i męczennik prezentacja Korona fakulteti
Korona fakulteti Bugtong halimbawa
Bugtong halimbawa Nagbibigay na'y sinasakal pa
Nagbibigay na'y sinasakal pa Mate bulic korona
Mate bulic korona Korona
Korona Korona vrijeme inkubacije
Korona vrijeme inkubacije Teme za prezentaciju iz informatike
Teme za prezentaciju iz informatike Kako zavrsiti prezentaciju
Kako zavrsiti prezentaciju Uvod u prezentaciju
Uvod u prezentaciju Prezentacija primer
Prezentacija primer Powerpoint prezentacije primeri
Powerpoint prezentacije primeri Pravila za prezentaciju
Pravila za prezentaciju Hvala na paznji prezentacija
Hvala na paznji prezentacija Pozadine kola
Pozadine kola Kako zavrsiti prezentaciju
Kako zavrsiti prezentaciju Kako završiti prezentaciju
Kako završiti prezentaciju Prezentacije iz informatike
Prezentacije iz informatike Kako napraviti dobru prezentaciju
Kako napraviti dobru prezentaciju Slike za kraj prezentacije
Slike za kraj prezentacije Uvod u prezentaciju
Uvod u prezentaciju Ekonomske teme za prezentaciju
Ekonomske teme za prezentaciju Dobra prezentacija
Dobra prezentacija Dvije duzi koje se nadovezuju
Dvije duzi koje se nadovezuju Opisna geometrija
Opisna geometrija Presek pravih
Presek pravih što je kvadar
što je kvadar Geometrija 4 razred
Geometrija 4 razred Togri tortburchak
Togri tortburchak Geometrija reznog alata
Geometrija reznog alata Grf
Grf Trokut formule
Trokut formule Smailusis kampas
Smailusis kampas Premice daljice poltraki vaje
Premice daljice poltraki vaje Opseg pravokutnika zadaci za 4 razred
Opseg pravokutnika zadaci za 4 razred Matematika 4 razred trokut
Matematika 4 razred trokut Nacrtna geometrija mongeova projekcija
Nacrtna geometrija mongeova projekcija Nacrtna geometrija gradjevinski fakultet
Nacrtna geometrija gradjevinski fakultet Mjerenje površina 4 razred
Mjerenje površina 4 razred Osnovni i izvedeni pojmovi u geometriji
Osnovni i izvedeni pojmovi u geometriji Filip triplat
Filip triplat Filip lamański
Filip lamański Filip kurek
Filip kurek Filip drajfus
Filip drajfus Filip rewakowicz
Filip rewakowicz Filip malmberg
Filip malmberg Filip triplat
Filip triplat Povratak filipa latinovicza analiza likova
Povratak filipa latinovicza analiza likova Filip triplat
Filip triplat Area nervina area radicularis
Area nervina area radicularis Magda filip
Magda filip Sveti filip i jakov plaže
Sveti filip i jakov plaže Filip jokanovic
Filip jokanovic Filip rozanek
Filip rozanek Weronika nazarko
Weronika nazarko Pavel pai
Pavel pai Filip jukić
Filip jukić Filip staničić
Filip staničić Sara filip
Sara filip Defabularizacija
Defabularizacija Filip latinovicz otac
Filip latinovicz otac Peli filip
Peli filip Filip lin
Filip lin Zan mitrev klinika
Zan mitrev klinika Deseminacija
Deseminacija Ludwig filip
Ludwig filip Oš sesvetska sela
Oš sesvetska sela Filip vondra
Filip vondra Filip hanik
Filip hanik Filip abraham ku leuven
Filip abraham ku leuven Filip simovic
Filip simovic