F 4110 Kvantov fyzika atomrnch soustav letn semestr






























- Slides: 101

F 4110 Kvantová fyzika atomárních soustav letní semestr 2008 - 2009 XI. Inversní linie čpavku: Sláva a pád KOTLÁŘSKÁ 29. DUBNA 2008 1

Úvodem • inversní linie čpavku jako případ spontánního narušení symetrie • kvantově chemický výklad tvaru molekuly čpavku • symetrie čtyřatomových molekul • normální kmity čpavku a dublety • vysvětlení dubletu tunelováním napříč barierou • explicitní výpočet pro modely dvou typů • čpavkové hodiny • dvouhladinový maser

Pyramidální molekula: případ spontánního narušení symetrie

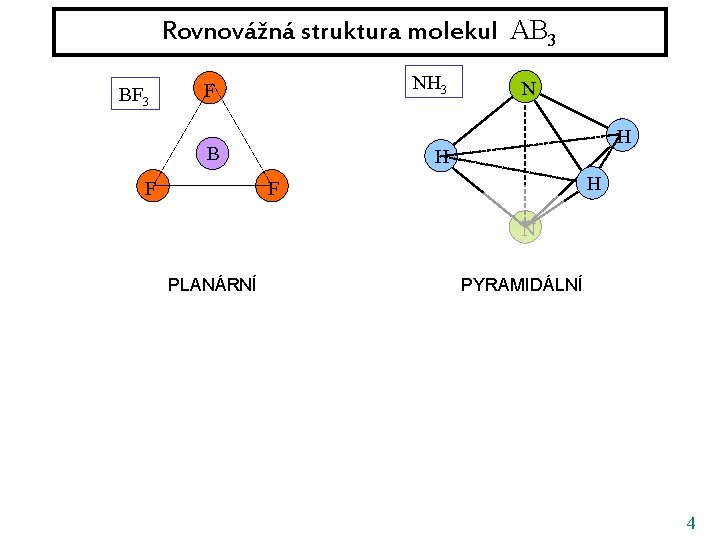
Rovnovážná struktura molekul AB 3 BF 3 NH 3 F B F N H H H F N PLANÁRNÍ PYRAMIDÁLNÍ 4

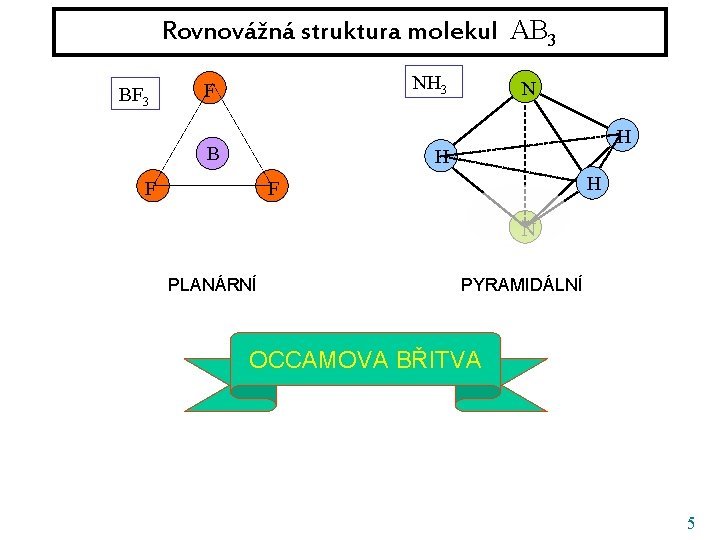
Rovnovážná struktura molekul AB 3 BF 3 NH 3 F B N H H F N PLANÁRNÍ PYRAMIDÁLNÍ OCCAMOVA BŘITVA 5

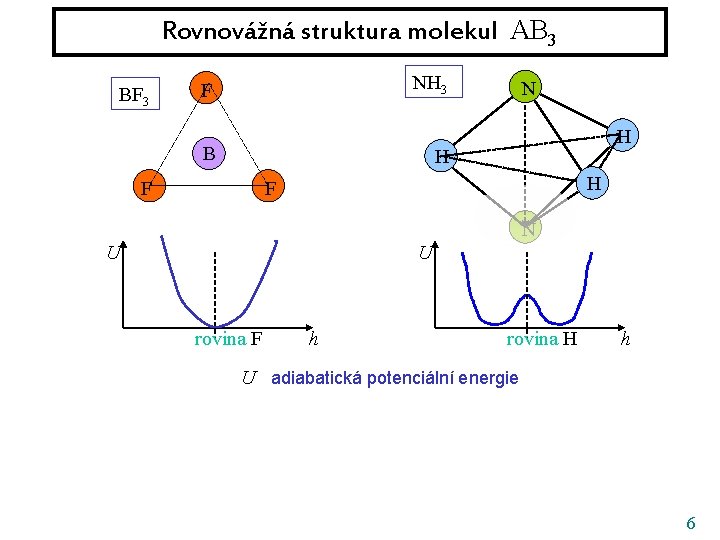
Rovnovážná struktura molekul AB 3 BF 3 NH 3 F B N H H F N U U rovina F h rovina H h U adiabatická potenciální energie 6

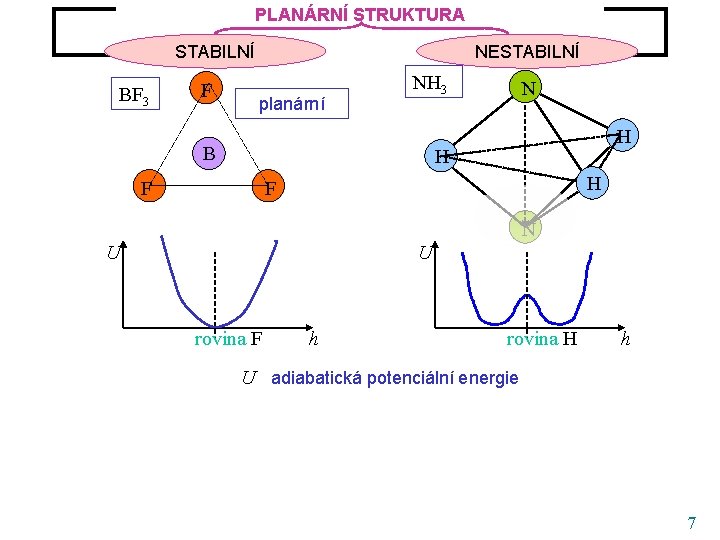
PLANÁRNÍ STRUKTURA Rovnovážná struktura molekul AB 3 STABILNÍ BF 3 F NESTABILNÍ planární NH 3 B N H H F N U U rovina F h rovina H h U adiabatická potenciální energie 7

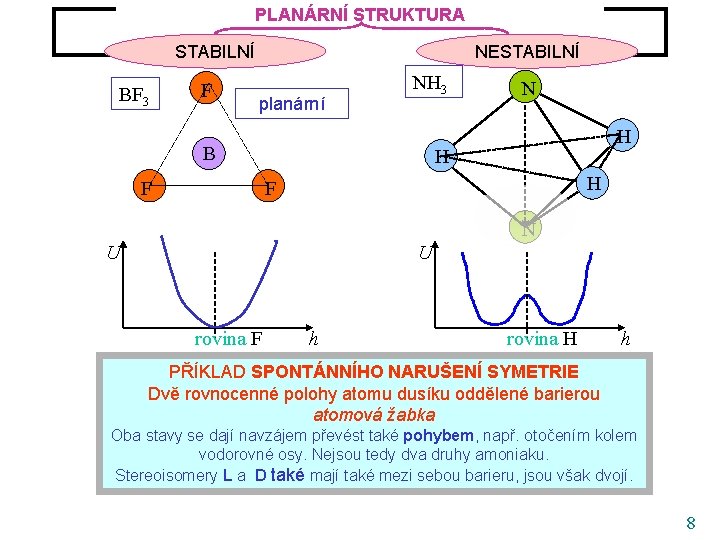
PLANÁRNÍ STRUKTURA Rovnovážná struktura molekul AB 3 STABILNÍ BF 3 F NESTABILNÍ planární NH 3 B F N H H H F N U U rovina F h rovina H h PŘÍKLADUSPONTÁNNÍHO NARUŠENÍ SYMETRIE adiabatická potenciální energie Dvě rovnocenné polohy atomu dusíku oddělené barierou atomová žabka Oba stavy se dají navzájem převést také pohybem, např. otočením kolem vodorovné osy. Nejsou tedy dva druhy amoniaku. Stereoisomery L a D také mají také mezi sebou barieru, jsou však dvojí. 8

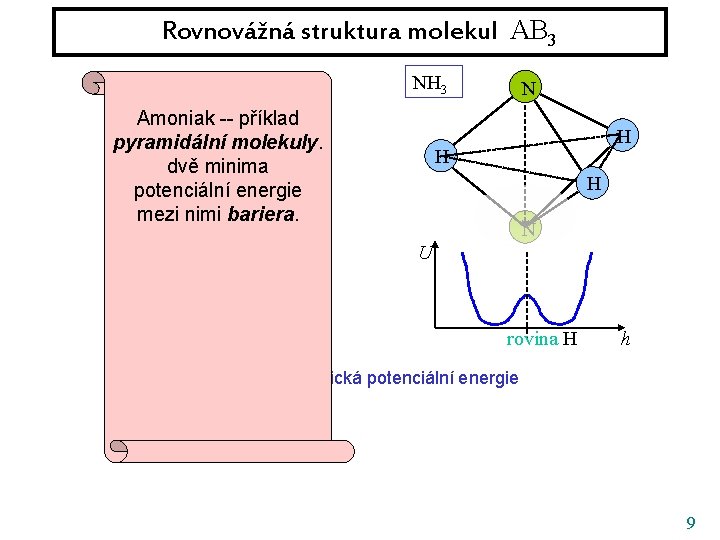
Rovnovážná struktura molekul AB 3 F BF 3 Amoniak -- příklad pyramidální molekuly. B dvě minima F F potenciální energie mezi nimi bariera. U NH 3 N H H H N U V případě amoniaku máme navíc: Bariera je kvantová a dovoluje rovina F h rovina H tunelování U adiabatická potenciální energie mezi oběma stavy. Ty jsou nestacionární h 9

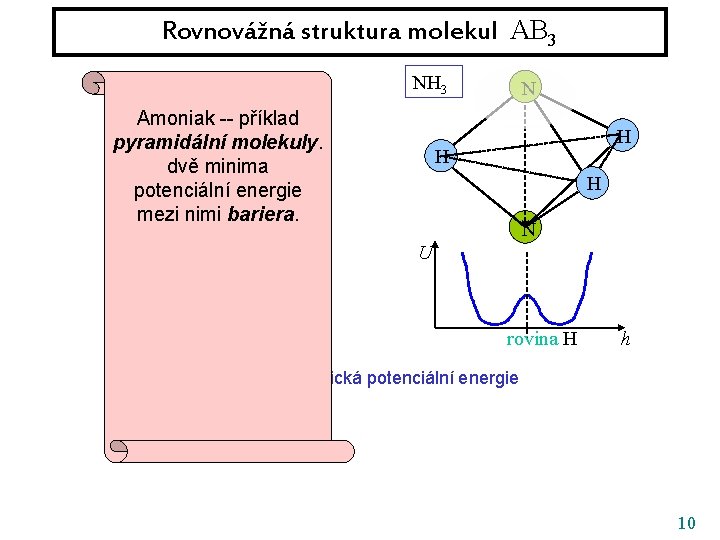
Rovnovážná struktura molekul AB 3 F BF 3 Amoniak -- příklad pyramidální molekuly. B dvě minima F F potenciální energie mezi nimi bariera. U NH 3 N H H H N U V případě amoniaku máme navíc: Bariera je kvantová a dovoluje rovina F h rovina H tunelování U adiabatická potenciální energie mezi oběma stavy. Ty jsou nestacionární h 10

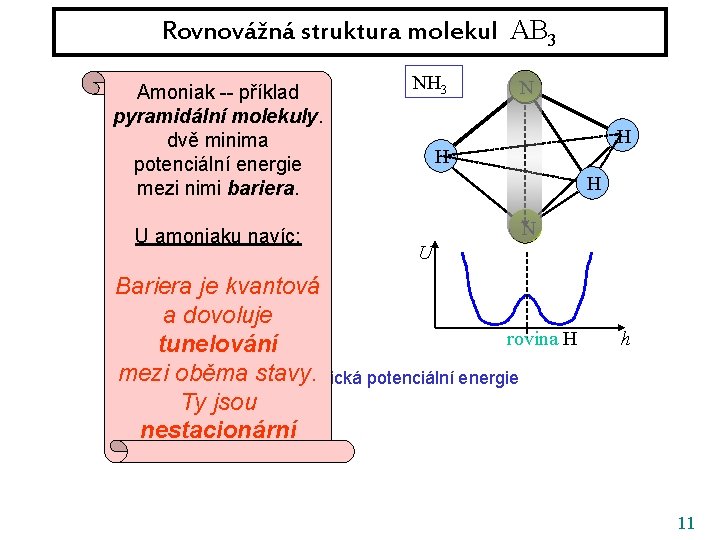
Rovnovážná struktura molekul AB 3 F -- příklad BFAmoniak 3 pyramidální molekuly. dvě minima B potenciální energie mezi nimi bariera. F F U U amoniaku navíc: NH 3 N H H H N U Bariera je kvantová a dovoluje rovina F h rovina H tunelování mezi oběma. Ustavy. adiabatická potenciální energie Ty jsou nestacionární h 11

Fyzikální příčiny spontánního narušení symetrie

Východiskem je periodický systém 13

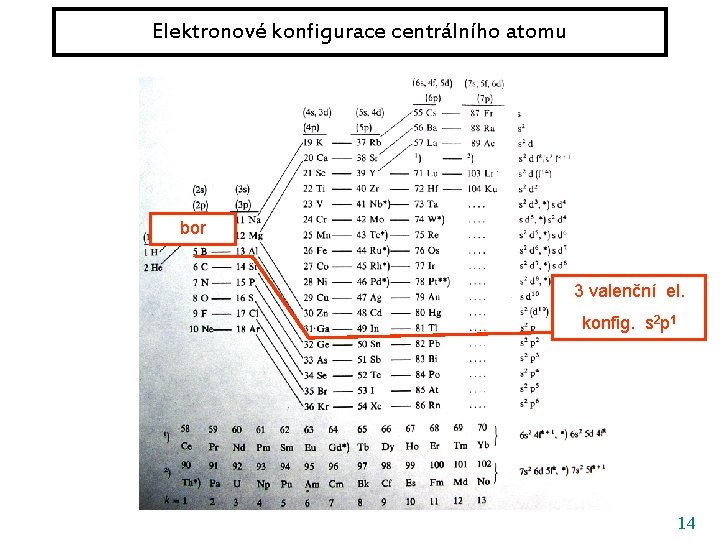
Elektronové konfigurace centrálního atomu bor 3 valenční el. konfig. s 2 p 1 14

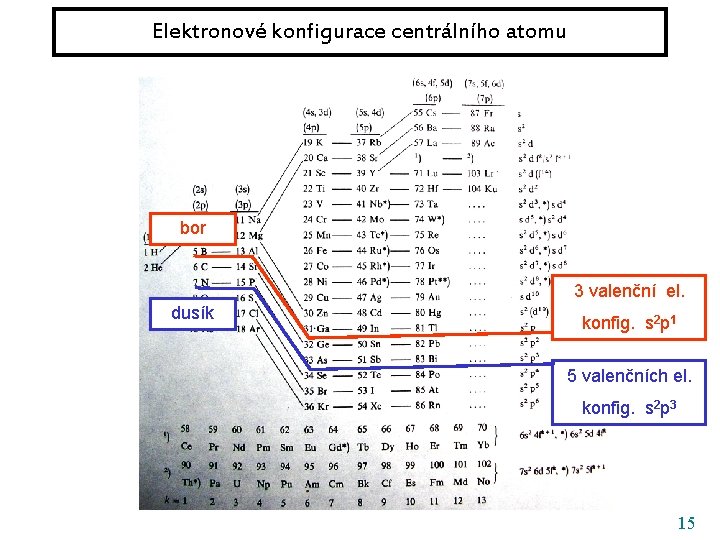
Elektronové konfigurace centrálního atomu bor 3 valenční el. dusík konfig. s 2 p 1 5 valenčních el. konfig. s 2 p 3 15

Starobylá úprava periodické tabulky 16

Starobylá úprava periodické tabulky oxidy 17

Starobylá úprava periodické tabulky hydridy oxidy 18

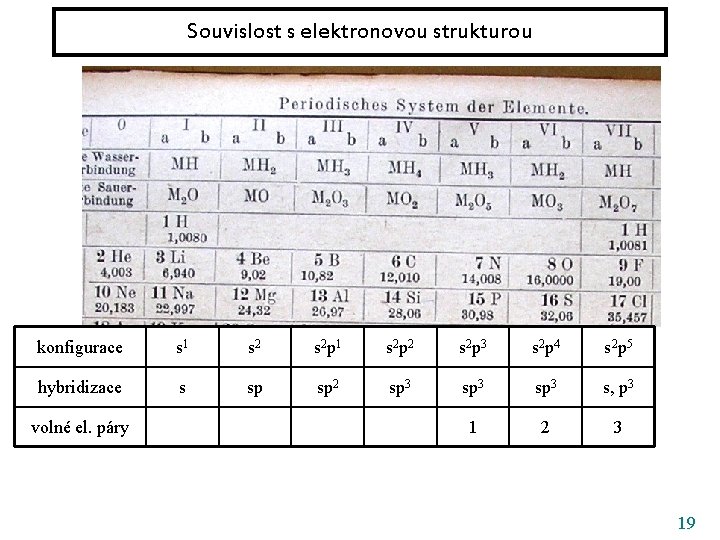
Souvislost s elektronovou strukturou konfigurace s 1 s 2 p 2 s 2 p 3 s 2 p 4 s 2 p 5 hybridizace s sp sp 2 sp 3 s, p 3 1 2 3 volné el. páry 19

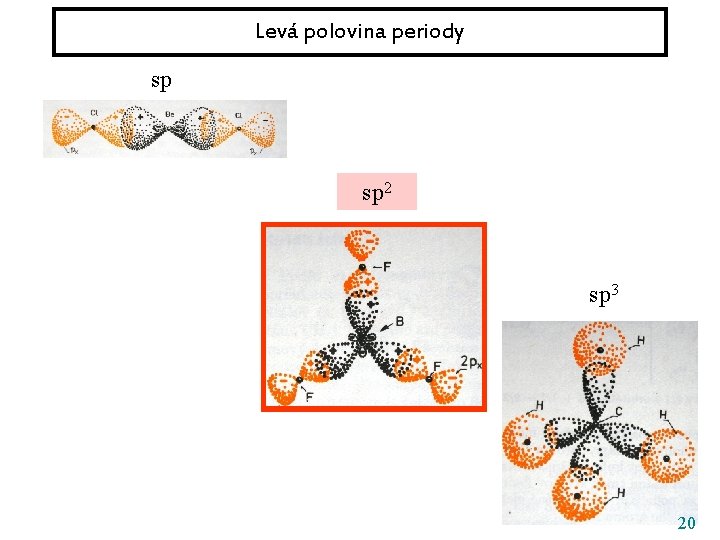
Levá polovina periody sp sp 2 sp 3 20

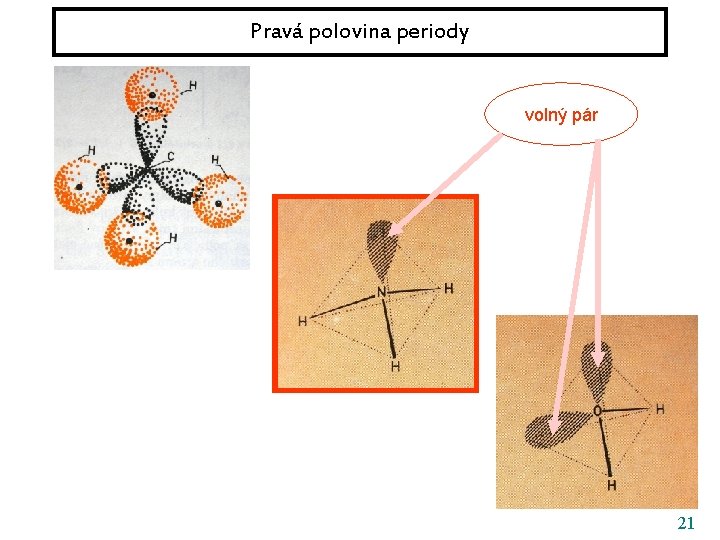
Pravá polovina periody volný pár 21

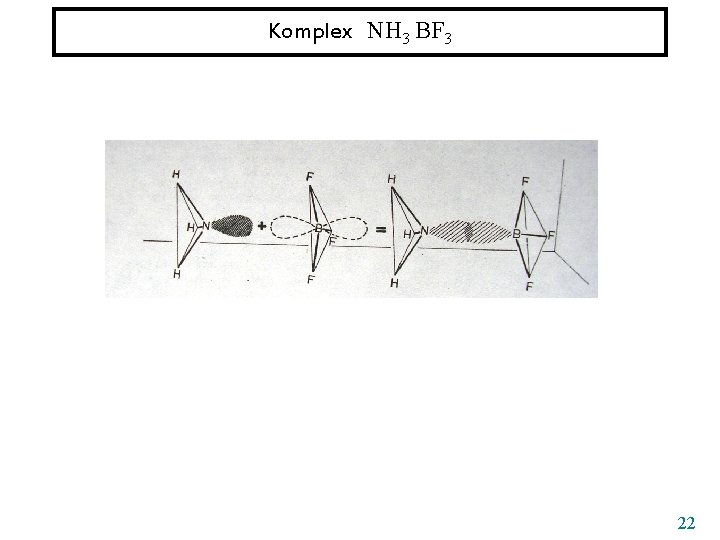
Komplex NH 3 BF 3 22

Pyramidální molekula: geometrická struktura

24

25

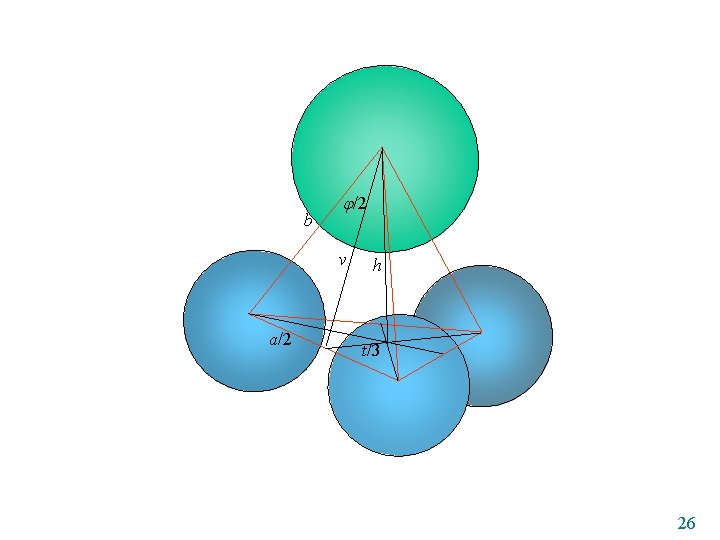
b /2 v a/2 h t/3 26

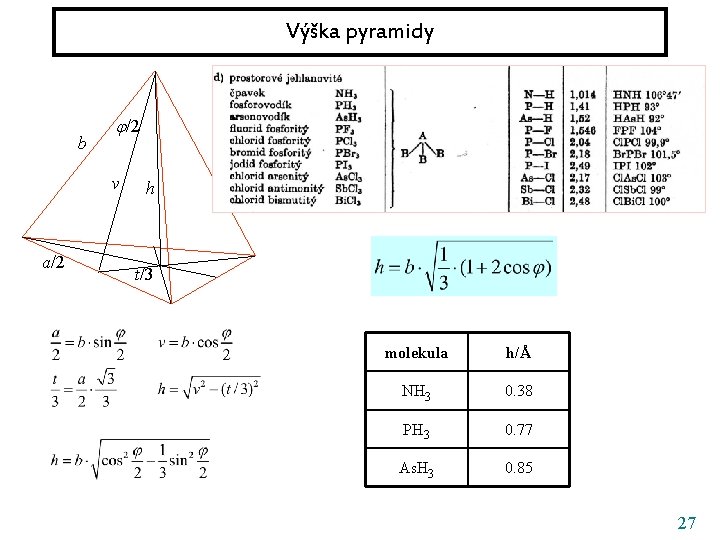
Výška pyramidy b /2 v a/2 h t/3 molekula h/Å NH 3 0. 38 PH 3 0. 77 As. H 3 0. 85 27

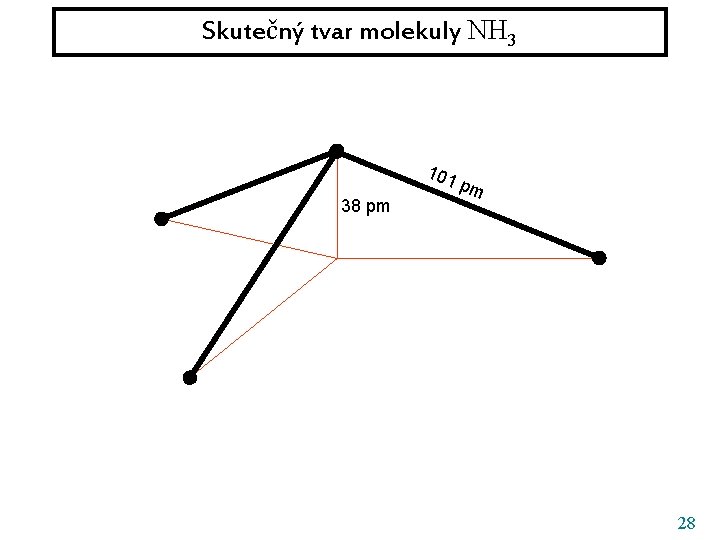
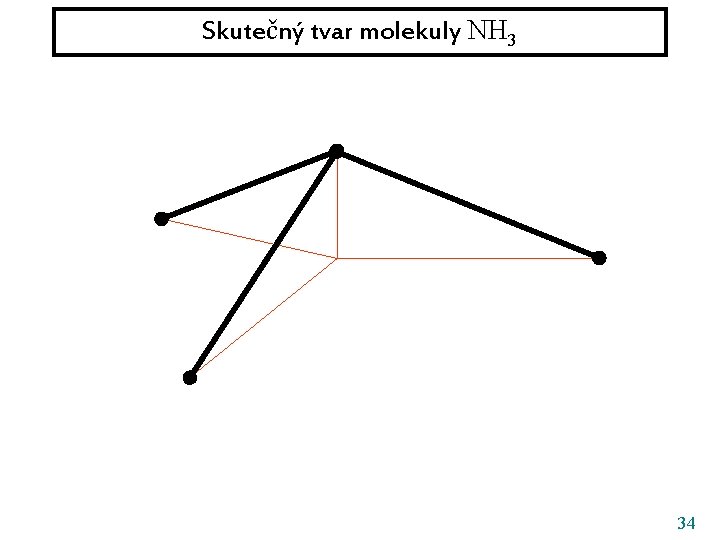
Skutečný tvar molekuly NH 3 101 38 pm pm 28

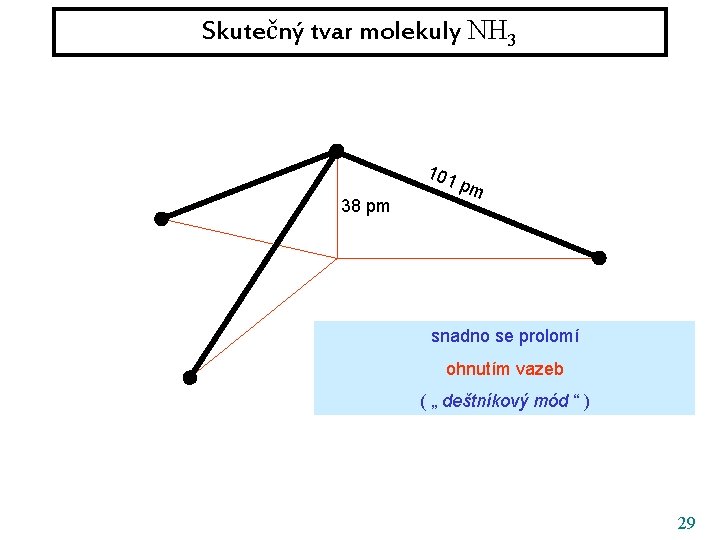
Skutečný tvar molekuly NH 3 101 38 pm pm snadno se prolomí ohnutím vazeb ( „ deštníkový mód “ ) 29

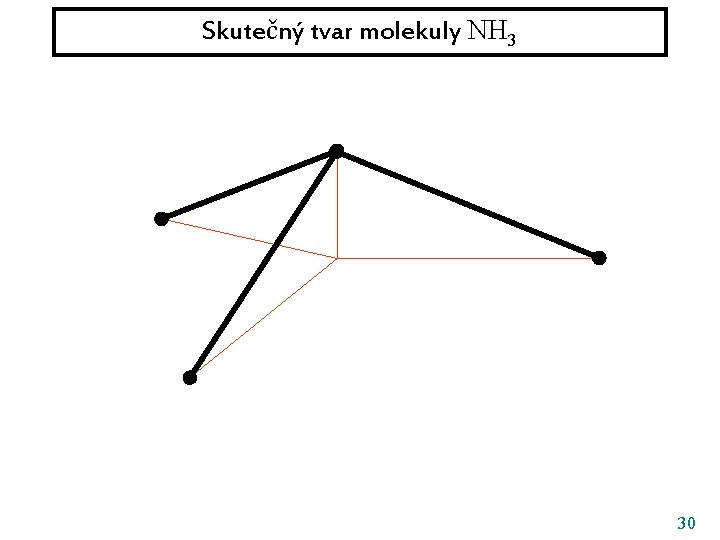
Skutečný tvar molekuly NH 3 30

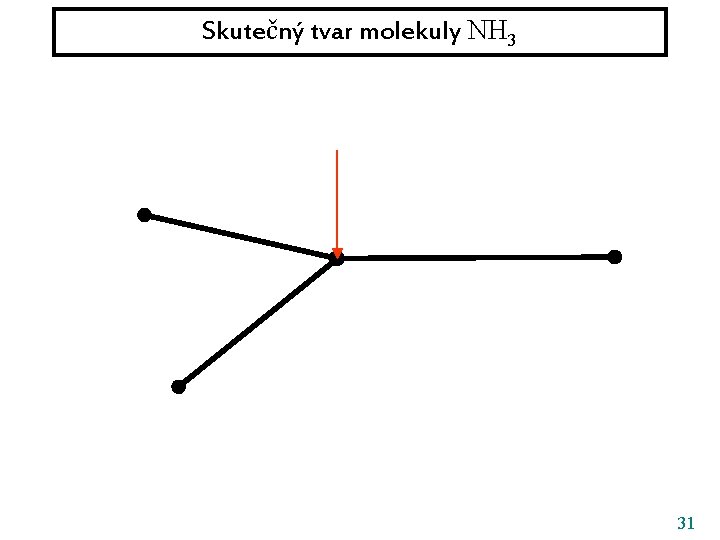
Skutečný tvar molekuly NH 3 31

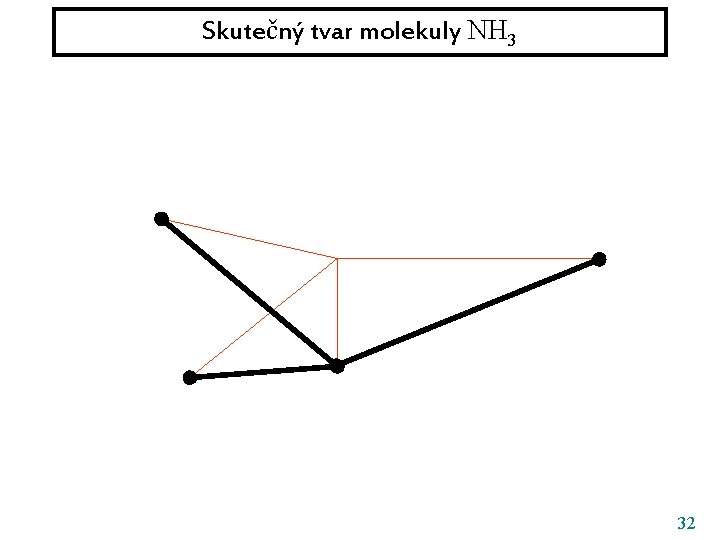
Skutečný tvar molekuly NH 3 32

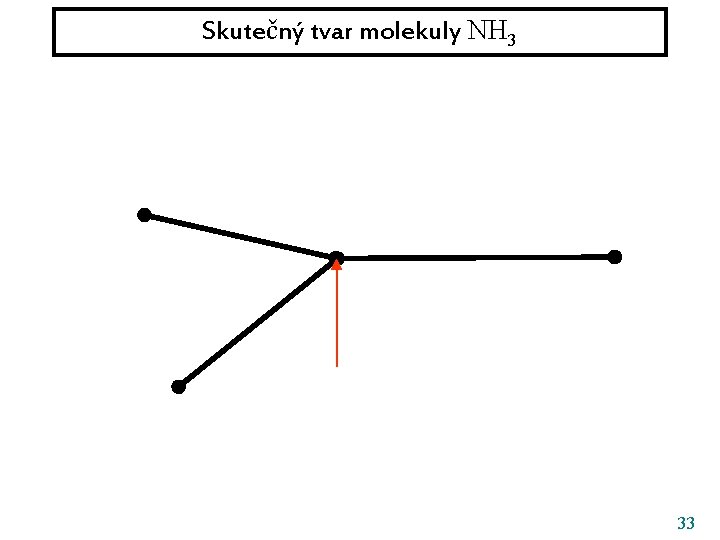
Skutečný tvar molekuly NH 3 33

Skutečný tvar molekuly NH 3 34

Pyramidální molekula: bodová symetrie

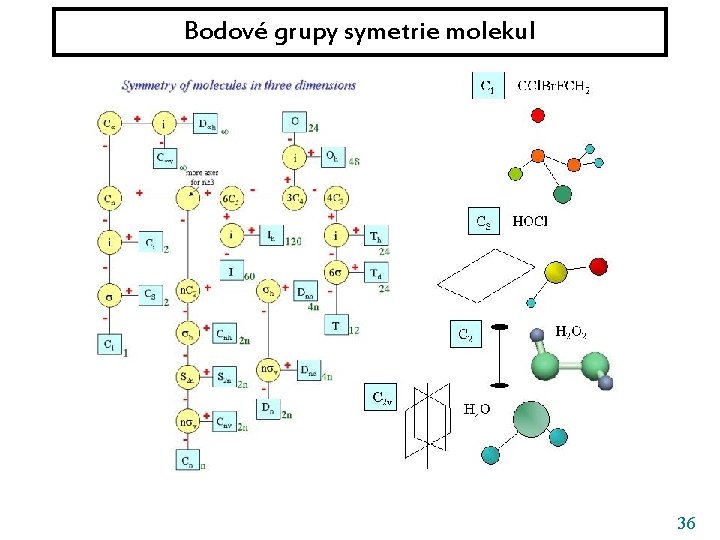
Bodové grupy symetrie molekul 36

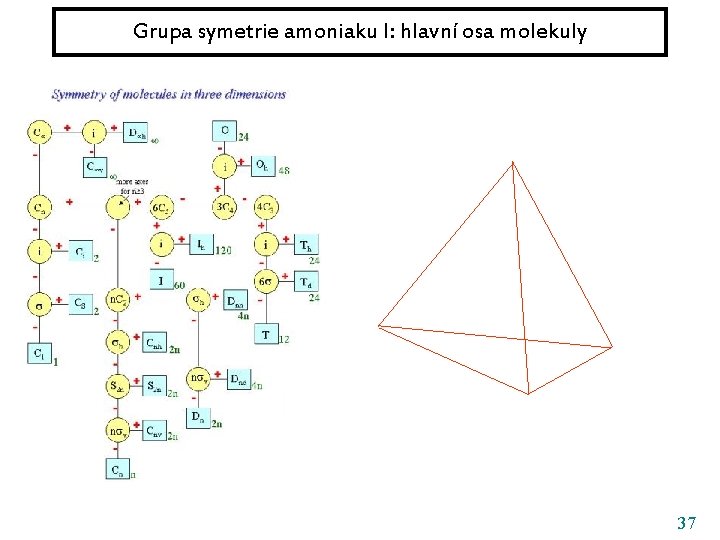
Grupa symetrie amoniaku I: hlavní osa molekuly 37

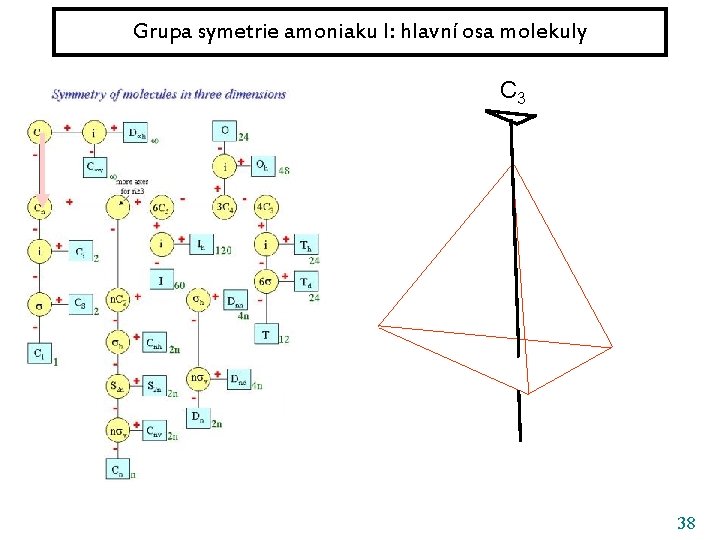
Grupa symetrie amoniaku I: hlavní osa molekuly C 3 38

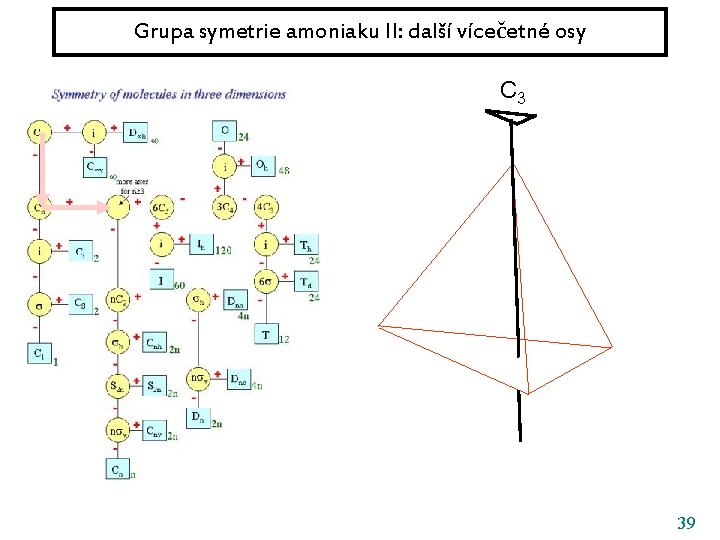
Grupa symetrie amoniaku II: další vícečetné osy C 3 39

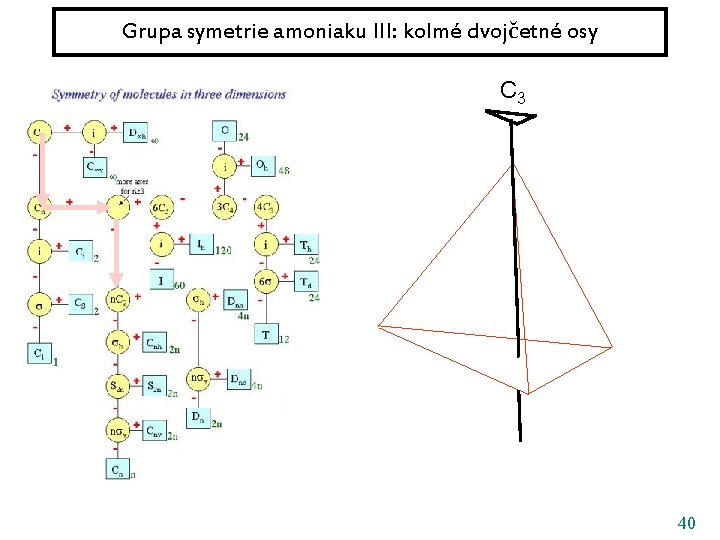
Grupa symetrie amoniaku III: kolmé dvojčetné osy C 3 40

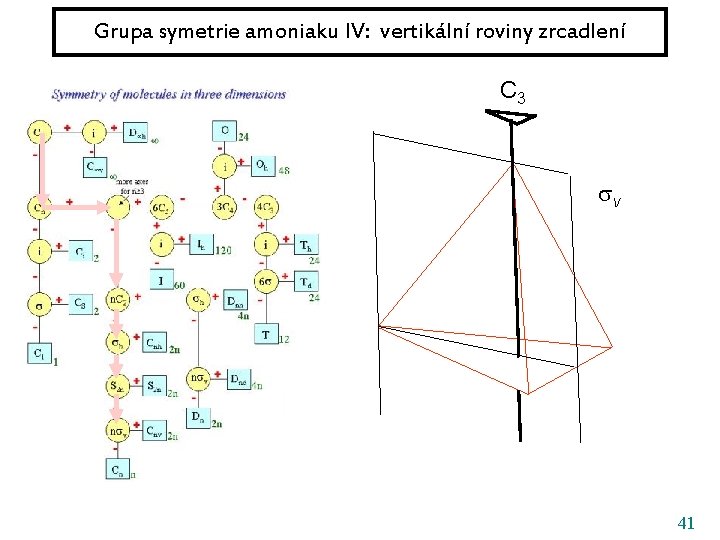
Grupa symetrie amoniaku IV: vertikální roviny zrcadlení C 3 v 41

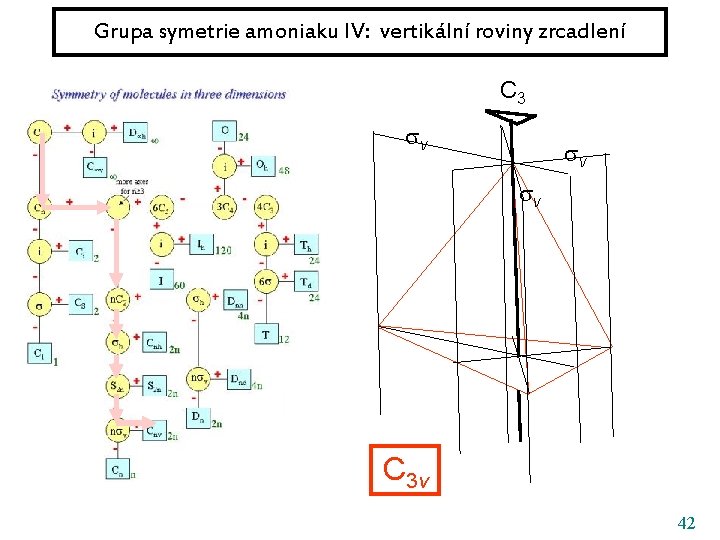
Grupa symetrie amoniaku IV: vertikální roviny zrcadlení C 3 v v v C 3 v 42

Planární nebo bipyramidální molekula: bodová symetrie

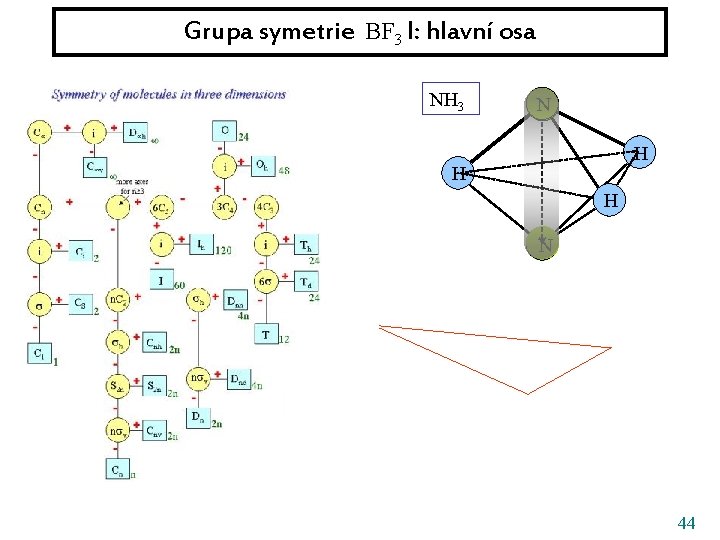
Grupa symetrie BF 3 I: hlavní osa NH 3 N H H H N 44

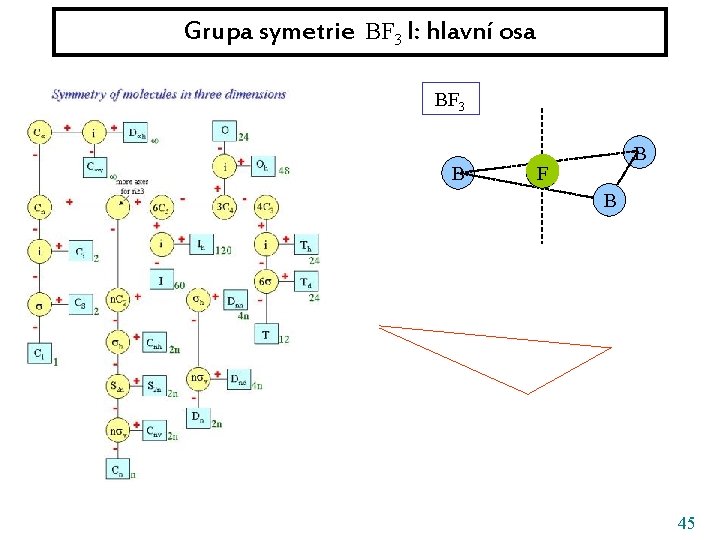
Grupa symetrie BF 3 I: hlavní osa BF 3 B B FN B 45

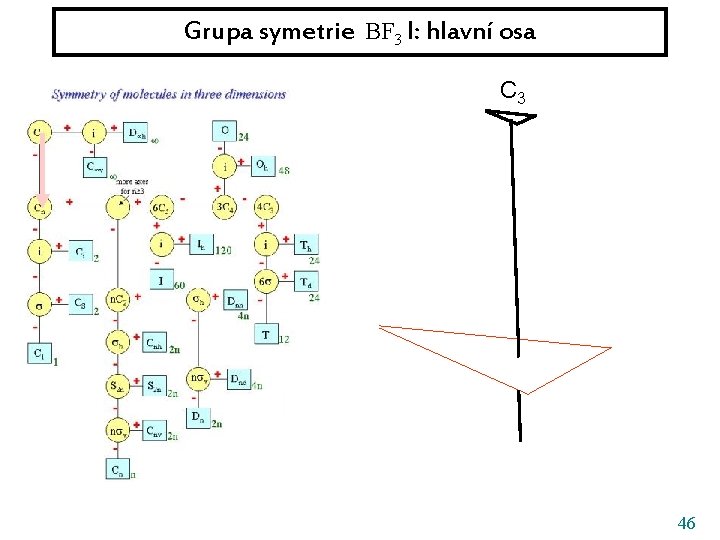
Grupa symetrie BF 3 I: hlavní osa C 3 46

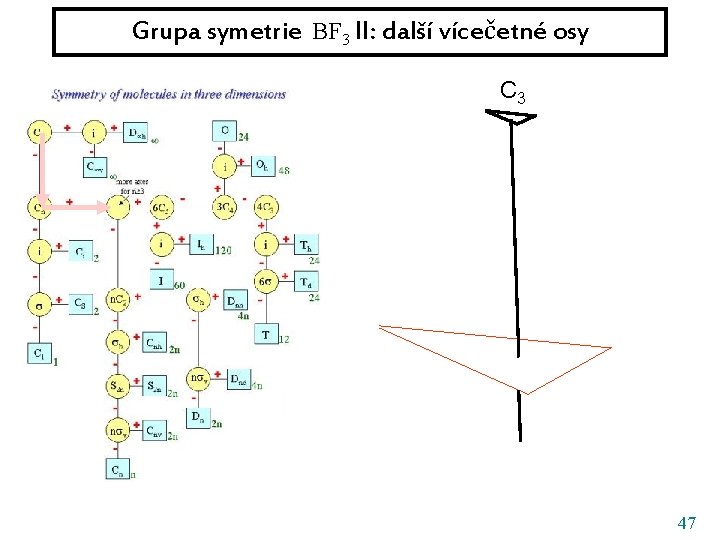
Grupa symetrie BF 3 II: další vícečetné osy C 3 47

Grupa symetrie BF 3 II: kolmé dvojčetné osy C 3 48

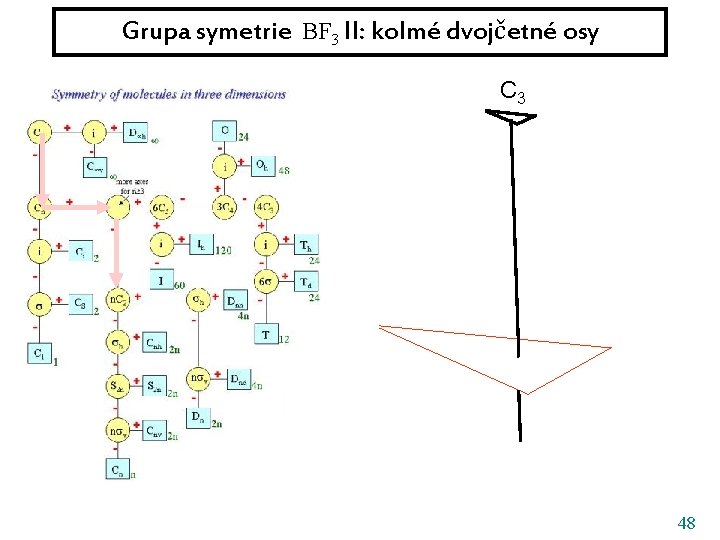
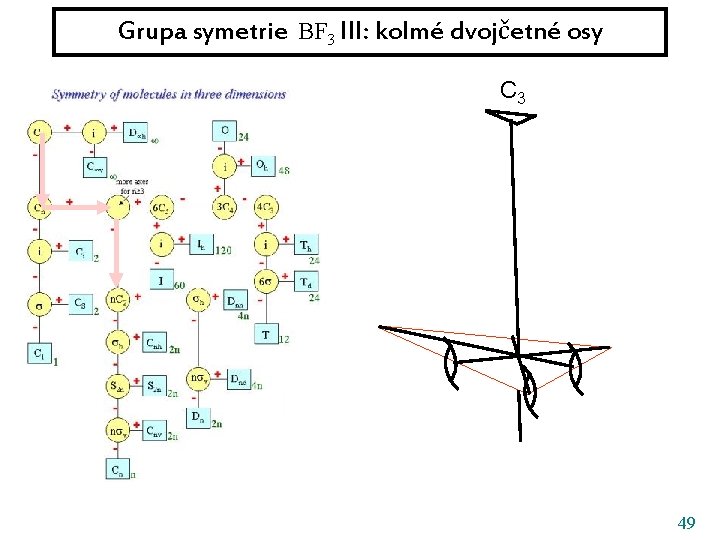
Grupa symetrie BF 3 III: kolmé dvojčetné osy C 3 49

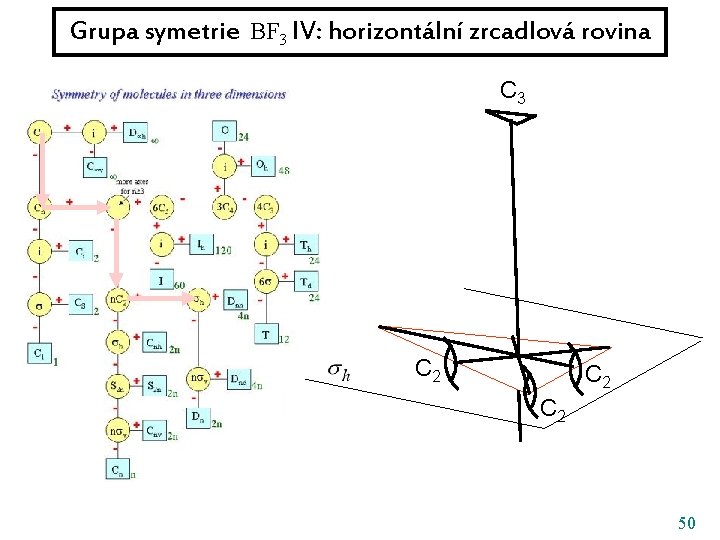
Grupa symetrie BF 3 IV: horizontální zrcadlová rovina C 3 C 2 C 2 50

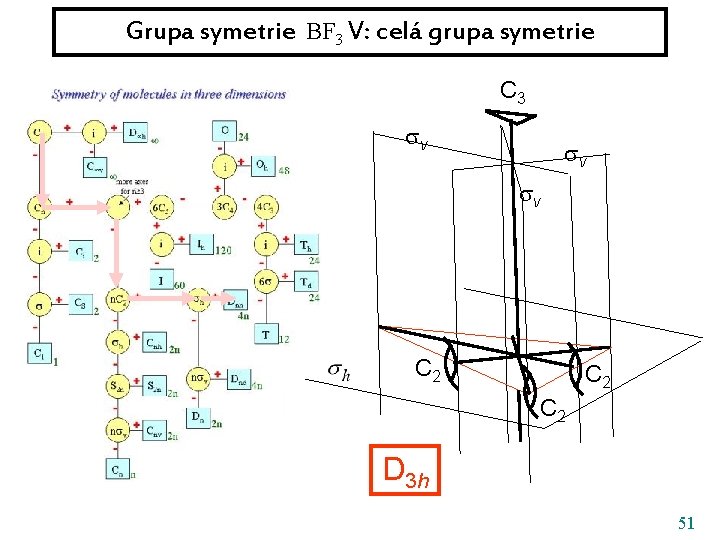
Grupa symetrie BF 3 V: celá grupa symetrie C 3 v v v C 2 C 2 D 3 h 51

Pyramidální molekula: normální kmity

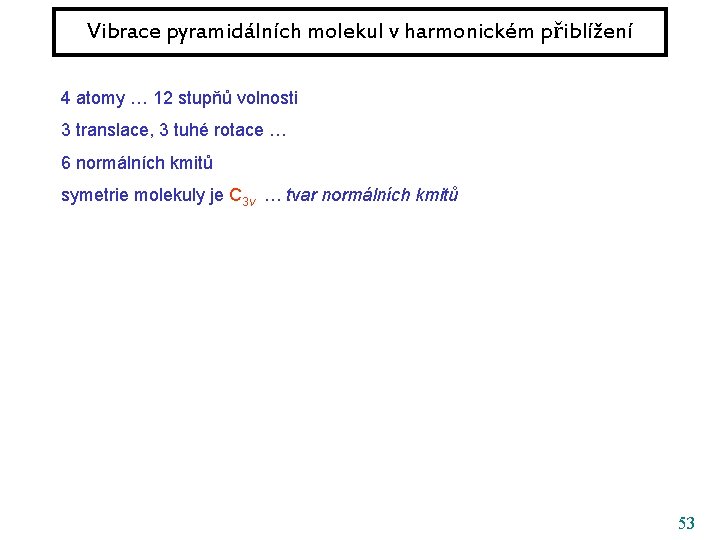
Vibrace pyramidálních molekul v harmonickém přiblížení 4 atomy … 12 stupňů volnosti 3 translace, 3 tuhé rotace … 6 normálních kmitů symetrie molekuly je C 3 v … tvar normálních kmitů 53

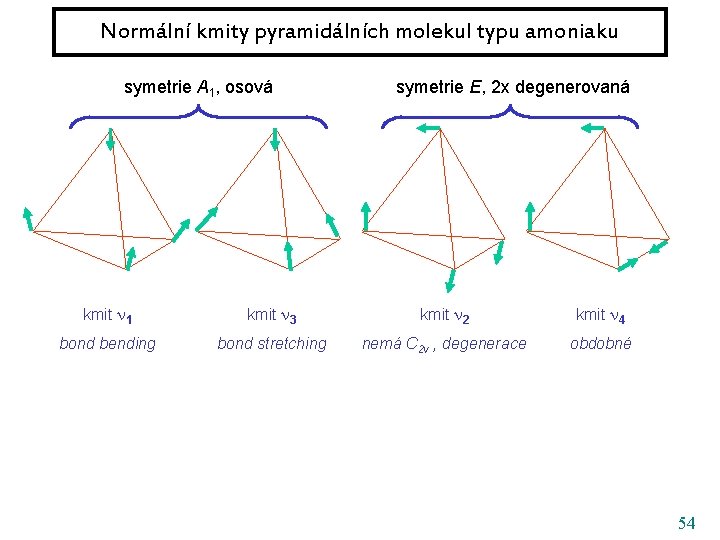
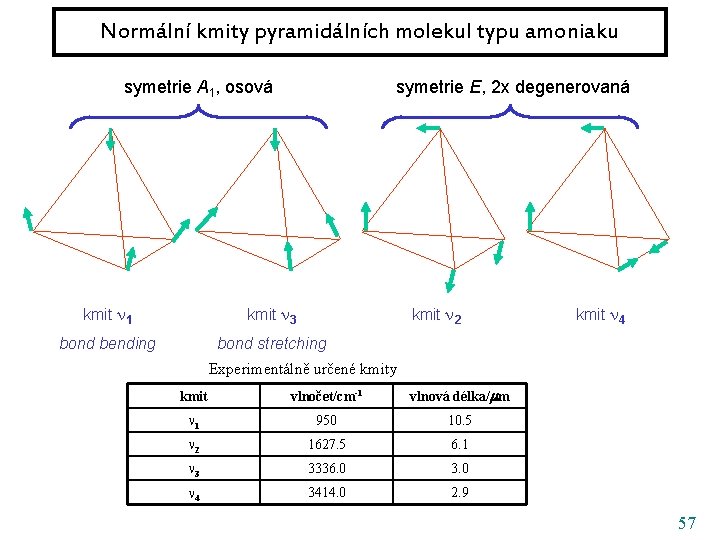
Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná kmit 1 kmit 3 kmit 2 kmit 4 bond bending bond stretching nemá C 2 v , degenerace obdobné 54

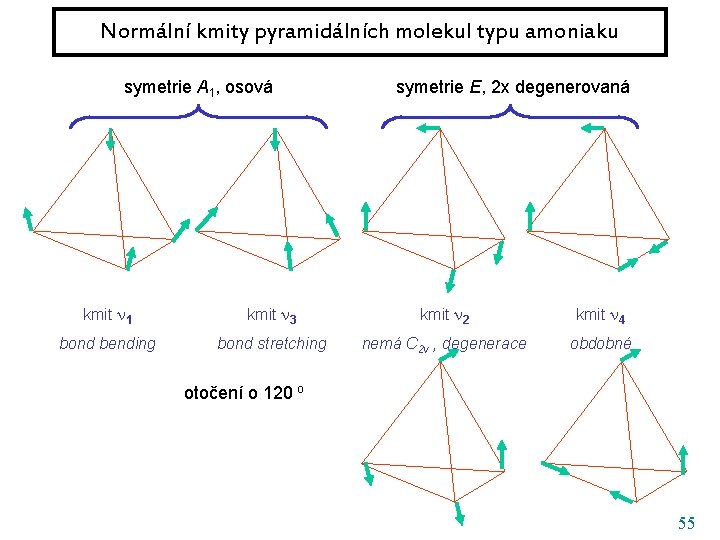
Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná kmit 1 kmit 3 kmit 2 kmit 4 bond bending bond stretching nemá C 2 v , degenerace obdobné otočení o 120 o 55

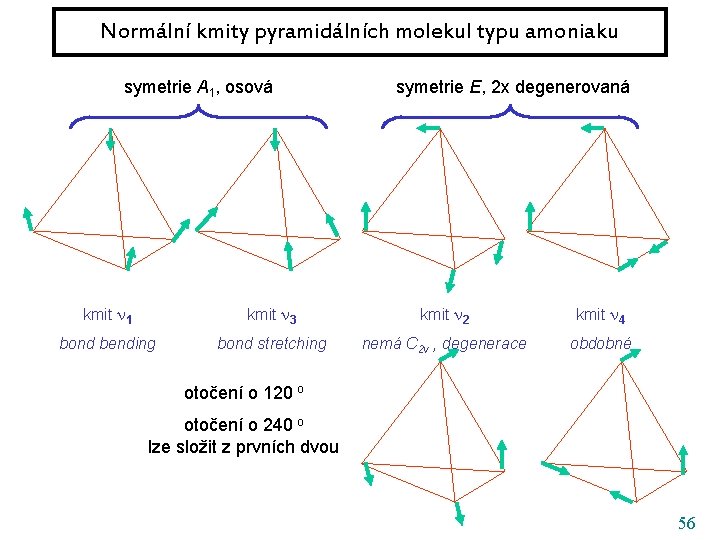
Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná kmit 1 kmit 3 kmit 2 kmit 4 bond bending bond stretching nemá C 2 v , degenerace obdobné otočení o 120 o otočení o 240 o lze složit z prvních dvou 56

Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná kmit 1 kmit 3 kmit 2 bond bending bond stretching kmit 4 Experimentálně určené kmity kmit vlnočet/cm-1 vlnová délka/ m 1 950 10. 5 2 1627. 5 6. 1 3 3336. 0 3. 0 4 3414. 0 2. 9 57

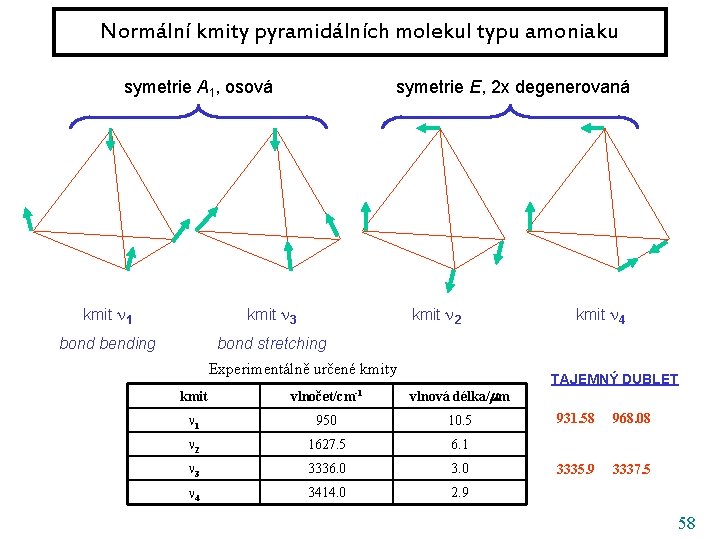
Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná kmit 1 kmit 3 kmit 2 bond bending bond stretching Experimentálně určené kmity kmit vlnočet/cm-1 vlnová délka/ m 1 950 10. 5 2 1627. 5 6. 1 3 3336. 0 3. 0 4 3414. 0 2. 9 kmit 4 TAJEMNÝ DUBLET 931. 58 968. 08 3335. 9 3337. 5 58

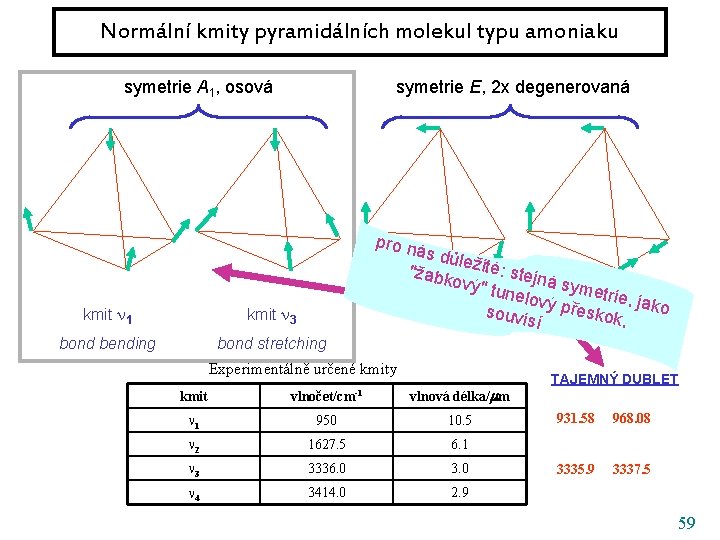
Normální kmity pyramidálních molekul typu amoniaku symetrie A 1, osová symetrie E, 2 x degenerovaná pro n ás dů le "žabk žité: stejn á ový" t unelo symetrie, vý pře ja sko k 4, ko kmit 2 souvis kmit í kmit 1 kmit 3 bond bending bond stretching Experimentálně určené kmity kmit vlnočet/cm-1 vlnová délka/ m 1 950 10. 5 2 1627. 5 6. 1 3 3336. 0 3. 0 4 3414. 0 2. 9 TAJEMNÝ DUBLET 931. 58 968. 08 3335. 9 3337. 5 59

Pyramidální molekula: tunelování

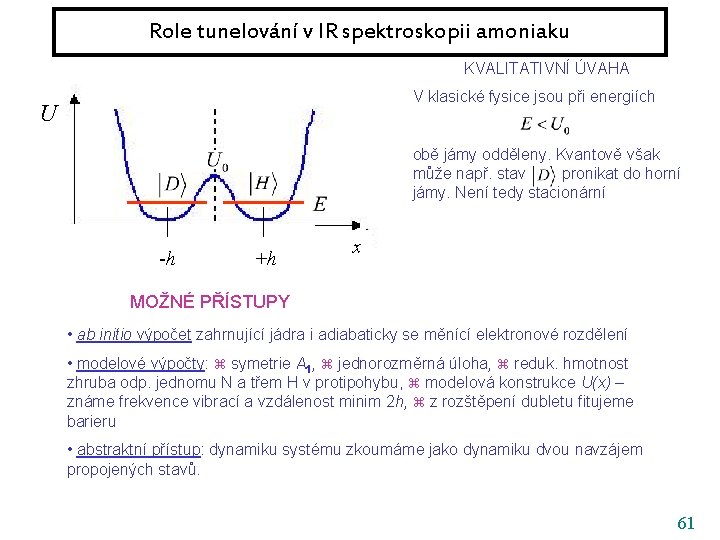
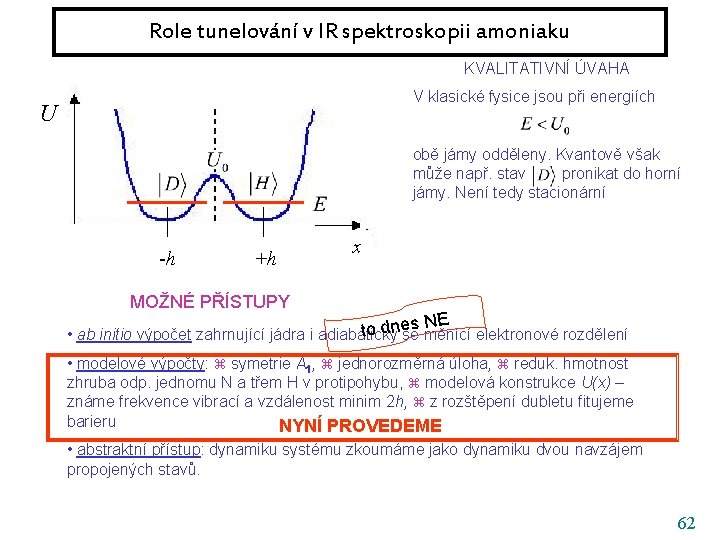
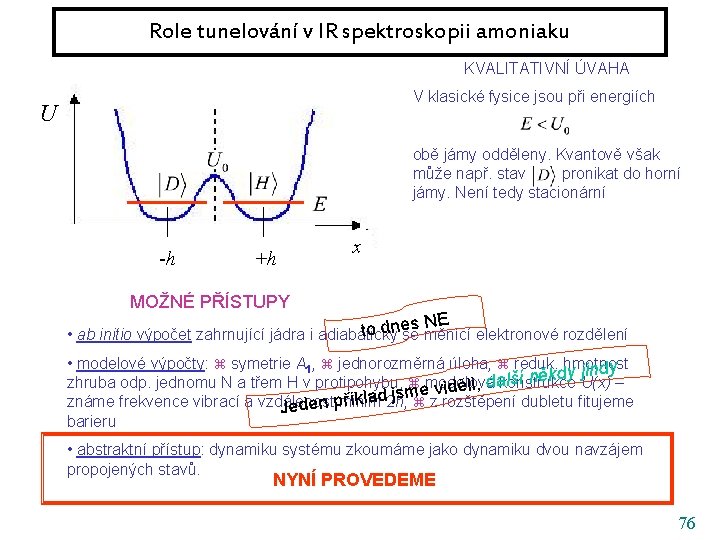
Role tunelování v IR spektroskopii amoniaku KVALITATIVNÍ ÚVAHA V klasické fysice jsou při energiích U obě jámy odděleny. Kvantově však může např. stav pronikat do horní jámy. Není tedy stacionární -h +h x MOŽNÉ PŘÍSTUPY • ab initio výpočet zahrnující jádra i adiabaticky se měnící elektronové rozdělení • modelové výpočty: symetrie A 1, jednorozměrná úloha, reduk. hmotnost zhruba odp. jednomu N a třem H v protipohybu, modelová konstrukce U(x) – známe frekvence vibrací a vzdálenost minim 2 h, z rozštěpení dubletu fitujeme barieru • abstraktní přístup: dynamiku systému zkoumáme jako dynamiku dvou navzájem propojených stavů. 61

Role tunelování v IR spektroskopii amoniaku KVALITATIVNÍ ÚVAHA V klasické fysice jsou při energiích U obě jámy odděleny. Kvantově však může např. stav pronikat do horní jámy. Není tedy stacionární -h +h x MOŽNÉ PŘÍSTUPY es NE n d o t • ab initio výpočet zahrnující jádra i adiabaticky se měnící elektronové rozdělení • modelové výpočty: symetrie A 1, jednorozměrná úloha, reduk. hmotnost zhruba odp. jednomu N a třem H v protipohybu, modelová konstrukce U(x) – známe frekvence vibrací a vzdálenost minim 2 h, z rozštěpení dubletu fitujeme barieru NYNÍ PROVEDEME • abstraktní přístup: dynamiku systému zkoumáme jako dynamiku dvou navzájem propojených stavů. 62

Příklad modelového výpočtu Implementace modelového postupu podle E. Merzbachera • redukovaná hmotnost • modelová potenciální energie všechno je tu známo, bariera je zcela určena. Její výška se rovná • na každé polopřímce lineární oscilátor: přechází Schrödingerova rovnici na posunutý • na hranici obou poloos se provede sešití dílčích řešení. 63

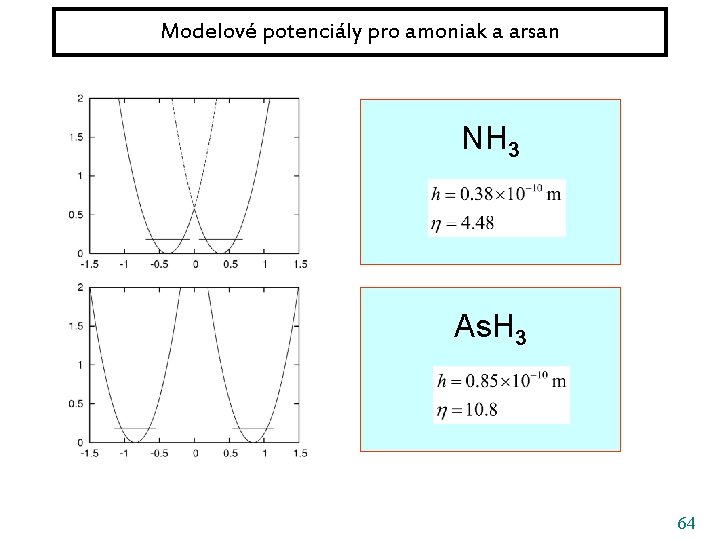
Modelové potenciály pro amoniak a arsan NH 3 As. H 3 64

Příklad modelového výpočtu Implementace modelového postupu podle E. Merzbachera • redukovaná hmotnost • modelová potenciální energie všechno je tu známo, bariera je zcela určena. Její výška se rovná • na každé polopřímce lineární oscilátor: přechází Schrödingerova rovnici na posunutý • na hranici obou poloos se provede sešití dílčích řešení. 65

Řešení a výsledky modelového výpočtu • Použití speciálních funkcí Pro obecnou hodnotu energie je SR pro lineární oscilátor řešena tzv. funkcemi parabolického cylindru Partikulární řešení se správnou asymptotikou při je Všechno se najde v příručkách, jako je Abramowicz&Stegun, nebo v Mathematica, … • Použití symetrie systém je symetrický vůči počátku, řešení jsou tedy buď lichá, nebo sudá. • Sešití při x = 0 bezrozměrná šířka bariéry 66

67

Řešení a výsledky modelového výpočtu • Použití speciálních funkcí Pro obecnou hodnotu energie je SR pro lineární oscilátor řešena tzv. funkcemi parabolického cylindru Partikulární řešení se správnou asymptotikou při je Všechno se najde v příručkách, jako je Abramowicz&Stegun, nebo v Mathematica, … • Použití symetrie systém je symetrický vůči počátku, řešení jsou tedy buď lichá, nebo sudá. • Sešití při x = 0 bezrozměrná šířka bariéry 68

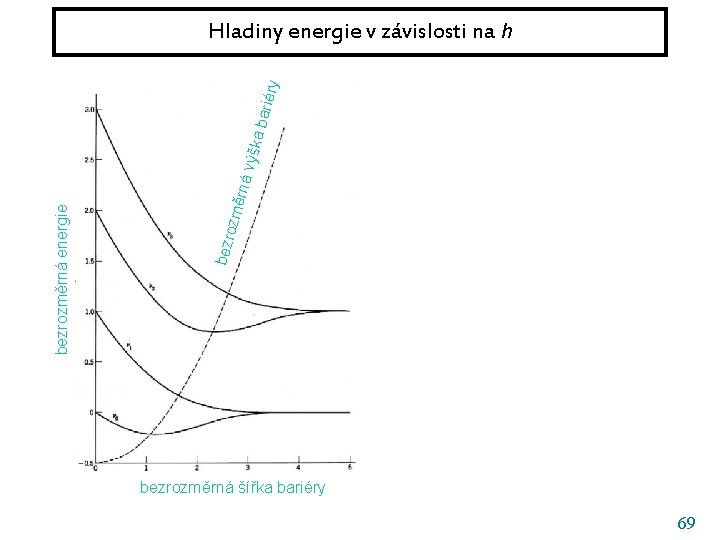
ěrná bezr ozm bezrozměrná energie výšk a ba riéry Hladiny energie v závislosti na h bezrozměrná šířka bariéry 69

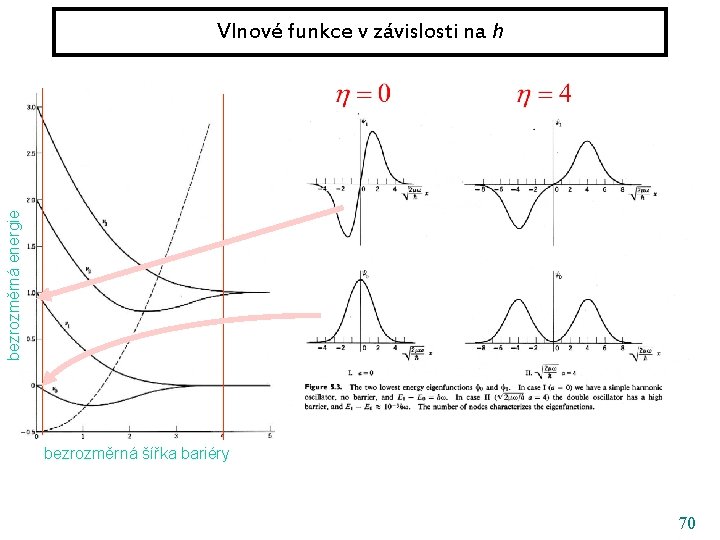
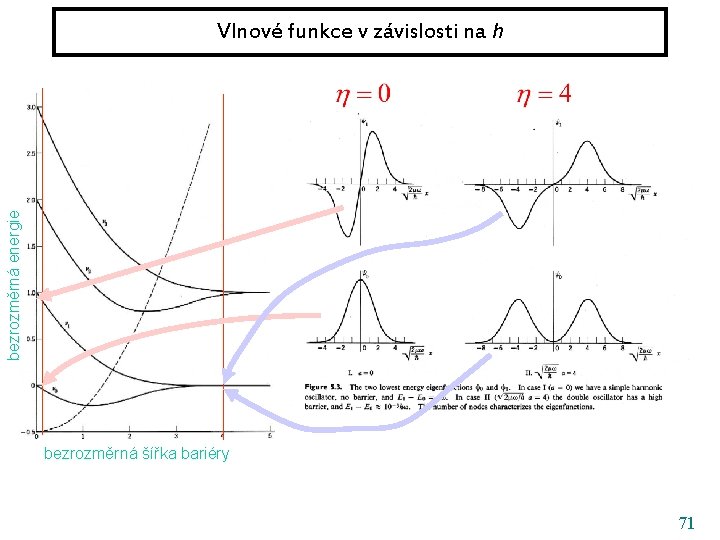
bezrozměrná energie Vlnové funkce v závislosti na h bezrozměrná šířka bariéry 70

bezrozměrná energie Vlnové funkce v závislosti na h bezrozměrná šířka bariéry 71

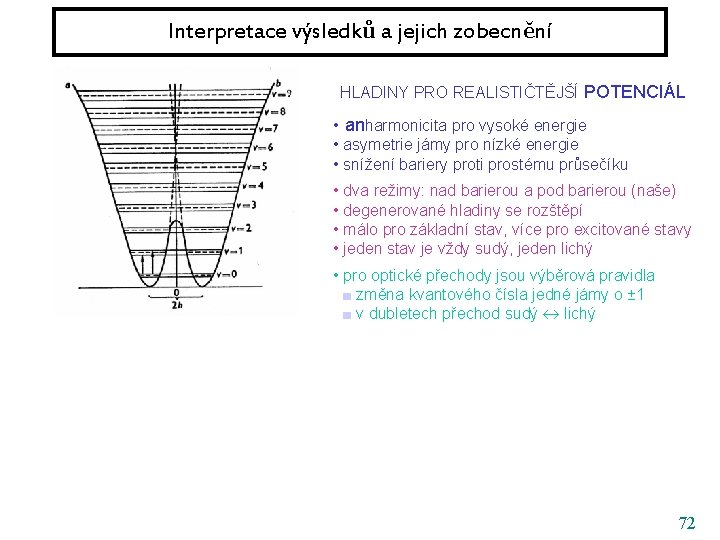
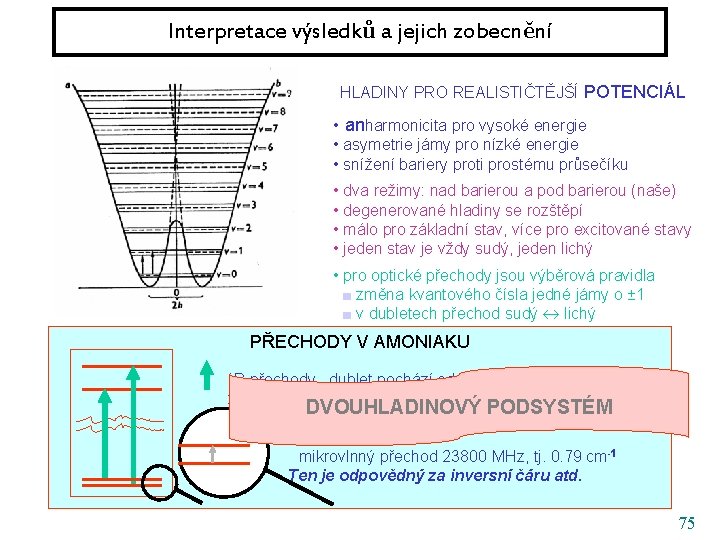
Interpretace výsledků a jejich zobecnění HLADINY PRO REALISTIČTĚJŠÍ POTENCIÁL • anharmonicita pro vysoké energie • asymetrie jámy pro nízké energie • snížení bariery proti prostému průsečíku • dva režimy: nad barierou a pod barierou (naše) • degenerované hladiny se rozštěpí • málo pro základní stav, více pro excitované stavy • jeden stav je vždy sudý, jeden lichý • pro optické přechody jsou výběrová pravidla ■ změna kvantového čísla jedné jámy o ± 1 ■ v dubletech přechod sudý lichý 72

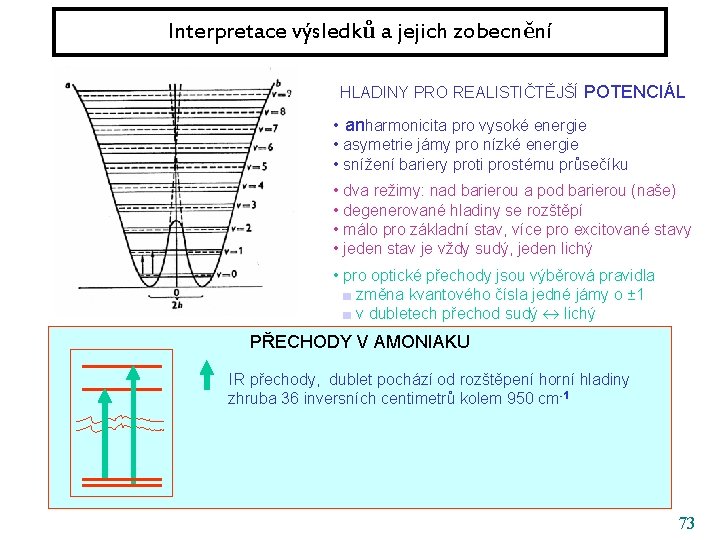
Interpretace výsledků a jejich zobecnění HLADINY PRO REALISTIČTĚJŠÍ POTENCIÁL • anharmonicita pro vysoké energie • asymetrie jámy pro nízké energie • snížení bariery proti prostému průsečíku • dva režimy: nad barierou a pod barierou (naše) • degenerované hladiny se rozštěpí • málo pro základní stav, více pro excitované stavy • jeden stav je vždy sudý, jeden lichý • pro optické přechody jsou výběrová pravidla ■ změna kvantového čísla jedné jámy o ± 1 ■ v dubletech přechod sudý lichý PŘECHODY V AMONIAKU IR přechody, dublet pochází od rozštěpení horní hladiny zhruba 36 inversních centimetrů kolem 950 cm -1 73

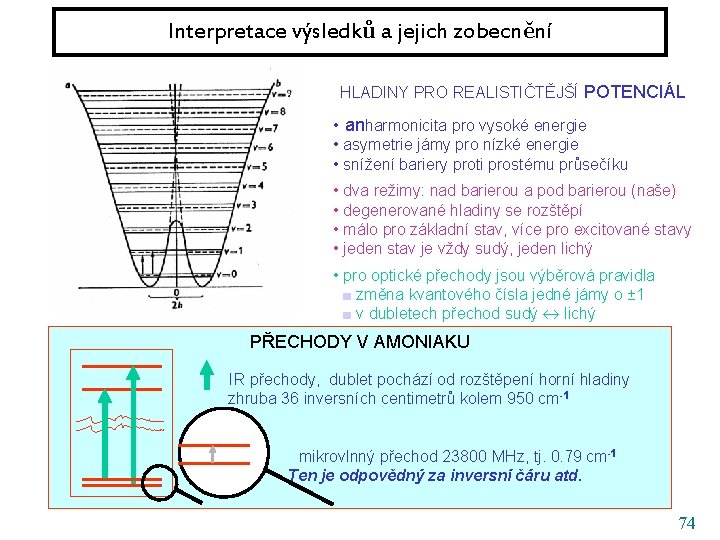
Interpretace výsledků a jejich zobecnění HLADINY PRO REALISTIČTĚJŠÍ POTENCIÁL • anharmonicita pro vysoké energie • asymetrie jámy pro nízké energie • snížení bariery proti prostému průsečíku • dva režimy: nad barierou a pod barierou (naše) • degenerované hladiny se rozštěpí • málo pro základní stav, více pro excitované stavy • jeden stav je vždy sudý, jeden lichý • pro optické přechody jsou výběrová pravidla ■ změna kvantového čísla jedné jámy o ± 1 ■ v dubletech přechod sudý lichý PŘECHODY V AMONIAKU IR přechody, dublet pochází od rozštěpení horní hladiny zhruba 36 inversních centimetrů kolem 950 cm -1 mikrovlnný přechod 23800 MHz, tj. 0. 79 cm-1 Ten je odpovědný za inversní čáru atd. 74

Interpretace výsledků a jejich zobecnění HLADINY PRO REALISTIČTĚJŠÍ POTENCIÁL • anharmonicita pro vysoké energie • asymetrie jámy pro nízké energie • snížení bariery proti prostému průsečíku • dva režimy: nad barierou a pod barierou (naše) • degenerované hladiny se rozštěpí • málo pro základní stav, více pro excitované stavy • jeden stav je vždy sudý, jeden lichý • pro optické přechody jsou výběrová pravidla ■ změna kvantového čísla jedné jámy o ± 1 ■ v dubletech přechod sudý lichý PŘECHODY V AMONIAKU IR přechody, dublet pochází od rozštěpení horní hladiny zhruba 36 inversních centimetrů kolem 950 cm -1 DVOUHLADINOVÝ PODSYSTÉM mikrovlnný přechod 23800 MHz, tj. 0. 79 cm-1 Ten je odpovědný za inversní čáru atd. 75

Role tunelování v IR spektroskopii amoniaku KVALITATIVNÍ ÚVAHA V klasické fysice jsou při energiích U obě jámy odděleny. Kvantově však může např. stav pronikat do horní jámy. Není tedy stacionární -h +h x MOŽNÉ PŘÍSTUPY es NE n d o t • ab initio výpočet zahrnující jádra i adiabaticky se měnící elektronové rozdělení • modelové výpočty: symetrie A 1, jednorozměrná úloha, reduk. hmotnost y jindy d k ě n í lš a zhruba odp. jednomu N a třem H v protipohybu, modelová viděli, d konstrukce U(x) – e m js d la řík 2 h, z rozštěpení dubletu fitujeme známe frekvence vibrací a vzdálenost Jeden pminim barieru • abstraktní přístup: dynamiku systému zkoumáme jako dynamiku dvou navzájem propojených stavů. NYNÍ PROVEDEME 76

Dynamika dvouhladinového systému Schrödingerova rovnice Dvoustavový systém Systém vázaných rovnic pro koeficienty ekvivalentní se SR 77

Dynamika dvouhladinového systému Stacionární stavy ´ ve shodě s modelovým výpočtem 78

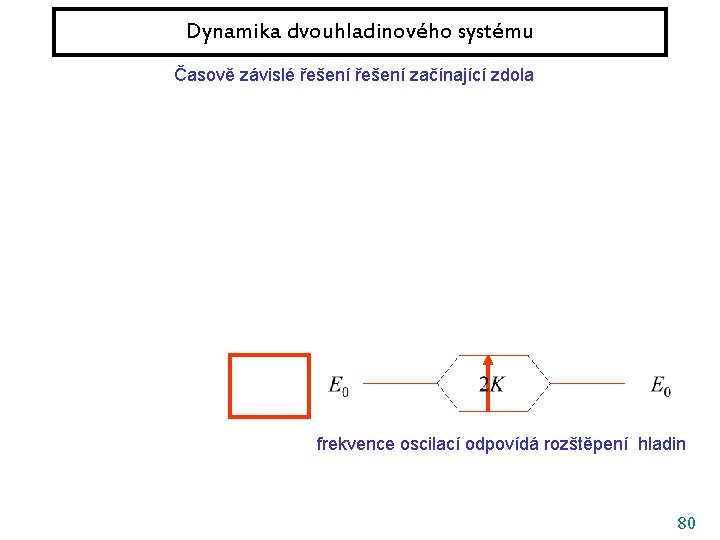
Dynamika dvouhladinového systému Časově závislé řešení začínající zdola 79

Dynamika dvouhladinového systému Časově závislé řešení začínající zdola frekvence oscilací odpovídá rozštěpení hladin 80

Čpavkové hodiny: první „atomové hodiny“

Oficiální zdůvodnění pro stavbu čpavkových hodin v NBS The Bureau atomic clock program sought to provide a spectroscopic standard capable of being used as a new atomic standard of time and frequency to replace the mean solar day and so change the arbitrary units of time to atomic ones. With such a clock, new precise values might be found for the velocity of light; new measurements of the rotation of the earth would provide a new tool for geophysicists; and new measurments of the mean sidereal year might test whether Newtonian and atomic time are the same, yielding important results for relativity theory and cosmology. 82

Čpavkové hodiny Trochu divná historie resonátor Dr. Condon ředitel NBS Stabilisace parami amoniaku byla známa pro klystrony už za války a možná i dřív. Po válce se rozpoutala soutěž o "atomový" časový standard. NBS (nyní NIST) se rozhodl pro rychlou akci a použít amoniaku k řízení křemenných hodin, ač se vědělo, že perspektivní jsou spíš elektronové přechody v parách alkalických kovů. Dr. Lyons konstruktér Sám přechod měl šířku čáry jen 1 k. Hz, to bylo slibné. Problém ale nastal s Dopplerovým rozšířením a také s tlakovou závislostí šířky čáry. Nikdy nebyla přesnost lepší než 10 -8 a proto nebyla předstižena časomíra odvozená od tropického roku, ačkoli denní cyklus Slunce byl zhruba srovnatelný. 83

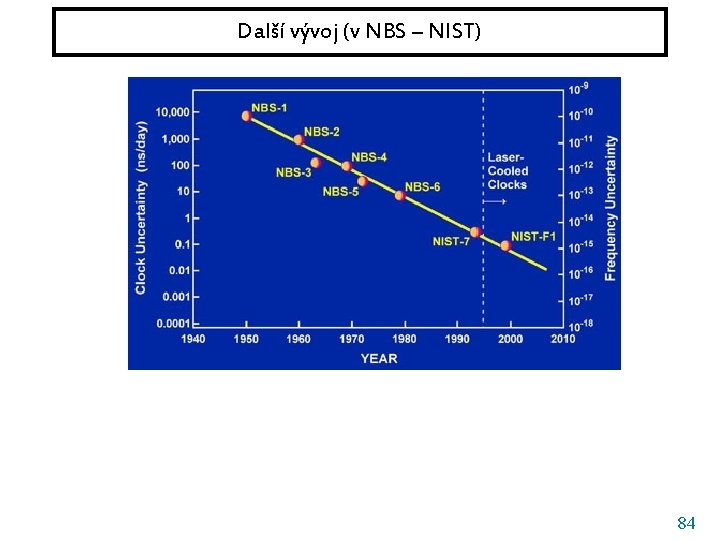
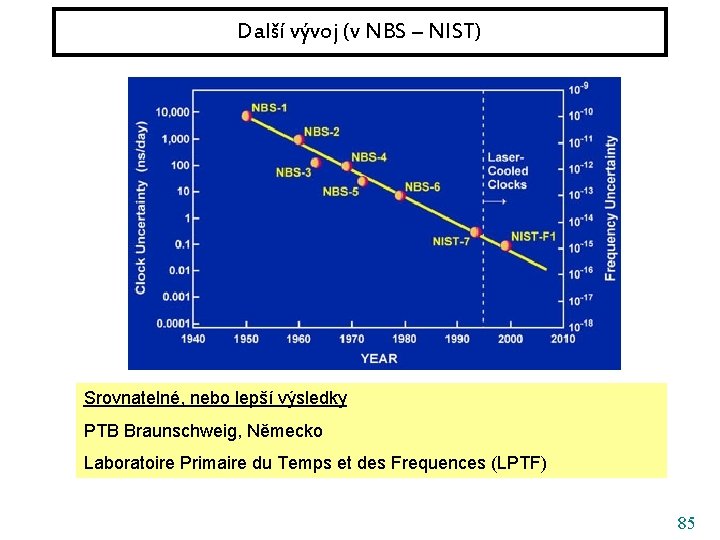
Další vývoj (v NBS – NIST) 84

Další vývoj (v NBS – NIST) Srovnatelné, nebo lepší výsledky PTB Braunschweig, Německo Laboratoire Primaire du Temps et des Frequences (LPTF) 85

Objev maseru

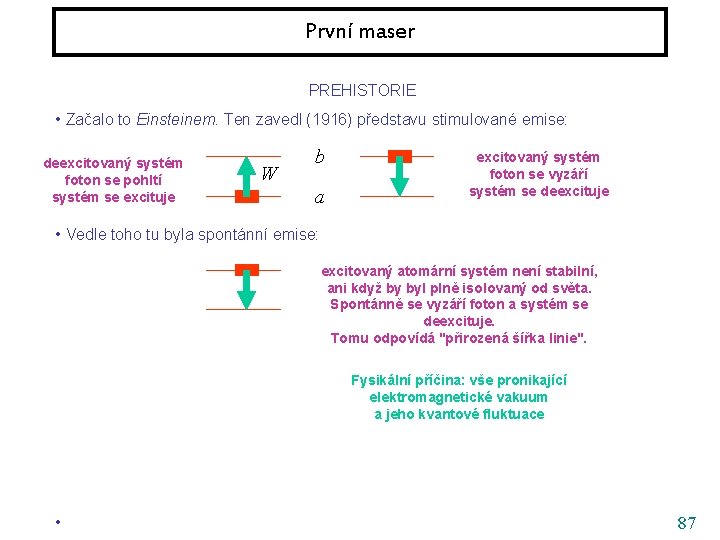
První maser PREHISTORIE • Začalo to Einsteinem. Ten zavedl (1916) představu stimulované emise: deexcitovaný systém foton se pohltí systém se excituje W b a excitovaný systém foton se vyzáří systém se deexcituje • Vedle toho tu byla spontánní emise: excitovaný atomární systém není stabilní, ani když by byl plně isolovaný od světa. Spontánně se vyzáří foton a systém se deexcituje. Tomu odpovídá "přirozená šířka linie". Fysikální příčina: vše pronikající elektromagnetické vakuum a jeho kvantové fluktuace • 87

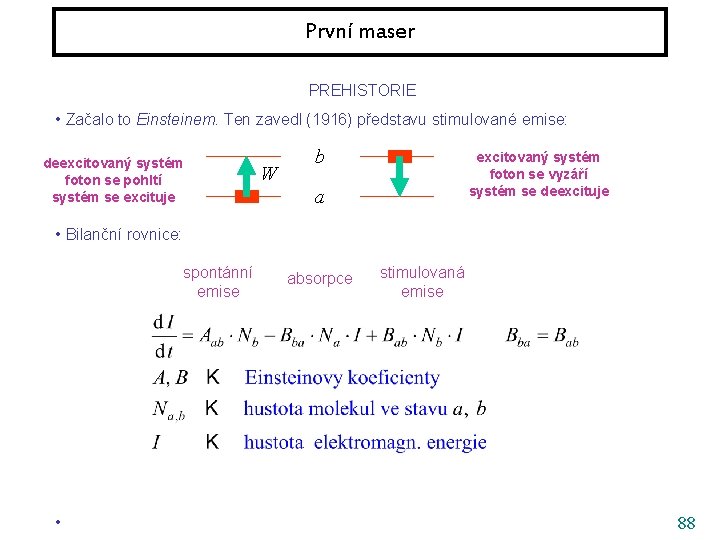
První maser PREHISTORIE • Začalo to Einsteinem. Ten zavedl (1916) představu stimulované emise: deexcitovaný systém foton se pohltí systém se excituje W b excitovaný systém foton se vyzáří systém se deexcituje a • Bilanční rovnice: spontánní emise • absorpce stimulovaná emise 88

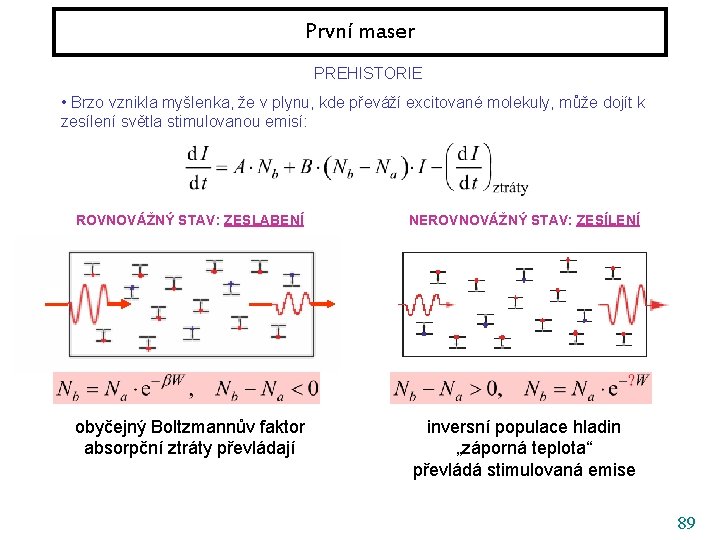
První maser PREHISTORIE • Brzo vznikla myšlenka, že v plynu, kde převáží excitované molekuly, může dojít k zesílení světla stimulovanou emisí: ROVNOVÁŽNÝ STAV: ZESLABENÍ NEROVNOVÁŽNÝ STAV: ZESÍLENÍ obyčejný Boltzmannův faktor absorpční ztráty převládají inversní populace hladin „záporná teplota“ převládá stimulovaná emise 89

První maser Jak toho ale dosáhnout? První, spíše demonstrační realisace vznikla v laboratoři C. H. Townese (Columbia U. ). Myšlenka v r. 1951, realisace v r. 1954. • Také zde vycházeli z válečných poznatků (CHT byl radarový specialista) • Záření uzavřít do kvalitního resonátoru, jen slabý přebytek výkonu vyvádět • Hlavní problém: stálá obnova inversní populace … průtokovým uspořádáním • Kde inversní populaci získat … separátorem 90

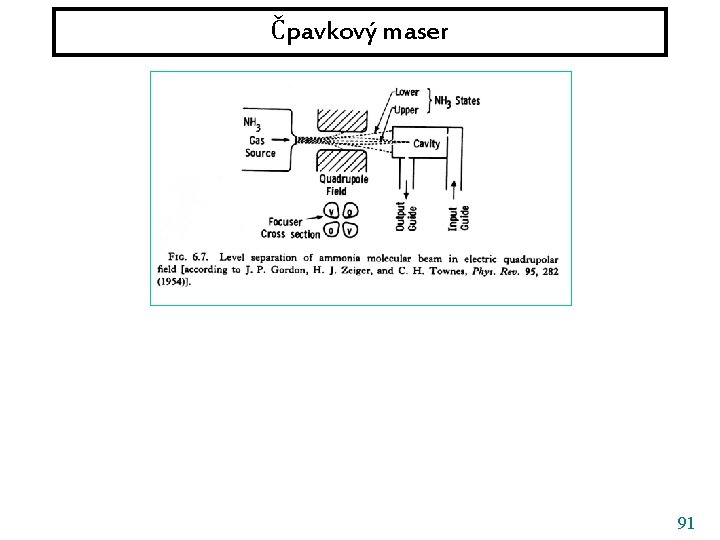
Čpavkový maser 91

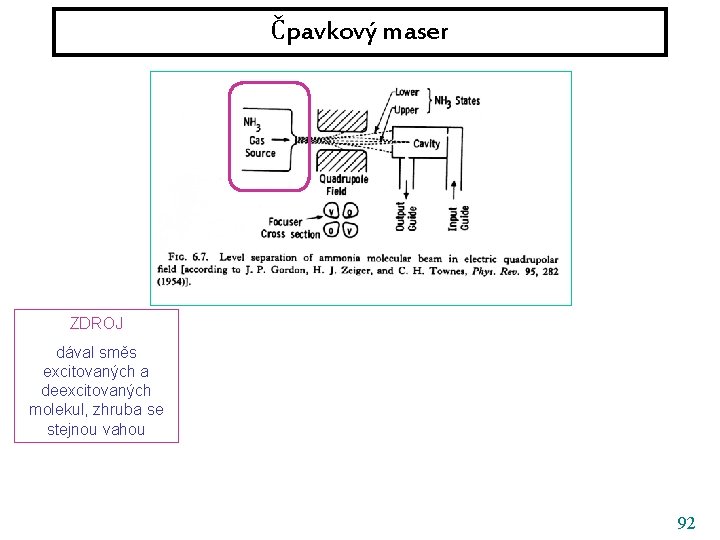
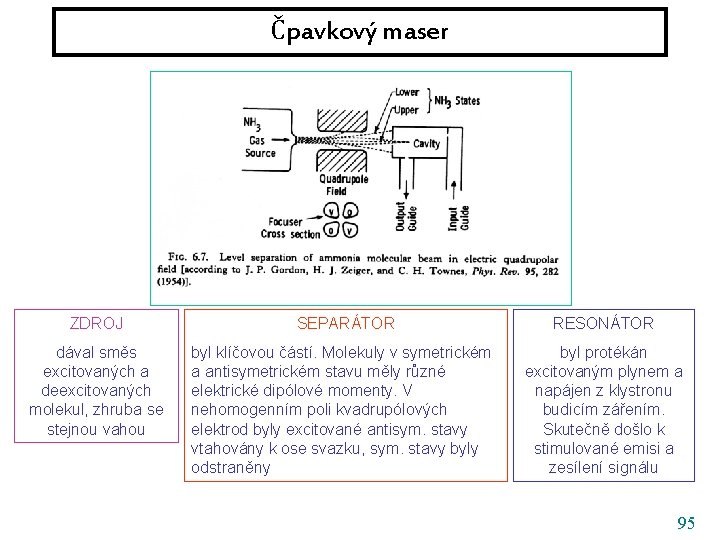
Čpavkový maser ZDROJ dával směs excitovaných a deexcitovaných molekul, zhruba se stejnou vahou 92

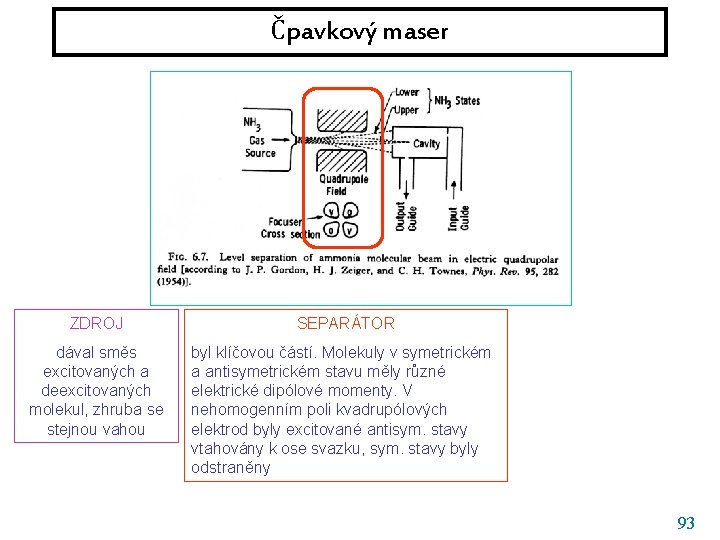
Čpavkový maser ZDROJ SEPARÁTOR dával směs excitovaných a deexcitovaných molekul, zhruba se stejnou vahou byl klíčovou částí. Molekuly v symetrickém a antisymetrickém stavu měly různé elektrické dipólové momenty. V nehomogenním poli kvadrupólových elektrod byly excitované antisym. stavy vtahovány k ose svazku, sym. stavy byly odstraněny 93

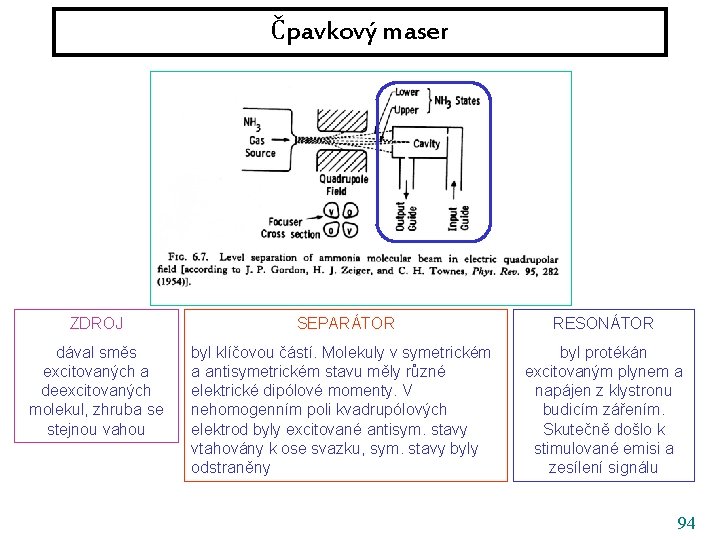
Čpavkový maser ZDROJ SEPARÁTOR RESONÁTOR dával směs excitovaných a deexcitovaných molekul, zhruba se stejnou vahou byl klíčovou částí. Molekuly v symetrickém a antisymetrickém stavu měly různé elektrické dipólové momenty. V nehomogenním poli kvadrupólových elektrod byly excitované antisym. stavy vtahovány k ose svazku, sym. stavy byly odstraněny byl protékán excitovaným plynem a napájen z klystronu budicím zářením. Skutečně došlo k stimulované emisi a zesílení signálu 94

Čpavkový maser ZDROJ SEPARÁTOR RESONÁTOR dával směs excitovaných a deexcitovaných molekul, zhruba se stejnou vahou byl klíčovou částí. Molekuly v symetrickém a antisymetrickém stavu měly různé elektrické dipólové momenty. V nehomogenním poli kvadrupólových elektrod byly excitované antisym. stavy vtahovány k ose svazku, sym. stavy byly odstraněny byl protékán excitovaným plynem a napájen z klystronu budicím zářením. Skutečně došlo k stimulované emisi a zesílení signálu 95

Townes a Gordon se svým maserem 96

Townes maser Gordon NP 1964 97

Vznik slova “Maser”: až ve druhém sdělení 98

Co pozorovali • zesílení mikrovlnného signálu • při průtoku amoniaku nad kritickou hodnotu systém fungoval jako generátor záření (autoři říkají oscilátor), tj. zářil i bez pomocné stimulace vnějším polem • vyzařovaná čára byla velmi ostrá … šířka 2 k. Hz při 23. 8 GHz vlastně tedy koherentní záření • s tím souvisel i mimořádně malý šum 99

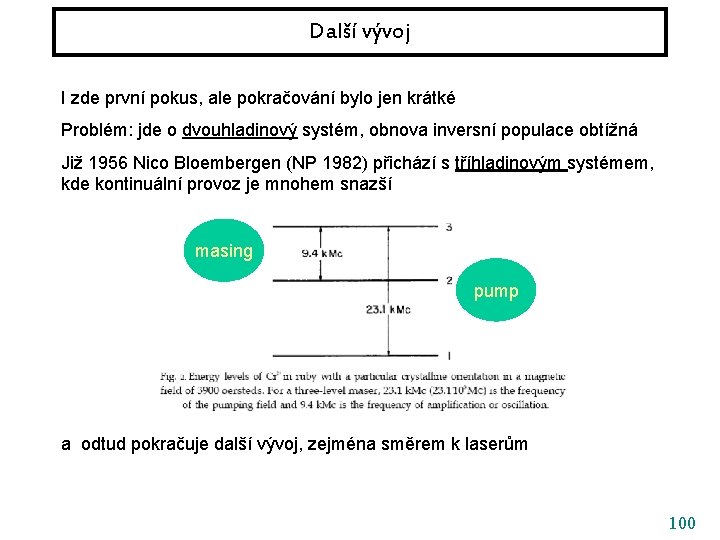
Další vývoj I zde první pokus, ale pokračování bylo jen krátké Problém: jde o dvouhladinový systém, obnova inversní populace obtížná Již 1956 Nico Bloembergen (NP 1982) přichází s tříhladinovým systémem, kde kontinuální provoz je mnohem snazší masing pump a odtud pokračuje další vývoj, zejména směrem k laserům 100

The end 101