Dijagramikorisne informacije o redoks reakcijama u otopini n










![elektron – ne postoji kao vrsta u otopini [e°]- aktivnost elektrona nema fizički smisao elektron – ne postoji kao vrsta u otopini [e°]- aktivnost elektrona nema fizički smisao](https://slidetodoc.com/presentation_image_h2/cb73d4f8617ab4994ee03cbf11d7711f/image-16.jpg)










- Slides: 37

Dijagrami-korisne informacije o redoks reakcijama u otopini n Latimerov dijagram n Frostov dijagram n Pourbaix-ov dijagram n p. E-p. H dijagram

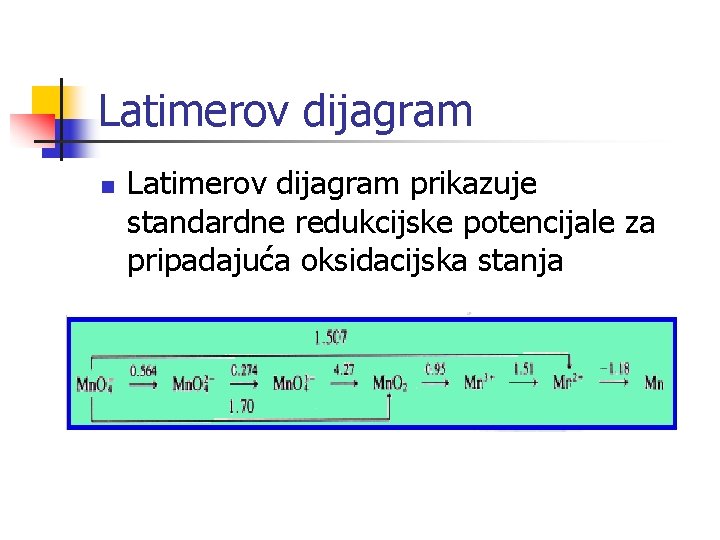
Latimerov dijagram n Latimerov dijagram prikazuje standardne redukcijske potencijale za pripadajuća oksidacijska stanja

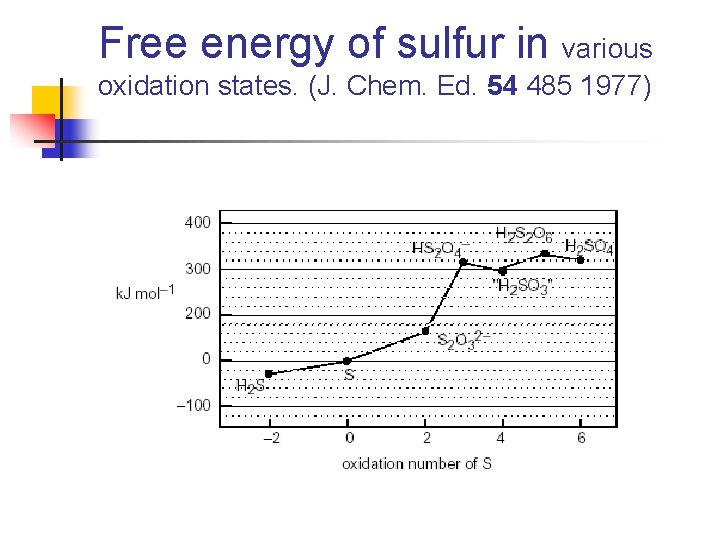
Free energy of sulfur in various oxidation states. (J. Chem. Ed. 54 485 1977)

Latimerovi dijagrami za klor i sumpor u vodenoj otopini

Frostov dijagram n Frostov dijagram pokazuje promjenu Gibsove energije kao funkciju različitih oksidacijskih stanja.

Analiza Frostovog dijagrama n n n n Mn (II) je najstabilnije oksidacijsko stanje mangana. Mn. O 42 - i Mn (III) skloni disproporcioniraju Mn. O 2 ne disproporcionira Mn. O 4 - je jako oksidacijsko sredstvo. Mangan u elementarnom stanju je srednje jako redukcijsko sredstvo Premda je termodinamički pogodna redukcija permanganata do Mn (II) iona, reakcija je spora osim u prisustvu katalizatora. Radi toga su otopine permanganata stabilne U bazičnim uvjetima ne postoji Mn 2+ već netopljivi Mn(OH)2

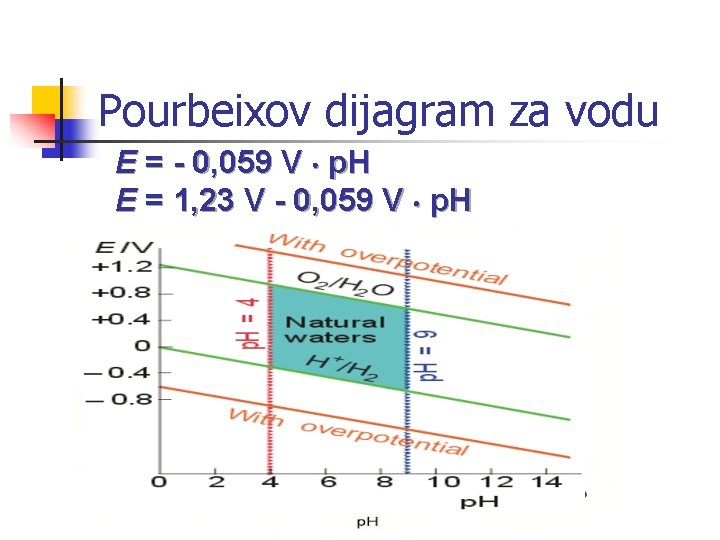
Pourbaix-ovi dijagrami i redoks reakcije u vodenoj otopini n n Voda može biti oksidacijsko sredstvo: H+ + e H 2 O + e - 1/ 1/ 2 H 2 o p. H = 7 E = -0, 414 - p. H = 14 E =-0, 828 H + OH 2 2 E = -0, 059 V p. H

n Voda može biti redukcijsko sredstvo: REDUCIRAJUĆE DJELOVANJE: o n n 1/ + + 2 e. O + 2 H 2 2 o -II + + 2 e. O + 2 H 2 2 o 2 O 2 + H 2 O + 2 e- -II H 2 O p. H =0 E = 1, 23 V p. H = 7 E = 0, 82 V 2 OH- p. H = 14 E = 0, 41 V

Pourbeixov dijagram za vodu E = - 0, 059 V p. H E = 1, 23 V - 0, 059 V p. H

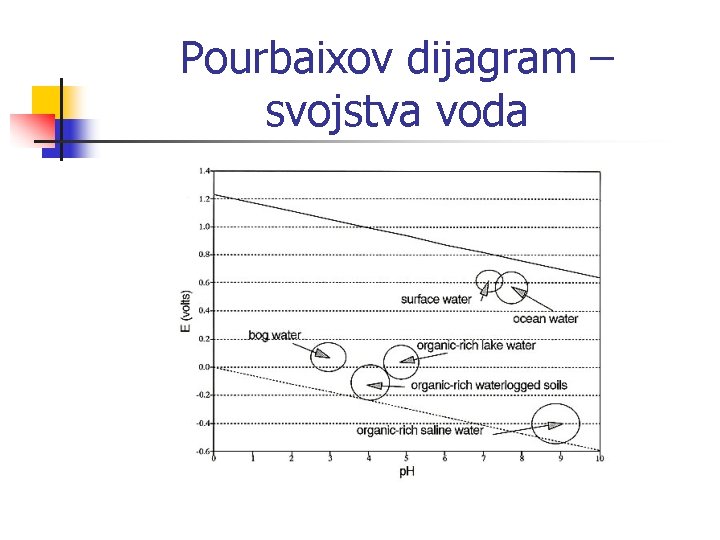
Pourbaixov dijagram – svojstva voda

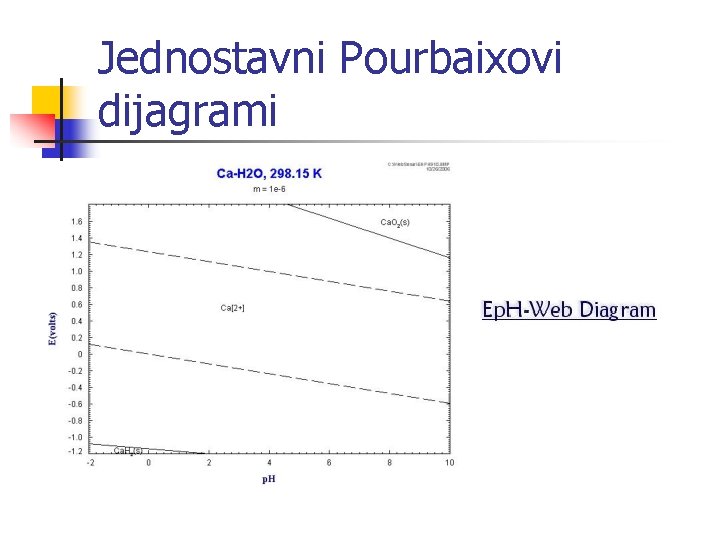
Jednostavni Pourbaixovi dijagrami

Purbeixov dijagram za mangan

Analiza Pourbeixova dijagrama n n Svaka točka na dijagramu odgovara termodinamički najstabilnijoj i najprisutnijoj formi elementa pri odabranom potencijalu i p. H vrijednosti Jaka oksidacijska sredstva nalaze se samo na vrhu Pourbaixova dijagrama. Permanganat je oksidacijsko sredstvu u širokom spektru p. H vrijednosti. Također je jako oksidacijsko sredstvo pri niskim p. H vrijednostima. n Reducirajuća sredstva nalaze se na dnu dijagrama. Mangan u elementarnom stanju je redukcijsko sredstvo pri svim p. H vrijednostima. A posebice je jako redukcijsko sredstvu u bazičnom području.

n n n Kada dominantno područje za odabrano oksidacijsko stanje nestaje potpuno ispod ili iznad odabrane p. H vrijednosti tada element podliježe disproporcioniranju Mn. O 42 - pokazuje tendenciju prema disproporcioniranju. Ionske vrste koje se nalaze u području od vrha prema dnu na odabranoj p. H vrijednosti ne pokazuju ni oksidacijska ni redukcijska svojstva kod te vrijednosti p. H.

Electronska aktivnost i p. E n n n n Kemijske reakcije koje se zbivaju spontano imaju negativnu ΔG (te radi toga pozitivnu vrijednost ΔE) ΔG = -z. FE U ravnoteži nema daljnjih promjena u kemijskom sastavu te je: ΔG = 0 Korištenjem tih informacija koristimo se kako bismo predviđali kemijski sastav u ravnoteži: E je proporcionalan G, odnosno G = -z. FE E je proporcionalan p. E (p. E = -log ae-)
![elektron ne postoji kao vrsta u otopini e aktivnost elektrona nema fizički smisao elektron – ne postoji kao vrsta u otopini [e°]- aktivnost elektrona nema fizički smisao](https://slidetodoc.com/presentation_image_h2/cb73d4f8617ab4994ee03cbf11d7711f/image-16.jpg)
elektron – ne postoji kao vrsta u otopini [e°]- aktivnost elektrona nema fizički smisao e- označava redukcijsku sposobnost otopine

Niska vrijednost p. E -izražena redukcijska svojstva otopine (niska vrijednost p. H – označava kisela svojstva). n n Za izračunavanje p. E pri nestandarnim uvjetima aktiviteta i tlaka rabi se Nernstova jednadžba Niski p. E – redukcijska svojstva Visoki p. E- oksidacijska svojstva

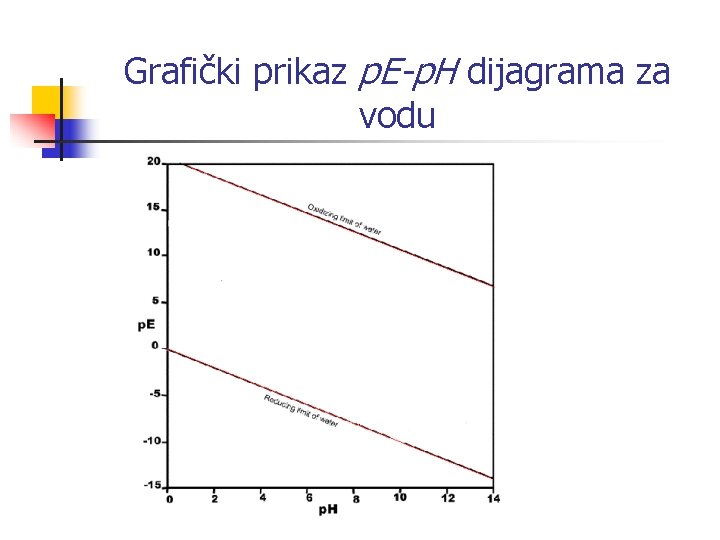
p. E-p. H dijagram vode n Voda se može oksidirati Voda se može reducirati Oksidacijski limit

Oksidacijski limit vode p. E = 20. 75 + log(H+) ili p. E = 20. 75 - p. H

Redukcijski limit vode Granične vrijednosti

Grafički prikaz p. E-p. H dijagrama za vodu

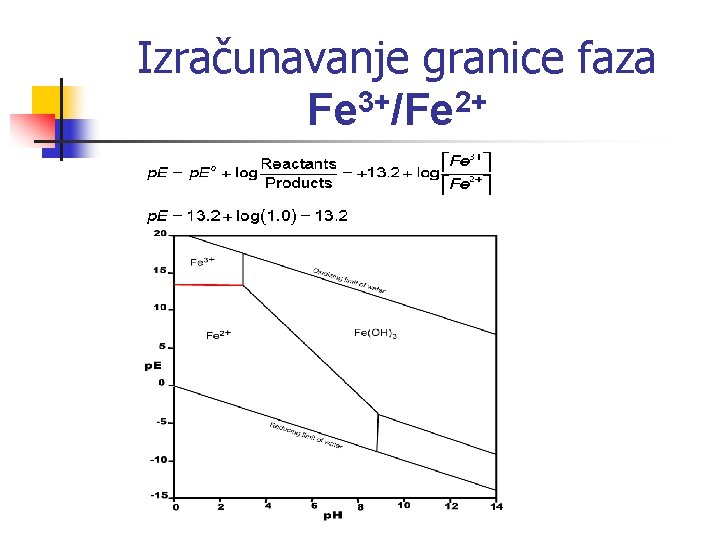
p. E-p. H dijagram za Fe-O 2 -H 2 O n Fe 2+ / Fe 3+ + e- Fe 2+ E 0 = 0. 780 V p. E = ( E 0/ 0. 0591) = 13. 2 V Nernstovom jednadžbom se izražava p. E za vrijednosti aktivnosti i tlaka koji nisu standardni odnosno: Granične koncentracija reaktanata i produkata su jednake Iznad granične vrijednost- stabilniji oksidacijski oblik Ispod granične vrijednosti- stabilniji reducirani oblik

n n n U vodenoj otopini nalaze se ionske vrste: Fe 2+ , Fe 3+ , OH- , H+ Maksimalna konc. (Fe 2+ , Fe 3+ = 10 -5 M) U otopini se nalaze ionske vrste: Fe 2+, Fe 3+ Fe(OH)3 , Fe(OH)2 Kemijske reakcije na granici faza su:

Izračunavanje granice faza 3+ 2+ Fe /Fe

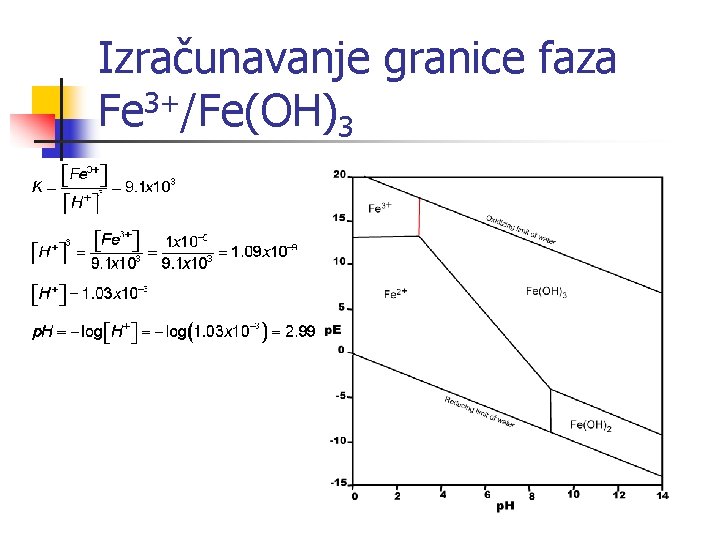
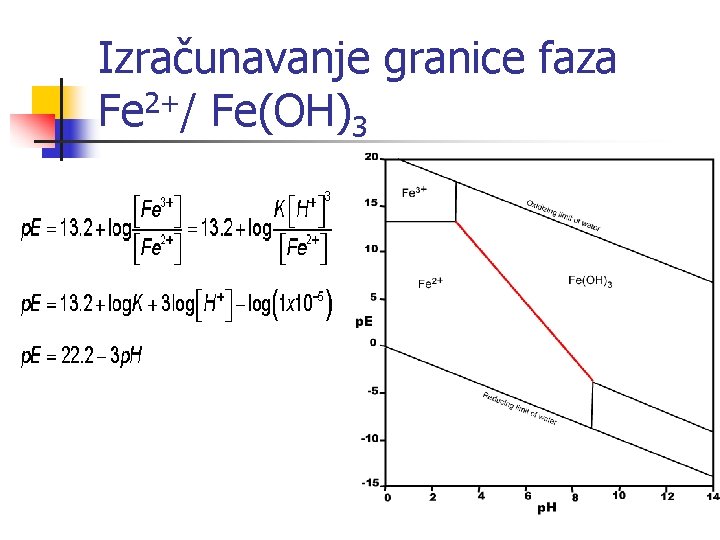
Izračunavanje granice faza Fe 3+/Fe(OH)3

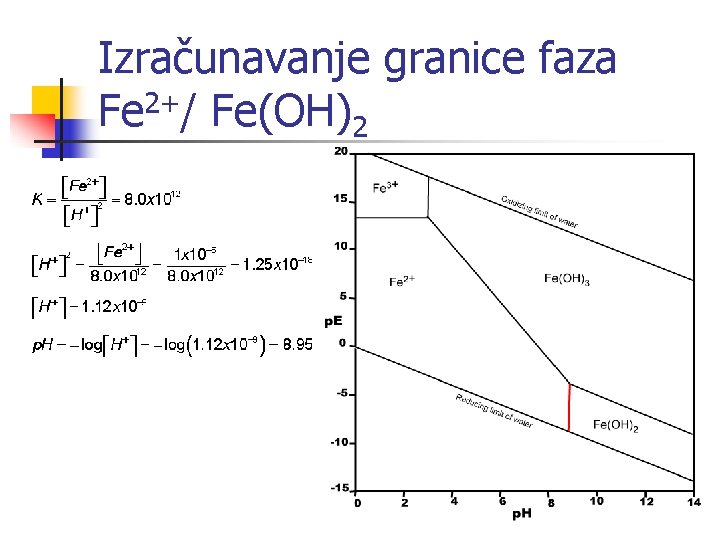
Izračunavanje granice faza Fe 2+/ Fe(OH)2

Izračunavanje granice faza Fe 2+/ Fe(OH)3

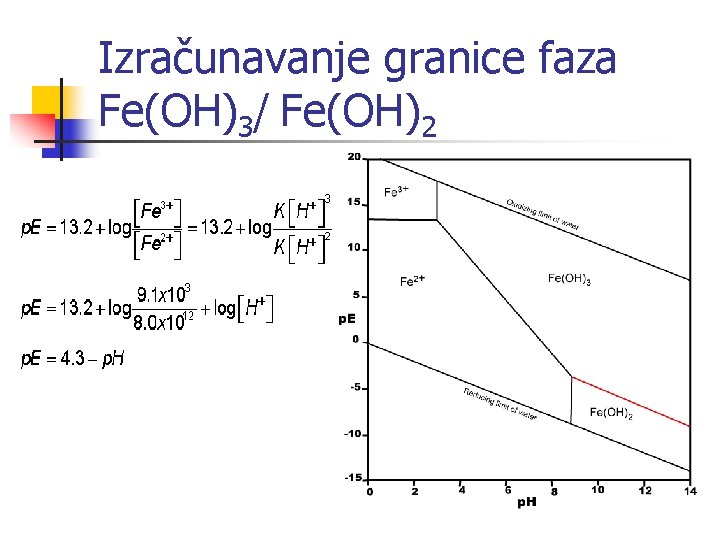
Izračunavanje granice faza Fe(OH)3/ Fe(OH)2

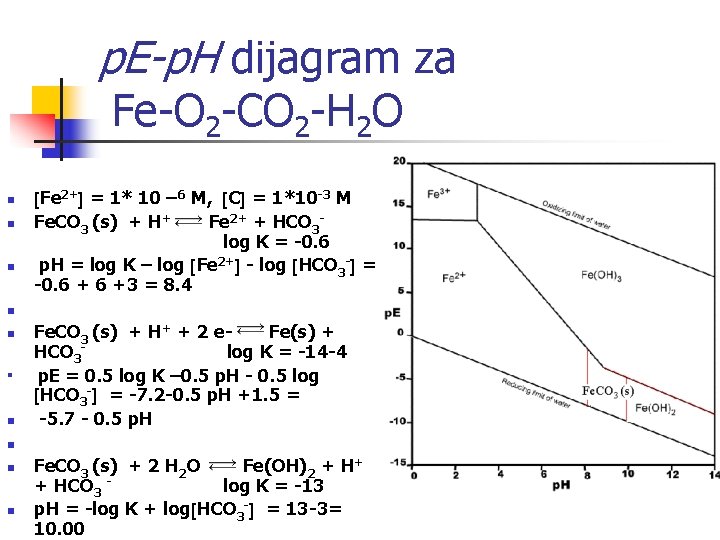
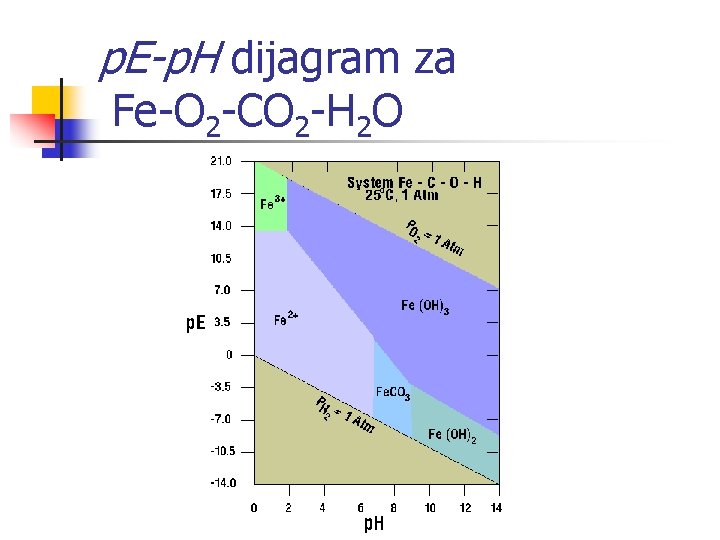
p. E-p. H dijagram za Fe-O 2 -CO 2 -H 2 O n n n Fe 2+ = 1* 10 – 6 M, C = 1*10 -3 M Fe. CO 3 (s) + H+ Fe 2+ + HCO 3 log K = -0. 6 p. H = log K – log Fe 2+ - log HCO 3 - = -0. 6 +3 = 8. 4 n n Fe. CO 3 (s) + H+ + 2 e. Fe(s) + HCO 3 log K = -14 -4 p. E = 0. 5 log K – 0. 5 p. H - 0. 5 log HCO 3 - = -7. 2 -0. 5 p. H +1. 5 = -5. 7 - 0. 5 p. H n n n Fe. CO 3 (s) + 2 H 2 O Fe(OH)2 + H+ + HCO 3 log K = -13 p. H = -log K + log HCO 3 - = 13 -3= 10. 00

p. E-p. H dijagram za Fe-O 2 -CO 2 -H 2 O

Praktična primjena p. E-p. H dijagrama n n n p. E/p. H dijagrami- grafički prikaz termodinamičkih podataka p. E/p. H dijagrami- ne daju informacije o brzini kemijskih reakcija Upućuju – što se može očekivati u prirodnom okolišu Omogučuju- tumačenje mnogih prirodnih fenomena, ali ne mogu odgovoriti na pitanje kako će se brzo te pojave dogoditi Geokemičari koriste p. E/p. H dijagrame za predviđanje vrste nastalih stijena

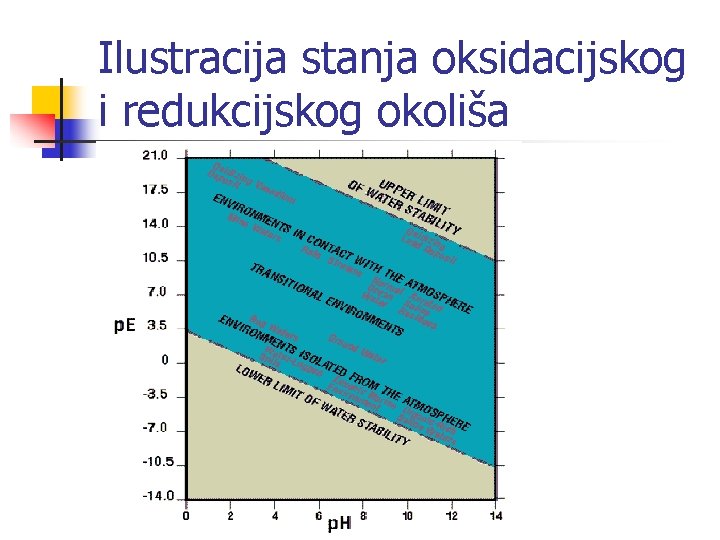
Ilustracija stanja oksidacijskog i redukcijskog okoliša

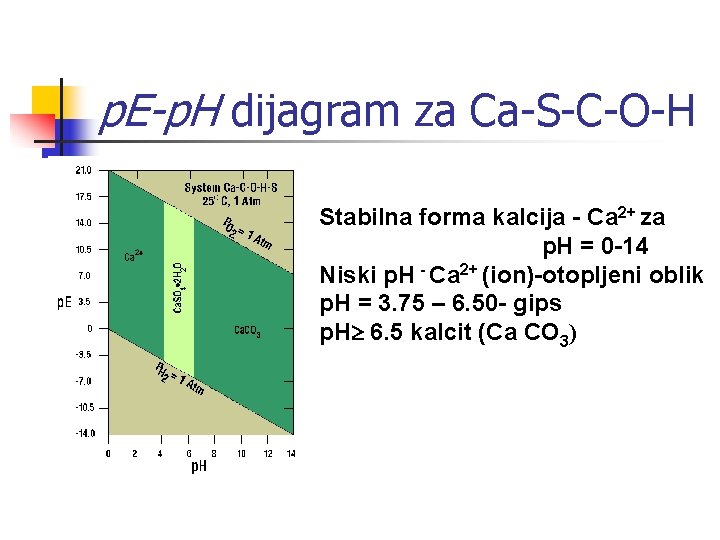
p. E-p. H dijagram za Ca-S-C-O-H Stabilna forma kalcija - Ca 2+ za p. H = 0 -14 Niski p. H - Ca 2+ (ion)-otopljeni oblik p. H = 3. 75 – 6. 50 - gips p. H 6. 5 kalcit (Ca CO 3)

p. E-p. H dijagram za Fe-C-O-H sustav Postoje četiri područja u kojima egzistiraju -Fe 2+, Fe 3+ Fe(OH)3 , Fe(OH)2 -Podzemna voda sadrži veliku količinu Fe(OH)2 -Aeracijom prelazi Fe(OH)2 u Fe(OH)3 –brzo -Precipitacija Fe(OH)3 –neposredno nakon -aeracije -Nastanak Fe. CO 3 (s) smanjuje područje Fe 2+ - iona- važnost karbonata u prirodnim vodama

Standardni redukcijski potencijali i p. E vrijednosti za najčešće rabljene redoks sustave

p. E u vodi i prirodnim vodenim sustavima Primjer: Izračunaj vrijednost p. E jezerske vode pri 10 C ako je p. H = 6. 4 i ako je ta voda u ravnoteži s atmosferskim kisikom pri PO 2 = 0. 21 atm.

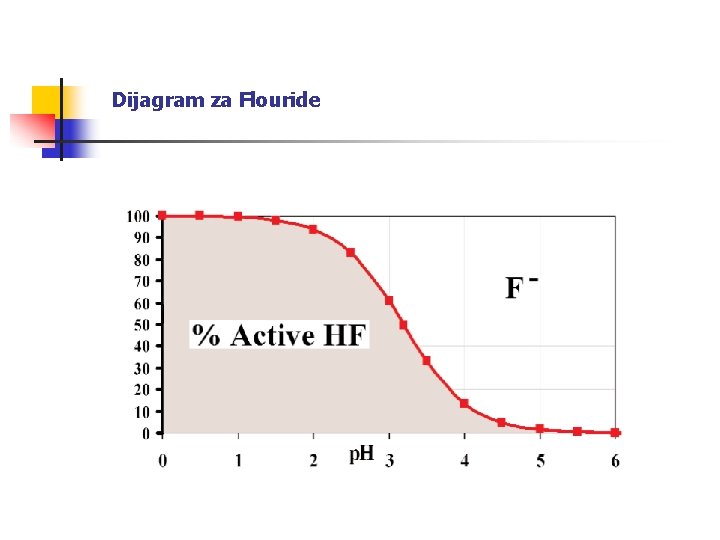
Dijagram za Flouride