Blm 5 Sulu zelti Tepkimelerine Giri Genel Kimya

Bölüm 5: Sulu Çözelti Tepkimelerine Giriş Genel Kimya Prensipler ve Modern Uygulamalar Petrucci • Harwood • Herring 8. Baskı
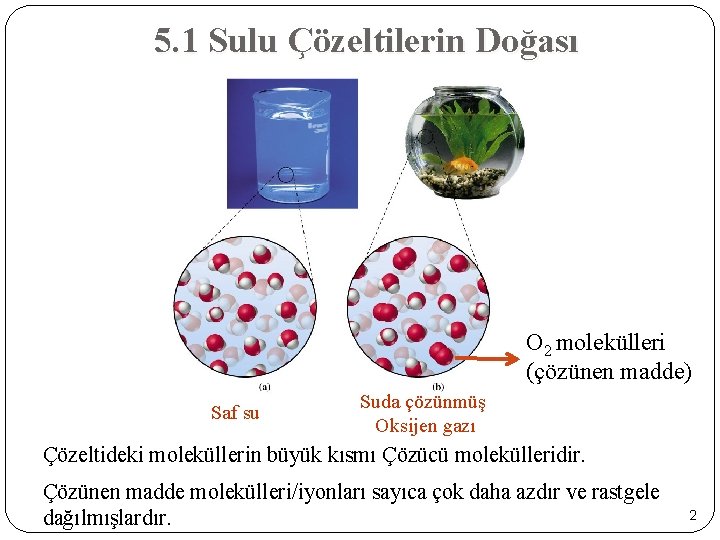
5. 1 Sulu Çözeltilerin Doğası O 2 molekülleri (çözünen madde) Saf su Suda çözünmüş Oksijen gazı Çözeltideki moleküllerin büyük kısmı Çözücü molekülleridir. Çözünen madde molekülleri/iyonları sayıca çok daha azdır ve rastgele dağılmışlardır. 2
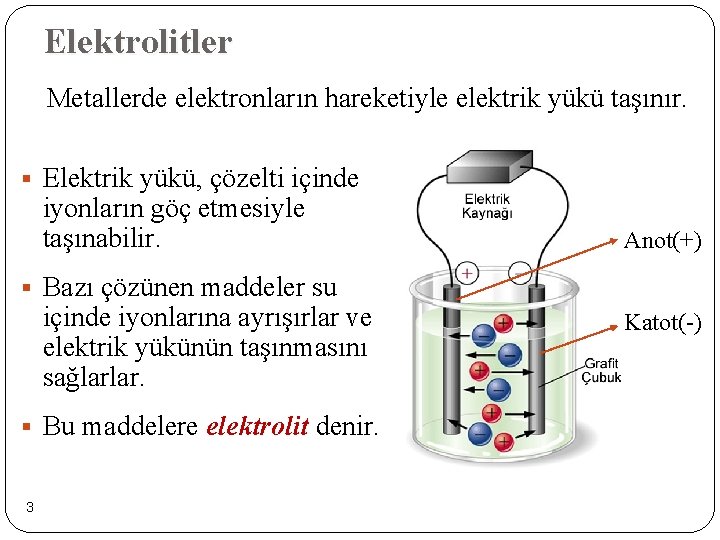
Elektrolitler Metallerde elektronların hareketiyle elektrik yükü taşınır. § Elektrik yükü, çözelti içinde iyonların göç etmesiyle taşınabilir. Anot(+) § Bazı çözünen maddeler su içinde iyonlarına ayrışırlar ve elektrik yükünün taşınmasını sağlarlar. § Bu maddelere elektrolit denir. 3 Katot(-)

Elektrolit Çeşitleri 1. Kuvvetli elektrolit tamamen iyonlarına ayrılır. • Elektriği iyi iletir. • Bütün suda çözünen iyonik bileşikler (ör. Na. Cl) ve bazı moleküler bileşikler (ör. HCl) 2. Zayıf elektrolit kısmen iyonlarına ayrılır. • Elektriği az iletir. 3. Elektrolit olmayan maddeler iyonlarına ayrılmazlar. • Elektriği İletmez. • Çoğu moleküler bileşikler. 4

Bir çözeltinin elektrik iletmesi çözeltinin içerisinde bulunan iyoların miktarına bağlıdır. Elektrolit olmayan Zayıf elektrolit İyon yok, Ampül yanmıyor Birkaç iyon var, ampül az ışıkla yanıyor 5 Güçlü elektrolit Birçok iyon var, Ampül güçlü bir ışıkla yanıyor
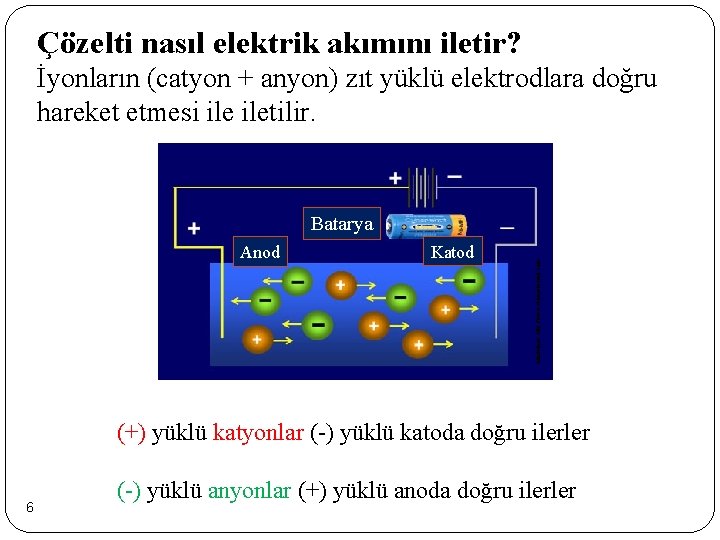
Çözelti nasıl elektrik akımını iletir? İyonların (catyon + anyon) zıt yüklü elektrodlara doğru hareket etmesi iletilir. Anode Katod Cathode Illustration: http: //www. chemistryland. com Batarya (+) yüklü katyonlar (-) yüklü katoda doğru ilerler 6 (-) yüklü anyonlar (+) yüklü anoda doğru ilerler
![Elektrolit Örnekleri 1. Kuvvetli Elektrolit: [% 100 ayrışma] Na. Cl (k) H 2 O Elektrolit Örnekleri 1. Kuvvetli Elektrolit: [% 100 ayrışma] Na. Cl (k) H 2 O](http://slidetodoc.com/presentation_image/1c70fe9df55045493c01fb48f364f59c/image-7.jpg)
Elektrolit Örnekleri 1. Kuvvetli Elektrolit: [% 100 ayrışma] Na. Cl (k) H 2 O Mg. Cl 2(k) Na+ (suda) + Cl- (suda) Mg 2+ (suda) + 2 Cl- (suda) Derişimin (Konsantrasyon) İfadesi: Mg. Cl 2(k) 0, 0050 M Mg. Cl 2 Mg 2+ (suda) + 2 Cl- (suda) 0, 0050 M 0, 0100 M (2 x 0, 0050) Stokiyometri: 7 [Mg 2+] = 0, 0050 M [Cl-] = 0, 0100 M [Mg. Cl 2] = 0 M
![2. Zayıf Elektrolit: [tam ayrışma olmaz] → CH 3 COO- (suda) + H+ (suda) 2. Zayıf Elektrolit: [tam ayrışma olmaz] → CH 3 COO- (suda) + H+ (suda)](http://slidetodoc.com/presentation_image/1c70fe9df55045493c01fb48f364f59c/image-8.jpg)
2. Zayıf Elektrolit: [tam ayrışma olmaz] → CH 3 COO- (suda) + H+ (suda) CH 3 CO 2 H (suda) ← 0, 1 mol 0, 0013 mol Sadece 0, 1 mol asetik asidin %1. 13’ü CH 3 COO- ve H+ iyonlarına ayrışır. 3. Elektrolit olmayan: [ayrışma yok; iyon yok] C 6 H 12 O 6 (k) H 2 O C 6 H 12 O 6 (suda) Moleküler bileşikler iyonlarına ayrışmazlar. 8 Diğer ör. CH 3 OH (suda), C 2 H 5 OH (suda)

Örnek 5 -1 Kuvvetli Elektrolit Çözeltilerinde İyon Konsantrasyonunun Hesaplanması. 0. 0165 M Al 2(SO 4)3 çözeltisi içindeki aluminyum ve sülfat iyonu konsantrasyonu nedir? Al 2(SO 4)3 (k) → 2 Al 3+(suda) + 9 3 SO 42 -(suda)
![Çözüm: Aluminyum konsantrasyonu: 0. 0165 mol Al 2(SO 4)3 2 mol Al 3+ [Al] Çözüm: Aluminyum konsantrasyonu: 0. 0165 mol Al 2(SO 4)3 2 mol Al 3+ [Al]](http://slidetodoc.com/presentation_image/1c70fe9df55045493c01fb48f364f59c/image-10.jpg)
Çözüm: Aluminyum konsantrasyonu: 0. 0165 mol Al 2(SO 4)3 2 mol Al 3+ [Al] = × 1 L 1 mol Al 2(SO 4)3 = 0. 0330 M Al 3+ Sülfat konsantrasyonu : [SO 4 10 2 -] 0. 0165 mol Al 2(SO 4)3 3 mol SO 42= × = 0. 0495 M SO 421 L 1 mol Al 2(SO 4)3

5 -2 Çökelme Tepkimeleri Bazı bileşikler suda çözünmezler. Çözünen iyonlar birleşerek suda çözünmeyen bileşikleri oluşturablirler. Çökelme olur. Ör: Pb. I 2 Ag+ (suda) + Cl- (suda) → Ag. Cl (k) Pb(NO 3)2 (suda) + 2 Na. I (suda) 11 Pb. I 2 (k) + 2 Na. NO 3 (suda) Videosunu izleyin: https: //youtu. be/2 EQzn. GPZY 5 A

Net İyonik Eşitlik Bütüncül Eşitlik: Ag. NO 3 (suda) + Na. I (suda)c → Ag. I (k) + Na. NO 3 (suda) İyonik Eşitlik: Ag+ (suda) + NO 3 - (suda) + Na+c(suda) + I- (suda) → Ag. I (k) + Na+ (suda) + NO 3 - (suda) Net iyonik eşitlik: Ag+ (suda) + c I- (suda) → Ag. I (k) Gözlemci iyonlar eşitlikten çıkarılınca net iyonik eşitlik sağlanır. 12 Gözlemci iyonlar: Na+ ve NO 3 -
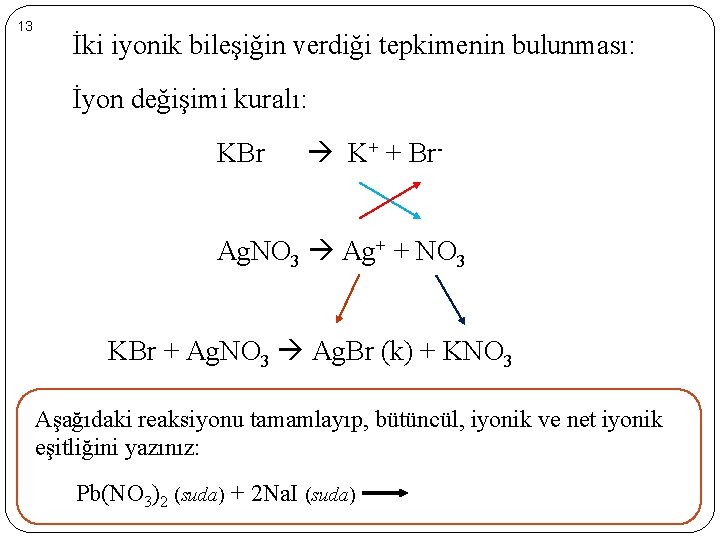
13 İki iyonik bileşiğin verdiği tepkimenin bulunması: İyon değişimi kuralı: KBr K+ + Br- Ag. NO 3 Ag+ + NO 3 KBr + Ag. NO 3 Ag. Br (k) + KNO 3 Aşağıdaki reaksiyonu tamamlayıp, bütüncül, iyonik ve net iyonik eşitliğini yazınız: Pb(NO 3)2 (suda) + 2 Na. I (suda)

Çözünürlük Kuralları Çözünürlük, belirli bir sıcaklıkta belirli bir miktarda çözücü içinde çözünecek olan en fazla çözünen miktarıdır. Bütün iyonik bileşikler güçlü elektrolitlerdir, ancak eşit oranda çözünmezler. Çözünen Bileşikler: • Alkali metal (Grup 1 A) ve amonyum bileşikleri Li+, Na+, K+, Rb+, Cs+ NH 4+ • Nitratlar, perkloratlar ve asetatlar NO 314 Cl. O 4 - CH 3 CO 2 - C 2 H 3 O 2 - CH 3 COO-

r e b e m e l z E 15 n i y

Çözünmeyen Bileşik Örnekleri Cd. S 16 Pb. S Ni(OH)2 Al(OH)3

Asitler Ör: HCl (suda), H 2 SO 4 (suda) CH 3 COOH (asetik asit) (kuvvetli asit) (zayıf asit) Asitlerin özellikleri: 1. Ekşi tat; Sirkenin tadı; asetik asit. Naranciye meyveler sitrik asit içerir. 2. Renk değişimine sebep olur. Ör. Asitler litmus kağıdının rengini maviden kırmızıya çevirir. 17 Bir parça tebeşir (çoğunlukla Ca. CO 3) HCl (suda) ile tepkimeye girer ve CO 2 gazı üretir.

Kuvvetli Asit Örnekleri: Kuvvetli asitler suda tamamen ayrışır: Ör: HCl (suda) �H+ (suda) + Cl- (suda) (Tüm HCl, H+ and Cl- iyonlarına yrışır. ) Zayıf asitler suda kısmen ayrışır: Zayıf Asitler: 18 Ör: HNO 2 kısmen H+ ve NO 2 - iyonlarına ayrışır. HNO 2 (suda) H+ (suda) + NO 2 - (suda) CH 3 COOH H+ + CH 3 CO 2 -

Asitler belli başlı metaller ile tepkimeye girip hidrojen gazı üretir: 2 HCl (suda) + Mg (k) Mg. Cl 2 (suda) + H 2 (g) Videyoyu izleryin: https: //youtu. be/cpy_Zh-8 s. KA Asitler carbonatlar ve bicarbonatlar ile tepkimeye girip karbondioksit ve su molekülleri üretir: 2 HCl (aq) + Ca. CO 3 (k) Ca. Cl 2 (aq) + CO 2 (g) + H 2 O (s) Sulu asit çözeltileri elektrik iletkenleridir. 19

Bazlar Ör: Na. OH (Kuvvetli baz) Na. OH (suda) → Na+ (suda) + OH- (suda) H 2 O NH 3 (Zayıf base) - (suda) + NH + (suda) NH 3 (suda) + H 2 O (s) ← OH 4 → Bazların özellikleri: Acı tat. Renk değişimine neden olur. Bazlar litmus kağıdının rengini kırmızıdan maviye çevirir. Sulu baz çözeltileri elektrik iletkenleridir. 20
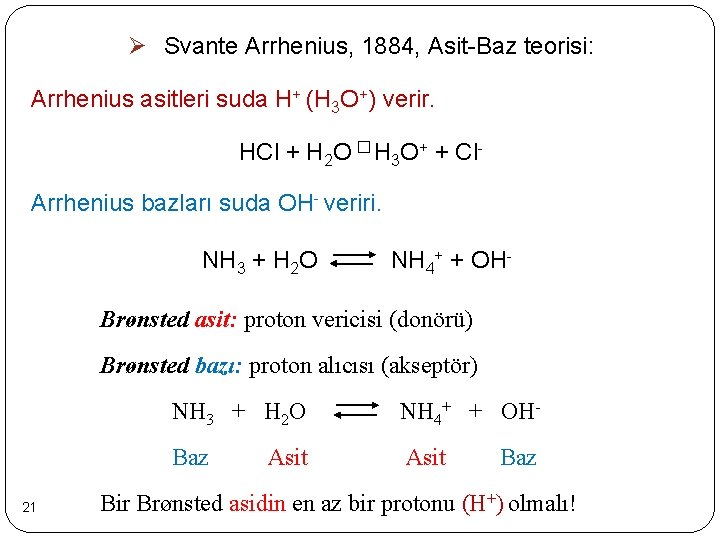
Ø Svante Arrhenius, 1884, Asit-Baz teorisi: Arrhenius asitleri suda H+ (H 3 O+) verir. HCl + H 2 O � H 3 O+ + Cl. Arrhenius bazları suda OH- veriri. NH 3 + H 2 O NH 4+ + OH- Brønsted asit: proton vericisi (donörü) Brønsted bazı: proton alıcısı (akseptör) 21 NH 3 + H 2 O NH 4+ + OH- Baz Asit Baz Bir Brønsted asidin en az bir protonu (H+) olmalı!
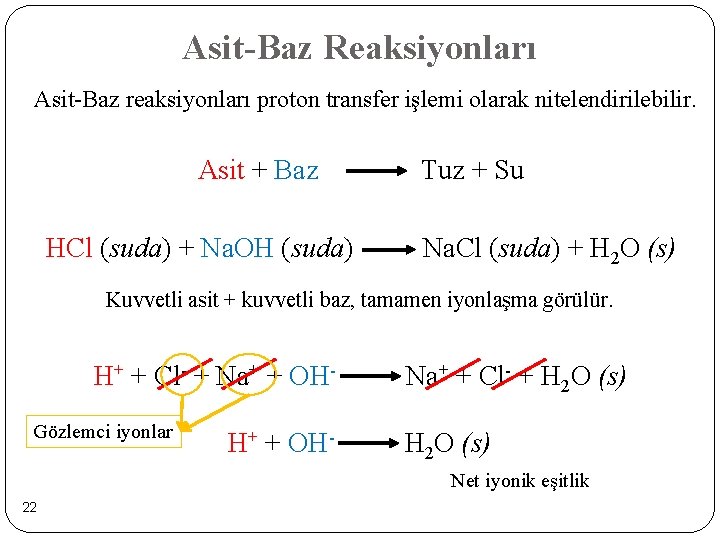
Asit-Baz Reaksiyonları Asit-Baz reaksiyonları proton transfer işlemi olarak nitelendirilebilir. Asit + Baz HCl (suda) + Na. OH (suda) Tuz + Su Na. Cl (suda) + H 2 O (s) Kuvvetli asit + kuvvetli baz, tamamen iyonlaşma görülür. H+ + Cl- + Na+ + OHGözlemci iyonlar H+ + OH- Na+ + Cl- + H 2 O (s) Net iyonik eşitlik 22

Asit-Baz Reaksiyonları - Örnek Aşağıdaki asit-baz reaksiyonunu için moleküler, iyonik ve net iyonik eşitlikleri yazın: Ø Hidrobromik asit (aq) + Baryum hidroksit (aq) Çözüm: Moleküler eşitlik: 2 HBr (aq) + Ba(OH)2 (aq) 23 Ba. Br 2(aq) + 2 H 2 O(s)

2 HBr (aq) + Ba(OH)2 (aq) Ba. Br 2(aq) + 2 H 2 O(s) Iyonik eşitlik: 2 H+(aq) + 2 Br−(aq) + Ba 2+(aq) + 2 OH−(aq) Ba 2+(aq) + 2 Br−(aq) + 2 H 2 O(s) Net iyonik eşitlik: 2 H+(aq) + 2 OH−(aq) veya H+(aq) + OH−(aq) 24 2 H 2 O(s) Ba 2+ ve Br− gözlemci iyonlardır.

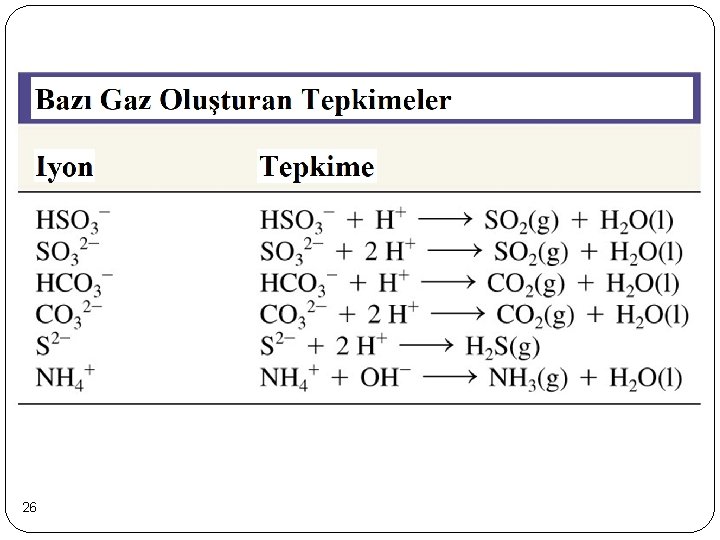
Asit-Baz Reaksiyonları - Örnek Mg(OH)2 (k) + 2 H+ (suda) → Mg 2+ (suda) + 2 H 2 O (s) c → Mg(OH)2 (k) + 2 CH 3 CO 2 H (suda) Mg 2+ (suda) + 2 CH 3 CO 2 - (suda) + 2 H 2 O (s) Ca. CO 3 (k) + 2 H+ (suda) → Ca 2+ (suda) + H 2 CO 3 (suda) Fakat: H 2 CO 3 (suda)c → H 2 O (s) + CO 2 (g) Ca. CO 3 (k) + 2 H+ (suda) → Ca 2+ (suda) + H 2 O (s) + CO 2 (g) 25
26

5 -4 Yükseltgenme-İndirgenme (Redoks Tepkimeler) Bu tip tepkimeler elektron transferi reaksiyonlarıdır. Yükseltgenme ve İndirgenme tepkimeleri mutlaka aynı anda olur. Yükseltgenme (oksidasyon): elektron kaybıyla yük daha (+) olur. İndirgenme (redüksiyon): elektron kazancıyla yük daha (-) olur. Ör. Hematit yüksek fırında ısıtılarak aşağıdaki gibi Demir metaline dönüştürülür. D Fe 2 O 3 (s) + 3 CO (g) → 2 Fe (l) + 3 CO 2 (g) Fe 3+ iyonu metalik demire (Fe 0) indirgenmiştir. 27 CO(g) molekülü CO 2 ye yükseltgenmiştir. 27

Yükseltgenme Basamağı Değişimleri Yükseltgenme basamaklarını (Y. B. ) göster: 3+ 2 - 2+ 2 - D 0 4+ 2 - Fe 2 O 3(k) + 3 CO(g) → 2 Fe(k) + 3 CO 2(g) Fe 3+ demir metaline indirgenir. CO(g) karbondioksite yükseltgenir. 28

Yükseltgenme ve İndirgenme Yükseltgenme Tepkime sırasında yükseltgenen elementin Y. B. ı artar. Elektronlar eşitliğin sağında yer alır. Ör. Ca → Ca 2+ + 2 e. Fe 2+ ➝ Fe 3+ + 1 eİndirgenme Tepkime sırasında indirgenen elementin Y. B. ı azalır. Elektronlar eşitliğin solunda yer alır Ör. O + 2 e- → O 2 Cl + 1 e- ➝ Cl 29

Yükseltgenler ve İndirgenler Yükseltgen (oksidant): Redoks tepkimesi sırasında bileşimindeki elementlerinden birinin Y. B. ı azalır (indirgenir). Başka bir maddeyi yükseltgeyen maddeye denir. Yükseltgenin kendisi indirgenir. İndirgen: Redoks tepkimesi sırasında bileşimindeki elementlerinden birinin Y. B. ı artar (yükseltgenir). Başka bir maddeyi indirgeyen maddeye denir. İndirgenin kendisi yükseltgenir.

Redoks Tepkimleri ve Yarı Tepkimeler Örnek: Bakır Sülfat Çözeltisinde Çinko 31 Zn (k) + Cu 2+ (suda) → Zn 2+ (suda) + Cu (k)

Zn (k) + Cu 2+ (suda) → Zn 2+ (suda) + Cu (k) Reaksiyonu yarı tepkimeler halinde gösterin. Yükseltgenme: Cu 2+ (aq) + 2 e- → Cu (k) İndirgenme: Net: 32 Zn (k) → Zn 2+ (suda) + 2 e- Cu 2+ (suda) + Zn (k) → Cu (k) + Zn 2+ (suda) Zn yükseltgendi. Cu 2+ indirgendi. Zn indirgeyici ajandır. (indirgen) Cu 2+ yükseltgeyici ajandır. (yükseltgen)

Örnek: Magnezyum ve oksijenin tepkimesi 2 Mg + O 2 Yükseltgenme yarı-tepkimesi (e- kaybı) : 2 Mg. O 2 Mg İndirgenme yarı-tepkimesi (e- kazancı): O 2 + 4 e. Tepkime: 2 Mg + O 2 + 4 e 2 Mg + O 2 33 2 Mg 2+ + 2 O 2 - 2 Mg 2+ + 4 e 2 O 2 - 2 Mg 2+ + 2 O 2 - + 4 e 2 Mg 2+ + 2 O 22 Mg. O

Redoks: Eşitliklerinin Denkleştirilmesi Ancak bazı tepkimeler inceleme yoluyla denkleştirilebilir. Tepkimelerin denkleştirilebilmesi için sistematik yöntemler: 34 1. Yarı Tepkime (İyon-Elektron) Metodu 2. Yükseltgenme Basamağı Metodu

Yükseltgenme Basamağı Metodu 1. Tepkime eşitliğinde görülen bütün elementlerin Y. B. ları yazın. 2. Yükseltgenen ve indirgenen elementleri belirleyin (Eşitliğin iki yanındaki indirgenen ve yükseltgenen bileşikleri birer çizgi ile birleştirerek Y. B. ındaki değişiklikleri gösterin). 3. Yükseltgenenler tarafından kaybedilen ve indirgenenler tarafından alınan elektronların sayıları hesaplayın. 4. Bu elektron sayılarını, alınan ve kaybedilen elektron sayılarını eşitlemek için katsayılarla çarpın. (Kendileriyle çarpıldığında alınan elektronların sayısı ile kaybedilen elektronların sayılarını eşitleyecek katsayıları belirleyin). 5. Bu katsayıları denkleştirme katsayıları olarak kullanın. 6. Eşitliği inceleyerek kalan elementleri denkleştirin. 35

Asidik Çözeltide Denkleştirme 1. Yarı tepkime eşitliklerini yazın. • H ve O dışındaki atomları denkleştirin. • Oksijenleri H 2 O kullanarak denkleştirin. • Hidrojenleri H+ kullanarak denkleştirin. • Yükleri e- kullanarak denkleştirin. 2. Yarı tepkimelerin elektron sayılarını denkleştirin. 3. Yarı tepkimeleri toplayın. 4. Denkliği kontrol edin. 36

ÖRNEK Asidik Çözeltide bir indirgenme-yükseltgenme eşitliğinin denkletirilmesi. Aşağıdaki eşitliği asidik çözeltide denkleştirin. . SO 32 - (suda) + Mn. O 4 - (suda) → SO 42 - (suda) + Mn 2+ (suda) 1. Y. B. larını belirleyin: 4+ 6+ 7+ 2+ SO 32 - (suda) + Mn. O 4 - (suda) → SO 42 - (suda) + Mn 2+ (suda) 2. Yarı tepkimeleri yazın: SO 32 - (suda) → SO 42 - (suda) + 2 e- (suda) 37 5 e- (suda) + Mn. O 4 - (suda) → Mn 2+ (suda)

Çözüm devamı: 3. H ve O dışındaki atomları denkleştirin: Diğer elementler burada zaten denkleşmiş halde. 4. Oksijenleri H 2 O ekleyerek denkleştirin: H 2 O (s) + SO 32 - (suda) → SO 42 - (suda) + 2 e- (suda) 5 e- (suda) + Mn. O 4 - (suda) → Mn 2+ (suda) + 4 H 2 O (s) 5. Hidrojeni H+ ekleyerek denkleştirin: H 2 O (s) + SO 32 - (suda) → SO 42 - (suda) + 2 e- (suda) + 2 H+ (suda) 8 H+ (suda) + 5 e- (suda) + Mn. O 4 - (suda) → Mn 2+ (suda) + 4 H 2 O (s) 38

6. Yüklerin denkleşip denkleşmediğini kontrol edin: Gerekirse yükleri denkleştirmek için e- ekleyin. 7. Yarı tepkimeleri e- ları eşitlemek için katsayılarla çarpın : 5 H 2 O (s) + 5 SO 32 - (suda) → 5 SO 42 - (suda) + 10 e- (suda) + 10 H+ (suda) 16 H+ (suda) + 10 e- (suda) + 2 Mn. O 4 - (suda) → 2 Mn 2+ (suda) + 8 H 2 O (s) 8. Yarı tepkimeleri toplayın ve sadeleştirin: 5 SO 32 - (suda) + 2 Mn. O 4 - (suda) + 6 H+ (suda) → 5 SO 42 - (suda) + 2 Mn 2+ (suda) + 3 H 2 O (s) Denkliği kontrol edin! 39

Bazik Çözeltide Denkleştirme 1. H+ in yerini OH- alır. 2. Denkleştirmeyi asidik çözeltideki gibi yapın. • Sonra H+ iyonlarını nötralize etmek için her iki tarafa da H+ iyonlarını ile aynı sayıda OH- ekleyin. • Tepkimenin her iki tarafında da oluşan H 2 O ları sadeleştirin. (H+ ve OH- birleşmesinden H 2 O oluşur) 3. Denkliği kontrol edin. 40

Redoks Tepkimeleri 41

Kuvvetli Yükseltgenler: • Mn. O 4 - (Asidik çözeltide) Mn+2 + H 2 O • Mn. O 2 (Asidik çözeltide) Mn+2 + H 2 O • Mn. O 4 - (Bazik veya nötür çözeltide) Mn. O 2 • Cr 2 O 72 - (Asidik çözeltide) Cr+3 + H 2 O • Cr 2 O 72 - (Bazik çözeltide) Cr. O 42 - + H 2 O • Cr. O 42 - (Bazik çözeltide) Cr. O 22 - + H 2 O • HNO 3 (Konsantre) NO 2 + H 2 O • HNO 3 (Seyreltik) NO + H 2 O • H 2 SO 4 (Sıcak, konsantre) SO 2 + H 2 O • Serbest Halojenler (Cl 2 vb. ) Cl • H 2 O 2 (Asidik çözeltide) H 2 O • H 2 O 2 (Bozulma) O 2 + H 2 O • Na 2 O 2 (Asidik çözeltide) Na. OH 42 • HCl. O 4 Cl- + H 2 O

Kuvvetli İndirgenler: • Cl- Cl 2 • SO 3 -2 , SO 2 , NO 2 - SO 42 - , NO 3 - vs. • Serbest Halojenler (Cl 2 vb. ) (seyreltik bazik çözelti) Cl. O • Serbest Halojenler (Cl 2 vb. ) (konsantre bazik çözelti) Cl. O 3 • S 2 O 32 - S 4 O 62 - 43

Örnek: Yükseltgen ve İndirgenin Belirlenmesi. Hidrojen peroksit, H 2 O 2, çok yönlü bir bileşiktir. Kullanıldığı alanlardan bazıları, odun hamuru ve tekstil maddelerinin beyazlatılması ve su arıtımında klor yerine kullanılmasıdır. a. Aşağıdaki tepkimelerde hidrojen peroksit in indirgen mi yoksa yükseltgen mi olduğunu belirleyiniz. b. Yarı-tepkimelerini yazınız. 44

-1 +2 -2 +3 a. H 2 O 2 (suda) + 2 Fe 2+ (suda) + 2 H+ → 2 H 2 O (s) + 2 Fe 3+ (suda) Demir yükseltgenmiştir ve peroksit indirgenmiştir. Peroksit bir yükseltgendir. -1 +7 b. 5 H 2 O 2 (suda) + 2 Mn. O 4 - (aq) + 6 H+ → +2 0 8 H 2 O (s) + 2 Mn 2+ (suda) + 5 O 2 (g) Mangan indirgenmiş ve peroksit yükseltgenmiştir. Peroksit bir indirgendir. 45

5 -7 Sulu Çözelti Tepkimelerinin Stokiyometrisi: Titrasyonlar. Titrasyonda, iki solüsyon arasındaki kimyasal reaksiyon tamamlanıncaya kadar, bilinmeyen konsantrasyondaki bir solüsyona damla bir konsantrasyon çözeltisi ilave edilir. Eşdeğerlik Noktası: Her iki tepkenin de tamamıyla tükendiği nokta. İndikatör: Eşdeğerlik noktasında veya buna çok yakın bir noktada renk değiştiren madde. Gösterge renk değiştirene kadar yavaşça bilinmeyen asite bazı ekleyin. 46

İndikatör renk değişimi 47

Örnek Redoks Titrasyonu Bir titrasyon deneyinde, bir öğrenci, 0, 5468 g KHP'yi nötralize etmek için 23, 48 m. L Na. OH çözeltisinin gerekli olduğunu tespit eder. Na. OH çözeltisinin konsantrasyonu (molaritesinde) nedir? KHP + Na. OH 1 mol KHP 48 → KNa. H + H 2 O 1 mol Na. OH
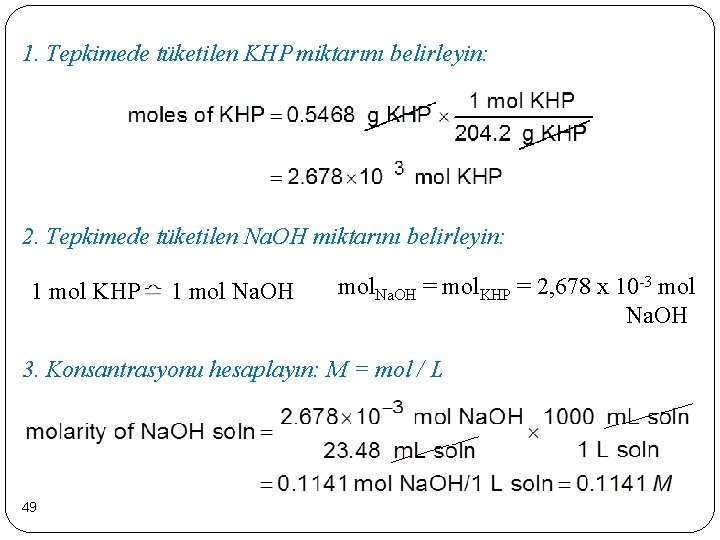
1. Tepkimede tüketilen KHP miktarını belirleyin: 2. Tepkimede tüketilen Na. OH miktarını belirleyin: 1 mol KHP 1 mol Na. OH mol. Na. OH = mol. KHP = 2, 678 x 10 -3 mol Na. OH 3. Konsantrasyonu hesaplayın: M = mol / L 49

Örnek Redoks Titrasyonu 0, 1568 g demir tel, Fe 2+ (aq) iyonuna çevrildikten sonra 26, 42 m. L KMn. O 4(aq) çözeltisi ile titre edilmiştir. KMn. O 4(aq) çözeltisinin Molaritesi nedir? 5 Fe 2+ (suda) + Mn. O 4 - (suda) + 8 H+ (suda) → 4 H 2 O(s) + 5 Fe 3+(suda) + Mn 2+(suda) 1. Kütle. Fe 50 mol. Fe 2. mol. KMn. O mol. Fe 2+ 4 mol. Mn. O Molarite. KMn. O 4 4 - mol. KMn. O 4

5 Fe 2+(aq) + Mn. O 4 -(aq) + 8 H+(aq)→ 4 H 2 O(s) + 5 Fe 3+(aq) + Mn 2+(aq) 1. Tepkimede tüketilen KMn. O 4 miktarını belirleyin: 2. Konsantrasyonu hesaplayın: M = mol / L 51

Alıştırma Sorusu: 18, 64 m. L 0, 1004 M Na. OH çözeltisini nötralize etmek için kaç gram HCl gerekir? Cvp: 0, 0683 g 52 Na. OH + HCl → Na. Cl + H 2 O

Alıştırma Sorusu 2: 10, 1 m. L H 2 SO 4 çözeltisini nötrleştirmek için 60, 2 m. L 0, 427 M KOH çözeltisi gerekirse, H 2 SO 4 çözeltisinin molaritesi nedir? Cvp: 1, 272 M 2 KOH + H 2 SO 4 → K 2 SO 4 + 2 H 2 O 53

Alıştırma Sorusu 3: Standardize edilmiş sodyum hidroksit çözeltisi, 25, 00 m. L bir sülfürik asit çözeltisinin titre edilmesi için kullanılır. Titrasyon, asidi tamamen nötralize etmek için 43, 79 m. L 0, 1172 M Na. OH çözeltisi gerektirir. Cvp = 0, 1026 M H SO H 2 SO 4 çözeltisinin konsantrasyonu nedir? 2 54 4
- Slides: 54