ELEKTROKMYA 1 NTENN KONU BALIKLARI Pilin yks Aktiflik

ELEKTROKİMYA 1

ÜNİTENİN KONU BAŞLIKLARI Pilin öyküsü Aktiflik Standart Elektrot Potansiyelleri Elektrokimyasal Hücreler 2

Luig GALVANİ (Biyolog) 1780 ‘de ölü kurbağalar üzerinde çalışma yaptı Daha sonra yaşadıklarını fizikçi VOLTA ile paylaştı. Volta bu olayın potansiyel farkından kaynaklandığını açıkladı Cu ve Ag levhalar arasına tuzlu suyla ıslatılmış kartonlar koyarak ilk Volta Pilini elde etti. 3

J. F DANİEL’in Çalışması Volta’nın yaptığı pil düzeneğini farklı kaplarda iki farklı yarı hücre oluşturarak elektrik enerjisi elde etti. Cu(SO 4)2 çözeltisine daldırılmış Cu içeren bir kap ve Zn(SO 4)2 çözeltisine daldırılmış Zn içeren başka bir kap tuz köprüsüyle birbirine bağlanarak oluşurmuştur. 4

Not: Galvani veya Daniel hücrelerinde pil kendiliğinden çalışır. Diğer bir ifadeyle, farklı standart elektrotlar ile hazırlanan bütün elektrokimyasal hücrelerde tepkime kendiliğinden gerçekleşir. Yani istemlidir, bu hücreler elektrik enerjisi üretir. Kendiliğinden istemli olmayan redoks tepkimelerinin bir dış elektrik enerjisi kaynağı zorlaması ile gerçekleşen düzeneklere Elektrolitik hücre denir. 5

Elektrokimyasal Hücre Elektrik enerjisini kimyasal enerjiye dönüştüren yada kimyasal enerjiyi elektrik enerjisine dönüştüren düzeneklere Elektrokimyasal Hücre denir. Elektrot: Çözeltiye daldırılmış iletken Elektrolit: İletken çözelti Tuz Köprüsü: Elektrokimyasal hücrede yük denkliğini sağlayan derişik çözelti 6

Standart İndirgenme Yarı Potansiyellerin Yorumu Tepkimeler çift yönlüdür, tepkime ters çevrildiğinde işaret değişir ∆H, ∆G, ∆S ve Kç gibi madde miktarından bağımsız olduğundan katsayısı değişen tepkimenin E° değeri değişmez. Tepkimeler tarafa toplanırken tepkimelerin potansiyelleri de toplanır. 7

Bir redoks tepkimesinde yükseltgenme ve indirgenme yarı tepkimelerinin standart potansiyelleri toplamı yani hücre potansiyeli pozitif (E°Hücre > 0) ise bu tepkime istemlidir. 2 Al(k) → 2 Al+3 + 6 e 3 Cu+2 + 6 e- → 3 Cu(k) E°= + 1. 662 V E°= + 0. 337 V 2 Al(k) + 3 Cu+2 → 2 Al+3 + 3 Cu(k) E°Hücre = + 1. 999 V tepkimesi için E°Hücre = + 1. 999 V > 0 olduğu için istemlidir. 8

İstemli redoks tepkimelerinden hücre potansiyeli büyük olan tepkime daha çok istemlidir. 2 Al(k) + 3 Cu+2 → 2 Al+3 + 3 Cu(k) E°Hücre = + 1. 999 V Cr(k) + Pb+2 → Cr+2 + Pb(k) E°Hücre = + 0. 282 V istemli olan birinci tepkimenin potansiyeli daha büyük olduğundan daha istemlidir. 9

Bir redoks tepkimesinde yükseltgenme ve indirgenme yarı tepkimelerinin standart potansiyelleri toplamı yani hücre potansiyeli negatif (E°Hücre ∠ 0) ise bu tepkime istemsizdir. 2 Ag(k) → 2 Ag+2 + 2 e Fe+2 + 2 e- → 2 Fe(k) E°= - 0. 799 V E°= - 0. 440 V 2 Ag(k) + 2 Fe+2 → 2 Ag+2 + 2 Fe(k) E°Hücre = - 1. 239 V tepkimesi için E°Hücre = - 1. 999 V ∠ 0 olduğu için istemsizdir 10

Standart Potansiyeller Kullanarak Galvanik Pilin Standart Hücre Potansiyelinin Belirlenmesi İndirgenme potansiyelleri arasındaki farktır. E°Hücre = E°Katot - E°Anot Veya yükseltgenme ve indirgenme yarı tepkimelerinin standart potansiyelleri toplamıdır E°Hücre = E°Yükseltgenme + E°İndirgenme 11
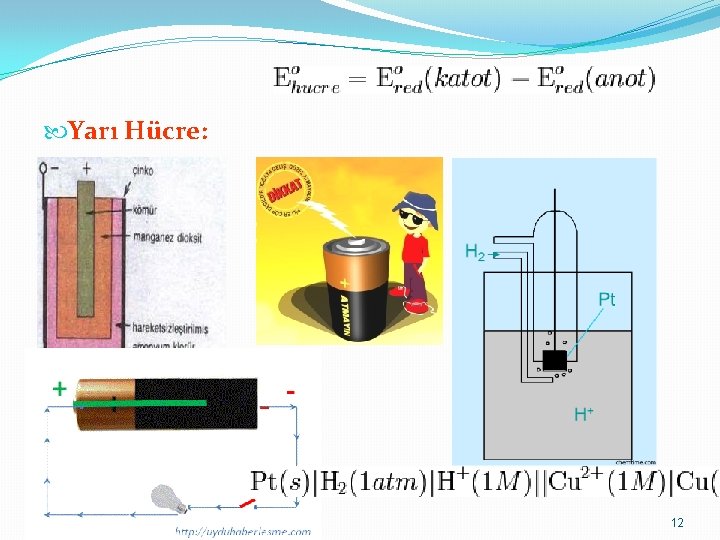
Yarı Hücre: 12
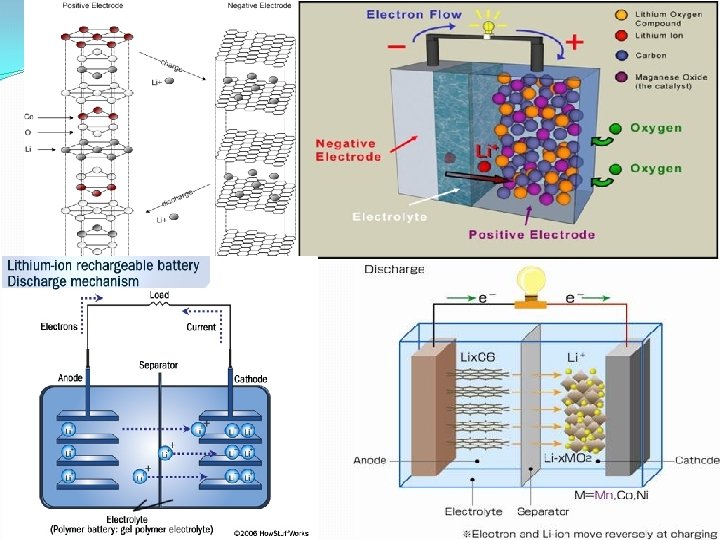
13

2. STANDART ELEKTROT POTANSİYELLERİ AKTİFLİK Elementlerin bileşik oluşturabilme kabiliyetlerine aktiflik denir. Kimyasal reaksiyonlarda, elektron veren element yükseltgenirken, elektron alan element indirgenir. Elektron veren (yükseltgenen) elemente indirgen, Elektron alan (indirgenen) elemente yükseltgen denir. 14

İletkenlik Birinci dereceden iletkenler: metallerdir ve serbest elektronlar sayesinde gerçekleşir. Ag, Cu, Pt iyi iletir. İkinci dereceden iletkenler: Suda çözündüğünde serbestçe hareket edebilen iyonlar sayesinde olur. Elektrolitik iletkenlik, ü İyonların sayısına ü İyonların yüküne ü İyonların göçme hızına ü Derişimine ü Sıcaklığa bağlıdır. 15

İNDİRGENME – YÜKSELTGENME REAKSİYONLARI (Redoks Reaksiyonları) Doğal Redoks Tepkimeleri (Kendiliğinden gerçekleşir. ) PİLLER Yapay Redoks Tepkimeleri (Elektrik enerjisi ile gerçekleşir. ) ELEKTROLİZ 16

YÜKSELTGENME YARI PİL POTANSİYELİ Elementlerin aktifliğinin karşılaştırılmasının bir diğer yolu da yükseltgenme yarı pil potansiyelidir. Bir elementin yükseltgenme yarı pil potansiyeli değeri ne kadar büyükse elektron verebilme kabiliyeti (aktifliği) o kadar büyüktür. 17

İNDİRGENME YARI PİL POTANSİYELİ Yükseltgenme yarı pil potansiyeli değerinin ters çevrilmiş hâlidir. 18

YARI PİL POTANSİYEL DEĞERLERİ NE ANLAM TAŞIR? Yükseltgenme yarı pil potansiyeli veya indirgenme yarı pil potansiyeli değerlerinin sıfırdan büyük (+) olması, gösterilen denklemin istemli olduğunu; sıfırdan küçük (–) olması ise gösterilen denklemin istemsiz olduğunu gösterir. Sayısal değerin büyüklüğü veya küçüklüğü ise olayın ne derece istemli veya istemsiz olduğunu gösterir. 19

Redoks Reaksiyonlarının Gerilimi İndirgenme yarı reaksiyonunun gerilimi Yükseltgenme yarı reaksiyonunun gerilimi Redoks reaksiyonunun gerilimi 20

Redoks Reaksiyonlarının Gerilimi Sıfırdan Büyük İse Tepkime Kendiliğinden Gerçekleşir. Redoks Reaksiyonlarının Gerilimi Sıfırdan Küçük İse Elektrik Enerjisi İle Gerçekleşir. 21

STANDART HİDROJEN YARI PİLİ Hidrojenin yükseltgenme ve indirgenme yarı pil potansiyeli oda şartlarında (25 °C ve 1 atm) 0, 00 volt kabul edilmiştir. H 2(g) → 2 H+ + 2 e ΔE° = 0, 00 volt 2 H+ + 2 e → H 2(g) ΔE° = 0, 00 volt Diğer maddelerin yükseltgenme yarı pil potansiyelleri standart hidrojen yarı pilinden yararlanılarak bulunur. 22

KONSANTRASYON DEĞİŞMESİNİN PİL GERİLİMİNE ETKİSİ Pillerde denge olayı vardır. Pile yapılan etkilerle sistem ürünler lehine kayarsa gerilim artar; girenler lehine kayarsa gerilim azalır. Gerilimin arttırılması, pilin ömrünün uzaması demektir. Gerilimin azalması ise, pilin ömrünün kısalması demektir. Pil kullanıldıkça, gerilim azalır. Gerilim 0 volta düşünce pil tükenmiştir. 23

PİLLER; kendiliğinden gerçekleşen redoks tepkimeleridir. Reaksiyonların Kendiliğinden Gerçekleşip Gerçekleşmediğinin Tahmin Edilebilmesi Ürünler daha kıymetli ise kendiliğinden gerçekleşmiştir. Ekzotermik tepkime ise kendiliğinden gerçekleşmiştir. Aktif metal yükseltgendi ise kendiliğinden oluşmuştur 24

KENDİLİĞİNDEN GERÇEKLEŞEN REDOKS TEPKİMELERİNİN KULLANIMI Piller Doğal Kaplama Nitel ve Nicel Analiz Metotları 25

KENDİLİĞİNDEN GERÇEKLEŞEN TEPKİMELER Kendiliğinden, kendine oluyor demek değildir. İnsan iradesi karışmadan olduğunu ifade için denmiştir. İnsan iradesinin karıştığı işlere göre çok daha mükemmel olduğunu belirtmek içindir. 26

ELEKTROKİMYASAL TEPKİMELERDE HESS PRENSİBİNİN UYGULANMASI 1) Bir elektrokimyasal pil tepkimesinde reaksiyon bir sayı ile çarpılırsa pil potansiyeli (ΔE°) bu sayı ile çarpılmaz. 2) Yükseltgenme ya da indirgenme yarı reaksiyonları ters çevrilirse pil potansiyeli işaret değiştirir. 3) Pil tepkimesi iki ya da daha fazla pil reaksiyonunun toplamından elde ediliyorsa, bu tepkimenin pil potansiyeli diğer reaksiyonların pil potansiyelleri toplamına eşit olur. 27

İndirgenme yarı reaksiyonun gerilimi ile yükseltgenme yarı reaksiyonun gerilimi birbirinin ters işaretlisidir. Örnek: Fe+2 + 2 e → Fe 0 E 0 = – 0, 44 V Fe 0 – 2 e → Fe+2 E 0 = +0, 44 V 28

Yarı tepkime genişletilince E 0 değeri aynen kalır, genişletilmez. Örnek: Ag+1 + 1 e → Ag 0 E 0 = +0, 80 V 2 Ag+1 + 2 e → 2 Ag 0 E 0 = +0, 80 V 29

3. ELEKTROKİMYASAL HÜCRELER 30

Ag. NO 3 çözeltisi demir kapta saklanabilir mi? 2 Ag+1 + 2 e → 2 Ag 0 E 0 indirgenme = +0, 80 V Fe 0 – 2 e → Fe+2 E 0 yükseltgenme = +0, 44 V 2 Ag++Fe 0 → 2 Ag 0+Fe+2 E 0 redoks = +1, 24 V E 0 redoks > 0 olduğundan saklanamaz; çünkü reaksiyona girer. 31

ŞEHİR ŞEBEKE SULARINDAN PAS AKMASI NORMALDİR 4 Fe 0 – 8 e → 4 Fe+2 E 0 yükseltgenme = +0, 44 V 4 Fe+2 – 4 e → 4 Fe+3 E 0 yükseltgenme = – 0, 77 V 3 O 2 + 12 e → 6 O– 2 4 Fe 0 + 3 O 2 → 2 Fe 2 O 3 E 0 indirgenme = +1, 23 V E 0 redoks= +0, 90 V 32

Metalik demirin, oksijenle paslanmasına ait reaksiyon denkleminin toplam gerilimi, pozitif sayısal değerdir. Rutubetli ortam oto katalizördür. Çünkü; oksijenin indirgenme yarı reaksiyonu tam yazıldığında ürünlerde su çıkmaktadır. Fe 2 O 3 pastır. Paslanmayan borular kullanılmadığı müddetçe, sulardan pas akacaktır. Demirin; yağlı boya, paslanmaz çelik üretimi vb. yollarla paslanmaya karşı korunması önemlidir. 33

Al(NO 3)3 çözeltisi Zn kaşık ile karıştırılabilir mi? Al+3 ’ün Al 0 ’a indirgenme gerilimi = – 1, 66 V Zn 0 ’ın Zn+2 ’ye yükseltgenme gerilimi = +0, 76 V Redoks tepkimesinin gerilimi = – 0, 90 V E 0 redoks < 0 olduğundan karıştırılabilir; çünkü reaksiyon olmaz. 34

PİLDEN BAŞKA KENDİLİĞİNDEN GERÇEKLEŞEN YAŞAMIMIZDAKİ REDOKS TEPKİMELERİNE BAZI ÖRNEKLER Asit Yağmurunun Çinko Olukları Aşındırması Demirin Altınla ve Gümüşle Kaplanması 35

Asit Yağmurunun Çinko Olukları Aşındırması Zn + H 2 SO 4 → Zn. SO 4 + H 2 Demirin Altınla ve Gümüşle Kaplanması Fe + 3 Au. NO 3 → Fe(NO 3)3 + 3 Au Fe + 3 Ag. NO 3 → Fe(NO 3)3 + 3 Ag 36

DOĞAL TEDAVİDE VE KORUYUCU HEKİMLİKTE (HİJYEN) BAŞLICA İKİ YOL VE REDOKS 1. Bitkilerle tedavi ve hijyen 2. Doğal şifalı sularla tedavi ve hijyen 37

BİTKİLERLE TEDAVİ VE HİJYEN Fotosentez olayı bir redoks reaksiyonudur. Bunun sonucunda bitkiler oluşur. Fotosentezde ve fotosentezin devamında yaprak gereklidir. Tedavide ve hijyende bitki yaprakları önemlidir. Sigara kâğıdı gibi ince yeşil yapraklar, yazın çok şiddetli sıcaklıkta bile aylarca yaş kalır, kurumaz. 38

DOĞAL ŞİFALI SULARLA TEDAVİ Yeraltından gelen sular karşılaştıkları sert taş, kaya ve toprağa çarptığında elektron aktarımı olur; örneğin, elementel demir (sıfır değerlikli demir) içeren bir kayayla su temas edince; demir, +2 hâline geçer. Sıfır değerlikli demir suda çözünmez. Oluşan demir +2 bileşiği ise suda az çözünür. 39

Bu redoks tepkimeleri sonucunda yeryüzüne çıkan kaynak suları ve şifalı sular az veya eser miktarda onlarca farklı minerali içerir. Ülkemizde Keçiborlu suyu, şifalı sulara örnektir. Köklerin ipek gibi yumuşak damarlarının sert taşları delmesi anında da benzer redoks reaksiyonları gerçekleşir. 40

KİMYA LABORATUVARLARINDAKİ LAVABO VE PİS SU BORULARI İLE KENDİLİĞİNDEN OLUŞAN TEPKİME İLİŞKİSİ Kimya laboratuvarlarındaki lavabolar, çelik lavabo olmamalıdır; çünkü çelik, asitlerle kimyasal tepkimeye girer. Zaten bu hususa dikkat edilmektedir. 41

Kimya laboratuvarlarında lavabolar ve çalışma tezgâhları laminant da olmamalıdır; çünkü laminant, çoğu çözelti ile tepkimeye girer ve leke kalır. Kimya laboratuvarlarında pis su boruları, bakır ve çinko olmamalıdır. Bakır asitlerle tepkimeye girer. Çinko ise hem asit hem baz hem de bazı çözeltilerle tepkimeye girer. Bu hususlara kimya laboratuvarlarının kurulmasında dikkat edilmektedir. 42

SANAYİDE YANLIŞ BİR UYGULAMA; DEMİRİN ÇİNKO İLE KAPLANMASI Yanlış olarak elektrolizle olur. Emaye kaplar buna örnektir. Kısa sürede çinko (sır) kalkar. Kap kullanılamaz hâle gelir. Çinko kap (emaye kap), demirin çinko ile elektroliz sonucu kaplanmasıyla üretilmiştir. Günümüzde büyük çapta hem üretimi hem de evlerde kullanımı terk edilmiştir. 43

ENDÜSTRİDE YAPILAN BİR HATA; DEMİRİN KROM İLE KAPLANMASI Kaplama ancak elektrolizle olur, kendiliğinden olmaz. Demir daha kıymetli metaldir. Kromun üzeri demirle kendiliğinden kaplanır; doğrusu budur. Ancak, demirin üzeri kromla kendiliğinden kaplanmaz. Demirin kromla kaplanması ancak elektrolizle olur. Kaplandıktan sonra da krom hemen kalkar. 44

Hem kromun ele batma tehlikesi vardır hem de alttaki demir paslanır. Krom kaplı musluklarda buna çokça rastlanır. Kromaj kaplı et kıyma makinelerinde ise alttaki demir paslandığından dolayı, kıyma makinesinde sabahları ilk çekilen kıymalar paslı olur. CABİR BİN HAYYAN (721– 805) Paslanmayan çelik alaşımı elde etmiştir. Çeliklerde paslanmayı önlemiştir. 45

DOĞAL METAL KAPLAMA Kaplama esnasındaki kimyasal reaksiyon kendiliğinden gerçekleşiyorsa buna doğal kaplama denir. Doğal kaplama ince olur, buna rağmen yıllar sonra bile aşınmaz. İndirgenme gerilimi en büyük olan, soy metallerdir. Soy metal iyonu içeren bir çözelti (altın suyu) içine örneğin bir demir yüzük daldırılırsa yüzük altınla kaplanır. 46

DOĞAL METAL KAPLAMANIN UYGULANDIĞI YERLER Sanayide demir metalinin nikel ile kaplanması Değersiz metalden yapılmış süs eşyalarının gümüş ile kaplanması Değersiz metalden yapılmış takıların altın ve gümüş ile kaplanması 47

REDOKS TEPKİMESİ VE ELMA Elma 1 sene boyunca ihtiyacımızın olduğu bir meyvedir, her mevsim turfanda elma bulunur. Fe+2 kanımızdaki hemoglobinin temel maddesidir. Gıdalardaki ve ilaçlardaki demir iyonu ise Fe+3’tür. Fe+2 ihtiyacımızı elma ve nisan yağmuru ile karşılamamız gerekir. Veyahut elma çekirdeği yenilmelidir. 48

Kansızlık için alınan Fe+3 preparatları bağırsakları tahrip eder ve genelde faydası görülemez. Çünkü ilaç olarak veya gıdalarla aldığımız Fe+3 vücudumuzda ancak elma çekirdeğiyle indirgenerek Fe+2’ye dönüşebilir. Günde 1 tane elma ile beraber 1 tane de elma çekirdeği yenmelidir. Elma çekirdeği 1 taneden fazla yenmemelidir. 1 adet elmada bulunan Fe+2, insanın günlük Fe+2 ihtiyacı kadardır. 49

Elmada Fe+2 zaten vardır. Elma ağacı, kökleri vasıtasıyla topraktan aldığı Fe+3’ü indirgeyerek Fe+2 hâline getirir ve meyvesinde depolar. Bu redoks tepkimesi günümüzde kimya laboratuvarlarında henüz gerçekleştirilememiştir. Çünkü, gerçekleştirilmesi zor bir kimyasal işlemdir. Kırmızı renkli Fe+2’nin laboratuvarlarda elde edilmesi bu nedenle mümkün değildir. 50

Nisan yağmuru bereketlidir ve içilirse şifalıdır. Genelde nisan ayında yağan ikinci yağmur, kırmızı renkli Fe+2 içerir. Bu Fe+2’nin kaynağı çöllerdeki tozdur. Sahra tozları nisan ayında rüzgârla dünyanın her yerine taşınır. Tozlar bulutların içine girince de yağış oluşur. Bu yağmurdan sonra arabaların üzeri kırmızılaşır. 51

YERYÜZÜNDE BULUNAN DOĞAL ELEMENTLER VE DOĞAL BİLEŞİKLER HANGİLERİDİR? 52

METALLERİN SERBEST YA DA BİLEŞİK OLARAK DOĞADA BULUNMASIDAKİ KURAL İndirgenme yarı pil gerilimi listesinde; indirgenme potansiyeli hidrojenden yüksek olan metaller, soy (altın, platin, gümüş) metaller ve yarı soy (bakır, cıva) metallerdir. Soy metaller doğada yalnız elementel hâlde bulunur, bileşikleri hâlinde bulunmaz. 53

Yarı soy metaller ise hem elementel hâlde hem de bileşiği hâlinde bulunur. Amalgam diş dolgular; cıva ve gümüş içerir. Altın diş dolgusu da vardır. Platin metali ise, protezlerde kullanılır. Bütün bu kullanımlarda altın, platin, gümüş ve cıva; aynen doğadaki gibi metalik hâldedir. Sıfır değerliklidir. Bu nedenle de sağlığa zararları yoktur. Bakır ve cıva da soy metaller gibi genelde doğada serbest hâlde bulunur. 54

Bakır ve cıva metallerine, yarı soy metal denmesinin sebebi; doğada doğal bileşiklerinin de olmasıdır. Bu 5 element dışındaki bütün metaller, yaklaşık 70 metal doğada yalnız bileşikleri hâlinde bulunur, hiçbiri serbest hâlde bulunmaz. Örneğin doğada Na, Ca, Al yoktur. Na. Cl (yemek tuzu), Ca. CO 3 (mermer), Al 2 O 3 (alüminyum metalinin elektroliz yöntemiyle elde edildiği boksit cevheri) vardır. 55

Tabiatta bulunan ve suda çözünmeyen doğal metal bileşiklerine cevher (filiz) denir. Genellikle kaya tuzu gibi suda çözünenler yerin derinliklerinde, suda çözünmeyenler ise yerin üstündedir. Demir ve nikelin indirgenme potansiyeli hidrojenden az olmasına rağmen, yerkürenin merkezinde erimiş elementel hâlde de bulunurlar. 56

İnsan evrenin küçültülmüş bir örneği olduğundan; evrende hangi doğal element ve bileşik varsa, insanda numunesi vardır. Zemin yüzündeki doğal element ve doğal bileşiklerin çok faydalı görevleri vardır. Özellikle de insanın hizmetine koşmaktadırlar. 57

AMETALLERİN SERBEST YA DA BİLEŞİK OLARAK DOĞADA BULUNMASIDAKİ KURAL F 2 gazı ve Cl 2 gazı, tabiatta bulunmaz. Doğada florür bileşikleri ve klorür bileşikleri vardır. F 2 gazı ve Cl 2 gazından başka bütün ametaller; doğada, hem elementel hâlde hem de bileşiği hâlinde bulunur. Tabloda bunlar örneklerle gösterilmiştir: 58
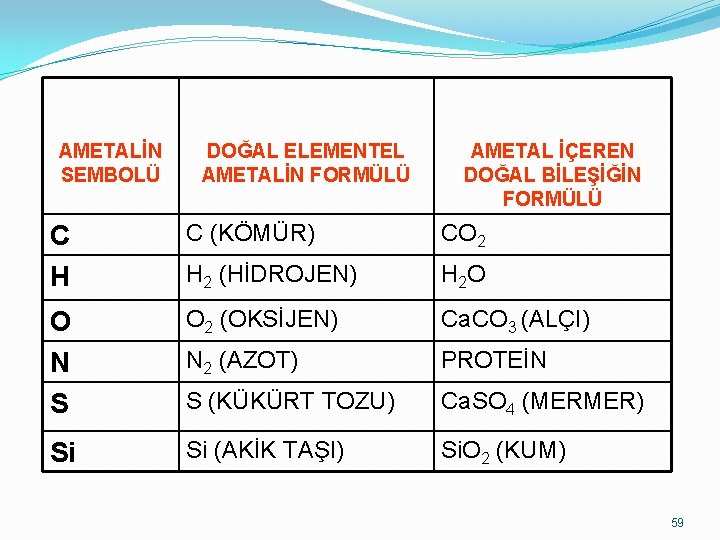
AMETALİN SEMBOLÜ DOĞAL ELEMENTEL AMETALİN FORMÜLÜ AMETAL İÇEREN DOĞAL BİLEŞİĞİN FORMÜLÜ C H C (KÖMÜR) CO 2 H 2 (HİDROJEN) H 2 O O N S O 2 (OKSİJEN) Ca. CO 3 (ALÇI) N 2 (AZOT) PROTEİN S (KÜKÜRT TOZU) Ca. SO 4 (MERMER) Si Si (AKİK TAŞI) Si. O 2 (KUM) 59

ELEKTROKİMYASAL PİLLER Kimyasal enerjiyi elektrik enerjisine çeviren sistemler pil olarak adlandırılır. Kimyasal pillerde yükseltgenme ve indirgenme yarı reaksiyonları ayrı kaplarda gerçekleştirilir. Kaplar bir tuz köprüsü ile ve elektrotlar da iletken tel ile bağlandığında devreden akımın geçtiği görülür. 60

Bir elektrokimyasal pilde tuz köprüsü, her bir kaptaki yük dengesini sağlamak içindir. Tuz köprüsünün içerisindeki çözelti suda çok çözünen KNO 3, KCl, Na. NO 3, NH 4 Cl gibi tuzların çözeltisidir. Çözeltisi U borusunun içerisine konulmuştur. Dökülmemesi için uçları pamukla veya bir tamponla kapatılır. 61

Kaplara ters olarak yerleştirilir. Tuz köprüsünde katyonlar katoda, anyonlar anoda göç ederler. Bir kimyasal pildeki yükseltgenmenin ve indirgenmenin olduğu çubuklar elektrottur. Yükseltgenmenin olduğu elektrota anot, indirgenmenin olduğu elektrota katot denir. Anot ve katotta gerçekleşen reaksiyonların toplamı pil reaksiyonudur. 62

KONSANTRASYON FARKINDAN DOLAYI ÇALIŞAN PİLLER (DERİŞİM PİLİ) Aynı cins elektrotlardan oluşan pillerde pil çözeltileri arasında konsantrasyon farkı varsa bu tür piller de çalışır. 63

REDOKS REAKSİYONUNUN PİL OLABİLMESİ İÇİN GEREKLİ ŞARTLAR 1) Yükseltgenme ve indirgenme reaksiyonları ayrı kaplarda gerçekleştirilmelidir. 2) Elektronların dış devreden iletken tel yardımıyla akışı sağlanmalıdır. 3) Çözeltiler tuz köprüsü ile birleştirilmelidir. 4) Bir kimyasal pilin çalışabilmesi için pil çiftleri arasında ya konsantrasyon ya da aktiflik farkı olmalıdır. 64

PİL ÇEŞİTLERİ Pilleri genel olarak iki ana gruba ayırmak mümkündür: Doldurulamayan Piller İçerisindeki kimyasal enerji tükendiğinde şarj edilemeyen pillerdir. Doldurulabilen Piller İçerisindeki kimyasal enerji tükendiğinde şarj edilebilen pillerdir. 65

PİL KONUSUNDA DİKKAT EDİLMESİ GEREKEN HUSUSLAR Piller daima taze satın alınmalıdır. Gereksiz yere bol miktarda pil alıp saklanmamalıdır. Çünkü zamanla bayatlar ve ömrü azalır. Saklanması gerekiyorsa, buzdolabı gibi soğuk ve serin yerlerde saklanmalıdır. Piller, devamlı güneş ışığı alan yerlerde tutulmamalıdır, soğuk ve karanlık yerlerde saklanmalıdır. 66

Pillerin kutupları birbirine değdirilmemeli, kısa devre yaptırılmamalıdır. Aksi durumda pil ömrünü kaybeder. Uzun süre kullanılmayan cihazlardaki piller akarak cihaza zarar verebilir. Bu nedenle kullanılmayan cihazların pillerini çıkarmak ihmal edilmemelidir. Bir aleti pil takılı iken 30 gün çalıştırmıyorsak, pili aletin içinden çıkarmalıyız. Aksi durumda pil sızmasından ve pilin kendine deşarjından dolayı alet zarar görür. 67

Şarj edilmeyen piller ve özellikle de lityum türleri kesinlikle şarj işlemine tabi tutulmamalıdır. Aksi takdirde aşırı ısınma, şişme, gaz çıkışı, alevlenme ve hatta patlama görülebilir. 68

PİLİN ÇEVREYE ZARARI Piller en pahalı enerji kaynakları arasında yer almaktadır. Ayrıca bünyesinde çok pahalı ürünler bulundurmaktadır. Hatta içeriğinde riskli kimyasallar vardır. Bu yüzden piller yutulduğunda tehlikeli ve ölümcül olabilirler. 69

Artık çoğu bölgelerde, kullanılmış pillerdeki toksik maddelerin geri kazanımı için, geri dönüşüm merkezleri kurulmuştur. Çevreye atılan atık piller çevre kirliliğine sebep olur. Güneş ısısının etkisiyle atık pillerin patlama olasılığı kaçınılmazdır. Patlama mekanik zarar doğurur. Bundan başka, patlama sonucu pilin içindeki kimyasal maddeler dışarı çıkar. Bu kimyasallar, insan sağlığı için risk unsuru taşır. 70

ATIK PİLLER NEREYE ATILMALI? Ömürleri tükenen piller, diğer evsel atıklardan ayrı olarak atık pil kutularına atılmalıdır. Biriktirilen bu atık piller geçici depolama alanlarında depolandıktan sonra gerekli birimlerce ve gerekli yöntemlerle bertaraf edilmektedir. Atık piller yakılmamalıdır, denize atılmamalıdır ve toprağa gömülmemelidir. 71

ATIK PİLLERİN TOPLANMASI Atık piller evsel atıklardan ayrı toplanmalıdır. Atık piller, pil ürünlerinin dağıtımını ve satışını yapan işletmeler veya belediyeler tarafından oluşturulan atık pil toplama noktalarına bırakılmalıdır. Atık piller, ekolojik sisteme uyum sağlayabilecek şekilde depolanmalı, toplanmalı, taşınmalıdır. 72

ATIK PİLİN BERTARAFI VEYA GERİ DÖNÜŞÜMÜ Atık piller toplandıktan sonra toprak altında inşa edilmiş, geçirimsizlik koşulları sağlanmış, nemden arındırılmış, meteorolojik şartlardan korunmuş, kapalı, sızdırmaz ve su geçirmez özellikli depolama alanlarına gömülür veya geri kazanımı yapılır veya ihracat yoluyla muhtemel olumsuz çevresel etkileri giderilir. 73
- Slides: 73