Termohemija Energetske promene pri fizikim i hemijskim procesima
































- Slides: 43

Termohemija Energetske promene pri fizičkim i hemijskim procesima

Termohemija Poglavlje 2. 2 Termohemija je deo termodinamike i bavi se proučavanjem toplotom raymenjenom pri hemijskim i fizičkim promenama, a bazira se na I zakonu termodinamike. Do toplotnih promena dolazi pošto različite supstancije u različitim stanjima imaju različite količine unutrašnje energije odnosno toplotne sadržaje, pa će ukupni sadržaj energije sistema u krajnjem stanju (fizičke ili hemijske promene) biti najčešće različit od ukupnog sadržaja energije u početnom stanju, tako da termodinamički procesi mogu biti • praćeni oslobađanjem (egzotermni) ili • apsorpcijom (endotermni) energije u obliku toplote.

Termohemijske jednačine, promena standardne entalpije Termohemijske jednačine obuhvataju hemijsku jednačinu sa oznakom stanja svake od supstancija koja u promeni učestvuje (pošto toplotni sadržaj zavisi od stanja), temperaturu pri kojoj se promena dešava kao i odgovarajuću energetsku promenu. Da bi se odgovarajuće toplotne promene mogle porediti, definiše se promena standardne entalpije, ΔHθ koja predstvlja promenu entalpije za proces u kome su supstancije u početnom i krajnjem stanju u standardnim stanjima. Standardno stanje supstancije pri određenoj temperaturi je njen čist oblik pritisku od 1 bara. Primedba-standardna entalpija se može dati za bilo koju temperaturu ali se uobičajeno daje na 298, 15 K (250 C)

Veza promene entalpije i promene unutrašnje energije Za idealno gasno stanje veza između entalpije i unutrašnje energije je: a za konačnu promenu stanja sistema: gde je promena broja molova gasovitih komponenata u reakciji. Tri mola gasa su zamenjena sa dva mola tečnosti pa je: Razlika je negativna jer toplota odlazi iz sistema, a sistem se kontrahuje jer se gradi tečna voda.

Primer veze U, H Za reakciju, 2 CO (g) + O 2 (g) 2 CO 2 (g), na 298 K 2 CO (g) + O 2 qp = -566, 0 k. J, izračunati qv and w. (g) Rešenje: Rad je zbog promene zapremine, w = -P V = -(nf – ni) R T H = -( 2 – 3) · 8, 3145 J mol – 1 K– 1 · 298 K = + 2500 J = + 2 , 5 k. J mol – 1 q. P= H = – 566, 0 k. J mol – 1 qv = U = – 566, 0 – (– 2, 5) k. J = – 563, 5 k. J Primedba: 3 mola gasa je redukovano do 2 mola, sistem mora primati rad da bi se komprimovao do istog P, U w 2 CO 2 (g)

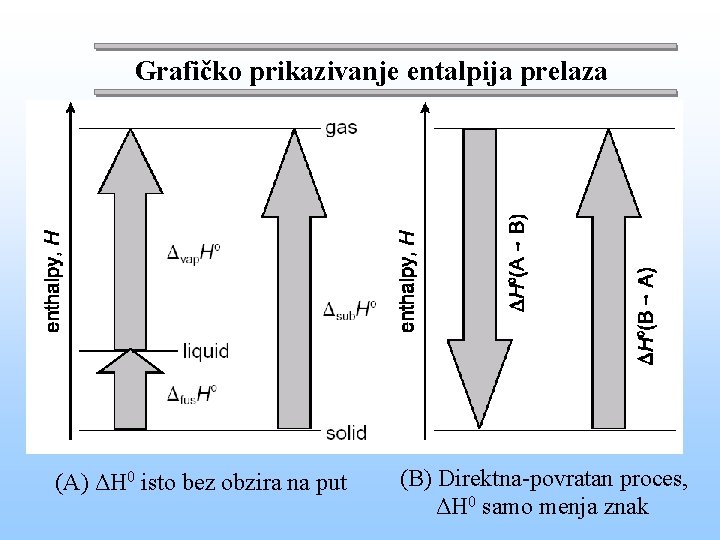
Entalpije fizičkih promena Standardna entalpija prelaza, pr. H 0, je promena standardne entalpije pri promenu fizičkog stanja (faze) supstancije. (A) Entalpija je funkcija stanja, nezavisna od načina prelaska iz početnog u krajnje stanje: ista vredmost za ΔH 0 bez obzira kako se promena dešava sublimacija H 2 O(č) H 2 O(g) Δsub. H 0 ključanje H 2 O(t) H 2 O(g) Δisp. H 0 topljenje H 2 O(č) H 2 O(t) Δtop. H 0 (B) Entalpija je funkcija stanja pa ΔH 0 samo menja znak kada se promene dešava u jednom ili drugom smeru, ΔH 0(A B)=- ΔH 0(B A) Primer: Kondenzacija Isparavanje H 2 O(g) H 2 O(t) Δisp. H 0(373)=-40, 66 k. J/mol H 2 O(t) H 2 O(g) Δisp. H 0(373)=40, 66 k. J/mol

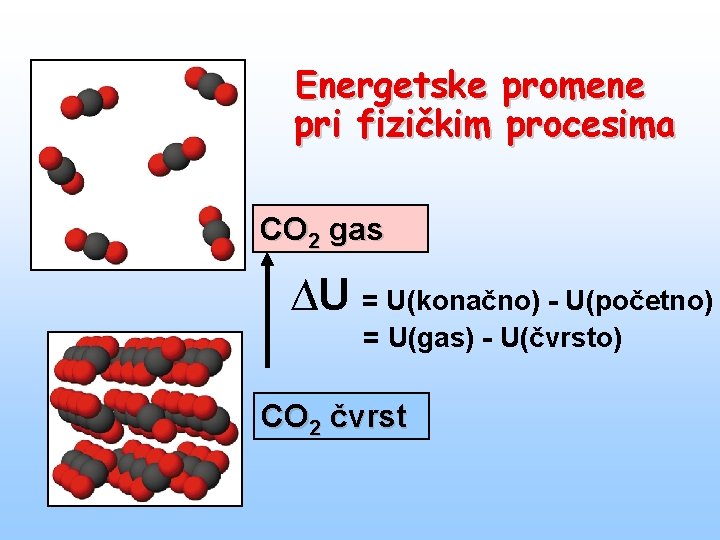
Energetske promene pri fizičkim procesima CO 2 gas ∆U = U(konačno) - U(početno) = U(gas) - U(čvrsto) CO 2 čvrst

Grafičko prikazivanje entalpija prelaza (A) ΔH 0 isto bez obzira na put (B) Direktna-povratan proces, ΔH 0 samo menja znak

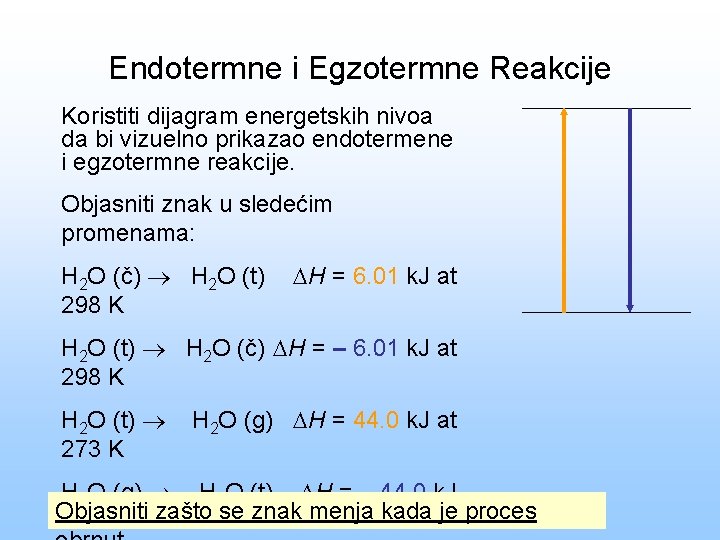
Endotermne i Egzotermne Reakcije Koristiti dijagram energetskih nivoa da bi vizuelno prikazao endotermene i egzotermne reakcije. Objasniti znak u sledećim promenama: H 2 O (č) H 2 O (t) 298 K H = 6. 01 k. J at H 2 O (t) H 2 O (č) H = – 6. 01 k. J at 298 K H 2 O (t) 273 K H 2 O (g) H = 44. 0 k. J at H 2 O (g) H 2 O (t) H = – 44. 0 k. J Objasniti at 273 K zašto se znak menja kada je proces

Entalpije različitih prelaza Različiti tipovi prelaza koji su praćeni odgovarajućim promenama entalpija prikazani prema IUPAC-u Prelaz Proces Oznaka* Fazni prelaz Faza trs. H Topljenje s l fus. H Isparavanje l g vap. H Sublimacija s g sub. H Mešanje fluida Čisto smeša mix. H Rastvaranje Rastvorak rastvor sol. H Hidratacija X (g) X(aq) hyd. H Atomizacija Vrste(s, l, g) atomi(g) at. H Jonizacija X(g) X+(g) + e (g) ion. H Vezivanje elektrona X(g) + e (g) X (g) eg. H Reakcija Reaktanti produkti r H Sagorevanje Jedinjenje(s, l, g)+O 2(g)+H 2 O(l, g) c. H Formiranje Elementi jedinjenje f. H

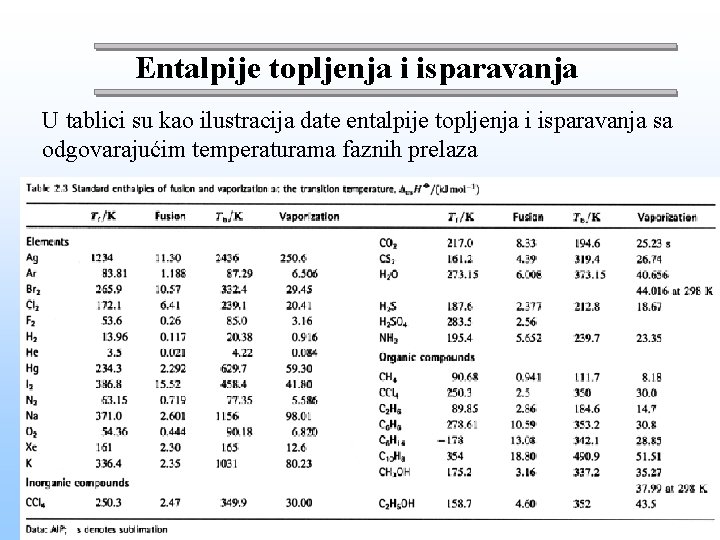
Entalpije topljenja i isparavanja U tablici su kao ilustracija date entalpije topljenja i isparavanja sa odgovarajućim temperaturama faznih prelaza

Entalpije drugih fizičkih promena Entalpija jonizacije, H 0 i predstavlja promenu entalpije koja prati jonizaciju jednog mola gasovite supstancije: A(g) A+(g) + e(g) H 0 i = U 0 i + RT Energija jonizacije, Ui je promena unutrašnje energije jonizacije pri T=0 Pošto je RT(298)≈ 2, 5 k. J mol 1, to se može uzeti da je: H 0 i≈ U 0 i≈Ui. Promena standardne entalpije koja prati vezivanje elektrona za atom, jon ili molekul u gasnoj fazi je entalpija vezivanja elektrona: A(g) + e-(g) A-(g) H 0 ea = U 0 ea – RT = Uea RT H 0 ea elektronski afinitet

Entalpija disocijacije veze, H 0(A B), je standardna promena entalpije za proces u kome se raskida veza A B: A B(g) A(g) + B(g) H 0(A B) gde A i B mogu biti atomi ili grupe atoma C(č)+2 H 2(g)→CH 4(g) C(č)→C(g) 1/2 H 2(g)→H(g) ΔHof=-74. 81 k. J/mol ΔHos=716, 7 k. J/mol ΔHod=218, 0 k. J/mol Kombinacijom gornjih jednačina: CH 4(g) → C(č)+2 H 2(g) C(č)→C(g) 2 H 2(g)→ 4 H(g) ΔHo=74. 81 k. J/mol ΔHo=716, 7 k. J/mol ΔHo=4 x 218, 0=872 k. J/mol Dobijamo entalpiju atomizacije metana: CH 4(g)→C(g)+4 H(g) ΔHof=1663, 5 k. J/mol Četvrtina ove vrednosti 415, 9 k. J/mol je entalpija veze ili jačina veze.

Toplote rastvaranja Standardna molarna entalpija rastvaranja, H 0 ras, m, neke supstancije predstavlja promenu standardne entalpije pri rastvaranja jednog mola te supstancije u određenoj količini rastvarača. Ovo je integralna toplota rastvaranja koja zavisi od koncentracije nagrađenog rastvora. Diferencijalna toplota rastvaranja predstavlja standardnu toplotu rastvaranja koja prati rastvaranje 1 mola supstancije u beskonačno velikoj količini rastvora određene koncentracije, čiji dalji dodatak ne dovodi do promene koncentracije i toplote rastvaranja

Entalpije hemijskih promena Standardna entalpija reakcije, Δr. H 0(T) je promena entalpije kada reaktanti u standardnom stanju daju produkte u standardnom stanju Čisti ne izmešani reaktanti u standardnim stanjima Čisti odvojeni produkti u standardnim stanjima Primer: CH 4(g)+2 O 2(g) CO 2(g)+2 H 2 O(t) Δsag. H 0=-890 k. J/mol Primedba: Toplotna promena mešanja i odvajanja je zanemarljivo mala u poređenju sa standardnom entalpijom rekcije

Entalpija sagorevanja Standardna molarna entalpija sagorevanja, H 0 sag, m, je promena standardne entalpije pri sagorevanju jednog mola organske supstancije do CO 2 i H 2 O, ako supstancija sadrži C, H ili O i još do N 2 ili azotne ili sumporne okside ako sadrži N ili S. Po Dato je, jednačini C 12 H 22 O 11 (s) + 12 O 2 (g) 12 CO 2 (g) + 11 H 2 O (l), H = – 5650 k. J Koliko se toplote oslobodi kada 10. 0 g of saharoze (Mr= 342. 3), pošto ste je konzumirali, svarili i potpuno sagoreli (oksidovali)? Rešenje: 1 mol S – 5650 Dati uslovi 342. 3 se odbnose na humano korišćenje saharoze g k. J – znači oslobođena energija (S), S 1 mol S Zadatak: Odrediti U i w = – 16, 506 k. J 10. 0 g. S

Standardne molarne entalpije Ako se razmotri reakcija: 2 A+B 3 C+D Standardna entalpija reakcije se računa kao: gde su ν stehiometrijski koeficijenti, pa je: gde je Hm 0(J) standardna molarna entalpija vrste J. Za reakciju opšteg tipa: gde su: υi stehiometrijski koeficijenti, pozitivni za produkte a negativni za reaktante, Ai hemijski simboli, promena standardne entalpije reakcije je: H 0 T = i H 0 T, i odnosno U 0 T = i U 0 T, i.

Standardna entalpija nastajanja (formiranja) Standardna molarna entalpija formiranja (ili nastajanja), H 0 f, m, je promena standardne entalpije pri formiranju jednog mola jedinjenja iz elemenata u njihovim referentnim stanjima. Referentno stanje elementa definiše se kao njegovo najstabilnije stanje pritisku od 1 bara i na posmatranoj temperaturi. Po konvenciji su entalpije elemenata u njihovom referentnom stanu jednake nuli. Primeri: Azot Živa Ugljenik Sumpor Kalaj N 2(g) Hg(t) C(grafit) S(rombični) Sn(beli) Standardna entalpija nastajanja tečnog benzena na 298 K: 6 C(č, grafit)+3 H 2(g) C 6 H 6(t) ΔHf, m 0=49 k. J/mol

∆Hfo, standardna molarna entalpija formiranja H 2(g) + 1/2 O 2(g) --> H 2 O(g) ∆Hfo (H 2 O, g)= -241. 8 k. J/mol Po definiciji, ∆Hfo = 0 za elemente u njihovim standardnim stanjima.

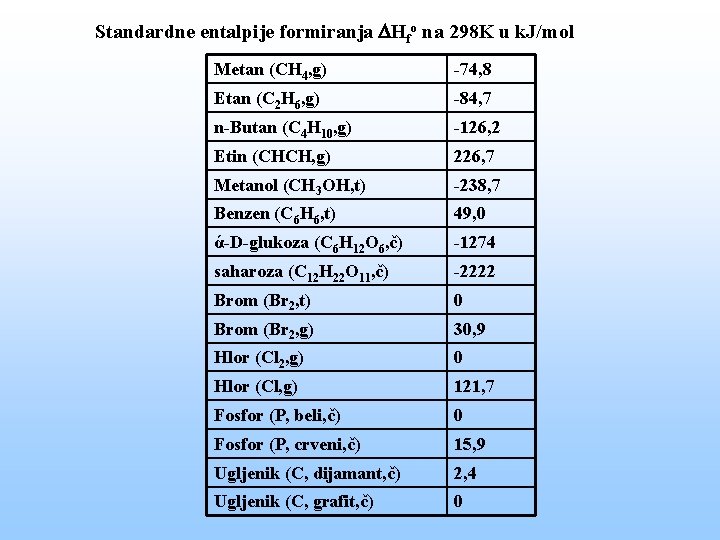
Standardne entalpije formiranja Hfo na 298 K u k. J/mol Metan (CH 4, g) -74, 8 Etan (C 2 H 6, g) -84, 7 n-Butan (C 4 H 10, g) -126, 2 Etin (CHCH, g) 226, 7 Metanol (CH 3 OH, t) -238, 7 Benzen (C 6 H 6, t) 49, 0 ά-D-glukoza (C 6 H 12 O 6, č) -1274 saharoza (C 12 H 22 O 11, č) -2222 Brom (Br 2, t) 0 Brom (Br 2, g) 30, 9 Hlor (Cl 2, g) 0 Hlor (Cl, g) 121, 7 Fosfor (P, beli, č) 0 Fosfor (P, crveni, č) 15, 9 Ugljenik (C, dijamant, č) 2, 4 Ugljenik (C, grafit, č) 0

Standardne entalpije formiranja Jedinjenje Hf. k. J (Objasni) Reakcija C (grafit) C Cdjiamant 1. 9 (dijamant) (fazni prelaz) Br 2 (t) Br 2 (g) Br 2(g) 30. 9 (prelazi u gas na 298 K) P 4 (crveni) -17. 6 beli) P 4(č, crveni) P 4 (č, (Beli P je standardno stanje) H (g) 217. 8 ½ H 2 (g) H Hf° k. J mol– 1 jedinjenja H 2 O (l)– 285. 8 H 2 O (g) – 241. 8 CO (g) – 110. 5 CO 2 (g) – 393. 5 CH 4 (g) – 74. 8 C 2 H 2 (g) + 226. 7 C 2 H 4 (g) + 52. 4 C 2 H 6 (g) – 84. 7 CH 3 OH (l) – 238. 7 C 2 H 5 OH (l) – 277. 7

Termohemijski podaci Postoje tablice termohemijskih i uopšte termodinamičkih podataka za različite naučne i tehničke primene. NIST(National biro of standards)-ov sajt ima termohemijske podatke za preko 6000 organskih i neorganskih jedinjenja. Takođe ima podatke za preko 9000 reakcija i podataka za jone u preko 16 000 jedinjenja. Pored toga postoje razni termohemijski

Entalpija reakcije preko entalpija formiranja Može se smatrati kao da se reakcija odigrava razlaganjem reaktanata do elemenata i onda formiranja produkata iz ovih elemenata. Vrednost ΔHr 0 čitave reakcije je suma entalpija rasformiranja reaktanata do elemenata i formiranja produkata iz elemenata. Prva entalpija je entalpija formiranja reaktanata sa suprtonim znakom tako da je entalpija reakcije razlika suma entalpija formiranja produkata i reaktanata:

Korišćenje standardnih entalpija formiranja Izračunati ∆H reakcije? Uopšte, kada su SVE entalpije formiranja poznate, može se odrediti entalpija reakcije! ∆Horxn= ∆Hfo(produkti) - ∆Hfo (reaktanti) Zapamtite uvek je ∆ = krajnje – početno

Primer: Medjutim: Toplota neke reakcije se može izračunati iz toplota formiranja svih supstancija koje u reakciji učestvuju, a takođe je moguće da se iz poznate toplote reakcije i toplota formiranja svih supstancija sem jedne, izračuna toplota formiranja te supstancije kao u reakciji: O 3(g) O 2(g) + O(g) ? H 0298=106, 5 k. J mol 1 Kako je toplota formiranja ozona poznata, ΔHf. m 0(O 3)=-142, 7 k. J/mol, to je standardna toplota nastajanja atomskog kiseonika: H 0 f(O) = 106, 5 k. J mol 1 + 142, 7 k. J mol 1= =249, 2 k. J mol 1

Termohemijski zakoni • Lavoazije i Laplas su došli do zaključka, mereći toplote različitih hemijskih reakcija, da je toplota apsorbovana pri razlaganju jednog jedinjenja jednaka toploti koja se oslobodi kada se to jedinjenje nagradi iz elemenata. Posledica toga je da su termohemijske reakcije povratne.

Antoine Laurent Lavoisier (1743 -1794 ) Bio između ostalog hemičar i ekonomista a najpoznatiji u objašnjenju uloge kiseonika u sagorevanju. Školovao se prvo za advokata a zatim za geologa. 1765 objašnjava kako da se poboljša osvetljavanje Pariza. 1768. biva izabran u Kraljevsku akademiju nauke. Kasnije se bavi različitim zanimanjima a u vreme Francuske revolucije dospeva i u zatvor. Dao je prvo flogistonsku teoriju a zatim i pravo objašnjenje sagorevanja. Smatra se ocem moderne hemije. Potvrdio zakon o održanju mase, objasnio proces disanja, ali i tvorac pogrešne kaloričke teorije.

Pierre-Simon Laplace (1749 – 1827) Obrazovao se u benediktanskoj školi a zatim počeo studije teologije. Međutim ubrzo je otkriven njegov veliki talenat za matematiku i toj nauci je dao najveći doprinos Primenjuje matematičke metode u fizici, posebno matematici a radio je i u oblasti kapilarnog dejstva, dvojnog prelamanja, brzine zvuka i teorije toplote.

Termohemijski zakoni • Zakon konstantnosti toplotnog zbira dao je Hes (Hess). On je zaključio da je ukupna toplota hemijske reakcije pri konstantnom pritisku ista, bez obzira u koliko stupnjeva se reakcija izvodi. Posledica ovog zakona je da se termohemijske jednačine mogu sabirati i oduzimati.

Germain Henri Hess (1802 -1850) Rođen u Ženevi. Mladost proveo u Rusiji. Studirao na Univerzitetu Dorpat (Tartu, Estonija) i u Štokholmu kod Bercelijusa. Vraća se u Rusiju i učestvuje u geološkoj ekspediciji na Ural a zatim počinje medicinsku praksu u Irkutsku. Od 1830. u Petrogradu postaje profesor na Tehnološkom institutu. Njegov najznačajniji rad objavljen je 1840 a odnosi se na konstantnost toplotnog zbira. 1842 formuliše i svoj drugi zakon termoneutralnosti prema kome pri reakcijama izmene neutralnih soli u vodenim rastvorima nema toplotnih efekata.

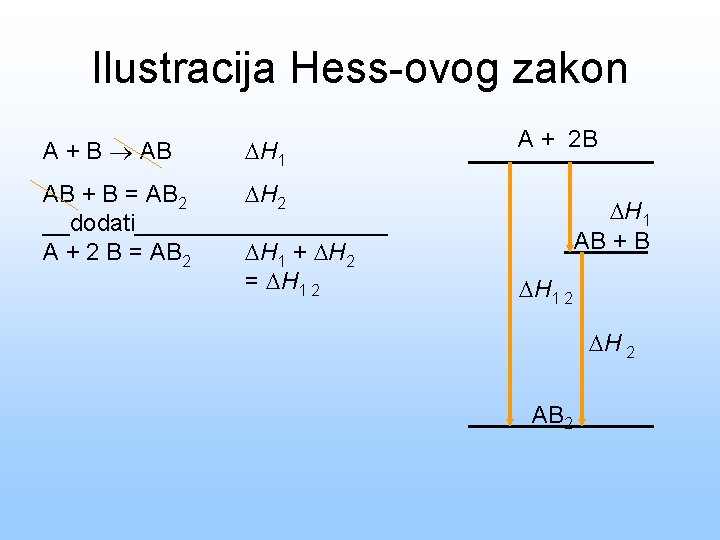
Ilustracija Hess-ovog zakon A + B AB H 1 AB + B = AB 2 H 2 __dodati__________ A + 2 B = AB 2 H 1 + H 2 = H 1 2 A + 2 B H 1 AB + B H 1 2 H 2 AB 2

Hess-ov zakon toplotnog zbira Promena entalpije čitavog procesa je suma promena entalpija individualnih koraka Primer: Problem: izračunati toplotu reakcije oksidacije sumpora do sumportrioksida prema reakcijama: 1) S (s) + O 2 (g) SO 2 (g) H 1 = -296. 0 k. J 2) 2 SO 2 (g) + O 2 (g) 2 SO 3 (g) H 2 = -198. 2 k. J 3) S (s) + 3/2 O 2 (g) SO 3 (g) H 3 = ?

ENTALPIJA REAKCIJA Razmotrimo nastajanje vodene pare H 2(g) + 1/2 O 2(g) --> H 2 O(g) + 241. 8 k. J Egzotermna reakcija — toplota je “proizvod” i ∆H = – 241. 8 k. J

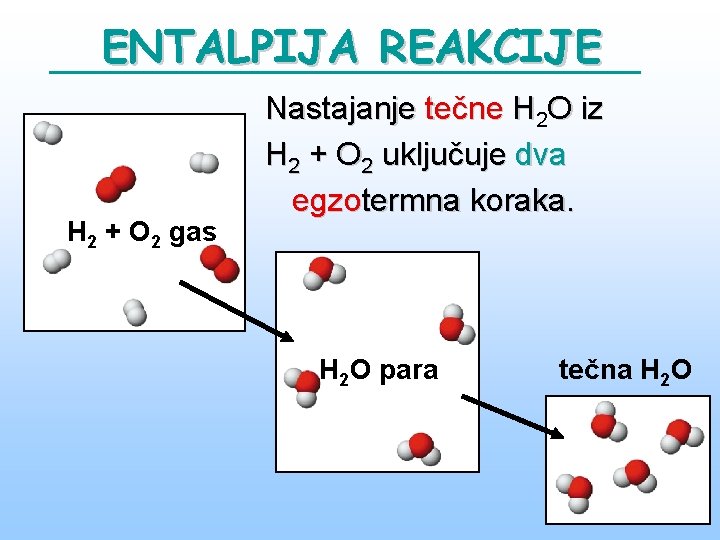
ENTALPIJA REAKCIJE H 2 + O 2 gas Nastajanje tečne H 2 O iz H 2 + O 2 uključuje dva egzotermna koraka. H 2 O para tečna H 2 O

ENTALPIJA REAKCIJE Nastajanje tečne H 2 O uključuje dva egzotermna koraka. H 2(g) + 1/2 O 2(g) ---> H 2 O(g) + 242 k. J H 2 O(g) ---> H 2 O(t) + 44 k. J ________________ H 2(g) + 1/2 O 2(g) --> H 2 O(t) + 286 k. J Primer HESOVOG ZAKONA

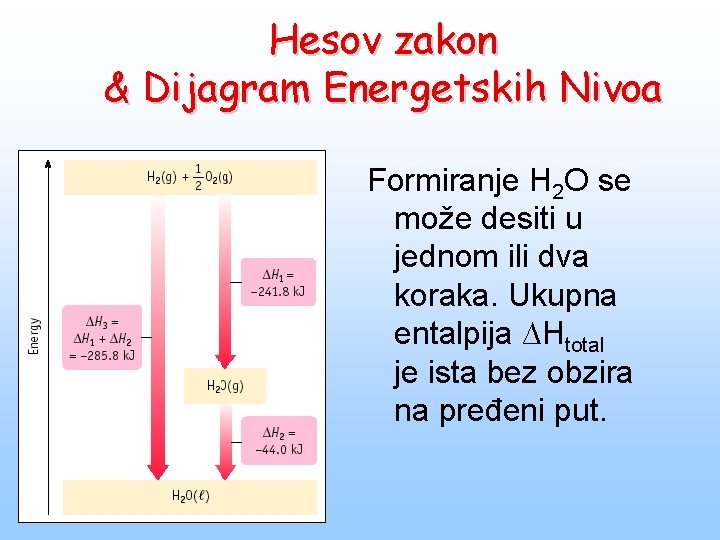
Hesov zakon & Dijagram Energetskih Nivoa Formiranje H 2 O se može desiti u jednom ili dva koraka. Ukupna entalpija ∆Htotal je ista bez obzira na pređeni put.

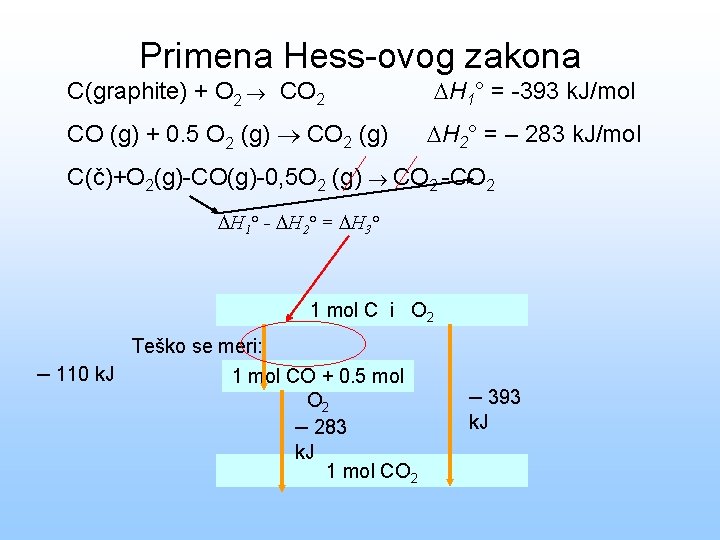
Primena Hess-ovog zakona C(graphite) + O 2 CO 2 H 1° = -393 k. J/mol CO (g) + 0. 5 O 2 (g) CO 2 (g) H 2° = – 283 k. J/mol C(č)+O 2(g)-CO(g)-0, 5 O 2 (g) CO 2 -CO 2 H 1° - H 2° = H 3° 1 mol C i O 2 Teško se meri: – 110 k. J 1 mol CO + 0. 5 mol O 2 – 283 k. J 1 mol CO 2 – 393 k. J

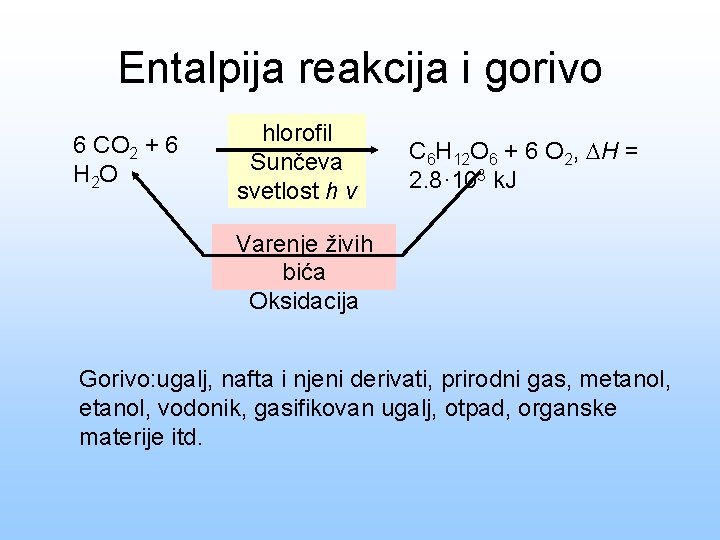
Entalpija reakcija i gorivo 6 CO 2 + 6 H 2 O hlorofil Sunčeva svetlost h v C 6 H 12 O 6 + 6 O 2, H = 2. 8· 103 k. J Varenje živih bića Oksidacija Gorivo: ugalj, nafta i njeni derivati, prirodni gas, metanol, vodonik, gasifikovan ugalj, otpad, organske materije itd.

Entalpija kompleksiranjahidratacije Cu. SO 4(č)+5 H 2 O(t) Cu. SO 4 5 H 2 O(č) Hhidro=-134 k. J/mol

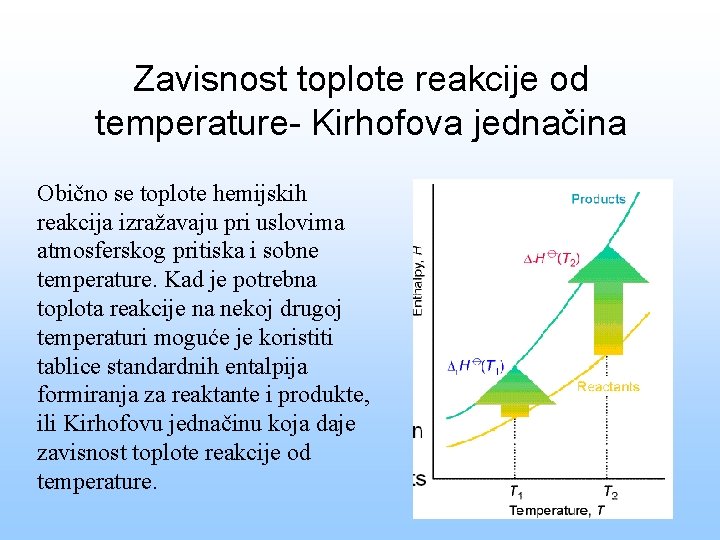
Zavisnost toplote reakcije od temperature- Kirhofova jednačina Obično se toplote hemijskih reakcija izražavaju pri uslovima atmosferskog pritiska i sobne temperature. Kad je potrebna toplota reakcije na nekoj drugoj temperaturi moguće je koristiti tablice standardnih entalpija formiranja za reaktante i produkte, ili Kirhofovu jednačinu koja daje zavisnost toplote reakcije od temperature.

Gustav Robert Kirchhoff (1824 -1887) Školovao se u Kenigsbergu. 1845. formulisao je dva zakona u vezi električne struje. 1854. postaje profesor u Hajdelbergu. Bavio se takođe zračenjem crnog tela. 1859 uočava da svaki element ima karakterističan spektar. Sa Bunzenom predstavlja pionire spektralne analize. 1861. posmatrajući spektar sunca, identifikovao prisutne elemente i objasnio poreklo tamnih linija u spektru. Takođe je otkrio dva nova elementa Cs i Rb. Od 1875 prelazi u Berlin i kao profesor matematičke fizike piše 4 toma čuvenog dela Vorlesungen über mathematische Physik (1876 -94).

I put: H 1 + (CP)B T II put: (CP)A T + H 2 Ove energetske promene moraju biti međusobno jednake saglasno prvom zakonu termodinamike: H 1 + (CP)B T = H 2 + (CP)A T Kirhofova (Kirchhoff) jednačine u diferencijalnom obliku: pri P=const. pri V=const.

Razdvajanjem promenljivih, može se izvršiti integracija u razmatranom temperaturskom intervalu od T 1 do T 2 : CP = a + b. T+c. T 2 +…
 Dijagram energetskih promena
Dijagram energetskih promena Termicki gradijent
Termicki gradijent Proces odobravanja kredita
Proces odobravanja kredita Hemijska reakcija sagorevanja metanola
Hemijska reakcija sagorevanja metanola Vanjski procesi oblikovanja reljefa
Vanjski procesi oblikovanja reljefa Finansiranje energetske efikasnosti
Finansiranje energetske efikasnosti Finansiranje energetske efikasnosti
Finansiranje energetske efikasnosti Energetske zone
Energetske zone Glasovne promene prezentacija
Glasovne promene prezentacija Globalne promene u zivotnoj sredini i njihove posledice
Globalne promene u zivotnoj sredini i njihove posledice Je nais et meurs dans l'eau. qui suis-je
Je nais et meurs dans l'eau. qui suis-je Euploidija
Euploidija Sedi organi costituzionali italiani
Sedi organi costituzionali italiani Bitka pri világoši
Bitka pri világoši Pgd dob pri šentvidu
Pgd dob pri šentvidu Osebna zaščitna sredstva pri delu z bolnikom
Osebna zaščitna sredstva pri delu z bolnikom Tasba pri
Tasba pri Starojudovski duhovnik iz stare zaveze
Starojudovski duhovnik iz stare zaveze Hypernatriæmi pri
Hypernatriæmi pri Clo ze zahraničí
Clo ze zahraničí štivan pri devinu
štivan pri devinu Metodický postup při nácviku písně
Metodický postup při nácviku písně Bitka pri solferine
Bitka pri solferine Karol martel
Karol martel Makaronizmus
Makaronizmus čím sa líši vyparovanie od varu
čím sa líši vyparovanie od varu Zmluva o vykonan�� pr��ce
Zmluva o vykonan�� pr��ce Bri vs pri
Bri vs pri Nesieme pane chlieb a víno
Nesieme pane chlieb a víno Aproktno prebavilo
Aproktno prebavilo Kako se vozač treba ponašati na skliskom kolniku?
Kako se vozač treba ponašati na skliskom kolniku? Při exkurzi jsme shlédli celý podnik
Při exkurzi jsme shlédli celý podnik Oš šmartno pri litiji e učilnica
Oš šmartno pri litiji e učilnica Prva pomoc pri poraneni mozgu a miechy
Prva pomoc pri poraneni mozgu a miechy Pri eaudit
Pri eaudit Naselje pri novem mestu
Naselje pri novem mestu Prežívam radosť v srdci svojom akordy
Prežívam radosť v srdci svojom akordy Modernm
Modernm Ravnanje z ljudmi pri delu
Ravnanje z ljudmi pri delu Aleksander veliki predstavitev
Aleksander veliki predstavitev Uloga radne kocnice
Uloga radne kocnice Invokacija u epovima
Invokacija u epovima živočíchy vodného spoločenstva
živočíchy vodného spoločenstva Pranostiky uhorky do jarka
Pranostiky uhorky do jarka