chemia stosowana I temat utlenianie i redukcja stopie














- Slides: 17

chemia stosowana I temat: utlenianie i redukcja

stopień utlenienia pierwiastków Stopień utlenienia atomu określa jaki ładunek miałby atom, gdyby elektrony były przekazywane między atomami (nie-uwspólniane). Reguły • dla prostych jonów stopień utlenienia = ładunek • dla pierwiastków stopień utlenienia = 0 • dla związków kowalencyjnych każdą uwspólnioną parę elektronową przypisuje się do atomu o większej elektroujemności • identyczne atomy dzielą parę elektronową wiązania między siebie Wnioski • F-I • HI (z niemetalami) lub H-I (z metalami) • O-II (reguła) O-I (nadtlenki, np. H 2 O 2) OII (OF 2) Jeśli stopień utlenienia rośnie - zachodzi reakcja utleniania. Jeśli stopień utlenienia maleje - zachodzi reakcja redukcji.

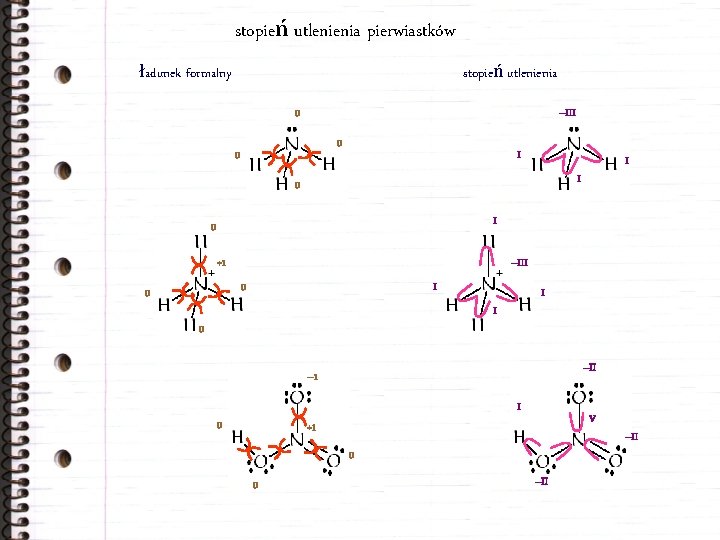
stopień utlenienia pierwiastków ładunek formalny stopień utlenienia 0 –III 0 0 I I I 0 +1 –III 0 0 I I I 0 –II – 1 I 0 V +1 0 0 –II

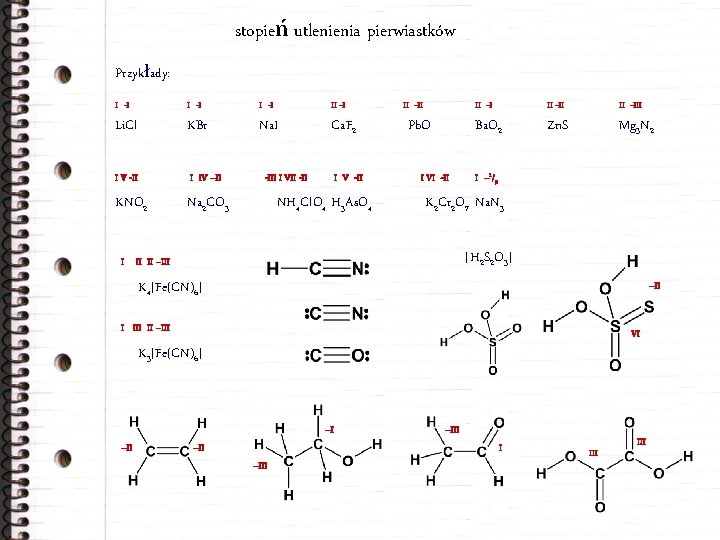
stopień utlenienia pierwiastków Przykłady: I -I II -I Li. Cl KBr Na. I Ca. F 2 I V -II I IV –II KNO 2 Na 2 CO 3 -III I VII -II I V -II NH 4 Cl. O 4 H 3 As. O 4 II -II Pb. O I VI -II II -III Ba. O 2 Zn. S Mg 3 N 2 I – 1/3 K 2 Cr 2 O 7 Na. N 3 [H 2 S 2 O 3] I II II –III K 4[Fe(CN)6] –II I II –III VI K 3[Fe(CN)6] –I –II –III III

reakcje utleniania - redukcji (redoks) Mg 0 + Cl 02 Mg. IICl–I 2 Zn 0 + 2 HICl–I Zn. IICl–I 2 + H 02 Mg 0 Mg 2+ + 2 e /× 1 Zn 0 Zn 2+ + 2 e /× 1 Cl 02 + 2 e 2 Cl– /× 1 2 H+ + 2 e H 02 /× 1 2 Fe 3+ + 2 I– 2 Fe 2+ + I 02 3 Cu 2+ + 2 Al 0 3 Cu 0 + 2 Al 3+ 2 Fe 3+ + 2 e Fe 2+ /× 1 2 I– I 02 + 2 e Al 0 Al 3+ + 3 e /× 2 Cu 2+ + 2 e Cu 0 /× 3 /× 1 2 Mn. VIIO 4– + 5 Sn 2+ + 16 H+ 2 Mn 2+ + 5 Sn 4+ + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 Sn 2+ Sn 4+ + 2 e /× 5

reakcje utleniania - redukcji (redoks) 2 NVO 3– + 3 Cu 0 + 8 H+ 3 Cu 2+ + 2 NIIO + 4 H 2 O NVO 3– + 3 e + 4 H+ NIIO + 2 H 2 O /× 2 Cu 0 Cu 2+ + 2 e /× 3 2 NVO 3– + Cu 0 + 4 H+ Cu 2+ + 2 NIIO 2 + 2 H 2 O NVO 3– + e + 2 H+ NIVO 2 + H 2 O /× 2 Cu 0 Cu 2+ + 2 e /× 1 2 Mn. VIIO 4– + 5 H 2 O–I 2 + 6 H+ 2 Mn 2+ + 5 O 02 + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 H 2 O–I 2 2 H+ + O 02 + 2 e /× 5

reakcje utleniania - redukcji (redoks) 2 Cr 3+ + 3 H 2 O–I 2 + 10 O–IIH– 2 Cr. VIO 42– + 8 H 2 O–II H 2 O–I 2 + 2 e 2 O–IIH– /× 3 Cr 3+ + 8 OH– Cr. VIO 42– + 4 H 2 O + 3 e /× 2 Cr. VI 2 O 72– + 3 H 2 CIII 2 O 4 + 8 H+ 2 Cr 3+ + 6 CIVO 2 + 7 H 2 O Cr. VI 2 O 72– + 6 e + 14 H+ 2 Cr 3+ + 7 H 2 O /× 1 H 2 CIII 2 O 4 2 CIVO 2 + 2 H+ + 2 e /× 3 Pb. IVO 2 + 2 Cl– + 4 H+ Pb 2+ + Cl 02 + 2 H 2 O Pb. IVO 2 + 2 e + 4 H+ Pb 2+ + 2 H 2 O /× 1 2 Cl– Cl 02 + 2 e /× 1

wpływ środowiska na reakcje redoks kwaśne 2 Mn. VIIO 4– + 5 H 2 S–II + 6 H+ 2 Mn 2+ + 5 S 0 + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 H 2 S–II 2 H+ + S 0 + 2 e /× 5 obojętne 2 Mn. VIIO 4– + 3 H 2 S–II 2 Mn. IVO 2 + 3 S 0 + 2 OH– + 2 H 2 O Mn. VIIO 4– + 3 e + 2 H 2 O Mn. IVO 2 + 4 OH– /× 2 H 2 S–II + 2 OH– S 0 + 2 H 2 O + 2 e zasadowe 2 Mn. VIIO 4– + H 2 S–II + 2 OH– 2 Mn. VIO 42– + S 0 + 2 H 2 O Mn. VIIO 4– + e Mn. VIO 42– H 2 S–II + 2 OH– S 0 + 2 H 2 O + 2 e /× 1 /× 2 /× 3

reakcje synproporcjonowania (redoks) Hg 2+ + Hg 0 Hg 22+ S 2– + S 0 S 22– 2 S 0 + 2 e S 22– /×(1/2) 2 Hg 2+ + 2 e Hg 22+ /×(1/2) 2 S 2– S 22– + 2 e /×(1/2) 2 Hg 0 Hg 22+ + 2 e Cl– + Cl. IO– + 2 H+ Cl 02 + H 2 O 2 Cl. IO– + 4 H+ + 2 e Cl 02 + 2 H 2 O /×(1/2) 2 Cl– Cl 02 + 2 e /×(1/2) 5 Br– + Br. VO 3– + 6 H+ 3 Br 02 + 3 H 2 O 2 Br. VO 3– + 12 H+ + 10 e Br 02 + 6 H 2 O /×(1/2) 2 Br– Br 02 + 2 e /×(5/2)

reakcje dysproporcjonowania (redoks) 2 Cu+ Cu 0 + Cu 2+ Hg 22+ + S 2– Hg. IIS + Hg 0 Hg 22+ + 2 e 2 Hg 0 Cu+ + e Cu 0 /× 1 Cu+ Cu 2+ + e /× 1 /×(1/2) Hg 22+ + 2 S 2– 2 Hg. IIS + 2 e /×(1/2) 3 Cl. IO– 2 Cl– + Cl. IO 3– Cl. IO– + 2 H+ + 2 e Cl– + H 2 O /× 2 Cl. IO– + 2 H 2 O Cl. IO 3– + 4 H+ + 2 e /× 1 3 Mn. VIO 42– + 4 H+ 2 Mn. VIIO 4– +Mn. IVO 2 + 2 H 2 O Mn. VIO 42– + 4 H+ + 2 e Mn. IVO 2 + 2 H 2 O /× 1 Mn. VIO 42– Mn. VIIO 4– + e /× 2

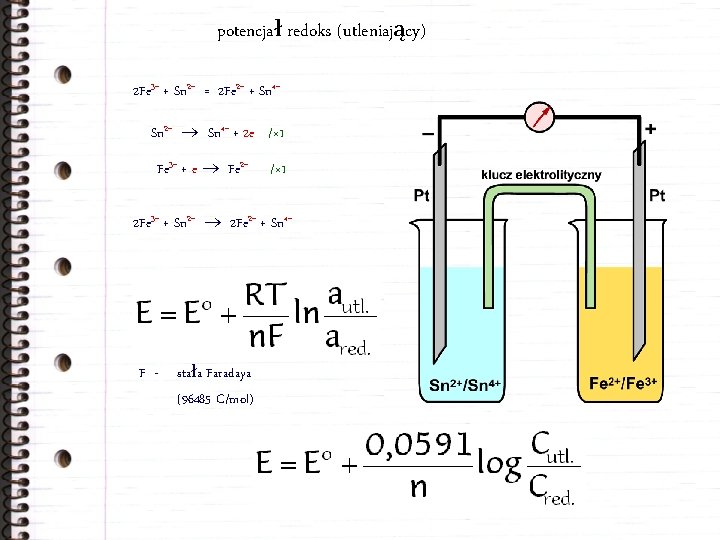
potencjał redoks (utleniający) 2 Fe 3+ + Sn 2+ = 2 Fe 2+ + Sn 4+ Sn 2+ Sn 4+ + 2 e /× 1 Fe 3+ + e Fe 2+ /× 1 2 Fe 3+ + Sn 2+ 2 Fe 2+ + Sn 4+ F - stała Faradaya (96485 C/mol)

potencjał redoks (utleniający) Li+/Li K+/K Ca 2+/Ca Na+/Na Mg 2+/Mg Al 3+/Al Zn 2+/Zn Cr 3+/Cr Fe 2+/Fe Ni 2+/Ni Pb 2+/Pb H+/H 2/Pt Cu 2+/Cu Ag+/Ag Au+/Au E° = – 3, 045 V E° = – 2, 925 V E° = – 2, 866 V E° = – 2, 714 V E° = – 2, 363 V E° = – 1, 662 V E° = – 0, 763 V E° = – 0, 744 V E° = – 0, 440 V E° = – 0, 250 V E° = – 0, 126 V E° = 0, 000 V E° = +0, 337 V E° = +0, 799 V E° = + 1, 50 V SO 42–/SO 32–, OH– NO 3–/NO 2– Sn 4+/Sn 2+ Cu 2+/Cu+ I 2/I– Mn. O 4–/Mn. O 2, OH– Fe 3+/Fe 2+ Cl. O–/Cl–, OH– NO 3–, H+/NO Br 2/Br– Mn. O 2, H+/Mn 2+ Cr 2 O 72–, H+/Cr 3+ Cl 2/Cl– Mn. O 4–, H+/Mn 2+ Co 3+/Co 2+ F 2/F– E° = – 1, 12 V E° = +0, 01 V E° = +0, 153 V E° = +0, 536 V E° = +0, 588 V E° = +0, 771 V E° = +0, 89 V E° = +0, 96 V E° = +1, 065 V E° = +1, 23 V E° = +1, 360 V E° = +1, 51 V E° = +1, 81 V E° = +2, 87 V

potencjał redoks (utleniający) Dla układu H+/H 2/g//Pt przyjmuje się, że E° = 0 V. Potencjały innych układów wyznacza się porównawczo. Sn 4+ + 2 e = Sn 2+ E° = 0, 15 V 2 Fe 3+ + Sn 2+ 2 Fe 2+ + Sn 4+ Fe 3+ + e = Fe 2+ E° = 0, 77 V E Fe 3+/Fe 2+ = E° E Fe 3+/Fe 2+ Sn 4+/Sn 2+ w stanie równowagi: SEM = 0, 62 + 0, 0591 log 1 + = E° SEM = EFe 3+/Fe 2+ – ESn 4+/Sn 2+ + CFe 3+ CFe 2+ 0, 0591 log 2 CSn 4+ CSn 2+ SEM = 0, 62 + 0, 0591 log 1 · 2 C 2 Fe 3+ · CSn 2+ C 2 Fe 2+ · CSn 4+ C 2 Fe 3+ · CSn 2+ =0! C 2 Fe 2+ · CSn 4+ log K = 0, 62 · 1 · 2 = 21, 0 0, 0591

przewidywanie kierunku reakcji 2 Fe 2+ + 2 Hg 2+ =? = 2 Fe 3+ + Hg 22+ Fe 3+ + e = Fe 2+ E° = 0, 77 V 2 Hg 2+ + 2 e = Hg 22+ E° = 0, 91 V 2 Fe 2+ + 2 Hg 2+ 2 Fe 3+ + Hg 22+ Mn. VIIO 4– + e = Mn. VIO 42– E° = 0, 54 V 2 Mn. VIO 42– + Cl 0 + Br 0 2 Mn. VIO 42– I 0 2 Mn. VIO 42– + 2 2 Mn. VIIO 4– + Cl– Cl 02 + 2 e = 2 Cl– E° = 1, 358 V + Br– Br 02 + 2 e = 2 Br– E° = 1, 065 V + I– I 02 + 2 e = 2 I– E° = 0, 53 V

wpływ p. H na potencjał redoks utl. + m. H+ + ne red + 0, 5 m. H 2 O utl + 0, 5 m. H 2 O + ne red. + m. OH– dla stężeń utl. /red. = 1 M p. H = 0 3 7 11 14 E= 1, 52 1, 24 0, 86 0, 48 0, 20 E= 1, 26 0, 96 0, 57 0, 18 – 0, 12 Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O Cr. VIO 42– + 4 H 2 O + 3 e Cr 3+ + 8 OH– Wzrost p. H zwiększa potencjał redoks.

wpływ kompleksowania na potencjał redoks W przypadku kompleksowania formy utlenionej potencjał się obniża. W przypadku kompleksowania formy zredukowanej potencjał się podwyższa. Fe 3+/Fe 2+ Co 3+/Co 2+ Au+/Au E° = +0, 771 V [Fe(CN)6]3–/[Fe(CN)6]4– E° = +0, 36 V [Co(CN)6]3–/[Co(CN)6]4– E° = +0, 83 V [Au(CN)2]–/Au E° = – 0, 76 V E° = +1, 81 V E° = + 1, 50 V

chemia stosowana I KONIEC