Stopie utlenienia atomu okrela jaki adunek miaby atom
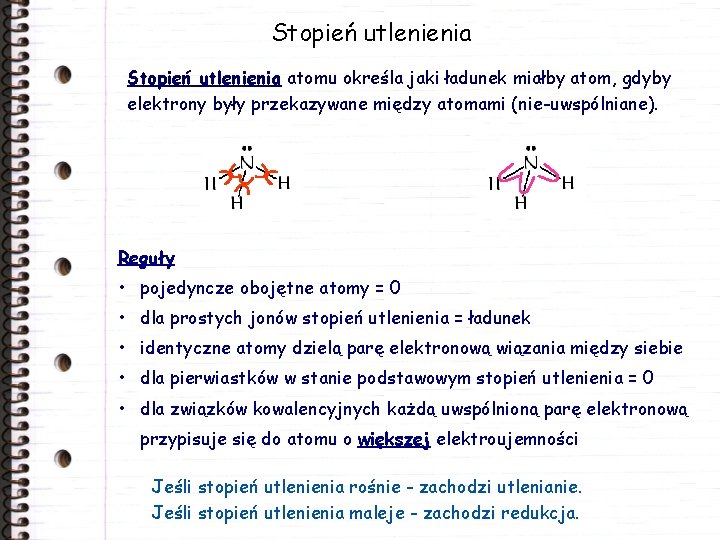
Stopień utlenienia atomu określa jaki ładunek miałby atom, gdyby elektrony były przekazywane między atomami (nie-uwspólniane). Reguły • pojedyncze obojętne atomy = 0 • dla prostych jonów stopień utlenienia = ładunek • identyczne atomy dzielą parę elektronową wiązania między siebie • dla pierwiastków w stanie podstawowym stopień utlenienia = 0 • dla związków kowalencyjnych każdą uwspólnioną parę elektronową przypisuje się do atomu o większej elektroujemności Jeśli stopień utlenienia rośnie - zachodzi utlenianie. Jeśli stopień utlenienia maleje - zachodzi redukcja.
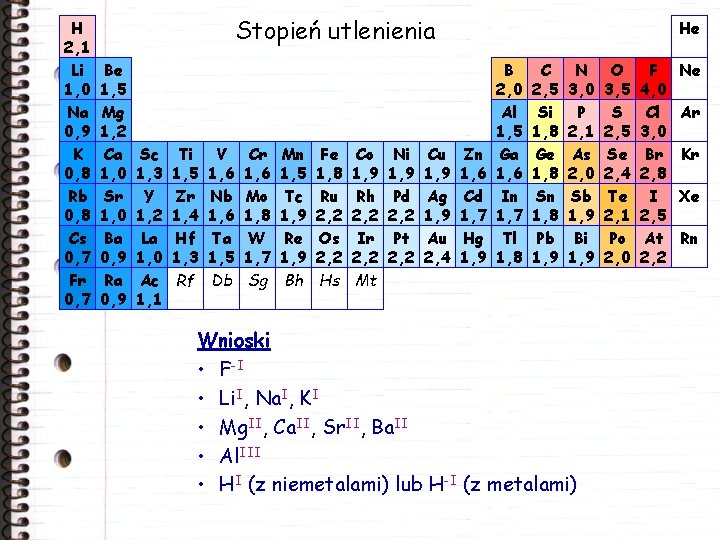
H 2, 1 Li 1, 0 Na 0, 9 K 0, 8 Rb 0, 8 Cs 0, 7 Fr 0, 7 Stopień utlenienia Be 1, 5 Mg 1, 2 Ca 1, 0 Sr 1, 0 Ba 0, 9 Ra 0, 9 Sc 1, 3 Y 1, 2 La 1, 0 Ac 1, 1 Ti 1, 5 Zr 1, 4 Hf 1, 3 Rf V 1, 6 Nb 1, 6 Ta 1, 5 Db Cr 1, 6 Mo 1, 8 W 1, 7 Sg Mn 1, 5 Tc 1, 9 Re 1, 9 Bh Fe 1, 8 Ru 2, 2 Os 2, 2 Hs Co 1, 9 Rh 2, 2 Ir 2, 2 Mt Ni 1, 9 Pd 2, 2 Pt 2, 2 Cu 1, 9 Ag 1, 9 Au 2, 4 He Zn 1, 6 Cd 1, 7 Hg 1, 9 B 2, 0 Al 1, 5 Ga 1, 6 In 1, 7 Tl 1, 8 C 2, 5 Si 1, 8 Ge 1, 8 Sn 1, 8 Pb 1, 9 N 3, 0 P 2, 1 As 2, 0 Sb 1, 9 Bi 1, 9 Wnioski • F-I • Li. I, Na. I, KI • Mg. II, Ca. II, Sr. II, Ba. II • Al. III • HI (z niemetalami) lub H-I (z metalami) O 3, 5 S 2, 5 Se 2, 4 Te 2, 1 Po 2, 0 F 4, 0 Cl 3, 0 Br 2, 8 I 2, 5 At 2, 2 Ne Ar Kr Xe Rn
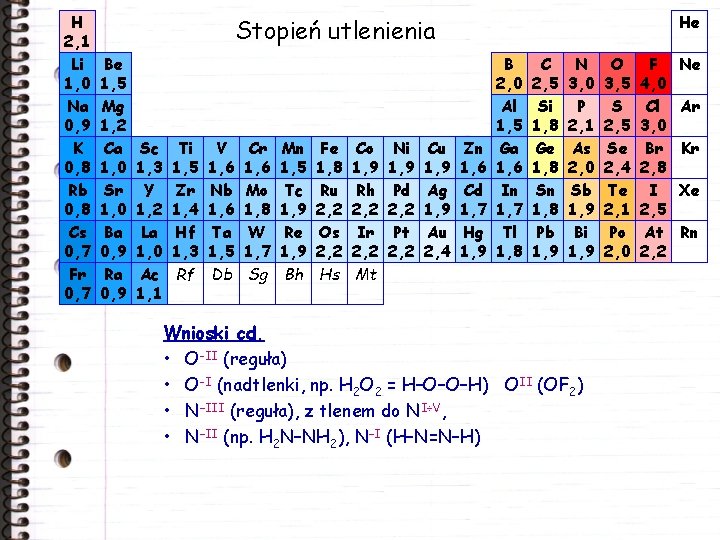
H 2, 1 Li 1, 0 Na 0, 9 K 0, 8 Rb 0, 8 Cs 0, 7 Fr 0, 7 He Stopień utlenienia Be 1, 5 Mg 1, 2 Ca 1, 0 Sr 1, 0 Ba 0, 9 Ra 0, 9 Sc 1, 3 Y 1, 2 La 1, 0 Ac 1, 1 Ti 1, 5 Zr 1, 4 Hf 1, 3 Rf V 1, 6 Nb 1, 6 Ta 1, 5 Db Cr 1, 6 Mo 1, 8 W 1, 7 Sg Mn 1, 5 Tc 1, 9 Re 1, 9 Bh Fe 1, 8 Ru 2, 2 Os 2, 2 Hs Co 1, 9 Rh 2, 2 Ir 2, 2 Mt Ni 1, 9 Pd 2, 2 Pt 2, 2 Cu 1, 9 Ag 1, 9 Au 2, 4 Zn 1, 6 Cd 1, 7 Hg 1, 9 B 2, 0 Al 1, 5 Ga 1, 6 In 1, 7 Tl 1, 8 C 2, 5 Si 1, 8 Ge 1, 8 Sn 1, 8 Pb 1, 9 N 3, 0 P 2, 1 As 2, 0 Sb 1, 9 Bi 1, 9 Wnioski cd. • O-II (reguła) • O-I (nadtlenki, np. H 2 O 2 = H–O–O–H) OII (OF 2) • N–III (reguła), z tlenem do NI÷V, • N–II (np. H 2 N–NH 2), N–I (H–N=N–H) O 3, 5 S 2, 5 Se 2, 4 Te 2, 1 Po 2, 0 F 4, 0 Cl 3, 0 Br 2, 8 I 2, 5 At 2, 2 Ne Ar Kr Xe Rn
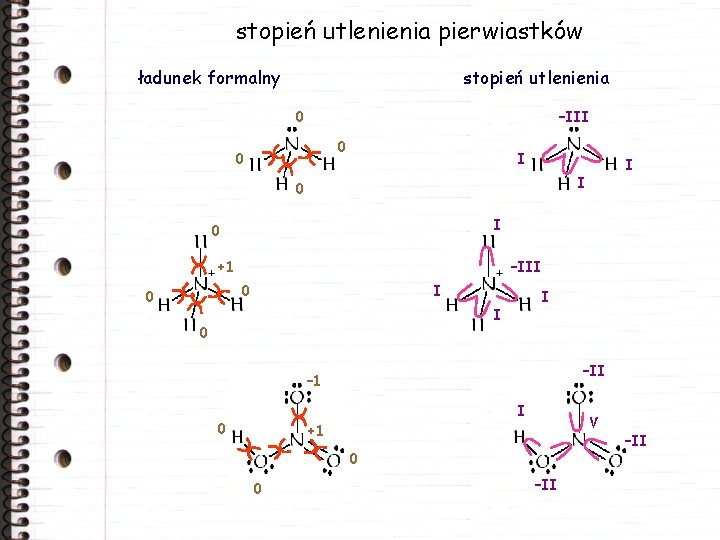
stopień utlenienia pierwiastków ładunek formalny stopień utlenienia 0 –III 0 0 I I 0 +1 –III 0 0 I I 0 –II – 1 I 0 V +1 0 0 –II
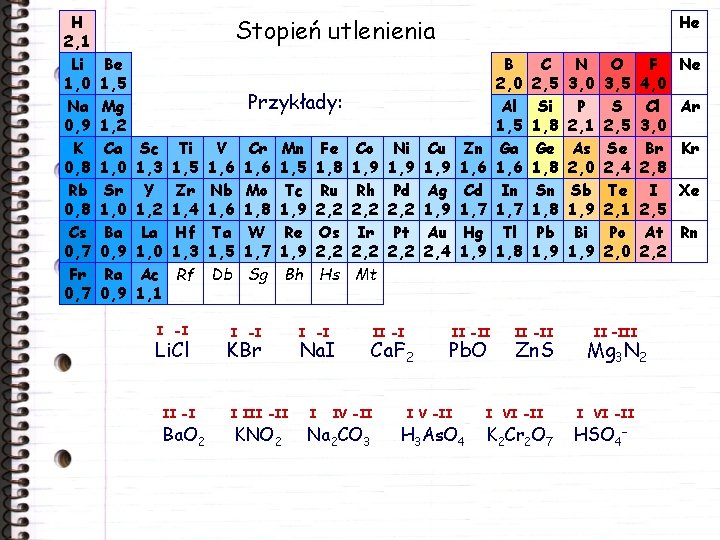
H 2, 1 Li 1, 0 Na 0, 9 K 0, 8 Rb 0, 8 Cs 0, 7 Fr 0, 7 He Stopień utlenienia Be 1, 5 Mg 1, 2 Ca 1, 0 Sr 1, 0 Ba 0, 9 Ra 0, 9 Przykłady: Sc 1, 3 Y 1, 2 La 1, 0 Ac 1, 1 Ti 1, 5 Zr 1, 4 Hf 1, 3 Rf I -I Li. Cl II -I Ba. O 2 V 1, 6 Nb 1, 6 Ta 1, 5 Db Cr 1, 6 Mo 1, 8 W 1, 7 Sg Mn 1, 5 Tc 1, 9 Re 1, 9 Bh I -I KBr I III -II KNO 2 Fe 1, 8 Ru 2, 2 Os 2, 2 Hs Co 1, 9 Rh 2, 2 Ir 2, 2 Mt I -I Na. I I II -I Ca. F 2 IV -II Na 2 CO 3 Ni 1, 9 Pd 2, 2 Pt 2, 2 Cu 1, 9 Ag 1, 9 Au 2, 4 Zn 1, 6 Cd 1, 7 Hg 1, 9 II -II Pb. O I V -II H 3 As. O 4 B 2, 0 Al 1, 5 Ga 1, 6 In 1, 7 Tl 1, 8 C 2, 5 Si 1, 8 Ge 1, 8 Sn 1, 8 Pb 1, 9 II -II Zn. S N 3, 0 P 2, 1 As 2, 0 Sb 1, 9 Bi 1, 9 O 3, 5 S 2, 5 Se 2, 4 Te 2, 1 Po 2, 0 II –III F 4, 0 Cl 3, 0 Br 2, 8 I 2, 5 At 2, 2 Mg 3 N 2 I VI -II K 2 Cr 2 O 7 HSO 4– Ne Ar Kr Xe Rn
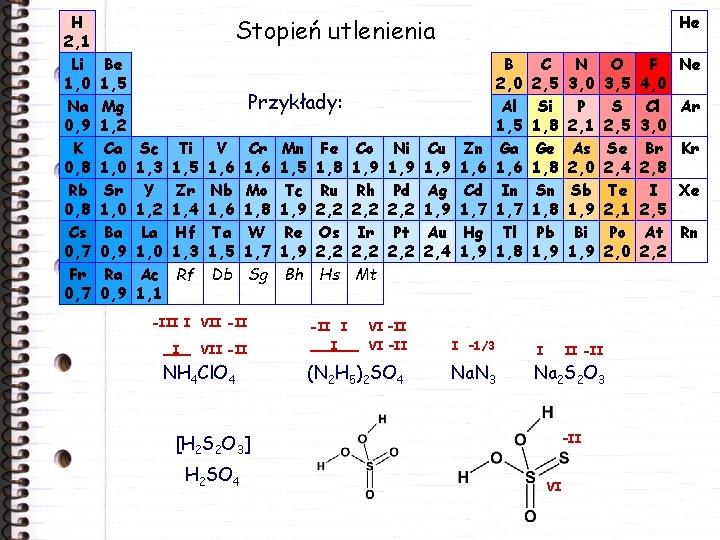
H 2, 1 Li 1, 0 Na 0, 9 K 0, 8 Rb 0, 8 Cs 0, 7 Fr 0, 7 He Stopień utlenienia Be 1, 5 Mg 1, 2 Ca 1, 0 Sr 1, 0 Ba 0, 9 Ra 0, 9 Przykłady: Sc 1, 3 Y 1, 2 La 1, 0 Ac 1, 1 Ti 1, 5 Zr 1, 4 Hf 1, 3 Rf V 1, 6 Nb 1, 6 Ta 1, 5 Db Cr 1, 6 Mo 1, 8 W 1, 7 Sg -III I VII -II NH 4 Cl. O 4 Mn 1, 5 Tc 1, 9 Re 1, 9 Bh Fe 1, 8 Ru 2, 2 Os 2, 2 Hs -II I I Co 1, 9 Rh 2, 2 Ir 2, 2 Mt Ni 1, 9 Pd 2, 2 Pt 2, 2 Cu 1, 9 Ag 1, 9 Au 2, 4 Zn 1, 6 Cd 1, 7 Hg 1, 9 B 2, 0 Al 1, 5 Ga 1, 6 In 1, 7 Tl 1, 8 C 2, 5 Si 1, 8 Ge 1, 8 Sn 1, 8 Pb 1, 9 O 3, 5 S 2, 5 Se 2, 4 Te 2, 1 Po 2, 0 VI –II I – 1/3 (N 2 H 5)2 SO 4 Na. N 3 I II -II Na 2 S 2 O 3 [H 2 S 2 O 3] H 2 SO 4 N 3, 0 P 2, 1 As 2, 0 Sb 1, 9 Bi 1, 9 –II VI F 4, 0 Cl 3, 0 Br 2, 8 I 2, 5 At 2, 2 Ne Ar Kr Xe Rn
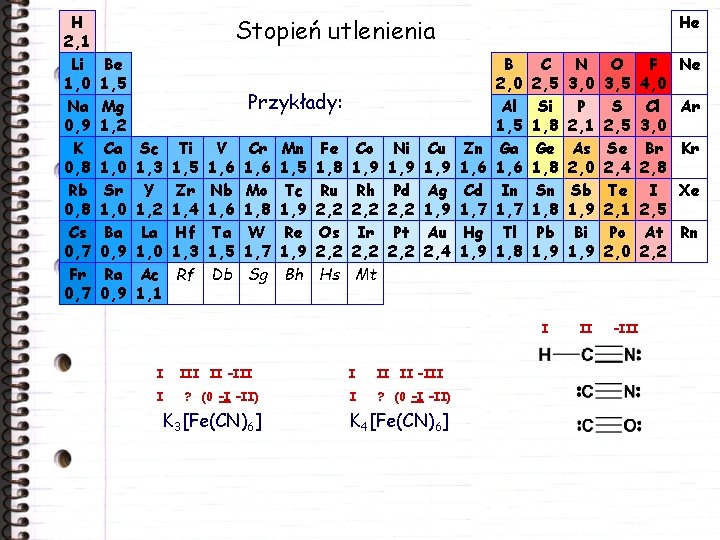
H 2, 1 Li 1, 0 Na 0, 9 K 0, 8 Rb 0, 8 Cs 0, 7 Fr 0, 7 He Stopień utlenienia Be 1, 5 Mg 1, 2 Ca 1, 0 Sr 1, 0 Ba 0, 9 Ra 0, 9 Przykłady: Sc 1, 3 Y 1, 2 La 1, 0 Ac 1, 1 Ti 1, 5 Zr 1, 4 Hf 1, 3 Rf V 1, 6 Nb 1, 6 Ta 1, 5 Db Cr 1, 6 Mo 1, 8 W 1, 7 Sg Mn 1, 5 Tc 1, 9 Re 1, 9 Bh Fe 1, 8 Ru 2, 2 Os 2, 2 Hs Co 1, 9 Rh 2, 2 Ir 2, 2 Mt Ni 1, 9 Pd 2, 2 Pt 2, 2 Cu 1, 9 Ag 1, 9 Au 2, 4 Zn 1, 6 Cd 1, 7 Hg 1, 9 B 2, 0 Al 1, 5 Ga 1, 6 In 1, 7 Tl 1, 8 C 2, 5 Si 1, 8 Ge 1, 8 Sn 1, 8 Pb 1, 9 I III II –III ? (0 –I –II) K 3[Fe(CN)6] I II II –III I ? (0 –I –II) K 4[Fe(CN)6] N 3, 0 P 2, 1 As 2, 0 Sb 1, 9 Bi 1, 9 II O 3, 5 S 2, 5 Se 2, 4 Te 2, 1 Po 2, 0 –III F 4, 0 Cl 3, 0 Br 2, 8 I 2, 5 At 2, 2 Ne Ar Kr Xe Rn
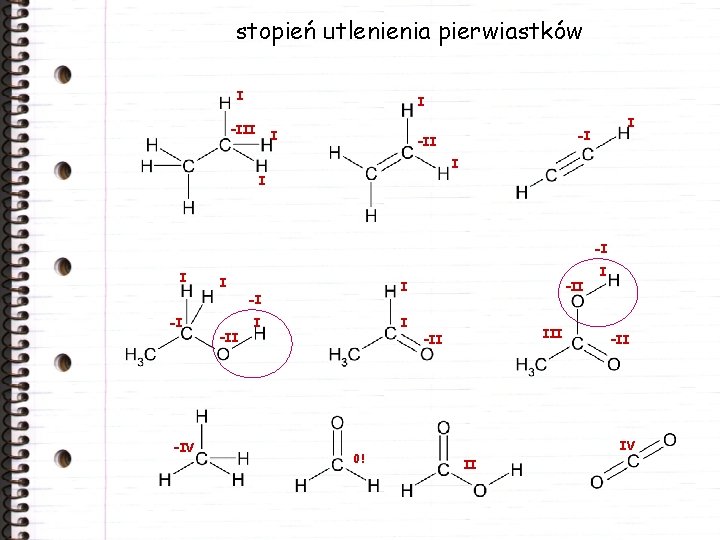
stopień utlenienia pierwiastków I I –III I I -I –II I I -I -I –IV –II I III –II 0! I –II IV II

reakcje utleniania - redukcji (redoks) Mg 0 + Cl 02 Mg. IICl–I 2 Mg 0 Mg 2+ + 2 e /× 1 Cl 02 + 2 e 2 Cl– Zn 0 Zn 2+ + 2 e /× 1 2 Fe 3+ + 2 I– 2 Fe 2+ + I 02 2 Fe 3+ + 2 e Fe 2+ /× 1 2 I– I 02 + 2 e Zn 0 + 2 HICl–I Zn. IICl–I 2 + H 02 /× 1 2 H+ + 2 e H 02 /× 1 3 Cu 2+ + 2 Al 0 3 Cu 0 + 2 Al 3+ Al 0 Al 3+ + 3 e /× 2 Cu 2+ + 2 e Cu 0 /× 3 2 Mn. VIIO 4– + 5 Sn 2+ + 16 H+ 2 Mn 2+ + 5 Sn 4+ + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 Sn 2+ Sn 4+ + 2 e /× 5

reakcje utleniania - redukcji (redoks) 2 NVO 3– + 3 Cu 0 + 8 H+ 3 Cu 2+ + 2 NIIO + 4 H 2 O NVO 3– + 3 e + 4 H+ NIIO + 2 H 2 O /× 2 Cu 0 Cu 2+ + 2 e /× 3 2 NVO 3– + Cu 0 + 4 H+ Cu 2+ + 2 NIIO 2 + 2 H 2 O NVO 3– + e + 2 H+ NIVO 2 + H 2 O /× 2 Cu 0 Cu 2+ + 2 e /× 1 2 Mn. VIIO 4– + 5 H 2 O–I 2 + 6 H+ 2 Mn 2+ + 5 O 02 + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 H 2 O–I 2 2 H+ + O 02 + 2 e /× 5

reakcje utleniania - redukcji (redoks) 2 Cr 3+ + 3 H 2 O–I 2 + 10 O–IIH– 2 Cr. VIO 42– + 8 H 2 O–II H 2 O–I 2 + 2 e 2 O–IIH– /× 3 Cr 3+ + 8 OH– Cr. VIO 42– + 4 H 2 O + 3 e /× 2 Cr. VI 2 O 72– + 3 H 2 CIII 2 O 4 + 8 H+ 2 Cr 3+ + 6 CIVO 2 + 7 H 2 O Cr. VI 2 O 72– + 6 e + 14 H+ 2 Cr 3+ + 7 H 2 O /× 1 H 2 CIII 2 O 4 2 CIVO 2 + 2 H+ + 2 e /× 3 Pb. IVO 2 + 2 Cl– + 4 H+ Pb 2+ + Cl 02 + 2 H 2 O Pb. IVO 2 + 2 e + 4 H+ Pb 2+ + 2 H 2 O /× 1 2 Cl– Cl 02 + 2 e /× 1

wpływ środowiska na reakcje redoks kwaśne 2 Mn. VIIO 4– + 5 H 2 S–II + 6 H+ 2 Mn 2+ + 5 S 0 + 8 H 2 O Mn. VIIO 4– + 5 e + 8 H+ Mn 2+ + 4 H 2 O /× 2 H 2 S–II 2 H+ + S 0 + 2 e /× 5 obojętne 2 Mn. VIIO 4– + 3 H 2 S–II 2 Mn. IVO 2 + 3 S 0 + 2 OH– + 2 H 2 O Mn. VIIO 4– + 3 e + 2 H 2 O Mn. IVO 2 + 4 OH– /× 2 H 2 S–II + 2 OH– S 0 + 2 H 2 O + 2 e /× 3 zasadowe 2 Mn. VIIO 4– + H 2 S–II + 2 OH– 2 Mn. VIO 42– + S 0 + 2 H 2 O Mn. VIIO 4– + e Mn. VIO 42– /× 2 H 2 S–II + 2 OH– S 0 + 2 H 2 O + 2 e /× 1

reakcje synproporcjonowania (redoks) S 2– + S 0 S 22– 2 S 0 + 2 e S 22– /×(1/2) 2 S 2– S 22– + 2 e /×(1/2) Hg 2+ + Hg 0 Hg 22+ 2 Hg 2+ + 2 e Hg 22+ /×(1/2) 2 Hg 0 Hg 22+ + 2 e /×(1/2) Cl– + Cl. IO– + 2 H+ Cl 02 + H 2 O 2 Cl. IO– + 4 H+ + 2 e Cl 02 + 2 H 2 O /×(1/2) 2 Cl– Cl 02 + 2 e /×(1/2) 5 Br– + Br. VO 3– + 6 H+ 3 Br 02 + 3 H 2 O 2 Br. VO 3– + 12 H+ + 10 e Br 02 + 6 H 2 O /×(1/2) 2 Br– Br 02 + 2 e /×(5/2)

reakcje dysproporcjonowania (redoks) 2 Cu+ Cu 0 + Cu 2+ Cu+ + e Cu 0 /× 1 Cu+ Cu 2+ + e /× 1 Hg 22+ + S 2– Hg. IIS + Hg 0 Hg 22+ + 2 e 2 Hg 0 /×(1/2) Hg 22+ + 2 S 2– 2 Hg. IIS + 2 e /×(1/2) 3 Cl. IO– 2 Cl– + Cl. IO 3– Cl. IO– + 2 H+ + 2 e Cl– + H 2 O /× 2 Cl. IO– + 2 H 2 O Cl. IO 3– + 4 H+ + 2 e /× 1 3 Mn. VIO 42– + 4 H+ 2 Mn. VIIO 4– +Mn. IVO 2 + 2 H 2 O Mn. VIO 42– + 4 H+ + 2 e Mn. IVO 2 + 2 H 2 O /× 1 Mn. VIO 42– Mn. VIIO 4– + e /× 2
- Slides: 14