Todo gs exerce uma PRESSO ocupando um certo














































- Slides: 61


Todo gás exerce uma PRESSÃO, ocupando um certo VOLUME à determinada TEMPERATURA Aos valores da pressão, do volume e da temperatura chamamos de ESTADO DE UM GÁS Assim: V = 5 L T = 300 K P = 1 atm erto Rob n o n ame g A f. Pro

Os valores da pressão, do volume e da temperatura não são constantes, então, dizemos que PRESSÃO (P), VOLUME (V) e TEMPERATURA (T) são VARIÁVEIS DE ESTADO DE UM GÁS P 1 = 1 atm P 2 = 2 atm P 3 = 6 atm V 1 = 6 L V 2 = 3 L V 3 = 3 L T 1 = 300 K T 2 = 300 K T 3 = 900 K Robe n o n e gam A. f o Pr rto

Denominamos de pressão de um gás a colisão de suas moléculas com as paredes do recipiente em que ele se encontra to f. A Pro non e gam er b o R

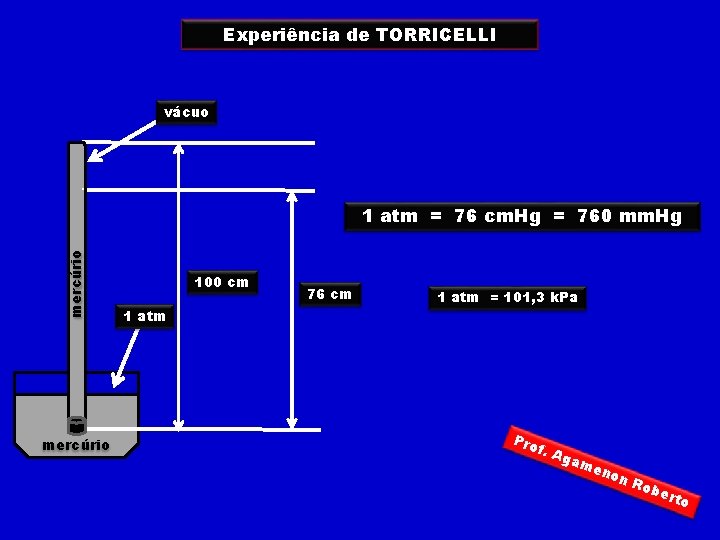
Experiência de TORRICELLI vácuo mercúrio 1 atm = 76 cm. Hg = 760 mm. Hg mercúrio 100 cm 1 atm 76 cm 1 atm = 101, 3 k. Pa Pro f. A gam eno n. R obe rto

É o espaço ocupado pelo gás 1 L = 1000 m. L = 1000 cm 3 Nos trabalhos científicos a unidade usada é a escala absoluta ou Kelvin (K) T = t + 273 rto Robe n o n e Agam. f o r P

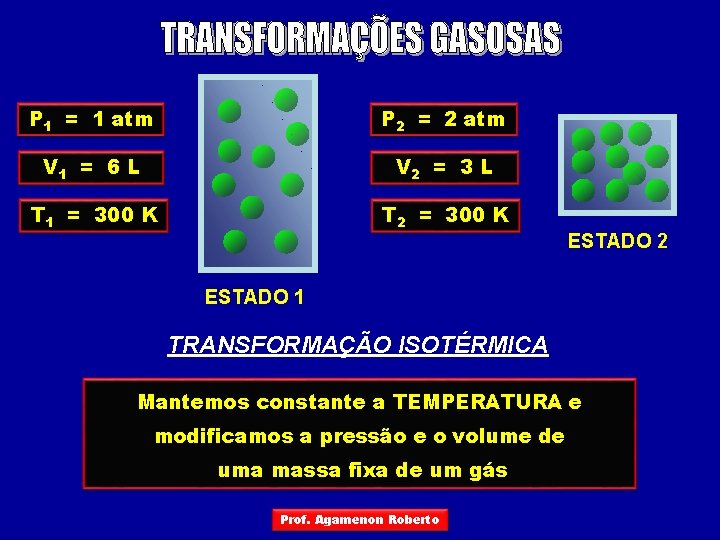
P 1 = 1 atm P 2 = 2 atm V 1 = 6 L V 2 = 3 L T 1 = 300 K T 2 = 300 K ESTADO 2 ESTADO 1 TRANSFORMAÇÃO ISOTÉRMICA Mantemos constante a TEMPERATURA e modificamos a pressão e o volume de uma massa fixa de um gás Prof. Agamenon Roberto

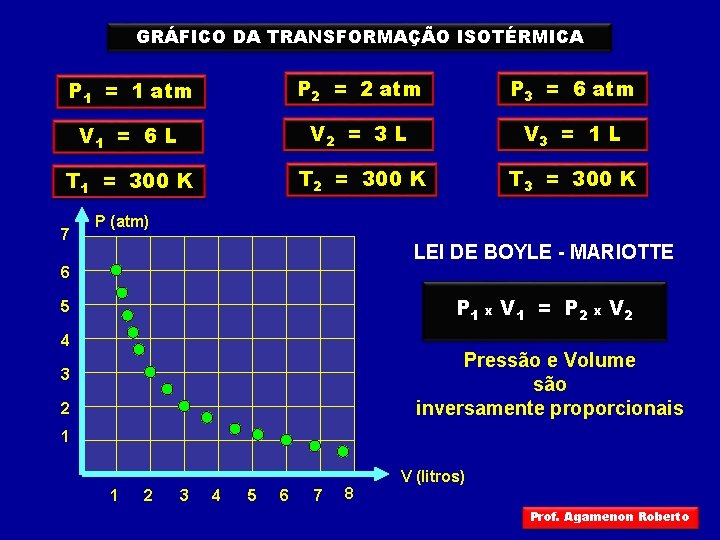
GRÁFICO DA TRANSFORMAÇÃO ISOTÉRMICA P 1 = 1 atm P 2 = 2 atm P 3 = 6 atm V 1 = 6 L V 2 = 3 L V 3 = 1 L T 1 = 300 K T 2 = 300 K T 3 = 300 K 7 P (atm) LEI DE BOYLE - MARIOTTE 6 PP 1 xx V V 1= constante = P 2 x V 2 5 4 Pressão e Volume são inversamente proporcionais 3 2 1 1 2 3 4 5 6 7 8 V (litros) Prof. Agamenon Roberto

TRANSFORMAÇÃO ISOTÉRMICA

P 1 = 1 atm P 2 = 1 atm V 1 = 6 L V 2 = 3 L T 1 = 300 K T 2 = 150 K ESTADO 2 ESTADO 1 TRANSFORMAÇÃO ISOBÁRICA Mantemos constante a PRESSÃO e modificamos a temperatura absoluta e o volume de uma massa fixa de um gás Prof. Agam enon Robe rto

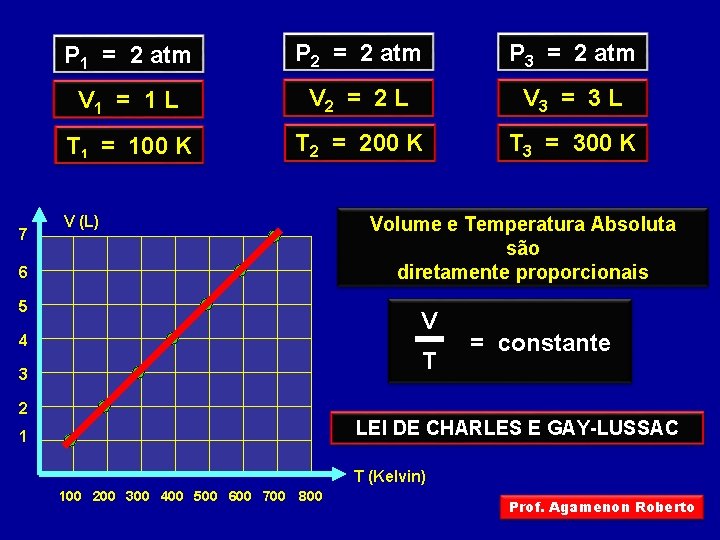
7 P 1 = 2 atm P 2 = 2 atm P 3 = 2 atm V 1 = 1 L V 2 = 2 L V 3 = 3 L T 1 = 100 K T 2 = 200 K T 3 = 300 K V (L) 6 5 Volume e Temperatura Absoluta são diretamente proporcionais V 4 T 3 2 = constante LEI DE CHARLES E GAY-LUSSAC 1 T (Kelvin) 100 200 300 400 500 600 700 800 Prof. Agamenon Roberto

P 1 = 4 atm P 2 = 2 atm V 1 = 6 L V 2 = 6 L T 1 = 300 K T 2 = 150 K ESTADO 1 ESTADO 2 TRANSFORMAÇÃO ISOCÓRICA Mantemos constante o VOLUME e modificamos a temperatura absoluta e a pressão de uma massa fixa de um gás o rt n Robe o gamen Prof. A

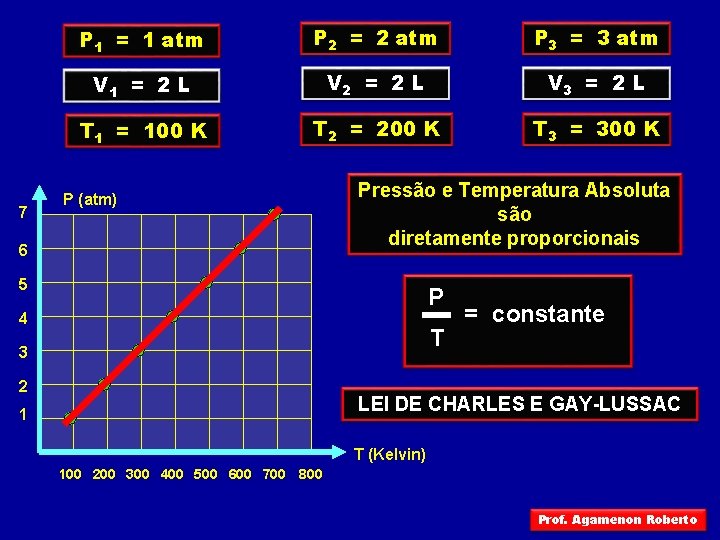
7 P 1 = 1 atm P 2 = 2 atm P 3 = 3 atm V 1 = 2 L V 2 = 2 L V 3 = 2 L T 1 = 100 K T 2 = 200 K T 3 = 300 K P (atm) 6 Pressão e Temperatura Absoluta são diretamente proporcionais 5 P 4 T 3 2 = constante LEI DE CHARLES E GAY-LUSSAC 1 T (Kelvin) 100 200 300 400 500 600 700 800 Prof. Agamenon Roberto


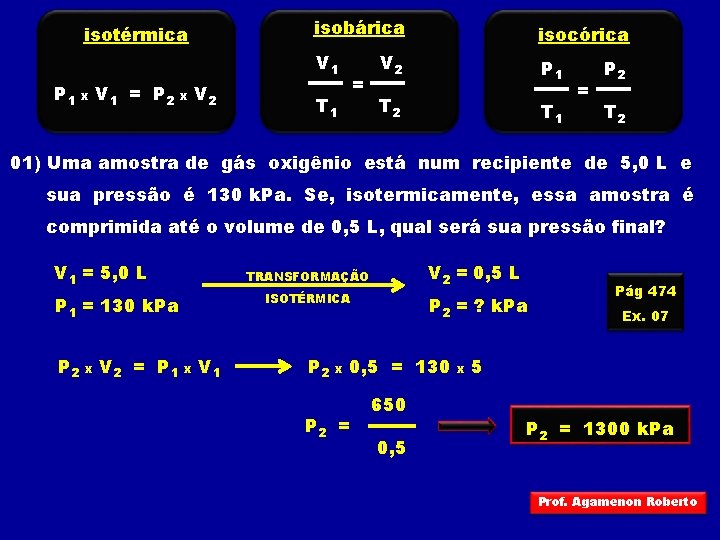
isotérmica P 1 x V 1 = P 2 x V 2 isobárica isocórica V 1 V 2 P 1 T 2 T 1 = P 2 T 2 01) Uma amostra de gás oxigênio está num recipiente de 5, 0 L e sua pressão é 130 k. Pa. Se, isotermicamente, essa amostra é comprimida até o volume de 0, 5 L, qual será sua pressão final? V 1 = 5, 0 L ISOTÉRMICA P 1 = 130 k. Pa P 2 x V 2 = P 1 V 2 = 0, 5 L TRANSFORMAÇÃO x V 1 P 2 x P 2 = ? k. Pa 0, 5 = 130 P 2 = 650 0, 5 x Pág 474 Ex. 07 5 P 2 = 1300 k. Pa Prof. Agamenon Roberto

isotérmica P 1 x V 1 = P 2 x V 2 isobárica isocórica V 1 V 2 P 1 T 2 T 1 = = P 2 T 2 02) Uma amostra de nitrogênio gasoso encontra-se a 27ºC e 1 atm. Se essa amostra sofrer uma transformação isocórica até chegar a 177ºC, qual será a pressão final? T 1 = 27ºC TRANSFORMAÇÃO ISOCÓRICA P 1 = 1 atm T 2 = 177ºC Pág 480 P 2 = ? atm Ex. 24 T 1 = 27ºC + 273 = 300 K T 2 = 177ºC + 273 = 450 K P 1 T 1 = P 2 1 T 2 300 = P 2 450 P 2 = 1, 5 atm Prof. Agamenon Roberto

03) Considere uma determinada quantidade de gás carbônico em um recipiente de 15 m 3, a 1 atm e 57ºC. Se esse gás for transferido para outro recipiente de 20 m 3, qual deverá a temperatura final (em ºC), a fim de que a pressão não se altere? V 1 = 15 m 3 TRANSFORMAÇÃO P 1 = 1 atm ISOBÁRICA T 1 = 57ºC V 2 = 20 m 3 P 2 = 1 atm T 2 = ? ºC Pág 480 Ex. 27 T 1 = 57ºC + 273 = 330 K V 1 T 1 = on gamen Prof. A V 2 15 T 2 330 o Robert = 20 T 2 = 440 K – 273 = 167ºC

04) Um recipiente cúbico de aresta 20 cm contém um gás à pressão de 0, 8 atm. Transfere-se esse gás para um cubo de 40 cm de aresta, mantendo-se constante a temperatura. A nova pressão do gás é de: a) 0, 1 atm. DESAFIO 20 cm b) 0, 2 atm. c) 0, 4 atm. 40 cm T = constante d) 1, 0 atm e) 4, 0 atm. 20 cm 40 cm P = 0, 8 atm V = 8000 20 8 a 3 L 3 P’ = ? atm 3 3 L cm 3 40 64000 64 V’ = a cm 3 P’ x V’ = P x V P’ x 64 = 0, 8 x 8 P’ = 6, 4 P’ = 0, 1 atm 64 Prof. Agamenon Roberto

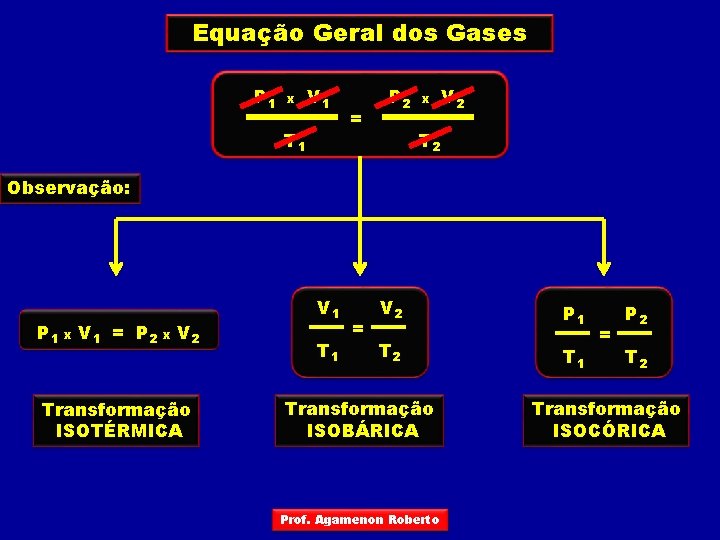
Equação Geral dos Gases P 1 x V 1 T 1 = P 2 x V 2 T 2 Observação: P 1 x V 1 = P 2 x V 2 Transformação ISOTÉRMICA V 1 T 1 = V 2 P 1 T 2 T 1 Transformação ISOBÁRICA Prof. Agamenon Roberto = P 2 Transformação ISOCÓRICA

P 1 x V 1 T 1 P 2 = x V 2 T 2 01) Uma amostra de 1 mol de gás oxigênio ocupa 22, 4 L a 0ºC e 1 atm. Empregue a equação geral dos gases para prever qual será o volume dessa mesma amostra de gás se estivesse submetida a uma temperatura de 273ºC e a uma pressão de 0, 5 atm V 1 = 22, 4 L P 1 = 1 atm P 2 = 0, 5 atm T 1 = 0ºC 1 x = 273 V 2 = T 2 = 273ºC + 273 = 546 K T 2 = 273ºC 22, 4 2 T 1 = 0ºC + 273 = 273 K V 2 = ? L x 0, 5 22, 4 0, 5 x 546 V 2 1 x 22, 4 1 = 0, 5 x V 2 2 V 2 = 89, 6 L Prof. Agamenon Roberto

02) A partir de dados enviados de Vênus por sondas espaciais norte – americanas e soviéticas, pode-se considerar que, em certos pontos da superfície desse planeta, a temperatura é de 327ºC e a pressão atmosférica é de 100 atm. Sabendo-se que na superfície da Terra o volume molar de um gás ideal é 24, 6 L a 27ºC e 1, 00 atm, qual seria o valor desse volume nesses pontos de Vênus? V 1 = ? L P 1 = 100 atm P 2 = 1, 00 atm T 1 = 327ºC 100 x 600 V 1 = 49, 2 100 T 1 = 327ºC + 273 = 600 K V 2 = 24, 6 L T 2 = 27ºC + 273 = 300 K T 2 = 27ºC 1 x 24, 6 300 100 x 2 V 1 = 0, 492 L = 492 m. L 1 x 24, 6 1 Pág. 486 Ex. 11 Prof. Agamenon Roberto

03) Certa massa de gás hidrogênio ocupa um volume de 100 litros a 5 atm e – 73°C. A que temperatura essa massa de hidrogênio irá ocupar um volume de 1000 litros na pressão de 1 atm? a) 400°C. V 1 = 100 L b) 273°C. P 1 = 5 atm c) 100°C. T 1 = – 73°C + 273 = 200 K d) 127°C. V 2 = 1000 L e) 157°C. P 2 = 1 atm P 1 x T 1 V 1 = P 2 x V 2 T 2 = ? 5 x 100 200 T 2 = = 2000 5 1 x 1000 T 2 5 x 2 1 = 1 x 1000 T 2 = 400 K – 273 = 127°C Prof. Agamenon Roberto

Dizemos que um gás se encontra nas CNTP quando: P = 1 atm ou 760 mm. Hg e T = 0 °C ou 273 K É o volume ocupado por um mol de um gás Nas CNTP o volume molar de qualquer gás é de 22, 4 L Pro f. A gam eno n. R obe rto

HIPÓTESE DE AVOGADRO Gás METANO V=2 L P = 1 atm T = 300 K Gás CARBÔNICO Volumes IGUAIS de gases quaisquer, nas mesmas condições de TEMPERATURA e PRESSÃO contêm a mesma quantidade de MOLÉCULAS Prof. Agamenon Roberto

01) Faça uma previsão do volume ocupado por uma amostra de 3, 5 mol de gás nitrogênio nas CNTP? 3, 5 mol 3, 5 Ex. 03 22, 4 L 1 mol 1 Pág. 486 V = 22, 4 V 1 x V = 3, 5 x 22, 4 V = 78, 4 L Prof. Agamenon Roberto

02) A 25ºC e 1 atm o volume molar dos gases é 24, 5 L. Nessas condições de pressão e temperatura, qual será o volume ocupado por 64 g de gás ozônio, O 3? Dado: massa molar do ozônio = 48 g/mol 1 mol 48 64 = 48 g 24, 5 L 64 g V 24, 5 V 48 x V = Pág. 486 Ex. 07 V = 64 x 24, 5 1568 48 V = 32, 67 L Prof. Agamenon Roberto

03) Um balão contém 1, 20 g de nitrogênio gasoso, N 2; outro balão, de mesmo volume, contém 0, 68 g de um gás X. Ambos os balões estão à mesma temperatura e pressão. A massa molecular do gás X será aproximadamente igual a: Dado: N = 14 u. m. a. Pág. 487 a) 16. 1, 20 g de N 2 b) 10. c) 18. d) 30. e) 32. n. N = n X x T, V, P Ex. 15 T, V, P 2 m. N 2 MX 0, 68 g de X 1, 2 = 28 x = 0, 68 m. X 1, 20 MX 28 MX = 28 = x 0, 68 1, 2 0, 68 MX MX = 16 u. m. a. Prof. Agamenon Roberto

Lei do Gás Ideal (Equação de Clapeyron) P x T V = constante P Para 1 mol de gás nas CNTP x V = T P Para 2 mol de gás nas CNTP x Para n mol de gás nas CNTP Generalizando teremos: P x V V = n x = = T x x x R 22, 4 = 0, 082 273 1 V T P 1 22, 4 x 2 273 1 x 22, 4 273 x x n = 2 x 0, 082 = n x 0, 082 T Prof. Agamenon Roberto

P R = 0, 082 atm x L mol x K x V = n R = 62, 3 x R T x mm. Hg mol x x L K R = 8, 315 k. Pa x L mol x K 01) Ao realizar a reação de ferro metálico com uma solução aquosa de ácido clorídrico, um químico recolheu 83, 15 L de gás hidrogênio a 100 k. Pa de pressão e a 27ºC. Qual a quantidade em mols de gás hidrogênio na amostra recolhida? P x 100 n= V = n x x R x T 83, 15 = n 100 x 8, 315 83, 15 x 300 x 8, 315 x 300 n = 3, 33 mols Pág. 491 Ex. 31 Prof. Agamenon Roberto

P R = 0, 082 atm x L mol x K x V = n R = 62, 3 x R T x mm. Hg mol x x L K R = 8, 315 k. Pa x L mol x K 02) Há dúvida se certa amostra de gás é de oxigênio (O 2), nitrogênio (N 2) ou dióxido de carbono (CO 2). Medidas revelaram que a massa da amostra é 0, 70 g, seu volume é 750 m. L, sua pressão é 0, 82 atm e sua temperatura é 27ºC. Com base nessas informações, é possível decidir entre um dos três gases, como sendo o que existe na amostra? Explique. P x V = n 0, 82 n= x x T 0, 75 = n x 0, 82 x 0, 082 x R 0, 082 x 300 n= 0, 75 x 300 n = 0, 025 mol M= m M 0, 70 0, 025 O gás é o N 2 Prof. Agamenon Roberto 0, 025 = 0, 70 M M = 28 u Pág. 491 Ex. 33

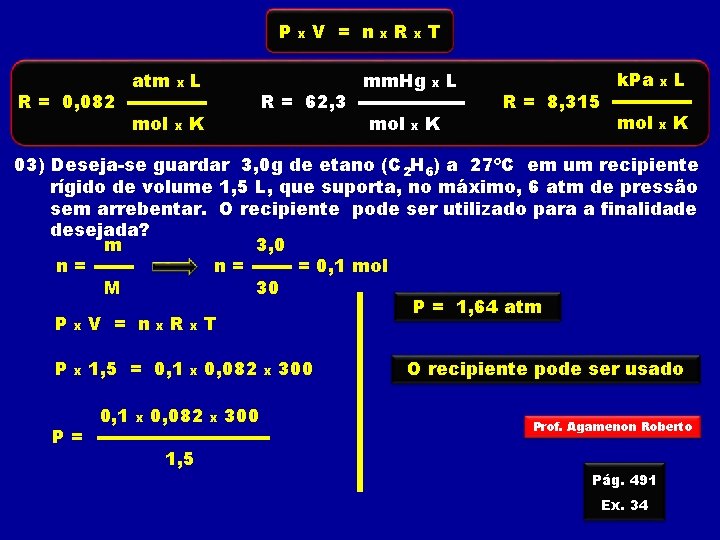
P R = 0, 082 atm x L mol x K x V = n R = 62, 3 x R T x mm. Hg mol x x K L R = 8, 315 k. Pa x L mol x K 03) Deseja-se guardar 3, 0 g de etano (C 2 H 6) a 27ºC em um recipiente rígido de volume 1, 5 L, que suporta, no máximo, 6 atm de pressão sem arrebentar. O recipiente pode ser utilizado para a finalidade desejada? m 3, 0 n= n= = 0, 1 mol M 30 P = 1, 64 atm Px. V = nx. Rx. T P x P= 1, 5 = 0, 1 x x 0, 082 1, 5 0, 082 x 300 O recipiente pode ser usado Prof. Agamenon Roberto Pág. 491 Ex. 34

04) 2, 2 g de um gás estão contidos num recipiente de volume igual a 1, 75 litros, a uma temperatura de 77 o. C e pressão e 623 mm. Hg. Este gás deve ser: Dados: H = 1 u; C = 12 u; O = 16 u; N = 14 u; S = 32 u a) NO. m = 2, 2 g b) H 2 S. V = 1, 75 L c) SO 2. T = 77ºC = 350 K d) CO 2. P = 623 mm. Hg e) NH 3. P 623 x 1, 75 = x V = 2, 2 M M = 44 g/mol x Prof. Agamenon Roberto m M 62, 3 x x R 350 x T M = 2, 2 x 62, 3 x 350 623 x 1, 75 CO 2 = 12 + 32 = 44 g/mol

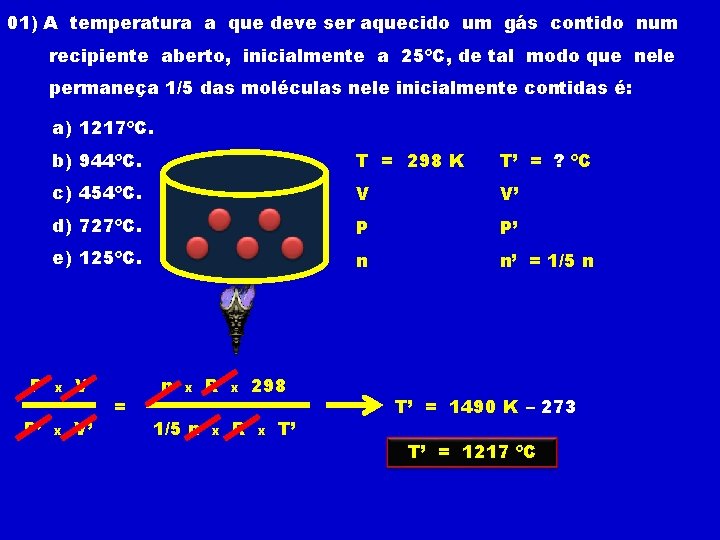
05) A temperatura a que deve ser aquecido um gás contido num recipiente aberto, inicialmente a 25ºC, de tal modo que nele permaneça 1/5 das moléculas nele inicialmente contidas é: a) 1217ºC. b) 944ºC. T = 25ºC 298 K T’ = ? ºC c) 454ºC. V V’ d) 727ºC. P P’ e) 125ºC. n n’ = 1/5 n Prof. Agamenon Roberto P x V P’ x V’ = n x 1/5 n R x x R 298 x T’ T’ = 1490 K – 273 T’ = 1217 ºC

P R = 0, 082 atm x L mol x K x V = n R = 62, 3 x R T x mm. Hg mol x x K L R = 8, 315 k. Pa x L mol x K 06) Um recipiente de 1 L contém gás nitrogênio a 5 atm e um outro recipiente, de 3 L, contém gás oxigênio a 2 atm. Ambos estão na mesma temperatura. a) Em qual deles há mais moléculas? 5 N 2 5 2 x x 1 3 = n n’ x x x 1 = n R R x x x R x T O 2 T 5 T’ 6 = n n’ 2 x n’ = 3 = n’ 6 5 x R n b) Determine a relação entre o número de moléculas de gás? n’ n = 6 5 Prof. Agamenon Roberto Pág. 491 Ex. 38 x T’

Mistura de Gases Estas misturas funcionam como se fosse um único gás PA V A TA n A PB VB TB n. B P V T Podemos estudar a mistura gasosa ou relacionar a mistura gasosa com os gases nas condições iniciais pelas expressões P. V = n. T. R. T gamen Prof. A o ert on Rob P x V T = P A x VA TA + P B x VB TB

01) Considere a mistura de 0, 5 mol de CH 4 e 1, 5 mol de C 2 H 6, contidos num recipiente de 30 L a 300 K. A pressão total, em atm, é igual a: a) 1, 64 atm. b) 0, 82 atm. c) 0, 50 atm. d) 0, 41 atm. e) 0, 10 atm. P. V = n. T. R. T P. 30 = 2. 0, 082. 300 P = 2. 0, 82. 30 30 P = 1, 64 atm Prof. Agamenon Roberto

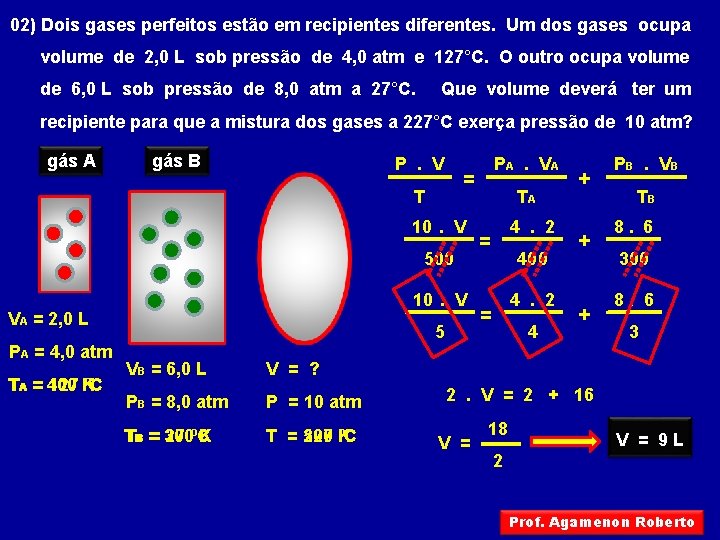
02) Dois gases perfeitos estão em recipientes diferentes. Um dos gases ocupa volume de 2, 0 L sob pressão de 4, 0 atm e 127°C. O outro ocupa volume de 6, 0 L sob pressão de 8, 0 atm a 27°C. Que volume deverá ter um recipiente para que a mistura dos gases a 227°C exerça pressão de 10 atm? gás A gás B P. V = T g 10. V 500 10. V VA = 2, 0 L PA = 4, 0 atm TAA = 400 127 K ºC 5 VB = 6, 0 L V = ? PB = 8, 0 atm P = 10 atm TBB = 300 27 ºC K T = 500 227 K ºC PA. V A TA 4. 2 = 400 4. 2 = 4 + + + PB. V B TB 8. 6 300 8. 6 3 2. V = 2 + 16 V = 18 V = 9 L 2 Prof. Agamenon Roberto

Pressão Parcial de um Gás A P P x T V x = Gás B V = n. T PA x x VA TA R x + T PB VB x TB Mantendo o VOLUME e a TEMPERATURA P’A é a pressão parcial do gás A P’A x V = n. A P’A x V T = x R PA x T VA P’B é a pressão parcial do gás B P’B x V = n. B P’B x V T = Lei de DALTON: P = PA + PB Prof. Agamenon Roberto x R PB x T VB

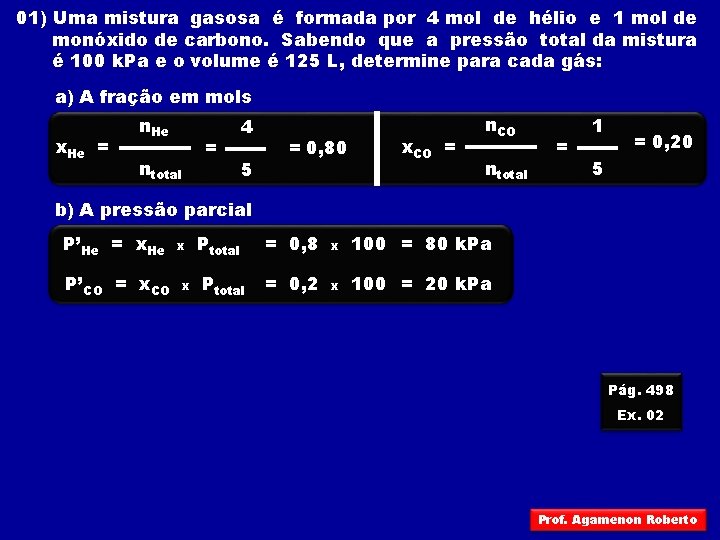
01) Uma mistura gasosa é formada por 4 mol de hélio e 1 mol de monóxido de carbono. Sabendo que a pressão total da mistura é 100 k. Pa e o volume é 125 L, determine para cada gás: a) A fração em mols x. He = n. He ntotal = 4 5 = 0, 80 x. CO = n. CO ntotal = 1 = 0, 20 5 b) A pressão parcial P’He = x. He P’CO = x. CO x x Ptotal = 0, 8 x 100 = 80 k. Pa Ptotal = 0, 2 x 100 = 20 k. Pa Pág. 498 Ex. 02 Prof. Agamenon Roberto

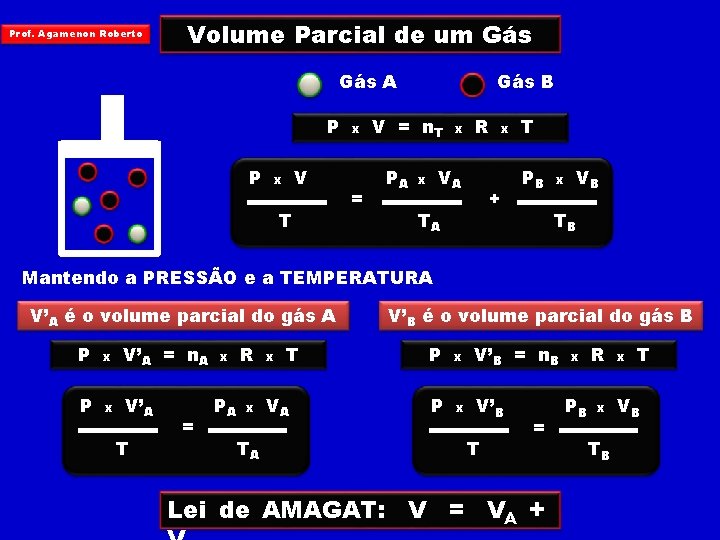
Prof. Agamenon Roberto Volume Parcial de um Gás A P P V x T x = Gás B V = n. T PA x R VA x x + TA T PB x VB TB Mantendo a PRESSÃO e a TEMPERATURA V’A é o volume parcial do gás A P x V’A = n. A P x V’A T = x R PA x T VA V’B é o volume parcial do gás B P x V’B = n. B P x V’B T = Lei de AMAGAT: V = VA + x R PB x T VB

01) Uma mistura gasosa é formada por 4 mol de hélio e 1 mol de monóxido de carbono. Sabendo que a pressão total da mistura é 100 k. Pa e o volume é 125 L, determine para cada gás: a) A fração em mols x. He = n. He ntotal = 4 5 = 0, 80 x. CO = n. CO ntotal = 1 = 0, 20 5 b) A pressão parcial RESPONDIDA ANTES c) O volume parcial V’CO = x. CO x Vtotal = 0, 2 x 125 = 25 L V’He = x. He x Vtotal = 0, 8 x 125 = 100 L Pág. 498 Ex. 02 Prof. Agamenon Roberto

Densidade dos Gases Gás hidrogênio (H 2) Gás carbônico (CO 2) O gás H 2 é menos denso que o ar atmosférico O gás CO 2 é mais denso que o ar atmosférico Prof. Agamenon Roberto

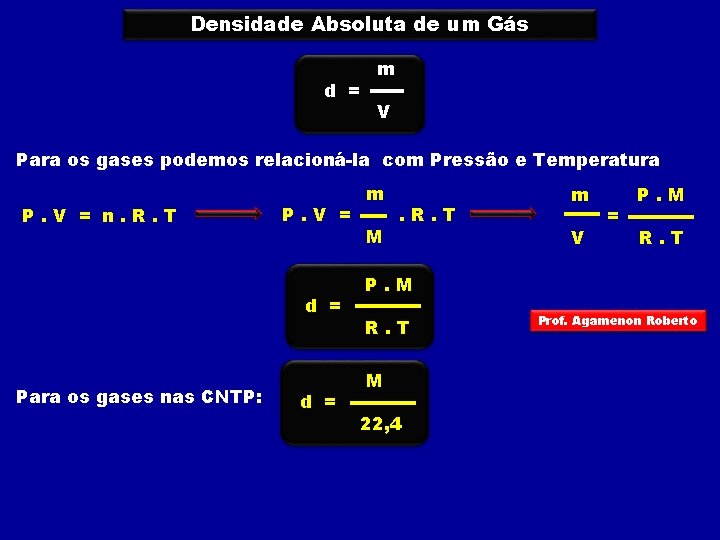
Densidade Absoluta de um Gás d = m V Para os gases podemos relacioná-la com Pressão e Temperatura P. V = n. R. T P. V = d = Para os gases nas CNTP: d = m M . R. T m V = P. M R. T M 22, 4 Prof. Agamenon Roberto

01) A densidade absoluta do gás oxigênio (O 2) a 27ºC e 3 atm de pressão é: Dado: O = 16 u d = x g/L a) 16 g/L. T = 27°C + 273 = 300 K b) 32 g/L. P = 3 atm c) 3, 9 g/L. MO 2 = 32 u d) 4, 5 g/L. R = 0, 082 atm. L / mol. K e) 1, 0 g/L. d = P x M R x T = 3 x 0, 082 32 x 300 = 96 24, 6 d = 3, 9 g/L Prof. Agamenon Roberto

02) A densidade de um gás é 1, 96 g/L medida nas CNTP. A massa molar desse gás é: a) 43, 90 g / mol. b) 47, 89 g / mol. c) 49, 92 g / mol. d) 51, 32 g / mol. e) 53, 22 g / mol. d = 1, 96 M 22, 4 M = 1, 96 x 22, 4 M = 43, 90 g/mol Prof. Agamenon Roberto

DENSIDADE RELATIVA É obtida quando comparamos as densidades de dois gases, isto é, quando dividimos as densidades dos gases, nas mesmas condições de temperatura e pressão Gás A P d. A = d. A d. B = P R x x R MA x x MA T Gás B d. B = T R x P x x T MB d A, B P R = d A , Ar = x x MB T MA MB MA 28, 96

01) A densidade do gás carbônico em relação ao gás metano é igual a: Dados: H = 1 u; C = 12 u; O = 16 u a) 44. b) 16. d CO , CH = 2 4 c) 2, 75. d) 0, 25 e) 5, 46 M CO 2 = 12 + 2 M CH 4 = 12 + 4 M 44 CO 2 M 16 CH 4 x = 2, 75 16 = 44 u. m. a. x 1 = 16 u. m. a. Prof. Agamenon Roberto

02) A densidade relativa do gás oxigênio (O 2) em relação ao ar atmosférico é: Dado: O = 16 u a) 16. b) 2. d. O 2 , Ar = M 32 O 2 28, 96 = 1, 1 c) 0, 5. d) 1, 1. e) 1, 43 Pro non f. A e gam rto e Rob

DIFUSÃO E EFUSÃO Quando abrimos um recipiente contendo um perfume, após certo tempo sentimos o odor do perfume Isso ocorre porque algumas moléculas do perfume passam para a fase gasosa e se dispersam no ar chegando até nossas narinas Esta dispersão recebe o nome de DIFUSÃO Prof. Agamenon Roberto

DIFUSÃO E EFUSÃO Uma bola de festas com um certo tempo murcha, isto ocorre porque a bola tem poros e o gás que se encontrava dentro da bola sai por estes poros Prof. Agamenon Roberto Este fenômeno denomina-se de EFUSÃO


A velocidade de difusão e de efusão é dada pela LEI DE GRAHAM que diz: A velocidade de difusão e de efusão de um gás é inversamente proporcional à raiz quadrada de sua densidade Nas mesmas condições de temperatura e pressão a relação entre as densidades é igual à relação entre suas massas molares, então: v. A v. B = d. B v. A d. A v. B = MB MA Prof. Agamenon Roberto

01) ( Mackenzie – SP ) Um recipiente com orifício circular contém os gases y e z. O peso molecular do gás y é 4, 0 e o peso molecular do gás z é 36, 0. A velocidade de escoamento do gás y será maior em relação à do gás z: a) 3 vezes b) 8 vezes c) 9 vezes My = 4 u Mz = 36 u d) 10 vezes vy e) 12 vezes vz = vy = 3 x Mz vy My vz = 3 36 9 4 vz Prof. Agamenon Roberto

01) A velocidade de difusão do gás hidrogênio é igual a 27 km/min, em determinadas condições de pressão e temperatura. Nas mesmas condições, a velocidade de difusão do gás oxigênio em km/h é de: Prof. Agamenon Roberto Dados: H = 1 g/mol; O = 16 g/mol. a) 4 km/h. v. H b) 108 km/h. v. O c) 405 km/h. d) 240 km/h. v. H 2 e) 960 km/h. v. O 2 27 x v. O 60 2 = 4 = 27 km/min = 27 km / (1/60) h 2 = x km/h 2 MO 2 = v. O 27 = 60 v. O MH 2 2 x 1620 4 2 = 405 km/h = 32 16 2

REVISÃO

01) A temperatura a que deve ser aquecido um gás contido num recipiente aberto, inicialmente a 25ºC, de tal modo que nele permaneça 1/5 das moléculas nele inicialmente contidas é: a) 1217ºC. b) 944ºC. T = 25ºC 298 K T’ = ? ºC c) 454ºC. V V’ d) 727ºC. P P’ e) 125ºC. n n’ = 1/5 n P x V P’ x V’ = n x 1/5 n R x x R 298 x T’ T’ = 1490 K – 273 T’ = 1217 ºC

02. (IFET) Dois balões de igual capacidade, A e B, mantidos na mesma temperatura, apresentam massas iguais de H 2(g) e O 2(g). A pressão do H 2(g) no balão A é igual a 1, 6 atm. Assinale a alternativa abaixo que corresponde a pressão que o O 2 (g) exerce no balão B. Dados: M(H 2) = 2 g/mol e M(O 2) = 32 g/mol. a) 0, 1 atm. b) 0, 5 atm. c) 1, 0 atm. d) 1, 6 atm. e) 2, 0 atm. PO 2 x VA = VB A PH 2 = 1, 6 atm 1, 6 x V PO 2 x V m. H 2 n. H 2 = 1, 6 H 2 M 2 H 2 x = m. O 2 n n. OO 2 2 M 32 O 2 m H 2 TA = T B =m B Po 2 = ? atm O 2 n. H 2 x R x T n. O 2 x R x T PO 2 = 3, 2 32 PO 2 = 0, 1 atm

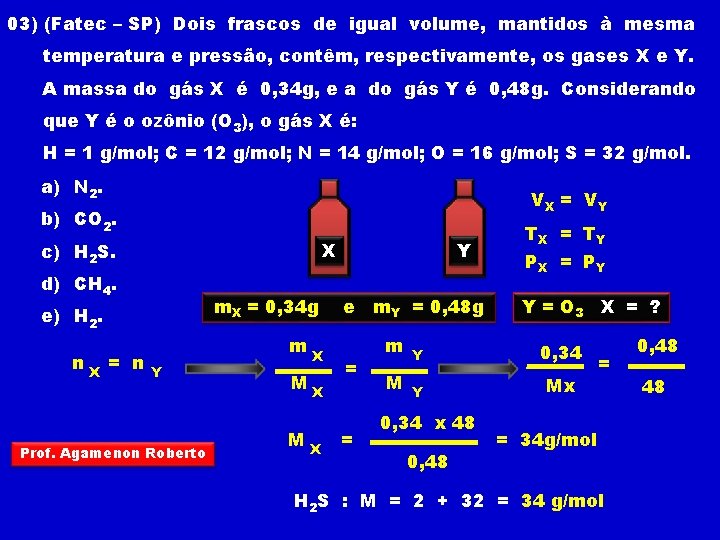
03) (Fatec – SP) Dois frascos de igual volume, mantidos à mesma temperatura e pressão, contêm, respectivamente, os gases X e Y. A massa do gás X é 0, 34 g, e a do gás Y é 0, 48 g. Considerando que Y é o ozônio (O 3), o gás X é: H = 1 g/mol; C = 12 g/mol; N = 14 g/mol; O = 16 g/mol; S = 32 g/mol. a) N 2. VX = V Y b) CO 2. X c) H 2 S. d) CH 4. m. X = 0, 34 g e) H 2. n. X = n m Y Prof. Agamenon Roberto X MX MX Y e m. Y = 0, 48 g = = TX = T Y PX = P Y Y = O 3 X = ? m Y 0, 34 M Y Mx 0, 34 x 48 0, 48 = = 34 g/mol H 2 S : M = 2 + 32 = 34 g/mol 0, 48 48

04) Um estudante de química armazenou em um cilindro de 10 L, 6 g de hidrogênio e 28 g de hélio. Sabendo-se que a temperatura é de 27°C no interior do cilindro. Calcule: Dados: H 2 = 2 g/mol; He = 4 g/mol I. O número de mol do H 2 e do He. 6 n. H 2 = 3 mol n. He = 28 4 = 7 mol II. A pressão total da mistura P x V = n. T x R x T P x 10 = 10 x 0, 082 x 300 P = 24, 6 atm III. A pressão parcial de cada componente da mistura P’H 2 x V = n. H 2 x P’H 2 x 10 = 3 0, 082 x P’H 2 = 7, 38 atm R x T x 300 P’He x V = n. He x P’He x 10 = 7 0, 082 x R x T x 300 P’He = 17, 22 atm Prof. Agamenon Roberto

05) Uma mistura gasosa contém 4 mols de gás hidrogênio, 2 mols de gás metano exercem uma pressão de 4, 1 atm, submetidos a uma temperatura de 27°C. Calcule os volumes parciais destes dois gases. n. H 2 = 4 mols n. CH 4 = 2 mols P = 4, 1 atm T = 300 27° C K P X V H 2 = n H 2 4, 1 X V’H 2 4 Rx. T = 4 x 0, 082 x 300 4, 1 X V’CH 4 = 2 x 0, 082 x 300 x 0, 082 V’H 2 = 24 L V’ H 2 = ? V’ CH 4 = ? x 4, 1 x 300 2 x V’CH 4 = 12 L 0, 082 x 300 4, 1 Prof. Agamenon Roberto

06) Uma mistura gasosa contém 6 mols de gás hidrogênio, 2 mols de gás metano e ocupa um recipiente de 82 L. Calcule os volumes parciais destes dois gases. n H 2 = 6 mols n CH 4 Podemos relacionar, também, o volume parcial com o volume total da mistura pela = 2 mols expressão abaixo V = 82 L V’ A = x A x H 2 = x CH 4 = 6 8 2 8 = 0, 75 = 0, 25 V’H 2 = 0, 75 V’CH 4 = 0, 25 x x x V 82 = 61, 5 L 82 = 20, 5 L Prof. Agamenon Roberto