Perchalcune reazioni decorrono spontaneamentefino alla conversione comple dei









![a. A + b. B c. C + d. D c ·[D]d [C] DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-30.jpg)
![a. A + b. B c. C + d. D c ·[D] d C a. A + b. B c. C + d. D c ·[D] d C](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-31.jpg)
![a. A + b. B c. C + d. D c ·[D]d [C] DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-32.jpg)
![a. A + b. B c. C + d. D c ·[D]d [C] DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-33.jpg)

- Slides: 41

Perchéalcune reazioni decorrono spontaneamentefino alla conversione comple dei reagenti nei prodotti mentre altre decorrono spontaneamente fino a raggiungere uno stato di equilibrio ?

I due principî della termodinamica 1° L’energia di un sistema termodinamico isolato non si crea né si distrugge ma si trasforma passando da una forma a un'altra 2° In ogni processo spontaneo l’entropia dell’universo aumenta

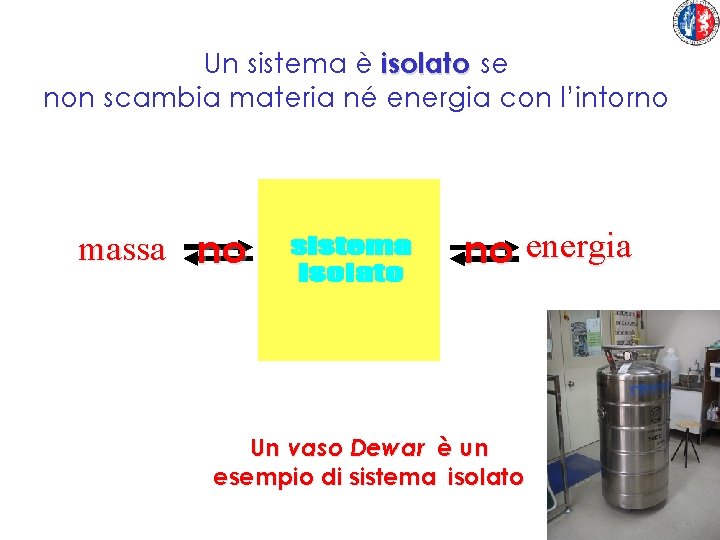
Un sistema è isolato se non scambia materia né energia con l’intorno massa no no energia Un vaso Dewar è un esempio di sistema isolato

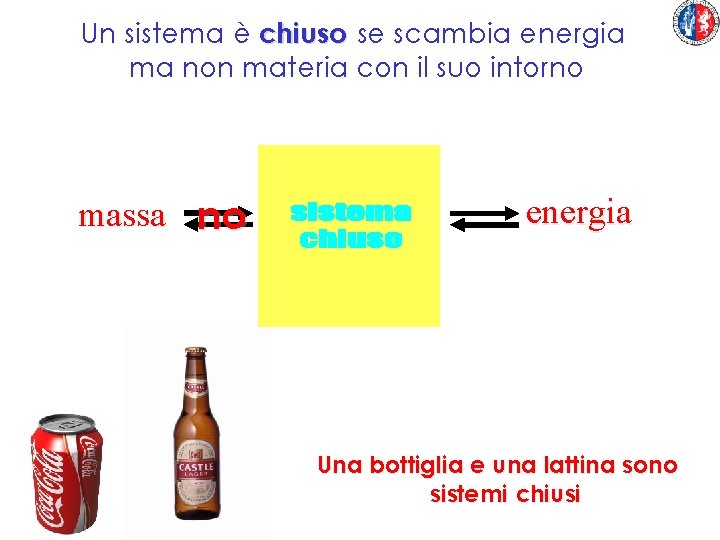
Un sistema è chiuso se scambia energia ma non materia con il suo intorno massa no energia Una bottiglia e una lattina sono sistemi chiusi

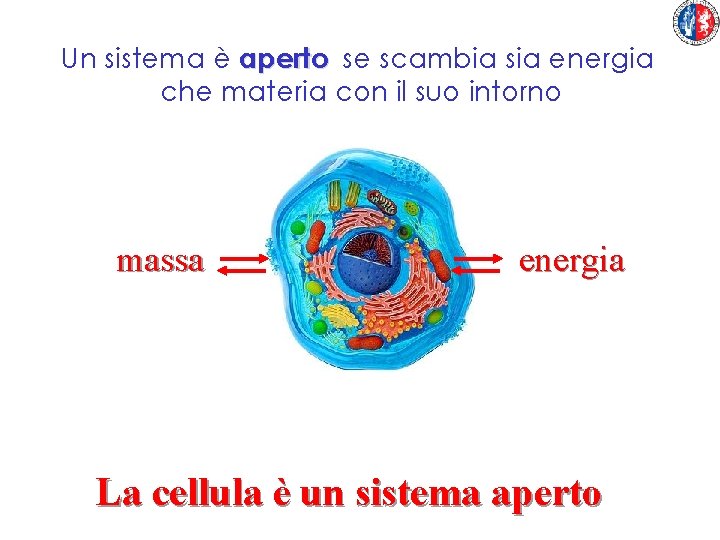
Un sistema è aperto se scambia sia energia che materia con il suo intorno massa energia La cellula è un sistema aperto

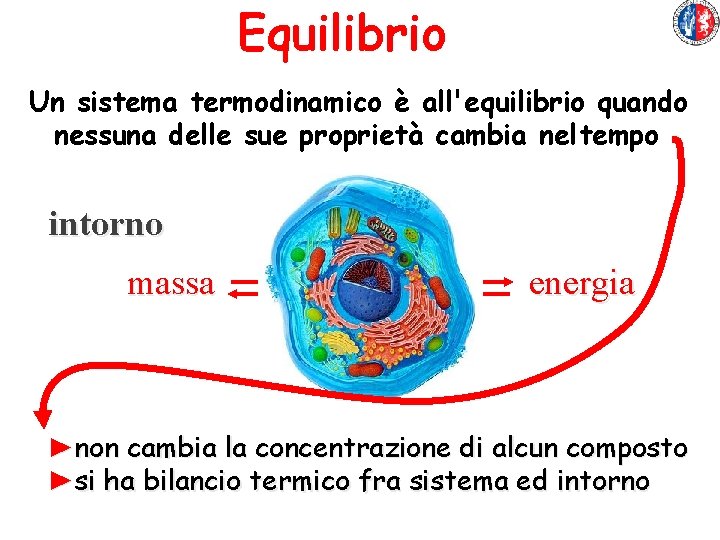
Equilibrio Un sistema termodinamico è all'equilibrio quando nessuna delle sue proprietà cambia nel tempo intorno massa energia ►non cambia la concentrazione di alcun composto ►si ha bilancio termico fra sistema ed intorno

Primo principio della termodinamica L’energia in un sistema termodinamico isolato non si crea né si distrugge ma si trasforma passando da una forma a un'altra

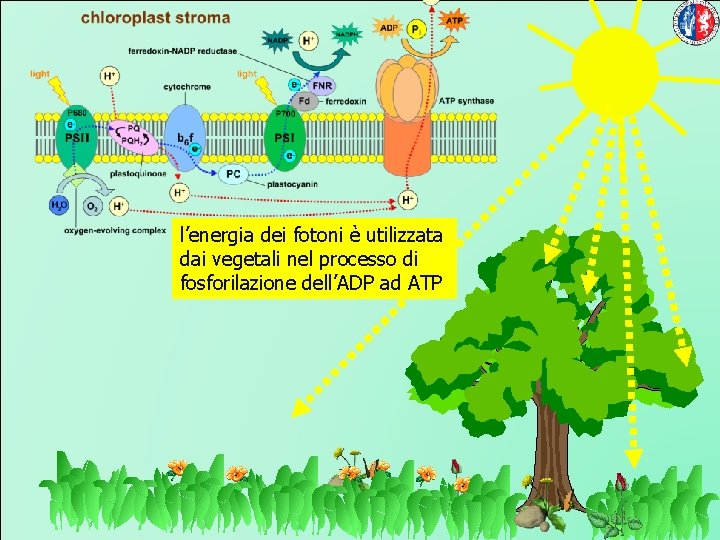
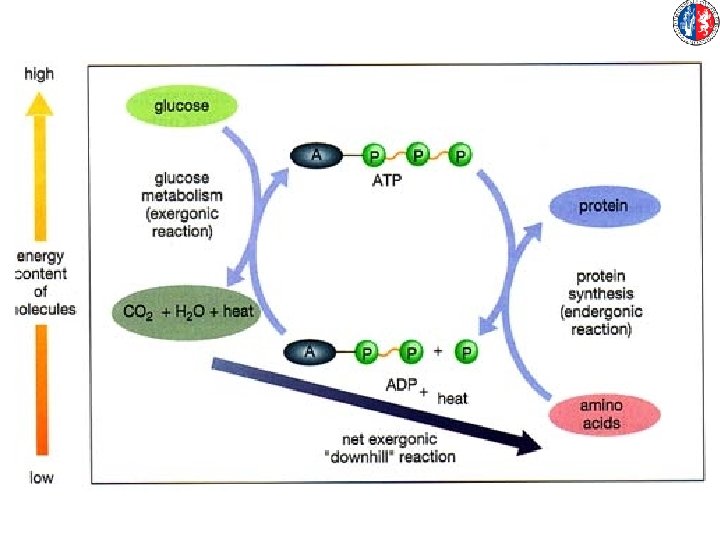
l’energia dei fotoni è utilizzata dai vegetali nel processo di fosforilazione dell’ADP ad ATP

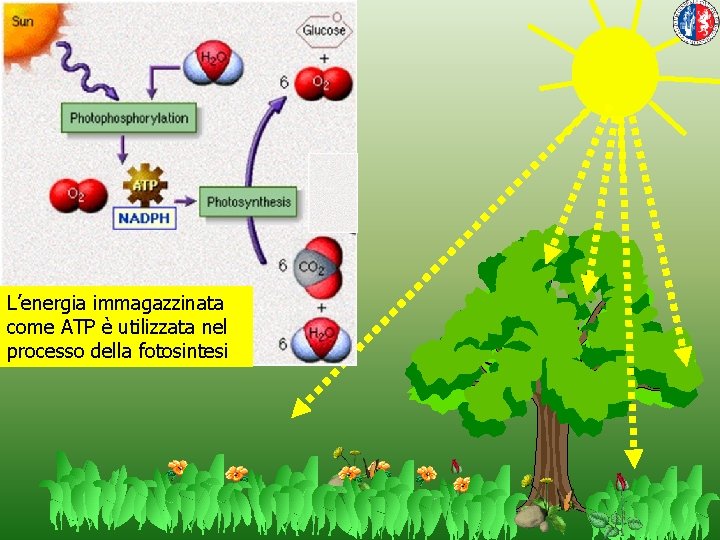
L’energia immagazzinata come ATP è utilizzata nel processo della fotosintesi

Gli animali erbivori traggono dai vegetali l’energia necessaria per la sintesi delle macromolecole e per compiere lavoro. Anche l’uomo converte l’energia chimica degli alimenti in lavoro ed in nuove strutture molecolari

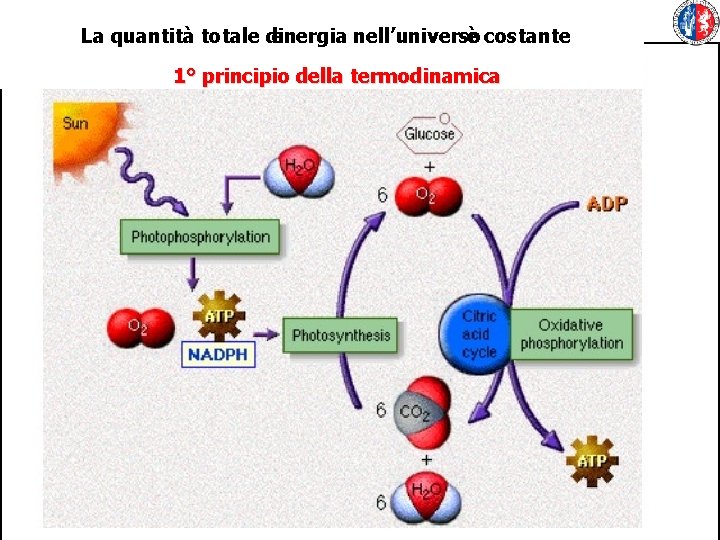
La quantità totale di energia nell’universo è costante 1° principio della termodinamica

Secondo principio della termodinamica I processi spontanei sono irreversibili Tomba del tuffatore (480 -470 a. C. ) Tempa del prete – Paestum

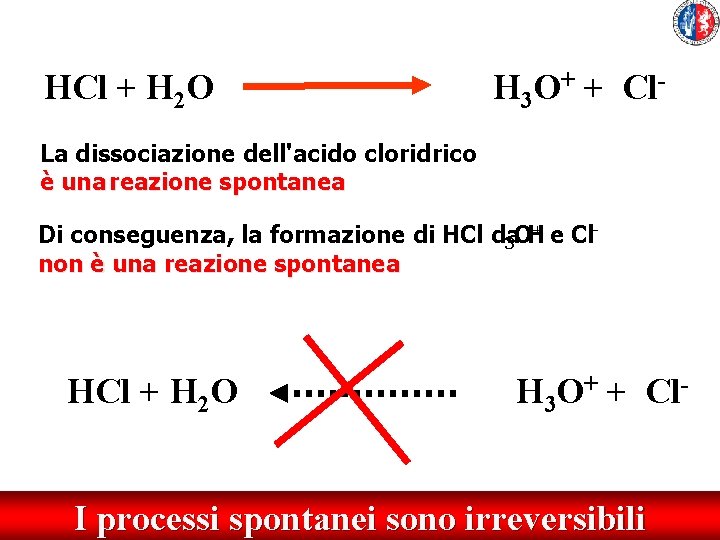
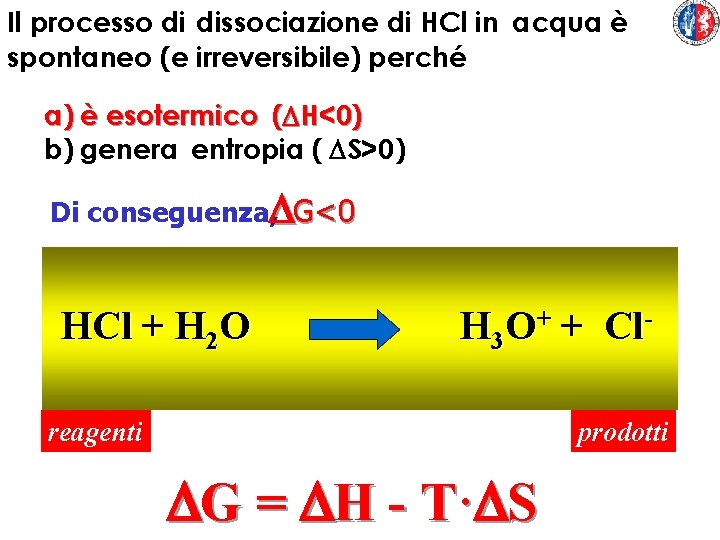
HCl + H 2 O H 3 O+ + Cl- La dissociazione dell'acido cloridrico è una reazione spontanea + Di conseguenza, la formazione di HCl da 3 OH e Cl non è una reazione spontanea HCl + H 2 O H 3 O+ + Cl- I processi spontanei sono irreversibili

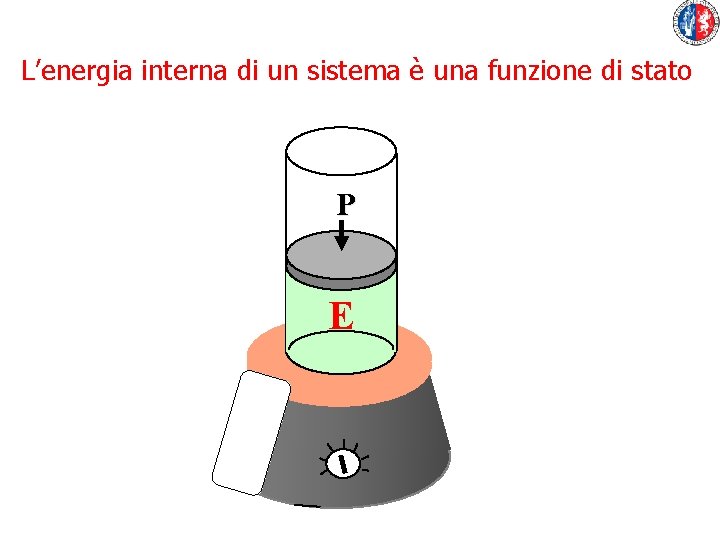
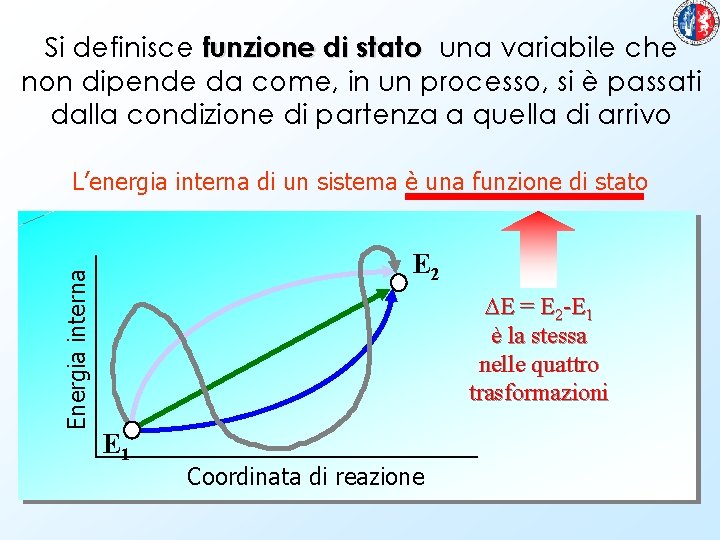
L’energia interna di un sistema è una funzione di stato P E

Si definisce funzione di stato una variabile che non dipende da come, in un processo, si è passati dalla condizione di partenza a quella di arrivo Energia interna L’energia interna di un sistema è una funzione di stato E 2 DE = E 2 -E 1 è la stessa nelle quattro trasformazioni E 1 Coordinata di reazione

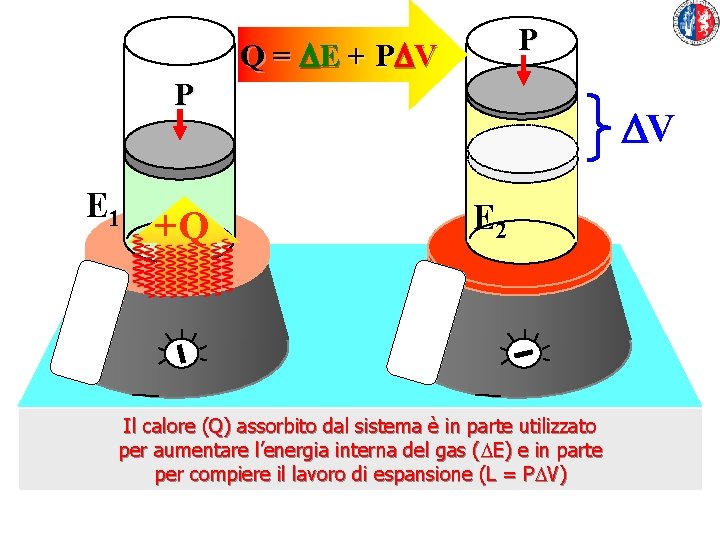
P Q = DE + PDV P E 1 +Q DV E 2 Il calore (Q) assorbito dal sistema è in parte utilizzato per aumentare l’energia interna del gas (DE) e in parte per compiere il lavoro di espansione (L = PDV)

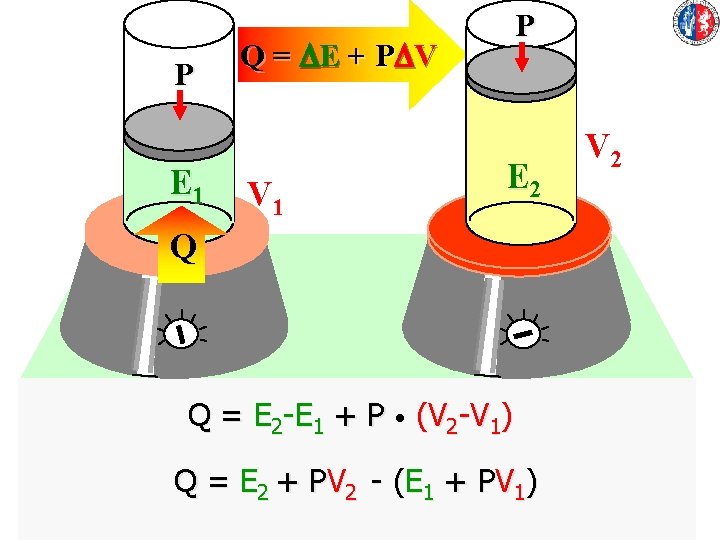
P E 1 P Q = DE + PDV V 1 E 2 Q Q = E 2 -E 1 + P • (V 2 -V 1) Q = E 2 + P V 2 - ( E 1 + P V 1 ) V 2

Definendo una nuova funzione di stato: l’entalpia H dalla equazione. . . Q = E 2 + PV 2 - (E 1 + PV 1) deriva che il calore scambiato, a pressione costante, fra il sistema e il suo intorno è: Q = H 2 - H 1 = DH DH > 0 DH < 0 processo endotermico processo esotermico

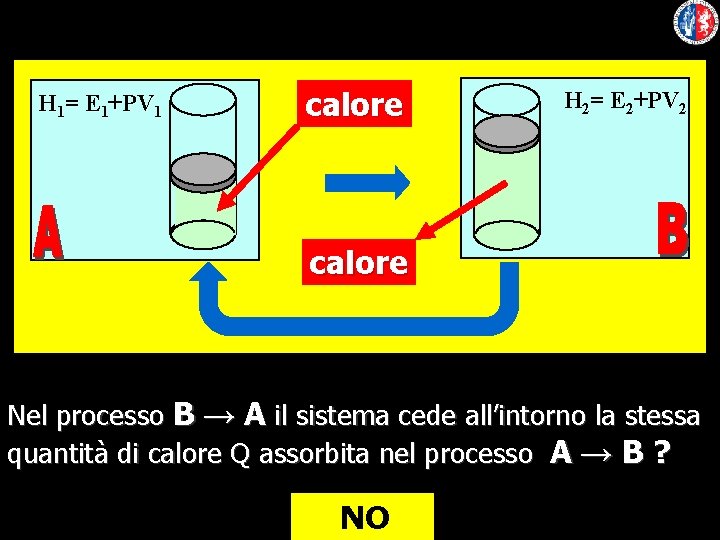
H 1= E 1+PV 1 calore H 2= E 2+PV 2 calore Nel processo B → A il sistema cede all’intorno la stessa quantità di calore Q assorbita nel processo A → B ? NO

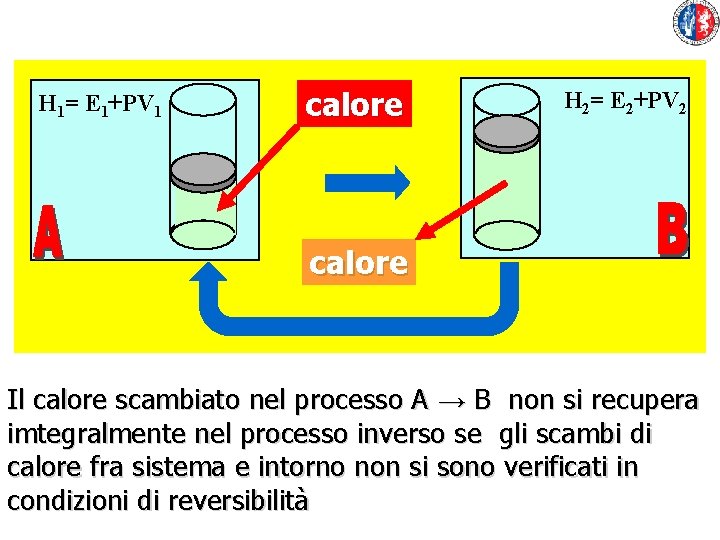
H 1= E 1+PV 1 calore H 2= E 2+PV 2 calore Il calore scambiato nel processo A → B non si recupera imtegralmente nel processo inverso se gli scambi di calore fra sistema e intorno non si sono verificati in condizioni di reversibilità

Q S = T Si definisceentropiadi un sistema il rapporto fra il suo contenuto termico e la sua temperaturaassoluta

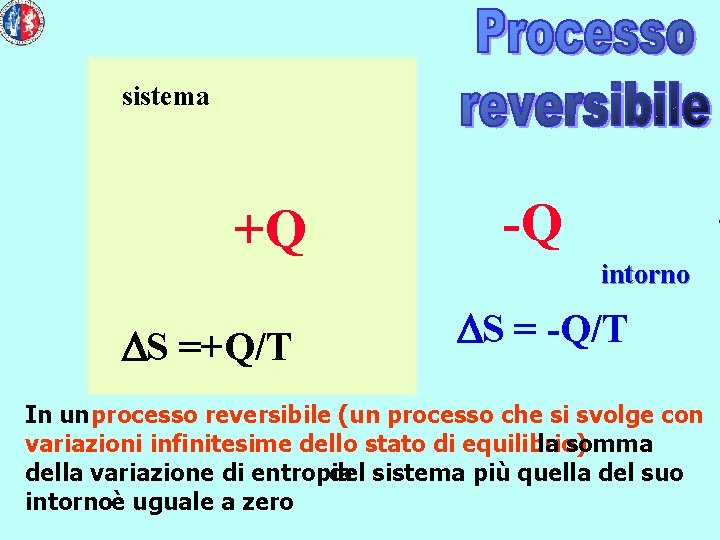
sistema +Q DS =+Q/T -Q intorno DS = -Q/T In un processo reversibile (un processo che si svolge con variazioni infinitesime dello stato di equilibrio) la somma della variazione di entropia del sistema più quella del suo intornoè uguale a zero

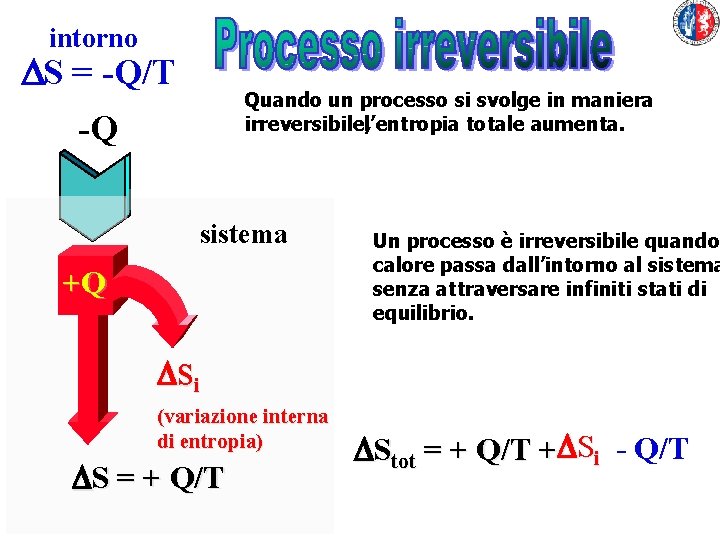
intorno DS = -Q/T Quando un processo si svolge in maniera irreversibile, l’entropia totale aumenta. -Q sistema +Q Un processo è irreversibile quando calore passa dall’intorno al sistema senza attraversare infiniti stati di equilibrio. D si (variazione interna di entropia) DS = + Q/T DStot = + Q/T +DSi - Q/T

La funzione di stato ENERGIA LIBERA è definita come G=H- . TS Essendo H , S , T funzioni di stato, anche G è una funzione di stato. In un processo isotermo in cui varîno sia H che S: G 2 -G 1 = H 2 -H 1 - T· (S 2 -S 1) DG = DH - T·DS

Il processo di dissociazione di HCl in acqua è spontaneo (e irreversibile) perché a) è esotermico (DH<0) b) genera entropia ( DS>0 ) Di conseguenza, DG<0 HCl + H 2 O H 3 O+ + Cl- reagenti prodotti DG = DH - T·DS

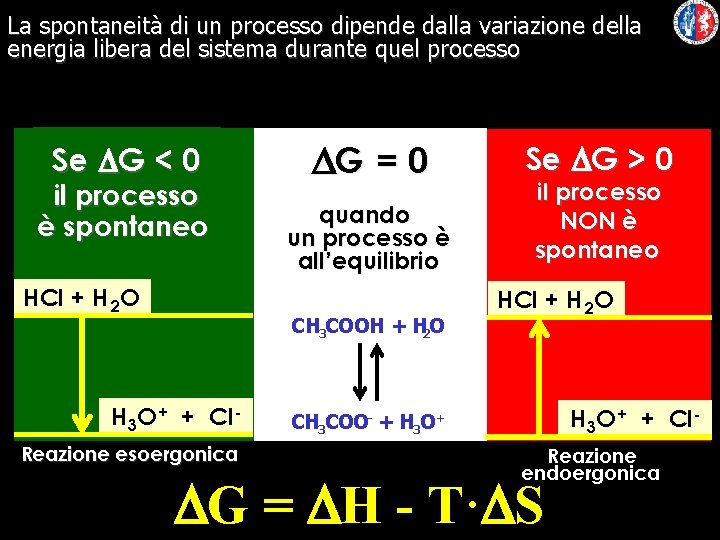
La spontaneità di un processo dipende dalla variazione della energia libera del sistema durante quel processo Se DG < 0 il processo è spontaneo HCl + H 2 O DG = 0 quando un processo è all’equilibrio CH 3 COOH + H 2 O H 3 O + + Cl Reazione esoergonica Se DG > 0 il processo NON è spontaneo HCl + H 2 O H 3 O + + Cl - CH 3 COO- + H 3 O+ Reazione endoergonica DG = DH - T·DS


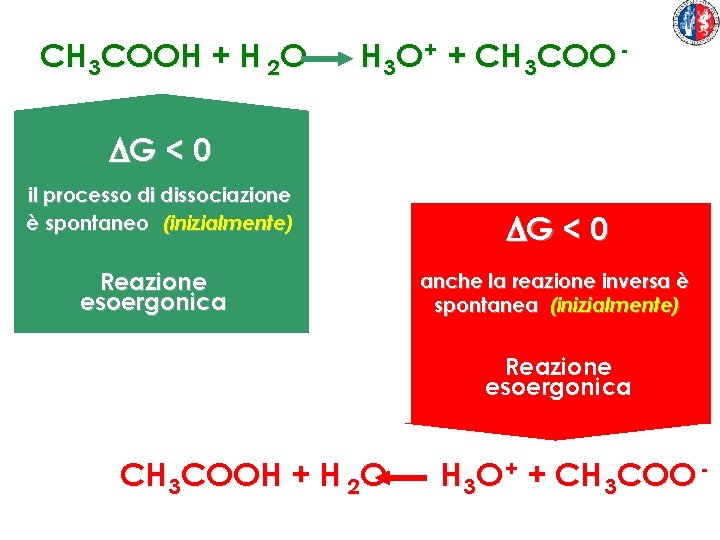
CH 3 COOH + H 2 O H 3 O + + CH 3 COO - DG < 0 il processo di dissociazione è spontaneo (inizialmente) Reazione esoergonica DG < 0 anche la reazione inversa è spontanea (inizialmente) Reazione esoergonica CH 3 COOH + H 2 O H 3 O + + CH 3 COO -

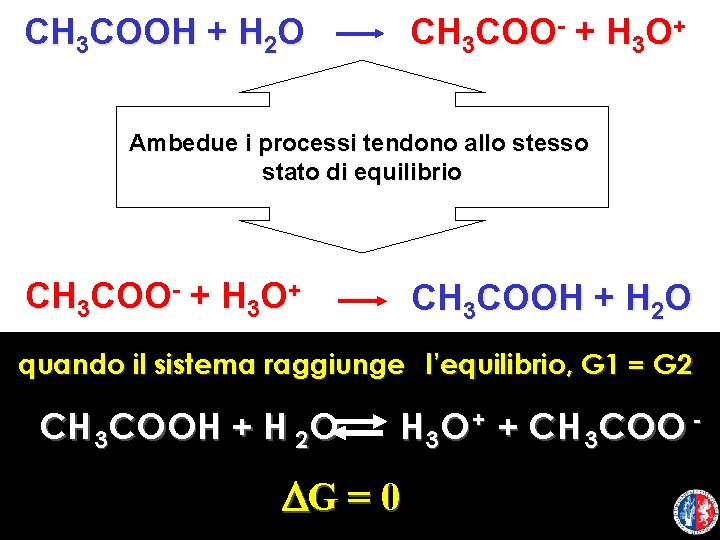
CH 3 COOH + H 2 O CH 3 COO- + H 3 O+ Ambedue i processi tendono allo stesso stato di equilibrio CH 3 COO- + H 3 O+ CH 3 COOH + H 2 O quando il sistema raggiunge l’equilibrio, G 1 = G 2 CH 3 COOH + H 2 O H 3 O + + CH 3 COO - DG = 0
![a A b B c C d D c Dd C DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-30.jpg)
a. A + b. B c. C + d. D c ·[D]d [C] DG = DGo + RT·ln [A]a ·[B]b Data una reazione di equilibrio generica, il DG è funzione delle concentrazioni di reagenti e prodotti
![a A b B c C d D c D d C a. A + b. B c. C + d. D c ·[D] d C](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-31.jpg)
a. A + b. B c. C + d. D c ·[D] d C D [C] DG = DGo + RT·ln A a ·[B] Bb [A] Se le concentrazioni di reagenti e prodotti sono 1 M si ha: c · 1 d 1 DG = DGo + RT·ln a b 1 · 1 Qualsiasi sia il valore dei coefficienti stechiometrici a, b, c, d, risulta, in queste condizioni, che: D G = D Go
![a A b B c C d D c Dd C DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-32.jpg)
a. A + b. B c. C + d. D c ·[D]d [C] DG = DGo + RT·ln [A]a ·[B]b Il valore di DGo si può ricavare dalla costante di equilibrio (e viceversa)
![a A b B c C d D c Dd C DG a. A + b. B c. C + d. D c ·[D]d [C] DG](https://slidetodoc.com/presentation_image_h2/7a655e4f202ff71f6c871e2efb71177e/image-33.jpg)
a. A + b. B c. C + d. D c ·[D]d [C] DG = DGo + RT·ln [A]a ·[B]b Se si è all’equilibrio, equilibrio DG = 0 , e quindi : c ·[D]d [C] 0 = DGo + RT·ln a [A] ·[B]b Essendo il sistema all’equilibrio, le concentrazioni di reagenti e prodotti sono le concentrazioni di equilibrio e quindi si ha: DGo = - RT·ln K

a. A + b. B c. C + d. D Se il sistema non è all’equilibrio e le concentrazioni sono tutte diverse da 1 M, per stabilire se una reazione come questa è spontanea verso destra o verso sinistra si applica l’equazione: [C]c ·[D]d DG = DGo + RT·ln [A]a ·[B]b Se DG< 0 a. A + b. B c. C + d. D Se DG> 0 a. A + b. B c. C + d. D


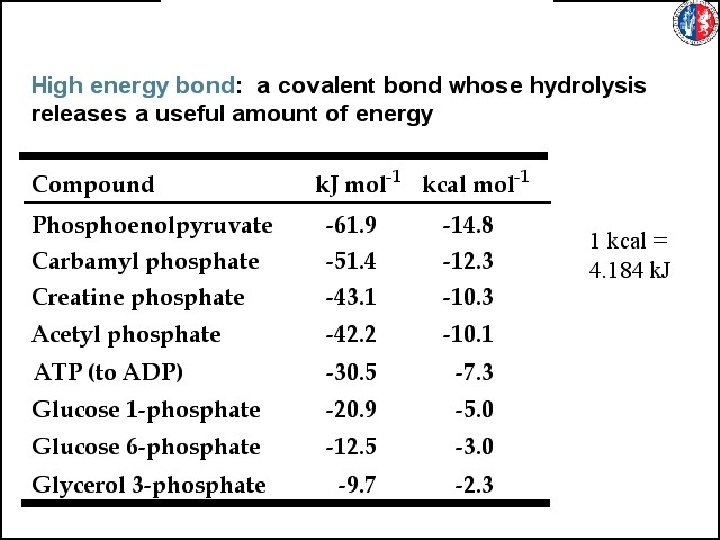
ATP DG 0’= -30. 5 k. J/mole ADP O HO P OH OH DG = DH - T·DS

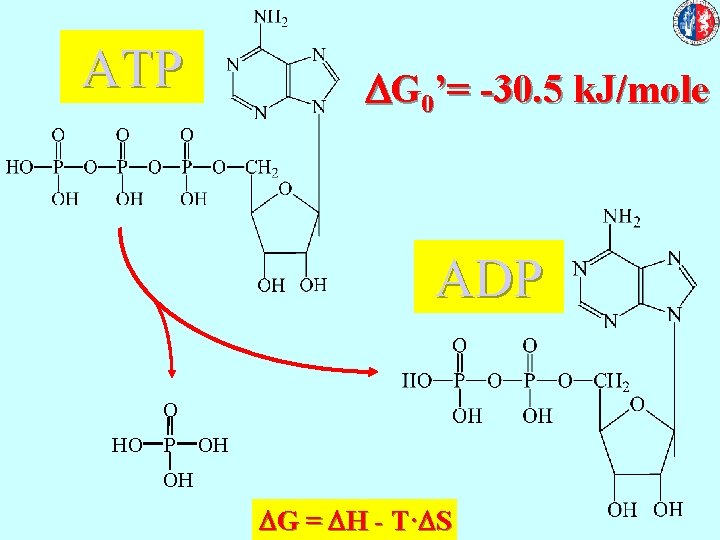
idrolisi OO- O- O- DS > 0 O- H 3 PO 4 + O- O-

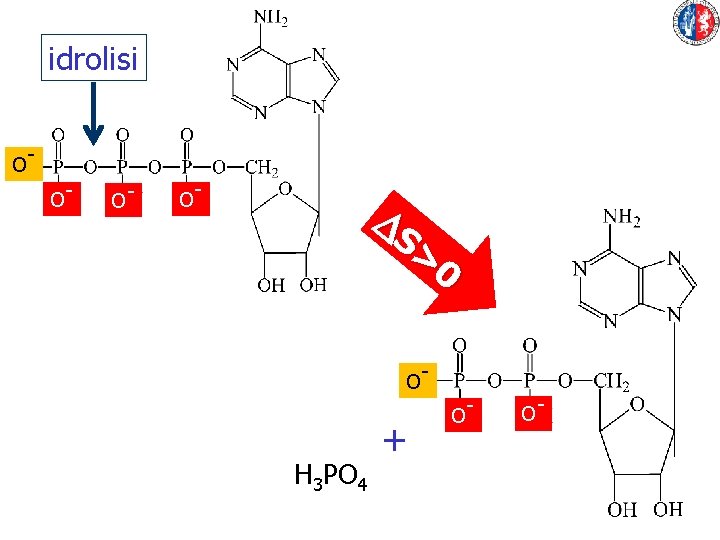
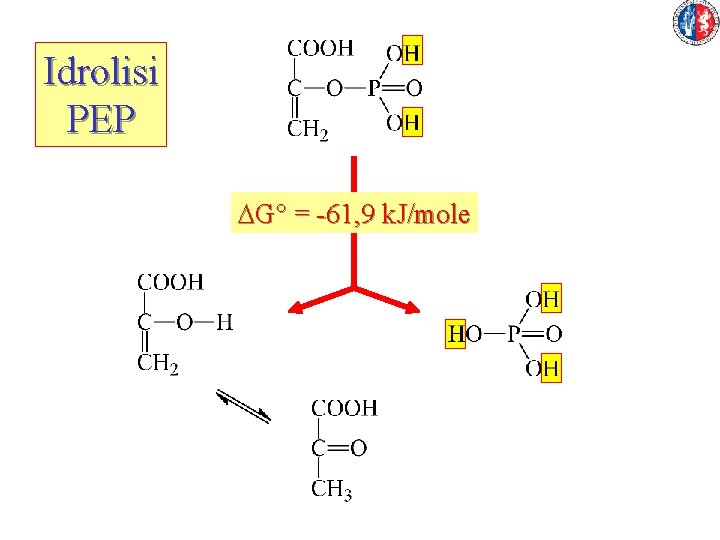
Idrolisi PEP DG° = -61, 9 k. J/mole

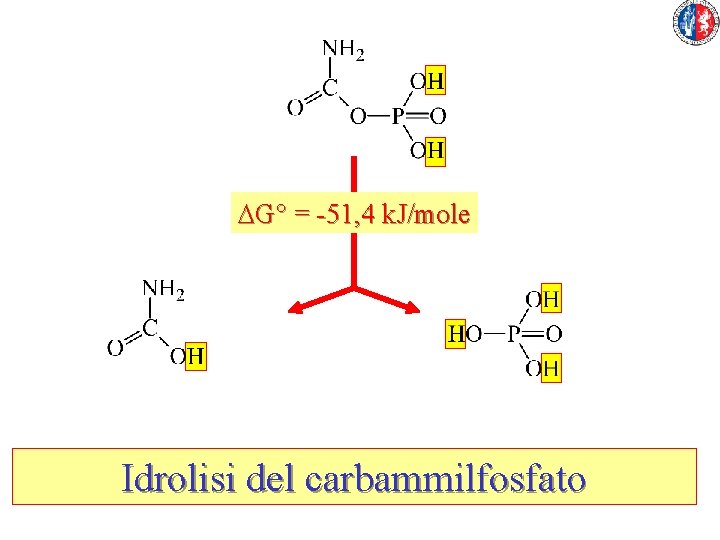
DG° = -51, 4 k. J/mole Idrolisi del carbammilfosfato

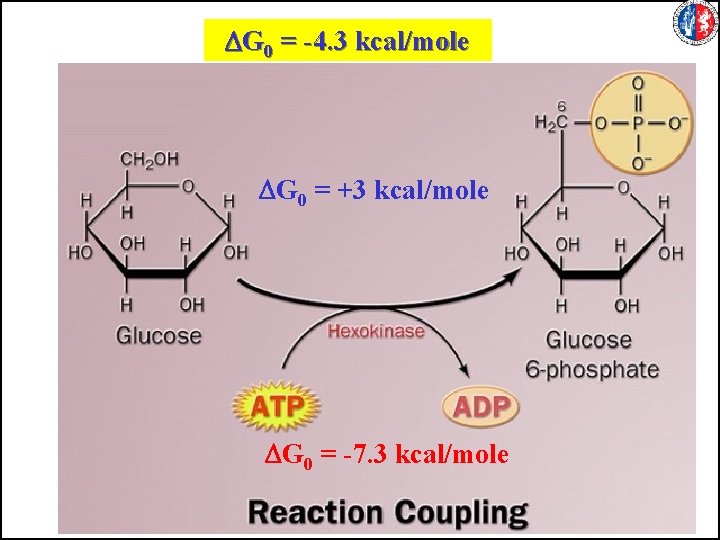
DG 0 = -4. 3 kcal/mole DG 0 = +3 kcal/mole DG 0 = -7. 3 kcal/mole
