LAgenzia Italiana del Farmaco AIFA quale promotore della











































- Slides: 49

L’Agenzia Italiana del Farmaco (AIFA) quale promotore della ricerca clinica indipendente Ufficio Ricerca & Sviluppo - AIFA L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Ricerca indipendente: argomenti ü Quale contesto: il ruolo della ricerca all’interno dell’attività delle agenzie regolatorie ü Ricerca indipendente: cosa è e perché ne abbiamo bisogno ü Come promuovere la ricerca indipendente ü Il programma dell’AIFA e l’identificazione delle priorità ü Possibili ricadute ü Problemi aperti e conclusioni L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Il contesto: come integrare conoscenze e decisioni regolatorie (Reform of drug regulation -. . . WA Ray & M Stein. NEJM 2006; 354: 194 -201) ü Sperimentazioni cliniche: informazione completa sugli studi in corso e sui risultati ottenuti ü L’informazione indipendente e la formazione ü Gli studi post marketing ü Studi aggiuntivi raccomandati alle aziende ü Commercializzazione in condizioni controllate ü Revisione periodica delle conoscenze ü Studi indipendenti L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Perché è importante la ricerca indipendente (1) ü Le popolazioni trascurate dalla ricerca commerciale ü Scarso interesse di mercato (pazienti con malattie rare; sottogruppi di non responder) ü Aumentato rischio per la ricerca (bambini, donne in gravidanza, anziani con polipatol. ) ü Incertezza degli esiti della ricerca ü Incidenza di eventi avversi ü Problemi di compliance e organizzazione L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Perché è importante la ricerca indipendente (2) ü Gli aspetti trascurati dalla ricerca commerciale: interessi potenzialmente in conflitto ü Interesse per farmaci fuori brevetto ü Interesse per il follow up a lungo termine ü Interesse a valutare le ADR su grandi popolazioni ü Interesse a confrontarsi con altre strategie/interventi efficaci ü Interesse a utilizzare end point clinici forti (tempi più lunghi e maggiori difficoltà) L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Cosa caratterizza la ricerca indipendente ü La ricerca pubblica indipendente? può essere considerata ü Principali elementi caratterizzanti: ü Definizione del protocollo dello studio ü Proprietà dei dati ü Libertà di analisi e di pubblicazione ü Finanziamento basato sul merito scientifico ü Assenza (contenimento) dei conflitti di interesse L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Cosa fare per favorire la ricerca indipendente ü Contesto normativo favorevole: sperimentazione no profit in Italia per es. , ü Finanziamenti L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Regulazione della ricerca non-profit in Italia (DM 17 December 2004) ü Promossa da istituzioni pubbliche o non profit ü Assenza di interessi commerciali (per es. , non proprietà di brevetti) ü Proprietà dei dati da parte del ricercatore ü I farmaci in commercio sono a carico del SSN ü L’assicurazione è ricompresa nell’ambito dell’attività clinica generale o di ricerca della struttura ü E’ gratuito il parere obbligatorio dei comitati etici L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Il fondo per la ricerca indipendente AIFA (Art. 48, Legge 326/2003) ü Fra i compiti dell’Agenzia vi è quello di promuovere la ricerca scientifica di carattere pubblico sui settori strategici del farmaco ü E’ costituito un fondo alimentato dal 5% delle spese per attività di promozione delle aziende farmaceutiche L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

L’utilizzo del fondo del 5% (Art. 48, Legge 326/2003) ü Farmaci orfani per malattie rare e farmaci non ancora autorizzati ma che rappresentano una speranza di cura per patologie gravi ü Ricerca sull’uso dei farmaci e in particolare: studi clinici comparativi tra medicinali tesi a dimostrare il valore terapeutico aggiuntivo; studi su farmaci orfani; studi sull’appropriatezza e l’informazione ü Centro di informazione indipendente sui medicinali ü Programma di farmacovigilanza attiva L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

La ricerca indipendente dell’AIFA: ü Cosa è stato fatto? ü Come è stato fatto? ü Quale rapporto con l’attività regolatoria dell’AIFA? ü Problemi aperti ü Conclusioni L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

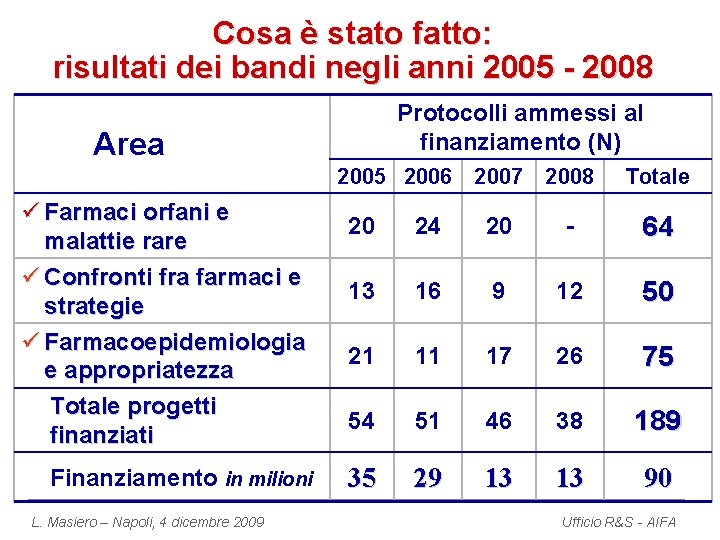
Cosa è stato fatto: risultati dei bandi negli anni 2005 - 2008 Protocolli ammessi al finanziamento (N) Area 2005 2006 2007 2008 ü Farmaci orfani e malattie rare ü Confronti fra farmaci e strategie ü Farmacoepidemiologia e appropriatezza Totale progetti finanziati Finanziamento in milioni L. Masiero – Napoli, 4 dicembre 2009 Totale 20 24 20 - 64 13 16 9 12 50 21 11 17 26 75 54 51 46 38 189 35 29 13 13 90 Ufficio R&S - AIFA

Come è stato fatto: trasparenza e merito ü Attività istruttoria e audizioni da parte della CRS ü Definizione dei temi del Bando da parte della CRS e approvazione da parte del Cd. A dell’AIFA ü Pubblicazione del Bando AIFA (requisiti, procedure di presentazione, ( modalità di valutazione) ü Presentazione tramite portale AIFA delle lettere di intenti (in italiano) ü Valutazione delle lettere di intenti da parte della CRS e selezione delle proposte da ammettere alla seconda fase di valutazione ü Presentazione tramite portale AIFA di un protocollo di ricerca (in inglese) da parte dei responsabili scientifici dei progetti ammessi ü Valutazione finale da parte di commissioni (study session) composte da referee stranieri e italiani ü Comunicazioni dei risultati ü Corso GCP per la conduzione degli studi ü Firma del contratto e avvio del finanziamento degli studi L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Come è stato fatto: la Commissione Ricerca e Sviluppo (CRS) ü Il ruolo: ü Identificare i temi di ricerca del call for proposals; ü Condurre la prima fase del processo di selezione delle proposte; ü Supervisionare l’andamento dei progetti ü ü ü Lucio Annunziato Renato Bernardini Sergio Bonini Maria Del Zompo Antonio Francavilla L. Masiero – Napoli, 4 dicembre 2009 ü ü ü Enrico Garaci Silvio Garattini (presidente) Alessandro Liberati Giampietro Rupolo Gloria Saccani Jotti Ufficio R&S - AIFA

Come è stato fatto: l’individuazione dei temi ü Suggerimenti da parte dei ricercatori ü Audizioni con istituzioni e associazioni ü Documenti pervenuti ü Discussione interna alla CRS ü Rapporto con il Cd. A L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Suggerimenti per il bando AIFA (www. agenziafarmaco. it) L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Quale rapporto con l’attività dell’AIFA ü Quali temi: ü nuove conoscenze con ricadute nella pratica clinica e/o regolatorie ü interesse commerciale è limitato ü Quali farmaci: innanzitutto A o H ü Quali confronti: non solo singoli farmaci ma strategie ü Quali tipi di studio: soprattutto fasi 3 -4; sperimentali e osservazionali (dal 2007 anche revisioni sistematiche) L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Aree di ricerca 2005 -2008 1. Farmaci orfani per malattie rare e sottogruppi di pazienti non responder (Bandi 2005 -2007) ü Gruppi limitati di popolazione e studi limitati sia per i farmaci approvati che designati dall’EMEA 2. Confronto fra farmaci e strategie terapeutiche ü Interesse limitato a valutare l’efficacia relativa 3. Farmacoepidemiologia e strategie di promozione dell’appropriatezza ü Immissione in commercio sempre più rapida, con dati ancora limitati L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

La presentazione delle proposte ü Due fasi di presentazione e valutazione, con indicazioni per ricercatori e per revisori: ü Lettere di intenti ü Protocolli L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Presentazione di una lettera di intenti L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Come è stato fatto I fase di valutazione: selezione delle lettere di intenti da parte della CRS ü Valutazioni singole: da parte di almeno 3 componenti della CRS ü Pertinenza al tema ü ü Rilevanza per l’SSN (35 punti) ü ü Esperienza proponente (20 punti) Qualità scientifica dello studio (35 punti) Congruità economica (10 punti) ü Discussione plenaria e votazione (con motivazione) ü Regole interne scritte e condivise sui conflitti di interesse L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Risultati della valutazione delle lettere di intenti dei bandi 2005 -2008 Area üFarmaci orfani e malattie rare Lettere di Intenti 454 üConfronti fra farmaci e strategie 449 üFarmacoepi-demiologia e appropriatezza 616 Totale L. Masiero – Napoli, 4 dicembre 2009 1. 519 Protocolli ammessi 106 (23%) 90 (20%) 160 (26%) 356 (23%) Ufficio R&S - AIFA

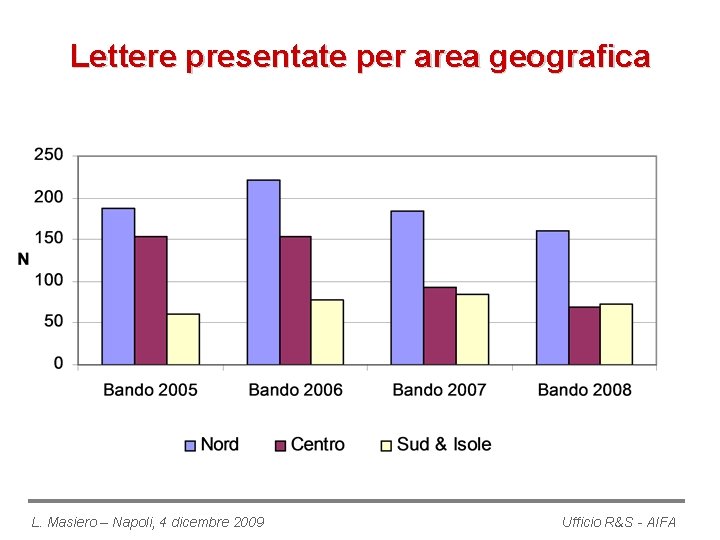
Lettere presentate per area geografica L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

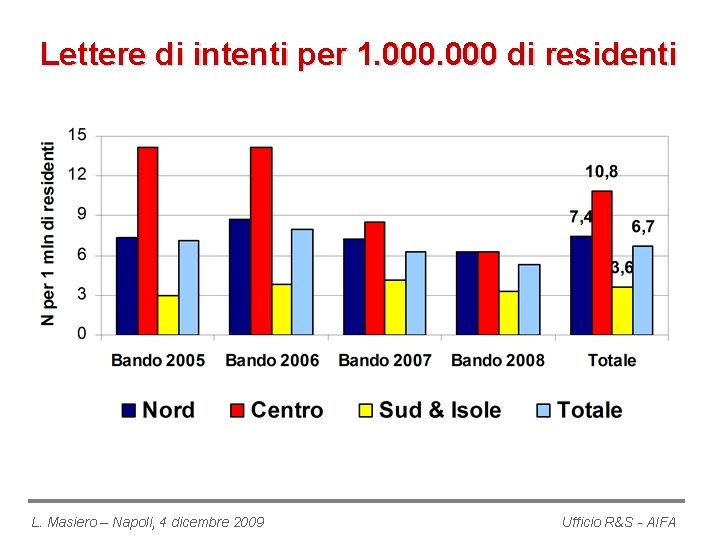
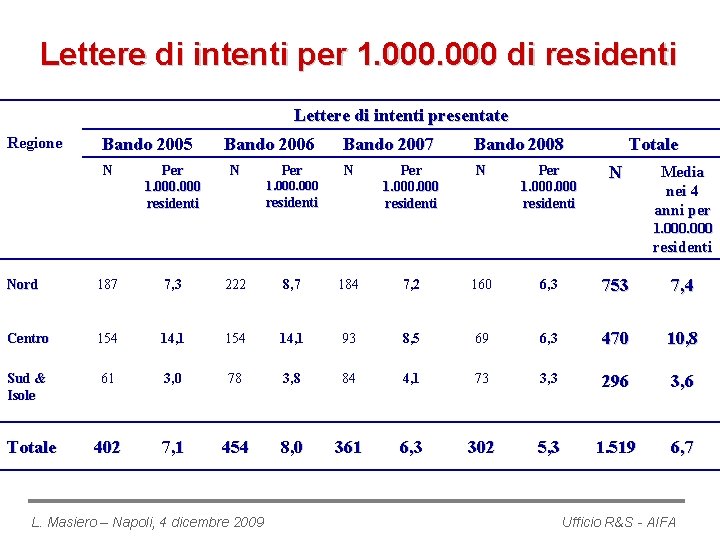
Lettere di intenti per 1. 000 di residenti L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

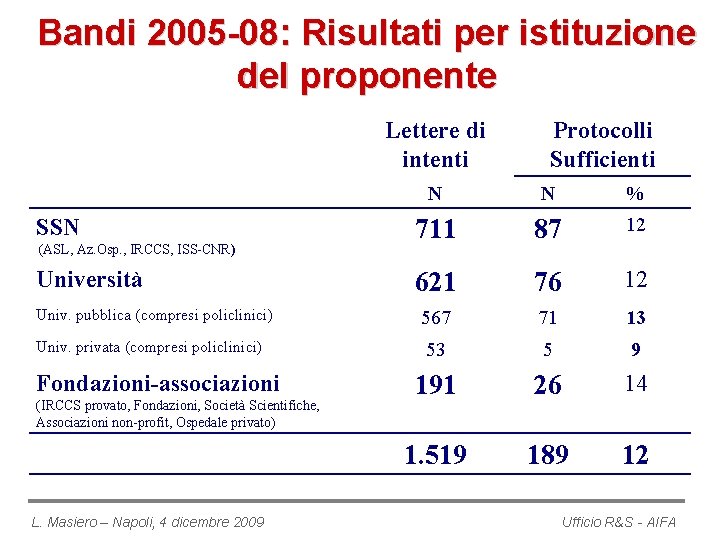
Bandi 2005 -08: Risultati per istituzione del proponente Lettere di intenti SSN (ASL, Az. Osp. , IRCCS, ISS-CNR) Università Univ. pubblica (compresi policlinici) Univ. privata (compresi policlinici) Fondazioni-associazioni (IRCCS provato, Fondazioni, Società Scientifiche, Associazioni non-profit, Ospedale privato) L. Masiero – Napoli, 4 dicembre 2009 Protocolli Sufficienti N N % 711 87 12 621 76 12 567 71 13 53 5 9 191 26 14 1. 519 189 12 Ufficio R&S - AIFA

Come è stato fatto II fase di valutazionesel dei protocolli da parte delle study session ü Study session 2008 con 24 esperti (per metà stranieri; diversi dalla CRS) ü Per ciascun protocollo: ü 3 reviewer (con commenti scritti e votazione da casa) ü Discussione plenaria; votazione formulazione di un final statment L. Masiero – Napoli, 4 dicembre 2009 e Ufficio R&S - AIFA

Processo di revisione: sistema di punteggio ü Punteggio finale: 1. 0 -5. 0 ü 1. 0 -2. 9: insufficiente ü 3. 0 -3. 9: sufficiente / bassa priorità ü 4. 0 -5. 0: eccellente / alta priorità ü Ranking finale di tutti i protocolli, per area tematica e complessivo L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Trasparenza nel processo di valutazione: conflitti di interesse ü Processo di valutazione affidato a due commissioni indipendenti ü Meccanismo di finanziamento basato unicamente sulla valutazione di merito scientifico ü Regole interne scritte sui conflitti di interesse per ü CRS ü Study session L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Trasparenza nel processo di valutazione: conflitti di interesse ü Referees should abstain from participating in the revision process of a specific protocol, if he/she: ü Is involved in one of the working units of the study ü Belongs to the same institution of the PI ü Has collaborated with the PI in research projects in the last 5 years ü Has or will have a direct advantage from the study approval ü Has any other perception of conflict of interest L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Trasparenza nel processo di valutazione e merito delle decisioni ü Un meccanismo trasparente è anche garanzia di merito? ü “Sensibilità” e “specificità” della valutazione ü Alcune critiche: ü Impossibilità di rispondere alle osservazioni dei referee ü Limitazione spettro di competenze interne a ciascuna study session L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Il finanziamento ü Sulla base del ranking della Study session ü In oltre il 30% dei progetti è finanziato tutto l’importo richiesto ü I progetti devono di norma concludersi in un triennio ü Cofinanziamento aziende farmaceutiche ü Farmaci off label e preparazioni in doppio cieco ü Per i farmaci orfani approvati o designati dall’EMEA cofinanziamento anche per singolo progetto L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Quale rapporto con l’attività AIFA: il caso della neurologia ü Efficacia e tossicità dei trattamenti per la sclerosi multipla (Area 2, 2005) ü Trattamento farmacologico dell'epilessia con riferimento ai casi di resistenza (Area 3, 2005) ü Strategie terapeutiche per ottimizzare il trattamento dell’ictus cerebrovascolare (Area 2, 2006) ü Studi sul trattamento con farmaci antipsicotici dei disturbi del comportamento dei pazienti con demenza (Area 3, 2006) ü Confronto fra strategie terapeutiche per l’ottimizzazione della terapia della malattia di Parkinson (Area 2, 2007) L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Bando 2006 • Studi sul trattamento con farmaci antipsicotici dei disturbi del comportamento dei pazienti con demenza • Nota: si fa riferimento a studi su strategie che comprendono il confronto fra farmaci antipsicotici tipici e di seconda generazione Motivazione • Pur essendo gli antipsicotici tipici e atipici ampiamente usati nei pazienti con demenza, diversi aspetti richiedono un approfondimento. In particolare: • il profilo beneficio-rischio • è sovrapponibile fra le diverse sostanze? • è sovrapponibile fra i diversi gruppi (tipici vs atipici)? • le indicazioni attuali per le diverse sostanze sono coerenti con l’evidenza scientifica? L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Bando 2005: es. di studi approvati di interesse oncologico ü ü ü FATA – First Adjuvant Trial on all aromatase inhibitors in early breast cancer. A phase 3 study comparing anastrozole, letrozole and exemestane, upfront (for 5 years) or sequentially (for 3 years after 2 years of tamoxifen), as adjuvant treatment of postmenopausal patients with endocrineresponsive breast cancer A randomized trial investigating the role of FOLFOX-4 regimen duration (3 versus 6 months) and bevacizumab as adjuvant therapy for patients with stage II/III colon cancer Evaluation of a population-based multi-modal intervention to improve the quality of cancer pain analgesic treatment L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Bando 2006: es. di studi approvati di interesse oncologico ü Efficacy and toxicity of trastuzumab at the maintaining dose of 1 mg/kg/week vs the standard dose of 2 mg/kg/week in combination with chemotherapy in metastatic breast cancer patients ü Short-HER: multicentric randomised phase III trial of adjuvant chemotherapy plus 3 vs 12 months of trastuzumab in breast cancer patients with HER 2 positive disease ü Sequential treatment strategy for metastatic colorectal cancer: a phase III randomized multicenter study of chemotherapy (CT) with or without bevacizumab as firstline therapy followed by two phase III randomized studies of CT alone or CT plus bevacizumab with or without cetuximab as second-line therapy L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Farmacovigilanza e appropriatezza (es. studi approvati) ü ü ü Identificazione del dosaggio di acido folico efficace nel ridurre le malformazioni congenite nel loro insieme, le cardiopatie congenite, la sindrome di Down. Trial clinico controllato randomizzato nelle donne in età fertile: 5 mg verso 0, 4 mg di acido folico. Valutazione della risposta anticorpale e della persistenza della memoria immunologica verso l'epatite b in coorti di bambini vaccinati con vaccini esavalenti Pharmacists’ outreach visits and new information formats: cluster and single-doctor randomised controlled trials for evaluating their feasibility and impact on knowledge, attitudes and prescribing practices of general practitioners L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Il coinvolgimento dell’AIFA Obiettivo CRS e Ufficio R&S: promuovere la qualità della ricerca e sostenere gli studi avviati ü Relazioni intermedie: aspetti scientifici e amministrativi ü Incontri annuali all’AIFA sullo stato di avanzamento dei progetti: 27 ottobre 2009 ü Partecipazione a seminari periodici degli studi sullo stato di avanzamento ü Rapporti scientifici finali che vengono valutati dalla CRS ü Pubblicazioni L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

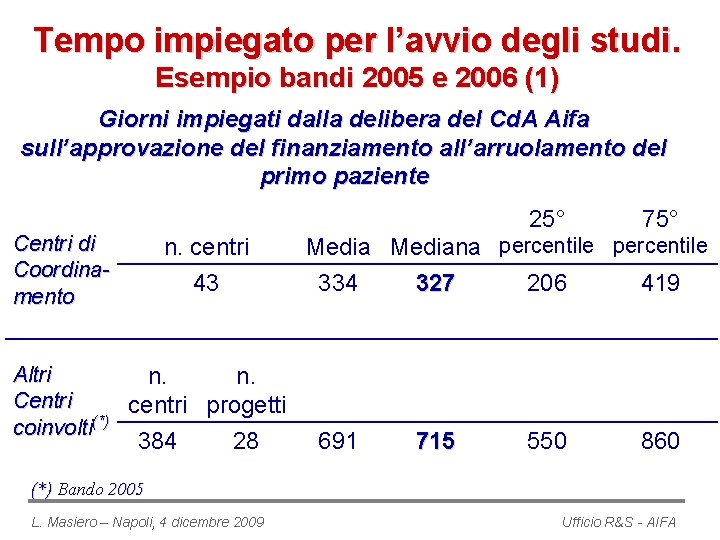
Tempo impiegato per l’avvio degli studi. Esempio bandi 2005 e 2006 (1) Giorni impiegati dalla delibera del Cd. A Aifa sull’approvazione del finanziamento all’arruolamento del primo paziente 25° Centri di Coordinamento n. centri 43 Altri n. n. Centri centri progetti (*) coinvolti 384 28 75° Mediana percentile 334 327 206 419 691 715 550 860 (*) Bando 2005 L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Tempo impiegato per l’avvio degli studi. Esempio bandi 2005 e 2006 (2) Giorni impiegati dall’invio della documentazione ai Comitati Etici all’arruolamento del primo paziente Centri di Coordinamento Altri Centri coinvolti 25° n. centri 43 75° Mediana percentile 229 264 203 375 n. n. centri progetti 511 41 L. Masiero – Napoli, 4 dicembre 2009 312 272 190 394 Ufficio R&S - AIFA

Libertà di analisi e di pubblicazione I ricercatori non devono richiedere autorizzazioni per le analisi dei dati e le pubblicazioni Diffondere adeguatamente i risultati ü pubblicazioni ü rapporto scientifico finale per l’AIFA L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Alcuni problemi aperti ü L’individuazione di quesiti clinici rilevanti nelle “aree grigie” ü Non basta una buona idea: l’importanza delle unità di ricerca clinica ü I tempi dall’idea all’avvio di uno studio alla diffusione dei risultati ü Cofinanziamenti ü La gestione dei conflitti di interesse (per valutatori e proponenti) ü Difficoltà organizzative: rapporto con i comitati etici Ø rapporto con i centri satellite Ø ü Potenziali ricadute commerciali ü Farmaco fuori indicazione e assicurazione L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Il cofinanziamento ü La ricerca indipendente è in sé un cofinanziamento pubblico ü Contributo finanziario e non copertura totale costi ü Personale di ruolo e strutture ü Cofinanziamento aziende farmaceutiche ü Farmaci off label e preparazioni per doppio cieco ü Finanziamento per una tematica (aree 2 e 3) ü Per i farmaci orfani approvati o designati dall’EMEA cofinanziamento anche per singolo progetto L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Disponibilità del farmaco fuori indicazione (DM 17 December 2004) ü L’uso del farmaco fuori indicazione non implica necessariamente un incremento di spesa ü Alcuni esempi § Multicenter RCT of azathioprine versus interferon beta- in relapsing-remitting multiple sclerosis § Efficacy and toxicity of trastuzumab at the maintaining dose of 1 mg/kg/week vs the standard dose of 2 mg/kg/week in combination with chemotherapy in metastatic breast cancer § Alzheimer's Disease (AD) and antipsychotics: a long term, multicentre, double blind, randomised clinical trial § A randomized controlled trial of alteplase (rt-PA) vs standard treatment in acute ischemic hemispheric stroke in patients aged more than 80 years, where thrombolysis is initiated within 3 hours after stroke onset L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Disponibilità del farmaco fuori indicazione ü Lettera Direttore AIFA e Assessore Toscana Assicurazione ü È stata compiuta una riflessione sul tema (DM del 14 luglio 2009) ma sussistono problemi di adeguamento da parte dei Centri L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Ricadute della ricerca AIFA ü Nuove conoscenze: ü ü ü Stimolo allo sviluppo di competenze nella ricerca: ü ü ü creazione e consolidamento di reti di ricerca diffusione di competenze di ricerca: dalla stesura dei protocolli all’applicazione delle GCP Sviluppo di ricerche coinvolgano anche i paesi in via di sviluppo ü ü ü “aree grigie” temi per i quali è assente un interesse commerciale Adattamenti alle condizioni specifiche Sviluppo di competenze autonome Come gestire le possibili ricadute commerciali? L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Conclusioni ü L’esperienza AIFA mostra che • si può stimolare la ricerca indipendente sui farmaci • si può creare un meccanismo di valutazione trasparente e rigoroso ü E’ importante verificare che i nuovi studi: • siano basati su una revisione sistematica di quello che già si conosce • indichino le potenziali conoscenze aggiuntive rispetto all’insieme delle conoscenze disponibili sul quesito in studio ü Attenzione a garantire la qualità degli studi indipendenti L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Molte grazie per ogni informazione ulteriore ü Ufficio Ricerca & Sviluppo: ü Alessia Cirilli, Alessandra Correggia, Lucia Masiero, Stefania Ribaldi, Guido Panté, Anna Venezia e Carlo Tomino ü email: ricerca&sviluppo@aifa. gov. it L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Biomedical research: are we getting value for money? Iain Chalmers, 2006 ü There is insufficient concern to ensure that new studies: ü are designed in the light of systematic assessment of what is known already ü are reported in ways that show what contribution they have made to the totality of evidence addressing the questions concerned L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA

Lettere di intenti per 1. 000 di residenti Lettere di intenti presentate Regione Bando 2005 N Per 1. 000 residenti Bando 2006 N Per Bando 2007 Bando 2008 N N 1. 000 residenti Per 1. 000 residenti Totale N Media nei 4 anni per 1. 000 residenti Nord 187 7, 3 222 8, 7 184 7, 2 160 6, 3 753 7, 4 Centro 154 14, 1 93 8, 5 69 6, 3 470 10, 8 Sud & Isole 61 3, 0 78 3, 8 84 4, 1 73 3, 3 296 3, 6 402 7, 1 454 8, 0 361 6, 3 302 5, 3 1. 519 6, 7 Totale L. Masiero – Napoli, 4 dicembre 2009 Ufficio R&S - AIFA