Gio vin dy Nguyn nh Quyt trng THCS











- Slides: 14

Giáo viên dạy: Nguyễn Đình Quyết, trường THCS Minh Diệu (thực hiện tháng 01/2018


Giáo viên dạy: Nguyễn Đình Quyết, trường THCS Minh Diệu (thực hiện tháng 01/2013

I. PHI KIM CÓ NHỮNG TÍNH CHẤT VẬT LÝ NÀO ? Kết luận - Ở điều kiện thường, phi kim tồn tại ở 3 trạng thái: Rắn, lỏng, khí. Các em ha y đọc thông tin sgk rồi cho nhận xét tính - Phần lớn các phi kim không dẫn điện, dẫn nhiệt, có nhiệt độ nóng chất vật lý của phi kim ? chảy thấp. -Một số phi kim độc : clo, brom, iot.

II. PHI KIM CÓ NHỮNG TÍNH CHẤT HÓA HỌC NÀO ? 1. Tác dụng với kim loại: Từphương nhữngtrình kiếnđãthức học, em emcóhãy hoàn Từ các hoànđã thành, nhận xét gì về Nhiềut/d phivới kim khácloại? tác với kim trình loại tạo ? thành muối. thành cácdụng phương phi- kim o t 2 Al. Cl 2 Al + 3 Cl 2 (trắng) Fe (vàng lục) + (trắng) to S (trắng xám) (vàng) 3 Fe. S (đen) - Oxi tác dụng với kim loại tạo thành oxit. 4 Al (trắng) 2 Cu (đỏ) + 3 O 2 to (không màu) + O 2 (không màu) to 2 Al 2 O 3 (trắng) 2 Cu. O (đen)

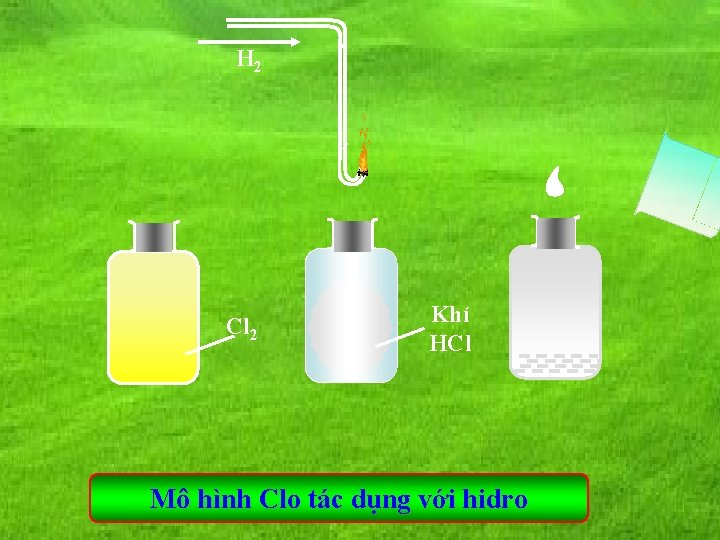
II. PHI KIM CÓ NHỮNG TÍNH CHẤT HÓA HỌC NÀO ? 2. Tác dụng với hiđro: - Oxi + khí hiđro hơi nước. o t O 2 + 2 H 2 O - Clo tác dụng với hiđro. Các em quan sa t thí nghiệm rồi cho nhận xét.

H 2 Cl 2 Khí HCl Mô hình Clo tác dụng với hidro

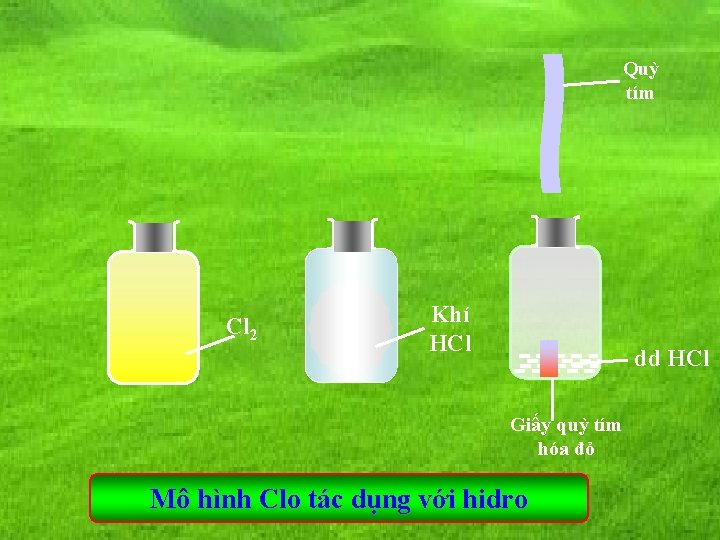
Quỳ tím Cl 2 Khí HCl dd HCl Giấy quỳ tím hóa đỏ Mô hình Clo tác dụng với hidro

I. PHI KIM CÓ NHỮNG TÍNH CHẤT HÓA HỌC NÀO ? 2. Tác dụng với hiđro: - Oxi + khí hiđro hơi nước. O 2 + 2 H 2 to 2 H 2 O - Clo tác dụng với hiđro. H 2 + Cl 2 to 2 HCl C + 2 H 2 to CH 4 H 2 + S to H 2 S Các em hãy viết hoàn thành hai PTHH tiếp theo, rồi rút ra kết luận chung phi kim tác dụng với hidro ? C + H 2 to H 2 + S to * Phi kim phản ứng với hiđro tạo thành hợp chất khí. ? ?

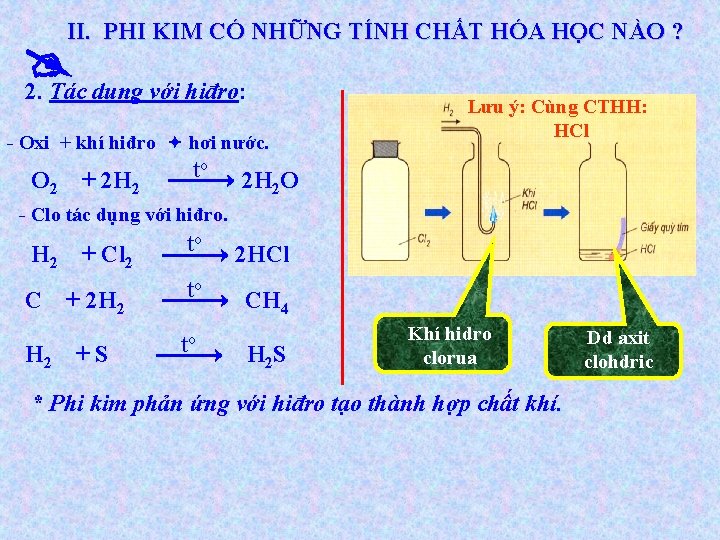
II. PHI KIM CÓ NHỮNG TÍNH CHẤT HÓA HỌC NÀO ? 2. Tác dụng với hiđro: - Oxi + khí hiđro hơi nước. O 2 + 2 H 2 to Lưu ý: Cùng CTHH: HCl 2 H 2 O - Clo tác dụng với hiđro. H 2 + Cl 2 to 2 HCl C + 2 H 2 to CH 4 H 2 + S to H 2 S Khí hidro clorua * Phi kim phản ứng với hiđro tạo thành hợp chất khí. Dd axit clohdric

I. PHI KIM CÓ NHỮNG TÍNH CHẤT HÓA HỌC NÀO ? 3. Tác dụng với oxi. C + O 2 4 P + 5 O 2 to CO ? 2 to 2 P? O 2 5 Em Nhận hãy xét: hoàn Nhiều thành phi các kimphương tác dụng trình với trên oxi tạo rồi cho nhận thànhxét? oxit axit.

Mức độ hoạt động của phi kim dựa vào hai khả năng 4. Mức độ hoạt động của phi kim - Khả năng phi kim phản ứng với kim loại: Thí dụ: (III) o t 2 Fe. Cl 3 3 Cl 2 + 2 Fe Cl 2 > S (II) Suy ra o t S + Fe Fe. S - Khả năng phi kim phản ứng với hidro: Thí dụ: as 2 HCl (Phản ứng xảy ra cần có ánh sáng) Cl 2 + H 2 F 2 > Cl 2 Suy ra F 2 + H 2 2 HF (Phản ứng xảy ra ngay cả trong bóng tối) + Phi kim họat động mạnh như: flo, oxi, clo, . . . + Phi kim họat động yếu hơn: lưu hùynh, photpho, cacbon, silic, . . .

- Phi kim tồn tại ở 3 trạng thái : Rắn, lỏng, khí. Phần lớn các phi kim không dẫn điện, dẫn nhiệt. Một số phi kim độc như clo, bro, iot. - Phi kim tác dụng được với kim loại, hidro và oxi. - Mức độ hoạt động của phi kim căn cứ vào khả năng phản ứng với kim loại và hidro

Bài tập 5/T 76 Phi kim (1) Oxit axit(1) (2) Oxit axit(2) Muối sunfat không tan Ta lập sơ đồ + O 2 S SO 2 + O 2 SO 3 + H 2 O H 2 SO 4 (3) (5) Axit (4) Muối sunfat tan + Na 2 O Các em tự viết các phương trình * Lưu ý: Để học tốt chương này, mỗi em cần có một bảng tuần hoàn Na 2 SO 4 + Ba. Cl 2 Ba. SO 4